文档内容
专题 09 反应速率、化学平衡
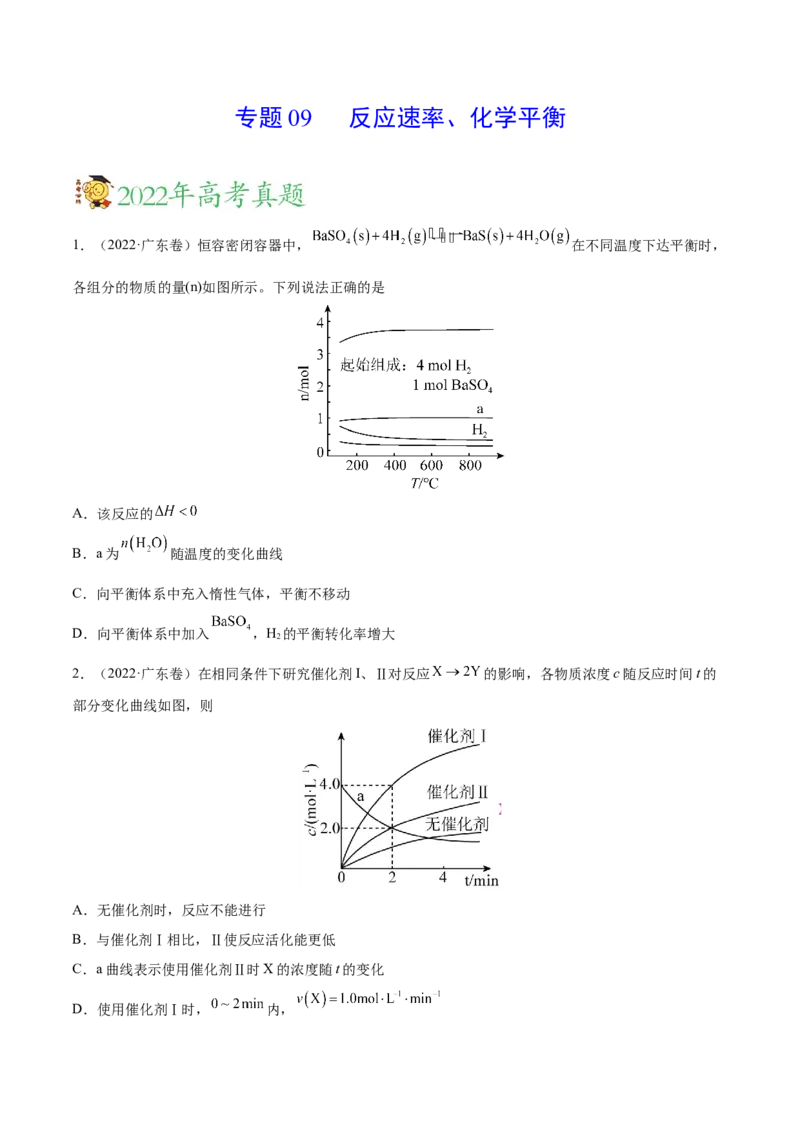
1.(2022·广东卷)恒容密闭容器中, 在不同温度下达平衡时,
各组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
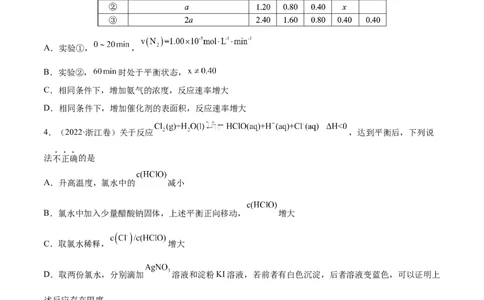
2.(2022·广东卷)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间t的
部分变化曲线如图,则
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,3.(2022·浙江卷)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
4.(2022·浙江卷)关于反应 ,达到平衡后,下列说
法不正确的是
A.升高温度,氯水中的 减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大
C.取氯水稀释, 增大
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上
述反应存在限度
5.(2022·湖南卷)向体积均为1L的两恒容容器中分别充入 和 发生反应:
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所
示。下列说法正确的是A. B.气体的总物质的量:
C.a点平衡常数: D.反应速率:
1.(2021·广东)反应 经历两步:① ;② 。反应体系中 、 、 的浓度c随
时间t的变化曲线如图所示。下列说法不正确的是
A.a为 随t的变化曲线
B. 时,
C. 时, 的消耗速率大于生成速率
D. 后,
2.(2021·河北)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:
①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表示为v=kc2(M) (k 、
1 1 2 2 1
k 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
2A.0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
3.(2021·浙江)相同温度和压强下,关于物质熵的大小比较,合理的是
A.
B.
C.
D.
4.(2021·浙江)一定温度下:在 的四氯化碳溶液( )中发生分解反应: 。
在不同时刻测量放出的 体积,换算成 浓度如下表:
171 282
0 600 1200 2220 x
0 0
1.40 0.96 0.66 0.48 0.35 0.24 0.12
下列说法正确的是
A. ,生成 的平均速率为B.反应 时,放出的 体积为 (标准状况)
C.反应达到平衡时,
D.推测上表中的x为3930
5.(2021·浙江)取50 mL过氧化氢水溶液,在少量I- 存在下分解:2HO=2H O+O↑。在一定温度下,测
2 2 2 2
得O 的放出量,转换成HO 浓度(c)如下表:
2 2 2
t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是
A.反应20min时,测得O 体积为224mL(标准状况)
2
B.20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C.第30min时的瞬时速率小于第50min时的瞬时速率
D.HO 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
6.(2021·浙江)在298.15 K、100 kPa条件下,N(g) +3H (g)=2NH (g) ΔH=-92.4 kJ·mol-1,N (g) 、H(g)
2 2 3 2 2
和NH (g)的比热容分别为29.1、28.9和35.6J·K-1·mol-1。一定压强下,1 mol反应中,反应物[N (g)
3 2
+3H (g)]、生成物[2NH (g)]的能量随温度T的变化示意图合理的是
2 3
A. B.
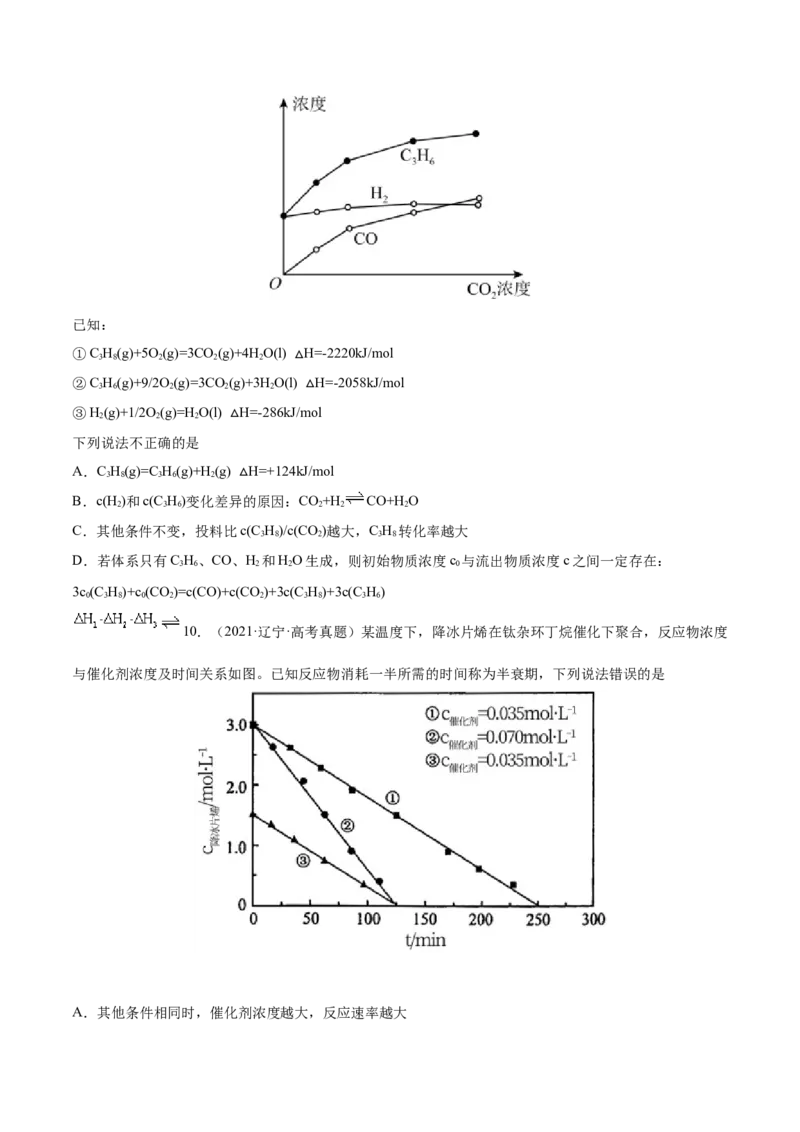
C. D.7.(2021·湖南)已知: ,向一恒温恒容的密闭容器中充入 和
发生反应, 时达到平衡状态I,在 时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随
时间的变化如图所示。下列说法正确的是
A.容器内压强不变,表明反应达到平衡
B. 时改变的条件:向容器中加入C
C.平衡时A的体积分数 :
D.平衡常数K:
8.(2021·北京·高考真题)有科学研究提出:锂电池负极材料(Li)由于生成LH而不利于电池容量的保持。
一定温度下,利用足量重水(D O)与含LiH的Li负极材料反应,通过测定n(D )/n(HD)可以获知
2 2
n(Li)/n(LiH)。
已知:①LiH+H O=LiOH+H ↑
2 2
②2Li(s)+H 2LiH H<0
2
下列说法不正⇌确的是△
A.可用质谱区分D 和HD
2
B.Li与DO的反应:2Li+2DO=2LiOD+D ↑
2 2 2
C.若n(Li)/n(LiH)越大,则n(D )/n(HD)越小
2
D.80℃反应所得n(D )/n(HD)比25℃反应所得n(D )/n(HD)大
2 2
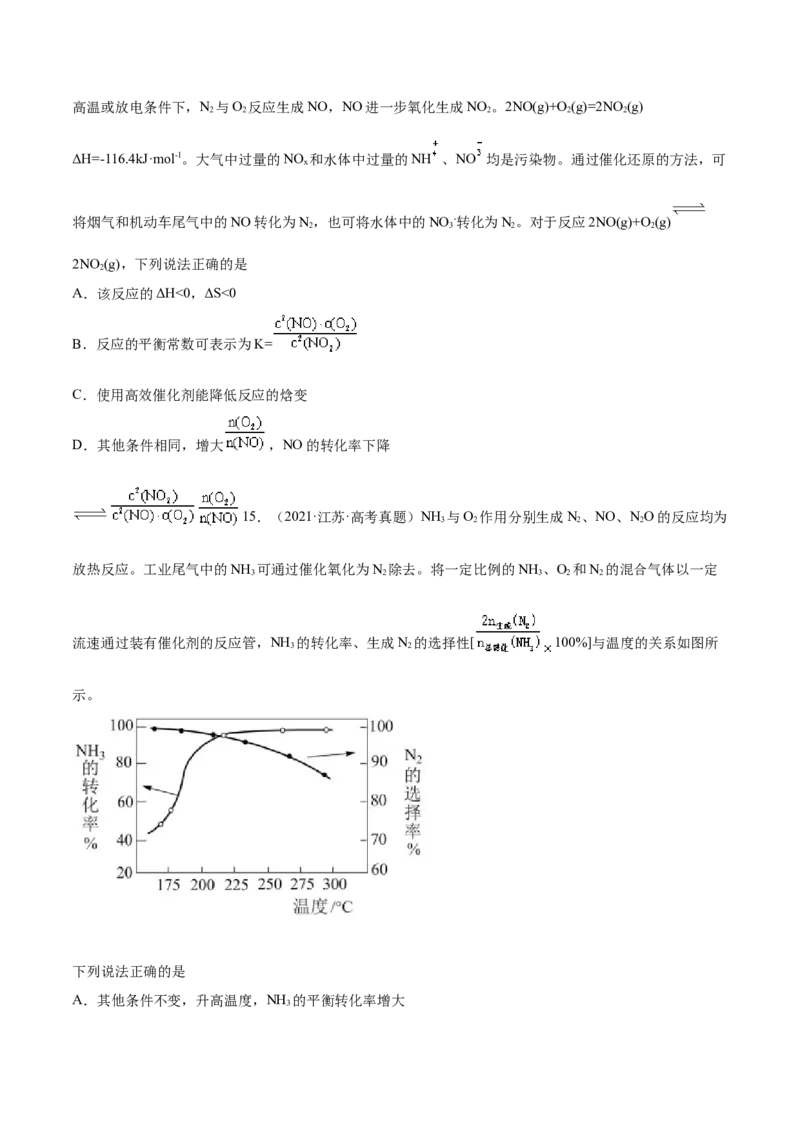
9.(2021·北京·高考真题)丙烷经催化脱氢可制丙烯:C H C H+H 。600℃,将一定浓度的 CO 与固
3 8 3 6 2 2
定浓度的C H 通过含催化剂的恒容反应器,经相同时间,流出的 C H、CO和H 浓度随初始 CO 浓度的
3 8 3 6 2 2
变化关系如图。已知:
①C H(g)+5O(g)=3CO (g)+4HO(l) H=-2220kJ/mol
3 8 2 2 2
②C
3
H
6
(g)+9/2O
2
(g)=3CO
2
(g)+3H
2
O(l)△ H=-2058kJ/mol
③H
2
(g)+1/2O
2
(g)=H
2
O(l) H=-286kJ/m△ol
下列说法不正确的是 △
A.C H(g)=C H(g)+H(g) H=+124kJ/mol
3 8 3 6 2
B.c(H
2
)和c(C
3
H
6
)变化差异△的原因:CO
2
+H
2
CO+H
2
O
C.其他条件不变,投料比c(C H)/c(CO )越大,C H 转化率越大
3 8 2 3 8
D.若体系只有C H、CO、H 和HO生成,则初始物质浓度c 与流出物质浓度c之间一定存在:
3 6 2 2 0
3c(C H)+c (CO)=c(CO)+c(CO )+3c(C H)+3c(C H)
0 3 8 0 2 2 3 8 3 6
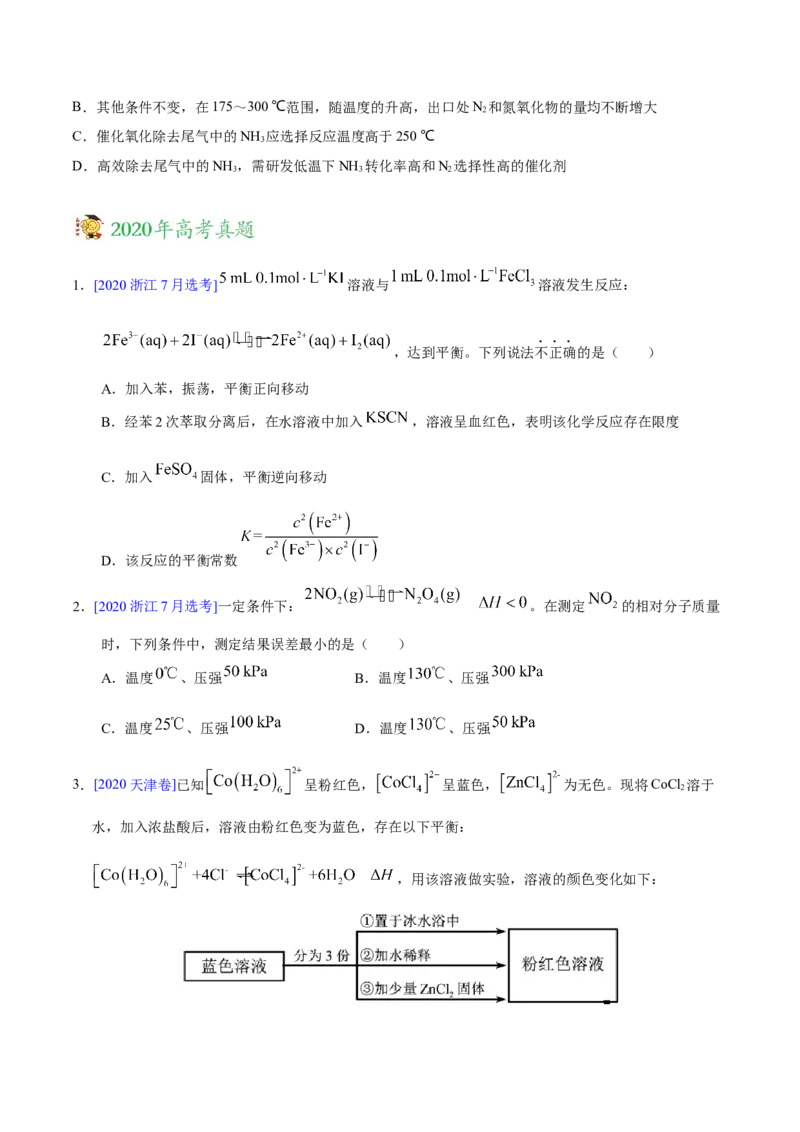
10.(2021·辽宁·高考真题)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度
与催化剂浓度及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是
A.其他条件相同时,催化剂浓度越大,反应速率越大B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为
D.条件②,降冰片烯起始浓度为 时,半衰期为
11.(2021·辽宁·高考真题)某温度下,
在恒容密闭容器中加入一定量X,发生反应 ,一段时间后达到平衡。下列说法错误的
是
A.升高温度,若 增大,则
B.加入一定量Z,达新平衡后 减小
C.加入等物质的量的Y和Z,达新平衡后 增大
D.加入一定量氩气,平衡不移动
12.(2021·海南·高考真题)制备水煤气的反应
,下列说法正确的是
A.该反应
B.升高温度,反应速率增大
C.恒温下,增大总压,HO(g)的平衡转化率不变
2
D.恒温恒压下,加入催化剂,平衡常数增大
13.(2021·福建·高考真题)实验室配制碘水时,通常将 溶于 溶液: 。关于该
溶液,下列说法正确的是
A. 的电子式为 B.滴入淀粉溶液,不变蓝
C.加水稀释,平衡逆向移动 D.加少量 固体平衡正向移动
14.(2021·江苏·高考真题)N 是合成氨工业的重要原料,NH 不仅可制造
2 3
化肥,还能通过催化氧化生产HNO;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在
3 3高温或放电条件下,N 与O 反应生成NO,NO进一步氧化生成NO 。2NO(g)+O (g)=2NO (g)
2 2 2 2 2
ΔH=-116.4kJ·mol-1。大气中过量的NO 和水体中过量的NH 、NO 均是污染物。通过催化还原的方法,可
x
将烟气和机动车尾气中的NO转化为N,也可将水体中的NO -转化为N。对于反应2NO(g)+O (g)
2 3 2 2
2NO (g),下列说法正确的是
2
A.该反应的ΔH<0,ΔS<0
B.反应的平衡常数可表示为K=
C.使用高效催化剂能降低反应的焓变
D.其他条件相同,增大 ,NO的转化率下降
15.(2021·江苏·高考真题)NH 与O 作用分别生成N、NO、NO的反应均为
3 2 2 2
放热反应。工业尾气中的NH 可通过催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以一定
3 2 3 2 2
流速通过装有催化剂的反应管,NH 的转化率、生成N 的选择性[ 100%]与温度的关系如图所
3 2
示。
下列说法正确的是
A.其他条件不变,升高温度,NH 的平衡转化率增大
3B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C.催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D.高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2
1.[2020浙江7月选考] 溶液与 溶液发生反应:
,达到平衡。下列说法不正确的是( )
A.加入苯,振荡,平衡正向移动
B.经苯2次萃取分离后,在水溶液中加入 ,溶液呈血红色,表明该化学反应存在限度
C.加入 固体,平衡逆向移动
D.该反应的平衡常数
2.[2020浙江7月选考]一定条件下: 。在测定 的相对分子质量
时,下列条件中,测定结果误差最小的是( )
A.温度 、压强 B.温度 、压强
C.温度 、压强 D.温度 、压强
3.[2020天津卷]已知 呈粉红色, 呈蓝色, 为无色。现将CoCl 溶于
2
水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
,用该溶液做实验,溶液的颜色变化如下:以下结论和解释正确的是
A.等物质的量的 和 中σ键数之比为3:2
B.由实验①可推知 H<0
C.实验②是由于c(H△2 O)增大,导致平衡逆向移动
D.由实验③可知配离子的稳定性:
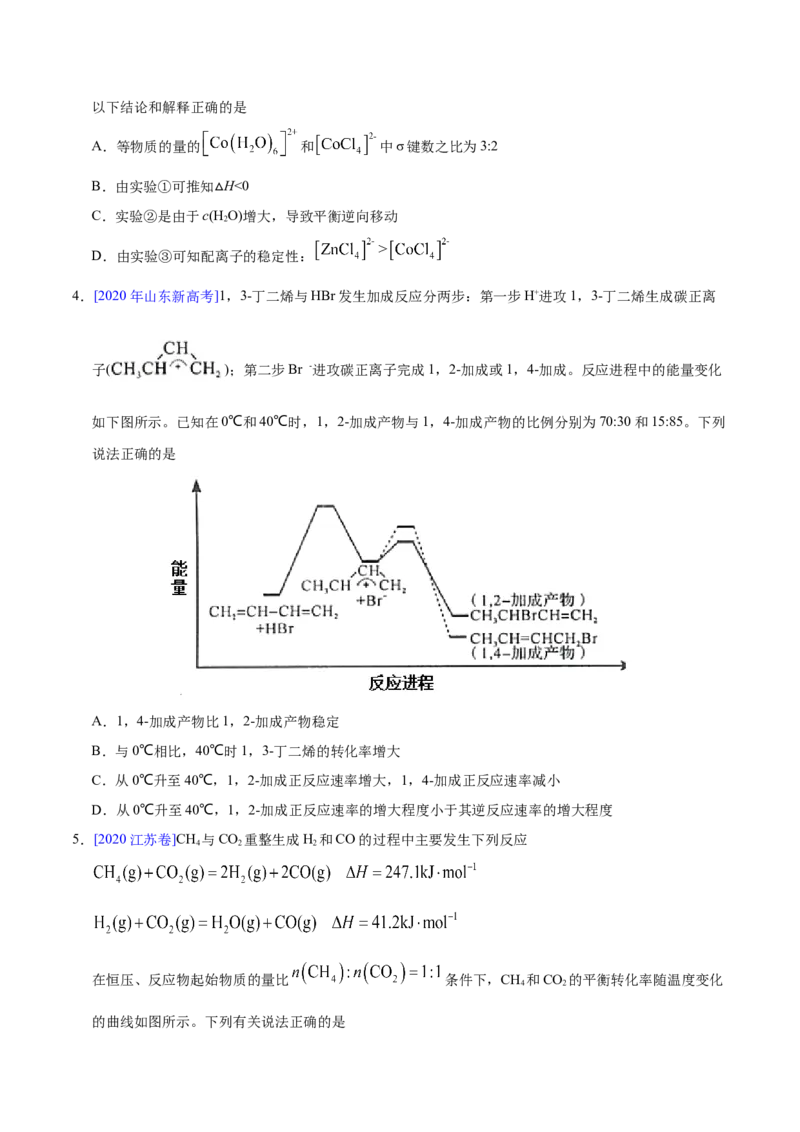
4.[2020年山东新高考]1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离
子( );第二步Br -进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化
如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列
说法正确的是
A.1,4-加成产物比1,2-加成产物稳定
B.与0℃相比,40℃时1,3-丁二烯的转化率增大
C.从0℃升至40℃,1,2-加成正反应速率增大,1,4-加成正反应速率减小
D.从0℃升至40℃,1,2-加成正反应速率的增大程度小于其逆反应速率的增大程度
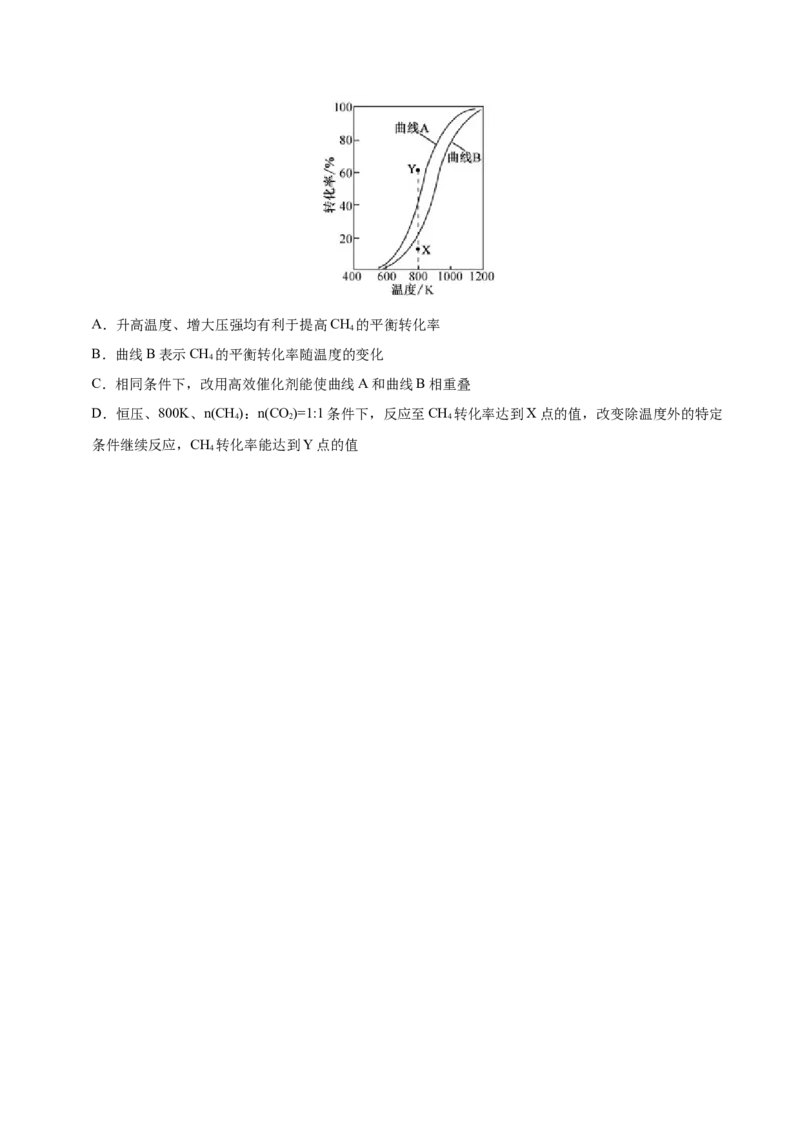
5.[2020江苏卷]CH 与CO 重整生成H 和CO的过程中主要发生下列反应
4 2 2
在恒压、反应物起始物质的量比 条件下,CH 和CO 的平衡转化率随温度变化
4 2
的曲线如图所示。下列有关说法正确的是A.升高温度、增大压强均有利于提高CH 的平衡转化率
4
B.曲线B表示CH 的平衡转化率随温度的变化
4
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800K、n(CH):n(CO)=1:1条件下,反应至CH 转化率达到X点的值,改变除温度外的特定
4 2 4
条件继续反应,CH 转化率能达到Y点的值
4