文档内容
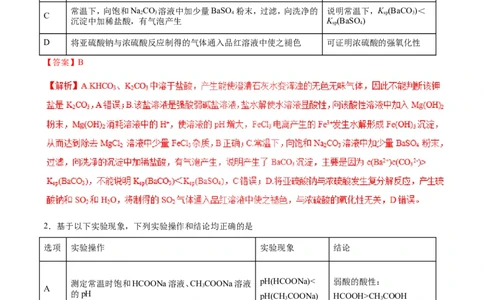
1.下列实验操作与预期实验目的或所得实验结论一致的是
选项 实验操作 实验目的或结论
A 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 说明该钾盐是KCO
2 3
向含有少量FeCl 的MgCl 溶液中加入足量Mg(OH) 粉末,搅拌一 除去MgCl 溶液中少量
B 3 2 2 2
段时间后过滤 FeCl
3
常温下,向饱和NaCO 溶液中加少量BaSO 粉末,过滤,向洗净的 说明常温下,K (BaCO)<
C 2 3 4 sp 3
沉淀中加稀盐酸,有气泡产生 K (BaSO)
sp 4
D 将亚硫酸钠与浓硫酸反应制得的气体通入品红溶液中使之褪色 可证明浓硫酸的强氧化性
【答案】B
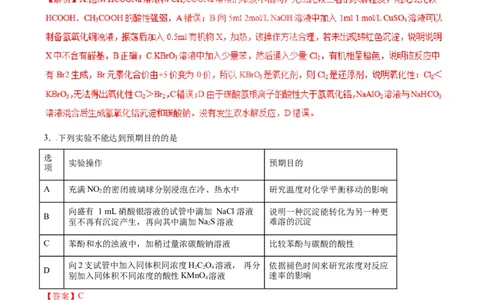
2.基于以下实验现象,下列实验操作和结论均正确的是
选项 实验操作 实验现象 结论
测定常温时饱和HCOONa溶液、CHCOONa溶液 pH(HCOONa)< 弱酸的酸性:
A 3
的pH pH(CH COONa) HCOOH>CH COOH
3 3
向5 mL 2 mol/L的NaOH溶液中加入1 mL 1
未出现砖红色沉
B mol·L-1的CuSO 溶液,振荡后再加入0.5 mL有机 说明X中不含醛基
4 淀
物X,加热C 向KBrO 溶液中加入少量苯,然后通入少量Cl 有机相呈橙红色 氧化性:Cl>Br
3 2 2 2[来源:学科网]
有白色絮状沉淀 二者水解相互促进生成氢
D NaAlO 溶液与NaHCO 溶液混合
2 3 生成 氧化铝沉淀
【答案】B
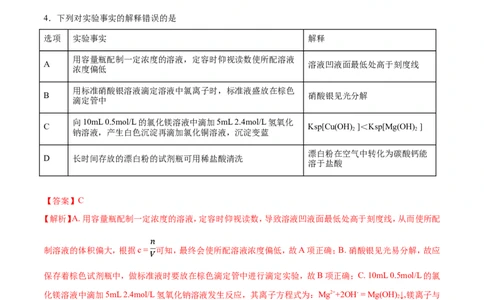
3.下列实验不能达到预期目的的是
选
实验操作 预期目的
项
A 充满NO 的密闭玻璃球分别浸泡在冷、热水中 研究温度对化学平衡移动的影响
2
向盛有 1 mL 硝酸银溶液的试管中滴加 NaCl 溶液 说明一种沉淀能转化为另一种更
B
至不再有沉淀产生,再向其中滴加NaS溶液 难溶的沉淀
2
C 苯酚和水的浊液中,加稍过量浓碳酸钠溶液 比较苯酚与碳酸的酸性
向2支试管中加入同体积同浓度HC O 溶液, 再分 依据褪色时间来研究浓度对反应
D 2 2 4
别加入同体积不同浓度的酸性KMnO 溶液 速率的影响
4
【答案】C4.下列对实验事实的解释错误的是
选项 实验事实 解释
用容量瓶配制一定浓度的溶液,定容时仰视读数使所配溶液
A 溶液凹液面最低处高于刻度线
浓度偏低
用标准硝酸银溶液滴定溶液中氯离子时,标准液盛放在棕色
B 硝酸银见光分解
滴定管中
向10mL 0.5mol/L的氯化镁溶液中滴加5mL 2.4mol/L氢氧化
C Ksp[Cu(OH) ]<Ksp[Mg(OH) ]
钠溶液,产生白色沉淀再滴加氯化铜溶液,沉淀变蓝 2 2
漂白粉在空气中转化为碳酸钙能
D 长时间存放的漂白粉的试剂瓶可用稀盐酸清洗
溶于盐酸
【答案】C
【解析】A. 用容量瓶配制一定浓度的溶液,定容时仰视读数,导致溶液凹液面最低处高于刻度线,从而使所配
制溶液的体积偏大,根据c = 可知,最终会使所配溶液浓度偏低,故A项正确;B. 硝酸银见光易分解,故应
保存着棕色试剂瓶中,做标准液时要放在棕色滴定管中进行滴定实验,故B项正确;C. 10mL 0.5mol/L的氯
化镁溶液中滴加5mL 2.4mol/L氢氧化钠溶液发生反应,其离子方程式为:Mg2++2OH- = Mg(OH) ↓,镁离子与
2
氢氧根离子按物质的量为1:2反应,则反应后氢氧化钠有剩余,再滴加氯化铜溶液,过量的氢氧根离子与铜离
子反应生成了氢氧化铜沉淀,而不是沉淀的转化,因此,不能通过比较其溶度积的大小来解释该现象,故C项
错误;D. 长时间存放的漂白粉会与空气中的二氧化碳反应,其化学方程式为:
Ca(ClO) +CO +H O=CaCO ↓+2HClO,生成的碳酸钙沉淀易溶于稀盐酸中,故D项正确。
2 2 2 3
5.根据下列实验内容得出的结论正确的是
选项 实验内容 结论A 向某溶液中滴加KSCN溶液,溶液变红 该溶液一定含Fe2+
B 向某溶液中滴加盐酸酸化BaCl 溶液,产生白色沉淀 该溶液一定含SO 2-
2 4
向某溶液中滴加NaOH溶液并加热,产生能使湿润的红色石蕊试
C 该溶液一定含NH +
纸变蓝的气体 4
D 向酸性KMnO 溶液中滴加某液体,KMnO 溶液褪色 该溶液一定含SO 2-
4 4 3
【答案】C
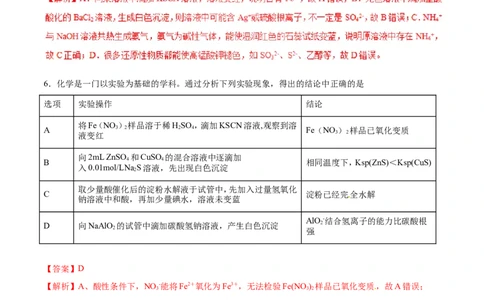
6.化学是一门以实验为基础的学科。通过分析下列实验现象,得出的结论中正确的是
选项 实验操作 结论
将Fe(NO )样品溶于稀HSO ,滴加KSCN溶液,观察到溶
A 3 2 2 4 Fe(NO ) 样品已氧化变质
液变红 3 2
向2mL ZnSO 和CuSO 的混合溶液中逐滴加
B 4 4 相同温度下,Ksp(ZnS)<Ksp(CuS)
入0.01mol/LNa S溶液,先出现白色沉淀
2
取少量酸催化后的淀粉水解液于试管中,先加入过量氢氧化
C 淀粉已经完全水解
钠溶液中和酸,再加少量碘水,溶液未变蓝
[来源:学.科.网Z.X.X.K]
AlO-结合氢离子的能力比碳酸根
D 向NaAlO 的试管中滴加碳酸氢钠溶液,产生白色沉淀 2
2 强
【答案】D
【解析】A、酸性条件下,NO -能将Fe2+氧化为Fe3+,无法检验Fe(NO ) 样品已氧化变质,故A错误;
3 3 2
B、ZnSO 和CuSO 的浓度未知,所以不能根据向2mL ZnSO 和CuSO 的混合溶液中逐滴加入0.01mol/LNa S
4 4 4 4 2
溶液,得出Ksp的大小关系,故B错误;C、取少量酸催化后的淀粉水解液于试管中,先加入过量氢氧化钠溶
液中和酸,再加少量碘水,因为碘可以与过量氢氧化钠反应,若碘反应后没有剩余,即使有淀粉存在,溶液也
不会变蓝,故不能判断淀粉是否完全水解,故C错误;D、向NaAlO 的试管中滴加碳酸氢钠溶液发生反应:
2
AlO-+HCO-+H 0= Al(OH) ↓+ CO2-,所以AlO-结合氢离子的能力比碳酸根强,故D正确。
2 3 2 3 3 2
7.下列设计的实验方案能达到相应实验目的的是
选项 实验目的 实验方案证明反应速率会随反应物浓度的增 用3mL稀硫酸与足量纯锌反应,产生气泡速率较慢,然后加
A
大而加快 入1mL 1mol·L−1CuSO 溶液,迅速产生较多气泡
4
将Fe(NO ) 样品溶于稀硝酸后,滴加KSCN溶液,观察溶液
B 检验Fe(NO ) 晶体是否已氧化变质 3 2
3 2 是否变红
证明“84”消毒液的氧化能力随溶 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同
C
液pH的减小而增强 时加入食醋,红色很快褪为无色
向2mL 0.1mol·L−1硝酸银溶液中加入1mL 0.1
证明氯化银的溶解度大于硫化银的
D
溶解度
mol·L−1 NaCl溶液,出现白色沉淀,再加入几滴0.1mol·L−1的
NaS溶液,有黑色沉淀生成
2
【答案】C
8.仅用下表提供的玻璃仪器(非玻璃仪器任选)就能实现相应实验目的的是
选项 实验目的 玻璃仪器
A 分离乙醇和水的混合物 分液漏斗、烧杯
B 鉴别 NaOH、Al (SO )、NaCO、KNO 四瓶无色溶液 试管、胶头滴管
2 4 3 2 3 3
常温下,用pH =13的NaOH溶液配制100mL、
100mL容量瓶、烧杯、玻璃棒、胶
C
头滴管
pH=12的NaOH溶液
分液漏斗、烧瓶、导管、集气瓶、
D 用MnO 固体和浓盐酸反应制备并收集Cl
2 2 烧杯
【答案】B9.下列气体的检验方法及现象、结论不相符的是
选项 检验方法及现象 结论
A 将气体通入品红溶液中,溶液褪色,加热溶液又变为红色 该气体为SO
2
将气体A通过灼热的CuO,黑色固体变红色,将产生的气
B 气体A为CO
体(密度大于空气的)通入澄清石灰中,澄清石灰水变浑浊
点燃气体B,火焰呈淡蓝色,将产生的气体通入无水
C 气体B为H
CuSO ,无水CuSO 变蓝色 2
4 4
D 用湿润的紫色石蕊试纸检验某气体,试纸先变红色,后褪色 该气体为Cl
2
【答案】C
【解析】A.SO 使品红溶液褪色,加热溶液又变为红色,故A不符合题意;B.CO+CuO Cu+CO ,黑色固体变
2 2
红色,将产生的CO 通入澄清石灰水中,生成CaCO ,澄清石灰水变浑浊,故B不符合题意;C.CH 、H 等气体
2 3 4 2
燃烧时,火焰均呈淡蓝色,均生成HO(g),可使无水CuSO 变蓝色,故C符合题意;D.Cl +H O HCl+HClO,
2 4 2 2
HCl使湿润的紫色石蕊试纸变红色,HClO使其褪色,D项不符合题意。
10.根据下列实验操作及现象推出的结论一定正确的是
选项 操作及现象 结论
A 向酸性KMnO 溶液中滴加HO 溶液至紫色褪去 氧化性:HO >KMnO
4 2 2 2 2 4
在CaCO 中加浓盐酸并将反应后所得气体直接通入NaSiO 溶液中,
B 3 2 3 酸性:HCO> H SiO
溶液变浑浊 2 3 2 3
C 向NaS溶液中滴加盐酸产生臭鸡蛋气味的气体 非金属性Cl>S
2
将FeCl 足量溶液滴加到Mg(OH) 悬浊液中,充分震荡,悬浊液由白色 溶解度
D 3 2
变为红褐色 Mg(OH) >Fe(OH)
2 3
【答案】D11.下列根据实验操作、现象及结论均正确的是
选项 实验操作 实验现象 实验结论
将石蜡油催化分解产生的气体通入酸
A 酸性高锰酸钾溶液褪色 该气体为乙烯
性高锰酸钾溶液中
先出现 白色沉淀,最终
B 向NaAlO 溶液中持续通入气体Y Y可能是CO 气体
2 沉淀又溶解 2
向等量同浓度的HO 溶液中分别加 加FeCl 溶液的HO 产 Fe3+对HO 分解的催化效果
C 2 2 3 2 2 2 2
入CuCl 、FeCl 溶液 生气泡较快 较好
2 3
取CHOONa溶液于试管中并加入几 CHCOONa溶液显碱性且存
D 3 溶液红色加深 3
滴酚酞,再加热 在水解平衡
【答案】D
12.下列实验操作与预期实验目的或所得实验结论一致的是
选项 实验操作 实验目的或结论
A 将溴乙烷与氢氧化钠溶液共热一段时间,再 检验水解产物中的溴离子向冷却后的混合液中滴加硝酸银溶液
向乙醇溶液中加入新制的银氨溶液,用酒精
B 确定乙醛中是否含有醛基
灯直接加热
C 向苯和酒精的混合液中加入金属钠 确定苯中是否有酒精
C HOH与浓硫酸170℃共热,制得的气体通
D 2 5 检验制得气体是否为乙烯
入酸性KMnO 溶液
4
【答案】C
13.对下列现象或事实的解释正确的是
选项 操作、现象或事实 解释或结论
A 常温下,饱和亚硫酸钠溶液的pH小于饱和碳酸钠溶液 常温下NaCO 水解程度大于NaSO
2 3 2 3
向FeCl 溶液中滴入几滴30%的HO 溶液,有气体产 FeCl 能催化过氧化氢分解,该分解反
B 3 2 2 3
生,一段时间后,溶液颜色加深 应为放热反应
一定是木炭与浓硝酸反应生成NO 呈
C 灼热的木炭放入浓硝酸中,放出红棕色气体 2
红棕色
向2.0mL1.0mo1·L-1的NaOH溶液中先加入3滴
说明Mg(OH) 沉淀可以转化为
D 1.0mo1·L-1MgCl 溶液,出现白色沉淀,再加入3滴 2
2 Fe(OH) 沉淀
1.0mo1·L-1FeCl 溶液产生红褐色沉淀。 3
3
【答案】B
【解析】A.饱和溶液的浓度不同,不能比较弱酸根的水解程度,应比较等浓度溶液的pH才能比较弱酸根的水
解程度,故A项错误;B.有气体产生,一段时间后溶液颜色加深,则过氧化氢分解生成氧气,并放热,则Fe3+能催化 HO 分解且该分解反应为放热反应,故B项正确;C.浓硝酸不稳定,易分解生成二氧化氮,可能
2 2
为硝酸的分解生成的二氧化氮,所以不一定是木炭与浓硝酸反应生成NO 呈红棕色,故D错误; D.氢氧化
2
钠过量,氢氧化钠和氯化镁、氯化铁反应都生成沉淀,所以不能证明Mg(OH)沉淀可以转化为Fe(OH)沉
2 3
淀,应利用沉淀的转化比较Ksp故D项错误。
14.下列实验目的、实验操作及推论均正确的是
选项 实验目的 实验操作及推论
用酸式滴定管量取25.00mL 18.4mol/L硫酸,加入250mL容量瓶
A 配制1.84mol/L的硫酸
中,加水定容至刻度线
用聚光束照射淀粉溶液看到一条光亮的通路,可推测淀粉分子的
B 检验淀粉分子的直径
直径大于10-7m
向该无色溶液中滴加氯化铁溶液和四氯化碳,振荡后静置,下层
C 检验某无色溶液中是否含有I-
呈紫色,可确定原溶液中含有I-
D 证明二氧化硫具有还原性 将二氧化硫通入氨水和BaCl 的混合溶液中,有白色沉淀生成
2
【答案】C
15.下列实验操作、现象和结论均正确的是( )
实验操作 实验现象 实验结论
A. 向某溶液中滴加K[Fe(CN) ]溶液 产生蓝色沉淀 该溶液中有Fe2+,无Fe3+
3 6
将溴乙烷与NaOH醇溶液加热反应产生的气 试管中的溶液紫色褪 溴乙烷发生了消去反应,
B.
体通入盛有酸性高锰酸钾的试管中 去 生成了乙烯气体
向蔗糖与稀硫酸加热反应后的溶液中先加入
C. 过量的NaOH溶液,再加入少量新制的氢氧化
溶液中产生砖红色沉
蔗糖水解产生了葡萄糖
铜悬浊液,加热5分钟 淀
铝箔熔化,失去光泽并
D. 用坩埚钳夹住一块铝箔在酒精灯上加热
滴落下来
金属铝的熔点较低
【答案】C【解析】A.实验结论错误,滴加K[Fe(CN)]溶液,生成蓝色沉淀是亚铁离子特征反应现象,但是不能证明没
3 6
有铁离子,还需要补加实验,验证铁离子存在与否,故A不正确;B.实验操作设计有问题,乙醇易挥发进入酸
性高锰酸钾溶液,与高锰酸钾发生氧化还原反应,使其褪色,干扰乙烯的测定,故B不正确;C.蔗糖水解生成
葡萄糖,先加入氢氧化钠调节pH至碱性,再加新制氢氧化铜,由于葡萄糖属于还原性糖含有醛基与新制氢氧
化铜反应生成砖红色沉淀氧化亚铜,故C正确;D.实验现象错误,氧化铝的熔点高于金属铝,铝箔熔化,失去
光泽但由于外面包了一层氧化铝并不滴落下来,故D不正确。
16.下列根据实验操作和现象所得出的结论不正确的是:
选项 实验操作与现象 结论
向鸡蛋清溶液中滴加醋酸铅溶液,产生白色沉淀,加水沉
A 蛋白质发生了变性
淀不消失
测定浓度均为0.1mol·L-1 Na CO 与NaSO 溶液的pH,
B 2 3 2 3 非金属性:S > C
NaCO 溶液的pH较大
2 3
C 苯酚的浊液中加入碳酸钠溶液,溶液变为无色 酸性:苯酚 > 碳酸氢钠溶液
向盛有Fe(NO ) 溶液的试管中加入0.1 mol·L-1的稀硫酸,
D 3 2 溶液中NO -被Fe2+还原为NO
试管口出现红棕色气体 3
【答案】B
17.下列选项中的操作、现象与结论完全一致的是( )
选项 操作 现象 结论
A 将苯滴入溴水中,振荡、静置 溴水层褪色 溴和苯发生加成反应
无水乙醇与浓硫酸共热至170℃,将产生气
B 溴水褪色 乙烯和溴水发生加成
体通入溴水
C 向CuSO 溶液中通入HS 出现黑色沉淀 酸性:HS>HSO
4 2 2 2 4
D 向AgCl 悬浊液中滴加饱和NaS 溶液 有黑色沉淀产生 Ksp(Ag S)< Ks(AgCl)
2 2【答案】D
18.用如图所示装置进行实验一将①滴入②中,②中实验现象和反应类型不完全正确的是
选项 ① ② ②中实验现象和反应类型 实验装置
A 苯 溴水 溴水橙色褪去,液体分层。加成反应
B 浓盐酸 浓硫酸 产生大量白雾。物理变化
[来源:Zxxk.Com][来源:Z#xx#k.Com] [来源:学|科|网]
C 双氧水 MnO 产生大量气泡。分解反应
2
D 浓硝酸 铜粉 产生红粽色气体。氧化还原反应
【答案】A
【解析】A、利用Br 单质易溶于苯,苯萃取溴水中溴单质,而使溴水褪色,属于物理变化,故A符合题意;
2
B、浓硫酸遇水放出大量的热,浓盐酸受热易挥发,属于物理变化,故B不符合题意;C、MnO 作催化剂,使
2
HO 分解成HO和O,故C不符合题意;D、铜与浓硝酸发生Cu+4HNO(浓)=Cu(NO)+2NO ↑+2HO,
2 2 2 2 3 3 2 2 2
产生红棕色气体NO ,该反应属于氧化还原反应,故D不符合题意。
2
19.下列实验操作、实验现象和实验结论均正确的是
选项 实验操作 实验现象 实验结论
将Fe(NO ) 样品溶于稀硫酸,滴加
A 3 2 溶液变红 稀硫酸能氧化Fe2+
KSCN溶液
B 向KMnO 酸性溶液中滴加乙二酸 溶液褪色 乙二酸具有氧化性
4
Ag+与NH ·H O能
C 向AgNO 溶液中滴加过量氨水 得到澄清溶液 3 2
3 大量共存
向1 mL 0.1 mol·L-1 Na S溶液中滴入
2 开始有白色沉淀生成;
D 2 mL 0.1 mol·L-1 ZnSO 溶液,再加入 K (CuS)HCO-
NaHCO 溶液的pH 为8 3
3
用坩埚钳夹住一小块用砂纸打磨过
C 熔化后的液态铝滴落下来 金属铝的熔点低
的铝箔在酒精灯上加热
两种气体使溴水褪色的
D 分别将乙烯与SO 通入溴水中 溴水均褪色
2 原理相同
【答案】B
21.下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
取1mL20%的淀粉溶液,加入适量稀硫
酸,水浴加热后取少量溶液,加入氢氧
A 溶液中出现砖红色沉淀 淀粉完全水解
化钠使溶液呈碱性,再加入几滴新制
Cu(OH) 悬浊液,加热
2
B 向NaSiO 溶液中滴加稀盐酸 产生白色胶状沉淀 非金属性:Cl>Si
2 3
C 向盛有2mL0.1mol/L的NaCl溶液的试 先产生白色沉淀,后白 Ksp(AgCl)>Ksp(AgI)管 中逐滴加入几滴0.1mol/L的
AgNO 溶液,充分反应后,再逐滴加入 色沉淀变为黄色沉淀
3
0.1mol/L的KI溶液
向待测液中加入适量的稀NaOH溶液, 湿润的蓝色石蕊试纸未 在待测液中不存在
D
将湿润的蓝色石蕊试纸放在试管口 变红 NH +
4
【答案】C
【解析】A、取1mL20%的淀粉溶液,加入适量稀硫酸,水浴加热后取少量溶液,加入氢氧化钠使溶液呈碱性,
再加入几滴新制Cu(OH) 悬浊液,加热 ,溶液中出现砖红色沉淀,说明溶液中含有葡萄糖,有淀粉水解,但不
2
能说明淀粉已完全水解,若要检验淀粉完全水解只需滴加几滴碘水,若溶液不变蓝则说明淀粉完全水解,选
项A错误;B.向硅酸钠溶液中滴加盐酸,有白色胶状沉淀生成,说明酸性盐酸大于硅酸,由于盐酸不是最高
价含氧酸,无法判断Cl、Si元素的非金属性,选项B错误;C.沉淀向更难溶的方向转化,Ksp(AgCl)>Ksp
(AgI),选项C正确;D、根据铵根离子时需要加热,选项中没有加热,不能确定一定不含铵根离子,故还可能
含有铵根离子,选项D错误。
22.下列设计的实验方案能达到相应实验目的的是
选项 实验目的 实验方案
证明“84”消毒液的氧化能力 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入
A
随溶液pH的减小而增强 食醋,红色很快褪为无色
证明反应速率会随反应物浓 用3 mL稀硫酸与足量纯锌反应,产生气泡速率较慢,然后加入1mL
B
度的增大而加快 1mol•L-1CuSO 溶液,迅速产生较多气泡
4
证明碳和浓硫酸共热生成的
C 将生成的气体直接通入澄清石灰水,有白色沉淀生成
气体中含有二氧化碳
证明氯化银的溶解度大于硫 向2 mL 0.1 mol•L-1硝酸银溶液中加入1mL 0.1mol•L-1 NaCl溶液,出
D
化银的溶解度 现白色沉淀,再加入几滴0.1 mol•L-1的NaS溶液,有黑色沉淀生成
2
【答案】A23.根据下列实验操作和现象所得出的结论错误的是
操作 现象 结论
蔗糖变成疏松多孔的海绵状 浓硫酸具有脱水性和强氧化
A 向蔗糖中加入浓硫酸
碳 性
溶液变成棕黄色,一段时间后
向盛有HO 溶液的试管加入几
B 2 2 溶液中有气泡出现,随后有红 Fe2+催化HO 分解产生O
滴酸化的硫酸亚铁溶液 2 2 2
褐色沉淀生成
铝片先用砂纸打磨,再加入到浓 浓硝酸具有强氧化性,常温
C 无明显现象
硝酸中 下,铝被浓硝酸钝化
向浓度均为0.1mol・L—1的
D KC1、KI混合液中逐滴滴加 出现黄色沉淀 K (AgCl)>K (AgI)
sp sp
AgNO 溶液
3
【答案】B
24.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 实验 现象 结论
A 将氯气通入品红溶液 溶液红色褪去 氯气具有漂白性
B 将铜粉加入1.0mol•L﹣1 溶液变蓝,有黑色固体出现 金属Fe比Cu活泼的Fe (SO ) 溶液中
2 4 3
用坩埚钳夹住用砂纸仔细
C 打磨过的铝箔在酒精灯上 熔化后的液态铝滴落下来 金属铝的熔点比较低
加热
浓硝酸中铜片很快开始溶解,并放出
向盛有少量浓硝酸、稀硝酸
红棕色气体;稀硝酸中过一会铜片表 浓硝酸氧化性强于稀硝
D 的两支试管中分别加入一
面才出现无色气体,气体遇空气变红 酸
片大小相同的铜片
棕色
【答案】D
【解析】A.品红褪色是生成次氯酸的原因,氯气不具有漂白性,A错误;B.铜和铁离子反应生成铜离子和亚铁
离子,没有黑色固体生成,现象描述错误,B错误;C.由于在表面生成熔点更高的氧化铝,铝箔熔化但不滴落,
现象描述错误,C错误;D.硝酸的浓度越大,氧化性越强,实验现象、结论描述正确,D正确。
25.下列实验“操作和现象”与“结论”都正确的是
选
操作和现象 结论
项
向盛有2mL0.1mol/LAgNO 溶液的试管中,先滴几滴0.1mol/LKCl溶液,
A 3 Ksp(AgCl)>Ksp(AgI)
再滴加0.1mol/LKI溶液。试管先出现白色沉淀,后出现淡黄色沉淀
Fe(NO ) 与HSO 不反
B 向装有Fe(NO ) 溶液的试管中加入几滴稀HSO 溶液,溶液颜色基本不变 3 2 2 4
3 2 2 4 应
在KI溶液中滴加少量氯水,再加入CCl ,充分振荡,液体分层,下层溶液
C 4 氯的非金属性比碘强
呈紫红色
用pH试纸测定同浓度的NaClO溶液和CHCOONa溶液的pH, 弱酸的酸性:
D 3
pH(NaClO)>pH(CH COONa) HClO