文档内容
专题 10 水溶液中的离子平衡
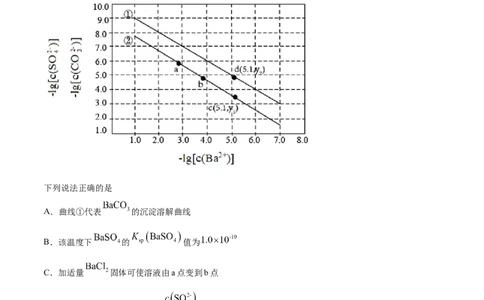
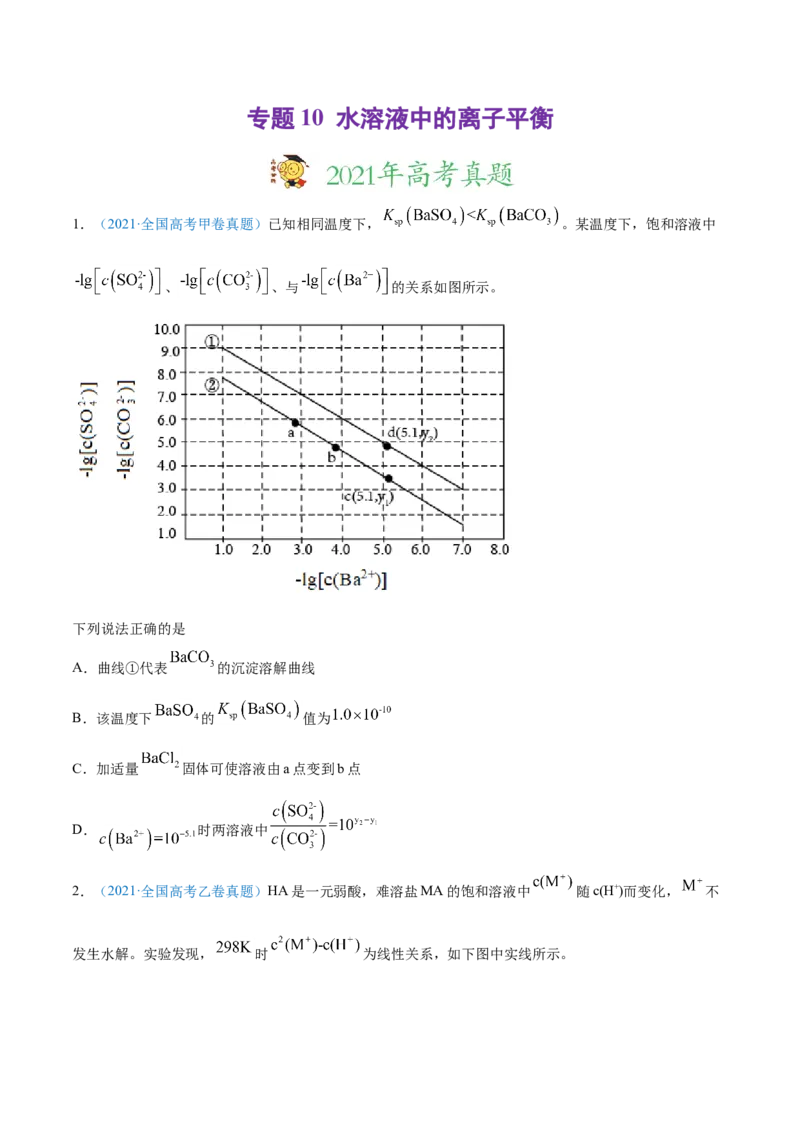
1.(2021·全国高考甲卷真题)已知相同温度下, 。某温度下,饱和溶液中
、 、与 的关系如图所示。
下列说法正确的是
A.曲线①代表 的沉淀溶解曲线
B.该温度下 的 值为
C.加适量 固体可使溶液由a点变到b点
D. 时两溶液中
2.(2021·全国高考乙卷真题)HA是一元弱酸,难溶盐MA的饱和溶液中 随c(H+)而变化, 不
发生水解。实验发现, 时 为线性关系,如下图中实线所示。下列叙述错误的是
A.溶液 时,
B.MA的溶度积度积
C.溶液 时,
D.HA的电离常数
3.(2021·广东高考真题)鸟嘌呤( )是一种有机弱碱,可与盐酸反应生成盐酸盐(用 表示)。已知
水溶液呈酸性,下列叙述正确的是
A. 水溶液的
B. 水溶液加水稀释, 升高
C. 在水中的电离方程式为:
D. 水溶液中:
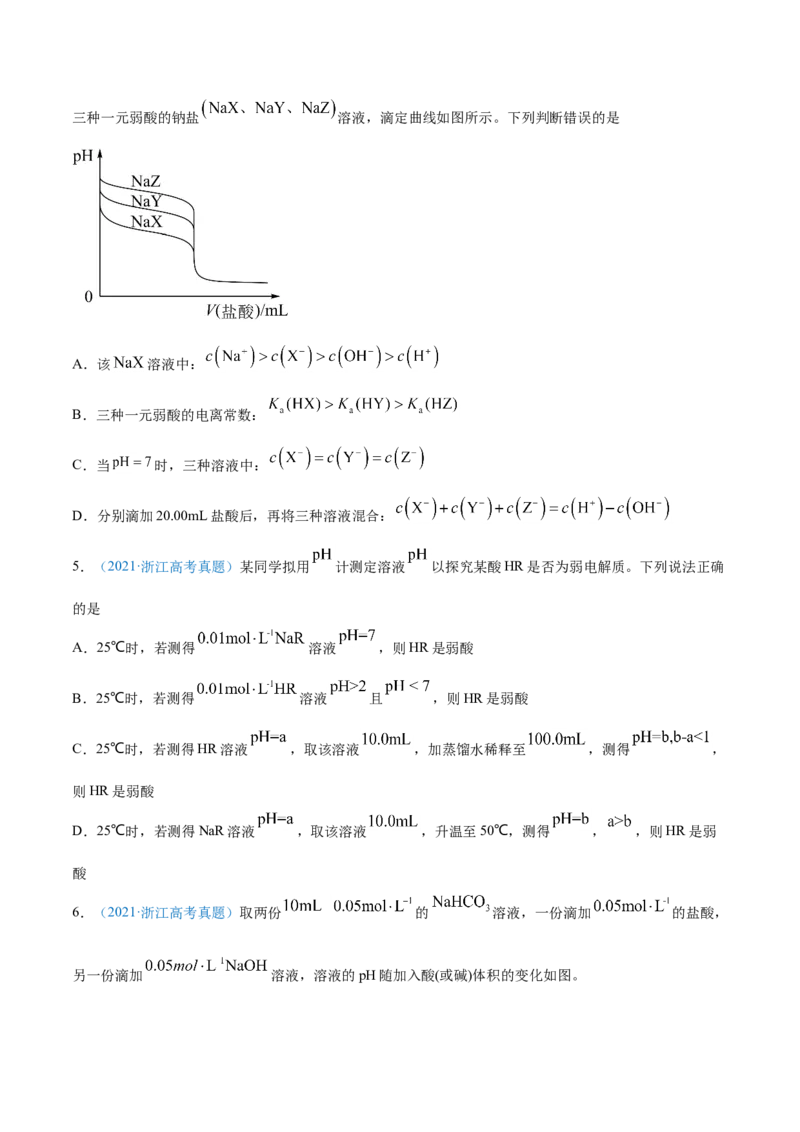
4.(2021·湖南高考真题)常温下,用 的盐酸分别滴定20.00mL浓度均为三种一元弱酸的钠盐 溶液,滴定曲线如图所示。下列判断错误的是
A.该 溶液中:
B.三种一元弱酸的电离常数:
C.当 时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
5.(2021·浙江高考真题)某同学拟用 计测定溶液 以探究某酸HR是否为弱电解质。下列说法正确
的是
A.25℃时,若测得 溶液 ,则HR是弱酸
B.25℃时,若测得 溶液 且 ,则HR是弱酸
C.25℃时,若测得HR溶液 ,取该溶液 ,加蒸馏水稀释至 ,测得 ,
则HR是弱酸
D.25℃时,若测得NaR溶液 ,取该溶液 ,升温至50℃,测得 , ,则HR是弱
酸
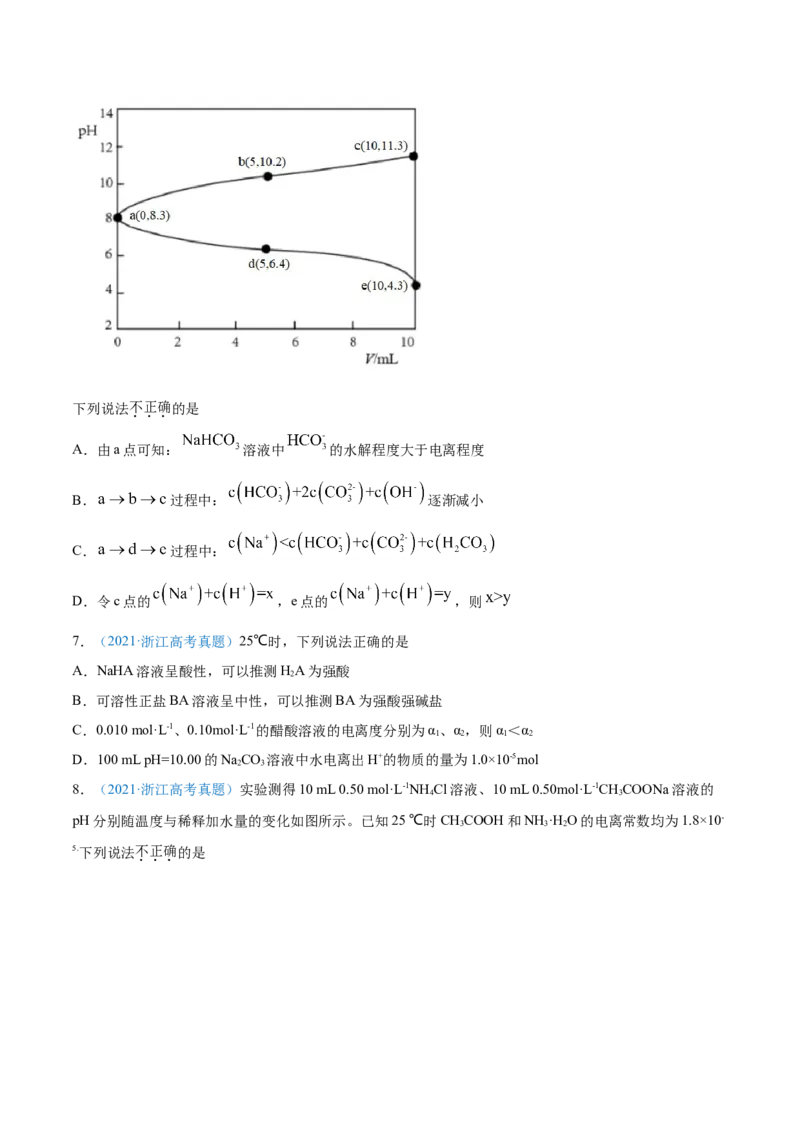
6.(2021·浙江高考真题)取两份 的 溶液,一份滴加 的盐酸,
另一份滴加 溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法不正确的是
A.由a点可知: 溶液中 的水解程度大于电离程度
B. 过程中: 逐渐减小
C. 过程中:
D.令c点的 ,e点的 ,则
7.(2021·浙江高考真题)25℃时,下列说法正确的是
A.NaHA溶液呈酸性,可以推测HA为强酸
2
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 mol·L-1、0.10mol·L-1的醋酸溶液的电离度分别为α 、α ,则α <α
1 2 1 2
D.100 mL pH=10.00的NaCO 溶液中水电离出H+的物质的量为1.0×10-5mol
2 3
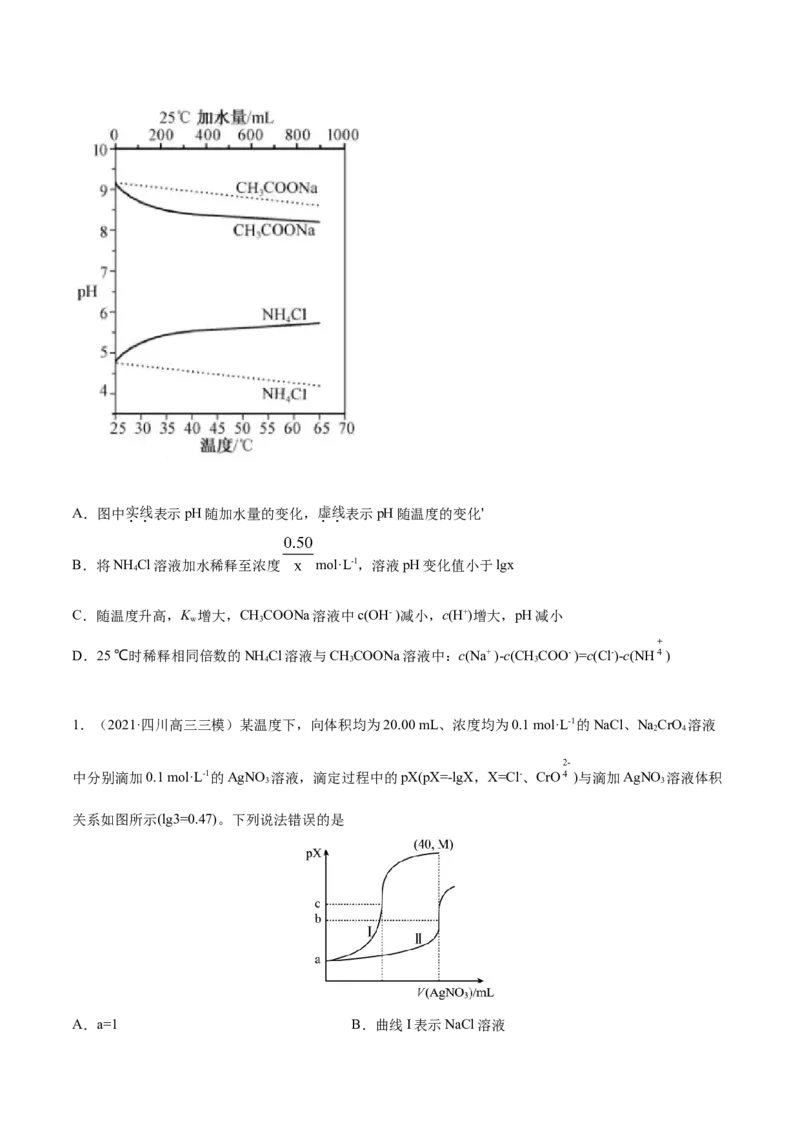
8.(2021·浙江高考真题)实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶液的
4 3
pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均为1.8×10-
3 3 2
5.下列说法不正确的是A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B.将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH变化值小于lgx
4
C.随温度升高,K 增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D.25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH )
4 3 3
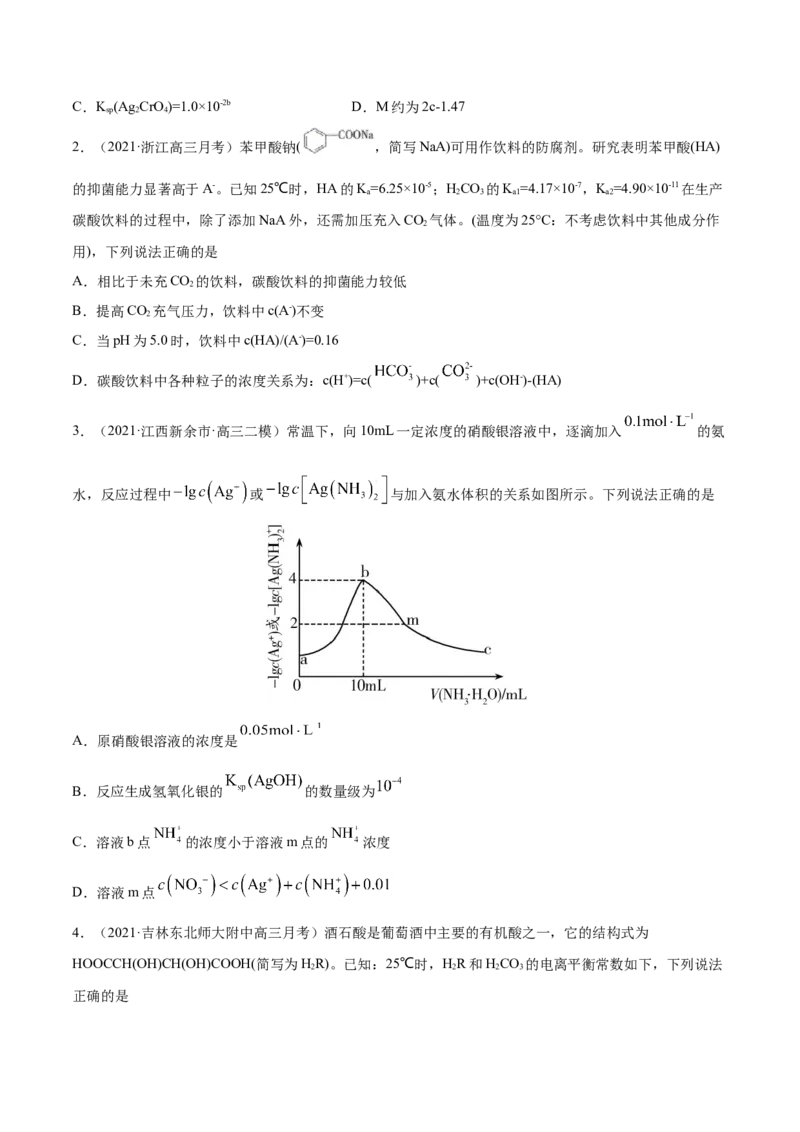
1.(2021·四川高三三模)某温度下,向体积均为20.00 mL、浓度均为0.1 mol·L-1的NaCl、NaCrO 溶液
2 4
中分别滴加0.1 mol·L-1的AgNO 溶液,滴定过程中的pX(pX=-lgX,X=Cl-、CrO )与滴加AgNO 溶液体积
3 3
关系如图所示(lg3=0.47)。下列说法错误的是
A.a=1 B.曲线I表示NaCl溶液C.K (Ag CrO)=1.0×10-2b D.M约为2c-1.47
sp 2 4
2.(2021·浙江高三月考)苯甲酸钠( ,简写NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)
的抑菌能力显著高于A-。已知25℃时,HA的K=6.25×10-5;HCO 的K =4.17×10-7,K =4.90×10-11在生产
a 2 3 a1 a2
碳酸饮料的过程中,除了添加NaA外,还需加压充入CO 气体。(温度为25°C:不考虑饮料中其他成分作
2
用),下列说法正确的是
A.相比于未充CO 的饮料,碳酸饮料的抑菌能力较低
2
B.提高CO 充气压力,饮料中c(A-)不变
2
C.当pH为5.0时,饮料中c(HA)/(A-)=0.16
D.碳酸饮料中各种粒子的浓度关系为:c(H+)=c( )+c( )+c(OH-)-(HA)
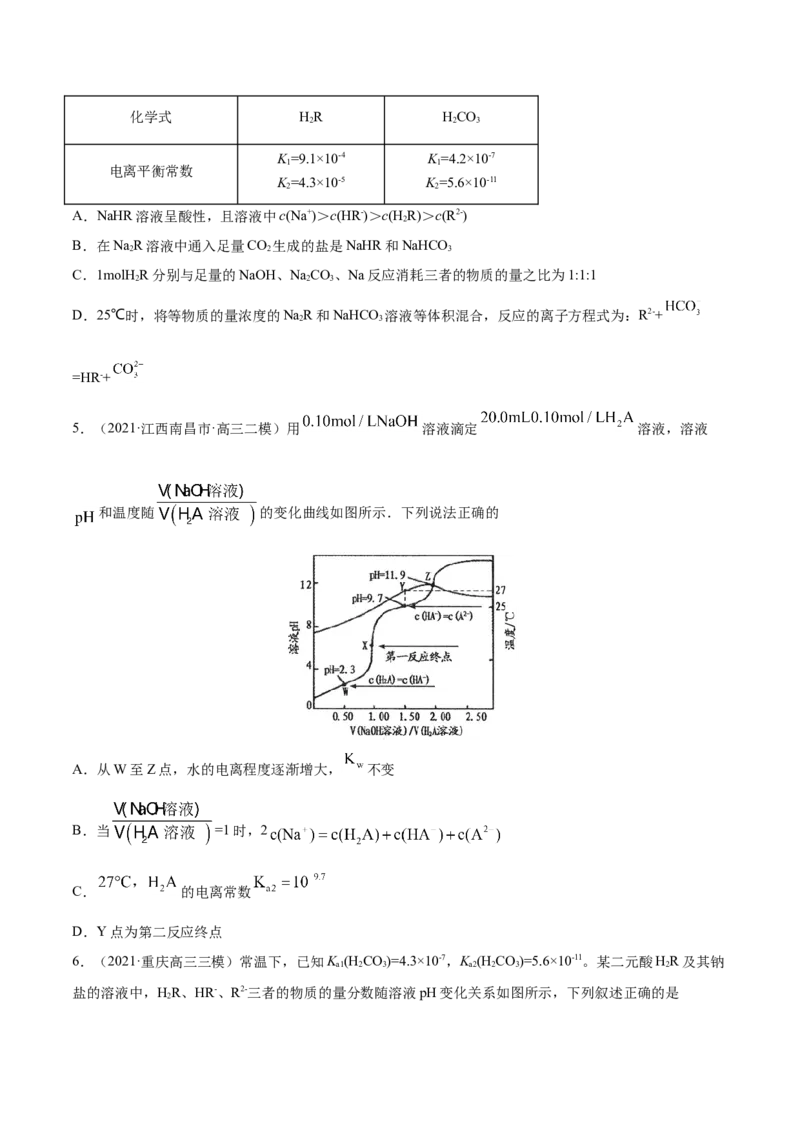
3.(2021·江西新余市·高三二模)常温下,向10mL一定浓度的硝酸银溶液中,逐滴加入 的氨
水,反应过程中 或 与加入氨水体积的关系如图所示。下列说法正确的是
A.原硝酸银溶液的浓度是
B.反应生成氢氧化银的 的数量级为
C.溶液b点 的浓度小于溶液m点的 浓度
D.溶液m点
4.(2021·吉林东北师大附中高三月考)酒石酸是葡萄酒中主要的有机酸之一,它的结构式为
HOOCCH(OH)CH(OH)COOH(简写为HR)。已知:25℃时,HR和HCO 的电离平衡常数如下,下列说法
2 2 2 3
正确的是化学式 HR HCO
2 2 3
K =9.1×10-4 K =4.2×10-7
1 1
电离平衡常数
K =4.3×10-5 K =5.6×10-11
2 2
A.NaHR溶液呈酸性,且溶液中c(Na+)>c(HR-)>c(H R)>c(R2-)
2
B.在NaR溶液中通入足量CO 生成的盐是NaHR和NaHCO
2 2 3
C.1molH R分别与足量的NaOH、NaCO、Na反应消耗三者的物质的量之比为1:1:1
2 2 3
D.25℃时,将等物质的量浓度的NaR和NaHCO 溶液等体积混合,反应的离子方程式为:R2-+
2 3
=HR-+
5.(2021·江西南昌市·高三二模)用 溶液滴定 溶液,溶液
和温度随 的变化曲线如图所示.下列说法正确的
A.从W至Z点,水的电离程度逐渐增大, 不变
B.当 =1时,2
C. 的电离常数
D.Y点为第二反应终点
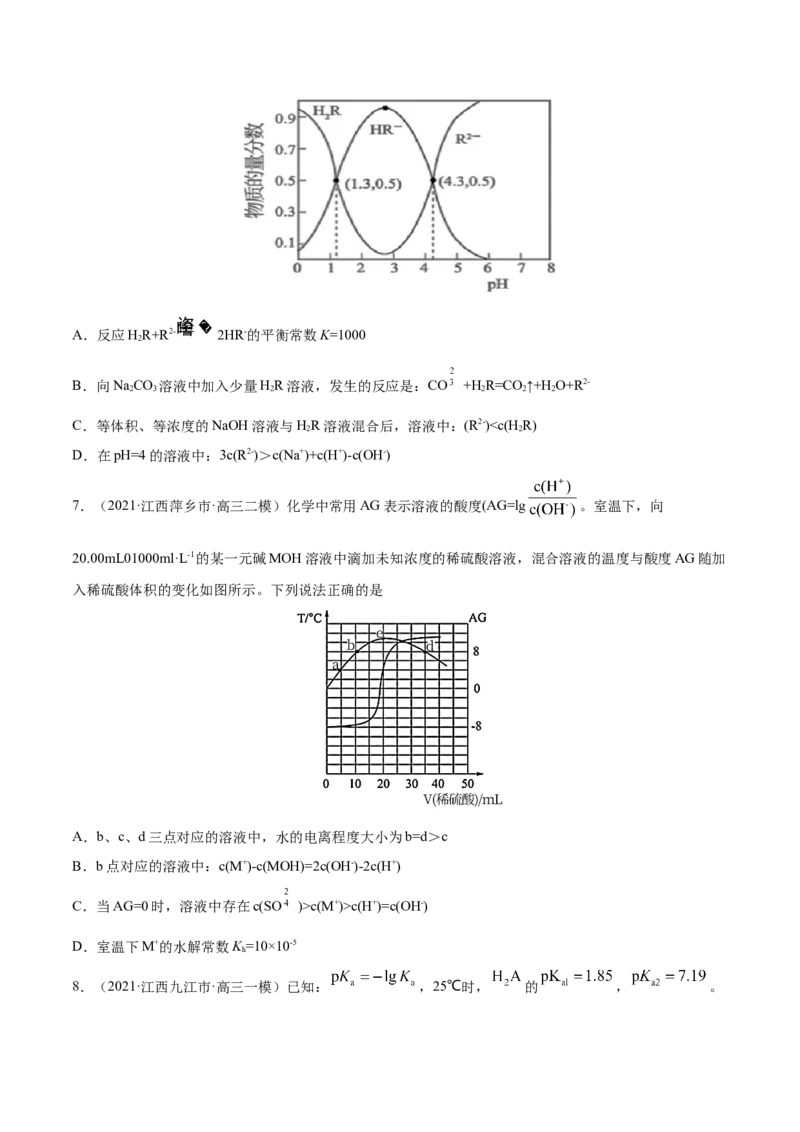
6.(2021·重庆高三三模)常温下,已知K (H CO)=4.3×10-7,K (H CO)=5.6×10-11。某二元酸HR及其钠
a1 2 3 a2 2 3 2
盐的溶液中,HR、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述正确的是
2A.反应HR+R2- 2HR-的平衡常数K=1000
2
B.向NaCO 溶液中加入少量HR溶液,发生的反应是:CO +H R=CO ↑+H O+R2-
2 3 2 2 2 2
C.等体积、等浓度的NaOH溶液与HR溶液混合后,溶液中:(R2-)c(M+)>c(H+)=c(OH-)
D.室温下M+的水解常数K =10×10-5
h
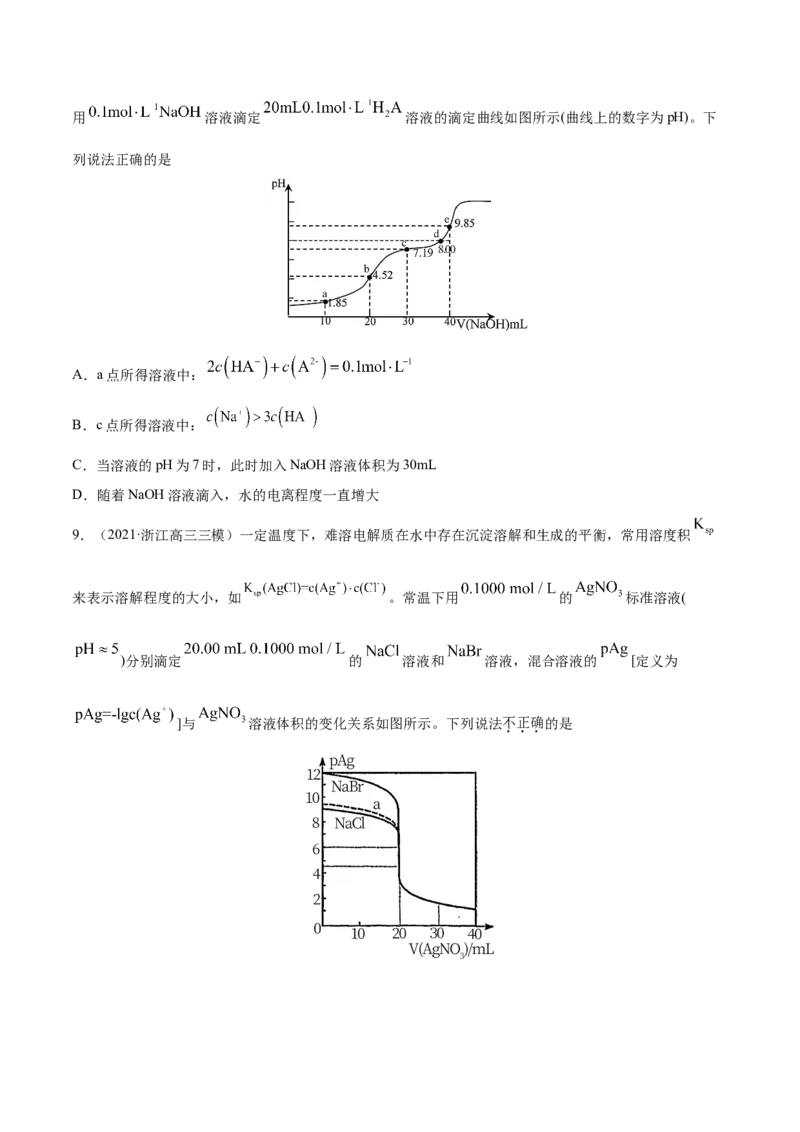
8.(2021·江西九江市·高三一模)已知: ,25℃时, 的 , 。用 溶液滴定 溶液的滴定曲线如图所示(曲线上的数字为pH)。下
列说法正确的是
A.a点所得溶液中:
B.c点所得溶液中:
C.当溶液的pH为7时,此时加入NaOH溶液体积为30mL
D.随着NaOH溶液滴入,水的电离程度一直增大
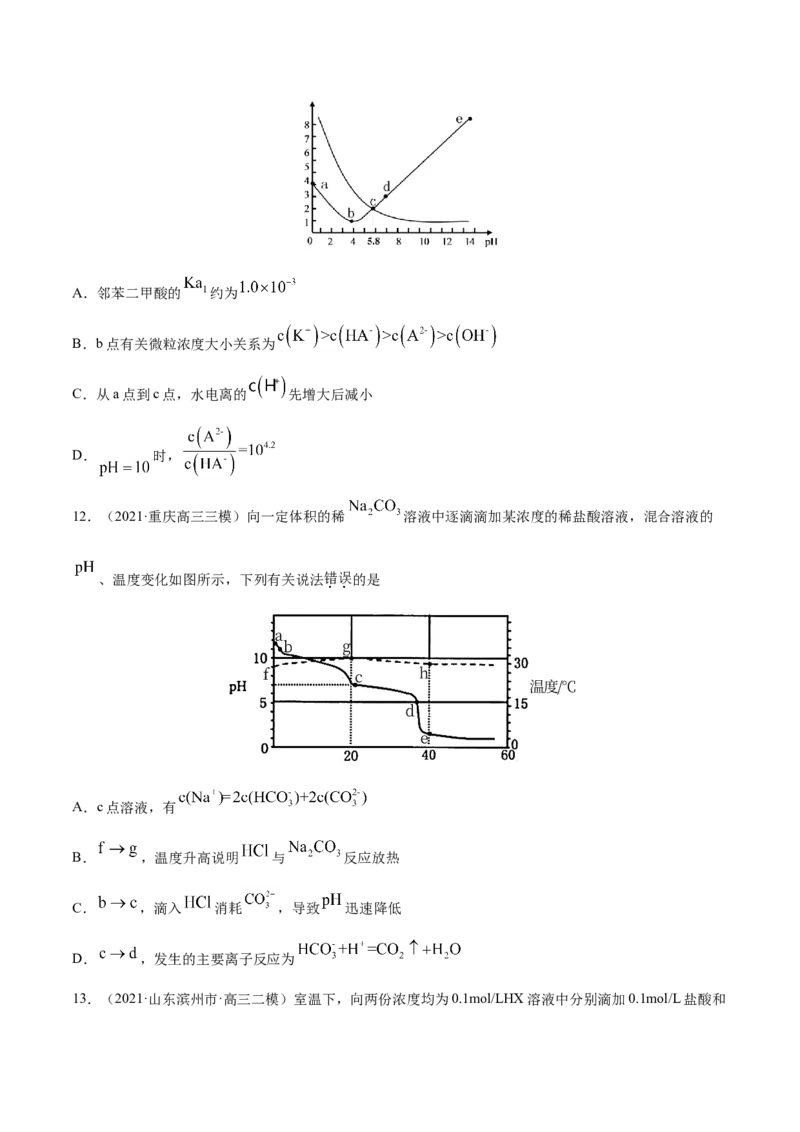
9.(2021·浙江高三三模)一定温度下,难溶电解质在水中存在沉淀溶解和生成的平衡,常用溶度积
来表示溶解程度的大小,如 。常温下用 的 标准溶液(
)分别滴定 的 溶液和 溶液,混合溶液的 [定义为
]与 溶液体积的变化关系如图所示。下列说法不正确的是A.
B.当 时, 溶液中:
C.当 时, 溶液中:
D.相同实验条件下,若改用 溶液,则滴定曲线(滴定终点前)可能变为
10.(2021·河南高三三模)常温下,铁的氢氧化物 ( 或3)的沉淀溶解平衡与溶液pH的关系
如图所示,其中 。下列叙述错误的是
A.Ⅰ表示 的曲线
B. 的
C.在Y点通入足量的 将达到R点(忽略溶液体积变化)
D.在Q点加水稀释可能移到M点
11.(2021·山东潍坊市·高三模拟) 时,向 邻苯二甲酸 溶液中加入 固
体,混合溶液的pH随 以及 的关系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发).
下列有关叙述错误的是A.邻苯二甲酸的 约为
B.b点有关微粒浓度大小关系为
C.从a点到c点,水电离的 先增大后减小
D. 时,
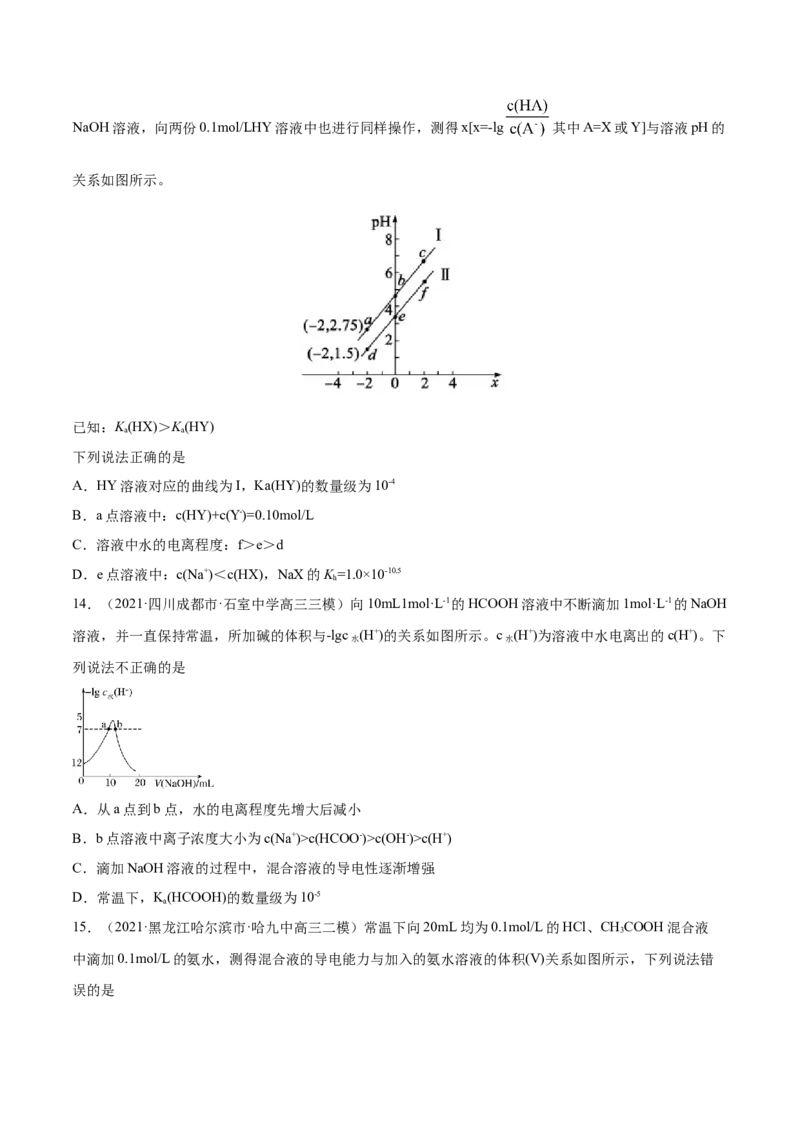
12.(2021·重庆高三三模)向一定体积的稀 溶液中逐滴滴加某浓度的稀盐酸溶液,混合溶液的
、温度变化如图所示,下列有关说法错误的是
A.c点溶液,有
B. ,温度升高说明 与 反应放热
C. ,滴入 消耗 ,导致 迅速降低
D. ,发生的主要离子反应为
13.(2021·山东滨州市·高三二模)室温下,向两份浓度均为0.1mol/LHX溶液中分别滴加0.1mol/L盐酸和NaOH溶液,向两份0.1mol/LHY溶液中也进行同样操作,测得x[x=-lg 其中A=X或Y]与溶液pH的
关系如图所示。
已知:K(HX)>K(HY)
a a
下列说法正确的是
A.HY溶液对应的曲线为I,Ka(HY)的数量级为10-4
B.a点溶液中:c(HY)+c(Y-)=0.10mol/L
C.溶液中水的电离程度:f>e>d
D.e点溶液中:c(Na+)<c(HX),NaX的K =1.0×10-10.5
h
14.(2021·四川成都市·石室中学高三三模)向10mL1mol·L-1的HCOOH溶液中不断滴加1mol·L-1的NaOH
溶液,并一直保持常温,所加碱的体积与-lgc (H+)的关系如图所示。c (H+)为溶液中水电离出的c(H+)。下
水 水
列说法不正确的是
A.从a点到b点,水的电离程度先增大后减小
B.b点溶液中离子浓度大小为c(Na+)>c(HCOO-)>c(OH-)>c(H+)
C.滴加NaOH溶液的过程中,混合溶液的导电性逐渐增强
D.常温下,K(HCOOH)的数量级为10-5
a
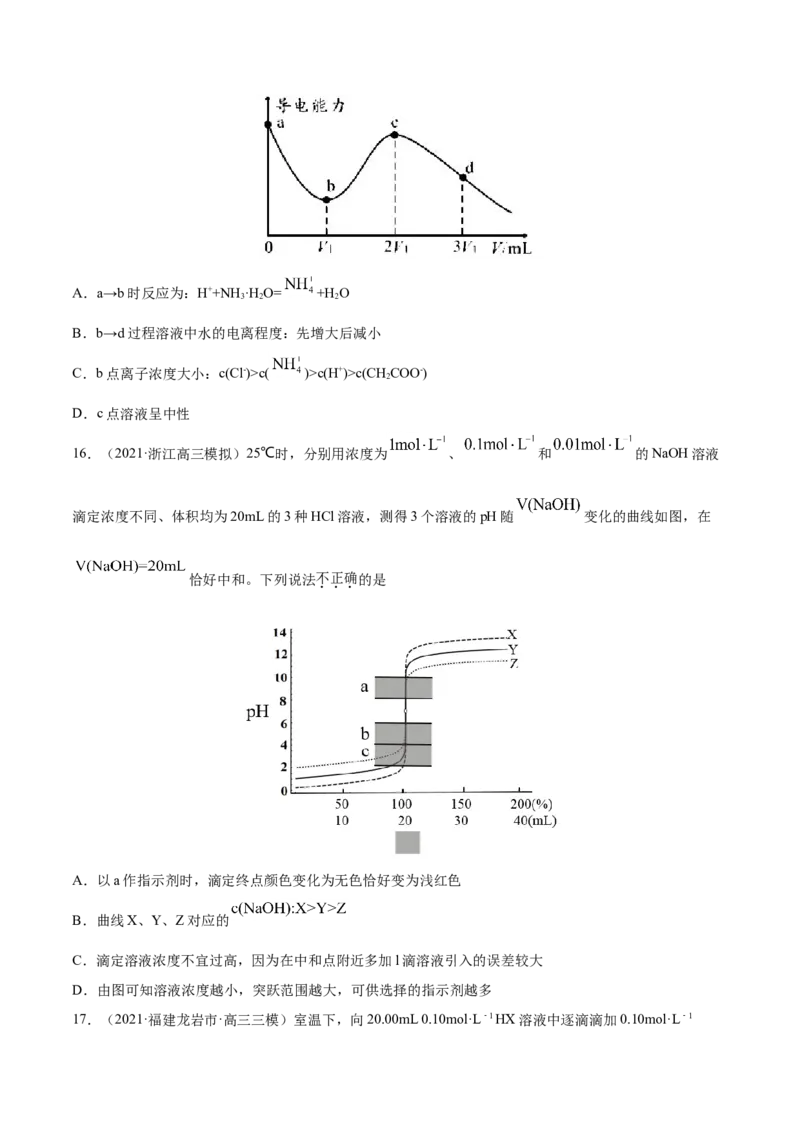
15.(2021·黑龙江哈尔滨市·哈九中高三二模)常温下向20mL均为0.1mol/L的HCl、CHCOOH混合液
3
中滴加0.1mol/L的氨水,测得混合液的导电能力与加入的氨水溶液的体积(V)关系如图所示,下列说法错
误的是A.a→b时反应为:H++NH·H O= +H O
3 2 2
B.b→d过程溶液中水的电离程度:先增大后减小
C.b点离子浓度大小:c(Cl-)>c( )>c(H+)>c(CH COO-)
2
D.c点溶液呈中性
16.(2021·浙江高三模拟)25℃时,分别用浓度为 、 和 的NaOH溶液
滴定浓度不同、体积均为20mL的3种HCl溶液,测得3个溶液的pH随 变化的曲线如图,在
恰好中和。下列说法不正确的是
A.以a作指示剂时,滴定终点颜色变化为无色恰好变为浅红色
B.曲线X、Y、Z对应的
C.滴定溶液浓度不宜过高,因为在中和点附近多加l滴溶液引入的误差较大
D.由图可知溶液浓度越小,突跃范围越大,可供选择的指示剂越多
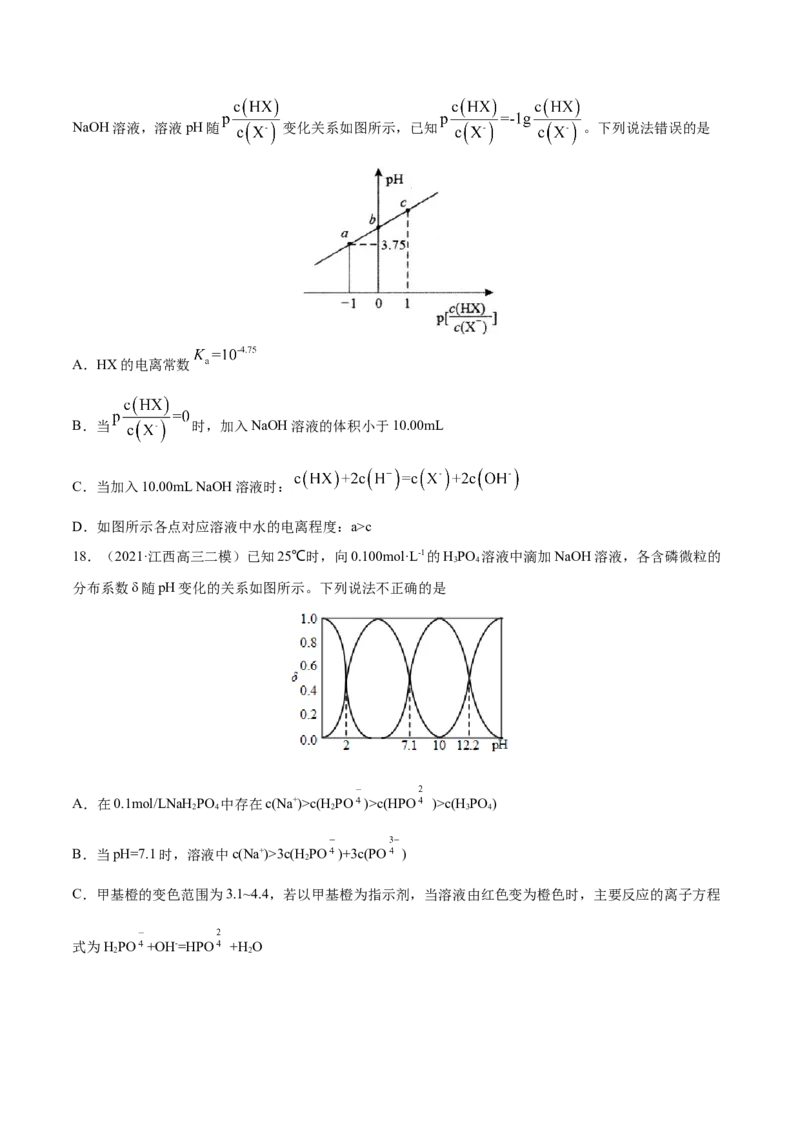
17.(2021·福建龙岩市·高三三模)室温下,向20.00mL 0.10mol·L﹣1 HX溶液中逐滴滴加0.10mol·L﹣1NaOH溶液,溶液pH随 变化关系如图所示,已知 。下列说法错误的是
A.HX的电离常数
B.当 时,加入NaOH溶液的体积小于10.00mL
C.当加入10.00mL NaOH溶液时:
D.如图所示各点对应溶液中水的电离程度:a>c
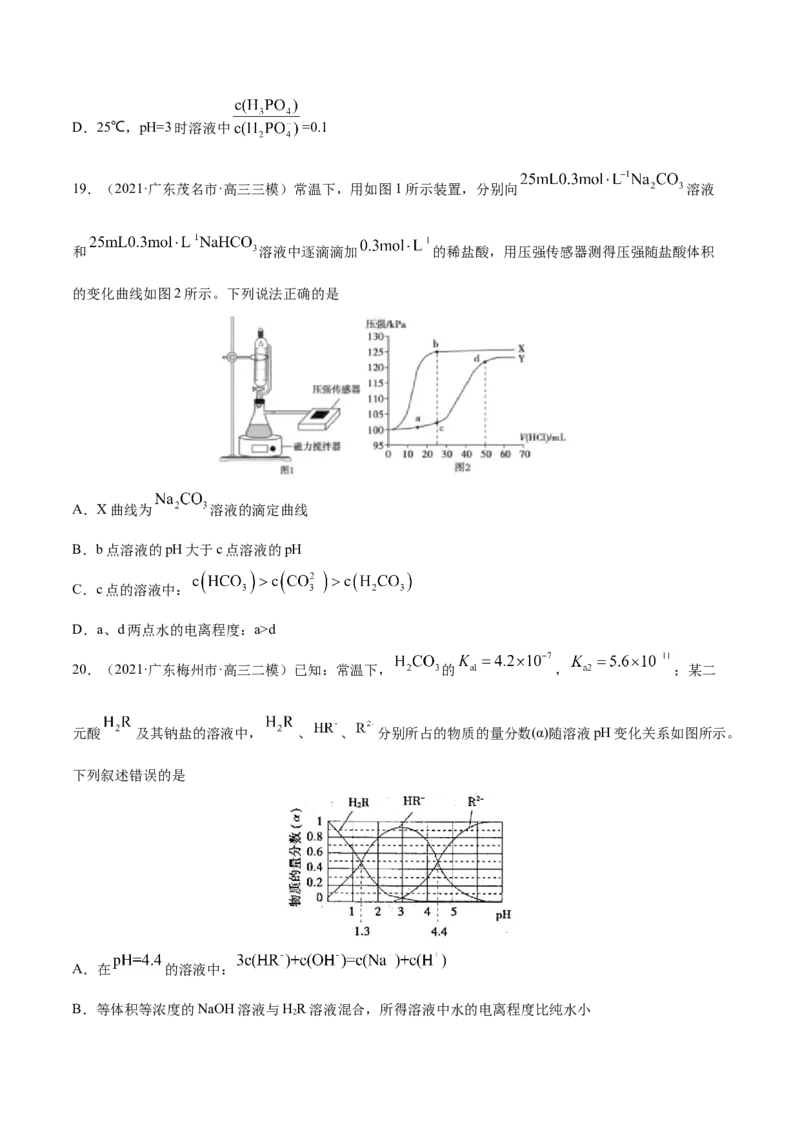
18.(2021·江西高三二模)已知25℃时,向0.100mol·L-1的HPO 溶液中滴加NaOH溶液,各含磷微粒的
3 4
分布系数δ随pH变化的关系如图所示。下列说法不正确的是
A.在0.1mol/LNaH PO 中存在c(Na+)>c(H PO )>c(HPO )>c(H PO )
2 4 2 3 4
B.当pH=7.1时,溶液中c(Na+)>3c(H PO )+3c(PO )
2
C.甲基橙的变色范围为3.1~4.4,若以甲基橙为指示剂,当溶液由红色变为橙色时,主要反应的离子方程
式为HPO +OH-=HPO +H O
2 2D.25℃,pH=3时溶液中 =0.1
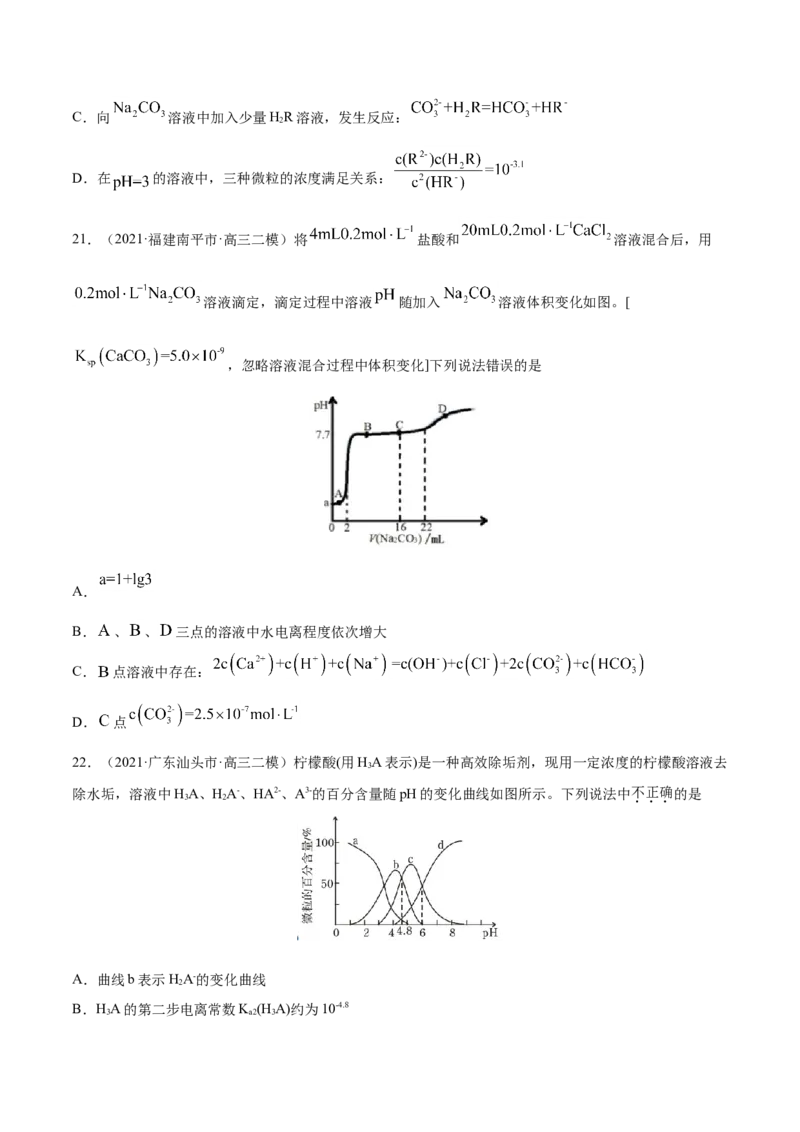
19.(2021·广东茂名市·高三三模)常温下,用如图1所示装置,分别向 溶液
和 溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积
的变化曲线如图2所示。下列说法正确的是
A.X曲线为 溶液的滴定曲线
B.b点溶液的pH大于c点溶液的pH
C.c点的溶液中:
D.a、d两点水的电离程度:a>d
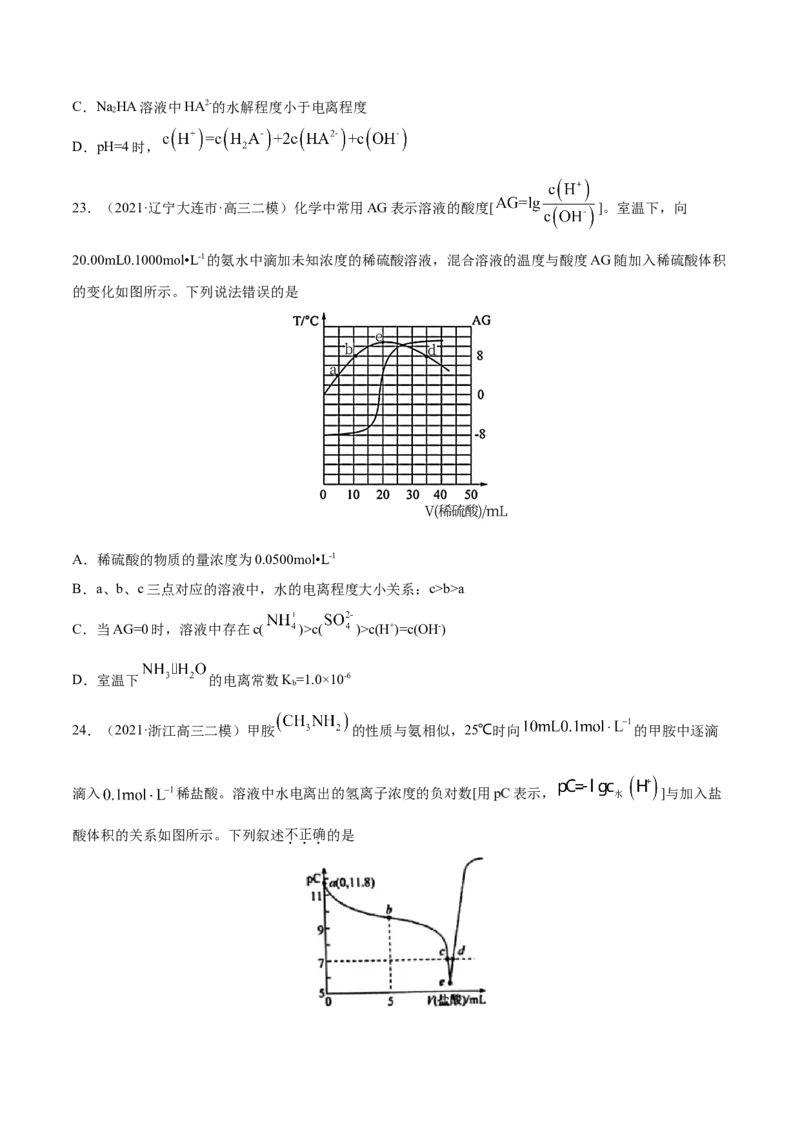
20.(2021·广东梅州市·高三二模)已知:常温下, 的 , ;某二
元酸 及其钠盐的溶液中, 、 、 分别所占的物质的量分数(α)随溶液pH变化关系如图所示。
下列叙述错误的是
A.在 的溶液中:
B.等体积等浓度的NaOH溶液与HR溶液混合,所得溶液中水的电离程度比纯水小
2C.向 溶液中加入少量HR溶液,发生反应:
2
D.在 的溶液中,三种微粒的浓度满足关系:
21.(2021·福建南平市·高三二模)将 盐酸和 溶液混合后,用
溶液滴定,滴定过程中溶液 随加入 溶液体积变化如图。[
,忽略溶液混合过程中体积变化]下列说法错误的是
A.
B. 、 、 三点的溶液中水电离程度依次增大
C. 点溶液中存在:
D. 点
22.(2021·广东汕头市·高三二模)柠檬酸(用HA表示)是一种高效除垢剂,现用一定浓度的柠檬酸溶液去
3
除水垢,溶液中HA、HA-、HA2-、A3-的百分含量随pH的变化曲线如图所示。下列说法中不正确的是
3 2
A.曲线b表示HA-的变化曲线
2
B.HA的第二步电离常数K (H A)约为10-4.8
3 a2 3C.NaHA溶液中HA2-的水解程度小于电离程度
2
D.pH=4时,
23.(2021·辽宁大连市·高三二模)化学中常用AG表示溶液的酸度[ ]。室温下,向
20.00mL0.1000mol•L-1的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积
的变化如图所示。下列说法错误的是
A.稀硫酸的物质的量浓度为0.0500mol•L-1
B.a、b、c三点对应的溶液中,水的电离程度大小关系:c>b>a
C.当AG=0时,溶液中存在c( )>c( )>c(H+)=c(OH-)
D.室温下 的电离常数K=1.0×10-6
b
24.(2021·浙江高三二模)甲胺 的性质与氨相似,25℃时向 的甲胺中逐滴
滴入 稀盐酸。溶液中水电离出的氢离子浓度的负对数[用pC表示, ]与加入盐
酸体积的关系如图所示。下列叙述不正确的是A. 的数量级为
B.甲胺的电离方程式:
C.b点溶液中甲胺的电离程度大于盐酸甲胺的水解程度
D.e点溶液:
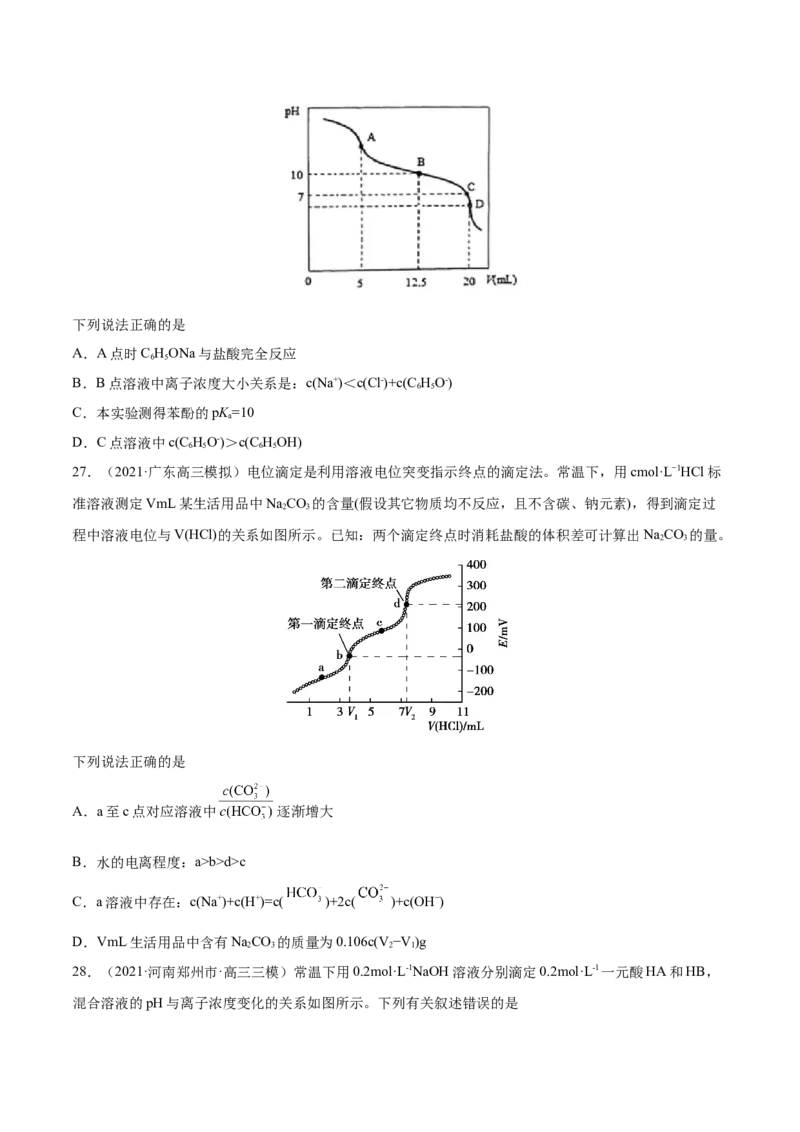
25.(2021·陕西西安市·高三二模)常温下将 溶液滴加到 溶液中,混合溶液的 与离子浓度
变化的关系如图所示(纵坐标为 )。下列叙述错误的是
A.曲线M表示pH与 的关系
B. = 104
C.图中a点对应溶液中:
D.溶液pH从2.6到6.6的过程中,水的电离程度逐渐增大
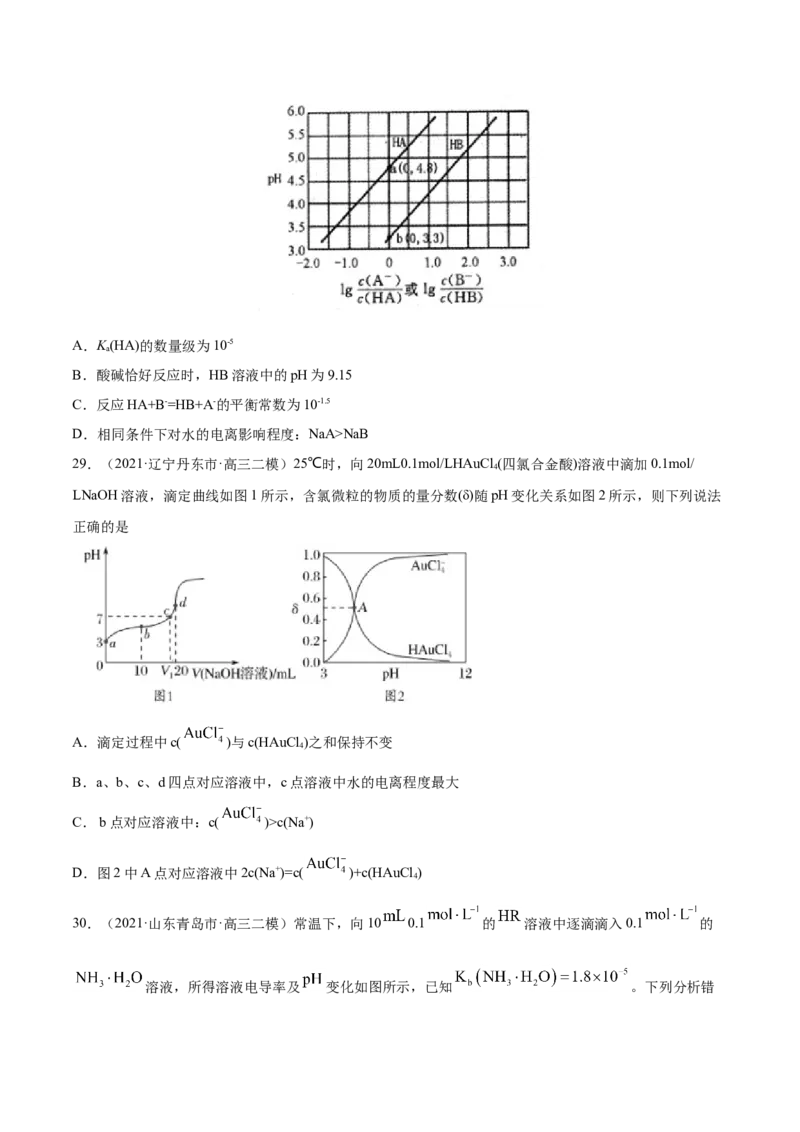
26.(2021·福建宁德市·高三三模)用返电位滴定法测定苯酚的电离常数:在苯酚溶液中加入适当过量的
NaOH溶液,得到NaOH和C HONa混合液,然后用盐酸滴定,得到如图曲线,A、D为两个滴定终点。
6 5下列说法正确的是
A.A点时C HONa与盐酸完全反应
6 5
B.B点溶液中离子浓度大小关系是:c(Na+)<c(Cl-)+c(C HO-)
6 5
C.本实验测得苯酚的pK=10
a
D.C点溶液中c(C HO-)>c(C HOH)
6 5 6 5
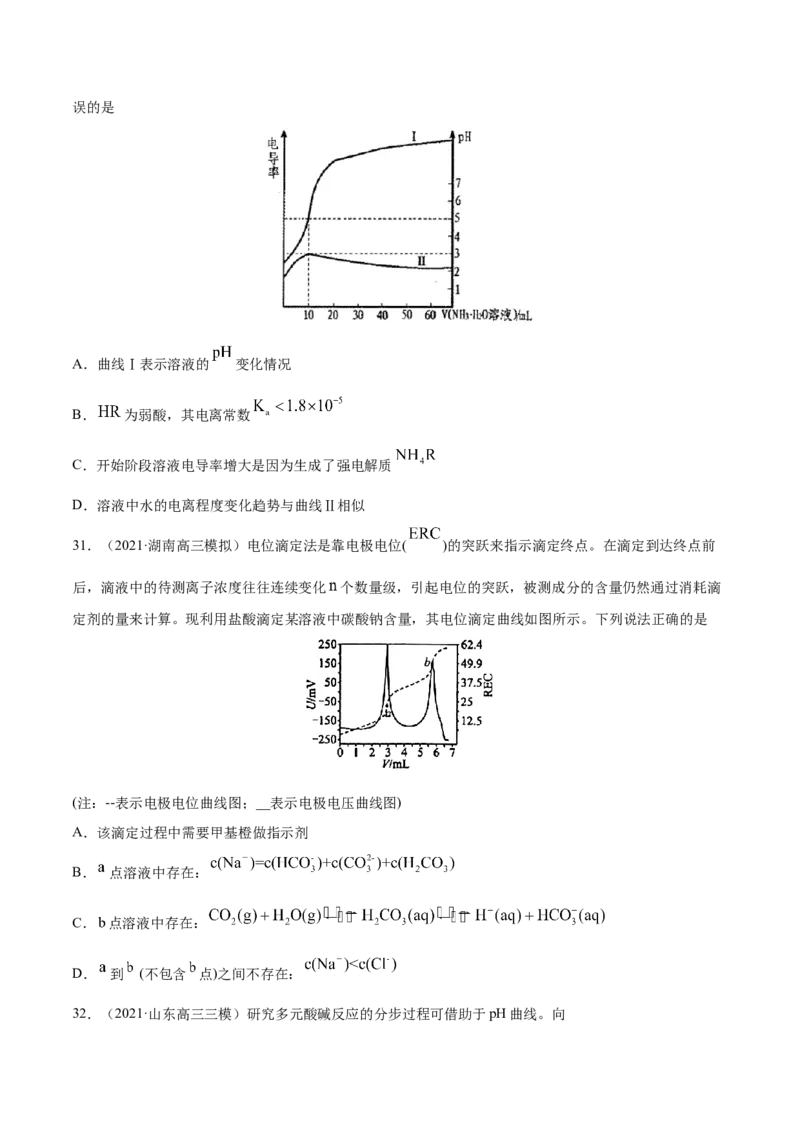
27.(2021·广东高三模拟)电位滴定是利用溶液电位突变指示终点的滴定法。常温下,用cmol·L−1HCl标
准溶液测定VmL某生活用品中NaCO 的含量(假设其它物质均不反应,且不含碳、钠元素),得到滴定过
2 3
程中溶液电位与V(HCl)的关系如图所示。已知:两个滴定终点时消耗盐酸的体积差可计算出NaCO 的量。
2 3
下列说法正确的是
A.a至c点对应溶液中 逐渐增大
B.水的电离程度:a>b>d>c
C.a溶液中存在:c(Na+)+c(H+)=c( )+2c( )+c(OH−)
D.VmL生活用品中含有NaCO 的质量为0.106c(V −V )g
2 3 2 1
28.(2021·河南郑州市·高三三模)常温下用0.2mol·L-1NaOH溶液分别滴定0.2mol·L-1一元酸HA和HB,
混合溶液的pH与离子浓度变化的关系如图所示。下列有关叙述错误的是A.K(HA)的数量级为10-5
a
B.酸碱恰好反应时,HB溶液中的pH为9.15
C.反应HA+B-=HB+A-的平衡常数为10-1.5
D.相同条件下对水的电离影响程度:NaA>NaB
29.(2021·辽宁丹东市·高三二模)25℃时,向20mL0.1mol/LHAuCl (四氯合金酸)溶液中滴加0.1mol/
4
LNaOH溶液,滴定曲线如图1所示,含氯微粒的物质的量分数(δ)随pH变化关系如图2所示,则下列说法
正确的是
A.滴定过程中c( )与c(HAuCl )之和保持不变
4
B.a、b、c、d四点对应溶液中,c点溶液中水的电离程度最大
C. b点对应溶液中:c( )>c(Na+)
D.图2中A点对应溶液中2c(Na+)=c( )+c(HAuCl )
4
30.(2021·山东青岛市·高三二模)常温下,向10 0.1 的 溶液中逐滴滴入0.1 的
溶液,所得溶液电导率及 变化如图所示,已知 。下列分析错误的是
A.曲线Ⅰ表示溶液的 变化情况
B. 为弱酸,其电离常数
C.开始阶段溶液电导率增大是因为生成了强电解质
D.溶液中水的电离程度变化趋势与曲线Ⅱ相似
31.(2021·湖南高三模拟)电位滴定法是靠电极电位( )的突跃来指示滴定终点。在滴定到达终点前
后,滴液中的待测离子浓度往往连续变化 个数量级,引起电位的突跃,被测成分的含量仍然通过消耗滴
定剂的量来计算。现利用盐酸滴定某溶液中碳酸钠含量,其电位滴定曲线如图所示。下列说法正确的是
(注:--表示电极电位曲线图;__表示电极电压曲线图)
A.该滴定过程中需要甲基橙做指示剂
B. 点溶液中存在:
C. 点溶液中存在:
D. 到 (不包含 点)之间不存在:
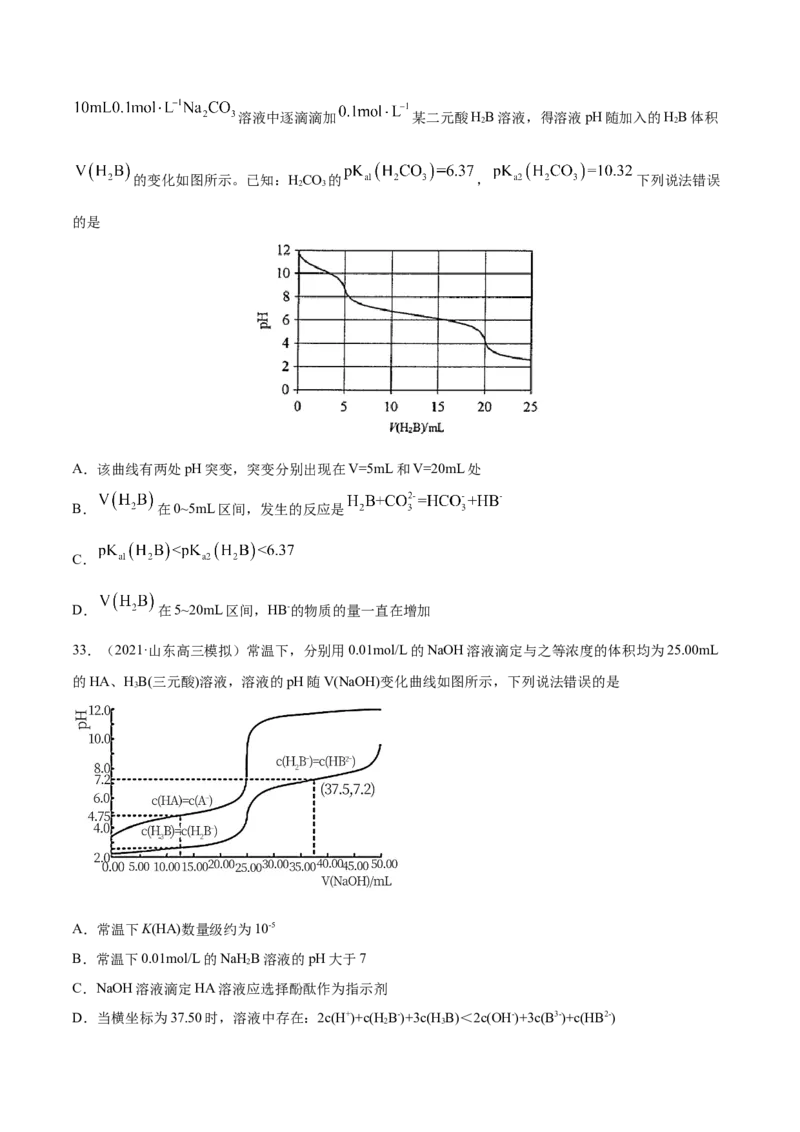
32.(2021·山东高三三模)研究多元酸碱反应的分步过程可借助于pH曲线。向溶液中逐滴滴加 某二元酸HB溶液,得溶液pH随加入的HB体积
2 2
的变化如图所示。已知:HCO 的 , 下列说法错误
2 3
的是
A.该曲线有两处pH突变,突变分别出现在V=5mL和V=20mL处
B. 在0~5mL区间,发生的反应是
C.
D. 在5~20mL区间,HB-的物质的量一直在增加
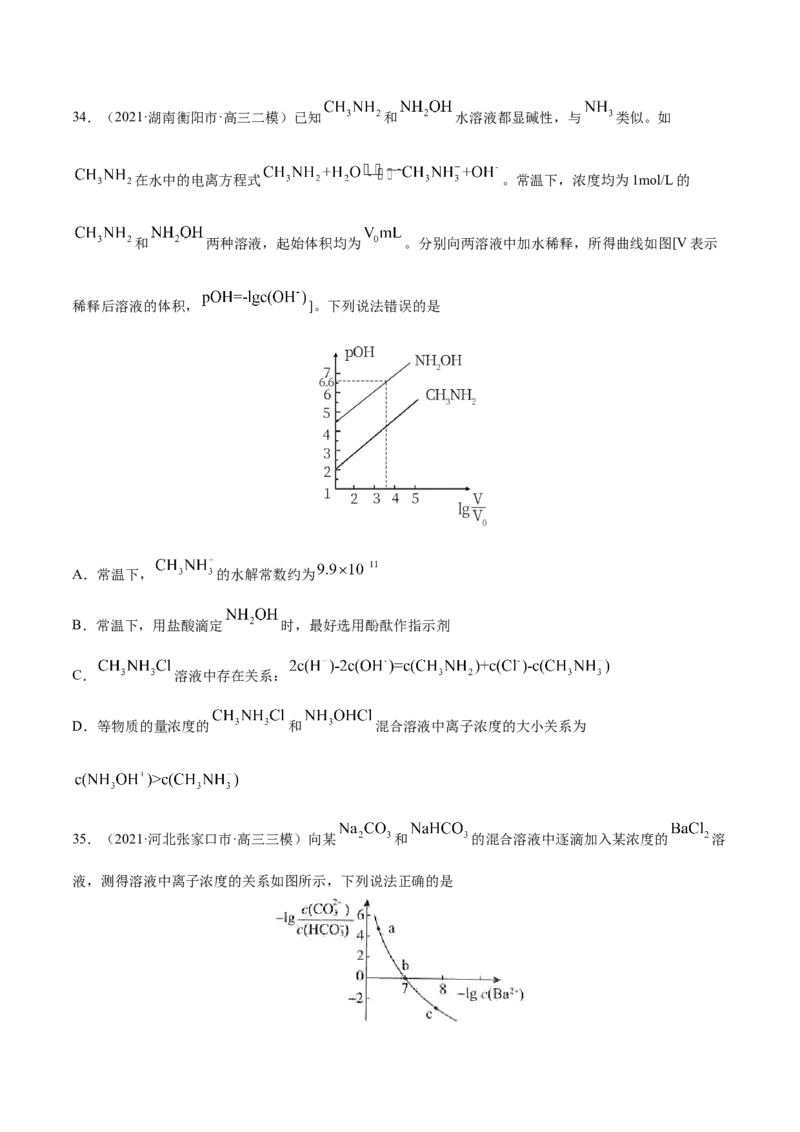
33.(2021·山东高三模拟)常温下,分别用0.01mol/L的NaOH溶液滴定与之等浓度的体积均为25.00mL
的HA、HB(三元酸)溶液,溶液的pH随V(NaOH)变化曲线如图所示,下列说法错误的是
3
A.常温下K(HA)数量级约为10-5
B.常温下0.01mol/L的NaH B溶液的pH大于7
2
C.NaOH溶液滴定HA溶液应选择酚酞作为指示剂
D.当横坐标为37.50时,溶液中存在:2c(H+)+c(H B-)+3c(H B)<2c(OH-)+3c(B3-)+c(HB2-)
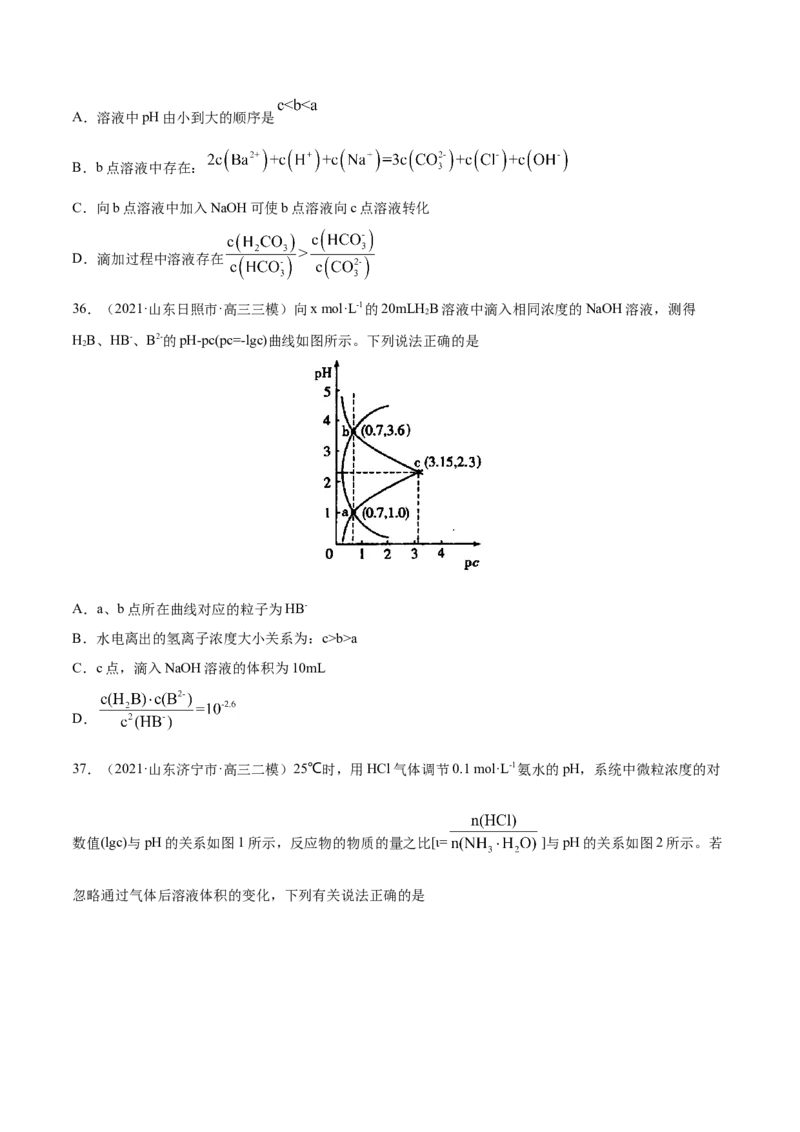
2 334.(2021·湖南衡阳市·高三二模)已知 和 水溶液都显碱性,与 类似。如
在水中的电离方程式 。常温下,浓度均为1mol/L的
和 两种溶液,起始体积均为 。分别向两溶液中加水稀释,所得曲线如图[V表示
稀释后溶液的体积, ]。下列说法错误的是
A.常温下, 的水解常数约为
B.常温下,用盐酸滴定 时,最好选用酚酞作指示剂
C. 溶液中存在关系:
D.等物质的量浓度的 和 混合溶液中离子浓度的大小关系为
35.(2021·河北张家口市·高三三模)向某 和 的混合溶液中逐滴加入某浓度的 溶
液,测得溶液中离子浓度的关系如图所示,下列说法正确的是A.溶液中pH由小到大的顺序是
B.b点溶液中存在:
C.向b点溶液中加入NaOH可使b点溶液向c点溶液转化
D.滴加过程中溶液存在
36.(2021·山东日照市·高三三模)向x mol·L-1的20mLH B溶液中滴入相同浓度的NaOH溶液,测得
2
HB、HB-、B2-的pH-pc(pc=-lgc)曲线如图所示。下列说法正确的是
2
A.a、b点所在曲线对应的粒子为HB-
B.水电离出的氢离子浓度大小关系为:c>b>a
C.c点,滴入NaOH溶液的体积为10mL
D.
37.(2021·山东济宁市·高三二模)25℃时,用HCl气体调节0.1 mol·L-1氨水的pH,系统中微粒浓度的对
数值(lgc)与pH的关系如图1所示,反应物的物质的量之比[ι= ]与pH的关系如图2所示。若
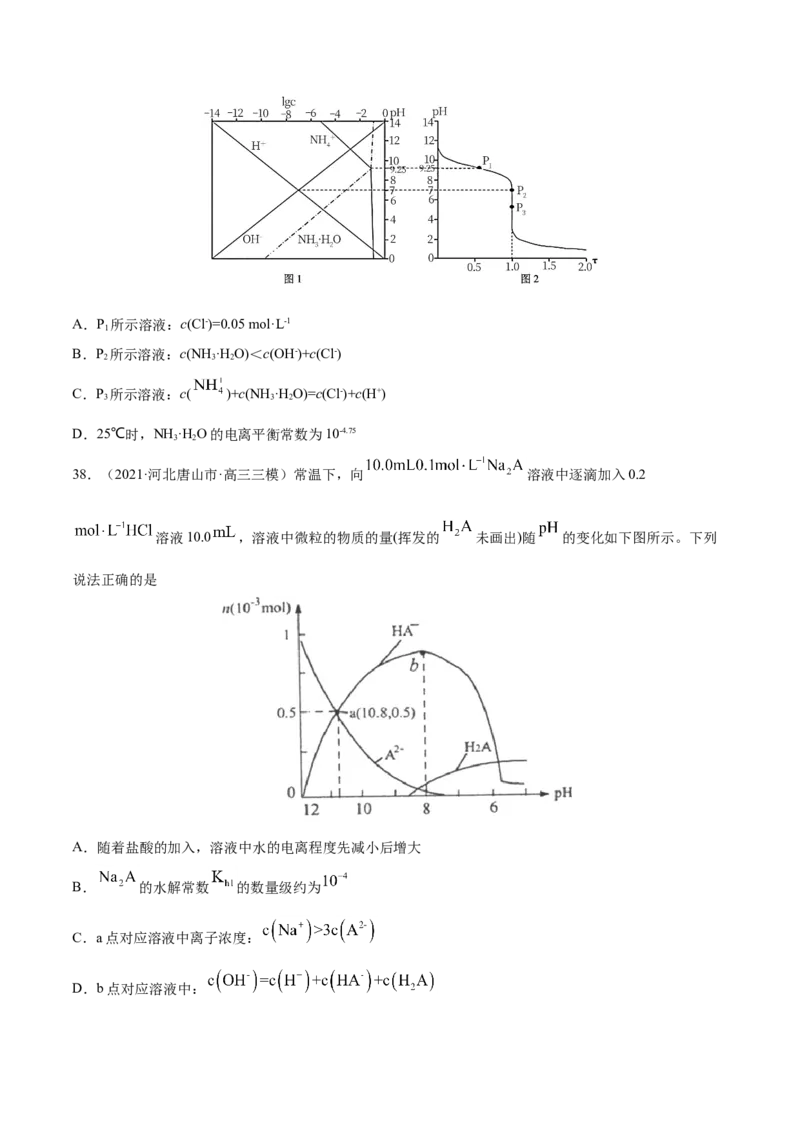
忽略通过气体后溶液体积的变化,下列有关说法正确的是A.P 所示溶液:c(Cl-)=0.05 mol·L-1
1
B.P 所示溶液:c(NH ·H O)<c(OH-)+c(Cl-)
2 3 2
C.P 所示溶液:c( )+c(NH ·H O)=c(Cl-)+c(H+)
3 3 2
D.25℃时,NH ·H O的电离平衡常数为10-4.75
3 2
38.(2021·河北唐山市·高三三模)常温下,向 溶液中逐滴加入0.2
溶液10.0 ,溶液中微粒的物质的量(挥发的 未画出)随 的变化如下图所示。下列
说法正确的是
A.随着盐酸的加入,溶液中水的电离程度先减小后增大
B. 的水解常数 的数量级约为
C.a点对应溶液中离子浓度:
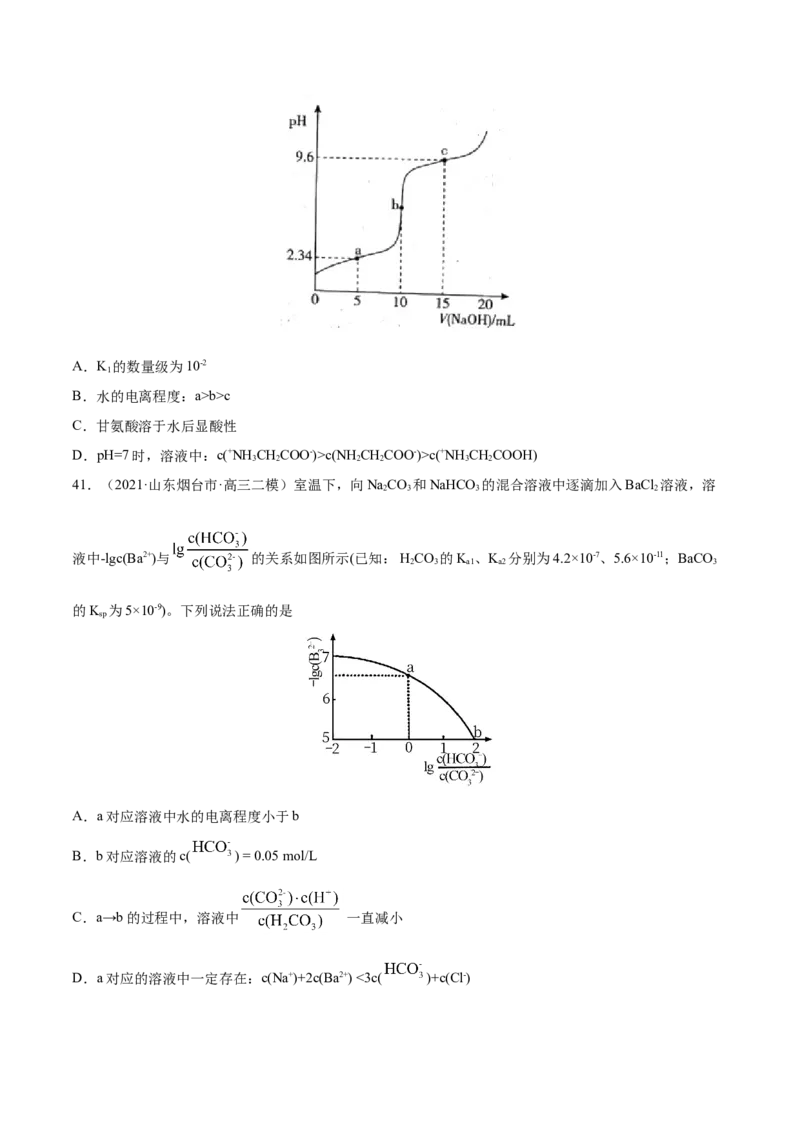
D.b点对应溶液中:39.(2021·河北邯郸市·高三三模)室温下实验室用 的氢氧化钠溶液滴定
醋酸溶液,滴定曲线如图所示(设 )。下列有关叙述正确的是
A.该条件下,醋酸的电离度(已电离的醋酸分子数与原醋酸分子数的比)约为1%
B.y点处加入的NaOH溶液体积小于
C.x→y→z的过程中,水的电离程度逐渐增大
D.y→z的曲线上任意一点,始终存在
40.(2021·山东临沂市·高三二模)25℃时,甘氨酸在水中存在下列关系:+NH CHCOOH
3 2
+NH CHCOO- NH CHCOO-,向10 mL 0.10 mol/L的+NH CHCOOH溶液中滴加0.10 mol/L的
3 2 2 2 3 2
NaOH溶液,溶液pH与所加NaOH溶液体积的关系如图所示。下列说法正确的是A.K 的数量级为10-2
1
B.水的电离程度:a>b>c
C.甘氨酸溶于水后显酸性
D.pH=7时,溶液中:c(+NH CHCOO-)>c(NHCHCOO-)>c(+NH CHCOOH)
3 2 2 2 3 2
41.(2021·山东烟台市·高三二模)室温下,向NaCO 和NaHCO 的混合溶液中逐滴加入BaCl 溶液,溶
2 3 3 2
液中-lgc(Ba2+)与 的关系如图所示(已知: HCO 的K 、K 分别为4.2×10-7、5.6×10-11;BaCO
2 3 a1 a2 3
的K 为5×10-9)。下列说法正确的是
sp
A.a对应溶液中水的电离程度小于b
B.b对应溶液的c( ) = 0.05 mol/L
C.a→b的过程中,溶液中 一直减小
D.a对应的溶液中一定存在:c(Na+)+2c(Ba2+) <3c( )+c(Cl-)