文档内容
专题 11 水溶液中的离子反应与平衡
1.下列化合物属于弱电解质的是( )
A.HClO B.Ba(OH) C.NH D.HClO
4 2 3
2.下列物质的水溶液因水解而呈酸性的是( )
A. NaHSO B. (NH )SO C. SO D. H SO
4 4 2 4 2 2 4
3.下列说法中,正确的是( )
A.强电解质溶液的导电能力一定比弱电解质强
B.冰醋酸是弱电解质,但液态时不能导电
C.盐酸中加入固体NaCl,因Cl-浓度增大,所以溶液酸性减弱
D.硫酸钠是强电解质,硫酸钡是弱电解质
4.下列物质在水溶液中存在着电离平衡的是( )
A.HF B.AgCl C.C HOH(酒精) D.Ca(OH)
2 5 2
5.下列物质按强电解质、弱电解质、非电解质顺序排列正确的是( )
A.氯化钠、硫酸钡、水 B.氢氧化钠、氯水、铜
C.硫酸、硫化氢、氨气 D.硫酸亚铁、硝酸、二氧化碳
6.下列溶液一定呈中性的是( )
A.c(H+)很小的溶液 B.c2(H+)=K
w
C.c(H+)=1×10-7mol·L-1 D.由强酸、强碱等物质的量反应得到的溶液
7.下列实验事实或数据可以说明次氯酸为弱电解质的是( )
A.常温下 的 溶液的pH=5.6
B.次氯酸具有漂白性
C.温度为25℃时,次氯酸的水溶液的pH<7
D.用HClO溶液做导电实验时,灯泡很暗
8.下列化学用语正确的是( )
A.NaHCO 水解的离子方程式:HCO -+ H O CO2-+H O+
3 3 2 3 3
B.NH Cl溶于DO中:NH ++D O NH ·HDO+D+
4 2 4 2 3
C.NaS显碱性原因:S2-+2H O HS+2OH-
2 2 2
D.向0.1 mol•L-1、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-=A2-+H O
2
9.下列电离方程式的书写正确的是( )A.熔融状态下NaHSO 的电离:NaHSO=Na++H++SO2-
4 4 4
B.HCO 的电离:HCO 2H++CO2-
2 3 2 3 3
C.Fe(OH) 的电离:Fe(OH) Fe3++3OH-
3 3
D.水溶液中NaHSO 的电离:NaHSO=Na++HSO -
4 4 4
10.下列关于电离常数的说法正确的是( )
A.电离常数随着弱电解质浓度的增大而增大
B.CHCOOH的电离常数表达式为K=
3 a
C.电离常数只受温度影响,与浓度无关
D.向CHCOOH溶液中加入少量CHCOONa固体,电离常数减小
3 3
11.下列说法不正确的是( )
A.某离子被沉淀完全是指该离子在溶液中的浓度为0
B.将KCl溶液从常温加热至100℃,溶液的pH变小但仍保持中性
C.常温下,NaCN溶液呈碱性,说明HCN是弱电解质
D.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大
12.关于水的电离,下列叙述中,正确的是( )
A.升高温度,水的平衡向正反应方向移动,K 增大,c(H+)不变
W
B.向水中加入少量硫酸,水的平衡向逆反应方向移动,K 不变,c(H+)增大
W
C.向水中加入氨水,水的平衡向逆反应方向移动,K 不变,c(OH-)降低
W
D.向水中加入少量固体NaCl,平衡向逆反应方向移动,K 不变,c(H+)降低
W
13.下列说法正确的是( )
A.1 mol·L-1的稀硫酸中存在OH-
B.K =10-14适用于任何温度、任何溶液
w
C.K 随溶液中c(H+)和c(OH-)的变化而改变
w
D.水的电离只受温度影响,酸碱性对其无影响
14.在由水电离出的c(OH-)=1×10-13mol•L-1的无色溶液中,一定能大量共存的离子组是( )
A.Cl-、AlO-、Na+、K+ B.Fe3+、NO -、K+、H+
2 3
C.NO -、Ba2+、K+、Cl- D.Al3+、SO 2-、NH +、Cl-
3 4 4
15.常温下,将pH=8的NaOH与pH=10的NaOH溶液等体积混合后,氢离子浓度最接近( )
A. (1×10-8-5×10-10)mol/L B.(1×10-8-5×10-10)mol/LC.(1×10-14-5×10-5)mol/L D.2×10-10mol/L
16.水的电离过程为HO H++OH-,在25℃时水的离子积为:K =1.0×10-14,在35℃时水的离子
2 w
积为:K =2.1×10-14,则下列叙述正确的是( )
w
A.水的电离是个吸热过程 B.35℃时c(H+)<c(OH-)
C.c(H+)随着温度的升高而降低 D.35℃时的水比25℃时的水电离程度小
17.25℃时,下列说法正确的是( )
A.0.1mol·L-1的某酸HA溶液中一定存在:c(HA)+c(HA-)+c(A2-)=0.1mol·L-1
2 2
B.中和等体积等浓度的氨水和NaOH溶液,氨水消耗的HCl的物质的量更多
C.某强碱弱酸盐NaA溶液,随着温度升高,pH一定增大
D.pH相同的CHCOONa溶液、C HONa溶液、NaCO 溶液、NaOH溶液,其浓度大小关系:
3 6 5 2 3
c(CHCOONa)>c(C HONa)>c(Na CO)>c(NaOH)
3 6 5 2
18.已知草酸HC O 是二元弱酸,常温下电离平衡常数:K =5.60×10-2,K =5.42×10-5。下列叙述错
2 2 4 a1 a2
误的是( )
A.HC O 溶液的电离程度随温度升高而增大
2 2 4
B.常温下,NaHC O 溶液呈碱性
2 4
C.0.001mol·L-1 Na C O 溶液中:c(Na+)=2×[c(C O2-)+c(HC O-)+c(H C O)]
2 2 4 2 4 2 4 2 2 4
D.常温下将pH=3的HC O 溶液与pH=11的NaOH溶液等体积混合,所得溶液呈酸性
2 2 4
19.邻苯二甲酸氢钾KHA溶液是一种常见的缓冲溶液,其可以用于标定NaOH溶液的浓度
(KHA+NaOH=KNaA+H O)。已知邻苯二甲酸的K (H A)=1.1×10-3,K (H A)=4.0×10-6.室温时下列指定溶液
2 a1 2 a2 2
中微粒物质的量浓度关系正确的是
A.0.1mol·L-1KHA溶液:c(K+)>c(HA-)+2c(A2-)
B.KHA溶液与NaOH溶液恰好完全中和后溶液:c(HA)+(HA-)+c(H+)=c(OH-)
2
C.等物质的量浓度的KHA和KNaA溶液中:c(K+)>(A2-)>c(Na+)>(HA-)
D.向0.1mol·L-1KHA中滴加NaOH溶液至pH=7:c(Na+)+c(H A)=c(A2-)
2
20.可溶性钡盐有毒,医院中常用硫酸钡这种钡盐(俗称钡餐)作为内服造影剂。医院抢救钡离子中毒
患者时除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。已知:Ksp(BaCO )=5.1×10-9;Ksp(BaSO )=
3 4
1.1×10-10。下列推断正确的是( )
A.BaCO 的溶度积常数表达式为 Ksp(BaCO )= n(Ba2+)·n(CO 2-)
3 3 3
B.可用2%~5%的NaSO 溶液给钡离子中毒患者洗胃
2 4
C.若误服含c(Ba2+)=1.0×10-5 mol·L-1的溶液时,会引起钡离子中毒
D.不用碳酸钡作为内服造影剂,是因为Ksp(BaCO )>Ksp(BaSO )
3 421.25℃时,下列说法正确的是( )
A.0.1mol·L-1的某酸HA溶液中一定存在:c(HA)+c(HA-)+c(A2-)=0.1mol·L-1
2 2
B.中和等体积等浓度的氨水和NaOH溶液,氨水消耗的HCl的物质的量更多
C.某强碱弱酸盐NaA溶液,随着温度升高,pH一定增大
D.pH相同的CHCOONa溶液、C HONa溶液、NaCO 溶液、NaOH溶液,其浓度大小关系:
3 6 5 2 3
c(CHCOONa)>c(C HONa)>c(Na CO)>c(NaOH)
3 6 5 2
22.已知草酸HC O 是二元弱酸,常温下电离平衡常数:K =5.60×10-2,K =5.42×10-5。下列叙述错
2 2 4 a1 a2
误的是( )
A.HC O 溶液的电离程度随温度升高而增大
2 2 4
B.常温下,NaHC O 溶液呈碱性
2 4
C.0.001mol·L-1 Na C O 溶液中:c(Na+)=2×[c(C O2-)+c(HC O-)+c(H C O)]
2 2 4 2 4 2 4 2 2 4
D.常温下将pH=3的HC O 溶液与pH=11的NaOH溶液等体积混合,所得溶液呈酸性
2 2 4
23.下列关于电解质溶液的说法中错误的是( )
A.等浓度、等体积的HCOOH溶液与HCOONa溶液混合后pH<7:c(HCOO-)>c(Na+)>c(H+)>
c(OH-)
B.新制氯水中:c(ClO-)+c(HClO)=c(Cl-)
C.已知K(HF)>K(H S),则同浓度的NaHS和NaF溶液的pH:NaHS>NaF
a a 2
D.NaCO 与NaHCO 的混合溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO-)+c(CO 2-)
2 3 3 3 3
24.邻苯二甲酸氢钾KHA溶液是一种常见的缓冲溶液,其可以用于标定NaOH溶液的浓度
(KHA+NaOH=KNaA+H O)。已知邻苯二甲酸的K (H A)=1.1×10-3,K (H A)=4.0×10-6.室温时下列指定溶液
2 a1 2 a2 2
中微粒物质的量浓度关系正确的是
A.0.1mol·L-1KHA溶液:c(K+)>c(HA-)+2c(A2-)
B.KHA溶液与NaOH溶液恰好完全中和后溶液:c(HA)+(HA-)+c(H+)=c(OH-)
2
C.等物质的量浓度的KHA和KNaA溶液中:c(K+)>(A2-)>c(Na+)>(HA-)
D.向0.1mol·L-1KHA中滴加NaOH溶液至pH=7:c(Na+)+c(H A)=c(A2-)
2
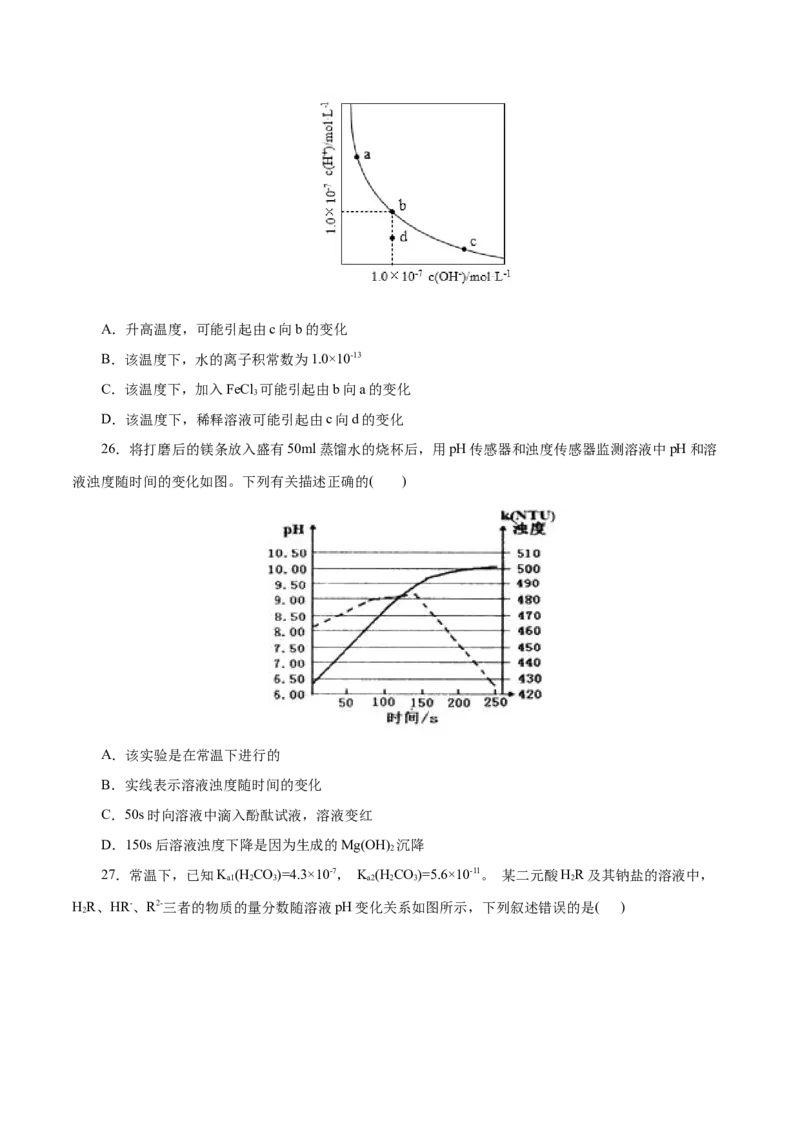
25.一定温度下,水溶液中 和 的浓度变化曲线如图,下列说法正确的是( )A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
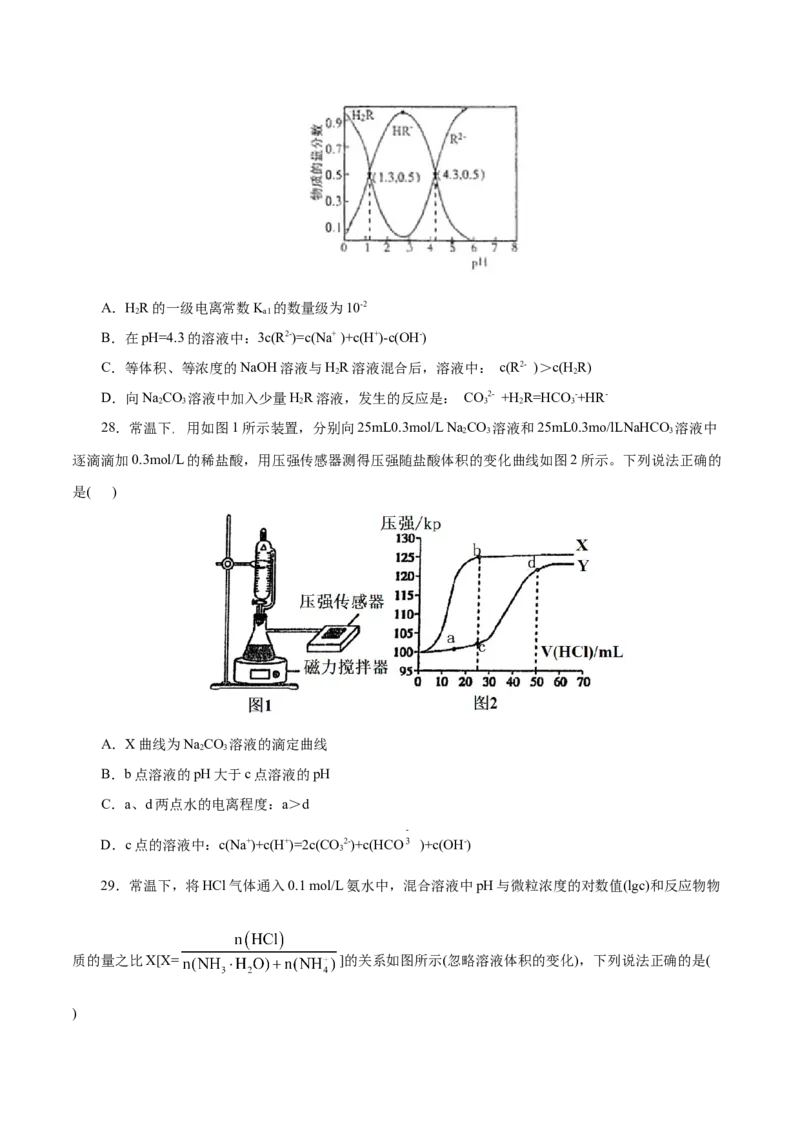
26.将打磨后的镁条放入盛有50ml蒸馏水的烧杯后,用pH传感器和浊度传感器监测溶液中pH和溶
液浊度随时间的变化如图。下列有关描述正确的( )
A.该实验是在常温下进行的
B.实线表示溶液浊度随时间的变化
C.50s时向溶液中滴入酚酞试液,溶液变红
D.150s后溶液浊度下降是因为生成的Mg(OH) 沉降
2
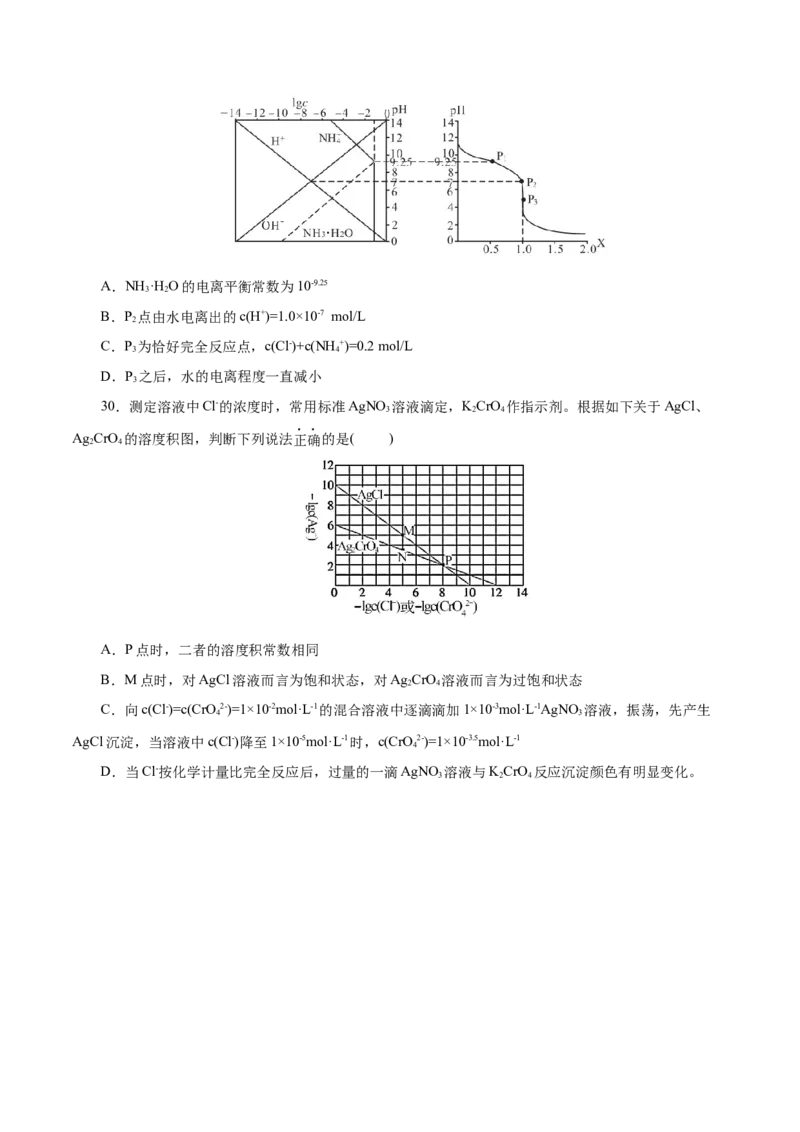
27.常温下,已知K (H CO)=4.3×10-7, K (H CO)=5.6×10-11。 某二元酸HR及其钠盐的溶液中,
a1 2 3 a2 2 3 2
HR、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述错误的是( )
2A.HR的一级电离常数K 的数量级为10-2
2 a1
B.在pH=4.3的溶液中:3c(R2-)=c(Na+ )+c(H+)-c(OH-)
C.等体积、等浓度的NaOH溶液与HR溶液混合后,溶液中: c(R2- )>c(HR)
2 2
D.向NaCO 溶液中加入少量HR溶液,发生的反应是: CO2- +H R=HCO-+HR-
2 3 2 3 2 3
28.常温下 用如图1所示装置,分别向25mL0.3mol/L Na CO 溶液和25mL0.3mo/lLNaHCO 溶液中
, 2 3 3
逐滴滴加0.3mol/L的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的
是( )
A.X曲线为NaCO 溶液的滴定曲线
2 3
B.b点溶液的pH大于c点溶液的pH
C.a、d两点水的电离程度:a>d
-
D.c点的溶液中:c(Na+)+c(H+)=2c(CO 2-)+c(HCO3 )+c(OH-)
3
29.常温下,将HCl气体通入0.1 mol/L氨水中,混合溶液中pH与微粒浓度的对数值(lgc)和反应物物
质的量之比X[X= ]的关系如图所示(忽略溶液体积的变化),下列说法正确的是(
)A.NH ·H O的电离平衡常数为10-9.25
3 2
B.P 点由水电离出的c(H+)=1.0×10-7 mol/L
2
C.P 为恰好完全反应点,c(Cl-)+c(NH+)=0.2 mol/L
3 4
D.P 之后,水的电离程度一直减小
3
30.测定溶液中Cl-的浓度时,常用标准AgNO 溶液滴定,KCrO 作指示剂。根据如下关于AgCl、
3 2 4
Ag CrO 的溶度积图,判断下列说法正确的是( )
2 4
A.P点时,二者的溶度积常数相同
B.M点时,对AgCl溶液而言为饱和状态,对Ag CrO 溶液而言为过饱和状态
2 4
C.向c(Cl-)=c(CrO 2-)=1×10-2mol·L-1的混合溶液中逐滴滴加1×10-3mol·L-1AgNO 溶液,振荡,先产生
4 3
AgCl沉淀,当溶液中c(Cl-)降至1×10-5mol·L-1时,c(CrO2-)=1×10-3.5mol·L-1
4
D.当Cl-按化学计量比完全反应后,过量的一滴AgNO 溶液与KCrO 反应沉淀颜色有明显变化。
3 2 4