文档内容
专题 13 化学工艺流程
1.常见金属元素(如Na、Mg、Al、Fe、Cu等)
(1)了解常见金属的活动顺序;
(2)了解常见金属、重要化合物的主要性质及其应用;
(3)了解合金的概念及其重要应用。
考纲
2.了解常见非金属元素(如H、C、N、O、Si、S、Cl等)单质及其化合物的主要性质及
应用;
3.掌握常见金属、非金属单质及其重要化合物的主要性质和应用;
4.了解常见非金属单质及其重要化合物对环境的影响;
5.了解常见无机非金属材料的重要成分、生产原料及其用途。
预计2023年将化学工艺或化学工业生产及最新科技成果融入其中,来考查考生的综合
能力。化学工艺流程题主要从以下两点设置:(1)环境与化学:主要涉及“废水、废
气、废渣”的来源,对环境的影响和处理原理。(2)重要化工生产及资源利用:旨在用
考情预测 所学的基本理论(氧化还原、化学平衡、盐类水解、电化学、热化学、有机物结构与性
质等)指导化工生产。从命题趋势来看,一般有三种题型:一是从实验设计和评价的角
度对化工生产进行模拟;二是根据一些化工生产的流程来考查考生的综合应用能力;三
是关于化工生产的相关计算。
核心素养 科学探究与创新意识 科学态度与社会责任
高频考点一 化学工艺流程与物质制备
物质制备类化工流程题常以某种物质(目标产物)的制备为基础,涉及原料的预处理、物质的制备原理、产品的分离及提纯等具体步骤,兼顾考查元素及其化合物、化学基本概念和基本理论、化学实验等知识。一个完
整的物质制备类化工生产流程一般包括以下具体内容:
1.原料预处理的六种常用方法
方法 目的
研磨、 减小固体的颗粒度或将液体雾化,增大反应物的接触面积,加快反应速率或使反应更
雾化 加充分
水浸 与水接触反应或溶解
酸浸 与酸接触反应或溶解,使可溶性离子进入溶液,不溶物通过过滤除去
碱浸 除去油污,溶解酸性氧化物、铝及其氧化物
除去可燃性杂质或使原料初步转化,如从海带中提取碘时的灼烧就是为了除去可燃性
灼烧
杂质
煅烧 改变结构,使一些物质能溶解,并使一些杂质在高温下氧化、分解,如煅烧高岭土
2.制备过程中控制反应条件的6种常用方法
常用于使某些金属离子形成氢氧化物沉淀。调节 pH所需的物质一般应满足两
调节溶液的 点:①能与H+反应,使溶液pH变大;②不引入新杂质。例如若要除去Cu2+中混
pH 有的Fe3+,可加入CuO、Cu(OH) 或Cu (OH) CO 等物质来调节溶液的pH,不可
2 2 2 3
加入NaOH溶液、氨水等
控制温度 根据需要升温或降温,改变反应速率或使平衡向需要的方向移动
控制压强 改变速率,影响平衡
使用合适的
加快反应速率,缩短达到平衡所需要的时间
催化剂
趁热过滤 防止某物质降温时析出
冰水洗涤 洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗
3.工艺流程中的常见专业术语
关键词 释 义
研磨、雾 将块状或颗粒状的物质磨成粉末或将液体雾化,增大反应物接触面积,以加快反应速
化 率或使反应更充分
使固体在高温下分解或改变结构、使杂质高温氧化、分解等。如煅烧石灰石、高岭
灼烧(煅烧)
土、硫铁矿
向固体中加入适当溶剂或溶液,使其中可溶性的物质溶解,包括水浸取、酸溶、碱
浸取
溶、醇溶等
浸出率 固体溶解后,离子在溶液中的含量的多少
酸浸 在酸性溶液中使可溶性金属离子进入溶液,不溶物通过过滤除去的过程
水浸 与水接触反应或溶解
过滤 固体与液体的分离
滴定 定量测定,可用于某种未知浓度物质的物质的量浓度的测定蒸发结晶 蒸发溶剂,使溶液由不饱和变为饱和,继续蒸发,过剩的溶质就会呈晶体析出
蒸发浓缩 蒸发除去部分溶剂,提高溶液的浓度
水洗 用水洗去可溶性杂质,类似的还有酸洗、醇洗等
酸作用 溶解、去氧化物(膜)、抑制某些金属离子的水解、除去杂质离子等
碱作用 去油污,去铝片氧化膜,溶解铝、二氧化硅,调节pH、促进水解(沉淀)
【典例剖析】
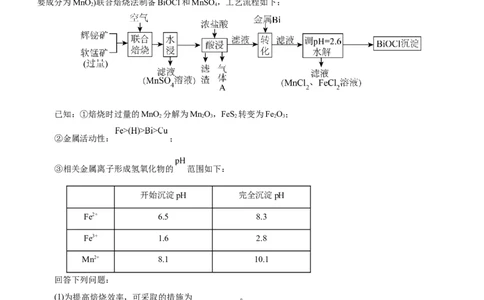
【例1】(2022•辽宁省选择性考试)某工厂采用辉铋矿(主要成分为BiS,含有FeS、SiO 杂质)与软锰矿(主
2 3 2 2
要成分为MnO )联合焙烧法制备BiOCl和MnSO ,工艺流程如下:
2 4
已知:①焙烧时过量的MnO 分解为MnO,FeS 转变为Fe O;
2 2 3 2 2 3
②金属活动性: ;
③相关金属离子形成氢氧化物的 范围如下:
开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为___________。
a.进一步粉碎矿石 b.鼓入适当过量的空气 c.降低焙烧温度
(2) Bi S 在空气中单独焙烧生成BiO,反应的化学方程式为___________。
2 3 2 3
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出Bi3+和Mn2+;②___________。
(4)滤渣的主要成分为___________(填化学式)。
(5)生成气体A的离子方程式为___________。
(6)加入金属 的目的是___________。【答案】(1)ab (2) 2Bi S+9O 2BiO+6SO
2 3 2 2 3 2
(3)抑制金属离子水解 (4) SiO
2
(5)Mn O+6H++2Cl-=2Mn2++ Cl ↑+3H O
2 3 2 2
(6)将Fe3+转化为Fe2+
【解析】联合焙烧:由已知信息①和第(2)问题干可知,发生转化:BiS→BiO+SO、FeS→Fe O+SO、
2 3 2 3 2 2 2 3 2
MnO →MnO+ MnSO ,故联合焙烧后得到BiO、Fe O、MnO、MnSO 和SiO;水浸:MnSO 进入滤液,
2 2 3 4 2 3 2 3 2 3 4 2 4
滤渣为BiO、Fe O、MnO 和SiO;酸浸:加入过量浓盐酸后,BiO 和Fe O 发生转化:BiO→Bi3+、
2 3 2 3 2 3 2 2 3 2 3 2 3
Fe O→Fe3+,因MnSO 有氧化性,会与浓盐酸发生氧化还原反应:MnO+6H++2Cl-=2Mn2++ Cl ↑+3H O,气体
2 3 4 2 3 2 2
A为Cl,滤渣主要为不溶于浓盐酸的SiO,滤液中金属离子为Bi3+、Fe3+、Mn2+;第(4)(5)问转化:由已知信
2 2
息②知,Fe的金属活动性强于Bi,且调pH=2.6时Mn2+和Fe2+进入滤液,可知加入金属Bi的目的是将Fe3+还原
为Fe2+。(1)a项,联合焙烧时,进一步粉碎矿石,可以增大矿石与空气的接触面积,能够提高焙烧效率,选项
a符合题意;b项,鼓入适当过量的空气有利于矿石充分反应,选项b符合题意;c项,降低焙烧温度,反应速
率减慢,不利于提高焙烧效率,选项c不符合题意;答案选ab;(2) Bi S 在空气中单独焙烧生成BiO,根据原
2 3 2 3
子守恒可知还应生成SO ,结合得失电子守恒,反应的化学方程式为2BiS+9O 2BiO+6SO;(3)加入浓
2 2 3 2 2 3 2
盐酸后,溶液中含有的离子主要为Bi3+、Fe3+、Mn2+、H+、Cl-,而酸浸后取滤液进行转化,故要防止金属离子
水解生成沉淀,进入滤渣,造成制得的BiOCl产率偏低;(4)滤渣主要为不溶于浓盐酸的SiO;(5)因MnO 有
2 2 3
氧化性,会与浓盐酸发生氧化还原反应:MnO+6H++2Cl-=2Mn2++ Cl ↑+3H O;(6)由已知信息③知,调pH=2.6
2 3 2 2
时,Fe3+会水解生成Fe(OH) 沉淀,但Fe2+还没开始沉淀,故要将Fe3+转化为Fe2+,在调pH后获得含FeCl 的滤
3 2
液,为了不引入新的杂质,加入Bi作还原剂。
【例2】(2022•山东卷)工业上以氟磷灰石[Ca F(PO )],含SiO 等杂质]为原料生产磷酸和石膏,工艺流程如
5 4 3 2
下:
回答下列问题:
(1)酸解时有 产生。氢氟酸与SiO 反应生成二元强酸HSiF,离子方程式为_______。
2 2 6
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比n(Na CO):n(SiF2-)= 1:1加入NaCO 脱氟,
2 3 6 2 3充分反应后,c(Na+)=_______ mol•L-1;再分批加入一定量的BaCO ,首先转化为沉淀的离子是_______。
3
BaSiF NaSiF CaSO BaSO
6 2 6 4 4
Ksp 1.0×10-6 4.0×10-6 9.0×10-4 1.0×10-10
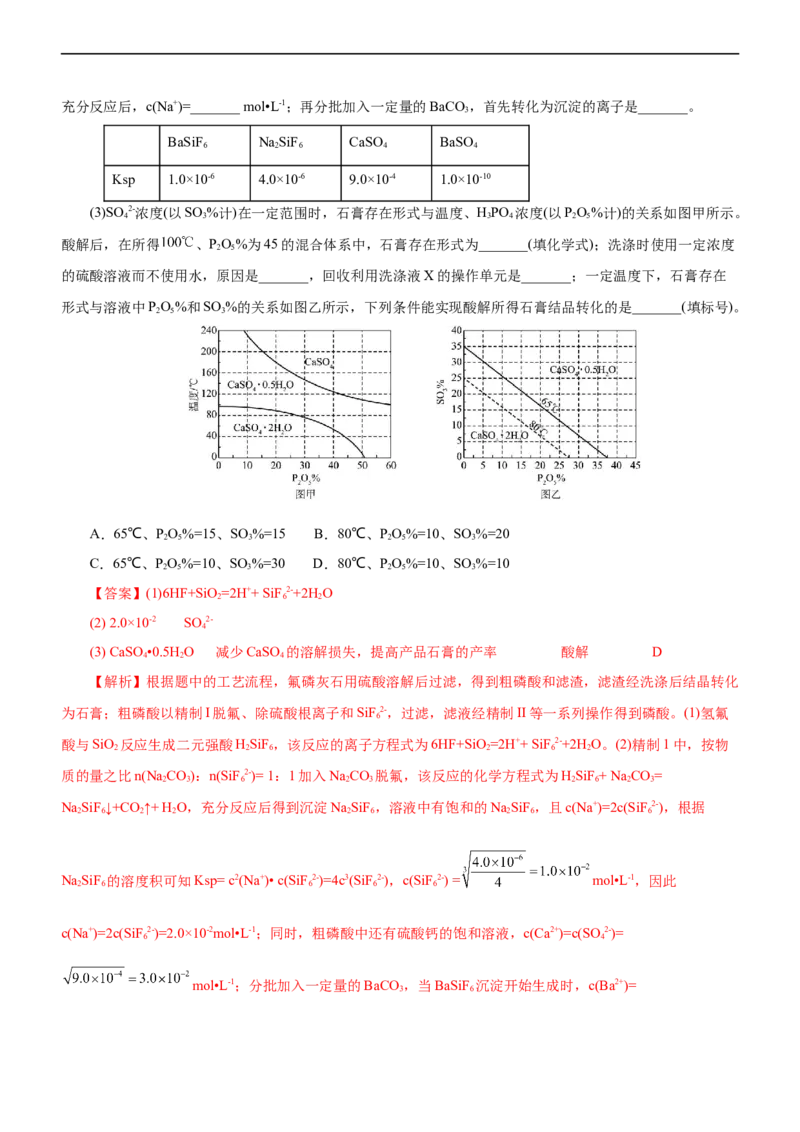
(3)SO 2-浓度(以SO %计)在一定范围时,石膏存在形式与温度、HPO 浓度(以PO%计)的关系如图甲所示。
4 3 3 4 2 5
酸解后,在所得 、PO%为45的混合体系中,石膏存在形式为_______(填化学式);洗涤时使用一定浓度
2 5
的硫酸溶液而不使用水,原因是_______,回收利用洗涤液X的操作单元是_______;一定温度下,石膏存在
形式与溶液中PO%和SO %的关系如图乙所示,下列条件能实现酸解所得石膏结品转化的是_______(填标号)。
2 5 3
A.65℃、PO%=15、SO %=15 B.80℃、PO%=10、SO %=20
2 5 3 2 5 3
C.65℃、PO%=10、SO %=30 D.80℃、PO%=10、SO %=10
2 5 3 2 5 3
【答案】(1)6HF+SiO =2H++ SiF2-+2H O
2 6 2
(2) 2.0×10-2 SO 2-
4
(3) CaSO •0.5HO 减少CaSO 的溶解损失,提高产品石膏的产率 酸解 D
4 2 4
【解析】根据题中的工艺流程,氟磷灰石用硫酸溶解后过滤,得到粗磷酸和滤渣,滤渣经洗涤后结晶转化
为石膏;粗磷酸以精制I脱氟、除硫酸根离子和SiF2-,过滤,滤液经精制II等一系列操作得到磷酸。(1)氢氟
6
酸与SiO 反应生成二元强酸HSiF,该反应的离子方程式为6HF+SiO =2H++ SiF2-+2H O。(2)精制1中,按物
2 2 6 2 6 2
质的量之比n(Na CO):n(SiF2-)= 1:1加入NaCO 脱氟,该反应的化学方程式为HSiF+ Na CO=
2 3 6 2 3 2 6 2 3
NaSiF↓+CO ↑+ H O,充分反应后得到沉淀NaSiF,溶液中有饱和的NaSiF,且c(Na+)=2c(SiF 2-),根据
2 6 2 2 2 6 2 6 6
NaSiF 的溶度积可知Ksp= c2(Na+)• c(SiF 2-)=4c3(SiF2-),c(SiF 2-) = mol•L-1,因此
2 6 6 6 6
c(Na+)=2c(SiF 2-)=2.0×10-2mol•L-1;同时,粗磷酸中还有硫酸钙的饱和溶液,c(Ca2+)=c(SO2-)=
6 4
mol•L-1;分批加入一定量的BaCO ,当BaSiF 沉淀开始生成时,c(Ba2+)=
3 6mol•L-1,当BaSO 沉淀开始生成时,c(Ba2+)= mol•L-1,因此,首先转
4
化为沉淀的离子是SO 2-,然后才是SiF2-。(3)根据图中的坐标信息,酸解后,在所得100℃、PO%为45的混
4 6 2 5
合体系中,石膏存在形式为CaSO•0.5HO;CaSO 在硫酸中的溶解度小于在水中的,因此,洗涤时使用一定浓
4 2 4
度的硫酸溶液而不使用水的原因是:减少CaSO 的溶解损失,提高产品石膏的产率;洗涤液X中含有硫酸,
4
其具有回收利用的价值,由于酸解时使用的也是硫酸,因此,回收利用洗涤液X的操作单元是:酸解。由图
甲信息可知,温度越低,越有利于实现酸解所得石膏结晶的转化,由图乙信息可知,位于65℃线上方的晶体
全部以CaSO•0.5HO形式存在,位于80℃线下方,晶体全部以CaSO•2H O形式存在,在两线之间的以两种
4 2 4 2
晶体的混合物形式存在:A项,PO%= l5、SO %= 15,由图乙信息可知,该点坐标位于两个温度线之间,故
2 5 3
不能实现晶体的完全转化,A不符合题意;B项,PO%= 10、SO %= 20,由图乙信息可知,该点坐标位于两
2 5 3
个温度线(65℃、80℃)之间,故不能实现晶体的完全转化, B不符合题意;C项,PO%= 10、SO %= 30,由
2 5 3
图乙信息可知,该点坐标位于,该点坐标位于65℃线上方,晶体全部以CaSO•0.5HO形式存在,故不能实现
4 2
晶体转化, C不符合题意;D项,PO%=10、SO %= 10,由图乙信息可知,该点坐标位于80℃线下方,晶体
2 5 3
全部以CaSO•2H O形式存在,故能实现晶体的完全转化,D符合题意;故选D。
4 2
【变式探究】
1.(2021•全国甲卷)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
(1)I 的一种制备方法如下图所示:
2
①加入 粉进行转化反应的离子方程式为_______,生成的沉淀与硝酸反应,生成_______后可循环使用。
②通入Cl 的过程中,若氧化产物只有一种,反应的化学方程式为_______;若反应物用量比n(Cl )/
2 2
n(FeI )=1.5时,氧化产物为_______;当n(Cl )/n(FeI )>1.5,单质碘的收率会降低,原因是_______。
2 2 2
(2)以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO,生成碘化物;再向混合溶液
3 2 3 3
中加入NaIO 溶液,反应得到I,上述制备I 的总反应的离子方程式为_______。
3 2 2
(3)KI溶液和CuSO 溶液混合可生成CuI沉淀和I,若生成1 mol I ,消耗的KI至少为_______ mol。I 在
4 2 2 2
KI溶液中可发生反应I+I- I-。实验室中使用过量的KI与CuSO 溶液反应后,过滤,滤液经水蒸气蒸馏
2 3 4
可制得高纯碘。反应中加入过量 的原因是_______。
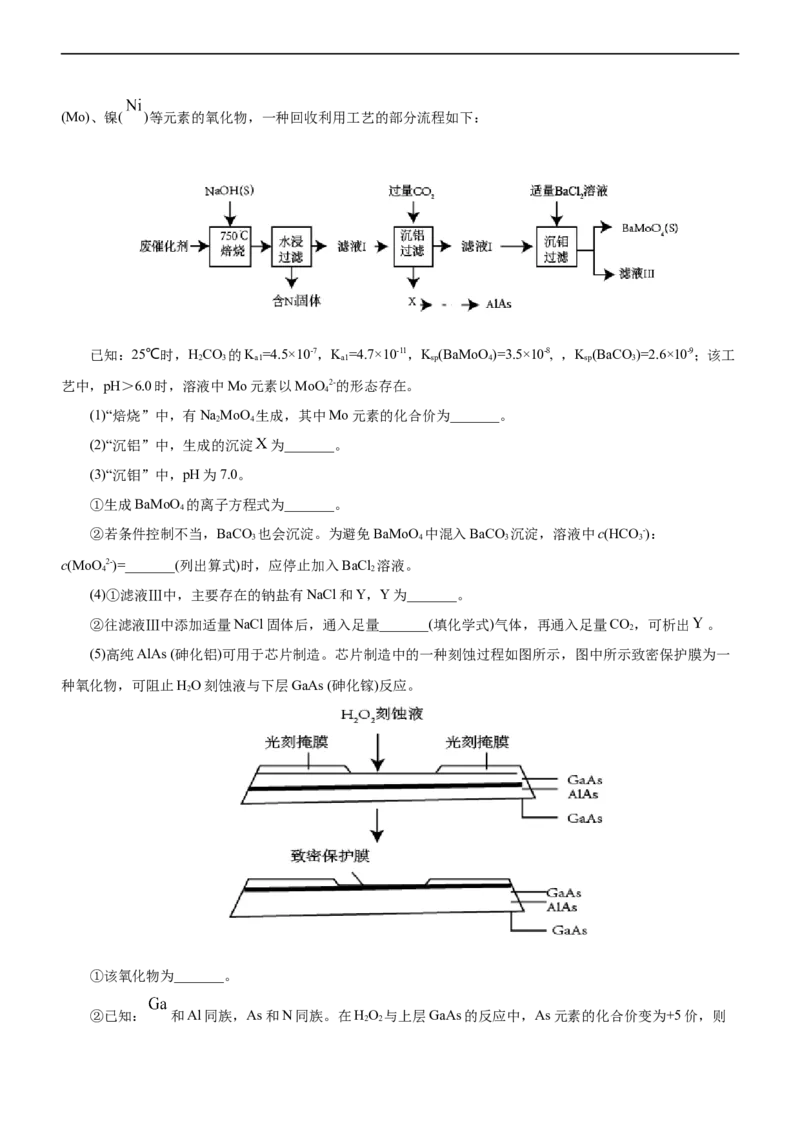
2.(2021•广东选择性考试)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼(Mo)、镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时,HCO 的K =4.5×10-7,K =4.7×10-11,K (BaMoO )=3.5×10-8, ,K (BaCO)=2.6×10-9;该工
2 3 a1 a1 sp 4 sp 3
艺中,pH>6.0时,溶液中Mo元素以MoO 2-的形态存在。
4
(1)“焙烧”中,有NaMoO 生成,其中Mo元素的化合价为_______。
2 4
(2)“沉铝”中,生成的沉淀 为_______。
(3)“沉钼”中,pH为7.0。
①生成BaMoO 的离子方程式为_______。
4
②若条件控制不当,BaCO 也会沉淀。为避免BaMoO 中混入BaCO 沉淀,溶液中c(HCO -):
3 4 3 3
c(MoO 2-)=_______(列出算式)时,应停止加入BaCl 溶液。
4 2
(4)①滤液Ⅲ中,主要存在的钠盐有NaCl和Y,Y为_______。
②往滤液Ⅲ中添加适量NaCl固体后,通入足量_______(填化学式)气体,再通入足量CO,可析出 。
2
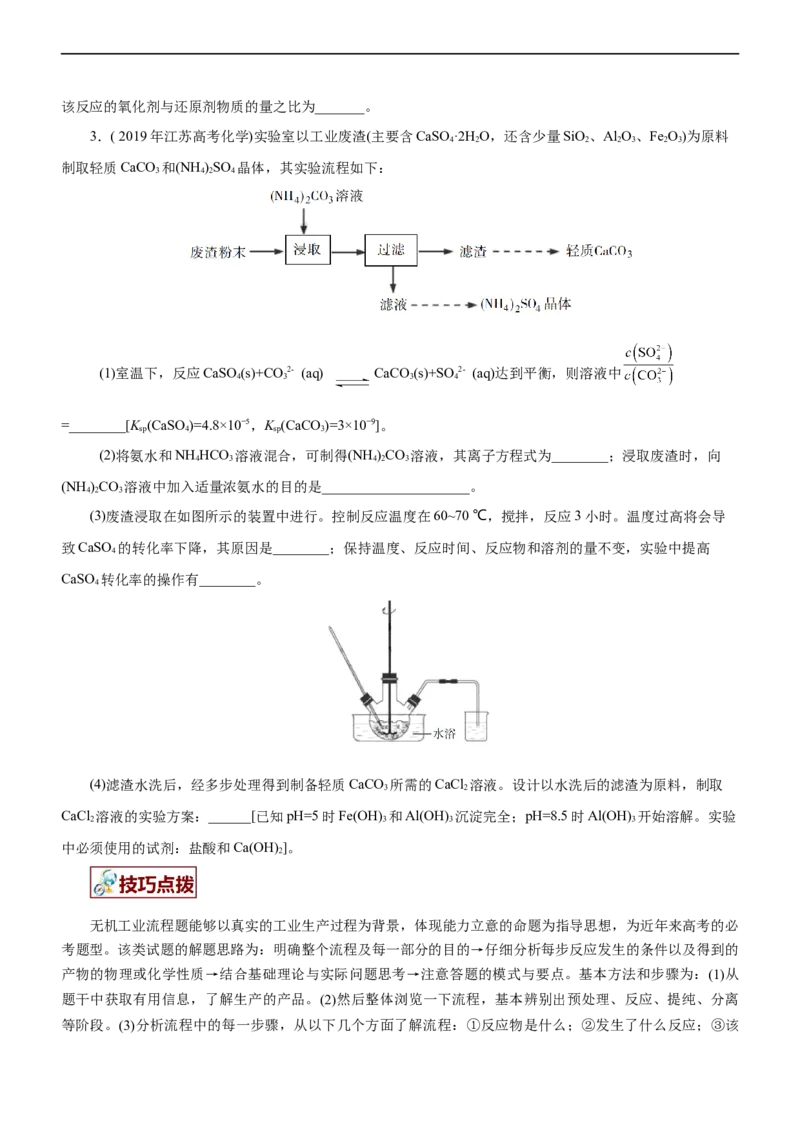
(5)高纯AlAs (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一
种氧化物,可阻止HO刻蚀液与下层GaAs (砷化镓)反应。
2
①该氧化物为_______。
②已知: 和Al同族,As和N同族。在HO 与上层GaAs的反应中,As元素的化合价变为+5价,则
2 2该反应的氧化剂与还原剂物质的量之比为_______。
3.( 2019年江苏高考化学)实验室以工业废渣(主要含CaSO·2H O,还含少量SiO、Al O、Fe O)为原料
4 2 2 2 3 2 3
制取轻质CaCO 和(NH )SO 晶体,其实验流程如下:
3 4 2 4
(1)室温下,反应CaSO(s)+CO2- (aq) CaCO (s)+SO 2- (aq)达到平衡,则溶液中
4 3 3 4
=________[K (CaSO)=4.8×10−5,K (CaCO)=3×10−9]。
sp 4 sp 3
(2)将氨水和NH HCO 溶液混合,可制得(NH )CO 溶液,其离子方程式为________;浸取废渣时,向
4 3 4 2 3
(NH )CO 溶液中加入适量浓氨水的目的是_____________________。
4 2 3
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60~70 ℃,搅拌,反应3小时。温度过高将会导
致CaSO 的转化率下降,其原因是________;保持温度、反应时间、反应物和溶剂的量不变,实验中提高
4
CaSO 转化率的操作有________。
4
(4)滤渣水洗后,经多步处理得到制备轻质CaCO 所需的CaCl 溶液。设计以水洗后的滤渣为原料,制取
3 2
CaCl 溶液的实验方案:______[已知pH=5时Fe(OH) 和Al(OH) 沉淀完全;pH=8.5时Al(OH) 开始溶解。实验
2 3 3 3
中必须使用的试剂:盐酸和Ca(OH) ]。
2
无机工业流程题能够以真实的工业生产过程为背景,体现能力立意的命题为指导思想,为近年来高考的必
考题型。该类试题的解题思路为:明确整个流程及每一部分的目的→仔细分析每步反应发生的条件以及得到的
产物的物理或化学性质→结合基础理论与实际问题思考→注意答题的模式与要点。基本方法和步骤为:(1)从
题干中获取有用信息,了解生产的产品。(2)然后整体浏览一下流程,基本辨别出预处理、反应、提纯、分离
等阶段。(3)分析流程中的每一步骤,从以下几个方面了解流程:①反应物是什么;②发生了什么反应;③该反应造成了什么后果,对制造产品有什么作用。抓住一个关键点:一切反应或操作都是为获得产品而服务。易
错点和难点是最后一问。
高频考点二 化学工艺流程与反应原理
化工生产过程中的主要生产阶段涉及多种化学反应原理,试题中根据生产流程中的有关化学知识步步设问,
只要明确实验目的,理解装置的作用以及工艺流程的原理,吸收题目新信息并能加以灵活运用。结合化学反应
原理类化工生产流程一般包括以下具体内容:
1.温度、浓度、压强的控制
术语 功能
温度 ①加快反应速率或溶解速率;②促进平衡向吸热方向移动;③除杂,除去热不稳定
的控 升温 的杂质,如NaHCO 、Ca(HCO )、KMnO 、I、NH Cl等物质。④使沸点相对较
3 3 2 4 2 4
制 低的原料气化
①防止某物质在高温时会溶解(或分解) ;② 使化学平衡向着题目要求的方向移动
降温 (放热方向);③使某个沸点较高的产物液化,使其与其他物质分离;④降低晶体的溶
解度,减少损失.
①防止某种物质温度过高时会分解或挥发;②为了使某物质达到沸点挥发出来;③
控温(用水 使催化剂的活性达到最好;④防止副反应的发生;⑤降温或减压可以减少能源成
浴或油浴 本,降低对设备的要求,达到绿色化学的要求;⑥如果题目中出现了包括产物在内
控温) 的各种物质的溶解度信息,则要根据它们的溶解度随温度升高而改变的情况,寻找
合适的结晶分离方法 ( 蒸发结晶或浓缩结晶) 。
增大反应 ①可加快反应速率 。对气体分子数减少的反应,加压使平衡向生成物方向移动。
浓 物浓 但压强太大,动力消耗更多,设备要求更高,成本增加,故必须综合考虑;②加压
度、 度 、 加 一般是提高气体反应物浓度措施 ,在气体和固体、液体反应的体系中并不适宜;
压强 压 ③生产中常使廉价易得的原料适当过量,以提高另一原料的利用率。
的控
制 减压蒸馏 减小压强,降低液体的沸点,防止(如浓HNO 3 、NH 3 .H 2 O、H 2 O 2 、NH 4 HCO 3 等)物
质分解;
2.pH的控制
术语 功能
(1)目的:调节pH值实质上是利用沉淀溶解平衡把某些离子转化成沉淀。(2)原则:不管是调高
还是调低,原则都是加过量的除杂剂而不引进新的杂质,这里分两种情况①如果要得到滤液,
控制溶 可加固体沉淀剂消耗H+或OH—,如除去含Cu2+溶液中混有的Fe3+,可通过加入CuO、Cu(OH) 、
2
液的 Cu(OH) CO 等;②要得到滤渣,则需加入碱性溶液,如氨水或氢氧化钠溶液。调低PH值的原
2 3
PH 则与调高PH的原则相同。(3)题目呈现方式:题中通常会以表格数据形式,或“已知信息”给
出需求的“适宜PH范围”的信息;(4)解题步骤:①判断溶液呈酸(或碱)性; ②判断调高还是调
低; ③选择合适的调节剂。
3.体系环境氛围及其它条件的控制
术语 功能
(1)蒸发或结晶时,加入相应的酸或碱,以抑制某些盐的水解;(2)需要在酸性气流中干燥
酸性、
FeCl 、AlCl 、MgCl 等含水晶体,以防止水解。如从海水中提取镁,从MgCl 的溶液里结晶
碱性 3 3 2 2
析出的是氯化镁结晶水合物,电解熔化氯化镁才能制得金属镁,要去除氯化镁晶体中的结晶
或 某
种 环
水"需要在氯化氢气流中加热,否则煅烧所得的最后固体不是MgCl
2
,而是熔点更高的MgO, 具
境 氛 有相似情况的还有FeCl 3 、 AlCl 3 等;(3)营造还原性氛围:加热煮沸酸液后再冷却,其目的是排
围 除酸溶液中的氧气,如用废铁制备绿矾晶体,需要把硫酸加热煮沸后再加入,同时还不能加入
过量,防止Fe2+被氧化;(4)营造氧化性氛围:加入氧化剂进行氧化,如加入绿色氧化剂 HO
2 2将 Fe2+ 氧化转化为Fe3+ 。
【典例剖析】
【例1】(2022•湖南选择性考试)钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为
TiO,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
2
已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
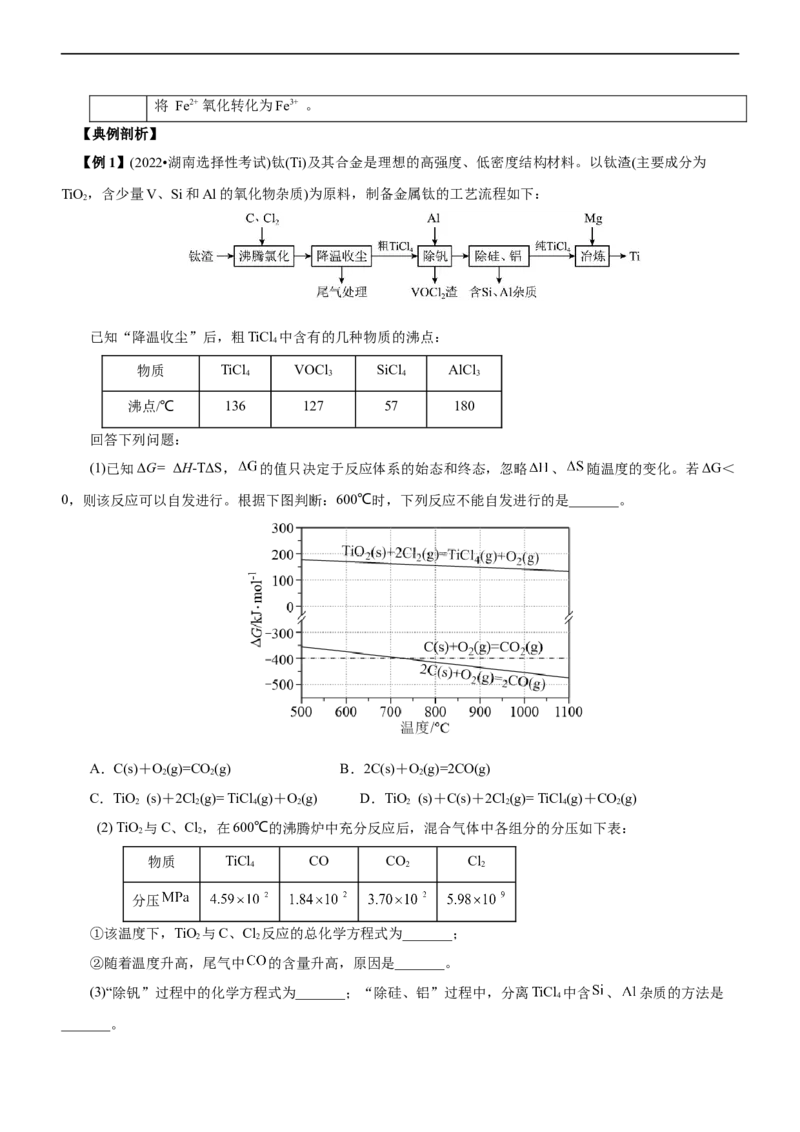
(1)已知ΔG= ΔH-TΔS, 的值只决定于反应体系的始态和终态,忽略 、 随温度的变化。若ΔG<
0,则该反应可以自发进行。根据下图判断:600℃时,下列反应不能自发进行的是_______。
A.C(s)+O(g)=CO (g) B.2C(s)+O(g)=2CO(g)
2 2 2
C.TiO (s)+2Cl(g)= TiCl (g)+O(g) D.TiO (s)+C(s)+2Cl(g)= TiCl (g)+CO(g)
2 2 4 2 2 2 4 2
(2) TiO 与C、Cl,在600℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
2 2
物质 TiCl CO CO Cl
4 2 2
分压
①该温度下,TiO 与C、Cl 反应的总化学方程式为_______;
2 2
②随着温度升高,尾气中 的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离TiCl 中含 、 杂质的方法是
4
_______。(4)“除钒”和“除硅、铝”的顺序_______(填“能”或“不能”)交换,理由是_______。
(5)下列金属冶炼方法与本工艺流程中加入 冶炼 的方法相似的是_______。
A.高炉炼铁 B.电解熔融氯化钠制钠 C.铝热反应制锰 D.氧化汞分解制汞
【答案】(1)C
(2) 5TiO+6C+10Cl 5TiCl +2CO+4CO 随着温度升高,CO 与C发生反应C+CO 2CO
2 2 4 2 2 2
(3) 3VOCl +Al=3VOCl +AlCl 蒸馏
3 2 3
(4) 不能 若先“除硅、铝”再“除钒”,“除钒”时需要加入Al,又引入Al杂质;
(5)AC
【解析】钛渣中加入C、Cl 进行沸腾氯化,转化为相应的氯化物,降温收尘后得到粗TiCl ,加入单质Al
2 4
除钒,再除硅、铝得到纯TiCl ,加入Mg还原得到Ti。(1)记①C(s)+O(g)=CO (g),②2C(s)+O(g)=2CO(g),
4 2 2 2
③TiO (s)+2Cl(g)= TiCl (g)+O(g),④TiO (s)+C(s)+2Cl(g)= TiCl (g)+CO(g);A项,由图可知,600℃
2 2 4 2 2 2 4 2
时C(s)+O(g)=CO (g)的ΔG<0,反应自发进行,故A不符合题意;B项,由图可知,600℃时2C(s)+
2 2
O(g)=2CO(g)的ΔG<0,反应自发进行,故B不符合题意;C项,由图可知,600℃时TiO (s)+2Cl(g)=
2 2 2
TiCl (g)+O(g)的ΔG>0,反应不能自发进行,故C符合题意;D项,根据盖斯定律,TiO (s)+C(s)+2Cl(g)=
4 2 2 2
TiCl (g)+CO(g)可由①+③得到,则600℃时其ΔG<0,反应自发进行,故D不符合题意;故选C;(2)①根据
4 2
表中数据可知,该温度下C主要生成CO和CO,根据相同条件下气体的压强之比是物质的量之比可知TiCl 、
2 4
CO和CO 的物质的量之比约是5:2:4,所以TiO 与C、Cl 反应的总化学方程式为5TiO+6C+10Cl
2 2 2 2 2
5TiCl +2CO+4CO ;②随着温度升高,CO 与C发生反应C+CO 2CO,导致CO含量升高;(3)“降温收
4 2 2 2
尘”后钒元素主要以VOCl 形式存在,加入Al得到VOCl 渣,根据得失电子守恒和元素守恒配平方程式为
3 2
3VOCl +Al=3VOCl +AlCl ;AlCl 、SiCl 与TiCl 沸点差异较大,“除硅、铝"过程中可采用蒸馏的方法分离
3 2 3 3 4 4
AlCl 、SiCl ;(4)若先“除硅、铝”再“除钒”,“除钒”时需要加入Al,又引入Al杂质,因此“除钒”和
3 4
“除硅、铝”的顺序不能交换;(5)本工艺中加入Mg冶炼Ti的方法为热还原法;A项,高炉炼铁的原理是用
还原剂将铁矿石中铁的氧化物还原成金属铁,属于热还原法,故A符合题意;B项,电解熔融氯化钠制取金属
钠的原理是电解法,故B不符合题意;C项,铝热反应制锰是利用Al作还原剂,将锰从其化合物中还原出来,
为热还原法,故C符合题意;D项,Hg为不活泼金属,可以直接用加热分解氧化汞的方法制备汞,故D不符
合题意;故选AC。
【例2】(2022•全国乙卷)废旧铅蓄电池的铅膏中主要含有PbSO 、PbO 、PbO和Pb。还有少量Ba、Fe、
4 2Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 PbSO PbCO BaSO BaCO
4 3 4 3
K 2.5×10-8 7.4×10-14 1.1×10-10 2.6×10-9
sp
一定条件下,一些金属氢氧化物沉淀时的 如下表:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Pb(OH)
3 2 3 2
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
(1)在“脱硫”中PbSO 转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择NaCO 的原因
4 2 3
________。
(2)在“脱硫”中,加入NaCO 不能使铅膏中BaSO 完全转化,原因是________。
2 3 4
(3)在“酸浸”中,除加入醋酸( ),还要加入HO。
2 2
(ⅰ)能被HO 氧化的离子是________;
2 2
(ⅱ) H O 促进了金属Pb在醋酸中转化为Pb(Ac) ,其化学方程式为________;
2 2 2
(ⅲ) H O 也能使PbO 转化为Pb(Ac) ,HO 的作用是________。
2 2 2 2 2 2
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是________。
(5)“沉铅”的滤液中,金属离子有________。
【答案】(1) PbSO (s)+CO2-(aq)= PbCO (s)+SO 2-(aq)
4 3 3 4
反应PbSO (s)+CO2- (aq)= PbCO (s)+SO 2- (aq)的平衡常数K= =3.4×105>105,PbSO 可以比较彻底
4 3 3 4 4
的转化为PbCO
3
(2)反应BaSO(s)+CO2- (aq)= BaCO (s)+SO 2- (aq)的平衡常数K= =0.04<<105,反应正向进行的程度
4 3 3 4有限
(3) Fe2+ Pb+HO+2HAc=Pb(Ac) +2H O 作还原剂
2 2 2 2
(4)Fe(OH) 、Al(OH) (5)Ba2+、Na+
3 3
【解析】铅膏中主要含有PbSO 、PbO 、PbO和Pb,还有少量Ba、Fe、Al的盐或氧化物等,向铅膏中加
4 2
入碳酸钠溶液进行脱硫,硫酸铅转化为碳酸铅,过滤,向所得固体中加入醋酸、过氧化氢进行酸浸,过氧化氢
可将溶液中的亚铁离子氧化为铁离子,酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时的pH可知,滤渣
主要成分为氢氧化铝、氢氧化铁,过滤后,向滤液中加入氢氧化钠溶液进行沉铅,得到氢氧化铅沉淀,滤液中
的金属阳离子主要为钠离子和钡离子,氢氧化铅再进行处理得到PbO。(1)“脱硫”中,碳酸钠溶液与硫酸铅反
应生成碳酸铅和硫酸钠,反应的离子方程式为:PbSO (s)+CO2- (aq)= PbCO (s)+SO 2- (aq),由一些难溶电解质
4 3 3 4
的溶度积常数的数据可知,K (PbCO )=7.4×10-14,K (PbSO )=2.5×10-8,反应PbSO (s)+CO2- (aq)= PbCO (s)
sp 3 sp 4 4 3 3
+SO2- (aq)的平衡常数K= = = = ≈3.4×105>105,说明可以转化的比
4
较彻底,且转化后生成的碳酸铅可由酸浸进入溶液中,减少铅的损失。(2)反应BaSO(s)+CO2- (aq)= BaCO (s)
4 3 3
+SO2- (aq)的平衡常数K= = = = ≈0.04<<105,说明该反应正向进行
4
的程度有限,因此加入碳酸钠不能使铅膏中的BaSO 完全转化。(3)(i)过氧化氢有氧化性,亚铁离子有还原性,
4
会被过氧化氢氧化为铁离子。(ii)过氧化氢促进金属Pb在醋酸溶液中转化为Pb(Ac) ,过氧化氢与Pb、HAc发
2
生氧还原反应生成Pb(Ac) 和HO,依据得失电子守恒和原子守恒可知,反应的化学方程式为:
2 2
Pb+HO+2HAc=Pb(Ac) +2H O。(iii)过氧化氢也能使PbO 转化为Pb(Ac) ,铅元素化合价由+4价降低到了+2价,
2 2 2 2 2 2
PbO 是氧化剂,则过氧化氢是还原剂。(4)酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时的pH可知,滤
2
渣主要成分为氢氧化铝、氢氧化铁。(5)依据分析可知,加入碳酸钠不能使铅膏中的BaSO 完全转化,铁离子、
4
铝离子转化为了氢氧化铁、氢氧化铝沉淀,铅转化为了氢氧化铅、最终变为了氧化铅,因此沉铅的滤液中,金
属离子有Ba2+和加入碳酸钠、氢氧化钠时引入的Na+。
【变式探究】
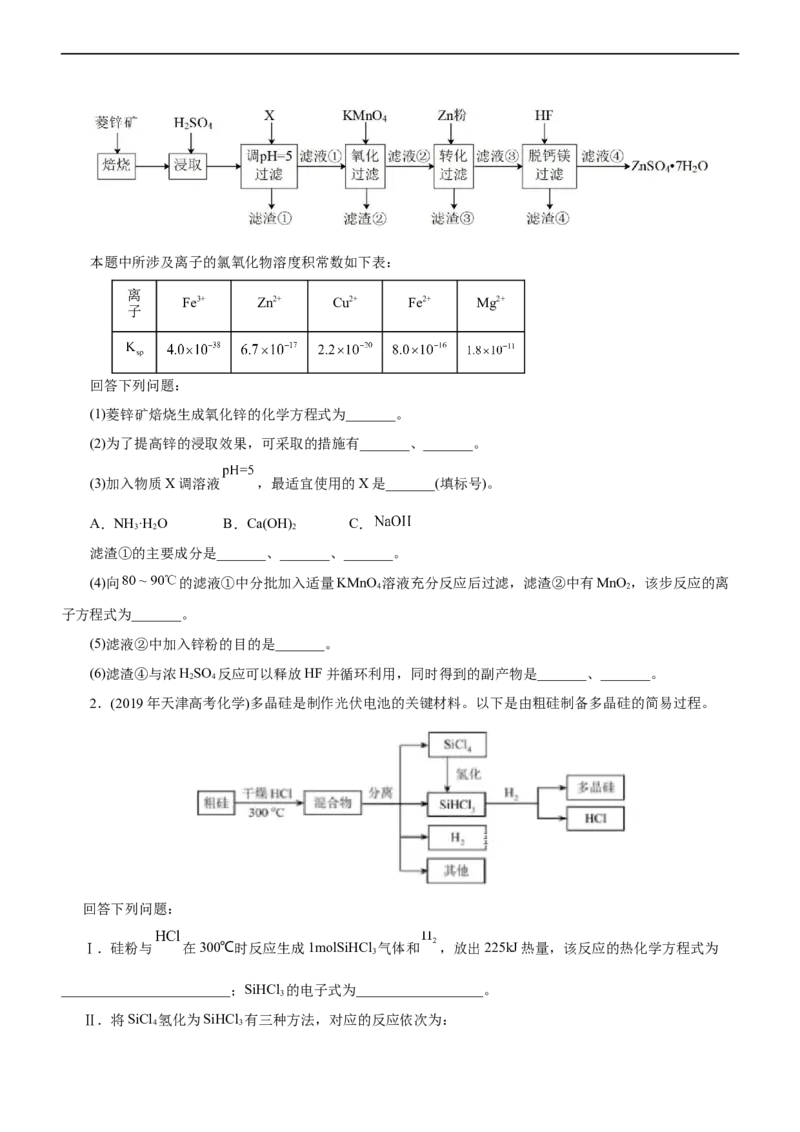
1.(2022•全国甲卷)硫酸锌(ZnSO)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫酸锌
4
可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合物。其制备流程
3 2
如下:本题中所涉及离子的氯氧化物溶度积常数如下表:
离
Fe3+ Zn2+ Cu2+ Fe2+ Mg2+
子
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
A.NH ·H O B.Ca(OH) C.
3 2 2
滤渣①的主要成分是_______、_______、_______。
(4)向 的滤液①中分批加入适量KMnO 溶液充分反应后过滤,滤渣②中有MnO,该步反应的离
4 2
子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓HSO 反应可以释放HF并循环利用,同时得到的副产物是_______、_______。
2 4
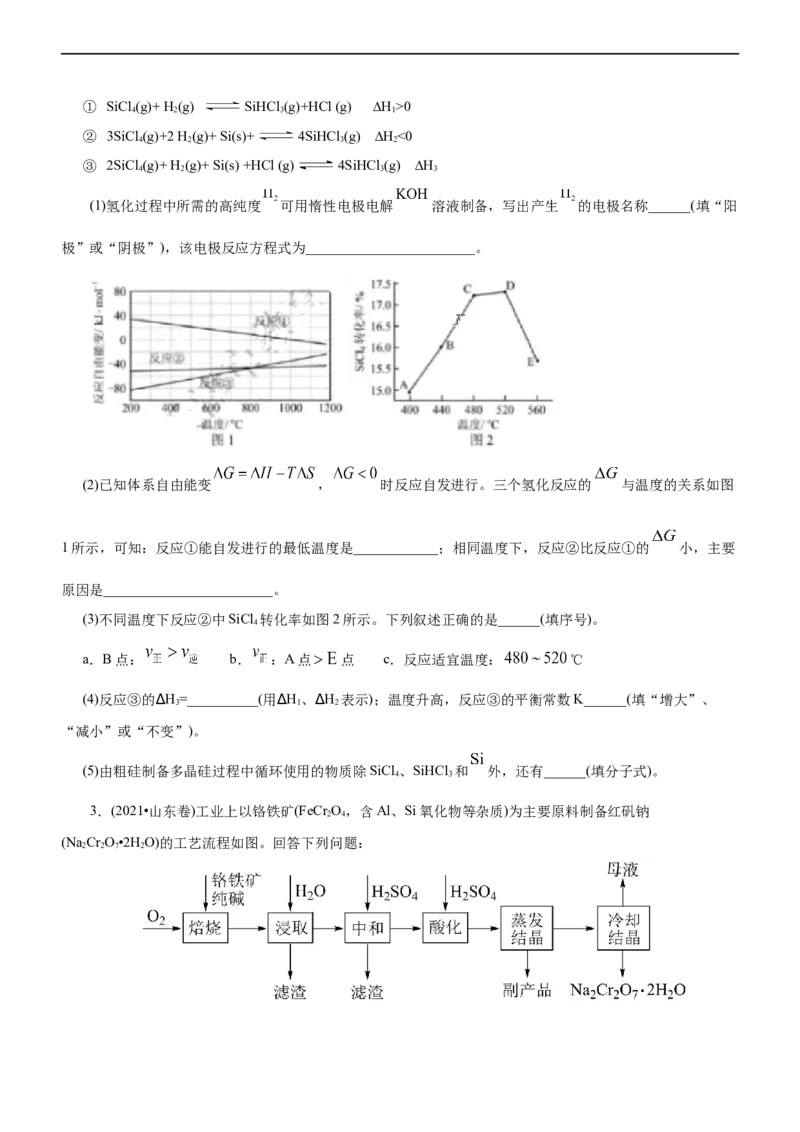
2.(2019年天津高考化学)多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
回答下列问题:
Ⅰ.硅粉与 在300℃时反应生成1molSiHCl 气体和 ,放出225kJ热量,该反应的热化学方程式为
3
________________________;SiHCl 的电子式为__________________。
3
Ⅱ.将SiCl 氢化为SiHCl 有三种方法,对应的反应依次为:
4 3① SiCl (g)+ H (g) SiHCl (g)+HCl (g) ∆H>0
4 2 3 1
② 3SiCl (g)+2 H (g)+ Si(s)+ 4SiHCl (g) ∆H<0
4 2 3 2
③ 2SiCl (g)+ H (g)+ Si(s) +HCl (g) 4SiHCl (g) ∆H
4 2 3 3
(1)氢化过程中所需的高纯度 可用惰性电极电解 溶液制备,写出产生 的电极名称______(填“阳
极”或“阴极”),该电极反应方程式为________________________。
(2)已知体系自由能变 , 时反应自发进行。三个氢化反应的 与温度的关系如图
1所示,可知:反应①能自发进行的最低温度是____________;相同温度下,反应②比反应①的 小,主要
原因是________________________。
(3)不同温度下反应②中SiCl 转化率如图2所示。下列叙述正确的是______(填序号)。
4
a.B点: b. :A点 点 c.反应适宜温度: ℃
(4)反应③的∆H=__________(用∆H、∆H 表示);温度升高,反应③的平衡常数K______(填“增大”、
3 1 2
“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除SiCl 、SiHCl 和 外,还有______(填分子式)。
4 3
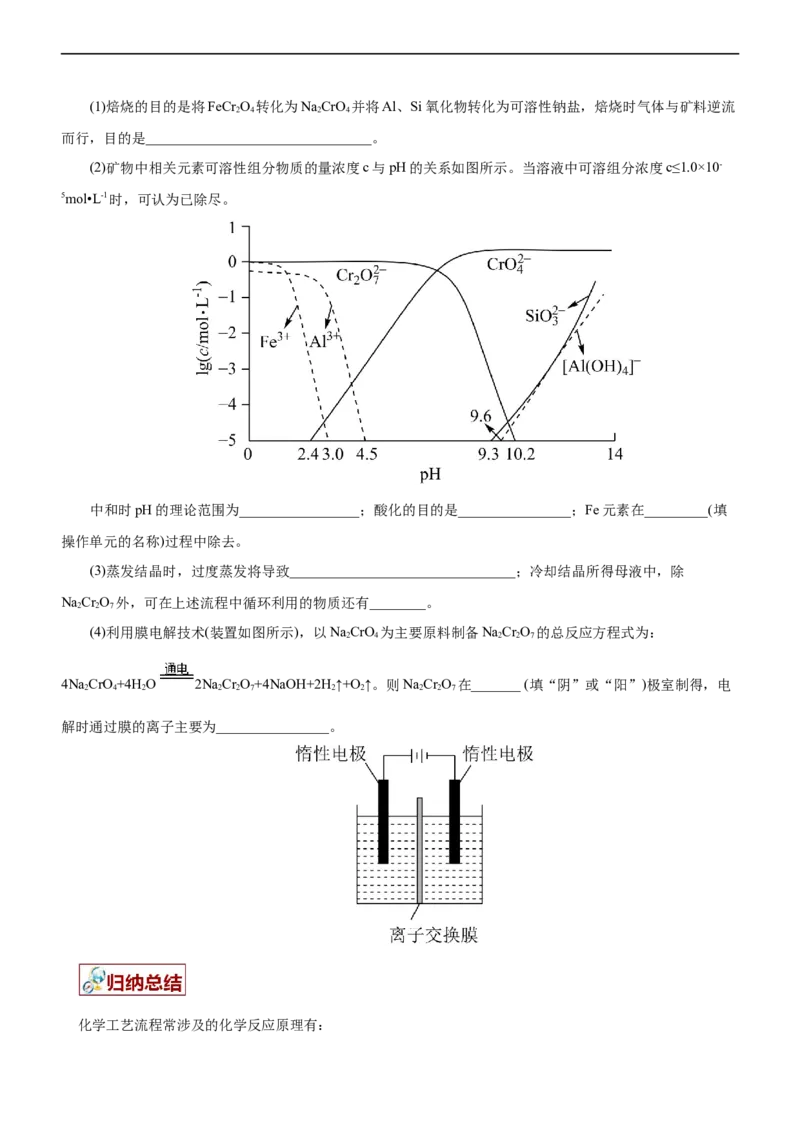
3.(2021•山东卷)工业上以铬铁矿(FeCrO,含Al、Si氧化物等杂质)为主要原料制备红矾钠
2 4
(Na Cr O•2H O)的工艺流程如图。回答下列问题:
2 2 7 2(1)焙烧的目的是将FeCr O 转化为NaCrO 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流
2 4 2 4
而行,目的是________________________________。
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度c≤1.0×10-
5mol•L-1时,可认为已除尽。
中和时pH的理论范围为_________________;酸化的目的是________________;Fe元素在_________(填
操作单元的名称)过程中除去。
(3)蒸发结晶时,过度蒸发将导致________________________________;冷却结晶所得母液中,除
NaCr O 外,可在上述流程中循环利用的物质还有________。
2 2 7
(4)利用膜电解技术(装置如图所示),以NaCrO 为主要原料制备NaCr O 的总反应方程式为:
2 4 2 2 7
4NaCrO+4H O 2NaCr O+4NaOH+2H↑+O ↑。则NaCr O 在_______ (填“阴”或“阳”)极室制得,电
2 4 2 2 2 7 2 2 2 2 7
解时通过膜的离子主要为________________。
化学工艺流程常涉及的化学反应原理有:(1)沉淀溶解平衡的相关应用:①沉淀的最小浓度控制;②沉淀转化的条件。
(2)反应速率及化学平衡理论在实际生产中的应用:①反应速率控制;②化学平衡移动;③化学平衡常数的
应用;④反应条件的控制。
(3)氧化还原反应的具体应用:①强弱规律;②守恒规律;③选择规律。
(4)盐类水解的具体应用:①水解规律;②水解反应的控制(抑制或促进)。
高频考点三 化学工艺流程与物质提纯
物质提纯类化工流程题以物质的分离、提纯为基础,涉及蒸发浓缩、趁热过滤、冷却结晶、蒸馏、萃取、
分液、重结晶、洗涤、干燥等基本操作,突出考查化学实验基本方法在物质分离、提纯中的作用。物质提纯类
化工流程题一般包括以下具体内容:
1.物质分离的6种常用方法
看目的 选方法
过滤
分离难溶物质和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法
(热滤或抽滤)
利用溶质在互不相溶的溶剂里的溶解度不同提纯分离物质,如用
萃取和分液
CCl 或苯萃取溴水中的溴
4
提纯溶解度随温度变化不大的溶质,如NaCl 蒸发结晶
提纯溶解度随温度变化较大的溶质,易水解的溶质或结晶水合物。如
冷却结晶
KNO、FeCl 、CuCl 、CuSO ·5H O、FeSO ·7H O等
3 3 2 4 2 4 2
分离沸点不同且互溶的液体混合物,如分离乙醇和甘油 蒸馏与分馏
利用气体易液化的特点分离气体,如合成氨工业采用冷却法分离氨气
冷却法
与氮气、氢气
2.获得产品阶段的主要操作
水洗:洗去晶体表面的杂质离子(适用于溶解度小的物质)
冰水洗涤:洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗
洗涤(冰水、
(适用于高温溶解度大、低温溶解度小的物质)
热水、有机
醇洗(常用于溶解度较大的物质):洗去晶体表面的杂质离子,并减少晶体在
溶剂)
洗涤过程中的溶解损耗(若对溶解度小的物质进行醇洗,则是为了洗去杂质离
子,并使其尽快干燥)
蒸发时的气
如从溶液中析出FeCl 、AlCl 、MgCl 等溶质时,应在HCl的气流中加热,以
3 3 2
体氛围抑制
防其水解
水解
如KCr O 和少量NaCl的混合溶液,若将混合溶液加热蒸发后再降温,则析
2 2 7
蒸发浓缩、
出的固体主要是KCr O ,母液中是NaCl和少量KCr O ,这样就可分离出
2 2 7 2 2 7
冷却结晶
大部分KCr O;同样原理可除去KNO 中的少量NaCl
2 2 7 3如NaCl和少量KCr O 的混合溶液,若将混合溶液蒸发一段时间,析出的固
2 2 7
蒸发结晶、
体主要是NaCl,母液中是KCr O 和少量NaCl;同样原理可除去NaCl中的
2 2 7
趁热过滤
少量KNO
3
3.“目的或原因”
目的或原因 答题模板
沉淀水洗的目的 除去××(可溶于水)杂质
a.减小固体的溶解度;b.除去固体表面吸附的杂质;c.乙醇挥发带走水
沉淀用乙醇洗涤的目的
分,使固体快速干燥
冷凝回流的作用及目的 防止××蒸气逸出脱离反应体系,提高××物质的转化率
防止××离子水解;防止××离子沉淀;确保××离子沉淀完全;防止××
控制溶液pH的目的
溶解等;促进/抑制××气体吸收/逸出
加过量A试剂的原因 使B物质反应完全(或提高B物质的转化率)等
温度过高××物质分解(如HO 、NH ·H O、浓硝酸、NH HCO 等)或××
2 2 3 2 4 3
温度不高于××℃的原因 物质挥发(如浓硝酸、浓盐酸)或××物质氧化(如NaSO 等)或促进××物
2 3
质水解(如AlCl 、FeCl 等)
3 3
减压蒸馏(减压蒸发)的 减小压强,使液体沸点降低,防止××物质受热分解(如HO 、浓硝
2 2
原因 酸、NH HCO 等)
4 3
蒸发、反应时的气体氛 抑制××离子的水解(如加热蒸发AlCl 溶液时需在HCl气流中进行;加
3
围 热MgCl ·6H O 得MgCl 时需在HCl气流中进行等)
2 2 2
配制某溶液前先煮沸水
除去溶解在水中的氧气,防止××物质被氧化
的原因
反应容器中和大气相通
指示容器中压强大小,避免反应容器中压强过大
的玻璃管的作用
【典例剖析】
【例1】(2022•江苏卷)实验室以二氧化铈(CeO)废渣为原料制备Cl-含量少的Ce (CO),其部分实验过程如
2 2 3 3
下:
(1)“酸浸”时CeO 与HO 反应生成Ce3+并放出O,该反应的离子方程式为_______。
2 2 2 2
(2)pH约为7的CeCl 溶液与NH HCO 溶液反应可生成Ce (CO) 沉淀,该沉淀中 含量与加料方式有关。
3 4 3 2 3 3
得到含Cl-量较少的Ce (CO) 的加料方式为_______(填序号)。
2 3 3
A.将NH HCO 溶液滴加到CeCl 溶液中
4 3 3
B.将CeCl 溶液滴加到NH HCO 溶液中
3 4 3(3)通过中和、萃取、反萃取、沉淀等过程,可制备 含量少的Ce (CO)。已知Ce3+能被有机萃取剂(简
2 3 3
称HA)萃取,其萃取原理可表示为
Ce3+ (水层)+3HA(有机层) Ce(A) (有机层)+3H+(水层)
3
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是_______。
②反萃取的目的是将有机层Ce3+转移到水层。使Ce3+尽可能多地发生上述转移,应选择的实验条件或采取
的实验操作有_______(填两项)。
③与“反萃取”得到的水溶液比较,过滤Ce (CO) 溶液的滤液中,物质的量减小的离子有_______(填化
2 3 3
学式)。
(4)实验中需要测定溶液中Ce3+的含量。已知水溶液中 可用准确浓度的(NH )Fe(SO ) 溶液滴定。以苯
4 2 4 2
代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充
完整实验方案:①准确量取25.00mL Ce3+溶液[c(Ce3+)约为0.2 mol·L-1],加氧化剂将 完全氧化并去除多余氧
化剂后,用稀硫酸酸化,将溶液完全转移到 容量瓶中后定容;②按规定操作分别将0.02000
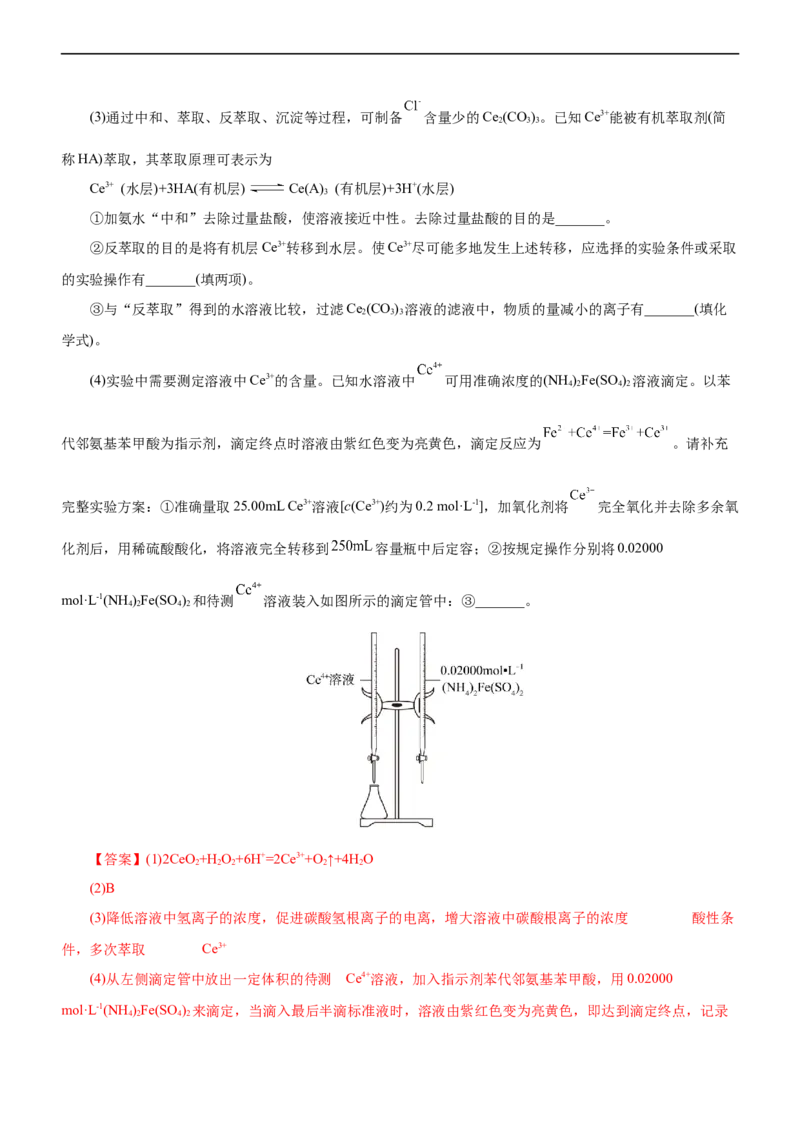
mol·L-1(NH )Fe(SO ) 和待测 溶液装入如图所示的滴定管中:③_______。
4 2 4 2
【答案】(1)2CeO+H O+6H+=2Ce3++O ↑+4H O
2 2 2 2 2
(2)B
(3)降低溶液中氢离子的浓度,促进碳酸氢根离子的电离,增大溶液中碳酸根离子的浓度 酸性条
件,多次萃取 Ce3+
(4)从左侧滴定管中放出一定体积的待测 Ce4+溶液,加入指示剂苯代邻氨基苯甲酸,用0.02000
mol·L-1(NH )Fe(SO ) 来滴定,当滴入最后半滴标准液时,溶液由紫红色变为亮黄色,即达到滴定终点,记录
4 2 4 2标准液的体积
【解析】首先用稀盐酸和过氧化氢溶液酸浸二氧化铈废渣,得到三价铈,加入氨水调节pH后用萃取剂萃
取其中的三价铈,增大三价铈浓度,之后加入稀硝酸反萃取其中的三价铈,再加入氨水和碳酸氢铵制备产物。
(1)根据信息反应物为CeO 与HO,产物为Ce3+和O,根据电荷守恒和元素守恒可知其离子方程式为:
2 2 2 2
2CeO+H O+6H+=2Ce3++O ↑+4H O;(2)反应过程中保持CeCl 少量即可得到含Cl-量较少的Ce (CO),故选
2 2 2 2 2 3 2 3 3
B;(3)①增大碳酸根离子的浓度有助于生成产物;②根据萃取原理可知,应选择的实验条件是酸性条件,为了
使Ce3+尽可能多地发生上述转移,可以采用多次萃取;③“反萃取”得到的水溶液中含有浓度较大的Ce3+,过
滤后溶液中Ce3+离子浓度较小;(4)应该用标准液滴定待测Ce4+溶液,用苯代邻氨基苯甲酸作指示剂,故答案为:
从左侧滴定管中放出一定体积的待测Ce4+溶液,加入指示剂苯代邻氨基苯甲酸,用0.02000
mol·L-1(NH )Fe(SO ) 来滴定,当滴入最后半滴标准液时,溶液由紫红色变为亮黄色,即达到滴定终点,记录
4 2 4 2
标准液的体积。
【例2】(2022•北京卷)铵浸法由白云石[主要成分为CaMg(CO ),含Fe O、SiO 杂质]制备高纯度碳酸钙和
3 2 2 3 2
氧化镁。其流程如下:
已知:
物质 Ca(OH) Mg(OH) CaCO MgCO
2 2 3 3
K
sp
(1)煅烧白云石的化学方程式为___________。
(2)根据下表数据分析:
n(NH Cl):n(CaO) CaO浸出率/ MgO浸出率/ w (CaCO )理论值/ w (CaCO )实测值/
4 3 3
98.4 1.1 99.7 -
98.8 1.5 99.2 99.5
98.9 1.8 98.8 99.5
99.1 6.0 95.6 97.6
已知:i.对浸出率给出定义ii.对w (CaCO )给出定义
3
①“沉钙”反应的化学方程式为___________。
②CaO浸出率远高于MgO浸出率的原因为___________。
③不宜选用的“n(NH Cl):n(CaO)”数值为___________。
4
④w (CaCO )实测值大于理论值的原因为___________。
3
⑤蒸馏时,随馏出液体积增大,MgO浸出率可出 增加至 ,结合化学反应原理解释MgO浸出
率提高的原因为___________。
(3)滤渣C为___________。
(4)可循环利用的物质为___________。
【答案】(1)CaMg(CO ) CaO+MgO+2CO ↑
3 2 2
(2) CaCl +NH·H O+CO=CaCO ↓+NHCl+H O Ca(OH) 的溶度积大于Mg(OH) ,溶液中Ca(OH) 能与
2 3 2 2 3 4 2 2 2 2
NH Cl反应,而Mg(OH) 不能 2.4:1 反应加入的CaO也转化为CaCO Mg(OH) +(NH)SO
4 2 3 2 4 2 4
MgSO +2NH↑+2H O,蒸馏时,NH 逸出促进NH +水解,溶液中H+浓度增大,有利于Mg(OH) 完全转化为
4 3 2 3 4 2
MgSO
4
(3)SiO、Fe O
2 2 3
(4)NH Cl、(NH )SO
4 4 2 4
【解析】由题给流程可知,白云石煅烧时,CaMg(CO ) 高温分解生成氧化钙和氧化镁,向煅烧后的固体
3 2
中加入氯化铵溶液和氧化钙,氧化钙和氯化铵溶液反应生成氯化钙和一水合氨,氧化镁与水反应生成氢氧化镁,
过滤得到含有氯化钙、一水合氨的滤液A和含有氢氧化镁、氧化铁、二氧化硅的滤渣B;向滤液A中通入二
氧化碳,二氧化碳与滤液A反应、过滤得到碳酸钙沉淀和氯化铵溶液;向滤渣B中加入硫酸铵溶液蒸馏,将
氢氧化镁转化为硫酸镁,氧化铁、二氧化硅与硫酸铵溶液不反应,过滤得到含有氧化铁、二氧化硅的滤渣C
和含有硫酸镁的滤液D;向滤液D中加入碳酸铵溶液,碳酸铵溶液与滤液D反应、过滤得到碳酸镁沉淀和硫
酸铵溶液,煅烧碳酸镁得到氧化镁,制备分离过程中氯化铵溶液和硫酸铵溶液可以循环利用。(1)白云石煅烧
时,CaMg(CO ) 高温分解生成氧化钙、氧化镁和二氧化碳,反应的化学方程式为CaMg(CO )
3 2 3 2
CaO+MgO+2CO ↑;(2)①由分析可知,“沉钙”时发生的反应为二氧化碳与氯化钙和一水合氨混合溶液反应生
2
成碳酸钙沉淀、氯化铵和水,反应的化学方程式为CaCl +NH·H O+CO=CaCO ↓+NHCl+H O;②由题给溶度
2 3 2 2 3 4 2
积数据可知,氢氧化钙的溶度积大于氢氧化镁,溶液中氢氧化钙的浓度大于氢氧化镁,能与氯化铵溶液反应生
成氯化钙和一水合氨,而氢氧化镁不能反应,所以氧化钙的浸出率远高于氧化镁;③由题给数据可知,氯化铵
和氧化钙的物质的量比为2.4:1时,氧化镁的浸出率最高,而碳酸钙的质量分数无论是理论值还是实测值都最低,所以不宜选用的物质的量比为2.4:1;④硫酸铵是强酸弱碱盐,铵根离子在溶液中的水解反应为吸热反
应,加热蒸馏时,氨气逸出促进铵根离子水解,溶液中氢离子浓度增大,有利于氢氧化镁完全溶解转化为硫酸
铵,所以氧化镁浸出率提高;(3)滤渣C为氧化铁、二氧化硅;(4)由分析可知,制备分离过程中氯化铵溶液和
硫酸铵溶液可以循环利用。
【变式探究】
1.(2022•广东选择性考试)稀土(RE)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土
矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸(C H COOH)熔点为44℃;月桂酸和(C H COO) RE均难溶于水。该工艺条件下,稀土离
11 23 11 23 3
子保持 价不变;(C H COO) Mg的K =1.8×10-8,Al(OH) 开始溶解时的pH为8.8;有关金属离子沉淀的相
11 23 2 sp 3
关pH见下表。
离子 Mg2+ Fe3+ Al3+ RE3+
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。
(2)“过滤1”前,用NaOH溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中Mg2+浓度为2.7g·Lˉ1。为尽可能多地提取RE3+,可提高
月桂酸钠的加入量,但应确保“过滤2”前的溶液中c(C H COO―)低于_______ mol·L-1 (保留两位有效数字)。
11 23
(4)①“加热搅拌”有利于加快RE3+溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂Pt Y。
3
①还原YCl 和PtCl 熔融盐制备Pt Y时,生成1molPt Y转移_______ mol电子。
3 4 3 3
②Pt Y/C用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化O 的还原,发生的电极反应为_______。
3 2
2.( 2019年新课标Ⅲ卷)高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与
硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:相关金属离子[c(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式
____________________________________________________。
(2)“氧化”中添加适量的MnO 的作用是将________________________。
2
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF 沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
2
_____________________________________________________________________。
(6)写出“沉锰”的离子方程式___________________________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNiCoMnO,其中Ni、Co、Mn的化合
x y z 2
价分别为+2、+3、+4。当x=y= 时,z=___________。
3.( 2019年新课标Ⅰ卷) 硫酸铁铵[NH Fe(SO )·xH O]是一种重要铁盐。为充分利用资源,变废为宝,在
4 4 2 2
实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是_________________。
(2)步骤②需要加热的目的是_________________,温度保持80~95 ℃,采用的合适加热方式是
_________________。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为__________(填标
号)。(3)步骤③中选用足量的HO,理由是_________________。分批加入HO,同时为了_________________,
2 2 2 2
溶液要保持pH小于0.5。
(4)步骤⑤的具体实验操作有______________,经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失
重5.6%。硫酸铁铵晶体的化学式为______________。
在解化工流程题无机物质的制备,常与物质分离与提纯联系在一起,制备的目标物质要容易分离出来,物
质分离与提纯有多种方法,总的说有物理方法和化学方法两大类:物理方法有过滤、蒸发、蒸馏、分液、萃取、
结晶、重结晶、渗析等;化学方法有沉淀法、热分解法、电解法、氧化还原法等;要根据目标物质的性质和特
点来选择适宜的制备、分离方法。在审题时,应粗看流程图,没必要看得非常明白(因耗时太多),然后接着往
下看问题作答,容易的迅速写下,做到“笔过留分”,难的再结合流程、信息回答。这样做耗时短,能得到大
部分分数。