文档内容
专题 41 工艺流程
(建议完成时间:45分钟 实际完成时间:_______分钟)
1.(2023·陕西渭南·统考模拟预测)铍及其化合物用途广泛,以绿柱石(主要组成是 ,
还含少量铁元素)和方解石(主要成分是 )为原料生产铍的工艺流程如图所示:
已知:铝铵矾 在不同温度下的溶解度如下表:
温度/℃ 0 10 20 30 40 60
溶解度/g 2.10 5.00 7.74 10.9 14.9 26.7
回答下列问题:
(1)绿柱石中Be元素的化合价为 。“熔炼”中生成气体的电子式为 。
(2)滤渣1中除 及难溶性硅酸盐外,还含有 (填化学式);“转化”后,要得到铝铵矾晶体,在中学实
验室中可采取的操作是 、 、过滤、洗涤、干燥。
(3)加 时,溶液中发生反应的离子方程式是 。
(4)“沉铍”时,若选用氢氧化钠溶液可能造成的影响是 ,所得母液中的主要溶质可返回到 工序循环利
用。
(5)“沉铍”时加入氨水调节pH至7.5,列式并计算说明此时溶液中的铍离子是否沉淀完全 。(已知:该条
件下, ;离子浓度 时,可认为离子沉淀完全)
(6)无水 可用作聚合反应的催化剂。 、 与足量C在600~800℃制备 的化学方程式为 。
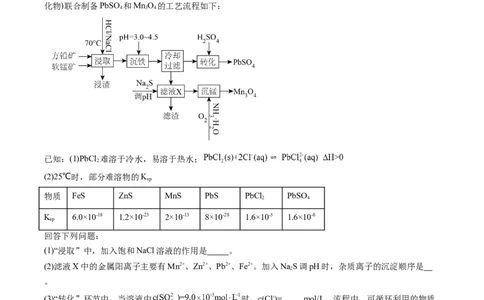
2.(2023·福建泉州·福建省永春第一中学校考模拟预测)工厂的含砷废水必须经过一定的处理。 某厂用
某含砷废水(含HAsO、HSO 、及少量Fe3+、Cu2+、Bi2+ )提取三氧化二砷(俗称砒霜,分子式:As O)的流
2 2 4 2 3
程如图:
已知:K [Fe(OH) ]=2.8 ×10-39,K [Cu(OH) ]=2.2 ×10-22,K [Bi(OH) ]=4.4 ×10-31。
sp 3 sp 2 sp 3
回答下列问题:
(1)滤渣a的成分是 (写化学式)。
1
原创精品资源学科网独家享有版权,侵权必究!(2)“沉淀”时,CuSO 溶液必须过量的原因是 。
4
(3)写出“还原”时Cu(AsO ) 与HO、SO 发生反应的化学方程式: 。
2 2 2 2
(4)红色还原渣(不溶于水)“氧化”时反应的离子方程式为 。
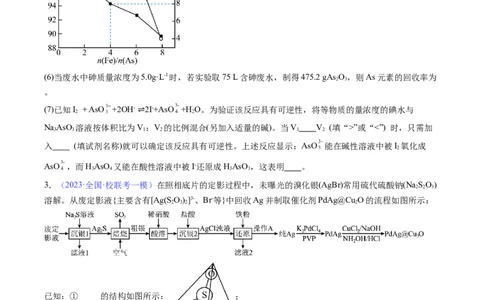
(5)“沉砷”后废水中残留的砷可用PFS(聚铁)进一步去除,用石灰乳调节废水的pH值,通入空气,PFS用
量[以 表示]、终点pH值与砷去除率的关系如图所示。PFS除砷的最佳条件是 。
(6)当废水中砷质量浓度为5.0g·L-1时,若实验取75 L含砷废水,制得475.2 gAs O,则As元素的回收率为
2 3
。
(7)已知I + AsO +2OH- 2I-+AsO +H O。为验证该反应具有可逆性,将等物质的量浓度的碘水与
2 2
Na
3
AsO
3
溶液按体积比为V⇌1 :V
2
的比例混合(另加入适量的碱)。当V
1
V
2
(填“>”或“<”) 时,只需加
入 (填试剂名称)就可以确定该反应具有可逆性。上述反应显示:AsO 能在碱性溶液中被I 氧化成
2
AsO ,而HAsO 又能在酸性溶液中被I-还原成HAsO ,这表明 。
3 4 3 3
3.(2023·全国·校联考一模)在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na SO)
2 2 3
溶解。从废定影液{主要含有[Ag(S O)]3-、Br-等}中回收Ag并制取催化剂PdAg@Cu O的流程如图所示:
2 3 2 2
已知:① 的结构如图所示: ;
② 。
请回答下列问题:
(1)写出NaSO 溶液溶解AgBr生成 的离子方程式: ,该反应的化学平衡常数为
2 2 3
。
(2)在 配合反应中,作配位原子的不可能是 (填字母)。a. 中的中心S原子 b. 中的端基S原子
(3)向滤液1中通入足量氯气后,通过一系列操作可分离出Br 。通入足量氯气后,Cl 发生的氧化还原反应
2 2
主要有 、 、 。
(4)“酸溶”过程中产生的有害气体是 (填化学式),实验室消除该有害气体的方法为 。
(5)操作 的目的是 。
(6)在制备PdAg@Cu O的反应中,NH OH被氧化成无污染物(N ),若获得0.5molPdAg@Cu O,理论上至少
2 2 2 2
需要NH OH g。
2
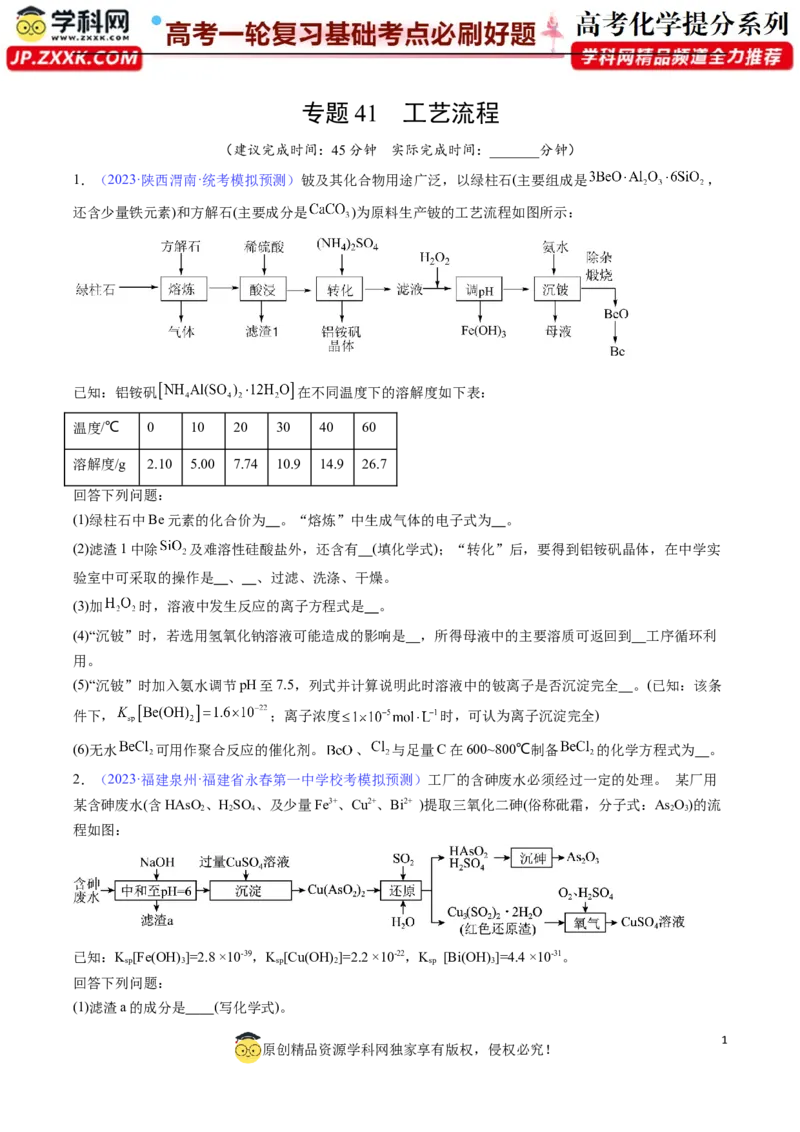
4.(2023·河北唐山·统考模拟预测)一种用方铅矿(PbS,含少量FeS)和软锰矿(MnO ,含少量铁、锌的氧
2
化物)联合制备PbSO 和MnO 的工艺流程如下:
4 3 4
已知:(1)PbCl 难溶于冷水,易溶于热水;
2
(2)25℃时,部分难溶物的K
sp
物质 FeS ZnS MnS PbS PbCl PbSO
2 4
K 6.0×10-18 1.2×10-23 2×10-13 8×10-28 1.6×10-5 1.6×10-8
sp
回答下列问题:
(1)“浸取”中,加入饱和NaCl溶液的作用是 。
(2)滤液X中的金属阳离子主要有Mn2+、Zn2+、Pb2+、Fe2+。加入NaS调pH时,杂质离子的沉淀顺序是
2
。
(3)“转化”环节中,当溶液中 时,c(Cl-)= mol/L。流程中,可循环利用的物质
是 (填化学式)。
(4)pH=8.5时,反应温度对MnO 的纯度和产率影响如图所示:
3 4①写出生成MnO 的离子方程式 。
3 4
②温度高于50℃,MnO 产率下降的主要原因是 。
3 4
(5)已知中心离子或原子上含有未成对电子的物质均有顺磁性。研究表明,MnO 的结构可表示为如图所示,
3 4
则MnO 的简单氧化物形式可写作 ,MnO (填“有”或“无”)顺磁性。
3 4 3 4
5.(2023·黑龙江大庆·统考一模)高铁酸钾 是新型多功能水处理剂,其生产工艺如图所示:
已知:① 与 溶液反应的产物与反应温度有关,温度较低时产物为 和 ;温度较
高时产物为 和 。
②同一条件下,溶液的碱性越强,高铁酸盐的稳定性越高。
回答下列问题:
(1)写出 与 溶液在较高温度下反应的离子方程式: 。
(2)向“溶液Ⅰ”中加入 固体起到的作用有降低 的溶解度、 、 ;
(3) 晶胞结构如图,设晶胞边长为apm,N 为阿伏加德罗常数的值,则距离最近的 间的距离为
A
,该晶体的密度为 。(列出计算式)(4)配制 溶液时,将 固体溶解在 水中(水的密度近似为 ),所得溶液的密度为
,则该溶液的物质的量浓度为 。(保留3位有效数字)
(5)步骤③发生的反应中氧化剂与还原剂的物质的量之比n(氧化剂)∶n(还原剂) 。对“湿产品”进行
“洗涤、干燥”时,洗涤剂最好选用 (填标号)溶液和异丙醇。
A. B. C.
6.(2023·黑龙江大庆·统考二模)水滑石具有特殊的层状结构,在催化、吸附等方面用途广泛,是一类极
具有研究潜质和使用价值的新材料。共沉淀法制备镁铝水滑石的工业生产流程如图所示。
请回答以下问题:
(1)基态镁原子的核外电子排布式为 。
(2)A1(NO) 力受热易分解,在实验室中需低温密封保存,Al(NO ) 在一定温度下分解的产物有氧化铝和物
3 3 3 3
质的量之比为4:1的两种气体,其中一种气体是单质,则该化学反应方程式为 ;反应釜中,NaCO
2 3
与Al(NO ) 在溶液中发生反应的离子方程式为 。
3 3
(3)陈化是沉淀反应完毕后,将初生的沉淀与母液一起放置一段时间,此过程中随着小晶粒的溶解,被吸附、
吸留和包藏在沉淀内部的杂质重新进入溶液,可提高沉淀的纯度。已知: ,
,则NaCO 与Mg(NO) 在溶液中反应生成沉淀的主要成分为 (填化学式)。
2 3 3 2
(4)检验洗涤液中是否含有钠离子的方法是 。
(5)控制烘干温度为100℃,不能高于此温度的原因是 。
(6)按上述流程用一定配比的原料制得某水滑石组成为 ,其中a、b、c、d为正整数。
取53g样品,用2L1mol·L-1的盐酸使其完全溶解,生成2.24LCO (已折算为标准状况),此时向溶液中滴加
2
1mol·L-1NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图,通过计算确定该水滑石的化学式为 。
7.(2023·山西晋城·晋城市第一中学校校考模拟预测) 作为一种新型锂电池正极材料受到广泛关
注。由菱锰矿( ,含有少量 、 、 、 等元素)制备 的流程如下:
已知: , , 。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为 。为提高溶矿速率,可采取的措施 (举1例)。
(2)加入少量 的作用是 。
(3)溶矿反应完成后,反应器中溶液 ,此时 ;用石灰乳调节至 ,除去
的金属离子是 。
(4)加入少量 溶液除去 ,生成的沉淀有 。
(5)在电解槽中,发生电解反应的离子方程式为 。
(6)煅烧窑中,生成 反应的化学方程式是 。
8.(2023·四川南充·统考模拟预测)某催化剂主要含Ni、Ni(OH) 、NiS及少量Zn、Fe、CuO、CaO、SiO
2 2
等杂质,从中制备金属Ni的工艺流程如下:
物质 NiS ZnS CuS FeS CaF
2
(2
0℃)
回答下列问题:(1)为提高废镍催化剂的浸出速率,可采取的措施有 (答一条即可)。
(2)反应 的平衡常数K= 。滤渣1的成分除CuS外还有 。
(3)NaClO氧化 为 的离子方程式为 。
(4)室温下用有机萃取剂HDEHP萃取金属离子的萃取率随溶液pH的变化如下左图。“萃取”时应调节溶
液pH的最佳范围是 。
(5)若用NaCO 溶液“沉镍”会产生 。为测定其组成,进行下列实验:称取干燥
2 3
沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如上图所示(300~480℃、500~750℃条件
下加热,收集到的气体产物均各只有一种,750℃以上残留固体为NiO)。则样品的化学式为 。
(6)“分解”时通N 的作用是 。
2
9.(2023·江西·校联考模拟预测)碲(Te)是重要的稀有元素,被誉为“现代高新技术材料的维生素”。一
种从碲化镉废料中(主要成分为CdTe、CdS、SiO)回收Te和Cd的工艺流程如图所示。
2
已知:室温下,饱和HS溶液的浓度为0.01mol·L-1,Ka=1.6×10-7,Ka=6.25×10-15;K (CdS)=1×10-26;K
2 1 2 sp sp
【Cd(OH) 】=5.3×10-15。
2
回答下列问题:
(1)“氧化浸出”时,温度控制在80℃的原因是 。“氧化浸出”过程中CdTe反应的离子方程式为
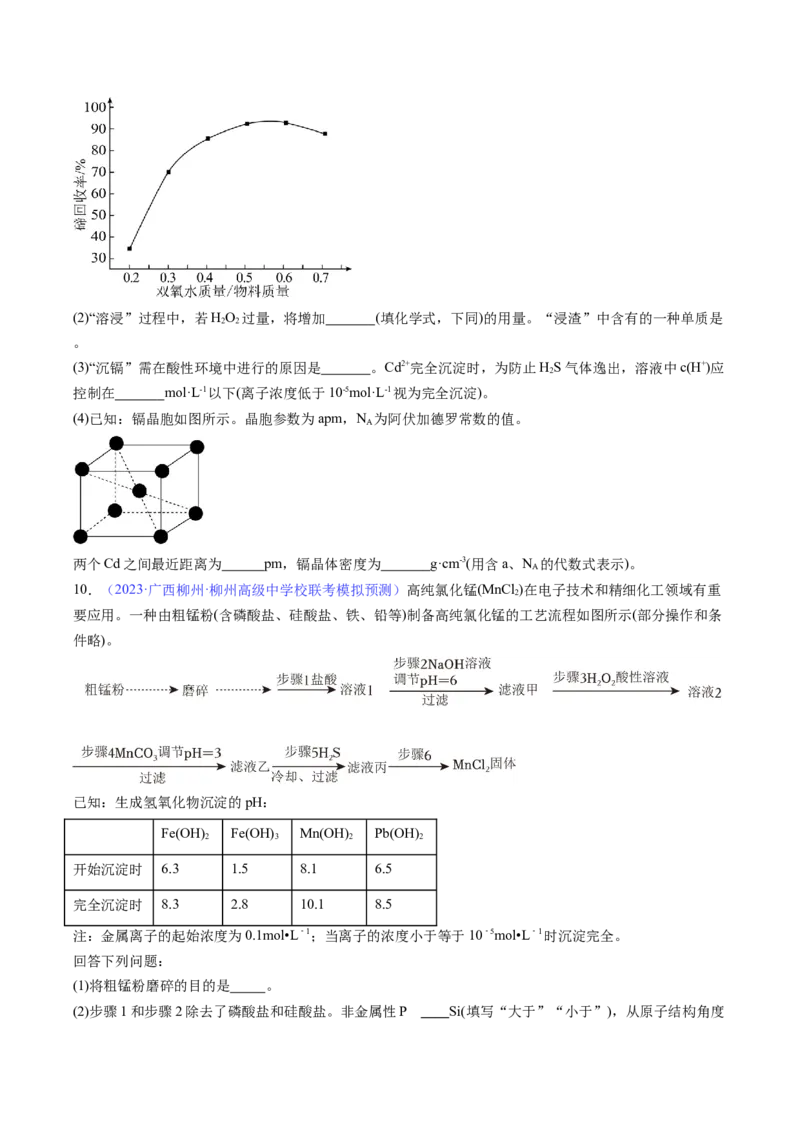
,其他条件不变,该过程中双氧水与物料质量比对碲回收率的影响如图所示。质量比高于0.6时,碲回收
率降低的原因是 。(2)“溶浸”过程中,若HO 过量,将增加 (填化学式,下同)的用量。“浸渣”中含有的一种单质是
2 2
。
(3)“沉镉”需在酸性环境中进行的原因是 。Cd2+完全沉淀时,为防止HS气体逸出,溶液中c(H+)应
2
控制在 mol·L-1以下(离子浓度低于10-5mol·L-1视为完全沉淀)。
(4)已知:镉晶胞如图所示。晶胞参数为apm,N 为阿伏加德罗常数的值。
A
两个Cd之间最近距离为 pm,镉晶体密度为 g·cm-3(用含a、N 的代数式表示)。
A
10.(2023·广西柳州·柳州高级中学校联考模拟预测)高纯氯化锰(MnCl )在电子技术和精细化工领域有重
2
要应用。一种由粗锰粉(含磷酸盐、硅酸盐、铁、铅等)制备高纯氯化锰的工艺流程如图所示(部分操作和条
件略)。
已知:生成氢氧化物沉淀的pH:
Fe(OH) Fe(OH) Mn(OH) Pb(OH)
2 3 2 2
开始沉淀时 6.3 1.5 8.1 6.5
完全沉淀时 8.3 2.8 10.1 8.5
注:金属离子的起始浓度为0.1mol•L﹣1;当离子的浓度小于等于10﹣5mol•L﹣1时沉淀完全。
回答下列问题:
(1)将粗锰粉磨碎的目的是 。
(2)步骤1和步骤2除去了磷酸盐和硅酸盐。非金属性P Si(填写“大于”“小于”),从原子结构角度解释非金属性不同的原因是 。
(3)所得滤液甲中的金属离子主要含有Mn2+、Fe2+和Pb2+等,且Pb2+不被HO 氧化。加入HO 目的是 。
2 2 2 2
(用离子方程式表示)。步骤4加入MnCO 得到沉淀的主要成分是 。
3
(4)已知PbS的K =8×10﹣28,MnS的K =2×10﹣10.步骤5的目的是除去Pb2+,反应的离子方程式是 ,
sp sp
为了保证Pb2+除尽,控制溶液中S2﹣浓度范围是 。(假设溶液中Mn2+、Pb2+的浓度是0.1mol•L﹣1)
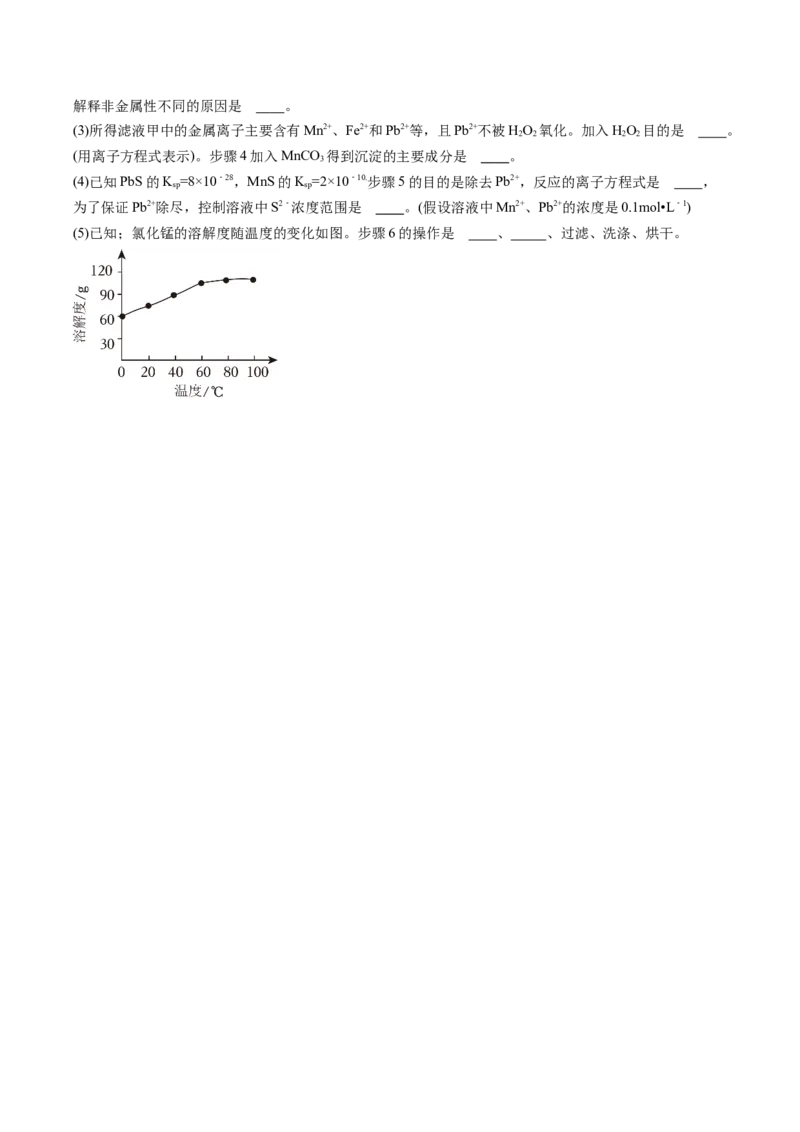
(5)已知;氯化锰的溶解度随温度的变化如图。步骤6的操作是 、 、过滤、洗涤、烘干。