文档内容
专题三 离子反应和离子方程式
必备知识 解读
一、离子反应和非离子反应
1.离子反应:有自由离子参加或生成的反应。
包括矿物或废料的酸溶、碱溶;从溶液中析出沉淀或晶体,或通过沉淀除去离子;加氧化
剂、还原剂溶解沉淀等复杂的氧化还原反应。
2.非离子反应:
(1).高温反应、煅烧矿石的反应。
(2). 燃烧反应
(3).气体反应。
总之不是在水溶液中进行的反应。
二、电解质、非电解质、电解质的电离
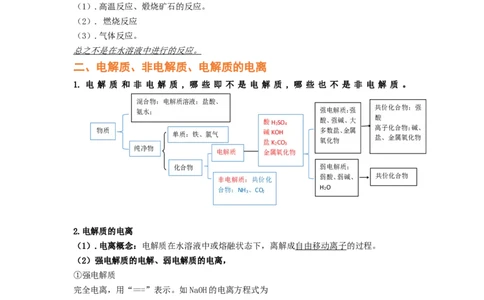
1. 电 解 质 和 非 电 解 质 , 哪 些 即 不 是 电 解 质 , 哪 些 也 不 是 非 电 解 质 。
混合物:电解质溶液:盐酸、
共价化合物:强
氨水; 强电解质:强
酸
酸H2SO4 酸、强碱、大
离子化合物:碱、
物质 单质:铁、氯气 碱KOH 多数盐、金属
盐、金属氧化物
盐K2CO3 氧化物
纯净物
电解质 金属氧化物
化合物 弱电解质:
弱酸、弱碱、 共价化合物
非电解质:共价化
合物:NH3 、CO2 H2O
2.电解质的电离
(1).电离概念:电解质在水溶液中或熔融状态下,离解成自由移动离子的过程。
(2)强电解质的电解、弱电解质的电离,
①强电解质
完全电离,用“===”表示。如NaOH的电离方程式为
NaOH===Na++OH-。
②弱电解质
部分电离,用“ ”表示。如HClO的电离方程式为HClO H++ClO-。
a.多元弱酸分步电离 ,且电离程度逐步减弱,以第一步电离为主。
如HS的电离方程式为 HS H++HS-;HS- H++S2-。
2 2
b.多元弱碱分步电离,但一步写出。
如Cu(OH) 的电离方程式为Cu(OH) Cu2++2OH-。
2 2
c.两性氢氧化物双向电离。
如Al(OH) 的电离方程式:H++AlO+HO Al(OH) Al3++3OH-。
3 2 3或[Al(OH)]-+H+ Al(OH) Al3++3OH-。
4 3
③酸式盐
a.强酸酸式盐完全电离,一步写出。
如NaHSO 在水溶液中的电离方程式为NaHSO===Na++H++SO,在熔融状态下的电离方程式
4 4
为NaHSO===Na++HSO。
4
b.多元弱酸酸式盐,第一步完全电离,其余部分电离。如 NaHCO 在水溶液中的电离方程
3
式为
NaHCO===Na++HCO,HCO H++CO。
3
3.电解质溶液怎么导电,导电性的强弱的比较。
(1)电解质溶液导电:电解质溶液中有能自由移动的阴、阳离子在电场的作用下移动导
电,在阳、阴两极产生氧化还原反应。
(2)导电性的强弱的比较:电解质溶液的导电性与溶液所有的阴或阳离子所带电荷的浓度
大小成正比。
(3)电解质溶液导电的变化:
三、离子方程式的书写
区别强电解质和弱电解质及非电解质的作用:写离子方程式时,是“拆”还是不“拆”,
就看是强电解质还是弱电解质。
1.书写离子反应方程式关键是“拆”:
能拆成离子的有:易溶的强电解质:强酸(HNO、HSO、HClO、HCl、HBr、HI、)强碱
3 2 4 4
(NaOH、KOH、Ca(OH)、Ba(OH))、易溶的盐(NHCl)。
2 2 4
不能拆成离子的或要写成整体的:沉淀或难溶物、气体、难电离的物质即弱电解质、碳化
物、氧化物、胶体、络合物或络离子(Fe(SCN)、Fe[Fe(CN)]、Ag(NH)]+)、弱酸
3 6 3 2
的酸式根(HCO、HS-、HSO)。
2. 未处于自由移动离子状态的反应,有关物质仍写化学式。
如浓硫酸参与的反应中,浓硫酸不能拆写成离子形式,而浓硝酸、浓盐酸要拆写成离子形
式。
3.氨水的写法
作为反应物写为 NH·HO;作为生成物,若有加热条件或浓度很大时,写为“NH↑+
3 2 3
HO”。
2
4.微溶物的写法
一般来说,微溶物的澄清溶液写成离子形式,微溶物呈悬浊状态或作生成物时写成化学
式,如澄清石灰水表示为“Ca2++2OH-”,而石灰乳则表示为“Ca(OH)”。
2
5.酸式盐的写法
①可溶性多元弱酸酸式盐的酸式酸根一律保留酸式酸根的书写形式,如 NaHCO 溶液中应拆
3
成“Na++HCO”,而不能拆成“Na++H++CO”。
②溶液中强酸的酸式盐一般拆写成离子形式,如溶液中NaHSO 应拆为“Na++H++SO”。
4应考能力 解 密
一、哪些离子之间可以发生离子反应,怎么反应
1.非氧化还原反应:复分解反应
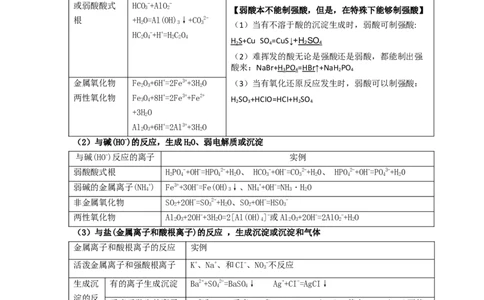
(1)与酸(H+)的反应,生成HO和弱电解质
2
与酸(H+)反应 实例 备注
的离子
OH- H++OH-=HO 记住弱酸的酸性强弱顺序
2
HSO>HPO>HAsO>HF>HNO>CHCOOH>HCO>HS>HPO-
弱酸根离子 CO2-+H+=HCO- 2 3 3 4 3 4 2 3 2 3 2 2 4
2 4 2 4 >HSO->HCIO>HCN>NH+>CHOH>HCO->HS->AL(OH)
3 4 6 5 3 3
或弱酸酸式 HCO-+AlO-
3 2 【弱酸本不能制强酸,但是,在特殊下能够制强酸】
根 +HO=Al(OH)↓+CO2-
2 3 3 (1)当有不溶于酸的沉淀生成时,弱酸可制强酸:
HCO-+H+=HCO
2 4 2 2 4
H S+Cu SO =CuS↓+H SO
2 4 2 4
(2)难挥发的酸无论是强酸还是弱酸,都能制出强
酸来:NaBr+H PO =HBr↑+NaH PO
3 4 2 4
金属氧化物 Fe
2
O
3
+6H+=2Fe3++3H
2
O (3)当有氧化还原反应发生时,弱酸可以制强酸:
两性氧化物 Fe 3 O 4 +8H+=2Fe3++Fe2+ H 2 SO 3 +HCIO=HCI+H 2 SO 4
+3HO
2
AlO+6H+=2Al3++3HO
2 3 2
(2)与碱(HO-)的反应,生成HO、弱电解质或沉淀
2
与碱(HO-)反应的离子 实例
弱酸酸式根 HPO-+OH-=HPO2-+HO、 HCO-+OH-=CO2-+H0、 HPO2-+OH-=PO3-+H0
2 4 4 2 3 3 2 4 4 2
弱碱的金属离子(NH+) Fe3++3OH-=Fe(OH)↓、NH++OH-=NH˙HO
4 3 4 3 2
非金属氧化物 SO+2OH-=SO2-+HO、SO+OH-=HSO-
2 3 2 2 3
两性氧化物 AlO+2OH-+3HO=2[Al(OH)]-或AlO+2OH-=2AlO-+HO
2 3 2 4 2 3 2 2
(3)与盐(金属离子和酸根离子)的反应 ,生成沉淀或沉淀和气体
金属离子和酸根离子的反应 实例
活泼金属离子和强酸根离子 K+、Na+、和CI-、NO-不反应
3
生成沉 有的离子生成沉淀 Ba2++SO2-=BaSO↓ Ag++CI-=AgCI↓
4 4
淀的反
反应后发生的离子 Fe2+和HCO-反应:Fe2++HCO-=FeCO↓+H+ 、其中FeCO↓+H+ 不能
3 3 3 3
应:
与反应物之一,继 共存,所以,H++HCO-=CO↑+HO,
3 2 2
续反应 两个反应和:Fe2++2HCO-=FeCO↓+CO↑+HO
3 3 2 2
又如:Mn2++2HCO-=MnCO↓+CO↑+HO
3 3 2 2
双水解反应和部分双水解反 Fe3++3AlO-+6HO=3Al(OH)↓+ Fe(OH)↓
2 2 3 3
应 Fe3++3CO2-+3HO=Fe(OH)↓+3HCO-
3 2 3 3
2Mg2++3CO2-+2HO=MgCO·Mg(OH)↓+2HCO-
3 2 3 2 3
2.氧化还原反应:强氧化性的离子与强还原性的离子发生反应,符合“强氧化性物质+强
还原性物质―→弱氧化性物质+弱还原性物质”。如:酸性KMnO 能氧化的离子顺序:S2->SO (SO 2-)>I->Fe2+>Br->CI-
4 2 3
HCIO能氧化的离子顺序:S2->SO (SO 2-)>I->Fe2+>Br->CI-
2 3
CI 能氧化的离子顺序:S2->SO (SO 2-)>I->Fe2+>Br-
2 2 3
H O 能氧化的离子顺序:S2->SO (SO 2-)>I->Fe2+
2 2 2 3
HNO 和浓H SO 能氧化的离子顺序:S2->SO (SO 2-)>I->Fe2+>Br-
3 2 4 2 3
Fe3+能氧化的离子顺序:S2->SO (SO 2-)>I-
2 3
3.络合反应类型:生成稳定的络合物或络离子。
常见的络合反应有:Fe3++3SCN-===Fe(SCN) ;
3
3Fe2++2[Fe(CN)]3-===Fe[Fe(CN)]↓;
6 6
AgOH+2NH·HO===[Ag(NH)]++OH-+2HO 。
3 2 3 2 2
二、高考中重要的化学反应
1.矿物或废料的酸溶、碱溶;加氧化剂、还原剂溶解沉淀等复杂的氧化还原反应。
(1)酸溶:多数弱酸盐沉淀,可以溶于酸:如:CaF(PO), Ca(OH)PO,MgFeFCO 。
5 4 3 4 2 3
FeTiO
3
+H
2
SO
4
(生成TiOSO
4
)、LiFePO
4.
金属氧化物或氢氧化物大多数可溶于酸,如:FeO 但是,SiO 不溶于酸。
3 4 2
CaF(PO) 加HSO 有CaSO↓、HF、Ca(HPO) 或HPO
5 4 3 2 4 4 2 4 2 3 4
(2)碱溶:加碱的目的:加NaOH或NaCO。A.洗涤,去油污. B.除去SiO. C.除去AIO
2 3 2 2 3
或AI
(3)加氧化剂、还原剂帮助溶解沉淀
① 少数弱酸盐不溶于酸的沉淀,可以溶于强氧化性的酸。如:CuS溶于 HNO ;
2 3
CuFeS 溶于HNO.
2 3
② 有些沉淀加NaSO 、H O 等还原剂帮助溶解
2 3 2 2
③ 有些沉淀加MnO 、KClO、NaClO、KMnO 、H O 等氧化剂进行溶解
2 3 4 2 2
④ 有些发生氧化还原反应,如:PbO+HCI
3 4
⑤ 有些不溶于稀酸。如:MnO 不溶于稀酸,但溶于浓HCI
2
(4)煅烧后,加酸加碱溶。
.加NaCO 要高温煅烧:NaCO+SiO NaSiO+CO
2 3。 2 3 2 2 3 2
NaCO+AIO 2NaAIO+CO 加酸溶
2 3 2 3 2 2
.CuS、CuFeS FeS高温煅烧后加酸溶
2 2、
.一些强酸盐沉淀,只能用还原剂煅烧后溶解。
如:BaSO 用C还原。
4
2.从溶液中析出沉淀或晶体,或通过沉淀除去离子;
(1).析出FeCO、MnCO、CaCO↓要加入:过量的HCO -、或氨水使溶液呈碱性。
3 3 3 3
Fe2+中加HCO -:写出离子方程式________________________________________________
3
Mn2+中加NHHCO 和氨水:写出离子方程式_________________________________________
4 3
Ca2+中通入CO 和氨水:________________________________________________
2【答案】Fe2++2HCO-=FeCO↓+CO↑+HO
3 3 2 2
Mn2++HCO-+NH.HO=MnCO↓+NH++HO
3 3 2 3 4 2
Ca2++CO+2NH.HO=CaCO↓+2NH++2HO
2 3 2 3 4 2
(2).溶液中:除去Ca2+:可加入CO2-、F-、CO2-等离子,再过滤生成生成CaCO↓.CaF↓
2 4 3 2 4 2
CaCO↓、
3
除Fe3+:可加入与H+反应的物质,调节PH值。生成Fe(OH)↓
3
除Mg2+:可加入F-后再过滤.生成MgF↓
2
除Fe2+ :可加入H O 或氯水,再调节PH值。Fe2+被氧化Fe3+,最后生成Fe(OH)↓
2 2 3
(3)易溶的物质在溶液中反应,生成溶解度较小的晶体。如:
Na FeO +KCl=K FeO ↓+NaCl K FeO 溶解度较小
2 4 2 4 2 4
3. 有些未知的反应,题目会告诉反应产物,要求写出方程式。
三、物质或离子推断
1.未知物质(或离子)之间的相互混合(通过实验的形式呈现),发生离子反应,产生一
定的现象,然后根据产生的不同的现象,判断未知物质(或离子)的成分。
2.要求同学掌握已知物质(离子)之间的离子反应,会产生什么现象,弄清离子反应与现
象的关系;根据现象,判断成分,弄清现象(沉淀、气体、颜色)与未知物质(或离
子)之间的关系。
高考实例剖析
高考怎么考《离子反应》题,根据高考指挥棒来学习《离子反应》题
【高考实例一】离子反应方程式的正误判断
例1.(2022·全国甲卷)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH +2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
2 4 4
=BaSO ↓+2H O
4 2
【答案】D
【解析】A项:硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为
NO或NO ,反应的离子方程式为4H++2NO +S2-=S↓+2NO ↑+2H O(浓)或8H++2NO +3S2-
2 2 2=3S↓+2NO↑+4H O(稀),A错误;
2
B项:明矾在水中可以电离出Al3+,可以与氨水中电离出的OH-发生反应生成Al(OH) ,但由
3
于氨水的碱性较弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为
3
Al3++3NH ·H O=Al(OH) ↓+3NH ,B错误;
3 2 3
C项:硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳
则根据其通入的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO
+H O+CO =H SiO ↓+CO (CO 少量)或SiO +2H O+2CO =H SiO ↓+2HCO (CO 过量),C
2 2 2 3 2 2 2 2 3 2
错误;
D项:将等物质的量浓度的Ba(OH) 与NH HSO 溶液以体积比1:2混合,Ba(OH) 电离出的
2 4 4 2
OH-与NH HSO 电离出的H+反应生成水,Ba(OH) 电离出的Ba2+与NH HSO 电离出的SO
4 4 2 4 4
反应生成BaSO 沉淀,反应的离子方程为为Ba2++2OH-+2H++SO =BaSO ↓+2H O,D
4 4 2
正确;
故答案选D。
【实战演练】
1.(2022届高考浙江卷)下列反应的离子方程式不正确的是
A.盐酸中滴加 溶液:
B. 溶液中通入过量 :
C.乙醇与 酸性溶液反应:
D.溴与冷的 溶液反应:
【答案】D【解析】A项:盐酸中滴加 溶液,发生离子反应生成硅酸沉淀,该反应的离子方程
式为 ,A正确;
B项:亚硫酸的酸性强于碳酸,因此, 溶液中通入过量 发生离子反应生成亚硫
酸氢钠和二氧化碳,该反应的离子方程式为 ,B正确;
C项:乙醇与 酸性溶液反应发生反应,乙醇被氧化为乙酸, 被还原为 ,
该反应的离子方程式为 ,
C正确;
D项:类比氯气与碱反应可知,溴与冷的 溶液反应生成溴化钠、次溴酸钠和水,该
反应的离子方程式为 ,D不正确。
综上所述,本题选D。
2.(2021年全国高考乙卷试题)下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙:
B.过量铁粉加入稀硝酸中:
C.硫酸铝溶液中滴加少量氢氧化钾溶液:
D.氯化铜溶液中通入硫化氢:
【答案】A
【解析】A项:硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离
子方程式为:C +CaSO =CaCO +S ,故A正确;
4 3
B项:过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式应为:3Fe+8H+
+2N =3Fe2++2NO↑+4H O,故B错误;
2C项:硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应
为:Al3++3OH-=Al(OH) ↓,故C错误;
3
D项:硫化氢为弱电解质,书写离子方程式时不能拆,离子方程式应为:Cu2+
+H S=CuS↓+2H+,故D错误;
2
答案选A。
【高考实例二】与离子反应有关的物质推断
例2.(2022·全国乙卷)某白色粉末样品,可能含有 、 、 和
。取少量样品进行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是
A. B.
C. D.
【答案】A
【解析】由题意可知,①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之
间能共存,
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在
Na S O ,发生反应S O +2H+=S↓+H O+SO ↑,离心分离,
2 2 3 2 2 2
③取②的上层清液,向其中滴加BaCl 溶液,有沉淀生成,则沉淀为BaSO ,说明固体中存
2 4
在Na SO ,不能确定是否有Na SO 和Na CO ,Na SO 与过量盐酸反应生成二氧化硫,
2 4 2 3 2 3 2 3
Na CO 与过量盐酸反应生成二氧化碳,而这些现象可以被Na S O 与过量盐酸反应的现
2 3 2 2 3
象覆盖掉,综上分析,该样品中确定存在的是:Na SO 、Na S O ,
2 4 2 2 3
答案选A。
【实战演练】
3.(2022学年甘肃天水市高三第一次考试)固体粉末X中可能含有Fe、FeO、CuO、MnO、KCl和KCO 中的若干种。为确定该固体粉末的成分,某同学依次进行了以下实
2 2 3
验:①将X加入足量水中,得到不溶物Y和溶液Z;②取少量Y加入足量浓盐酸,加
热,产生黄绿色气体,并有少量红色不溶物;③用玻璃棒蘸取溶液Z滴于pH试纸上,
试纸呈蓝色;④向溶液Z中滴加AgNO 溶液,生成白色沉淀。通过以上实验现象,下列
3
结论正确的是( )。
A.X中一定不存在FeO
B.不溶物Y中一定含有MnO 和CuO,而Fe与FeO中至少含有一种
2
C.Z溶液中一定含有KCO
2 3
D.若向④生成的白色沉淀中滴加过量盐酸,沉淀不完全溶解,则粉末X中含有KCl
【答案】C
【解析】①将X加入足量水中,得到不溶物Y和溶液Z,Y中含有Fe、FeO、CuO、MnO 中的
2
若干种;②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不溶
物,黄绿色气体为Cl,红色不溶物为Cu,说明Y中一定含有Fe、CuO、MnO;③用玻
2 2
璃棒蘸取溶液Z于pH试纸上,试纸呈蓝色,说明溶液呈碱性,则溶液Z中一定含有
KCO,可能含有KCl;④向溶液Z中滴加AgNO 溶液,生成白色沉淀,该沉淀一定含有
2 3 3
碳酸银,可能含有氯化银。
A项:不能确定X中是否含有FeO,A错误;
B项:不溶物Y中一定含有MnO、CuO和Fe,B错误;
2
C项:据以上分析,Z溶液中一定含有KCO,C正确;
2 3
D项:若向④生成的白色沉淀中滴加过量盐酸,沉淀不完全溶解,则粉末X中不一定含有
KCl,因为加入盐酸时引入了Cl-,D项错误。
4.(2022届浙江省精诚联盟高三适应性考试)某固体混合物X,含有Al(SO)、
2 4 3
FeCl、NaCO 和NaSiO 中的几种,进行如下实验:①X与水作用有气泡冒出,得到有
3 2 3 2 3
色沉淀Y和弱碱性溶液Z;②沉淀Y与足量NaOH溶液充分作用,部分溶解。下列说法
不正确的是( )。
A.沉淀Y一定能溶于盐酸
B.溶液Z中溶质一定不含NaSiO
2 3
C.混合物X至少含有三种成分
D.混合物X中一定含有NaCO、FeCl,可能含有Al(SO)
2 3 3 2 4 3
【答案】B
【解析】某固体混合物X,含有Al(SO)、FeCl、NaCO 和NaSiO 中的几种,①X与水
2 4 3 3 2 3 2 3
作用有气泡冒出,得到有色沉淀Y和弱碱性溶液Z,生成气体的物质只有NaCO,而几
2 3
种物质中没有酸,说明与NaCO 发生双水解反应生成二氧化碳气体,生成的有色沉淀
2 3
中一定存在氢氧化铁,可能含有氢氧化铝、硅酸;②沉淀Y与NaOH溶液作用,部分溶
解,说明有色沉淀中存在氢氧化铝或硅酸,则可能存在Al(SO) 或NaSiO 中的一
2 4 3 2 3
种。
A项:根据上述分析可知,沉淀Y一定含有氢氧化铁,一定能溶于盐酸。选项A正确;
B项:溶液Z中溶质可能含有Al(SO) 或NaSiO 中的至少一种,选项B不正确;
2 4 3 2 3
C项:混合物X中一定含有FeCl、NaCO,至少含有Al(SO) 或NaSiO 中的一种,则至
3 2 3 2 4 3 2 3少三种成分,选项C正确;
D项:混合物X中一定含有NaCO、FeCl,可能含有Al(SO),选项D正确。
2 3 3 2 4 3
【高考实例三】非选择题中的离子反应方程式
PbSO PbO PbO
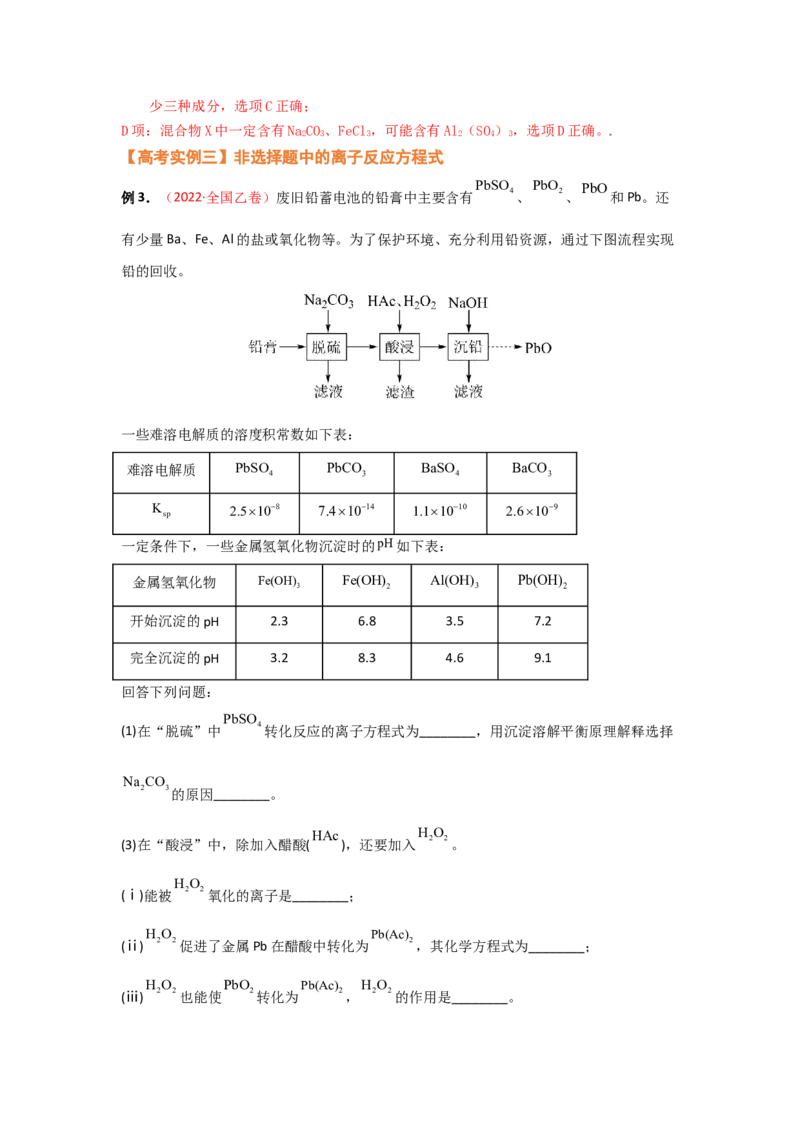
例3.(2022·全国乙卷)废旧铅蓄电池的铅膏中主要含有 4、 2、 和Pb。还
有少量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现
铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 PbSO PbCO BaSO BaCO
4 3 4 3
K 2.5108 7.41014 1.11010 2.6109
sp
一定条件下,一些金属氢氧化物沉淀时的pH如下表:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Pb(OH)
3 2 3 2
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
PbSO
(1)在“脱硫”中 4转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择
Na CO
2 3的原因________。
HAc H O
(3)在“酸浸”中,除加入醋酸( ),还要加入 2 2。
H O
(ⅰ)能被 2 2氧化的离子是________;
H O Pb(Ac)
(ⅱ)
2 2促进了金属Pb在醋酸中转化为 2,其化学方程式为________;
H O PbO Pb(Ac) H O
(ⅲ)
2 2也能使 2转化为 2, 2 2的作用是________。2- 2- 2- 2-
【答案】(1) PbSO (s)+CO3 (aq)= PbCO (s)+SO4 (aq) 反应PbSO (s)+CO3 (aq)= PbCO (s)+SO4
4 3 4 3
c(SO2-)
4
(aq)的平衡常数K=c(CO
3
2-)=3.4105>105,PbSO
4
可以比较彻底的转化为PbCO
3
(3) Fe2+ Pb+H O +2HAc=Pb(Ac) +2H O 作还原剂
2 2 2 2
【解析】铅膏中主要含有PbSO 、PbO 、PbO和Pb,还有少量Ba、Fe、Al的盐或氧化物等,
4 2
向铅膏中加入碳酸钠溶液进行脱硫,硫酸铅转化为碳酸铅,过滤,向所得固体中加入醋酸、
过氧化氢进行酸浸,过氧化氢可将溶液中的亚铁离子氧化为铁离子,酸浸后溶液的pH约为
4.9,依据金属氢氧化物沉淀时的pH可知,滤渣主要成分为氢氧化铝、氢氧化铁,过滤后,
向滤液中加入氢氧化钠溶液进行沉铅,得到氢氧化铅沉淀,滤液中的金属阳离子主要为钠
离子和钡离子,氢氧化铅再进行处理得到PbO。
(1)“脱硫”中,碳酸钠溶液与硫酸铅反应生成碳酸铅和硫酸钠,反应的离子方程式为:
2- 2-
PbSO (s)+CO3 (aq)= PbCO (s)+SO4 (aq),由一些难溶电解质的溶度积常数的数据可知,
4 3
2- 2-
K (PbCO )=7.4 10-14,K (PbSO )=2.5 10-8,反应PbSO (s)+CO3 (aq)= PbCO (s)+SO4 (aq)的平衡
sp 3 sp 4 4 3
c(SO2
4
-) c(Pb2+)c(SO2
4
-) K sp (PbSO 4 ) 2.510-8
常数K= c(CO 3 2-) =c(Pb2+)c(CO 3 2-)=K sp (PbCO 3 )= 7.410-14 ≈3.4 105>105,说明可以转化的
比较彻底,且转化后生成的碳酸铅可由酸浸进入溶液中,减少铅的损失。
(3)(i)过氧化氢有氧化性,亚铁离子有还原性,会被过氧化氢氧化为铁离子。
(ii)过氧化氢促进金属Pb在醋酸溶液中转化为Pb(Ac) ,过氧化氢与Pb、HAc发生氧还原
2
反应生成Pb(Ac) 和H O,依据得失电子守恒和原子守恒可知,反应的化学方程式为:
2 2
Pb+H O +2HAc=Pb(Ac) +2H O。
2 2 2 2
(iii)过氧化氢也能使PbO 转化为Pb(Ac) ,铅元素化合价由+4价降低到了+2价,PbO 是
2 2 2
氧化剂,则过氧化氢是还原剂。
【实战演练】
5.(2022·江西九江·二模)以碳酸锰铜矿(主要成分为MnCO 、CuCO ,还含有Fe O 、FeO
3 3 2 3
等杂质)为原料制备硫酸锰的一种工艺流程如下:(1)“氧化”时,反应的离子方程式为_______。可用一种试剂检验氧化后的溶液中是否含有
Fe2+,该试剂为_______(写化学式)。
(2)加入MnCO 调节pH=3.3时可以将Fe3+转化为Fe(OH) 而除去,该反应的离子方程式为
3 3
_______。
【答案】(1) MnO +2Fe2++4H+=2Fe3++Mn2++2H O K [Fe(CN) ] (或KMnO )
2 2 3 6 4
(2)3MnCO +2Fe3+ +3H O = 2Fe(OH) +3Mn2+ +3CO ↑
3 2 3 2
【解析】碳酸锰铜矿主要成分为MnCO 、CuCO ,还含有Fe O 、FeO杂质,用硫酸酸浸,
3 3 3 4
得到硫酸锰、硫酸铜、硫酸铁、硫酸亚铁的混合溶液,加入二氧化锰, Fe2+被氧化为
Fe3+;加入MnCO 调节pH生成氢氧化铁沉淀;过滤后向溶液中通入氨气生成氢氧化铜沉淀,
3
过滤,向滤液中加入NH HCO ,生成MnCO 沉淀,MnCO 沉淀中加硫酸,得到硫酸锰溶液,
4 3 3 3
以此解题。
(1)“氧化”时,二氧化锰把酸浸后的二价铁氧化为三价铁,离子方程式为: MnO +2Fe2+
2
+4H+=2Fe3++Mn2++2H O;二价铁和铁氰化钾相遇的时候会生成蓝色沉淀,可以用铁氰化钾来
2
检验,另外二价铁有还原性,可以使高锰酸钾褪色,可以用酸性高锰酸钾来检验,故答案
为:MnO +2Fe2++4H+=2Fe3++Mn2++2H O ;K [Fe(CN) ] (或KMnO );
2 2 3 6 4
(2)碳酸锰消耗三价铁水解产生的氢离子,导致氢离子浓度降低,促进三价铁水解,该反应
的离子方程式为:3MnCO +2Fe3+ +3H O = 2Fe(OH) +3Mn2+ +3CO ↑;
3 2 3 2