文档内容
专题十二 化学反应速率与化学平衡
考点一 化学反应速率及其影响因素
1.化学反应速率的计算
v(B)==。
用上式进行某物质反应速率计算时需注意以下几点:
(1)浓度变化只适用于气体和溶液中的溶质,不适用于固体和纯液体。
(2)化学反应速率是某段时间内的平均反应速率,而不是即时速率,且计算时取正值。
(3)同一反应用不同的物质表示反应速率时,数值可能不同,但意义相同。不同物质表示的反应速率之
比等于其化学计量数之比。
(4)计算反应速率时,若给出的是物质的量的变化值,要转化为物质的量浓度的变化值(计算时一定要
除以体积),再进行计算。
2.化学反应速率快慢的比较方法
首先看用各物质表示的速率单位是否统一,若不统一,换算成相同的单位。由于同一化学反应的反应
速率用不同物质表示时数值可能不同,所以比较反应的快慢不能只看数值的大小,而要进行一定的转化。
具体方法有:
(1)归一法:换算成用同一种物质表示的速率,一般换算成化学计量数小的物质。
(2)比值法:用各物质表示的反应速率除以对应各物质的化学计量数,然后再对求出的数值进行大小排
序,数值大的反应速率快。如反应mA+nB===pC+qD,在不同情况下测得的反应速率为v(A)和v(B),若
>,则反应速率v(A)>v(B)。
3.稀有气体对反应速率的影响
(1)恒容:充入“惰性气体”――→总压增大→物质浓度不变(活化分子浓度不变),反应速率不变。
(2)恒压:充入“惰性气体”――→体积增大――→物质浓度减小(活化分子浓度减小)――→反应速率
减慢。
4.纯液体、固体对化学反应速率的影响
在化学反应中,纯液体和固态物质的浓度为常数,故不能用固态物质的变化来表示反应速率,但是固
态反应物颗粒的大小是影响反应速率的条件之一,如煤粉由于表面积大,燃烧就比煤块快得多。
【跟踪训练】1.(2022·浙江·模拟预测)一定温度下,利用测压法在刚性反应器中研究固体催化剂作用下的A的分解反应: 。体系的总压强p随时间t的变化如表所示:
t/'min 0 100 150 250 420 540 580 900
p/kPa 12.1 13.3 13.9 15.l 17.14 18.58 19.06 a
下列说法正确的是A.100~250min,消耗A的平均速率为
B.推测a一定为22.9
C.适当升高体系温度,改用表面积更大的催化剂可加快反应速率
D.其他条件不变,改用容积更小的刚性反应器,反应速率增大
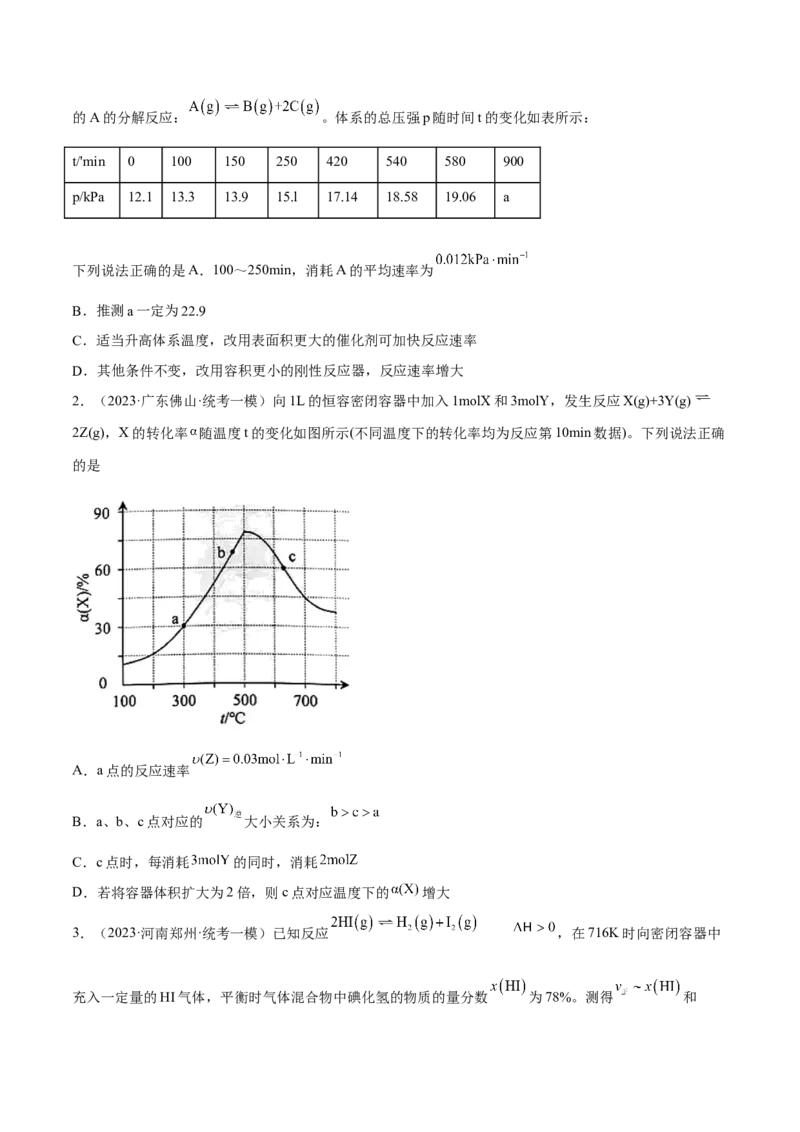
2.(2023·广东佛山·统考一模)向1L的恒容密闭容器中加入1molX和3molY,发生反应X(g)+3Y(g)
2Z(g),X的转化率 随温度t的变化如图所示(不同温度下的转化率均为反应第10min数据)。下列说法正确
的是
A.a点的反应速率
B.a、b、c点对应的 大小关系为:
C.c点时,每消耗 的同时,消耗
D.若将容器体积扩大为2倍,则c点对应温度下的 增大
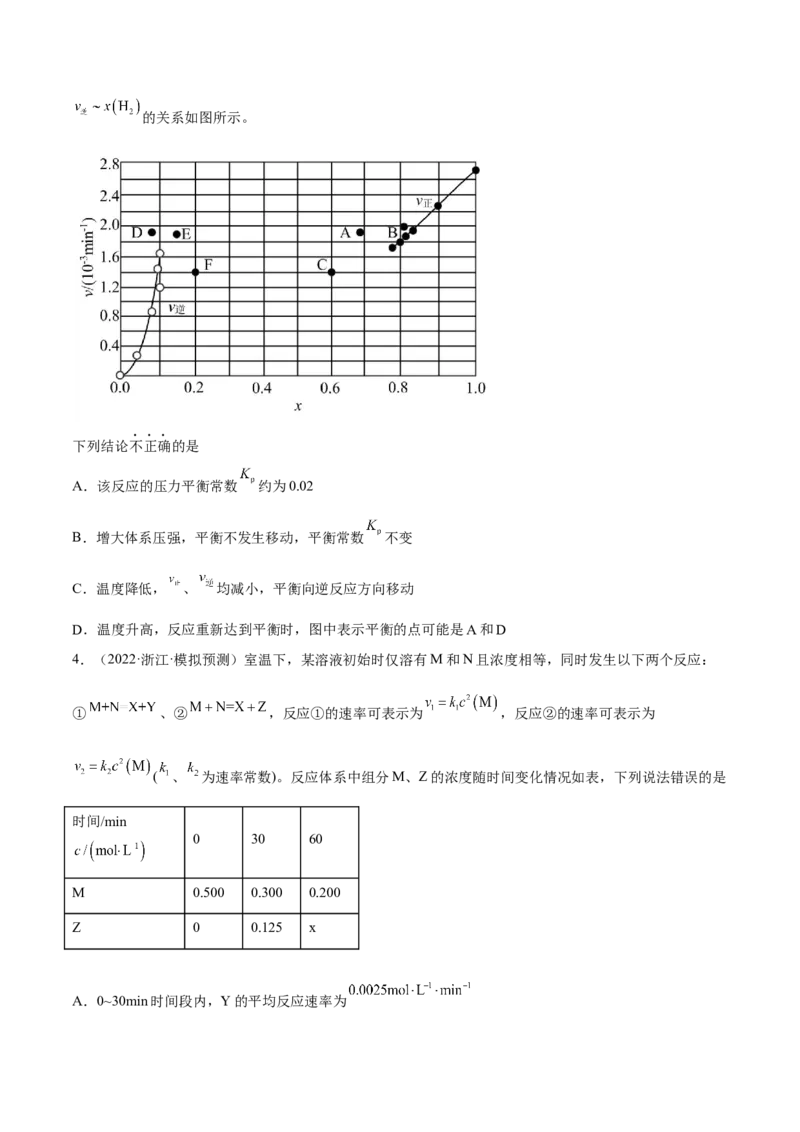
3.(2023·河南郑州·统考一模)已知反应 ,在716K时向密闭容器中
充入一定量的HI气体,平衡时气体混合物中碘化氢的物质的量分数 为78%。测得 和的关系如图所示。
下列结论不正确的是
A.该反应的压力平衡常数 约为0.02
B.增大体系压强,平衡不发生移动,平衡常数 不变
C.温度降低, 、 均减小,平衡向逆反应方向移动
D.温度升高,反应重新达到平衡时,图中表示平衡的点可能是A和D
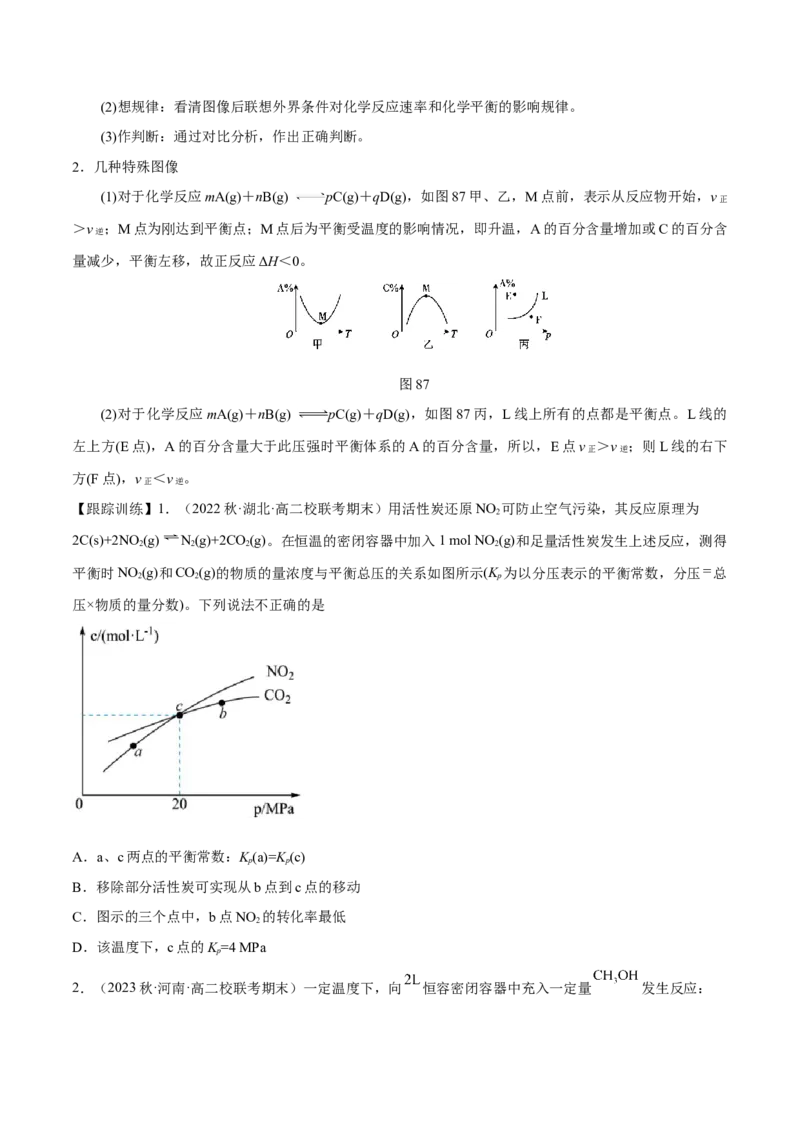
4.(2022·浙江·模拟预测)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:
① 、② ,反应①的速率可表示为 ,反应②的速率可表示为
( 、 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如表,下列说法错误的是
时间/min
0 30 60
M 0.500 0.300 0.200
Z 0 0.125 x
A.0~30min时间段内,Y的平均反应速率为B.反应开始后,体系中Y和Z的浓度之比保持不变,为3∶8
C.分析计算可得
D.反应①的活化能比反应②的活化能大
考点二 化学平衡及其影响因素
1.判断反应达到平衡状态的方法
(1)等——“逆向相等”:反应速率必须一个是正反应的速率,一个是逆反应的速率,且经过换算后同一种
物质的减少速率和生成速率相等。
(2)定——“变量不变”:如果一个量是随反应进行而改变的(即变量),当其“不变”时反应就达到平衡状
态;一个随反应的进行保持不变的量(即恒量),不能作为判断反应是否达到平衡状态的依据。
(3)依Q 与K关系判断:若Q=K,反应处于平衡状态。
c c
2.平衡移动方向的判断
(1)依勒夏特列原理判断。
(2)根据图像中正逆反应速率相对大小判断:若v >v ,则平衡向正反应方向移动;反之向逆反应方向移动。
正 逆
(3)依变化过程中速率变化的性质判断:若平衡移动过程中,正反应速率增大(减小),则平衡向逆(正)反应
方向移动。
(4)依浓度商(Q)规则判断:若某温度下Q<K,反应向正反应方向进行;Q>K,反应向逆反应方向进行。
c c c
【跟踪训练】1.(2022·上海·统考一模)某温度下,向密闭容器中充入等物质的量的 和
,发生反应 。达到平衡后,下列说法正确的是
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒温下,移走一定量的 , 变大, 变小
D.恒容下,充入一定量的 ,平衡时 的体积分数一定降低
2.(2022·上海·统考一模)一定温度下,某密闭容器中可逆反应 达到平衡,下列操作能使变小的是
A.恒压充入 B.恒容充入 C.恒容充入 D.恒容充入
3.(2022·辽宁沈阳·辽宁实验中学校考模拟预测)NH、NO 常用作火箭发射的推进剂。推进剂发生反应:
2 4 2 4
。下列有关说法错误的是
A.反应每生成0.3 mol N,转移电子的数目为
2
B.充有NO 的密闭容器中存在: ,增大容器体积,平衡正向移动,容器内气体颜
2 4
色变浅
C.碱性NH-空气燃料电池工作时,正极电极反应式为O+4e-+2H O=4OH-
2 4 2 2
D.NH 的电子式为
2 4
4.(2022·浙江温州·统考模拟预测)T℃,反应 ,在密闭容器中达到平衡
时的体积为100mL。已知密度:CaO(s): 、 : 。下列有关说法正确的是
A.恒温、恒容,体系中再加入56g ,平衡不移动
B.恒温、恒压,体系中再加入100g ,平衡不移动
C.恒温,压缩容器体积,平衡后,反应速率加快
D.恒温、恒压,体系中通入一定量 ,平衡正向移动,建立新的平衡状态
5.(2022·上海宝山·上海市行知中学校考模拟预测)往某恒温密闭容器中加入 ,发生反应:
,反应达到平衡后, 时缩小容器体积,x随时间(t)变化的关系如图所示。
x不可能是A. B. C. D.ρ(容器内气体密度)
考点三 化学反应速率及化学平衡的计算
1.化学平衡常数
(1)意义:化学平衡常数K表示反应进行的程度,K越大,反应进行的程度越大。K>105时,可以认为
该反应已经进行完全。K的大小只与温度有关。
(2)化学平衡常数表达式:对于可逆化学反应 mA(g)+nB(g) pC(g)+qD(g)在一定温度下达到化学
平衡时,K=。另可用压强平衡常数表示:
K =[p(C)为平衡时气体C的分压]
p
(3)依据化学方程式计算平衡常数
①同一可逆反应中,K ·K =1;
正 逆
②同一方程式中的化学计量数等倍扩大或缩小n倍,则新平衡常数K′与原平衡常K间的关系是:K′=
Kn或K′=。
③几个可逆反应方程式相加,得总方程式,则总反应的平衡常数等于分步反应平衡常数之积。
2.转化率、产率及分压的计算
反应物转化率=×100%
产物的产率=×100%
分压=总压×物质的量分数
【跟踪训练】1.(2022·四川成都·成都七中校考模拟预测) (s)与CO(g)主要发生如下反应。
①
②
反应的还原产物与温度密切相关。其他条件一定, (s)和CO(g)反应达平衡时,CO(g)的体积分数随温度的变化关系如图所示。下列说法不正确的是
A.反应 的焓变为
B.根据图象推测, 应当小于0
C.反应温度越高, 主要还原产物中铁元素的价态越低
D.温度高于1040℃时, (s)和CO(g)发生的主要反应的化学平衡常数
2.(2022·河南洛阳·校联考模拟预测)某温度下,在3L的恒容密闭容器中,仅充入1molX(g)和
2molY(g),发生反应:X(g)+mY(g) 3Z(g) H<0,当反应达到平衡时,测得X、Y、Z的体积分数分
△
别为30%、60%和10%。下列说法正确的是
A.反应起始的总压强与反应达到平衡时的总压强之比为2:3
B.该反应达到平衡后,若再充入0.3molX和0.3molZ,则此时的反应速率:v >v
正 逆
C.该反应从起始至达到平衡的过程中,总是存在c(X)+c)Y)+c(Z)=1mol·L-1
D.反应达到平衡后,若仅升高温度,则该反应的平衡常数增大
3.(2022·上海普陀·统考二模)某温度下,在①、②两个恒容密闭容器中发生反应:H(g)+
2
CO(g) HO(g)+CO(g),K=2.25。物质的起始浓度如下表:
2 2
⇌ 起始浓度(mol·L-1)
容器编号
H CO HO CO
2 2 2
① 0.1 0.1 0 0
② 0.2 0.1 0.2 0.1下列说法正确的是
A.反应开始,②中反应逆向进行 B.平衡时,①中c(CO)=0.04mol·L-1
2
C.①、②均达平衡时,各组分浓度相同 D.①中H 的平衡转化率为40%
2
4.(2022·重庆九龙坡·重庆市育才中学校考模拟预测)25℃时,恒容密闭容器中只含有X,发生反应:
,X的起始压强为 ,X分解的速率方程为: ,其中k定温下为常数。
生成的Y可快速建立平衡: ,平衡常数 。下列说法正确的是
A.当X分解的速率 时,W的压强为
B.若升高温度,Z和W的物质的量之比为 ,则
C.相同时间内,X的平均速率是Y的平均速率的2倍
D.若缩小体积,则单位时间内X的转化率减小
5.(2022·湖南长沙·长沙市明德中学校考二模)常压下羰基化法精炼镍的原理为:
。230℃时,该反应的平衡常数 。已知: 的沸点为
42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与 反应转化成气态 ;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A.升高温度,该反应的平衡常数减小
B.该反应达到平衡时,
C.第一阶段,在30℃和50℃两者之间选择反应温度,选30℃
D.第二阶段, 分解率较低
考点四 化学反应速率及化学平衡的图像问题探讨
1.化学反应速率、化学平衡图像题的解题思路
(1)看图像:一看轴(即纵坐标与横坐标的意义),二看点(即起点、拐点、交点、终点),三看线(即线的
走向和变化趋势),四看辅助线(如等温线、等压线、平衡线等),五看量的变化(如浓度变化、温度变化等)。(2)想规律:看清图像后联想外界条件对化学反应速率和化学平衡的影响规律。
(3)作判断:通过对比分析,作出正确判断。
2.几种特殊图像
(1)对于化学反应mA(g)+nB(g) pC(g)+qD(g),如图87甲、乙,M点前,表示从反应物开始,v
正
>v ;M点为刚达到平衡点;M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含
逆
量减少,平衡左移,故正反应ΔH<0。
图87
(2)对于化学反应mA(g)+nB(g) pC(g)+qD(g),如图87丙,L线上所有的点都是平衡点。L线的
左上方(E点),A的百分含量大于此压强时平衡体系的A的百分含量,所以,E点v >v ;则L线的右下
正 逆
方(F点),v <v 。
正 逆
【跟踪训练】1.(2022秋·湖北·高二校联考期末)用活性炭还原NO 可防止空气污染,其反应原理为
2
2C(s)+2NO (g) N(g)+2CO (g)。在恒温的密闭容器中加入1 mol NO (g)和足量活性炭发生上述反应,测得
2 2 2 2
平衡时NO (g)和CO(g)的物质的量浓度与平衡总压的关系如图所示(K 为以分压表示的平衡常数,分压 总
2 2 p
压×物质的量分数)。下列说法不正确的是
A.a、c两点的平衡常数:K (a)=K (c)
p p
B.移除部分活性炭可实现从b点到c点的移动
C.图示的三个点中,b点NO 的转化率最低
2
D.该温度下,c点的K =4 MPa
p
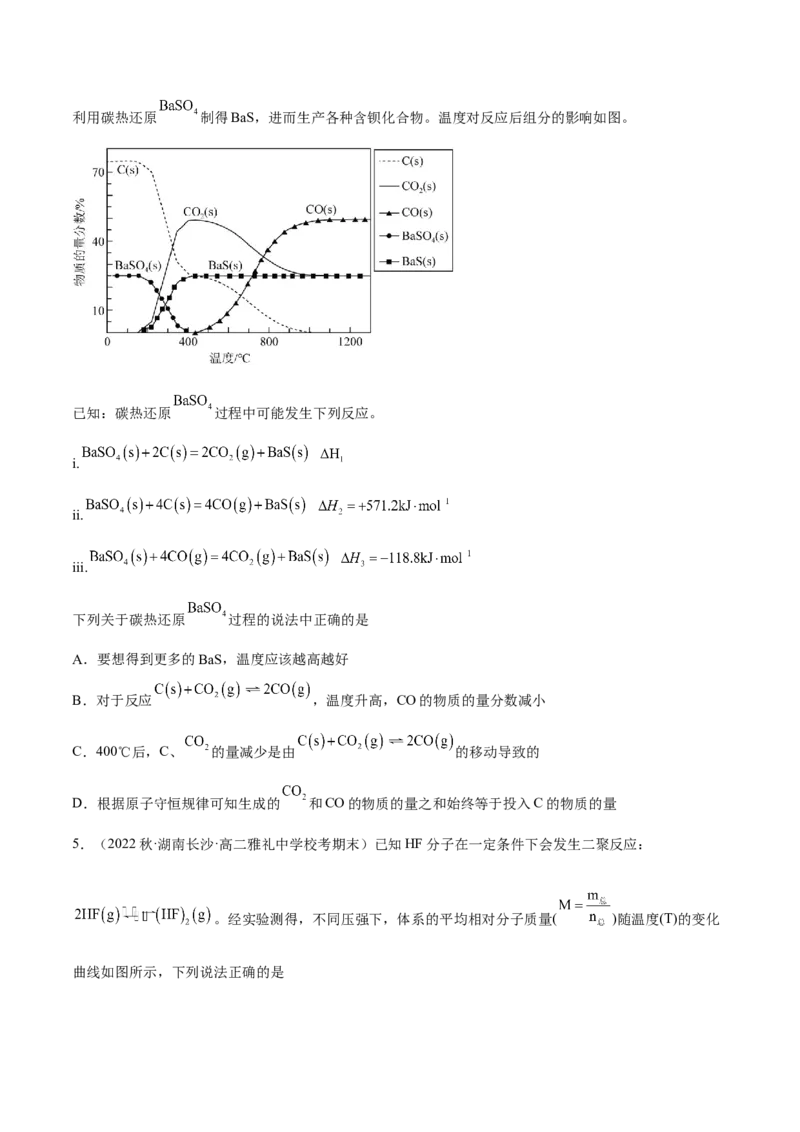
2.(2023秋·河南·高二校联考期末)一定温度下,向 恒容密闭容器中充入一定量 发生反应:,测得 的物质的量与温度、时间的关系如图所示:
下列叙述正确的是
A.该反应的
B. 时 温度下的正反应速率相等
C. 温度下, 内的反应速率
D. 温度下反应达到平衡后,再向容器中充入少量甲醇气体, 的平衡转化率不变
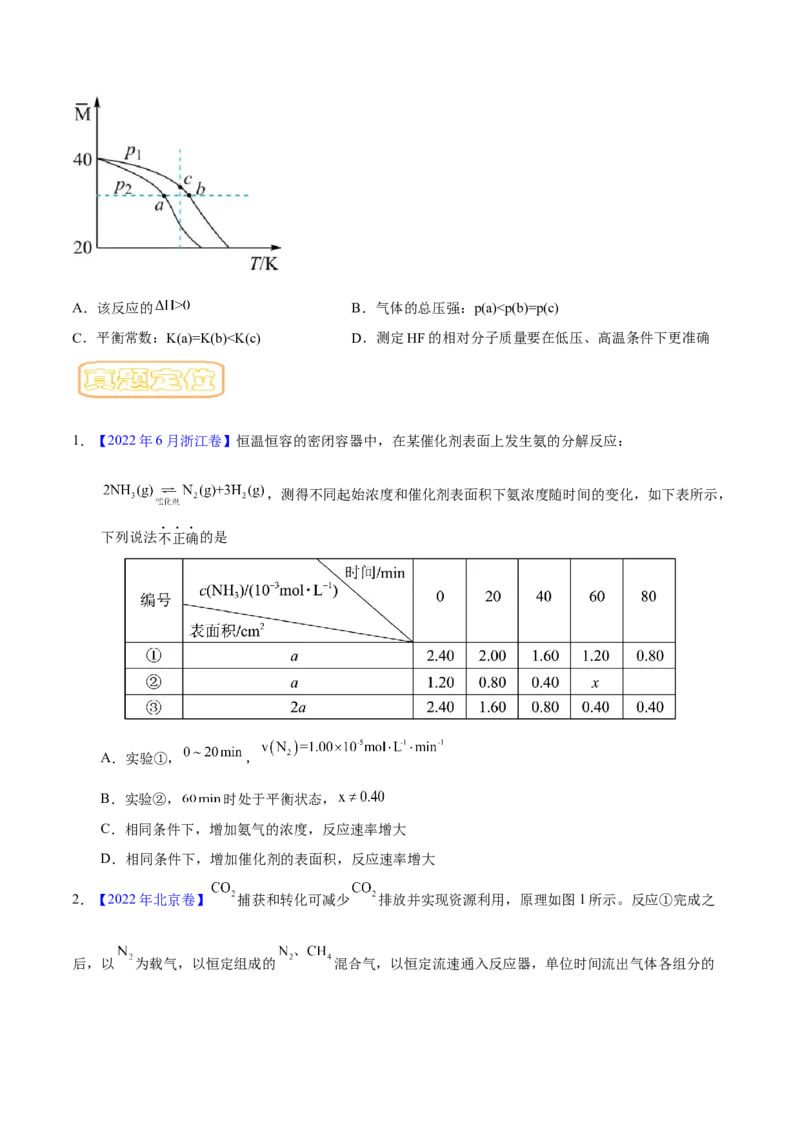
3.(2023春·河南洛阳·高三孟津县第一高级中学校考开学考试)工业生产硫酸的一步重要反应是
,如果该反应在容积不变的密闭容器中进行,下列各图表示当其他条件不
变时,改变某一条件对上述反应的影响,其中结论正确的是
A.图I表示催化剂对化学平衡的影响,且甲使用了催化剂
B.图II表示 平衡转化率与温度及压强的关系,可以判断
C.图III表示 时刻升高温度或增大压强对反应速率的影响
D.图IV中 三点体系对应的温度:
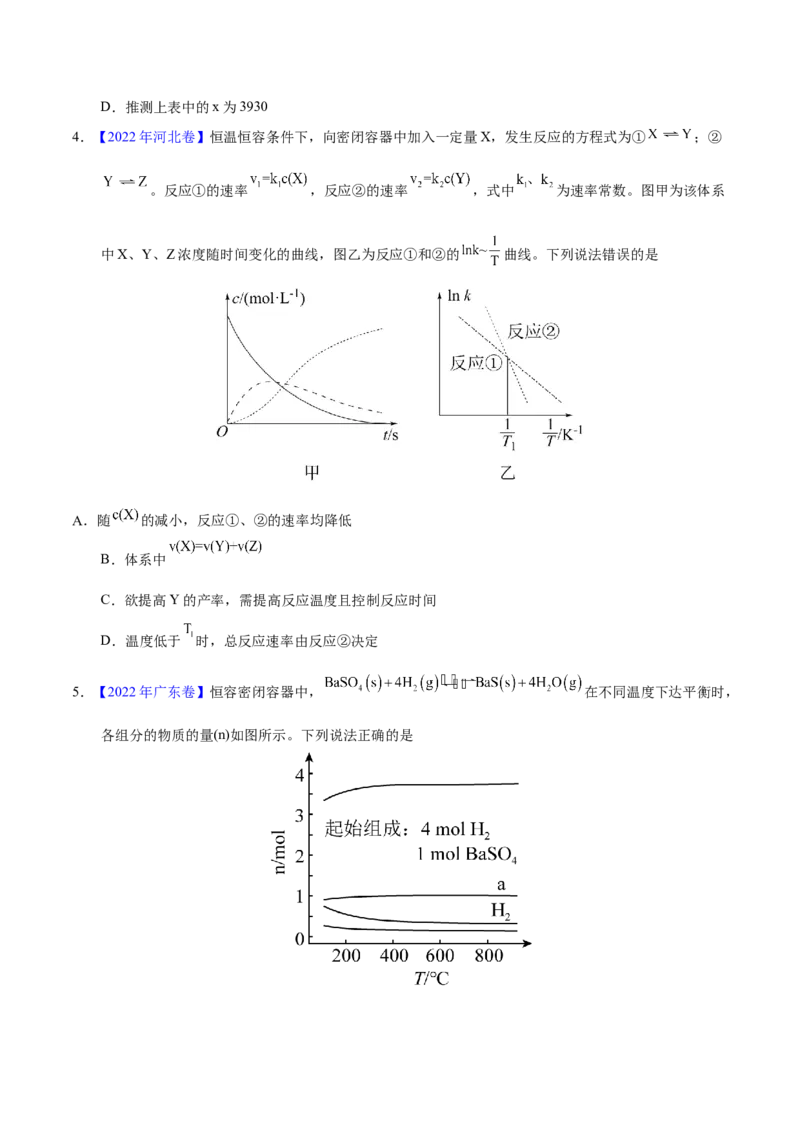
4.(广东省新高考普通高中学科综合素养评价2022-2023学年高三下学期开学调研考试化学试题)工业上利用碳热还原 制得BaS,进而生产各种含钡化合物。温度对反应后组分的影响如图。
已知:碳热还原 过程中可能发生下列反应。
i.
ii.
iii.
下列关于碳热还原 过程的说法中正确的是
A.要想得到更多的BaS,温度应该越高越好
B.对于反应 ,温度升高,CO的物质的量分数减小
C.400℃后,C、 的量减少是由 的移动导致的
D.根据原子守恒规律可知生成的 和CO的物质的量之和始终等于投入C的物质的量
5.(2022秋·湖南长沙·高二雅礼中学校考期末)已知HF分子在一定条件下会发生二聚反应:
。经实验测得,不同压强下,体系的平均相对分子质量( )随温度(T)的变化
曲线如图所示,下列说法正确的是A.该反应的 B.气体的总压强:p(a)乙>甲=丁 B.该温度下平衡常数K=400
C. 的平衡转化率: D.容器中 的物质的量浓度:丙=丁<甲
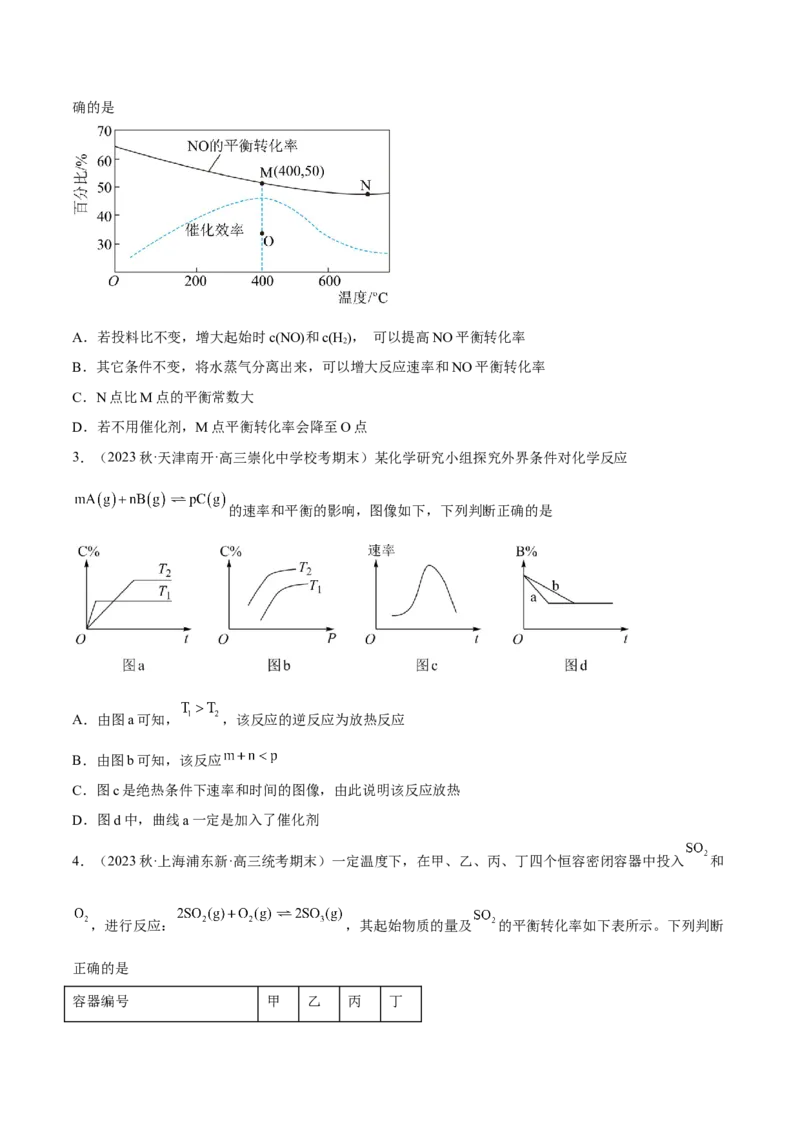
5.(2022秋·北京石景山·高三统考期末)甲烷催化氧化为合成气的主反应为:
。 转化率、 选择性 和 选择性
随温度变化如图所示。下列说法不正确的是
A. 时,副反应① 进行程度很小
B.对比图中 和 的选择性,推测可能存在副反应②
C. 转化率随温度升高而增大,可以用勒夏特列原理解释
D.增大压强使容器容积减小,可使单位体积内活化分子数增多,化学反应速率增大
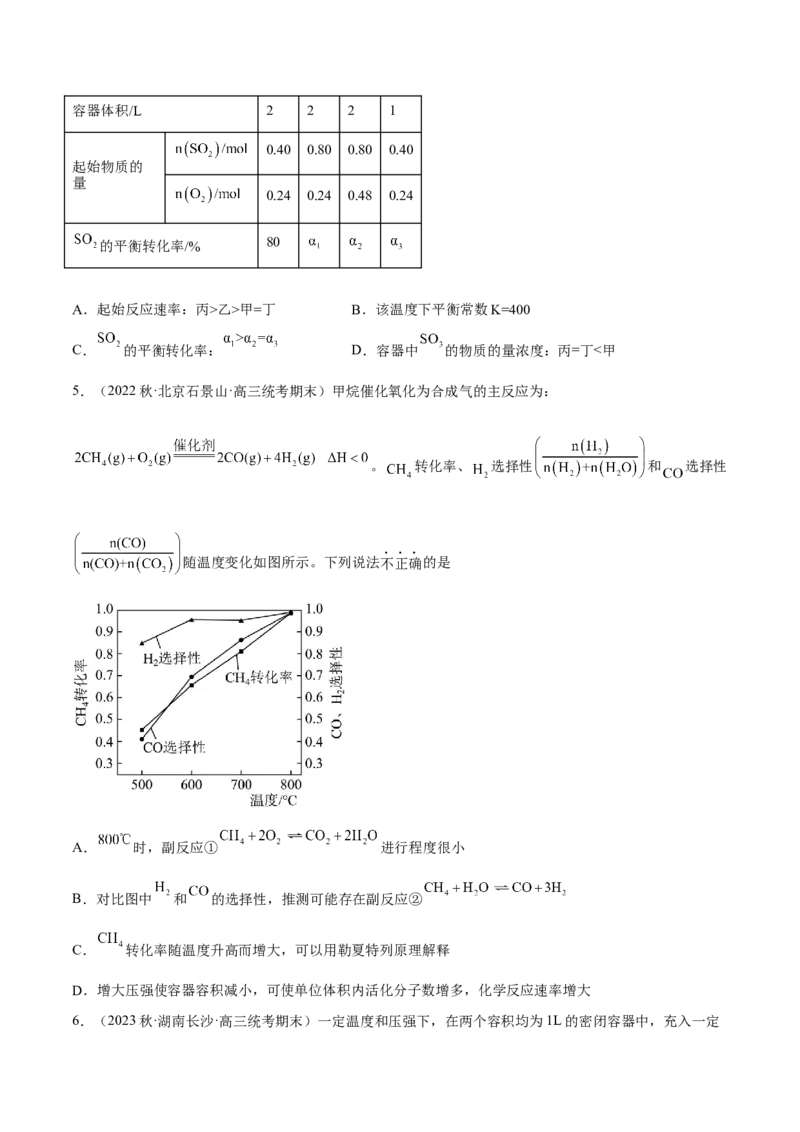
6.(2023秋·湖南长沙·高三统考期末)一定温度和压强下,在两个容积均为1L的密闭容器中,充入一定量的A和B,发生反应: 。相关反应数据如下表所示(已知在 、 下,A、B、
C、D都是气态)
容器编
压强 温度 起始物质的量/mol 10s时物质的量/mol
号
A B C
Ⅰ 0.2 0.2 0.05
Ⅱ 0.2 0.2 0.05
Ⅲ 0.2 0.2 0.05
下列说法正确的是A.该反应的
B.在容器Ⅲ中,A、B中至少有一种呈非气态
C.10s时,容器Ⅱ中的反应一定处于平衡状态
D.若起始时,向容器II中充入 、 、 和 ,反应将向正反应方向进行
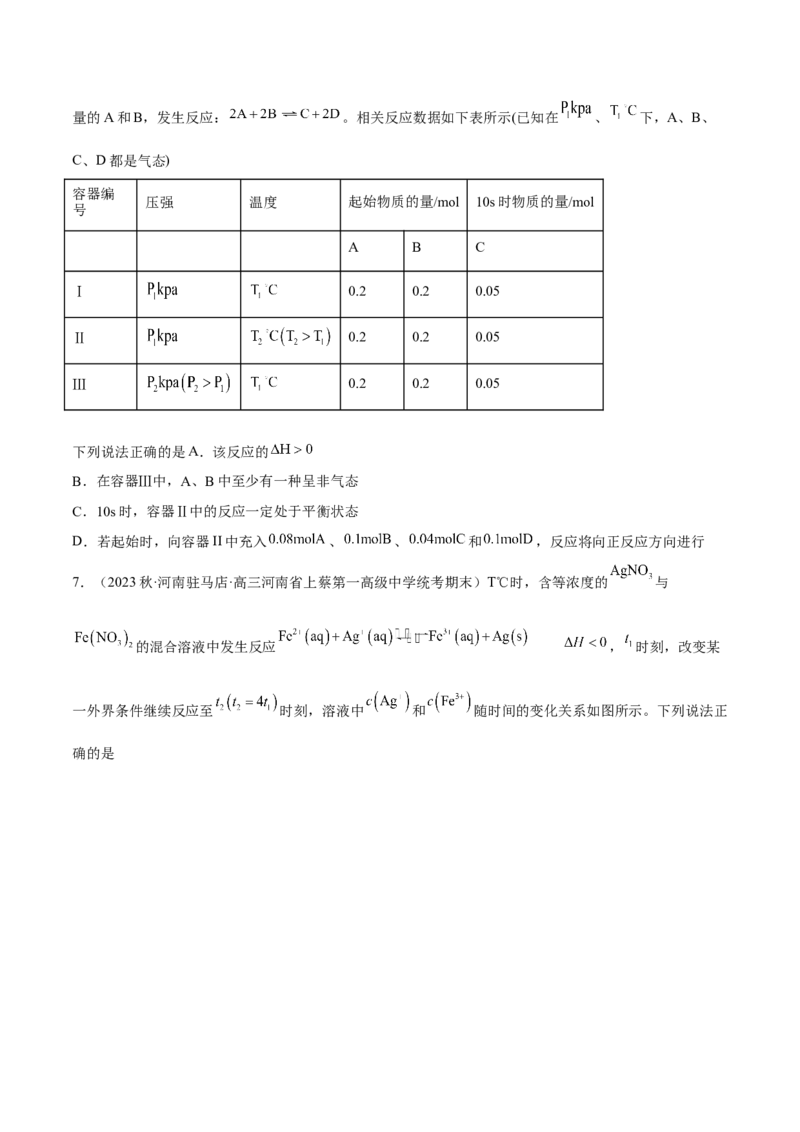
7.(2023秋·河南驻马店·高三河南省上蔡第一高级中学统考期末)T℃时,含等浓度的 与
的混合溶液中发生反应 , 时刻,改变某
一外界条件继续反应至 时刻,溶液中 和 随时间的变化关系如图所示。下列说法正
确的是已知:T℃时,该反应的化学平衡常数K=1。
A.若 时刻未改变外界条件,则此时该反应处于平衡状态
B.若 时刻反应达到平衡,则 时刻改变的条件可能为升温
C.若始终保持温度不变,则平均反应速率: ( 表示0~ s内 的平均反应速率, 表示0~ s
内 的平均反应速率)
D. 内 的平均反应速率为