文档内容
专题讲座(一) 化学计算的常用方法
目录
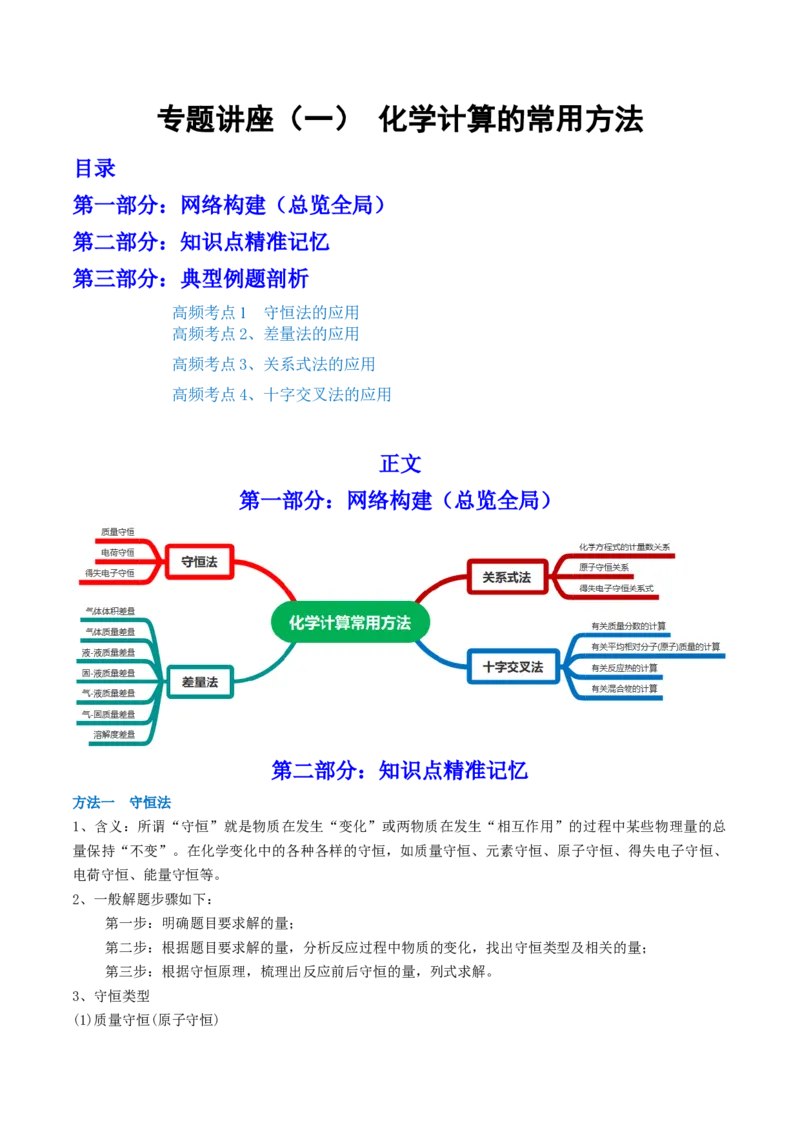
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 守恒法的应用
高频考点2、差量法的应用
高频考点3、关系式法的应用
高频考点4、十字交叉法的应用
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
方法一 守恒法
1、含义:所谓“守恒”就是物质在发生“变化”或两物质在发生“相互作用”的过程中某些物理量的总
量保持“不变”。在化学变化中的各种各样的守恒,如质量守恒、元素守恒、原子守恒、得失电子守恒、
电荷守恒、能量守恒等。
2、一般解题步骤如下:
第一步:明确题目要求解的量;
第二步:根据题目要求解的量,分析反应过程中物质的变化,找出守恒类型及相关的量;
第三步:根据守恒原理,梳理出反应前后守恒的量,列式求解。
3、守恒类型
(1)质量守恒(原子守恒)依据化学反应的实质是原子的重新组合,因而反应前后原子的总数和质量保持不变。质量守恒法解题时可
利用①整体守恒:即反应中反应物的总质量与生成物的总质量守恒;②局部守恒:即反应中反应物与产物
中某元素的原子或离子守恒或元素守恒。
(2)电荷守恒
依据电解质溶液呈电中性,即阳离子所带正电荷总数等于阴离子所带负电荷总数或离子方程式前后离子所
带电荷总数不变。利用电荷守恒法可以①配平离子方程式;②巧解某些化学计算题。
(3)得失电子守恒关系式
依据氧化还原反应中电子得失数目相等,即氧化剂得到的电子总数目等于还原剂失去的电子总数目。利用
得失电子守恒法可以①计算元素的化合价;②计算氧化(或还原)产物的量;③计算氧化剂、还原剂的消
耗量;④计算混合物的组成。
方法二 差量法
1、含义:差量法是指根据化学反应前后有关物理量发生的变化,找出“理论差量”。这种物
理量可以是质量、物质的量、气态物质的体积和压强、反应过程中的热量等。用差量法解题
时先把化学方程式中的对应差量(理论差量)跟实际差量列成比例,然后求解。
2、一般解题步骤如下:
第一步:准确写出有关反应的化学方程式;
第二步:深入细致地分析题意,关键在于有针对性地找出产生差量的“对象”及“理论差量”。该
“理论差量”可以是质量、物质的量、气体体积、压强等,且该差量的大小与参加反应的物质的有关量成
正比;
第三步:根据反应方程式,从“实际差量”寻找比例关系,列比例式求解。
3、差量类型
(1)气体体积差量
(2)气体质量差量
(3)液-液质量差量
(4)固-液质量差量
(5)气-液质量差量
(6)气-固质量差量
(7)溶解度差量
注意事项①x、y可表示物质的质量、物质的量、气体体积等,因而差量可指质量之差(△m)物质的量之差
(△n)或气体体积之差( V)等。
△
②分清“差量”是增还是减.在较复杂的情况,存在多个反应,可能差量的增减方向并不一致,这就要取其代
数和.若方向相同,则总差量等于各个分差量之和。
③正确分析形成差量的原因,找出对应的根据方程式得出的“理论差量”是差量法解题的关键。
方法三 关系式法
1、含义:关系式法是一种巧妙利用已知量与未知量之间关系进行解题的一种方法,一般适用于多步进行
的连续反应,因前一个反应的产物是后一个反应的反应物,可以根据中间物质的传递关系,找出原料和最
终产物的相应关系式。它是化学计算中的基本解题方法之一,利用关系式法可以将多步计算转化为一步计算,免去逐步计算中的麻烦,简化解题步骤,减少运算量,且计算结果不易出错,准确率高。
2、关系式建立的类型
(1)有关化学方程式的计量数关系式:在化学反应中,任何一种元素的总质量是守恒的,即最初反应物
中该元素的质量等于最终产物中该元素的质量。
(2)原子守恒关系式:各步反应的化学方程式,找出最初反应物与最终生成物的物质的量的关系式,再
进行一步计算。
(3)得失电子守恒关系式:根据氧化剂和还原剂得失守恒建立关系式,再进行一步计算。
3、一般解题步骤如下:
法1:
第一步:准确写出各步反应的化学方程式;
第二步:找出“中介”的物质,并确定最初反应物、中介物质、最终生成物之间量的关系;
第三步:确定最初反应物和最终生成物之间量的关系;
第四步:根据已知条件及关系式列出比例式计算求解。
法2:利用电子守恒或原子守恒直接确定关系式,然后列比例进行求算。
方法四 十字交叉法
1、含义:十字交叉法是解二元一次方程式的图解形式,应用于解二元混合体系且与平均值有关的计算问
题。它是一种具有简化解题思路、运算简便、计算速度快、计算不易出差错等优点的解题方法。其原理如
下:若 a、b(a > b)分别表示某二元组分中两种组分的量,c 表示 a、b 两组分的相对平均值,x、y
分别表示 a、b 在混合体系中所占的比例,则有二元一次方程组:
x+y=1 ①
ax+by=c ②
把②式除以①式并移项整理得:x/y=(c-b)/(a-c),由此可得到如下图式: 。
2、一般解题步骤如下:
第一步:确定交叉点上的物质物理量的平均数;
第二步:写出合成物质物理量的平均数的两个分量;
第三步:按斜线作差取绝对值,得出相应物质物理量的配比关系。
3、十字交叉法常用于求算类型:
(1)有关质量分数的计算;
(2)有关平均相对分子(原子)质量的计算;
(3)有关反应热的计算;
(4)有关混合物反应的计算。特别注意:
(1)确定好平均数和合成这个平均数的两个分量,在确定这些数量的过程中要遵照统一的基准。
(2)此方法所得比值是基准中产生两个分量的物质之间的配比,而不是各分量所示物质之间配比,其物理
量与基准中的物理量相同,即与中间值平均数单位中分母单位对应的物理量,如平均值单位为g/mol,单
位的分母为mol,对应的物理量为物质的量,则其配比为物质的量之比。
第三部分:典型例题剖析
高频考点1 守恒法的应用
例1、在空气中加热Co(OH) ,使其转化为钴的氧化物。加热过程中,固体质量与温度的关系如图所示。
2
290~500 ℃,发生反应的化学方程式为________________________________。
【解析】n[Co(OH)]==0.01 mol,根据钴原子守恒,m(Co)=0.590 g,290 ℃时,n(O)= mol=0.015
2
mol,故290 ℃时氧化物为CoO,根据钴原子守恒,500 ℃时n(O)=mol=0.013 3 mol,故500 ℃时氧化
2 3
物为CoO。
3 4
化学方程式为6CoO============4CoO+O↑。
2 3 3 4 2
【答案】6CoO============4CoO+O↑
2 3 3 4 2
【题后归纳】失重分析的一般规律
(1)失重一般先失去部分水或全部水,再失去非金属化物。
(2)晶体中金属质量不减少,仍在残留固体中。
(3)失重最后一般为金属氧化物,由质量守恒得m(O),由n(金属)∶n(O),即可求出失重后物质的化学式。
(4)根据金属原子守恒,可找出起始物与残留物之间关系。
【变式训练1】(原子守恒)有14 g NaO 、NaO、NaOH的混合物与100 g质量分数为15%的盐酸恰好反应,
2 2 2
蒸干溶液,最终得固体质量为( )
A.20.40 g B.28.60 g C.24.04 g D.无法计算
【解析】混合物与盐酸反应后所得溶液为氯化钠溶液,蒸干后得到 NaCl,由Cl-质量守恒关系可得100
g×15%×=m(NaCl)×,解得m(NaCl)≈24.04 g。
【答案】C
【变式训练2】(电荷守恒)把500 mL含有BaCl 和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠
2
的溶液,恰好使Ba2+完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使Cl-完全沉淀,该混合溶液
中K+浓度为( )
A.10(b-2a)mol·L-1 B.5(b-2a)mol·L-1
C.2(b-a)mol·L-1 D.10(2a-b)mol·L-1
【解析】混合溶液分成5等份,每份溶液浓度相同。根据Ba2++SO===BaSO↓可知,每份溶液中n(Ba2+)=
4n(NaSO)=a mol;根据Ag++Cl-===AgCl↓可知,每份溶液中n(Cl-)=n(Ag+)=b mol,根据电荷守恒可
2 4
知,每一份溶液中2n(Ba2+)+n(K+)=n(Cl-),则n(K+)=b mol-2a mol=(b-2a)mol,故c(K+)==
10(b-2a)mol·L-1。
【答案】A
【变式训练3】(电子守恒)某强氧化剂XO(OH)可被NaSO 还原。如果还原1.2×10-3 mol XO(OH)需用30
2 3
mL 0.1 mol·L-1的NaSO 溶液,那么X元素被还原后的物质可能是( )
2 3
A.XO B.XO
2 3
C.XO D.X
2
【解析】由题意知,S元素由+4价→+6价,假设反应后X的化合价为+x价,根据氧化还原反应中得失
电子数目相等可得,1.2×10-3 mol×(5-x)=0.03 L×0.1 mol·L-1×(6-4),解得x=0,所以X元素被
还原后的物质是X,D项正确。
【答案】D
高频考点2、差量法的应用
例2、为了检验某含有NaHCO 杂质的NaCO 样品的纯度,现将w g样品加热,其质量变为w g,则该样品
3 2 3 1 2
的纯度(质量分数)是( )
A. B.
C. D.
【解析】由题意知(w-w)g应为NaHCO 分解生成的CO 和HO的质量,设样品中NaHCO 质量为x g,由此
1 2 3 2 2 3
可得如下关系:
2NaHCO NaCO+CO ↑+ HO
3 2 3 2 2
2×84 62
x w-w
1 2
则x=,
故样品纯度为==。
【答案】A
【名师点睛】利用差量法进行方程式计算要注意前后固体质量的变化,并能列出方程组计算。减小的质量
=生成的二氧化碳和水的质量,求出 ,再利用关系式法求解。
【变式训练1】(质量差)将12 g CO和CO 的混合气体通过足量灼热的氧化铜后,得到气体的总质量为 18
2
g,则原混合气体中CO的质量分数为________。
【解析】设原混合气体中CO的质量分数为x。
CuO+CO Cu+CO 气体质量增加(差量)
2
28 g 44 g 44 g-28 g=16 g
12x g 18 g-12 g=6 g
=,解得x=87.5%。
【答案】87.5%
【变式训练2】(双选)(气体体积差)16 mL由NO与NH 组成的混合气体在催化剂作用下于400 ℃左右可发
3
生反应:6NO+4NH 5N +6HO(g),达到平衡时在相同条件下气体体积变为17.5 mL,则原混合气体中
3 2 2NO与NH 的物质的量之比可能为( )
3
A.5∶3 B.3∶2 C.4∶3 D.9∶7
【解析】根据反应前后气体体积的变化,可用差量法直接求解。
6NO+4NH 5N+6HO(g) ΔV(气体的体积差)
3 2 2
6 mL 4 mL 5 mL 6 mL 1 mL(理论差量)
9 mL 6 mL 17.5 mL-16 mL=1.5 mL(实际差量)
由此可知共消耗 15 mL NO与NH 的混合气体,还剩余 1 mL气体,假设剩余的气体全部是 NO,则
3
V(NO)∶V(NH)=(9 mL+1 mL)∶6 mL=5∶3;假设剩余的气体全部是NH ,则V(NO)∶V(NH)=9 mL∶(6
3 3 3
mL+1 mL)=9∶7,但因该反应是可逆反应,剩余气体实际上是NO、NH 的混合气体,故V(NO)∶V(NH)介
3 3
于9∶7与5∶3 之间,对照所给的数据知3∶2与4∶3在此区间内。
【答案】BC
【变式训练 3】(热量差量)高炉炼铁中发生的基本反应之一为:FeO(s)+CO(g) Fe(s)+CO(g)
2
△H=-11kJ/mol,将一定量的FeO和50molCO置于高内,测得反应放出热量110kJ,则此时CO 和CO的体积比
2
为
A.1:10 B.1:4 C.4:1 D.10:1
【解析】化学反方程式可知:
Feo(s)+CO(g)=Fe(s)+ CO(g)△H=-11.0kJ/mol
2
1mol 1mol 11 kJ
开始 50mol 0
消耗 10mol 生成10mo1 110kJ
解得n(CO):n(CO)=10:40=1:4
2
【答案】B。
【变式训练4】(物质的量差量)白色固体PCl 受热即挥发并发生分解:PCl(g) PCl(g)+Cl(g)。现
5 5 3 2
将5.84 g PCl 装入2.05 L真空密闭容器中,在277 ℃达到平衡,容器内压强为1.01×105Pa,经计算可
5
知平衡时容器内混合气体的物质的量为0.05 mol,求平衡时PCl 的分解率__________。
5
【解析】计算PCl 的起始物质的量,利用差量法计算参加反应的PCl 的物质的量,进而计算平衡时PCl 的
5 5 5
分解率。
5.84gPCl 的物质的量为 =0.028mol,设参加反应PCl 的物质的量为x,则:
5 5
PCl(g) PCl(g)+Cl(g) 物质的量增大
5 3 2
1 1
X 0.05mol-0.028mol=0.022mol故x=0.022mol,则平衡时PCl 的分解率 ,故答案为:平衡时PCl 的分解率为
5 5
78.6%。
【答案】78.6%。
高频考点3、关系式法的应用
例3、(2019·全国卷Ⅰ,节选)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150
℃时失掉1.5个结晶水,失重 5.6%。硫酸铁铵晶体的化学式为______________。
【解析】关系式:NHFe(SO)·xHO ~ 1.5HO
4 4 2 2 2
266+18x 1.5×18
故=5.6%,x≈12。
【答案】NHFe(SO)·12HO
4 4 2 2
【名师点睛】本题的易错点是要注意硫酸铁铵晶体加热失去1.5个结晶水,并不是全部结晶水。解题的难
点是硫酸铁铵晶体化学式的确定需要准确运用失重率的计算公式,即 ,
同时还应该明确失去结晶水的过程,知道硫酸铁铵失去的重量就是水的重量。
【变式训练1】(根据原子守恒找关系式)在氧气中燃烧0.22 g硫和铁组成的混合物,使其中的硫全部转
化为二氧化硫,把这些二氧化硫全部氧化成三氧化硫并转变为硫酸,这些硫酸可用10 mL 0.5 mol·L-1氢氧
化钠溶液完全中和,则原混合物中硫的百分含量为( )
A.72% B.40% C.36% D.18%
【解析】由S原子守恒和有关反应可得出:
S~HSO~2NaOH
2 4
32 g 2 mol
m(S) 0.5×10×10-3 mol
得m(S)=0.08 g
原混合物中w(S)=×100%=36%。
【答案】C
【变式训练2】(根据电子守恒找关系式)将1.08 g FeO完全溶解在100 mL 1.00 mol·L-1硫酸中,然后加
入25.00 mL K Cr O 溶 液,恰好使Fe2+全部转化为Fe3+,且Cr O中的铬全部转化为Cr3+。则KCr O 的物
2 2 7 2 2 2 7
质的量浓度是________。
【解析】由电子守恒知,FeO中+2价铁所失电子的物质的量与Cr O中+6价铬所得电子的物质的量相等,
2
×(3-2)=0.025 00 L×c(Cr O)×(6-3)×2,得c(Cr O)=0.100 mol·L-1。
2 2
【答案】0.100 mol·L-1
【变式训练3】(根据相关反应找关系式)金属锡的纯度可以通过下述方法分析:将试样溶于盐酸,反应
的化学方程式为 Sn+2HCl===SnCl +H↑,再加入过量的 FeCl 溶液,发生如下反应:SnCl +
2 2 3 22FeCl ===SnCl +2FeCl ,最后用已知浓度的KCr O 溶液滴定生成的Fe2+,反应的化学方程式为6FeCl +
3 4 2 2 2 7 2
KCr O +14HCl===6FeCl +2KCl+2CrCl +7HO。现有金属锡试样0.613 g,经上述反应后,共用去0.100
2 2 7 3 3 2
mol·L-1 KCr O 溶液16.0 mL。求试样中锡的百分含量(假定杂质不参加反应,锡的相对原子质量为119)。
2 2 7
【解析】Sn与KCr O 物质的量的关系:
2 2 7
3Sn~3SnCl ~6FeCl ~KCr O
2 2 2 2 7
3×119 g 1 mol
x 0.100×0.016 mol
x==0.571 2 g
w(Sn)=×100%≈93.2%。
【答案】93.2%。
高频考点4、十字交叉法的应用
例4、已知下列两个热化学方程式
2H(g)+O(g)=2HO(l)+571.6KJ
2 2 2
C H(g)+5O(g)=3CO(g)+4HO(l)+2220.0KJ.
3 8 2 2 2
实验测得 H 、C H 混合气体共 5mol完全燃烧时放热 3847KJ,则原混合气体中 H 、C H 的体积比是
2 3 8 2 3 8
( )
A.1:3 B.3:1 C.1:4 D.1:1
【解析】是求出每摩 H、C H 完全燃烧时放出的热量,然后用十字交叉法求出.
2 3 8
n
H 2 285.8 1450.6 H 2 1450.6 3
n
C 3 H 8 =
483.6
≈ 1
769.4
C H 2220. 0 483.6
3 8
【答案】B
n
A
n a a
【名师点睛】十字交叉法求出的 B 表示什么量之比,要视参加交叉的a 、a 、 的意义而定,a 、a 、
1 2 1 2
n
A
n
的量纲中分母是何种物理量, B 就是该物理量之比.在不同的情况,它可以是物质的量之比、气体体积
之比、质量之比、原子个数比等.
【变式训练1】有1.5L的C H 和C H 组成的混合气体,恰好能与同条件下的2.7L的H 完全加成生成乙烷,
2 4 2 2 2
则原混合气体中C H、C H 的体积比为( )
2 4 2 2
A.1: 1 B.1:2 C.1:4 D.4:12.7
【解析】每1L C H 、C H 分别加氢,消耗H 的量为1L、2L,平均每1L混合气体加H
量为1.5=1.8(L
2 4 2 2 2 2
),可用十字交叉法求解.
C H 1 0.2
2 4
1.8
C H 2 0.8
2 2
即 。
【答案】C
【变式训练2】 LiCO 和BaCO 的混合物与盐酸完全反应,所消耗盐酸的量与等质量的CaCO 和同浓度的
2 3 3 3
盐酸反应所消耗盐酸的量相等.则混合粉末中LiCO 和BaCO 的质量之比为
2 3 3
( )
A.3:5 B.5:3 C.7:5 D.5:7
【解析】首先请判断用下列十字交叉法求出两者之比是什么量之比.
LiCO 74 97
2 3 97
100 2 6 =?
BaCO 197 26
3
若设均与2 mol HCl反应,则所需的 LiCO 、BaCO 、CaCO 各1 mol,摩尔质量分别为 74g/mol、
2 3 3 3
197g/mol、100g/mol.故上面用十字交叉法求出的是LiCO 和BaCO 的物质的量之比.然后换算为质量比.
2 3 3
n m
Li
2
CO
3
97 Li
2
CO
3
97×74 7
n BaCO 3 = 26 m BaCO 3 = 26×197 =5 .
【答案】C