文档内容
专题讲座(一) 陌生化学方程式书写
1.由于氰化钠有剧毒,因此需要对“废液”中的氰化钠进行处理,通常选用漂白粉或漂白液在碱性
条件下将其氧化,其中一种产物为空气的主要成分,则在碱性条件下漂白液与氰化钠反应的离子方程式为
_______。
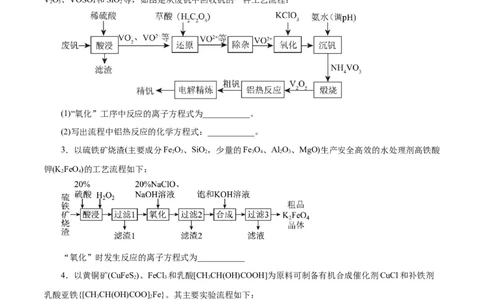
2.从工业废钒中回收金属钒既避免污染环境又有利于资源综合利用。某工业废钒的主要成分为
VO、VOSO 和SiO 等,如图是从废钒中回收钒的一种工艺流程:
2 5 4 2
(1)“氧化”工序中反应的离子方程式为___________。
(2)写出流程中铝热反应的化学方程式:___________。
3.以硫铁矿烧渣(主要成分Fe O、SiO,少量的Fe O、Al O、MgO)生产安全高效的水处理剂高铁酸
2 3 2 3 4 2 3
钾(K FeO)的工艺流程如下:
2 4
“氧化”时发生反应的离子方程式为___________
4.以黄铜矿(CuFeS)、FeCl 和乳酸[CHCH(OH)COOH]为原料可制备有机合成催化剂CuCl和补铁剂
2 3 3
乳酸亚铁{[CH CH(OH)COO] Fe}。其主要实验流程如下:
3 2
FeCl 溶液与黄铜矿发生反应的离子方程式为___________
3
5.高锰酸钾生产过程中产生的废锰渣(主要成分为MnO 、KOH、MgO和Fe O)可用于制备MnSO 晶
2 2 3 4体,工艺流程如下:
“反应Ⅲ”的离子方程式为___________
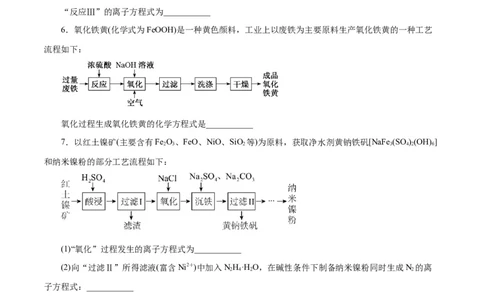
6.氧化铁黄(化学式为FeOOH)是一种黄色颜料,工业上以废铁为主要原料生产氧化铁黄的一种工艺
流程如下:
氧化过程生成氧化铁黄的化学方程式是___________
7.以红土镍矿(主要含有Fe O、FeO、NiO、SiO 等)为原料,获取净水剂黄钠铁矾[NaFe (SO )(OH) ]
2 3 2 3 4 2 6
和纳米镍粉的部分工艺流程如下:
(1)“氧化”过程发生的离子方程式为___________
(2)向“过滤Ⅱ”所得滤液(富含Ni2+)中加入NH·H O,在碱性条件下制备纳米镍粉同时生成N 的离
2 4 2 2
子方程式:___________
8.某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物
质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·7H O):
4 2(1)“碱浸”中NaOH的两个作用分别是_______;为回收金属,用稀硫酸将“滤液①”调为中性,生成
沉淀,写出该反应的离子方程式:_______。
(2)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH,写出该反应的
离子方程式:_______。
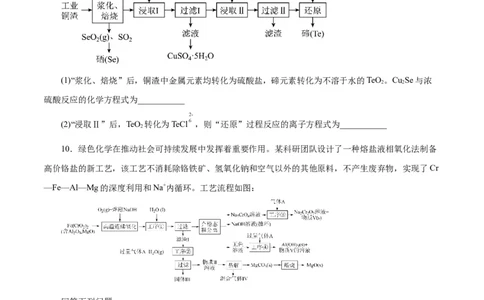
9.以某工业铜渣(主要成分为Cu、Cu Se、Cu Te,还有少量Ag)为原料制备胆矾、硒、碲的一种工艺
2 2
流程如下:
(1)“浆化、焙烧”后,铜渣中金属元素均转化为硫酸盐,碲元素转化为不溶于水的TeO 。Cu Se与浓
2 2
硫酸反应的化学方程式为___________
(2)“浸取Ⅱ”后,TeO 转化为TeCl ,则“还原”过程反应的离子方程式为___________
2
10.绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备
高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr
—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:
(1)工序③中发生反应的离子方程式为_______。
(2)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为_______。
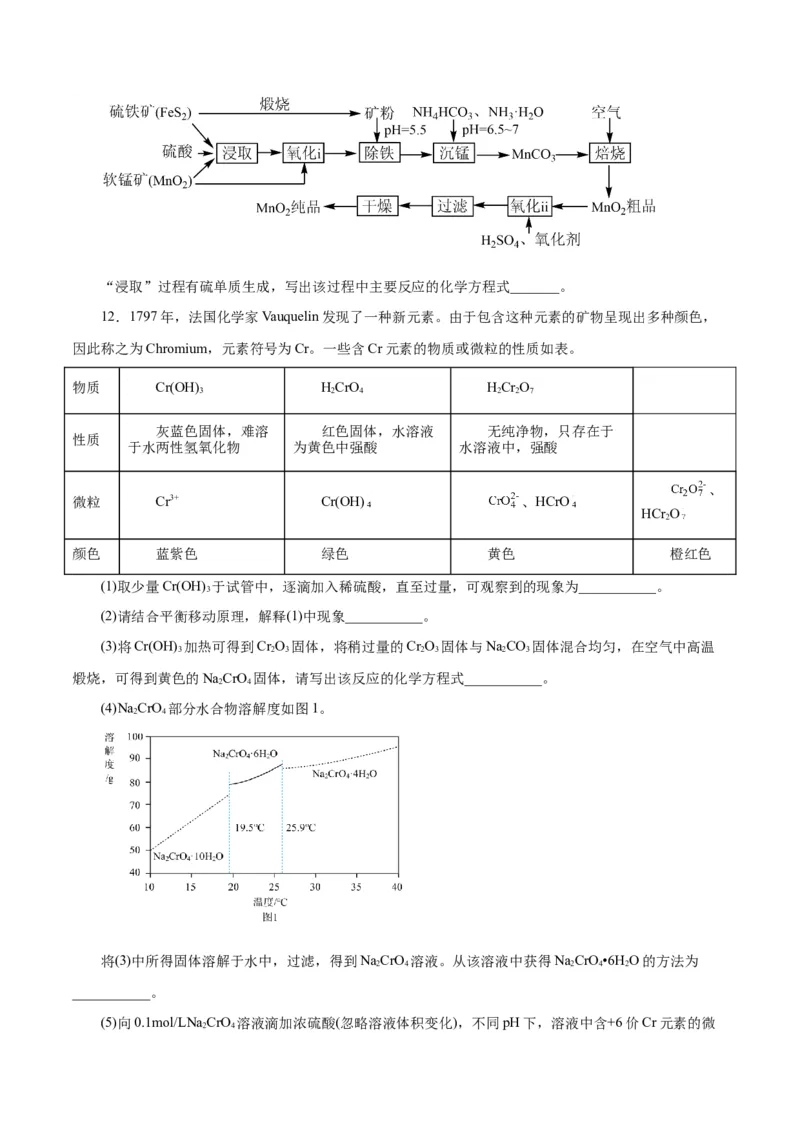
11.一种制取电池级二氧化锰的工艺流程如下图:“浸取”过程有硫单质生成,写出该过程中主要反应的化学方程式_______。
12.1797年,法国化学家Vauquelin发现了一种新元素。由于包含这种元素的矿物呈现出多种颜色,
因此称之为Chromium,元素符号为Cr。一些含Cr元素的物质或微粒的性质如表。
物质 Cr(OH) HCrO HCr O
3 2 4 2 2 7
灰蓝色固体,难溶 红色固体,水溶液 无纯净物,只存在于
性质
于水两性氢氧化物 为黄色中强酸 水溶液中,强酸
、
微粒 Cr3+ Cr(OH) 、HCrO
HCr O
2
颜色 蓝紫色 绿色 黄色 橙红色
(1)取少量Cr(OH) 于试管中,逐滴加入稀硫酸,直至过量,可观察到的现象为___________。
3
(2)请结合平衡移动原理,解释(1)中现象___________。
(3)将Cr(OH) 加热可得到Cr O 固体,将稍过量的Cr O 固体与NaCO 固体混合均匀,在空气中高温
3 2 3 2 3 2 3
煅烧,可得到黄色的NaCrO 固体,请写出该反应的化学方程式___________。
2 4
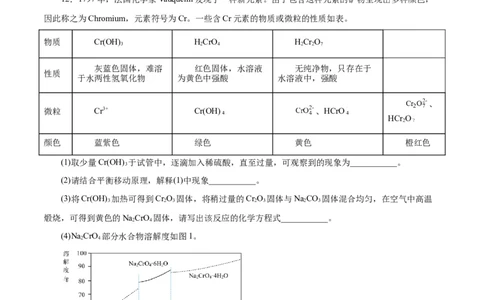
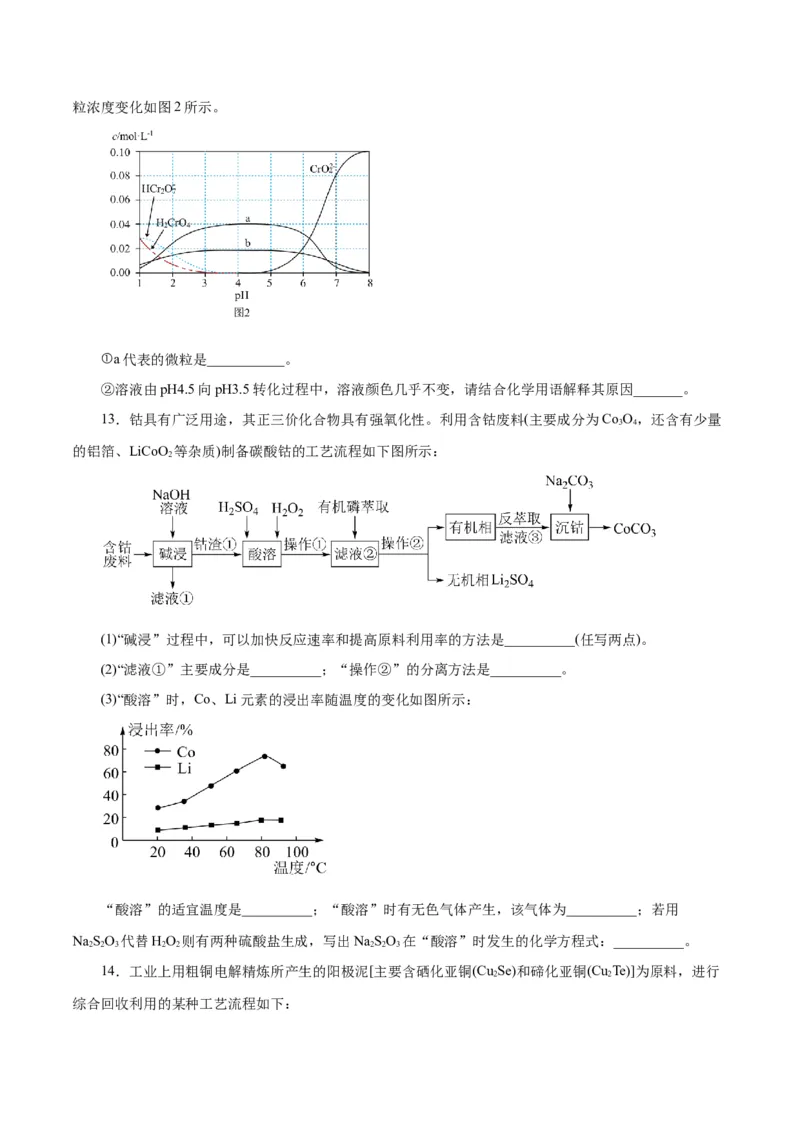
(4)Na CrO 部分水合物溶解度如图1。
2 4
将(3)中所得固体溶解于水中,过滤,得到NaCrO 溶液。从该溶液中获得NaCrO•6H O的方法为
2 4 2 4 2
___________。
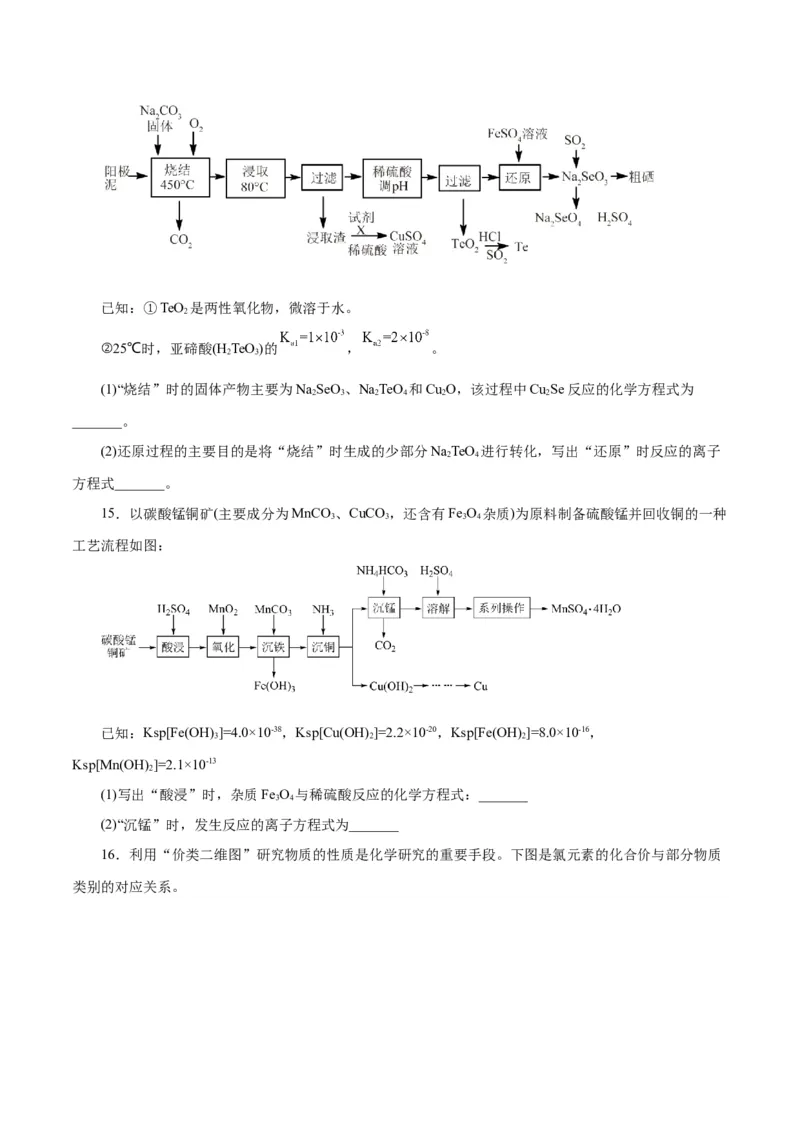
(5)向0.1mol/LNa CrO 溶液滴加浓硫酸(忽略溶液体积变化),不同pH下,溶液中含+6价Cr元素的微
2 4粒浓度变化如图2所示。
①a代表的微粒是___________。
②溶液由pH4.5向pH3.5转化过程中,溶液颜色几乎不变,请结合化学用语解释其原因_______。
13.钴具有广泛用途,其正三价化合物具有强氧化性。利用含钴废料(主要成分为Co O,还含有少量
3 4
的铝箔、LiCoO 等杂质)制备碳酸钴的工艺流程如下图所示:
2
(1)“碱浸”过程中,可以加快反应速率和提高原料利用率的方法是__________(任写两点)。
(2)“滤液①”主要成分是__________;“操作②”的分离方法是__________。
(3)“酸溶”时,Co、Li元素的浸出率随温度的变化如图所示:
“酸溶”的适宜温度是__________;“酸溶”时有无色气体产生,该气体为__________;若用
NaSO 代替HO 则有两种硫酸盐生成,写出NaSO 在“酸溶”时发生的化学方程式:__________。
2 2 3 2 2 2 2 3
14.工业上用粗铜电解精炼所产生的阳极泥[主要含硒化亚铜(Cu Se)和碲化亚铜(Cu Te)]为原料,进行
2 2
综合回收利用的某种工艺流程如下:已知:①TeO 是两性氧化物,微溶于水。
2
②25℃时,亚碲酸(H TeO )的 , 。
2 3
(1)“烧结”时的固体产物主要为NaSeO、NaTeO 和Cu O,该过程中Cu Se反应的化学方程式为
2 3 2 4 2 2
_______。
(2)还原过程的主要目的是将“烧结”时生成的少部分NaTeO 进行转化,写出“还原”时反应的离子
2 4
方程式_______。
15.以碳酸锰铜矿(主要成分为MnCO 、CuCO,还含有Fe O 杂质)为原料制备硫酸锰并回收铜的一种
3 3 3 4
工艺流程如图:
已知:Ksp[Fe(OH) ]=4.0×10-38,Ksp[Cu(OH) ]=2.2×10-20,Ksp[Fe(OH) ]=8.0×10-16,
3 2 2
Ksp[Mn(OH) ]=2.1×10-13
2
(1)写出“酸浸”时,杂质Fe O 与稀硫酸反应的化学方程式:_______
3 4
(2)“沉锰”时,发生反应的离子方程式为_______
16.利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质
类别的对应关系。(1)A、B、C三种物质中,属于电解质的是_______ (填化学式)。
(2)写出 的电离方程式_______。
(3)C可与HCl反应生成A,写出该反应的化学方程式_______。
(4)已知D可用于实验室制 ,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除
生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式_______。
17.铁酸HFeO 是一种多功能、高效无毒的新型绿色水处理剂,投入水中会迅速发生反应。
2 4
(1)H FeO 中Fe的化合价为________。
2 4
(2)已知:常温下高铁酸为紫黑色固体,将HFeO 投入水中,有气体生成,同时有红褐色沉淀产生,
2 4
则HFeO 与水反应的化学方程式为________。
2 4
(3)在工业上制备HFeO 的方法有多种。
2 4
Ⅰ.干法制备的反应原理如下:2FeSO +6Na O=aNa FeO+bM↑+2Na O+2Na SO
4 2 2 2 4 2 2 4
①b=________。
②每生成1molM,该反应转移电子的物质的量为________mol。
Ⅱ.湿法制备的工艺流程如下;
已知:HFeO 在强碱性溶液中的溶解度较小,高温易分解。
2 4
③反应a中,生成物除了HFeO 外,另一种盐的化学式为________。
2 4
④一系列操作包括过滤、________、________。
18.某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量,体积均为
1L),当闭合该装置的开关K时,观察到电流计的指针发生了偏转。请回答下列问题:(1)甲、乙、丙三池中为原电池的是______(填“甲池”、“乙池”或“丙池”),A电极的电极反应式
为______,C电极的电极反应式为______。
(2)丙池总反应的离子方程式为______。
(3)当甲池中B电极上消耗O 的体积为560mL(标准状况)时,理论上通过乙池的电量为______(法拉第
2
常数F=9.65×104C•mol-1,列式并计算),丙池溶液的pH为______(忽略溶液体积的变化)。
19.回答下列问题:
(1)下图是某化学兴趣小组探究化学能转变为电能的装置。
①若电极a为Zn、电极b为Ag、c为CuSO 溶液,开始时a电极与b电极质量相等,当电路中转移
4
0.2mol电子时,a电极与b电极质量差为_______g。
②若电极a为Mg、电极b为Al、c为NaOH溶液,则负极电极反应式为:_______。
③若电极a为Fe、电极b为Cu、c为浓硝酸,则正极电极反应式为:_______。
(2)燃料电池的工作原理是将燃料和氧化剂(如O)反应所放出的化学能直接转化为电能。现设计如图为
2
CH 燃料电池示意图,工作时电子流向如图所示。
4
写出电极A的电极方程式_______,电极A附近pH如何变化?_______ (填“变大”或“变小”)。
(3)Li-SOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl - SOCl
2 4 2.
电池的总反应可表示为:4Li+2SOCl = 4LiCl+S+ SO 。已知SOCl 会与水反应有刺激性气味的气体生成:
2 2 2SOCl + H O=2HCl↑+ SO ↑。电池正极发生的电极反应式为_______;组装该电池必须在无水、无氧的条件
2 2 2
下进行,原因是_______。
20.I.如图是利用电化学装置将SO 转化为重要的化工原料HSO 的原理示意图。
2 2 4
请回答下列问题:
(1)该装置将_______能转化为______能。
(2)催化剂b表面O 发生_______反应,其附近溶液酸性______(填“增强”、“不变”或“减弱”)。
2
(3)催化剂a表面的电极反应式:_______。
II.某废料铁泥主要成分是Fe O、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe O,设
2 3 2 3
计实验流程如图:
(4)步骤(I)充分反应后进行的实验操作名称是______。
(5)步骤(II)中加入HO 溶液后需要适当加热但温度不能过高,原因是______。
2 2
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢
氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由______。
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH) 沉淀,反应的离子方程式为______。
3