文档内容
大题突破 1 化学反应原理综合题题型研究
1.(2022·吉林延边一模)碳排放问题是第26届联合国气候变化大会讨论的焦点。我国向国际
社会承诺2030年实现“碳达峰”,2060年实现“碳中和”。为了实现这个目标,加强了对
CO 转化的研究。下面是CO 转化为高附加值化学品的反应。相关反应的热化学方程式如下:
2 2
反应Ⅰ:CO(g)+H(g)HO(g)+CO(g) ΔH
2 2 2 1
反应Ⅱ:CO(g)+2H(g)CHOH(g) ΔH=-90.0 kJ·mol-1
2 3 2
反应Ⅲ:CO(g)+3H(g)CHOH(g)+HO(g) ΔH=-49.0 kJ·mol-1
2 2 3 2 3
反应Ⅳ:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-165.0 kJ·mol-1
2 2 4 2 4
反应Ⅴ:2CO(g)+6H(g)C H(g)+4HO(g) ΔH=-122.7 kJ·mol-1
2 2 2 4 2 5
回答下列问题:
(1)反应Ⅲ一般认为通过反应Ⅰ、Ⅱ来实现,则反应Ⅰ的ΔH=________ kJ·mol-1;已知:由
1
实验测得反应Ⅰ的v正 =k
正
·c(CO
2
)·c(H
2
),v逆 =k
逆
·c(H
2
O)·c(CO)(k
正
、k
逆
为速率常数,与温
度、催化剂有关)。若平衡后升高温度,则________(填“增大”“不变”或“减小”)。
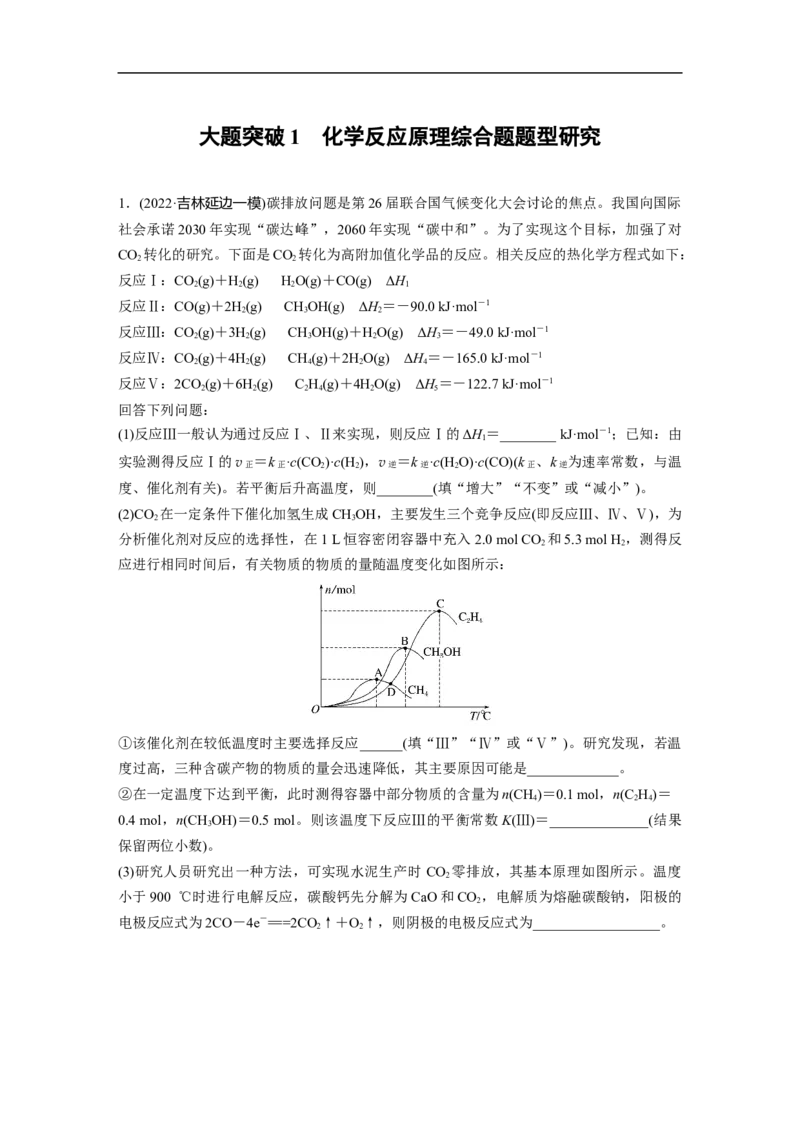
(2)CO 在一定条件下催化加氢生成CHOH,主要发生三个竞争反应(即反应Ⅲ、Ⅳ、Ⅴ),为
2 3
分析催化剂对反应的选择性,在1 L恒容密闭容器中充入2.0 mol CO 和5.3 mol H ,测得反
2 2
应进行相同时间后,有关物质的物质的量随温度变化如图所示:
①该催化剂在较低温度时主要选择反应______(填“Ⅲ”“Ⅳ”或“Ⅴ”)。研究发现,若温
度过高,三种含碳产物的物质的量会迅速降低,其主要原因可能是_____________。
②在一定温度下达到平衡,此时测得容器中部分物质的含量为n(CH)=0.1 mol,n(C H)=
4 2 4
0.4 mol,n(CHOH)=0.5 mol。则该温度下反应Ⅲ的平衡常数K(Ⅲ)=______________(结果
3
保留两位小数)。
(3)研究人员研究出一种方法,可实现水泥生产时 CO 零排放,其基本原理如图所示。温度
2
小于900 ℃时进行电解反应,碳酸钙先分解为CaO和CO ,电解质为熔融碳酸钠,阳极的
2
电极反应式为2CO-4e-===2CO↑+O↑,则阴极的电极反应式为__________________。
2 22.(2022·重庆模拟)碳达峰是指我国承诺2030年前,二氧化碳的排放不再增长。因此,诸多
科学家都在大力研究利用CO 和CO以减少碳的排放。
2
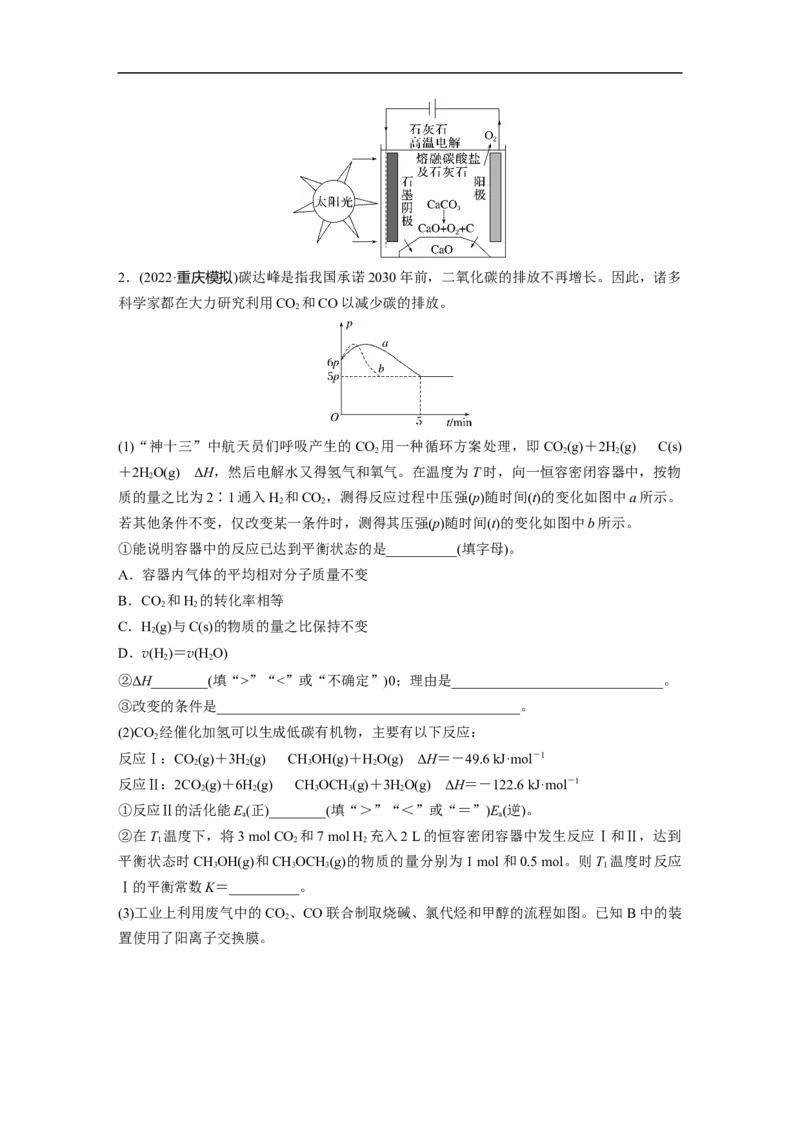
(1)“神十三”中航天员们呼吸产生的CO 用一种循环方案处理,即CO(g)+2H(g)C(s)
2 2 2
+2HO(g) ΔH,然后电解水又得氢气和氧气。在温度为T时,向一恒容密闭容器中,按物
2
质的量之比为2∶1通入H 和CO ,测得反应过程中压强(p)随时间(t)的变化如图中a所示。
2 2
若其他条件不变,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图中b所示。
①能说明容器中的反应已达到平衡状态的是__________(填字母)。
A.容器内气体的平均相对分子质量不变
B.CO 和H 的转化率相等
2 2
C.H(g)与C(s)的物质的量之比保持不变
2
D.v(H )=v(H O)
2 2
②ΔH________(填“>”“<”或“不确定”)0;理由是______________________________。
③改变的条件是___________________________________________。
(2)CO 经催化加氢可以生成低碳有机物,主要有以下反应:
2
反应Ⅰ:CO(g)+3H(g)CHOH(g)+HO(g) ΔH=-49.6 kJ·mol-1
2 2 3 2
反应Ⅱ:2CO(g)+6H(g)CHOCH (g)+3HO(g) ΔH=-122.6 kJ·mol-1
2 2 3 3 2
①反应Ⅱ的活化能E(正)________(填“>”“<”或“=”)E(逆)。
a a
②在T 温度下,将3 mol CO 和7 mol H 充入2 L的恒容密闭容器中发生反应Ⅰ和Ⅱ,达到
1 2 2
平衡状态时CHOH(g)和CHOCH (g)的物质的量分别为1 mol和0.5 mol。则T 温度时反应
3 3 3 1
Ⅰ的平衡常数K=__________。
(3)工业上利用废气中的CO 、CO联合制取烧碱、氯代烃和甲醇的流程如图。已知 B中的装
2
置使用了阳离子交换膜。①B中发生的总反应的离子方程式为_____________________________________________。
②若某废气中含有的 CO 和 CO 的体积比为 1∶1,废气中 CO 和 CO 的体积分数共为
2 2
8.96%。假设A中处理了标准状况下10 m3的废气,其中CO 和CO全部转化成CHOH,理
2 3
论上可制得C HCl________ kg。
2 4 2
3.(2022·安徽马鞍山二中模拟)研究含氮元素物质的反应对生产、生活、科研等方面具有重
要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C HN)。
2 8 2
已知:①C HN(l)+4O(g)===2CO(g)+N(g)+4HO(l) ΔH=-2 765.0 kJ·mol-1
2 8 2 2 2 2 2 1
②2O(g)+N(g)===NO(l)
2 2 2 4
ΔH=-19.5 kJ·mol-1
2
③HO(g)===HO(l) ΔH=-44.0 kJ·mol-1
2 2 3
则C HN(l)+2NO(l)===3N(g)+2CO(g)+4HO(g)的ΔH为__________。
2 8 2 2 4 2 2 2
(2)碘蒸气存在能大幅度提高NO的分解速率,反应历程为
2
第一步:I(g)―→2I(g)(快反应)
2
第二步:I(g)+NO(g)―→N(g)+IO(g)(慢反应)
2 2
第三步:IO(g)+NO(g)―→N(g)+O(g)+I(g)(快反应)
2 2 2
实验表明,含碘时NO分解速率方程v=k·c(N O)·[c(I)]0.5(k为速率常数)。下列表述正确的
2 2 2
是________(填字母)。
A.NO分解反应中,k值与碘蒸气浓度大小有关
2
B.v(第二步的逆反应)<v(第三步反应)
C.IO为反应的催化剂
D.第二步活化能比第三步大
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装
置中CO和NO发生反应:2NO(g)+2CO(g)===N(g)+2CO(g) ΔH=-746.8 kJ·mol-1。实
2 2
验测得:v正 =k
正
·p2(NO)·p2(CO),v逆 =k
逆
·p(N
2
)·p2(CO
2
)。其中k
正
、k
逆
分别为正、逆反应速
率常数,只与温度有关;p为气体分压(分压=物质的量分数×总压)。
①达到平衡后,仅升高温度,k 增大的倍数__________(填“大于”“小于”或“等于”)k
正
增大的倍数。
逆
②一定温度下在刚性密闭容器中充入CO、NO和N 的物质的量之比为2∶2∶1,压强为
2
p。达平衡时压强为0.9p,则=__________。
0 0
(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数K :
pⅰ.3N H(l)===4NH (g)+N(g) ΔH K
2 4 3 2 1 p1
ⅱ.4NH(g)===2N(g)+6H(g) ΔH K
3 2 2 2 p2
绘制pK -T和pK -T的线性关系如图所示(已知:pK =-lg K ):
p1 p2 p p
①由图可知,ΔH________(填“>”或“<”)0。
1
②反应3NH(l)===3N(g)+6H(g)的K=________(用K 、K 表示);该反应的ΔH______(填
2 4 2 2 p1 p2
“>”或“<”)0,写出推理过程:_____________________________________________。
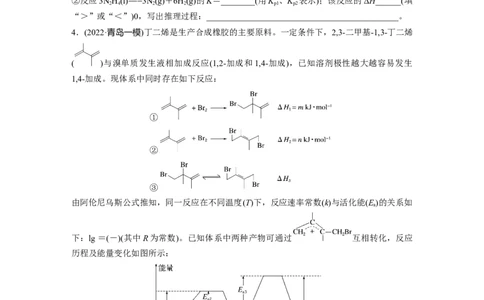
4.(2022·青岛一模)丁二烯是生产合成橡胶的主要原料。一定条件下,2,3-二甲基-1,3-丁二烯
( )与溴单质发生液相加成反应(1,2-加成和1,4-加成),已知溶剂极性越大越容易发生
1,4-加成。现体系中同时存在如下反应:
①
②
③
由阿伦尼乌斯公式推知,同一反应在不同温度(T)下,反应速率常数(k)与活化能(E)的关系如
a
下:lg =(-)(其中R为常数)。已知体系中两种产物可通过 互相转化,反应
历程及能量变化如图所示:
(1)由反应历程及能量变化图示判断,m______(填“>”“=”或“<”)n,ΔH =
3
_____________________________________________(用含不同活化能E 的式子表示)。
a
(2)其他条件不变的情况下,升高反应温度,对反应__________(填“①”或“②”)的速率提
高更有利,分析原因:______________________________________________________。(3)由反应历程及能量变化图示判断,产物中__________________(用系统命名法命名)含量更
大,若要提高该产物在平衡体系中的物质的量分数,还可采取的措施是__________________。
(4)在一定温度下,向某反应容器中加入1.0 mol 和一定量的Br 发生上述反应。测得
2
的平衡转化率为α,平衡时Br 为b mol,若以物质的量分数表示的平衡常数K,反
2 x
应③的平衡常数K =4,则产物 的选择性百分比为______,开始加入的Br 为
x3 2
________ mol,反应①的平衡常数K =__________。
x1
5.(2022·辽宁丹东一模)合成氨反应N(g)+3H(g)2NH (g)是目前最有效的工业固氮方法,
2 2 3
解决了数亿人口生存问题。
(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用“ad”表示。
该历程中反应速率最慢步骤的化学方程式为___________________________________。
(2)在T ℃、压强为0.9 MPa条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体
系中气体的含量与时间变化关系如图所示:
①反应20 min达到平衡,试求0~20 min内氨气的平均反应速率v(NH )=______ MPa·min-
3
1,
该反应的K =________ MPa-2(结果保留小数点后两位,K 为以分压表示的平衡常数)。
p p
②下列叙述能说明该条件下反应达到平衡状态的是__________(填字母)。
a.氨气的体积分数保持不变
b.容器中氢氮比保持不变
c.气体平均相对分子质量保持不变
d.气体密度保持不变③若起始条件相同,在恒容容器中发生反应,则达到平衡时H 的含量符合图中________(填
2
“d”“e”“f”或“g”)点。
(3)利用催化剂通过电化学反应在室温下合成氨的原理如图所示,该装置中阴极的电极反应
式为________________________________________________________________________。
(4)25 ℃时用氨水吸收甲酸可得到 HCOONH 溶液。已知 25 ℃时甲酸的电离常数 K =
4 a
1.75×
10-5,NH ·H O的电离常数K =2×10-5。计算反应NH ·H O+HCOOHHCOO-+NH+
3 2 b 3 2
HO的平衡常数K=__________。
2