文档内容
2023 年湖北省八市高三(3 月)联考
化学参考答案
1.C 2.C 3.C 4.B 5.D 6.D 7.B 8.C
9.B 10.B 11.A 12.B 13.D 14.D 15.D
16(13分)
(1)圆底烧瓶(1分),b(1分)。
(2)防止温度过高,反应速率过快(2分)(答减速即可得分)
(3)CrO +2HCl=CrO Cl +H O(2分)。(方程式不平不得分)
3 2 2 2
(4)加入过量氯化钠可产生过量的氯化氢气体,使更多的CrO 参与反应。(2分)
3
(5)将CrO Cl 迅速冷凝便于收集,提高产率(或答减缓铬酰氯挥发)(2分)
2 2
(6)B(1分)吸收未参与反应的HCl气体和逸出的铬酰氯蒸气,防止空气中的水蒸气进
入装置。(2分)(两条各1分未答吸收铬酰氯蒸气不扣分)
17(14分)
(1)相同(2分) (2)19(2分) (3) (2分)
(4)8(2分) (5)氨基(1分) 碳氟键(1分) 2HCl(1分)
(6)①加成反应(1分) ②形成的五元环较稳定(2分)(或答酰胺键比酯基稳定)
18(14分)
(1)MnO (或答二氧化锰)(2分)Mn O +2H+= MnO +Mn2++H O(2分)
2 2 3 2 2
(2)将溶液中的Mn2+氧化为MnO 沉淀除去;将溶液中的Fe2+氧化为Fe3+。(2分,两条各
2
1分)
(3)蒸发浓缩(1分) 冷却结晶(1分)
(4)ZnSO +C H O Ca=CaSO ↓+C H O Zn(2分) 降低葡萄糖酸锌的溶解度(2分)
4 12 22 14 4 12 22 14
(5)该同学也能制得葡萄糖酸锌,但产品可能不纯(2分)(答产品不纯即可得分)
19.(14分)
(1)能(2分)
(2)反应速率、平衡转化率、催化剂的活性(任写两点,2分)
(3)8.33或 25 (2分)
3
(4)8H++N +6e-=2NH +(2分)(或答 6H++N +6e-=2NH )
2 4 2 3
(5)①1.96%(2分)
② 高电压有利于竞争反应2H 2e H 的进行,从而不利于产NH (2分)
2 3
(6)N H 和N H (2分,对一个得1分,错写不多扣分)
2 2 2 4
12023 年湖北省八市高三(3 月)联考
化学参考答案
1.C 2.C 3.C 4.B 5.D 6.D 7.B 8.C
9.B 解析:A分子中含有8个手性碳原子
10.B 11.A 12.B 13.D
14.D 解析:A.H+在阴极得电子生成H原子,H与Fe(III)反应生成Fe(II),Fe(II)还原NO -
3
生成Fe(III)和NH +,Cl-在阳极失电子生成Cl ,Cl 与水反应生成HCl和HClO,NH +与HClO
4 2 2 4
反应生成N 。
2
D.a电极发生4Cl-−8e-+4H O=4HClO+4H+,b电极发生 NO+8e-+10H+=NH+ +3H O,
2 3 4 2
再根据HClO氧化NH+ 的离子方程式2NH+ +3HClO=N ↑+3Cl-+5H++3H O,根据分析
4 4 2 2
生成的4molHClO中有1.5mol变为氯离子,还有2.5molHClO在溶液中,因此在处理过程中
Cl-浓度不断减少
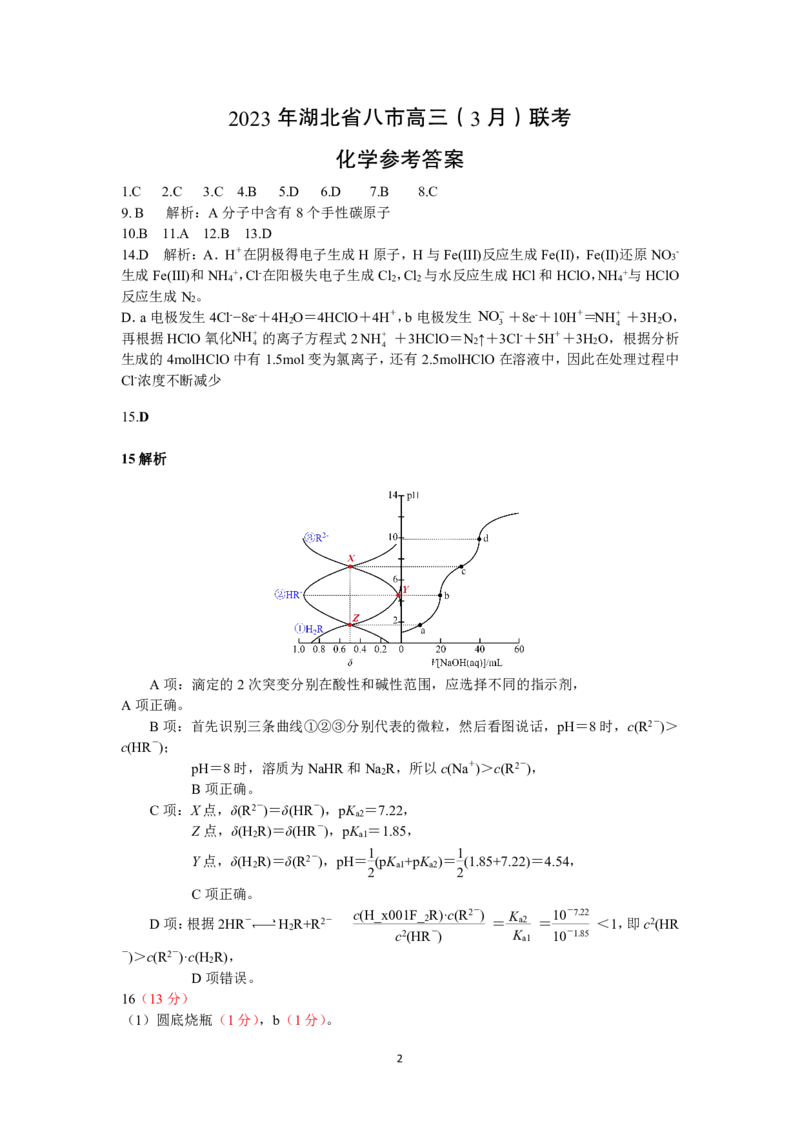
15.D
15解析
A项:滴定的2次突变分别在酸性和碱性范围,应选择不同的指示剂,
A项正确。
B项:首先识别三条曲线①②③分别代表的微粒,然后看图说话,pH=8时,c(R2-)>
c(HR-);
pH=8时,溶质为NaHR和Na R,所以c(Na+)>c(R2-),
2
B项正确。
C项:X点,δ(R2-)=δ(HR-),pK =7.22,
a2
Z点,δ(H R)=δ(HR-),pK =1.85,
2 a1
1 1
Y点,δ(H R)=δ(R2-),pH= (pK +pK )= (1.85+7.22)=4.54,
2 a1 a2
2 2
C项正确。
D项:根据2HR- H R+R2- c(H_x001F_ 2 R)·c(R2-) = K a2 = 10-7.22 <1,即c2(HR
2 c2(HR-) K
a1
10-1.85
-)>c(R2-)·c(H R),
2
D项错误。
16(13分)
(1)圆底烧瓶(1分),b(1分)。
2(2)防止温度过高,反应速率过快(2分)(答减速即可得分)
(3)CrO +2HCl=CrO Cl +H O(2分)。(方程式不平不得分)
3 2 2 2
(4)加入过量氯化钠可产生过量的氯化氢气体,使更多的CrO 参与反应。(2分)
3
(5)减缓铬酰氯挥发(2分)
(6)B(1分)吸收未参与反应的HCl气体和溢出的铬酰氯蒸气,防止空气中的水蒸气进
入装置。(2分)(两条各1分未答吸收铬酰氯蒸气不扣分)
【16解析】(1)由图可知A为圆底烧瓶。B中,冷凝水应下口进上口出。
(2)A中反应为放热反应,在反应前冷却浓硫酸可防止反应速率过快,同时也可防止A中
温度过高导致铬酰氯大量挥发。
(3)已知反应物CrO 和HCl,还知道生成物含有中CrO Cl ,写出反应物和生成物,配平
3 2 2
即可得到反应:CrO +2HCl=CrO Cl +H O。
3 2 2 2
(4)反应过程中有一部分氯化氢气体来不及与CrO 接触就逸出液面,导致CrO 反应不充
3 3
分。加入过量氯化钠可产生过量的氯化氢气体,使更多的CrO 参与反应,增大了铬酰氯的
3
产率。
(5)常温下铬酰氯易挥发,铬酰氯蒸气仅凭冷凝管冷却,难以转化为液体,用冰水浴可将
铬酰氯蒸气尽可能转化为液体,同时也可减少液态铬酰氯的挥发。
(6)尾气中含氯化氢气体和铬酰氯蒸气,铬酰氯与水反应可生成盐酸和铬酸,氢氧化钠溶
液可同时吸收氯化氢气体与铬酰氯蒸气。但铬酰氯易水解,不能将产物的收集装置直接连接
到装有氢氧化钠溶液的吸收装置中。碱石灰中含有氢氧化钠固体,氢氧化钠固体易吸潮,其
表面会吸收少量水分,氯化氢气体和铬酰氯蒸气通过吸潮后的氢氧化钠固体时可以被吸收。
17(14分)
(1)相同(2分) (2)19(2分) (3) (2分)
(4)8(2分) (5)氨基(1分) 碳氟键(1分) 2HCl(1分)
(6)①加成反应(1分) ②形成的五元环较稳定(2分)(或答酰胺键比酯基稳定)
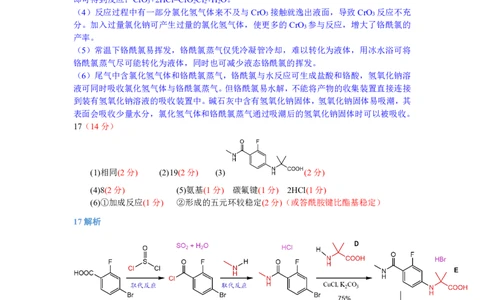
17解析
(1)A与SOCl 发生取代反应生成酰卤,得B,B与CH -NH 发生取代反应生成酰胺,
2 3 2
得化合物C,所以这两个反应的反应类型相同。
3(2)具有酰胺类物质的性质,苯环上第 3 个取代基可以是: 、
、 、 、 ,所以满足C的同分异构体
还有19种(5×4-1)。
(3)联系C和F的结构,容易判断C与 (D)发生取代反应生成化合物E
( )。
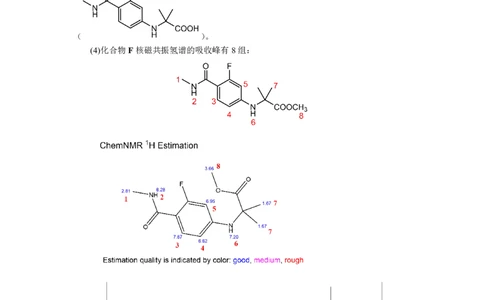
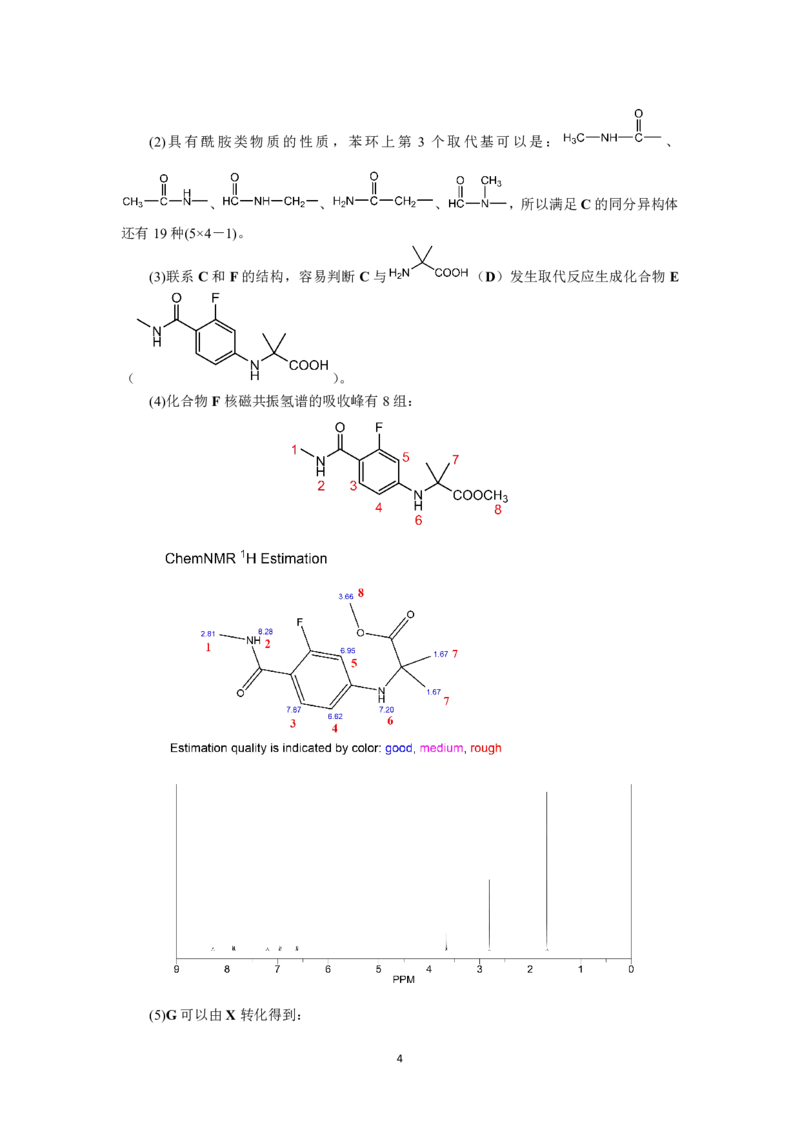
(4)化合物F核磁共振氢谱的吸收峰有8组:
(5)G可以由X转化得到:
4(6)
(五元环、六
元环较稳定)
18(14分)
(1)MnO (或答二氧化锰)(2分)Mn O +2H+= MnO +Mn2++H O(2分)
2 2 3 2 2
(2)将溶液中的Mn2+氧化为MnO 沉淀除去;将溶液中的Fe2+氧化为Fe3+。(2分,两条各
2
1分)
(3)蒸发浓缩(1分) 冷却结晶(1分)
(4)ZnSO +C H O Ca=CaSO ↓+C H O Zn(2分) 降低葡萄糖酸锌的溶解度(2分)
4 12 22 14 4 12 22 14
(5)该同学也能制得葡萄糖酸锌,但产品可能不纯(2分)(答产品不纯即可得分)
【18解析】(1)由已知①可知,反应物为Mn O 和H+生成物含有MnO 和Mn2+,写出反应
2 3 2
物和生成物,配平后可得到反应:Mn O +2H+=MnO +Mn2++H O。因此,沉淀1为MnO 。
2 3 2 2 2
(2)由已知②可知,Mn2+与Zn2+开始沉淀与完全沉淀的pH范围有部分重合的地方,难以
通过调pH将Mn2+除去,因此,Mn2+在此处应被氧化成MnO 沉淀除去。另外,氧化过程还
2
将溶液中的Fe2+氧化为Fe3+,并通过调节pH除去。
(3)由于葡萄糖酸锌极易溶于热水,溶于冷水,溶解度有一定的差异,可蒸发浓缩、冷却
结晶的操作分离提纯。
(4)由于CaSO 微溶,可写出复分解反应:ZnSO +C H O Ca=CaSO ↓+C H O Zn。
4 4 12 22 14 4 12 22 14
因为葡萄糖酸锌在水中的溶解度较大,可推知其即使经过浓缩后也不易结晶,向溶液中加入
少量乙醇后可降低葡萄糖酸锌的溶解度,使其顺利结晶。
(5)能得到葡萄糖酸锌,因为Zn(OH) 与H SO 反应生成ZnSO ,ZnSO 可与C H O Ca
2 2 4 4 4 12 22 14
反应生成C H O Zn,并在乙醇作用下顺利结晶。
12 22 14
19.(14分)
(1)能(2分)
(2)反应速率、平衡转化率、催化剂的活性(任写两点,2分)
(3)8.33L2/mol2或25 L2/mol2 (2分)(单位不写不扣分)
3
(4)8H++N +6e-=2NH +(2分)(或答 6H++N +6e-=2NH )
2 4 2 3
(5)①1.96%(2分)
② 高电压有利于竞争反应2H 2e H 的进行,从而不利于产NH (2分)
2 3
5(6)N H 和N H (2分,对一个得1分,错写不多扣分)
2 2 2 4
【19解析】
(1)△G=△H-T△S=-92400-298.15×(-200)<0,可以自发进行;
(3)列三段式:
2x
3
,解得x=0.3mol/L,则K
c2(NH3)
0.62
25
L2 /mol2
22x 7 c(N2)c3(H2) 0.20.63 3
(5)最大产率,则此时氨气的生成速率最大,为0.68mg/min。
0.68
氨气的实际产量为 0.04 mmol/min ,氨气的理论产量应以氮气100%转化为NH 进行
3
17
25 mL/min 100
计算,即 *2 mmol/min。故此时氨气的产率为1.96%。
24.5 L/mol 49
(6)要求结构对称,根据机理图,可以得知为HN=NH和H N-NH 。
2 2
6