文档内容
选择题突破十 A 组 基础巩固练
题组一 文字描述型离子浓度大小关系
1.(2023·江苏卷)室温下,用含少量Mn2+的MnSO 溶液制备MnCO 的过程如图所示。已知
4 3
K (MgF )=5.2×10-11,K(HF)=6.3×10-4。下列说法正确的是( )
sp 2 a
A.0.1 mol·L-1 NaF溶液中:c(F-)=c(Na+)+c(H+)
K (MgF )
sp 2
B.“除镁”得到的上层清液中:c(Mg2+)=
c(F-)
C.0.1 mol·L-1 NaHCO
溶液中:c(CO2-
)=c(H+)+c(H CO)-c(OH-)
3 3 2 3
D.“沉锰”后的滤液中:c(Na+)+c(H+)=c(OH-)+c(HCO- )+2c(CO2-
)
3 3
2.(2024·浙江温州一模)25 ℃时,某小组做如下两组实验:
实验Ⅰ:分别往浓度均为0.10 mol·L-1 NaHCO、NaCO 溶液中通入CO 至pH=7;
3 2 3 2
实验Ⅱ:在1.0 L 0.10 mol·L-1 Na CO 溶液中加入0.01 mol BaSO 固体,充分反应。
2 3 4
[已知:25 ℃,H CO 的电离常数 K =4.5×10-7、 K =4.7×10-11;K (BaCO)=2.6×10-9、K (BaSO)=1.1×10-
2 3 a a sp 3 sp 4
1 2
10。混合后溶液体积变化忽略不计]。下列说法不正确的是( )
A.0.10 mol·L-1 NaHCO、NaCO 溶液中水的电离程度:Na CO>NaHCO
3 2 3 2 3 3
B.实验Ⅰ结束后,Na CO、NaHCO
溶液中均有c(HCO-
)>c(H CO)
2 3 3 3 2 3
11
C.实验Ⅱ的转化存在平衡常数:K=
260
D.实验Ⅱ中,改用饱和NaCO 溶液,Na CO 的平衡转化率减小
2 3 2 3
题组二 滴定图像的分析
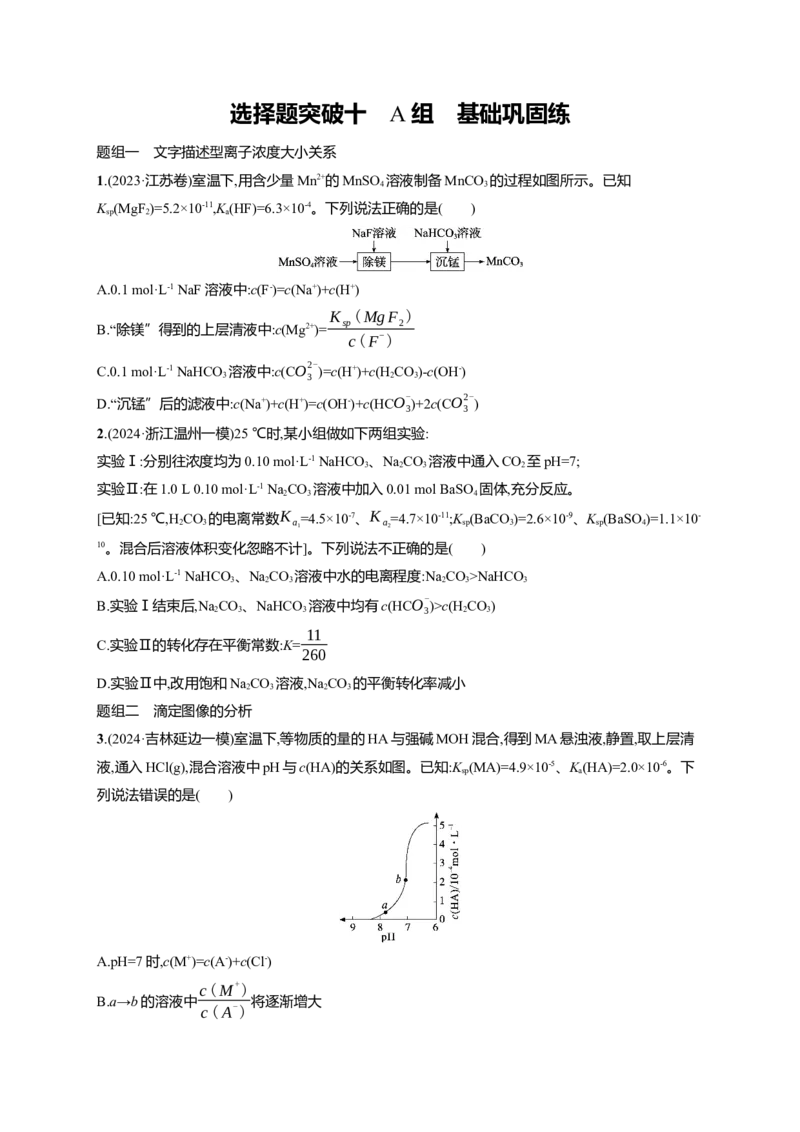
3.(2024·吉林延边一模)室温下,等物质的量的HA与强碱MOH混合,得到MA悬浊液,静置,取上层清
液,通入HCl(g),混合溶液中pH与c(HA)的关系如图。已知:K (MA)=4.9×10-5、K(HA)=2.0×10-6。下
sp a
列说法错误的是( )
A.pH=7时,c(M+)=c(A-)+c(Cl-)
c(M+)
B.a→b的溶液中 将逐渐增大
c(A-)C.上层清液中c(A-)=7.0×10-3 mol·L-1
D.c(HA)=c(A-)时,c(Cl-)c(ClO-)>c(Cl-)>c(H+)
D.氯水中存在平衡:Cl (aq)+H O(l) H+(aq)+Cl-(aq)+HClO(aq),该反应的平衡常数K约为10-5
2 2
题组三 对数图像的分析
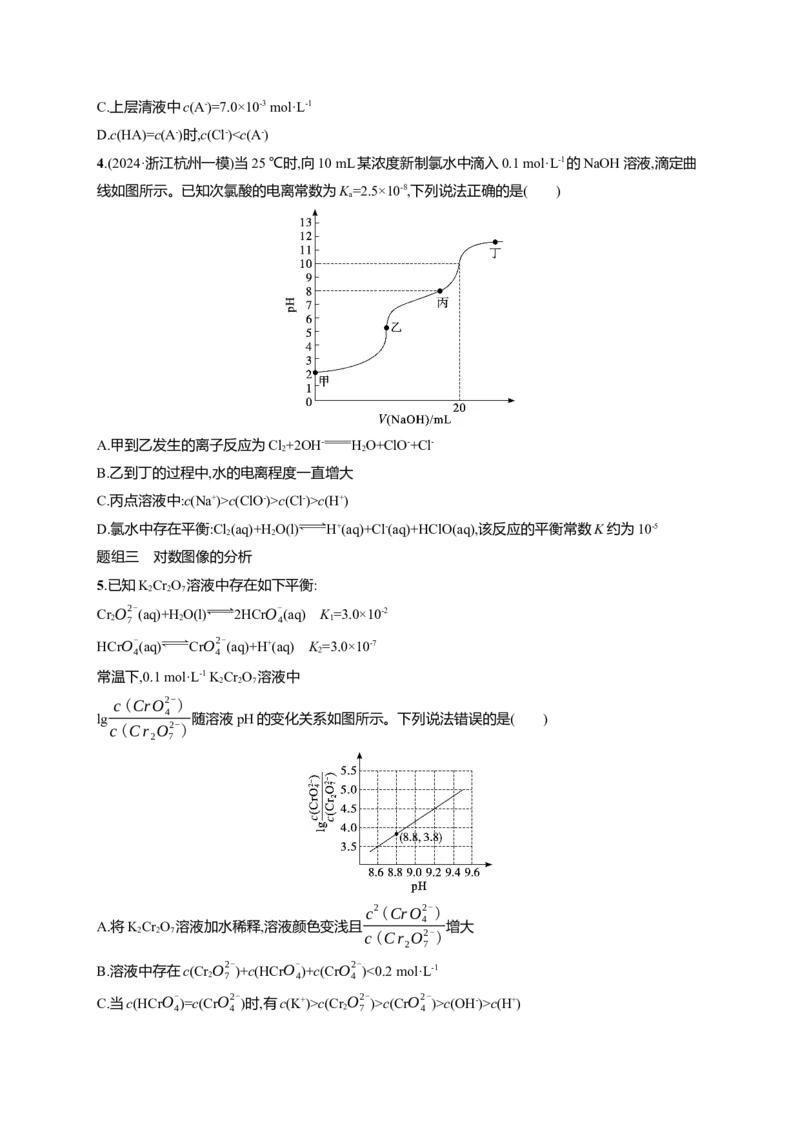
5.已知KCr O 溶液中存在如下平衡:
2 2 7
CrO2- (aq)+H O(l) 2HCrO- (aq) K =3.0×10-2
2 7 2 4 1
HCrO- (aq) CrO2- (aq)+H+(aq) K =3.0×10-7
4 4 2
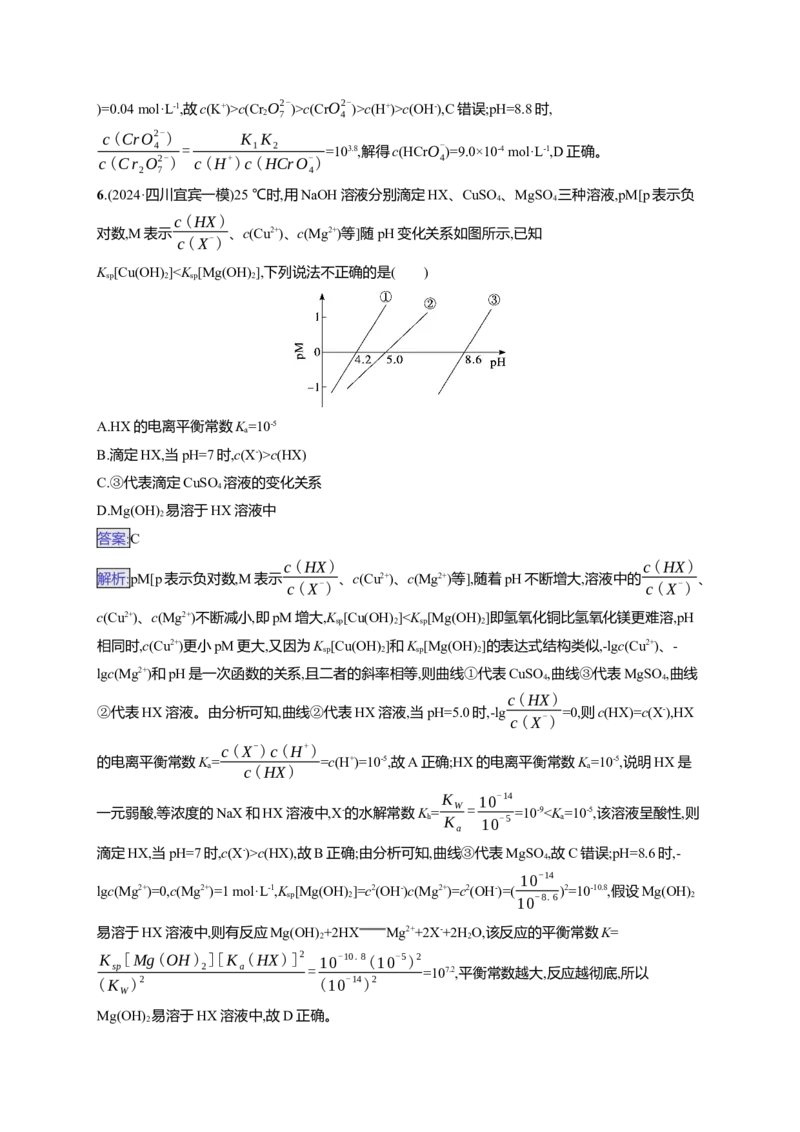
常温下,0.1 mol·L-1 K Cr O 溶液中
2 2 7
c(CrO2-)
4
lg 随溶液pH的变化关系如图所示。下列说法错误的是( )
c(Cr O2-)
2 7
c2(CrO2-)
4
A.将KCr O 溶液加水稀释,溶液颜色变浅且 增大
2 2 7 c(Cr O2-)
2 7
B.溶液中存在c(CrO2- )+c(HCrO- )+c(CrO2-
)<0.2 mol·L-1
2 7 4 4
C.当c(HCrO- )=c(CrO2- )时,有c(K+)>c(CrO2- )>c(CrO2-
)>c(OH-)>c(H+)
4 4 2 7 4D.pH=8.8时,溶液中c(HCrO-
)=9.0×10-4 mol·L-1
4
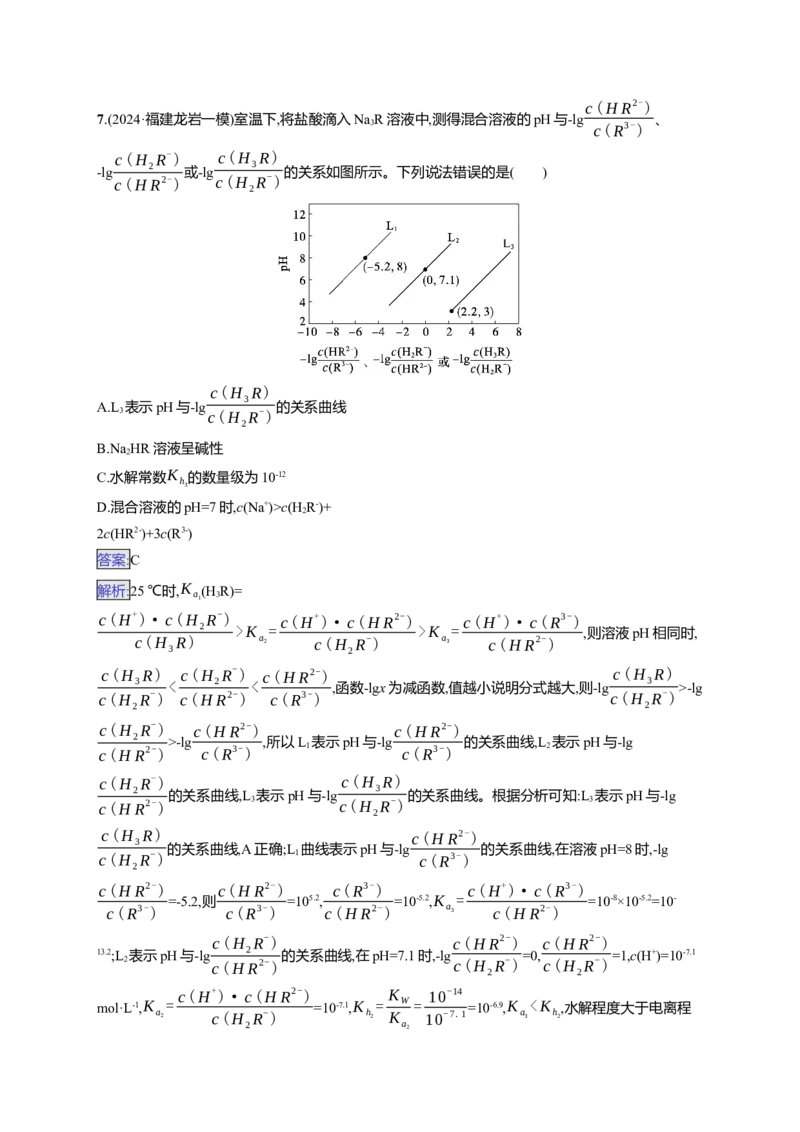
6.(2024·四川宜宾一模)25 ℃时,用NaOH溶液分别滴定HX、CuSO 、MgSO 三种溶液,pM[p表示负
4 4
c(HX)
对数,M表示 、c(Cu2+)、c(Mg2+)等]随pH变化关系如图所示,已知
c(X-)
K [Cu(OH) ]c(HX)
C.③代表滴定CuSO 溶液的变化关系
4
D.Mg(OH) 易溶于HX溶液中
2
c(H R2-)
7.(2024·福建龙岩一模)室温下,将盐酸滴入NaR溶液中,测得混合溶液的pH与-lg 、
3 c(R3-)
c(H R-) c(H R)
-lg 2 或-lg 3 的关系如图所示。下列说法错误的是( )
c(H R2-) c(H R-)
2
c(H R)
3
A.L 表示pH与-lg 的关系曲线
3 c(H R-)
2
B.Na HR溶液呈碱性
2
C.水解常数 K 的数量级为10-12
h
3
D.混合溶液的pH=7时,c(Na+)>c(H R-)+
2
2c(HR2-)+3c(R3-)
题组四 分布分数图像分析
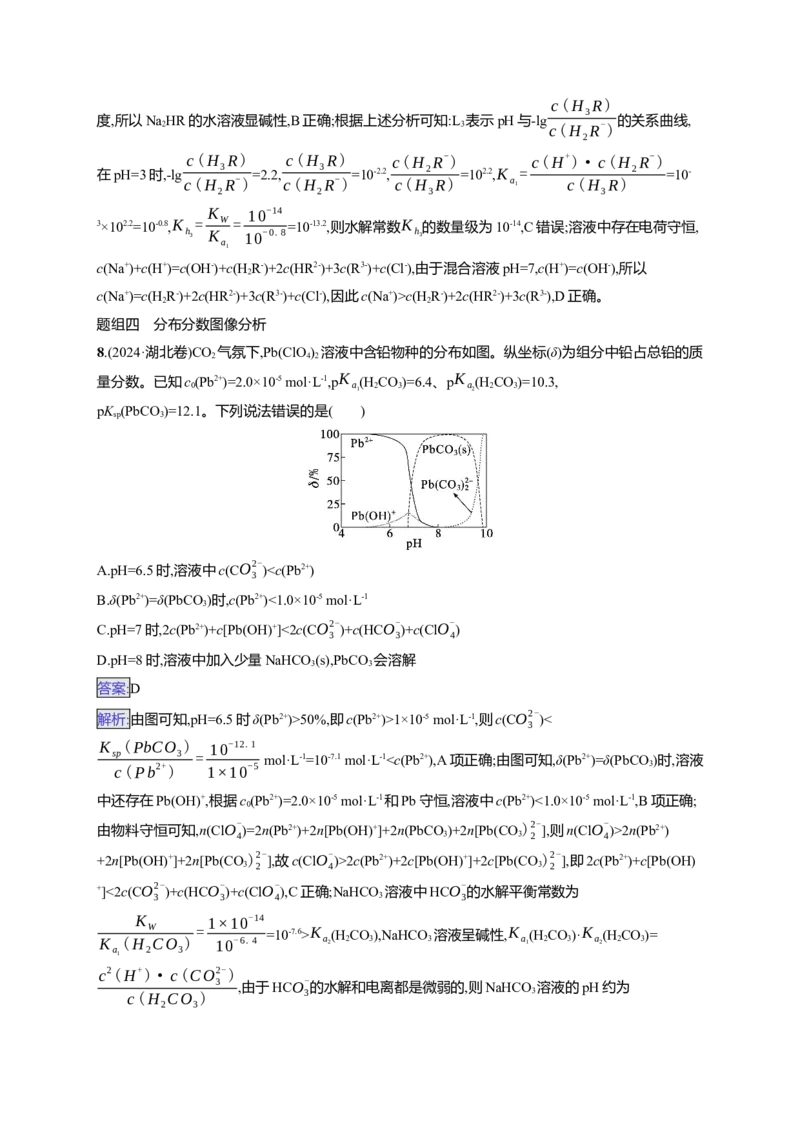
8.(2024·湖北卷)CO 气氛下,Pb(ClO ) 溶液中含铅物种的分布如图。纵坐标(δ)为组分中铅占总铅的质
2 4 2
量分数。已知c(Pb2+)=2.0×10-5 mol·L-1,pK (H CO)=6.4、pK (H CO)=10.3,
0 a 2 3 a 2 3
1 2
pK (PbCO )=12.1。下列说法错误的是( )
sp 3A.pH=6.5时,溶液中c(CO2-
)NaHCO
3 2 3 2 3 3
B.实验Ⅰ结束后,Na CO、NaHCO
溶液中均有c(HCO-
)>c(H CO)
2 3 3 3 2 3
11
C.实验Ⅱ的转化存在平衡常数:K=
260
D.实验Ⅱ中,改用饱和NaCO 溶液,Na CO 的平衡转化率减小
2 3 2 3
答案:D
解析:碳酸根的第一步水解程度远远大于第二步水解程度,所以0.10 mol·L-1 NaHCO、NaCO 溶液中
3 2 3
水解程度NaCO>NaHCO,水的电离程度NaCO>NaHCO,A正确;单一的NaHCO 溶液呈弱碱性,需
2 3 3 2 3 3 3
要通入少量的二氧化碳才能呈中性,此时溶液中以HCO-
为主,还有少量的碳酸根离子和碳酸分子,B
3
正确;实验Ⅱ发生反应:Na CO+BaSO NaSO +BaCO ,平衡常数K=
2 3 4 2 4 3
c(SO2-) c(SO2-)c(Ba2+) K (BaSO ) 1.1×10-10 11
4 = 4 = sp 4 = = ,C正确;该反应:CO2- (aq)
c(CO2-) c(CO2-)c(Ba2+) K (BaCO ) 2.6×10-9 260 3
3 3 sp 3
+BaSO (s)
SO2-
(aq)+BaCO (s)可看作气体平衡反应中的等体积类型,增大NaCO 溶液浓度,等同
4 4 3 2 3
于等体积气体反应中的增大压强,平衡不移动,Na CO 转化率不变,D错误。
2 3
题组二 滴定图像的分析
3.(2024·吉林延边一模)室温下,等物质的量的HA与强碱MOH混合,得到MA悬浊液,静置,取上层清
液,通入HCl(g),混合溶液中pH与c(HA)的关系如图。已知:K (MA)=4.9×10-5、K(HA)=2.0×10-6。下
sp a
列说法错误的是( )
A.pH=7时,c(M+)=c(A-)+c(Cl-)
c(M+)
B.a→b的溶液中 将逐渐增大
c(A-)
C.上层清液中c(A-)=7.0×10-3 mol·L-1
D.c(HA)=c(A-)时,c(Cl-)c(ClO-)>c(Cl-)>c(H+)
D.氯水中存在平衡:Cl (aq)+H O(l) H+(aq)+Cl-(aq)+HClO(aq),该反应的平衡常数K约为10-5
2 2
答案:D
解析:氯水中存在Cl(aq)+H O(l) H+(aq)+Cl-(aq)+HClO(aq),从图中可以看出,用NaOH溶液滴定氯
2 2
水,滴定过程中有两个突变点,则从甲到乙,主要发生HCl与NaOH的反应,平衡正向移动,此时溶液中
不再有氯气;从乙到pH=10的点,主要发生HClO与NaOH的反应,总反应为Cl+2NaOH
2
NaCl+NaClO+H O,溶液中氯原子总物质的量为10 mL×0.1 mol·L-1=10-3 mol。由分析可知,甲到乙发
2
生的非氧化还原反应主要为H++OH- HO,A错误;甲到丙的过程中,氯气与水反应的产物不断与
2
NaOH发生反应,水的电离程度一直增大;从丙到丁的过程中,溶液中c(NaOH)不断增大,对水电离的抑
制作用不断增大,水的电离程度不断减小,B错误;丙点为NaCl、NaClO、HClO混合溶液,且溶质的物
质的量有:n(NaCl)>n(NaClO)>n(HClO),所以c(Na+)>c(Cl-)>c(ClO-)>c(H+),C错误;氯水中存在平
衡:Cl (aq)+H O(l) H+(aq)+Cl-(aq)+HClO(aq),pH=10时,Cl 与NaOH刚好完全反应,由Cl+2NaOH
2 2 2 2
NaCl+NaClO+H O,可求出n (Cl)=2×0.001 mol=2×10-3 mol,根据起点pH=2,则氯水中有
2 总
c(H+)≈c(Cl-)≈c(HClO)≈0.01 mol·L-1,n(Cl-)+n(HClO)=0.01 mol·L-1×2×10 mL=2×10-4 mol,n(Cl )=(2×10-3
29×10-4mol
mol-2×10-4 mol)÷2=9×10-4 mol,c(Cl )= =9×10-2 mol·L-1,该反应的平衡常数K≈
2
10 mL
c(H+)×c(HClO)×c(Cl-) 10-2×10-2×10-2
= ≈10-5,D正确。
c(Cl ) 9×10-2
2
题组三 对数图像的分析
5.已知KCr O 溶液中存在如下平衡:
2 2 7
CrO2- (aq)+H O(l) 2HCrO- (aq) K =3.0×10-2
2 7 2 4 1
HCrO- (aq) CrO2- (aq)+H+(aq) K =3.0×10-7
4 4 2
常温下,0.1 mol·L-1 K Cr O 溶液中
2 2 7
c(CrO2-)
4
lg 随溶液pH的变化关系如图所示。下列说法错误的是( )
c(Cr O2-)
2 7
c2(CrO2-)
4
A.将KCr O 溶液加水稀释,溶液颜色变浅且 增大
2 2 7 c(Cr O2-)
2 7
B.溶液中存在c(CrO2- )+c(HCrO- )+c(CrO2-
)<0.2 mol·L-1
2 7 4 4
C.当c(HCrO- )=c(CrO2- )时,有c(K+)>c(CrO2- )>c(CrO2-
)>c(OH-)>c(H+)
4 4 2 7 4
D.pH=8.8时,溶液中c(HCrO-
)=9.0×10-4 mol·L-1
4
答案:C
解析:由CrO2-
(aq)+H O(l)
2HCrO- (aq)和HCrO-
(aq)
CrO2- (aq)+H+(aq)得,CrO2-
(aq)+H O(l)
2 7 2 4 4 4 2 7 2
c2(CrO2-)c2(H+)
2CrO2- (aq)+2H+(aq) K= 4 =K K2 =2.7×10-15。加水稀释,溶液颜色变浅,c(H+)
4 c(Cr O2-) 1 2
2 7
c2(CrO2-)
K
减小,又 4 = ,比值增大,由元素守恒得,2c(CrO2- )+c(HCrO- )+c(CrO2- )=0.2
c(Cr O2-) c2(H+) 2 7 4 4
2 7
mol·L-1,故c(CrO2- )+c(HCrO- )+c(CrO2-
)<0.2
mol·L-1,A、B正确;当c(HCrO- )=c(CrO2-
)时,
2 7 4 4 4 4
c2(CrO2-)
K
c(H+)=3.0×10-7 mol·L-1,显然c(OH-)c(CrO2- )>c(CrO2-
)>c(H+)>c(OH-),C错误;pH=8.8时,
2 7 4
c(CrO2-) K K
4 = 1 2 =103.8,解得c(HCrO- )=9.0×10-4 mol·L-1,D正确。
c(Cr O2-) c(H+)c(HCrO-) 4
2 7 4
6.(2024·四川宜宾一模)25 ℃时,用NaOH溶液分别滴定HX、CuSO 、MgSO 三种溶液,pM[p表示负
4 4
c(HX)
对数,M表示 、c(Cu2+)、c(Mg2+)等]随pH变化关系如图所示,已知
c(X-)
K [Cu(OH) ]c(HX)
C.③代表滴定CuSO 溶液的变化关系
4
D.Mg(OH) 易溶于HX溶液中
2
答案:C
c(HX) c(HX)
解析:pM[p表示负对数,M表示 、c(Cu2+)、c(Mg2+)等],随着pH不断增大,溶液中的 、
c(X-) c(X-)
c(Cu2+)、c(Mg2+)不断减小,即pM增大,K [Cu(OH) ]c(HX),故B正确;由分析可知,曲线③代表MgSO ,故C错误;pH=8.6时,-
4
10-14
lgc(Mg2+)=0,c(Mg2+)=1 mol·L-1,K [Mg(OH) ]=c2(OH-)c(Mg2+)=c2(OH-)=( )2=10-10.8,假设Mg(OH)
sp 2 10-8.6 2
易溶于HX溶液中,则有反应Mg(OH) +2HX Mg2++2X-+2H O,该反应的平衡常数K=
2 2
K [Mg(OH) ][K (HX)]2 10-10.8(10-5)2
sp 2 a = =107.2,平衡常数越大,反应越彻底,所以
(K )2 (10-14)2
W
Mg(OH) 易溶于HX溶液中,故D正确。
2c(H R2-)
7.(2024·福建龙岩一模)室温下,将盐酸滴入NaR溶液中,测得混合溶液的pH与-lg 、
3 c(R3-)
c(H R-) c(H R)
-lg 2 或-lg 3 的关系如图所示。下列说法错误的是( )
c(H R2-) c(H R-)
2
c(H R)
3
A.L 表示pH与-lg 的关系曲线
3 c(H R-)
2
B.Na HR溶液呈碱性
2
C.水解常数 K 的数量级为10-12
h
3
D.混合溶液的pH=7时,c(Na+)>c(H R-)+
2
2c(HR2-)+3c(R3-)
答案:C
解析:25 ℃时,K (H R)=
a 3
1
c(H+)·c(H R-) c(H+)·c(H R2-) c(H+)·c(R3-)
2 >K = >K = ,则溶液pH相同时,
c(H R) a 2 c(H R-) a 3 c(H R2-)
3 2
c(H R) c(H R-) c(H R2-) c(H R)
3 < 2 < ,函数-lgx为减函数,值越小说明分式越大,则-lg 3 >-lg
c(H R-) c(H R2-) c(R3-) c(H R-)
2 2
c(H R-) c(H R2-) c(H R2-)
2 >-lg ,所以L 表示pH与-lg 的关系曲线,L 表示pH与-lg
c(H R2-) c(R3-) 1 c(R3-) 2
c(H R-) c(H R)
2 的关系曲线,L 表示pH与-lg 3 的关系曲线。根据分析可知:L 表示pH与-lg
c(H R2-) 3 c(H R-) 3
2
c(H R) c(H R2-)
3
的关系曲线,A正确;L 曲线表示pH与-lg 的关系曲线,在溶液pH=8时,-lg
c(H R-) 1 c(R3-)
2
c(H R2-) c(H R2-) c(R3-) c(H+)·c(R3-)
=-5.2,则 =105.2, =10-5.2,K = =10-8×10-5.2=10-
c(R3-) c(R3-) c(H R2-) a 3 c(H R2-)
c(H R-) c(H R2-) c(H R2-)
13.2;L 表示pH与-lg 2 的关系曲线,在pH=7.1时,-lg =0, =1,c(H+)=10-7.1
2 c(H R2-) c(H R-) c(H R-)
2 2
c(H+)·c(H R2-) K 10-14
mol·L-1,K = =10-7.1,K = W = =10-6.9,K c(H R-)+2c(HR2-)+3c(R3-),D正确。
2 2
题组四 分布分数图像分析
8.(2024·湖北卷)CO 气氛下,Pb(ClO ) 溶液中含铅物种的分布如图。纵坐标(δ)为组分中铅占总铅的质
2 4 2
量分数。已知c(Pb2+)=2.0×10-5 mol·L-1,pK (H CO)=6.4、pK (H CO)=10.3,
0 a 2 3 a 2 3
1 2
pK (PbCO )=12.1。下列说法错误的是( )
sp 3
A.pH=6.5时,溶液中c(CO2-
)50%,即c(Pb2+)>1×10-5
mol·L-1,则c(CO2-
)<
3
K (PbCO ) 10-12.1
sp 3 = mol·L-1=10-7.1 mol·L-12n(Pb2+)
4 3 3 2 4
+2n[Pb(OH)+]+2n[Pb(CO )2- ],故c(ClO- )>2c(Pb2+)+2c[Pb(OH)+]+2c[Pb(CO )2- ],即2c(Pb2+)+c[Pb(OH)
3 2 4 3 2
+]<2c(CO2- )+c(HCO- )+c(ClO-
),C正确;NaHCO
溶液中HCO-
的水解平衡常数为
3 3 4 3 3
K 1×10-14
W = =10-7.6>K (H CO),NaHCO 溶液呈碱性,K (H CO)·K (H CO)=
K (H CO ) 10-6.4 a 2 2 3 3 a 1 2 3 a 2 2 3
a 2 3
1
c2(H+)·c(CO2-)
3 ,由于HCO- 的水解和电离都是微弱的,则NaHCO 溶液的pH约为
c(H CO ) 3 3
2 3pK (H CO )+pK (H CO )
a 2 3 a 2 3
1 2 =8.35,说明加入少量NaHCO 固体,溶液pH稍有增大,由题图可
3
2
知,当pH由8稍微增大时,PbCO 的物质的量也略有增加,即PbCO 不会溶解,D错误。
3 3