文档内容
选择题标准练(一)
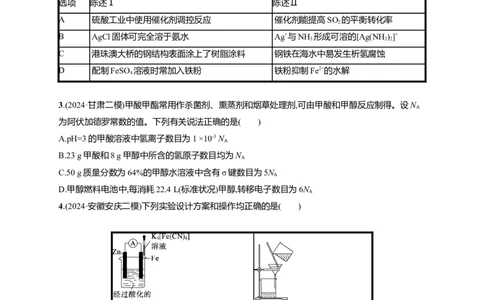
1.(2024·江苏泰州一模调研)下列物质的结构、性质、用途具有对应关系的是( )
A.浓硫酸具有脱水性,可用于干燥Cl
2
B.ClF 具有强氧化性,可用作火箭助燃剂
3
C.冰晶石微溶于水,可用作电解铝工业的助熔剂
D.HF分子之间形成氢键,HF(g)的热稳定性比HCl(g)的高
2.(2024·广东大亚湾区1月联合模拟)下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A 硫酸工业中使用催化剂调控反应 催化剂能提高SO 的平衡转化率
2
B AgCl固体可完全溶于氨水 Ag+与NH 形成可溶的[Ag(NH)]+
3 3 2
C 港珠澳大桥的钢结构表面涂上了树脂涂料 钢铁在海水中易发生析氢腐蚀
D 配制FeSO 溶液时常加入铁粉 铁粉抑制Fe2+的水解
4
3.(2024·甘肃二模)甲酸甲酯常用作杀菌剂、熏蒸剂和烟草处理剂,可由甲酸和甲醇反应制得。设N
A
为阿伏加德罗常数的值。下列有关说法正确的是( )
A.pH=3的甲酸溶液中氢离子数目为1 ×10-3 N
A
B.23 g甲酸和8 g甲醇中所含的氢原子数目均为N
A
C.50 g质量分数为64%的甲醇水溶液中含有σ键数目为5N
A
D.甲醇燃料电池中,每消耗22.4 L(标准状况)甲醇,转移电子数目为6N
A
4.(2024·安徽安庆二模)下列实验设计方案和操作均正确的是( )
A.验证铁电极是否受到保护 B.分离苯酚和水的混合物
C.析出[Cu(NH )]SO ·H O晶体 D.测定KI溶液的浓度
3 4 4 25.(2024·安徽黄山二模)下列有关离子方程式的书写正确的是( )
A.侯氏制碱法中制备NaHCO :NH+CO +H O
HCO- +NH+
3 3 2 2 3 4
B.酸性条件下催化电解CO 制CHCHOH的阴极电极反应式为2CO+12e-+12H+
2 3 2 2
CHCHOH+3H O
3 2 2
C.向苯酚钠溶液中通入少量二氧化碳:
O2-
2 +CO +H O 2 +C 3
2 2
D.碳酸铵溶液与氢氧化钙溶液反应:CO2-
+Ca2+ CaCO ↓
3 3
6.(2024·甘肃二模)离子液体一般指在室温或接近室温下呈液态的由离子构成的物质,主要包括室温
熔融盐、有机离子液体等。有机盐C HNH NO 属于离子液体,它的熔点只有12 ℃。下列说法正确
2 5 3 3
的是 ( )
A.C HNH NO 中只存在离子键
2 5 3 3
B.大多数离子液体由体积差距很大的阴、阳离子构成
C.NH
和NO-
的中心原子杂化方式相同
3 3
D.离子液体熔化时克服的是分子间作用力,所以熔点较低
7.(2024·江西九江十校第二次联考)维生素B 是一种吡啶衍生物,是维持蛋白质正常代谢的必要维生
6
素,其结构简式如下。已知:吡啶( )与苯类似,也具有芳香性。下列有关维生素B 说法正确的是
6
( )
A.该物质属于芳香烃
B.可发生取代反应和加成反应
C.碳原子不能同时在一个平面
D.1 mol该物质最多消耗3 mol NaOH
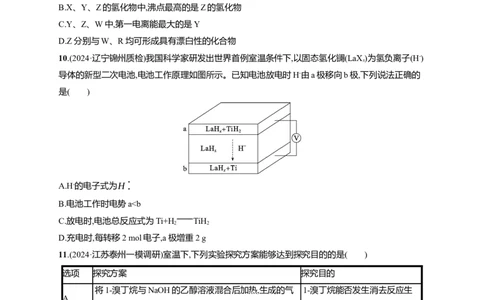
8.(2024·江西南昌一模)氯及其化合物种类繁多,部分含氯物质如图所示。下列说法错误的是( )
A.a与d的水溶液不能共存B.d与f都可以用于杀菌消毒
C.e的氧化性比h强
D.b与g反应可得c,每转移N 个电子可制得0.6 mol c(设N 代表阿伏加德罗常数的值)
A A
9.(2024·辽宁锦州质检)X、Y、Z、W、R为原子序数依次增大的前20号元素,X元素的s轨道电子数
是p轨道电子数的2倍,Z元素的最外层电子数是次外层电子数的3倍,常温下,0.05 mol·L-1 W的最高
价氧化物对应的水化物溶液中,由水电离出的c(OH-)为10-13 mol·L-1,R是前20号元素中电负性最小的
元素。下列说法错误的是( )
A.简单离子半径:Rv(b)
C.其他条件相同,在T 温度下,起始时向该容器中充入一定量的氮气,则反应达到平衡的时间小于t
1 1
0.05
D.在T 温度下,反应在0~t 内的平均速率为v(HOCHCHOH)= mol·L-1·s-1
2 2 2 2 4t
2
选择题标准练(一)
1.(2024·江苏泰州一模调研)下列物质的结构、性质、用途具有对应关系的是( )
A.浓硫酸具有脱水性,可用于干燥Cl
2
B.ClF 具有强氧化性,可用作火箭助燃剂
3
C.冰晶石微溶于水,可用作电解铝工业的助熔剂
D.HF分子之间形成氢键,HF(g)的热稳定性比HCl(g)的高
答案:B
解析:浓硫酸可用于干燥Cl,是因为其具有吸水性,A错误;ClF 具有强氧化性,可氧化燃料,可用作火箭
2 3
助燃剂,B正确;冰晶石可用作电解铝工业的助熔剂是因为其可以降低氧化铝的熔点,与其微溶于水的性质无关,C错误;HF(g)的热稳定性比HCl(g)的高,是因为H—F键能大于H—Cl键能,与HF分子之间
形成氢键的性质无关,D错误。
2.(2024·广东大亚湾区1月联合模拟)下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A 硫酸工业中使用催化剂调控反应 催化剂能提高SO 的平衡转化率
2
B AgCl固体可完全溶于氨水 Ag+与NH 形成可溶的[Ag(NH)]+
3 3 2
C 港珠澳大桥的钢结构表面涂上了树脂涂料 钢铁在海水中易发生析氢腐蚀
D 配制FeSO 溶液时常加入铁粉 铁粉抑制Fe2+的水解
4
答案:B
解析:催化剂不能提高平衡转化率,故硫酸工业中使用催化剂调控反应是为了加快反应速率,A错
误;Ag+与NH 形成可溶的[Ag(NH)]+,故AgCl固体可完全溶于氨水,B正确;钢铁在海水中易发生吸氧
3 3 2
腐蚀,C错误;FeSO 溶液易发生氧化,配制FeSO 溶液时常加入铁粉,主要是抑制亚铁离子的氧化,D错
4 4
误。
3.(2024·甘肃二模)甲酸甲酯常用作杀菌剂、熏蒸剂和烟草处理剂,可由甲酸和甲醇反应制得。设N
A
为阿伏加德罗常数的值。下列有关说法正确的是( )
A.pH=3的甲酸溶液中氢离子数目为1 ×10-3 N
A
B.23 g甲酸和8 g甲醇中所含的氢原子数目均为N
A
C.50 g质量分数为64%的甲醇水溶液中含有σ键数目为5N
A
D.甲醇燃料电池中,每消耗22.4 L(标准状况)甲醇,转移电子数目为6N
A
答案:B
解析:该甲酸溶液体积未知,无法计算氢离子数目,A错误;1个甲酸分子含有2个H原子,23 g甲酸即
0.5 mol甲酸含有1 mol H原子,1个甲醇分子含有4个H原子,8 g甲醇即0.25 mol甲醇含有1 mol H
原子,B正确;50 g质量分数为64%的甲醇水溶液中,m(CHOH)=32 g,m(H O)=18 g,各为1 mol,1 mol
3 2
CHOH中σ键数目为5N ,1 mol HO中σ键数目为2N ,因此50 g该溶液中σ键数目为7N ,C错误;
3 A 2 A A
标准状况下,甲醇为液体,D错误。
4.(2024·安徽安庆二模)下列实验设计方案和操作均正确的是( )A.验证铁电极是否受到保护 B.分离苯酚和水的混合物
C.析出[Cu(NH )]SO ·H O晶体 D.测定KI溶液的浓度
3 4 4 2
答案:C
解析:在酸化的氯化钠溶液中,可能会有少量铁与氢离子反应生成亚铁离子,所以不能用此装置来验证
铁电极是否受到保护,A错误;室温下苯酚在水中的溶解度是9.2 g,不能用过滤的方法分离,B错误;
[Cu(NH )]SO ·H O在乙醇中的溶解度比在水中的要小,因此向[Cu(NH )]SO 溶液中加入乙醇,将析
3 4 4 2 3 4 4
出深蓝色晶体[Cu(NH )]SO ·H O,C正确;溴水具有氧化性,能腐蚀橡胶,不能用碱式滴定管盛装,应用
3 4 4 2
酸式滴定管盛装,D错误。
5.(2024·安徽黄山二模)下列有关离子方程式的书写正确的是( )
A.侯氏制碱法中制备NaHCO :NH+CO +H O
HCO- +NH+
3 3 2 2 3 4
B.酸性条件下催化电解CO 制CHCHOH的阴极电极反应式为2CO+12e-+12H+
2 3 2 2
CHCHOH+3H O
3 2 2
C.向苯酚钠溶液中通入少量二氧化碳:
O2-
2 +CO +H O 2 +C 3
2 2
D.碳酸铵溶液与氢氧化钙溶液反应:CO2-
+Ca2+ CaCO ↓
3 3
答案:B
解析:侯氏制碱法中制备碳酸氢钠的反应为二氧化碳与氨气和氯化钠溶液反应生成碳酸氢钠沉淀和
氯化铵,反应的离子方程式为Na++NH+CO +H O NaHCO
↓+NH+
,A错误;酸性条件下催化电解二
3 2 2 3 4
氧化碳制乙醇时,通入二氧化碳的电极为电解池的阴极,酸性条件下二氧化碳在阴极得到电子发生还
原反应生成乙醇和水,电极反应式为2CO+12e-+12H+ CHCHOH+3H O,B正确;苯酚钠溶液与少
2 3 2 2
量二氧化碳反应生成苯酚和碳酸氢钠,反应的离子方程式为 +CO +H O
2 2
O-
+HC 3,C错误;碳酸铵溶液与氢氧化钙溶液反应生成碳酸钙沉淀、一水合氨,反应的离
子方程式为CO2- +2NH+
+Ca2++2OH- CaCO ↓+2NH·H O,D错误。
3 4 3 3 26.(2024·甘肃二模)离子液体一般指在室温或接近室温下呈液态的由离子构成的物质,主要包括室温
熔融盐、有机离子液体等。有机盐C HNH NO 属于离子液体,它的熔点只有12 ℃。下列说法正确
2 5 3 3
的是 ( )
A.C HNH NO 中只存在离子键
2 5 3 3
B.大多数离子液体由体积差距很大的阴、阳离子构成
C.NH
和NO-
的中心原子杂化方式相同
3 3
D.离子液体熔化时克服的是分子间作用力,所以熔点较低
答案:B
解析:C
HNH+ 与NO-
之间存在离子键,阴、阳离子内部存在共价键,A错误;阴、阳离子体积差距较
2 5 3 3
大,使得阴、阳离子间距离较大,离子键较弱,离子液体在室温或者接近室温会呈现液态,故大多数离
5-1×3
子液体由体积差距很大的阴、阳离子构成,B正确;NH 中心原子N的价层电子对数为3+ =4,
3 2
5+1-2×3
故杂化方式为sp3,NO-
的中心原子N的价层电子对数为3+ =3,杂化方式为sp2,C错误;离
3 2
子液体熔化时克服的是离子键,D错误。
7.(2024·江西九江十校第二次联考)维生素B 是一种吡啶衍生物,是维持蛋白质正常代谢的必要维生
6
素,其结构简式如下。已知:吡啶( )与苯类似,也具有芳香性。下列有关维生素B 说法正确的是
6
( )
A.该物质属于芳香烃
B.可发生取代反应和加成反应
C.碳原子不能同时在一个平面
D.1 mol该物质最多消耗3 mol NaOH
答案:B
解析:维生素B 中不含苯环,不属于芳香烃,A错误;维生素B 中含有羟基可以发生取代反应,吡啶(
6 6
)与苯类似,可发生加成反应,维生素B 是一种吡啶衍生物,故也能发生加成反应,B正确;吡啶(
6
)与苯类似,为平面形分子,维生素B 中碳原子直接连在环上,所以碳原子一定在同一平面上,C
6错误;与吡啶相连的羟基类似于酚羟基,能够与氢氧化钠反应,但醇羟基不与氢氧化钠反应,所以1 mol
该物质最多消耗1 mol NaOH,D错误。
8.(2024·江西南昌一模)氯及其化合物种类繁多,部分含氯物质如图所示。下列说法错误的是( )
A.a与d的水溶液不能共存
B.d与f都可以用于杀菌消毒
C.e的氧化性比h强
D.b与g反应可得c,每转移N 个电子可制得0.6 mol c(设N 代表阿伏加德罗常数的值)
A A
答案:A
解析:a为含有Cl-的盐,d为含有ClO-的盐,Cl-和ClO-在碱性条件下可以大量共存,A错误;d为含有
ClO-的盐,f为ClO ,二者都具有强氧化性,可以用于杀菌消毒,B正确;e为HClO,h为HClO,HClO的氧
2 4
化性比HClO
强,C正确;b为HCl,g为含有ClO- 的盐,两者反应可以生成Cl,离子方程式为ClO-
+6H+
4 3 2 3
+5Cl- 3Cl↑+3H
O,ClO-
中Cl元素由+5价下降到0价,每转移N 个电子,生成0.6 mol Cl ,D正确。
2 2 3 A 2
9.(2024·辽宁锦州质检)X、Y、Z、W、R为原子序数依次增大的前20号元素,X元素的s轨道电子数
是p轨道电子数的2倍,Z元素的最外层电子数是次外层电子数的3倍,常温下,0.05 mol·L-1 W的最高
价氧化物对应的水化物溶液中,由水电离出的c(OH-)为10-13 mol·L-1,R是前20号元素中电负性最小的
元素。下列说法错误的是( )
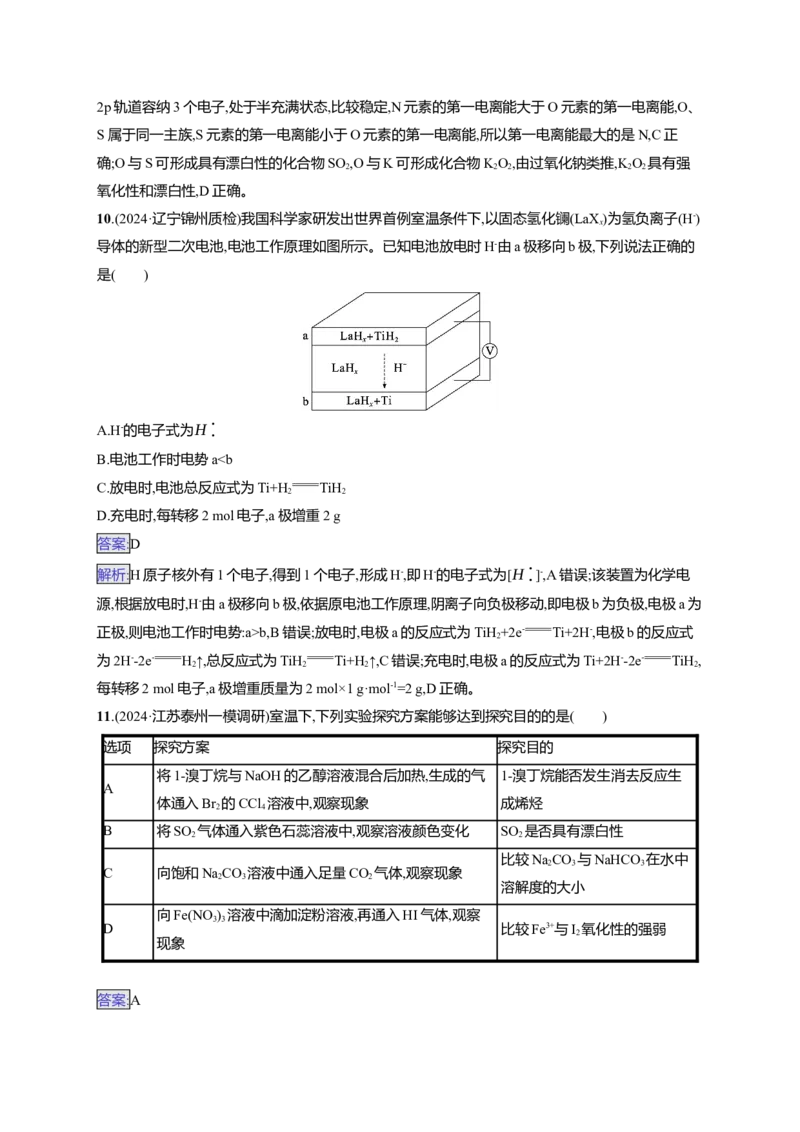
A.简单离子半径:Rb,B错误;放电时,电极a的反应式为TiH +2e- Ti+2H-,电极b的反应式
2
为2H--2e- H↑,总反应式为TiH Ti+H↑,C错误;充电时,电极a的反应式为Ti+2H--2e- TiH ,
2 2 2 2
每转移2 mol电子,a极增重质量为2 mol×1 g·mol-1=2 g,D正确。
11.(2024·江苏泰州一模调研)室温下,下列实验探究方案能够达到探究目的的是( )
选项 探究方案 探究目的
将1-溴丁烷与NaOH的乙醇溶液混合后加热,生成的气 1-溴丁烷能否发生消去反应生
A
体通入Br 的CCl 溶液中,观察现象 成烯烃
2 4
B 将SO 气体通入紫色石蕊溶液中,观察溶液颜色变化 SO 是否具有漂白性
2 2
比较NaCO 与NaHCO 在水中
2 3 3
C 向饱和NaCO 溶液中通入足量CO 气体,观察现象
2 3 2
溶解度的大小
向Fe(NO ) 溶液中滴加淀粉溶液,再通入HI气体,观察
3 3
D 比较Fe3+与I 氧化性的强弱
2
现象
答案:A解析:气体通入Br 的CCl 溶液中,溶液褪色,说明生成了烯烃,则证明发生了消去反应;将SO 气体通
2 4 2
入紫色石蕊溶液中,溶液变红,不能证明二氧化硫有漂白性;向饱和NaCO 溶液中通入足量CO 气体,
2 3 2
有晶体析出,根据NaCO+CO +H O 2NaHCO 分析得到,106 g碳酸钠反应得到168 g碳酸氢钠,生
2 3 2 2 3
成的碳酸氢钠增多,假设溶解度相同时也会有晶体析出,因此不能通过现象来比较NaCO 与NaHCO
2 3 3
在水中溶解度的大小;向Fe(NO ) 溶液中滴加淀粉溶液,再通入HI气体,溶液变蓝,由于硝酸的氧化性
3 3
强于铁离子,可能硝酸氧化了碘离子,因此不能比较Fe3+与I 氧化性的强弱。
2
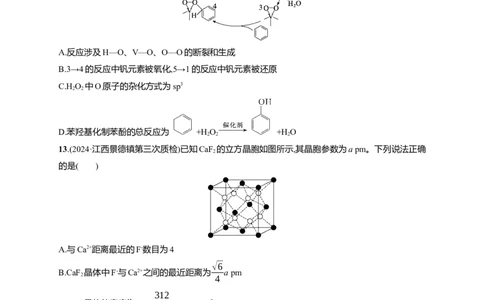
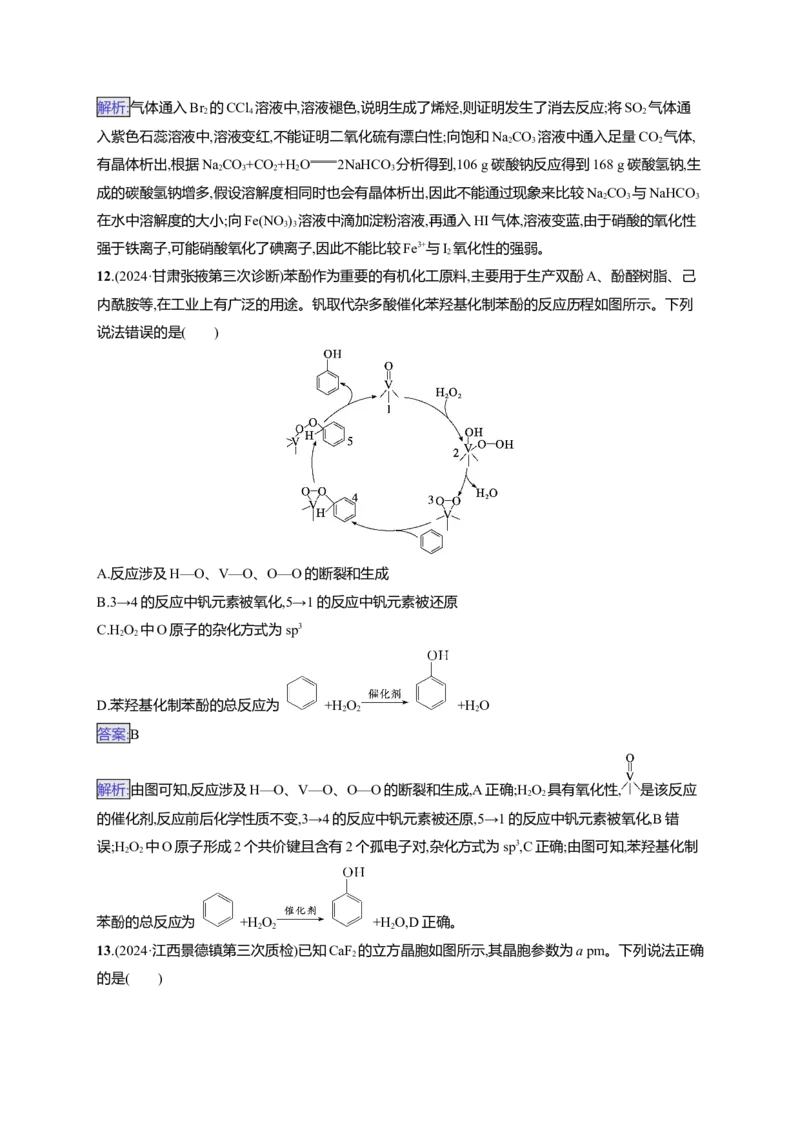
12.(2024·甘肃张掖第三次诊断)苯酚作为重要的有机化工原料,主要用于生产双酚A、酚醛树脂、己
内酰胺等,在工业上有广泛的用途。钒取代杂多酸催化苯羟基化制苯酚的反应历程如图所示。下列
说法错误的是( )
A.反应涉及H—O、V—O、O—O的断裂和生成
B.3→4的反应中钒元素被氧化,5→1的反应中钒元素被还原
C.H O 中O原子的杂化方式为sp3
2 2
D.苯羟基化制苯酚的总反应为 +H O +H O
2 2 2
答案:B
解析:由图可知,反应涉及H—O、V—O、O—O的断裂和生成,A正确;H O 具有氧化性, 是该反应
2 2
的催化剂,反应前后化学性质不变,3→4的反应中钒元素被还原,5→1的反应中钒元素被氧化,B错
误;H O 中O原子形成2个共价键且含有2个孤电子对,杂化方式为sp3,C正确;由图可知,苯羟基化制
2 2
苯酚的总反应为 +H O +H O,D正确。
2 2 2
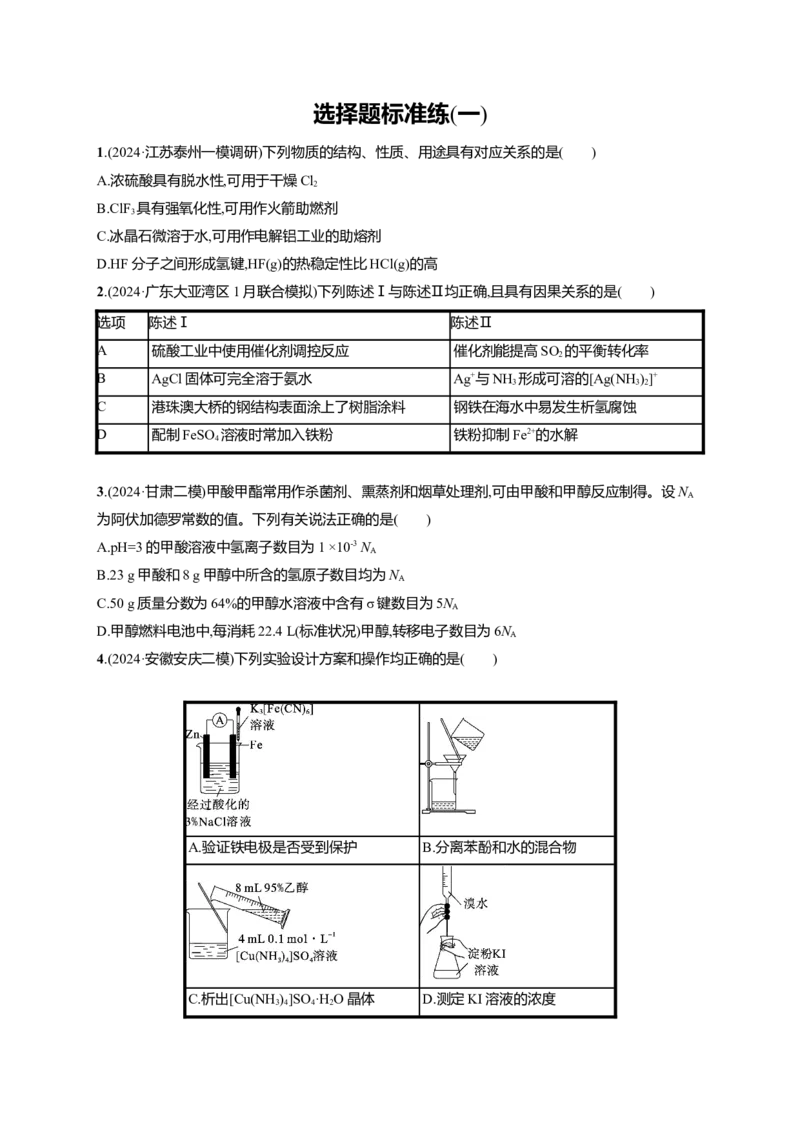
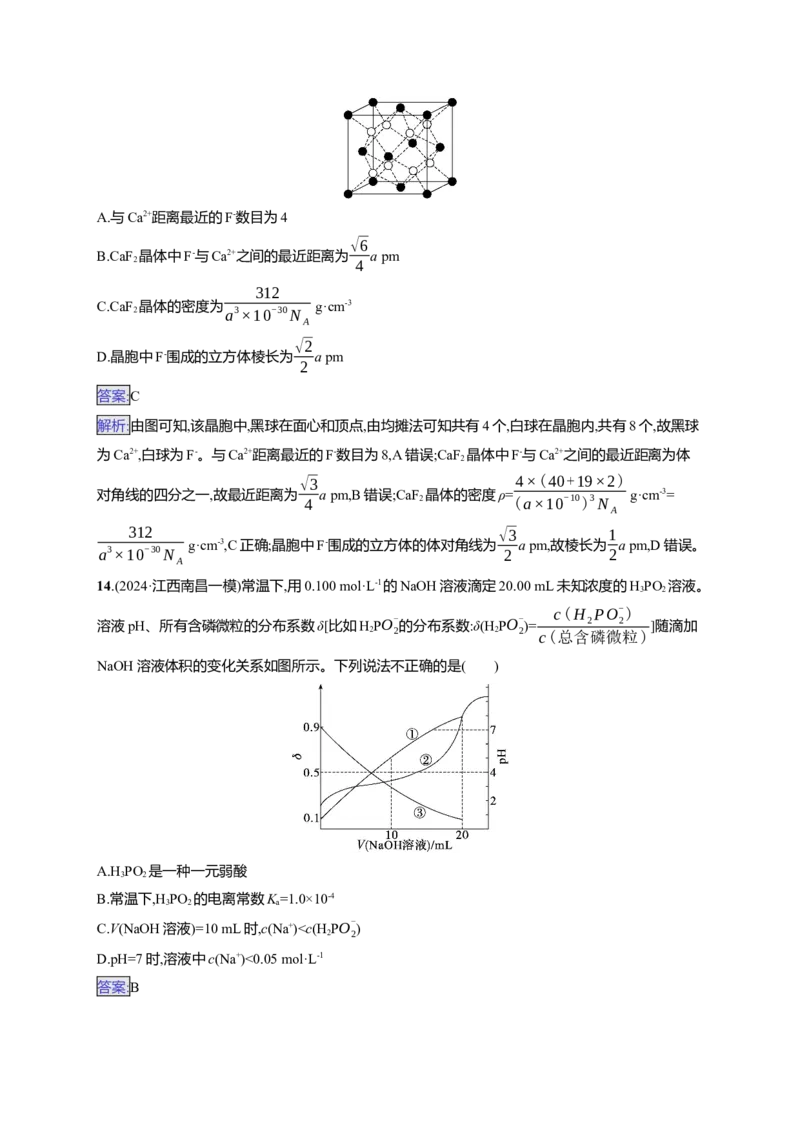
13.(2024·江西景德镇第三次质检)已知CaF 的立方晶胞如图所示,其晶胞参数为a pm。下列说法正确
2
的是( )A.与Ca2+距离最近的F-数目为4
√6
B.CaF 晶体中F-与Ca2+之间的最近距离为 a pm
2 4
312
C.CaF 2 晶体的密度为 a3×10-30N g·cm-3
A
√2
D.晶胞中F-围成的立方体棱长为 a pm
2
答案:C
解析:由图可知,该晶胞中,黑球在面心和顶点,由均摊法可知共有4个,白球在晶胞内,共有8个,故黑球
为Ca2+,白球为F-。与Ca2+距离最近的F-数目为8,A错误;CaF 晶体中F-与Ca2+之间的最近距离为体
2
√3
4×(40+19×2)
对角线的四分之一,故最近距离为 a pm,B错误;CaF 晶体的密度ρ= g·cm-3=
4 2 (a×10-10)3N
A
312 √3 1
g·cm-3,C正确;晶胞中F-围成的立方体的体对角线为 a pm,故棱长为 a pm,D错误。
a3×10-30N 2 2
A
14.(2024·江西南昌一模)常温下,用0.100 mol·L-1的NaOH溶液滴定20.00 mL未知浓度的HPO 溶液。
3 2
c(H PO-)
溶液pH、所有含磷微粒的分布系数δ[比如HPO- 的分布系数:δ(H PO- )= 2 2 ]随滴加
2 2 2 2 c(总含磷微粒)
NaOH溶液体积的变化关系如图所示。下列说法不正确的是( )
A.HPO 是一种一元弱酸
3 2
B.常温下,H PO 的电离常数K=1.0×10-4
3 2 a
C.V(NaOH溶液)=10 mL时,c(Na+)1.0×10-4,B错误;根据图像可知:当
2 a c(H PO )
3 2
V(NaOH)=10 mL时,c(H
PO-
)>c(H PO ),溶液为HPO 与NaH PO 的混合溶液,溶液中存在电荷守恒:
2 2 3 2 3 2 2 2
c(Na+)+c(H+)=c(OH-)+c(H
PO-
),此时溶液pH<7,溶液显酸性,则c(H+)>c(OH-),故c(Na+)v(b)
C.其他条件相同,在T 温度下,起始时向该容器中充入一定量的氮气,则反应达到平衡的时间小于t
1 1
0.05
D.在T 温度下,反应在0~t 内的平均速率为v(HOCHCHOH)= mol·L-1·s-1
2 2 2 2 4t
2
答案:C
解析:反应温度为T 和T,以c(H )随时间t的变化曲线作比较,Ⅱ比Ⅲ先达到平衡,所以T>T,温度升
1 2 2 1 2
高,c(H )增大,平衡逆向移动,逆反应吸热,正反应放热,故ΔH<0,A正确;升高温度,反应速率加快,T>T ,
2 1 2
则反应速率v(a)>v(b),B正确;向恒容容器中充入氮气,不影响反应物浓度,不影响反应速率,C错误;T
2
0.05
时,在0~t 内,Δc(H )=0.05 mol·L-1,则v(HOCHCHOH)= mol·L-1·s-1,D正确。
2 2 2 2 4t
2