文档内容
选择题突破九 B 组 能力提升练
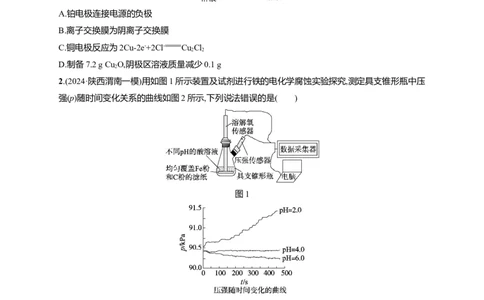
1.(2024·山东临沂一模)电解法制备Cu O的装置如图所示,已知生成Cu O的反应为Cu Cl+2OH-
2 2 2 2
Cu O+HO+2Cl-,下列说法错误的是( )
2 2
A.铂电极连接电源的负极
B.离子交换膜为阴离子交换膜
C.铜电极反应为2Cu-2e-+2Cl- Cu Cl
2 2
D.制备7.2 g Cu O,阴极区溶液质量减少0.1 g
2
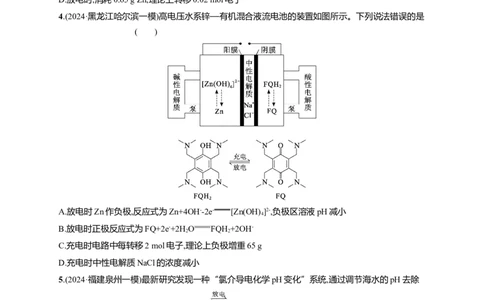
2.(2024·陕西渭南一模)用如图1所示装置及试剂进行铁的电化学腐蚀实验探究,测定具支锥形瓶中压
强(p)随时间变化关系的曲线如图2所示,下列说法错误的是( )
图1
图2
A.pH=2.0时,压强增大是因为生成H
2
B.pH=4.0时,不发生析氢腐蚀,只发生吸氧腐蚀
C.pH=6.0时,正极主要发生电极反应式为O+4e-+4H+ 2HO
2 2
D.整个过程中,负极电极反应式为Fe-2e- Fe2+
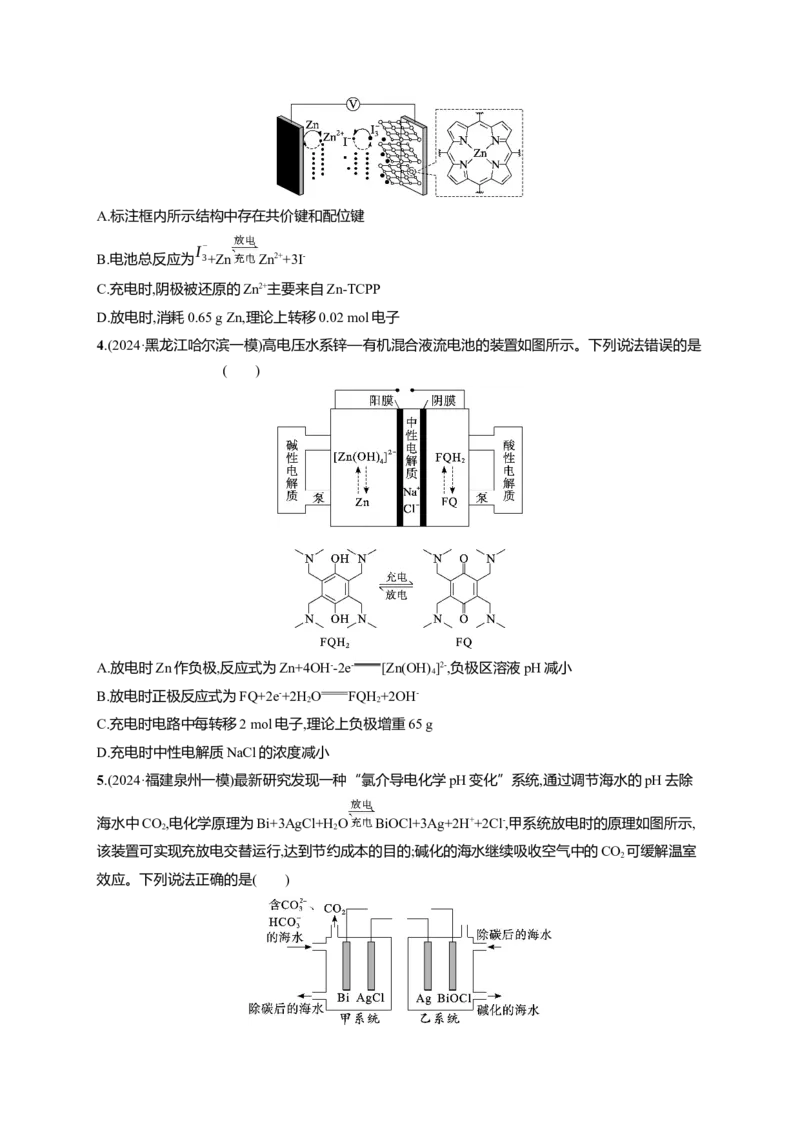
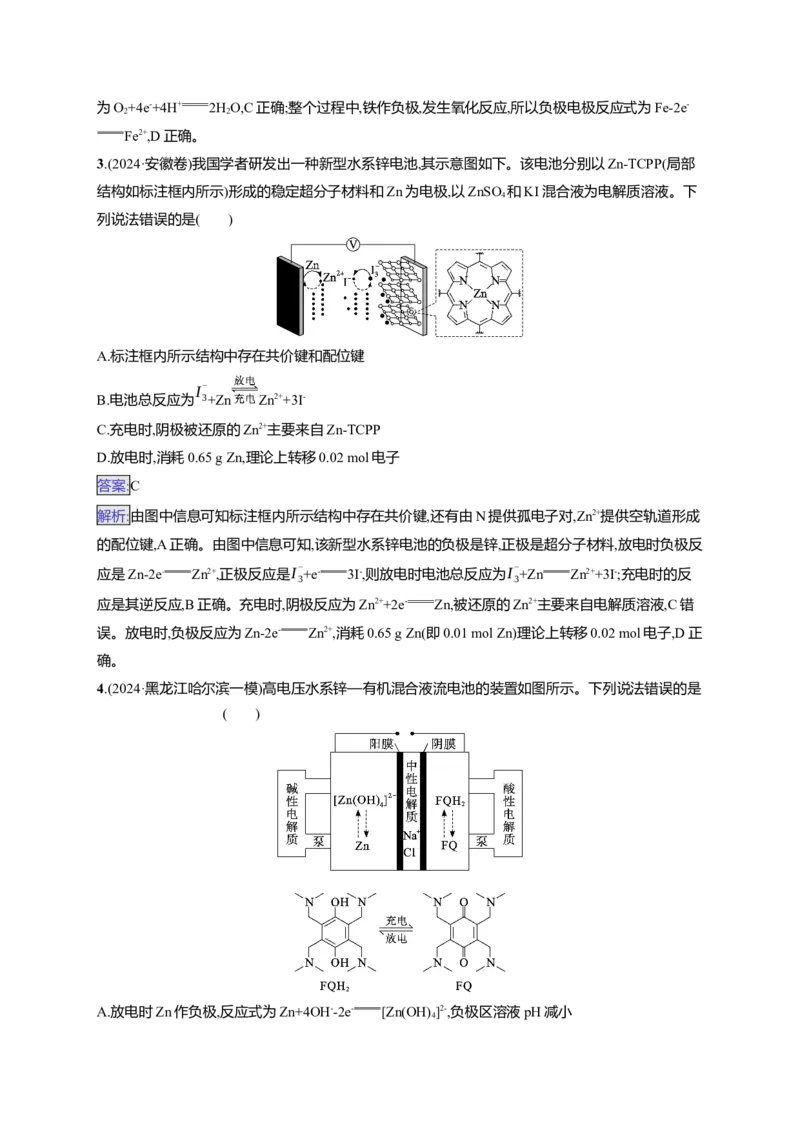
3.(2024·安徽卷)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以Zn-TCPP(局部
结构如标注框内所示)形成的稳定超分子材料和Zn为电极,以ZnSO 和KI混合液为电解质溶液。下
4
列说法错误的是( )A.标注框内所示结构中存在共价键和配位键
I-
B.电池总反应为 3+Zn Zn2++3I-
C.充电时,阴极被还原的Zn2+主要来自Zn-TCPP
D.放电时,消耗0.65 g Zn,理论上转移0.02 mol电子
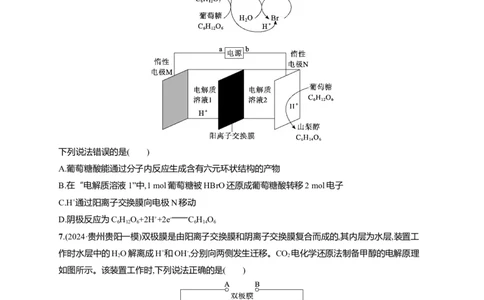
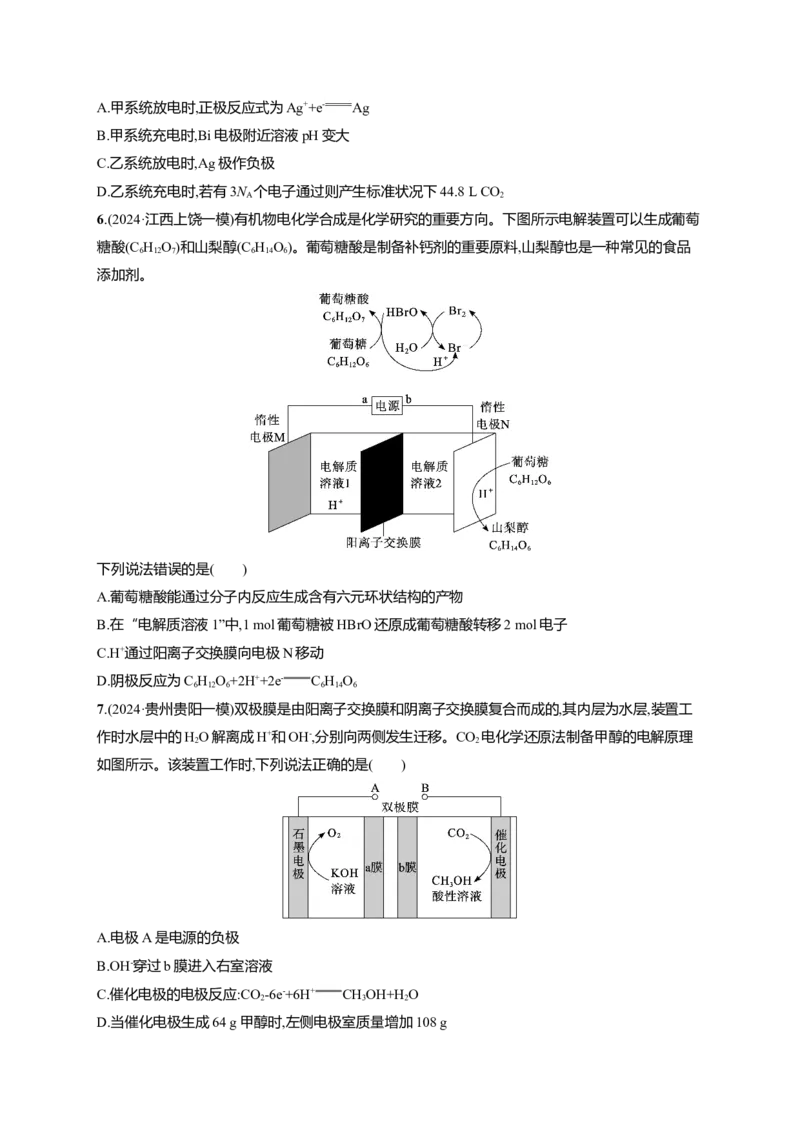
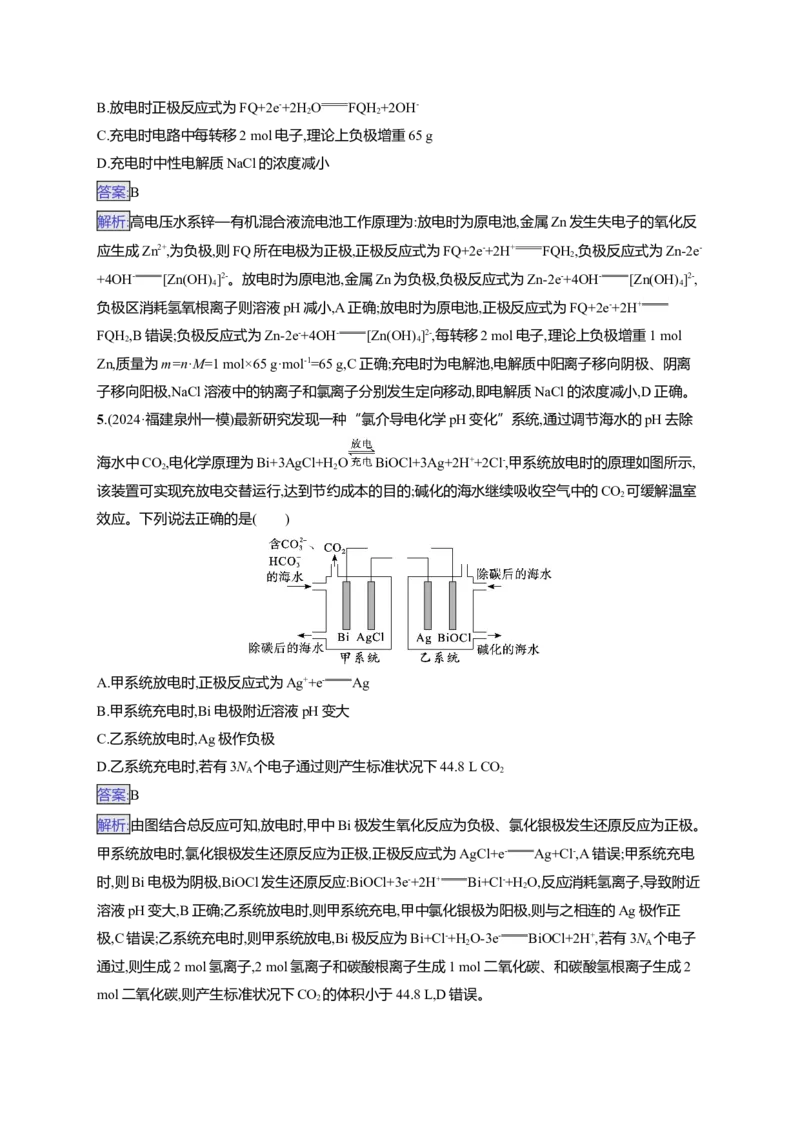
4.(2024·黑龙江哈尔滨一模)高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是
( )
A.放电时Zn作负极,反应式为Zn+4OH--2e- [Zn(OH) ]2-,负极区溶液pH减小
4
B.放电时正极反应式为FQ+2e-+2H O FQH +2OH-
2 2
C.充电时电路中每转移2 mol电子,理论上负极增重65 g
D.充电时中性电解质NaCl的浓度减小
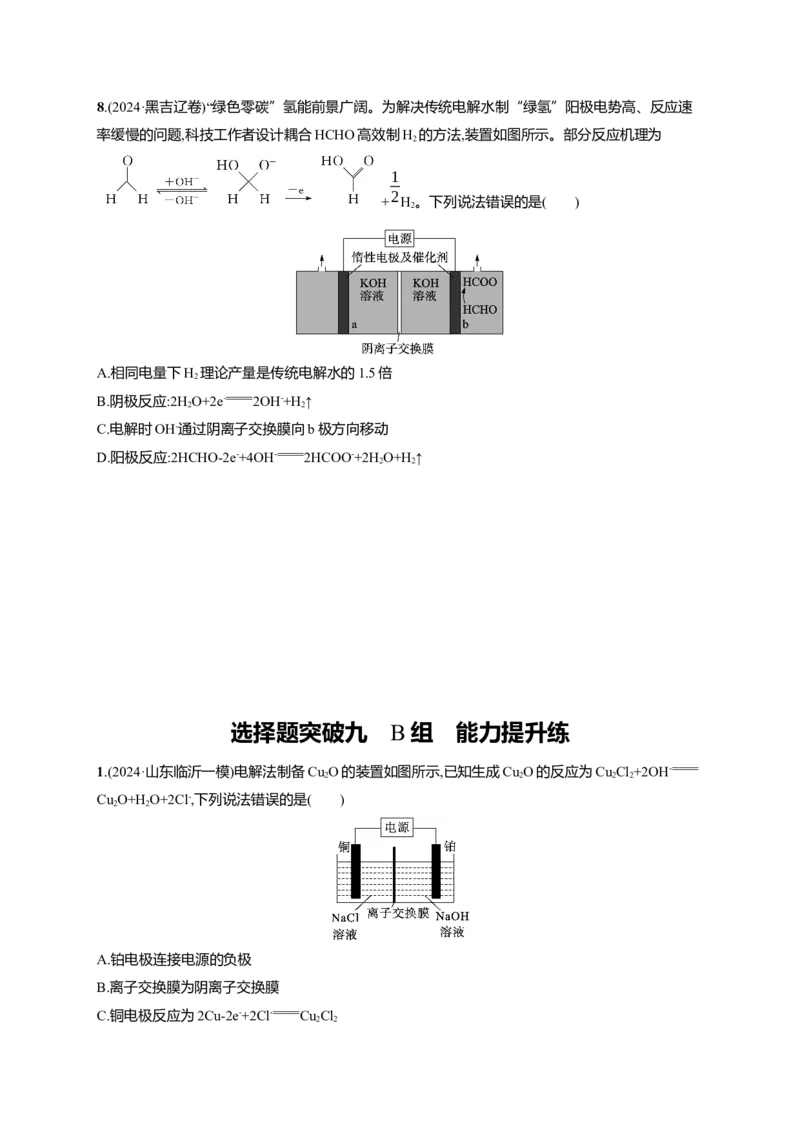
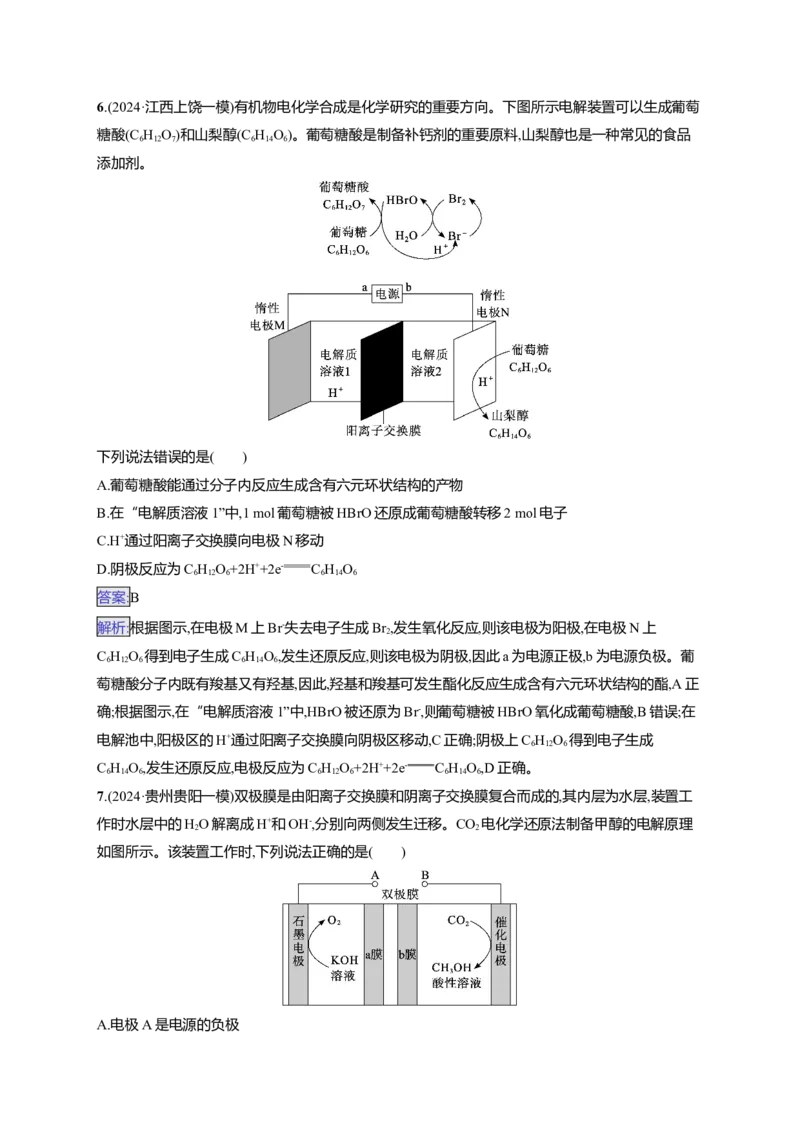
5.(2024·福建泉州一模)最新研究发现一种“氯介导电化学pH变化”系统,通过调节海水的pH去除
海水中CO,电化学原理为Bi+3AgCl+H O BiOCl+3Ag+2H++2Cl-,甲系统放电时的原理如图所示,
2 2
该装置可实现充放电交替运行,达到节约成本的目的;碱化的海水继续吸收空气中的CO 可缓解温室
2
效应。下列说法正确的是( )A.甲系统放电时,正极反应式为Ag++e- Ag
B.甲系统充电时,Bi电极附近溶液pH变大
C.乙系统放电时,Ag极作负极
D.乙系统充电时,若有3N 个电子通过则产生标准状况下44.8 L CO
A 2
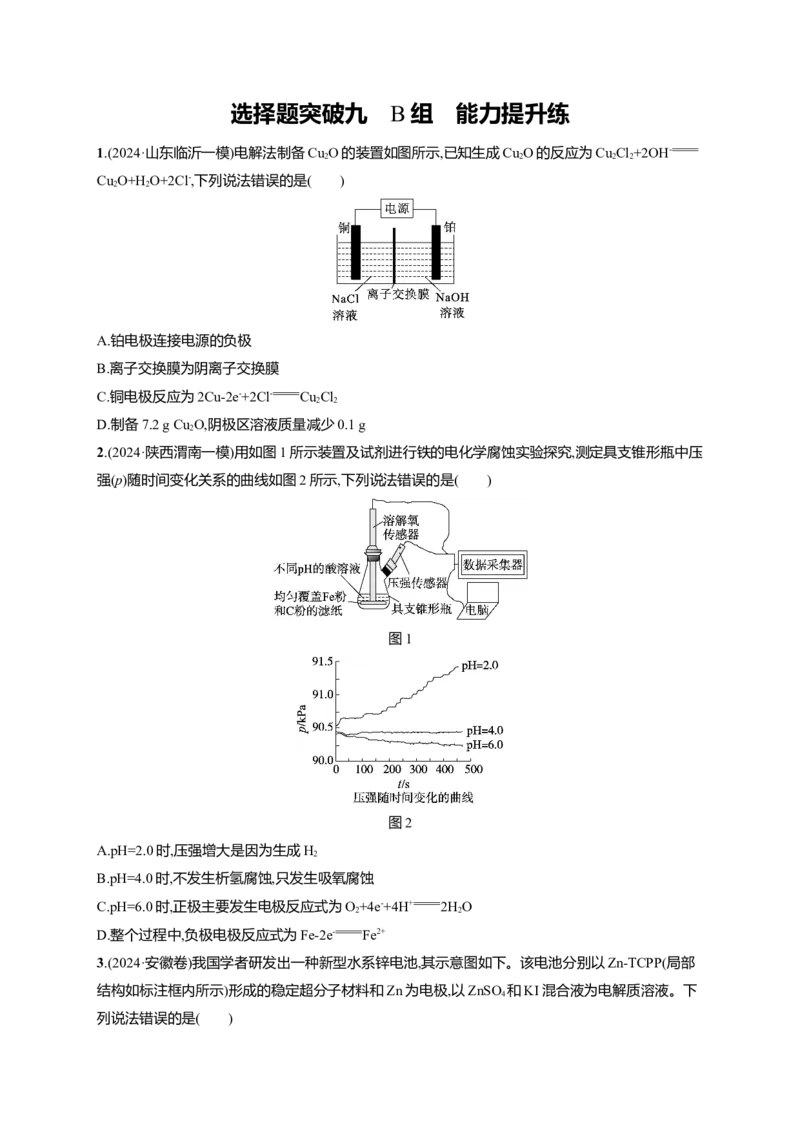
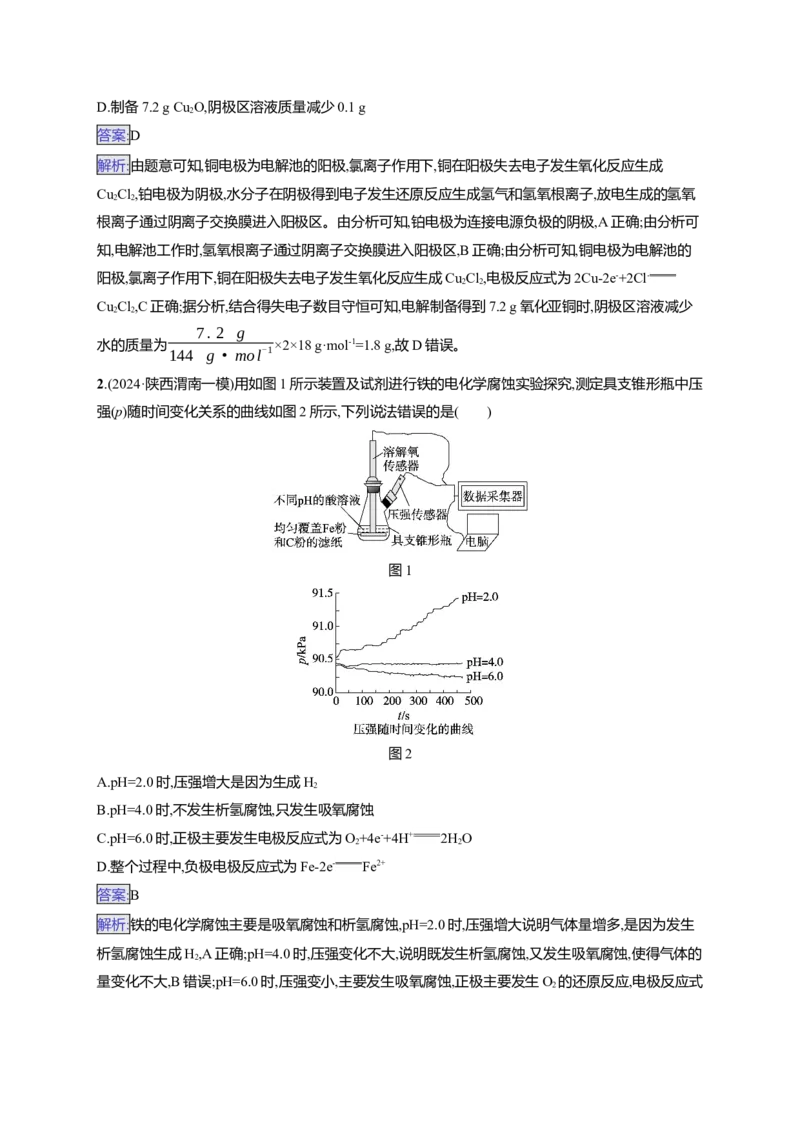
6.(2024·江西上饶一模)有机物电化学合成是化学研究的重要方向。下图所示电解装置可以生成葡萄
糖酸(C H O)和山梨醇(C H O)。葡萄糖酸是制备补钙剂的重要原料,山梨醇也是一种常见的食品
6 12 7 6 14 6
添加剂。
下列说法错误的是( )
A.葡萄糖酸能通过分子内反应生成含有六元环状结构的产物
B.在“电解质溶液1”中,1 mol葡萄糖被HBrO还原成葡萄糖酸转移2 mol电子
C.H+通过阳离子交换膜向电极N移动
D.阴极反应为C H O+2H++2e- C H O
6 12 6 6 14 6
7.(2024·贵州贵阳一模)双极膜是由阳离子交换膜和阴离子交换膜复合而成的,其内层为水层,装置工
作时水层中的HO解离成H+和OH-,分别向两侧发生迁移。CO 电化学还原法制备甲醇的电解原理
2 2
如图所示。该装置工作时,下列说法正确的是( )
A.电极A是电源的负极
B.OH-穿过b膜进入右室溶液
C.催化电极的电极反应:CO -6e-+6H+ CHOH+H O
2 3 2
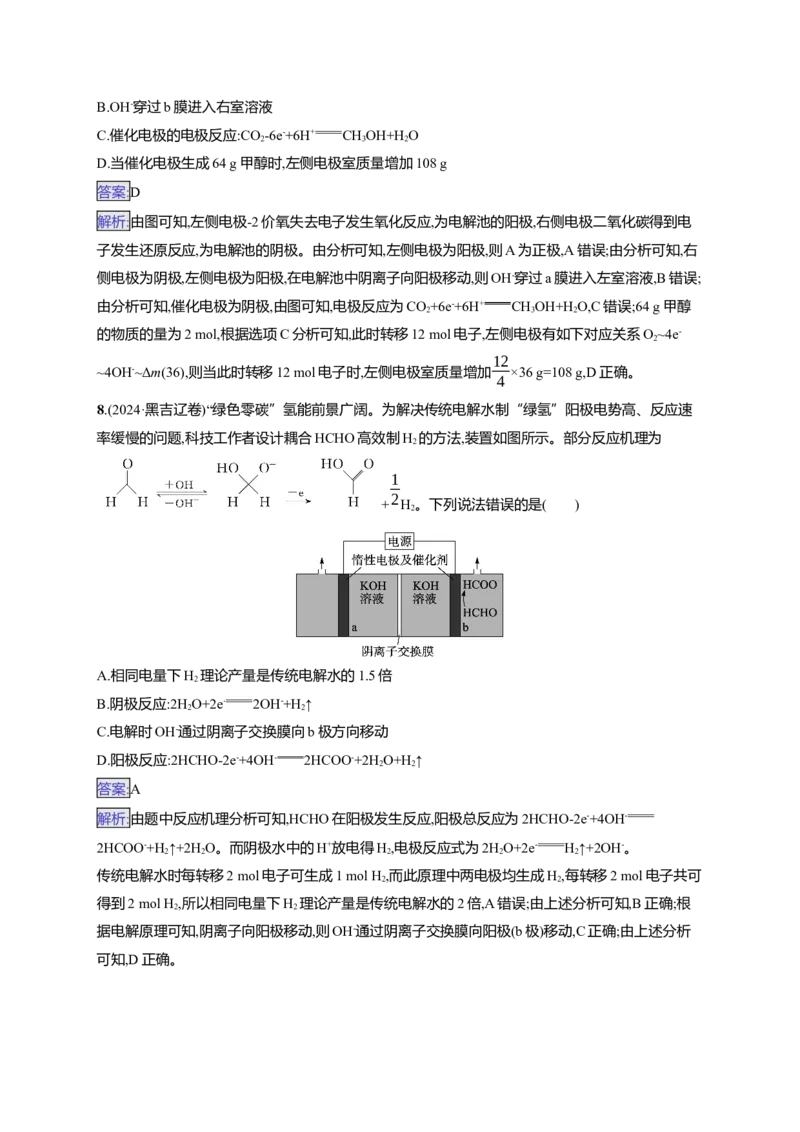
D.当催化电极生成64 g甲醇时,左侧电极室质量增加108 g8.(2024·黑吉辽卷)“绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、反应速
率缓慢的问题,科技工作者设计耦合HCHO高效制H 的方法,装置如图所示。部分反应机理为
2
1
2
+ H。下列说法错误的是( )
2
A.相同电量下H 理论产量是传统电解水的1.5倍
2
B.阴极反应:2H O+2e- 2OH-+H ↑
2 2
C.电解时OH-通过阴离子交换膜向b极方向移动
D.阳极反应:2HCHO-2e-+4OH- 2HCOO-+2H O+H↑
2 2
选择题突破九 B 组 能力提升练
1.(2024·山东临沂一模)电解法制备Cu O的装置如图所示,已知生成Cu O的反应为Cu Cl+2OH-
2 2 2 2
Cu O+HO+2Cl-,下列说法错误的是( )
2 2
A.铂电极连接电源的负极
B.离子交换膜为阴离子交换膜
C.铜电极反应为2Cu-2e-+2Cl- Cu Cl
2 2D.制备7.2 g Cu O,阴极区溶液质量减少0.1 g
2
答案:D
解析:由题意可知,铜电极为电解池的阳极,氯离子作用下,铜在阳极失去电子发生氧化反应生成
Cu Cl,铂电极为阴极,水分子在阴极得到电子发生还原反应生成氢气和氢氧根离子,放电生成的氢氧
2 2
根离子通过阴离子交换膜进入阳极区。由分析可知,铂电极为连接电源负极的阴极,A正确;由分析可
知,电解池工作时,氢氧根离子通过阴离子交换膜进入阳极区,B正确;由分析可知,铜电极为电解池的
阳极,氯离子作用下,铜在阳极失去电子发生氧化反应生成Cu Cl,电极反应式为2Cu-2e-+2Cl-
2 2
Cu Cl,C正确;据分析,结合得失电子数目守恒可知,电解制备得到7.2 g氧化亚铜时,阴极区溶液减少
2 2
7.2 g
水的质量为 ×2×18 g·mol-1=1.8 g,故D错误。
144 g·mol-1
2.(2024·陕西渭南一模)用如图1所示装置及试剂进行铁的电化学腐蚀实验探究,测定具支锥形瓶中压
强(p)随时间变化关系的曲线如图2所示,下列说法错误的是( )
图1
图2
A.pH=2.0时,压强增大是因为生成H
2
B.pH=4.0时,不发生析氢腐蚀,只发生吸氧腐蚀
C.pH=6.0时,正极主要发生电极反应式为O+4e-+4H+ 2HO
2 2
D.整个过程中,负极电极反应式为Fe-2e- Fe2+
答案:B
解析:铁的电化学腐蚀主要是吸氧腐蚀和析氢腐蚀,pH=2.0时,压强增大说明气体量增多,是因为发生
析氢腐蚀生成H,A正确;pH=4.0时,压强变化不大,说明既发生析氢腐蚀,又发生吸氧腐蚀,使得气体的
2
量变化不大,B错误;pH=6.0时,压强变小,主要发生吸氧腐蚀,正极主要发生O 的还原反应,电极反应式
2为O+4e-+4H+ 2HO,C正确;整个过程中,铁作负极,发生氧化反应,所以负极电极反应式为Fe-2e-
2 2
Fe2+,D正确。
3.(2024·安徽卷)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以Zn-TCPP(局部
结构如标注框内所示)形成的稳定超分子材料和Zn为电极,以ZnSO 和KI混合液为电解质溶液。下
4
列说法错误的是( )
A.标注框内所示结构中存在共价键和配位键
I-
B.电池总反应为 3+Zn Zn2++3I-
C.充电时,阴极被还原的Zn2+主要来自Zn-TCPP
D.放电时,消耗0.65 g Zn,理论上转移0.02 mol电子
答案:C
解析:由图中信息可知标注框内所示结构中存在共价键,还有由N提供孤电子对,Zn2+提供空轨道形成
的配位键,A正确。由图中信息可知,该新型水系锌电池的负极是锌,正极是超分子材料,放电时负极反
应是Zn-2e-
Zn2+,正极反应是I-
+e-
3I-,则放电时电池总反应为I-
+Zn Zn2++3I-;充电时的反
3 3
应是其逆反应,B正确。充电时,阴极反应为Zn2++2e- Zn,被还原的Zn2+主要来自电解质溶液,C错
误。放电时,负极反应为Zn-2e- Zn2+,消耗0.65 g Zn(即0.01 mol Zn)理论上转移0.02 mol电子,D正
确。
4.(2024·黑龙江哈尔滨一模)高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是
( )
A.放电时Zn作负极,反应式为Zn+4OH--2e- [Zn(OH) ]2-,负极区溶液pH减小
4B.放电时正极反应式为FQ+2e-+2H O FQH +2OH-
2 2
C.充电时电路中每转移2 mol电子,理论上负极增重65 g
D.充电时中性电解质NaCl的浓度减小
答案:B
解析:高电压水系锌—有机混合液流电池工作原理为:放电时为原电池,金属Zn发生失电子的氧化反
应生成Zn2+,为负极,则FQ所在电极为正极,正极反应式为FQ+2e-+2H+ FQH ,负极反应式为Zn-2e-
2
+4OH- [Zn(OH) ]2-。放电时为原电池,金属Zn为负极,负极反应式为Zn-2e-+4OH- [Zn(OH) ]2-,
4 4
负极区消耗氢氧根离子则溶液pH减小,A正确;放电时为原电池,正极反应式为FQ+2e-+2H+
FQH ,B错误;负极反应式为Zn-2e-+4OH- [Zn(OH) ]2-,每转移2 mol电子,理论上负极增重1 mol
2 4
Zn,质量为m=n·M=1 mol×65 g·mol-1=65 g,C正确;充电时为电解池,电解质中阳离子移向阴极、阴离
子移向阳极,NaCl溶液中的钠离子和氯离子分别发生定向移动,即电解质NaCl的浓度减小,D正确。
5.(2024·福建泉州一模)最新研究发现一种“氯介导电化学pH变化”系统,通过调节海水的pH去除
海水中CO,电化学原理为Bi+3AgCl+H O BiOCl+3Ag+2H++2Cl-,甲系统放电时的原理如图所示,
2 2
该装置可实现充放电交替运行,达到节约成本的目的;碱化的海水继续吸收空气中的CO 可缓解温室
2
效应。下列说法正确的是( )
A.甲系统放电时,正极反应式为Ag++e- Ag
B.甲系统充电时,Bi电极附近溶液pH变大
C.乙系统放电时,Ag极作负极
D.乙系统充电时,若有3N 个电子通过则产生标准状况下44.8 L CO
A 2
答案:B
解析:由图结合总反应可知,放电时,甲中Bi极发生氧化反应为负极、氯化银极发生还原反应为正极。
甲系统放电时,氯化银极发生还原反应为正极,正极反应式为AgCl+e- Ag+Cl-,A错误;甲系统充电
时,则Bi电极为阴极,BiOCl发生还原反应:BiOCl+3e-+2H+ Bi+Cl-+H O,反应消耗氢离子,导致附近
2
溶液pH变大,B正确;乙系统放电时,则甲系统充电,甲中氯化银极为阳极,则与之相连的Ag极作正
极,C错误;乙系统充电时,则甲系统放电,Bi极反应为Bi+Cl-+H O-3e- BiOCl+2H+,若有3N 个电子
2 A
通过,则生成2 mol氢离子,2 mol氢离子和碳酸根离子生成1 mol二氧化碳、和碳酸氢根离子生成2
mol二氧化碳,则产生标准状况下CO 的体积小于44.8 L,D错误。
26.(2024·江西上饶一模)有机物电化学合成是化学研究的重要方向。下图所示电解装置可以生成葡萄
糖酸(C H O)和山梨醇(C H O)。葡萄糖酸是制备补钙剂的重要原料,山梨醇也是一种常见的食品
6 12 7 6 14 6
添加剂。
下列说法错误的是( )
A.葡萄糖酸能通过分子内反应生成含有六元环状结构的产物
B.在“电解质溶液1”中,1 mol葡萄糖被HBrO还原成葡萄糖酸转移2 mol电子
C.H+通过阳离子交换膜向电极N移动
D.阴极反应为C H O+2H++2e- C H O
6 12 6 6 14 6
答案:B
解析:根据图示,在电极M上Br-失去电子生成Br ,发生氧化反应,则该电极为阳极,在电极N上
2
C H O 得到电子生成C H O,发生还原反应,则该电极为阴极,因此a为电源正极,b为电源负极。葡
6 12 6 6 14 6
萄糖酸分子内既有羧基又有羟基,因此,羟基和羧基可发生酯化反应生成含有六元环状结构的酯,A正
确;根据图示,在“电解质溶液1”中,HBrO被还原为Br-,则葡萄糖被HBrO氧化成葡萄糖酸,B错误;在
电解池中,阳极区的H+通过阳离子交换膜向阴极区移动,C正确;阴极上C H O 得到电子生成
6 12 6
C H O,发生还原反应,电极反应为C H O+2H++2e- C H O,D正确。
6 14 6 6 12 6 6 14 6
7.(2024·贵州贵阳一模)双极膜是由阳离子交换膜和阴离子交换膜复合而成的,其内层为水层,装置工
作时水层中的HO解离成H+和OH-,分别向两侧发生迁移。CO 电化学还原法制备甲醇的电解原理
2 2
如图所示。该装置工作时,下列说法正确的是( )
A.电极A是电源的负极B.OH-穿过b膜进入右室溶液
C.催化电极的电极反应:CO -6e-+6H+ CHOH+H O
2 3 2
D.当催化电极生成64 g甲醇时,左侧电极室质量增加108 g
答案:D
解析:由图可知,左侧电极-2价氧失去电子发生氧化反应,为电解池的阳极,右侧电极二氧化碳得到电
子发生还原反应,为电解池的阴极。由分析可知,左侧电极为阳极,则A为正极,A错误;由分析可知,右
侧电极为阴极,左侧电极为阳极,在电解池中阴离子向阳极移动,则OH-穿过a膜进入左室溶液,B错误;
由分析可知,催化电极为阴极,由图可知,电极反应为CO+6e-+6H+ CHOH+H O,C错误;64 g甲醇
2 3 2
的物质的量为2 mol,根据选项C分析可知,此时转移12 mol电子,左侧电极有如下对应关系O~4e-
2
12
~4OH-~Δm(36),则当此时转移12 mol电子时,左侧电极室质量增加 ×36 g=108 g,D正确。
4
8.(2024·黑吉辽卷)“绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、反应速
率缓慢的问题,科技工作者设计耦合HCHO高效制H 的方法,装置如图所示。部分反应机理为
2
1
2
+ H。下列说法错误的是( )
2
A.相同电量下H 理论产量是传统电解水的1.5倍
2
B.阴极反应:2H O+2e- 2OH-+H ↑
2 2
C.电解时OH-通过阴离子交换膜向b极方向移动
D.阳极反应:2HCHO-2e-+4OH- 2HCOO-+2H O+H↑
2 2
答案:A
解析:由题中反应机理分析可知,HCHO在阳极发生反应,阳极总反应为2HCHO-2e-+4OH-
2HCOO-+H ↑+2H O。而阴极水中的H+放电得H,电极反应式为2HO+2e- H↑+2OH-。
2 2 2 2 2
传统电解水时每转移2 mol电子可生成1 mol H ,而此原理中两电极均生成H,每转移2 mol电子共可
2 2
得到2 mol H ,所以相同电量下H 理论产量是传统电解水的2倍,A错误;由上述分析可知,B正确;根
2 2
据电解原理可知,阴离子向阳极移动,则OH-通过阴离子交换膜向阳极(b极)移动,C正确;由上述分析
可知,D正确。