文档内容
热点强化 2 氧化还原反应基本规律及应用
1.物质氧化态与还原态强弱的依存关系
物质的氧化态与还原态的依存关系如下:
氧化态还原态
越易失电子的物质(还原态),失电子后就越难得电子(氧化态);所以,氧化剂的氧化性越强,
得电子后生成的还原产物的还原性就越弱,反应生成的物质就越稳定,还原剂同理。
2.强弱规律及应用
(1)同时含有几种还原剂(或氧化剂),发生氧化还原反应时,还原性(或氧化性)强的优先反应,
即“强者优先”,如在FeBr 溶液中通入少量Cl 时,因为还原性: Fe 2 + > Br - ,所以 Fe 2 + 先
2 2
与Cl 反应,反应的离子方程式:2Fe2++Cl===2Fe3++2Cl-;在FeBr 溶液中通入足量Cl
2 2 2 2
时,反应的离子方程式:2Fe2++4Br-+3Cl===2Fe3++2Br +6Cl-。
2 2
(2)熟记常见的强弱顺序
氧化性:MnO(H+)>MnO>Cl>Br >Fe3+>I >S,还原性:Mn2+Fe2+>Cl->Co2
2 3
+。下列反应在水溶液中不可能发生的是( )
A.3Cl+6FeI===2FeCl +4FeI
2 2 3 3
B.Cl+FeI===FeCl +I
2 2 2 2
C.Co O+6HCl===2CoCl +Cl↑+3HO
2 3 2 2 2
D.2Fe3++2I-===2Fe2++I
2
答案 A
解析 A项,根据氧化性:Cl>FeCl >I ,因此氯气可以氧化Fe2+,也可以氧化I-,但是碘
2 3 2
离子还原性强于亚铁离子,碘离子会先被氯气氧化,正确的离子方程式是Cl 不足时:Cl +
2 2
2I-===2Cl-+I(Fe2+不反应),Cl 过量时:3Cl +2Fe2++4I-===6Cl-+2I +2Fe3+,反应不
2 2 2 2
可能发生;B项,根据反应的化学方程式可得出还原性:I->Cl-,反应可能发生;C项,根
据反应的化学方程式可得出还原性:Cl->Co2+,反应可能发生;D项,根据反应的化学方
程式可得出还原性:I->Fe2+,反应可能发生。
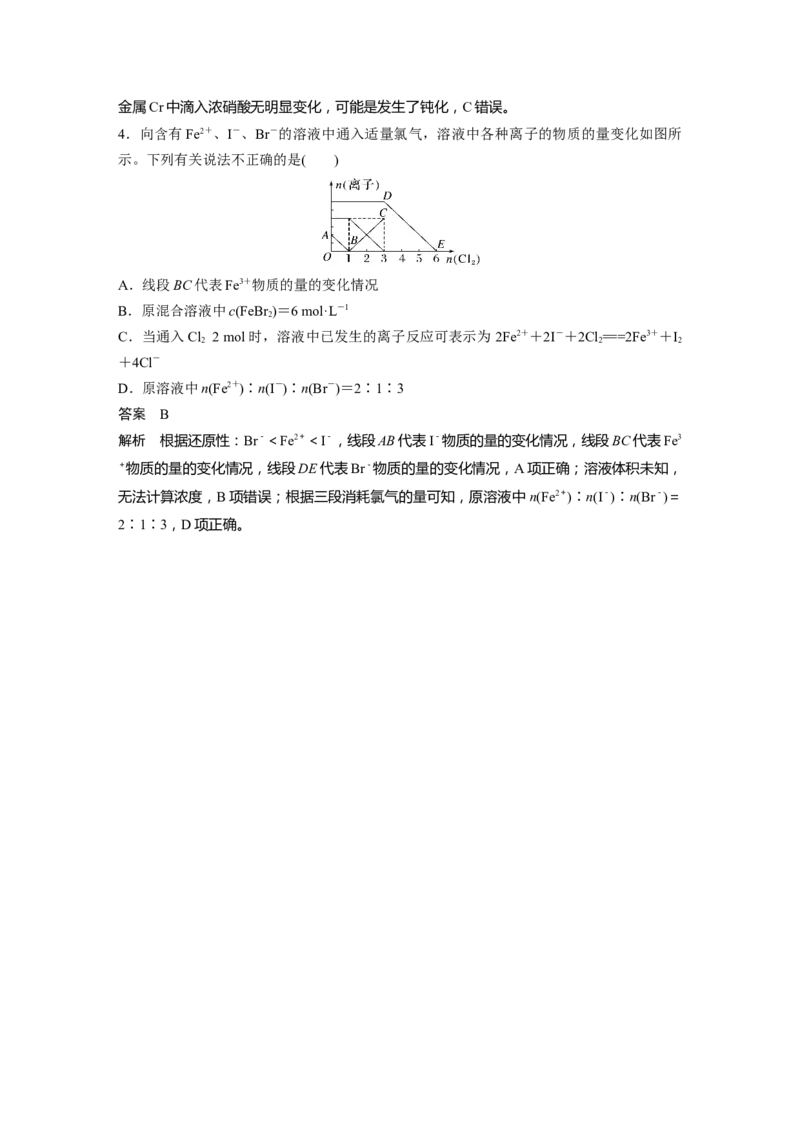
3.(2023·广东韶关模拟)已知有如下反应:
①KCr O+14HCl(浓)===2KCl+2CrCl +3Cl↑+7HO;②Cr+2HCl(稀)===CrCl +H↑;
2 2 7 3 2 2 2 2
③2KMnO +16HCl(稀)===2KCl+2MnCl +5Cl↑+8HO。下列说法正确的是( )
4 2 2 2
A.氧化性:KCr O>KMnO >Cl
2 2 7 4 2
B.反应③中氧化剂与还原剂的物质的量之比为5∶1
C.向金属Cr中滴入浓硝酸无明显变化,说明两者不能发生反应
D.向 Cr (SO ) 溶液中滴入酸性 KMnO 溶液,可发生反应:10Cr3++6MnO+
2 4 3 4
11HO===5Cr O+6Mn2++22H+
2 2
答案 D
解析 根据氧化性:氧化剂>氧化产物,结合①~③分别可得,氧化性:KCr O>Cl 、
2 2 7 2
HCl>CrCl 、 KMnO >Cl , ① 中 使 用 浓 盐 酸 , ③ 中 使 用 稀 盐 酸 , 则 氧 化 性 :
2 4 2
KMnO >K Cr O,A错误;反应③中,KMnO 是氧化剂,HCl是还原剂,根据得失电子守恒
4 2 2 7 4
可知,氧化剂和还原剂的物质的量之比为 1∶5,B错误;②中Cr与稀盐酸反应生成H ,向
2金属Cr中滴入浓硝酸无明显变化,可能是发生了钝化,C错误。
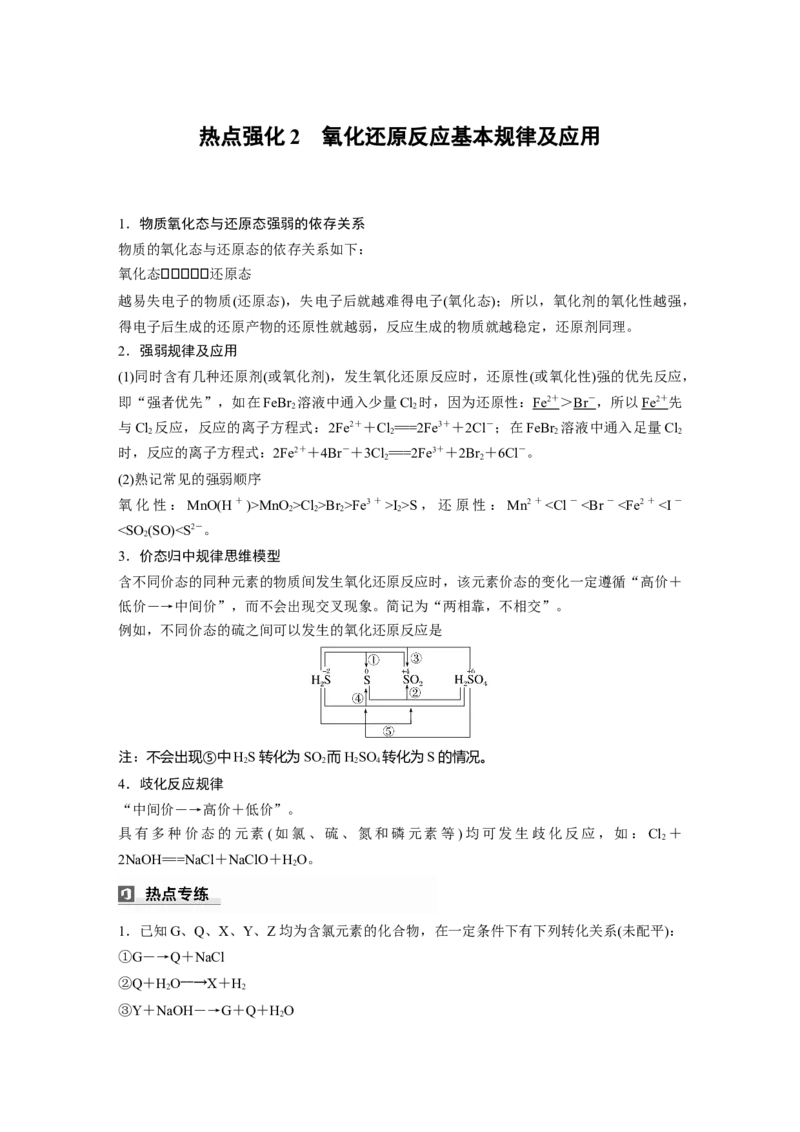
4.向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所
示。下列有关说法不正确的是( )
A.线段BC代表Fe3+物质的量的变化情况
B.原混合溶液中c(FeBr)=6 mol·L-1
2
C.当通入Cl 2 mol时,溶液中已发生的离子反应可表示为 2Fe2++2I-+2Cl===2Fe3++I
2 2 2
+4Cl-
D.原溶液中n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
答案 B
解析 根据还原性:Br-<Fe2+<I-,线段AB代表I-物质的量的变化情况,线段BC代表Fe3
+物质的量的变化情况,线段DE代表Br-物质的量的变化情况,A项正确;溶液体积未知,
无法计算浓度,B项错误;根据三段消耗氯气的量可知,原溶液中n(Fe2+)∶n(I-)∶n(Br-)=
2∶1∶3,D项正确。