文档内容
第 1 讲 物质的组成、性质和转化
[复习目标] 1.认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行
分类。2.熟知同类物质具有相似的性质,一定条件下各类物质可以相互转化。3.了解胶体是
一种常见的分散系,了解溶液和胶体的区别。
考点一 物质的组成与分类
1.物质的组成
(1)元素与物质的关系
(2)同素异形体
①定义:由同一种元素形成的________________________。
②性质:物理性质不同,化学性质有差异。同素异形体之间在一定条件下可以相互转化,这
种转化是________变化。
③常见元素的同素异形体
氧元素:________;碳元素:________________;磷元素:________________。
2.纯净物和混合物
纯净物:由同种单质或化合物组成的物质。
混合物:由几种不同的单质或化合物组成的物质。
[应用举例]现有下列物质:
①冰水混合物 ②爆鸣气 ③铝热剂 ④普通玻璃 ⑤水玻璃 ⑥有机玻璃 ⑦漂白粉
⑧TNT ⑨HSO ⑩含氧40%的氧化镁 ⑪花生油 ⑫福尔马林 ⑬密封保存的NO 气
2 4 2
体 ⑭CuSO ·5H O ⑮液氯 ⑯王水 ⑰KAl(SO )·12H O ⑱分子式为 C H 的烃
4 2 4 2 2 5 10
⑲分子式为C H 的芳香烃
7 8
其中一定为纯净物的是____________(填序号,下同);一定为混合物的是________________;
可能是纯净物,也可能是混合物的是________。
3.物质的分类
分类应依据事先设定的“标准”进行,“标准”不同,分类方法也不相同。在化学上常用的
分类方法有________分类法和________分类法。
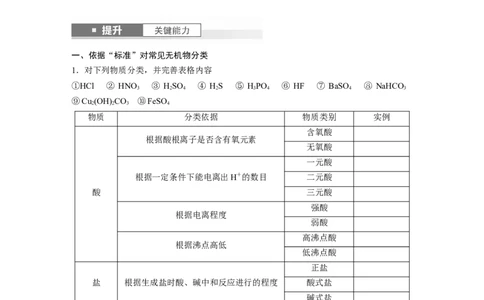
(1)树状分类法应用举例
请把下列物质的序号填写到下图的横线上:
①硫黄 ②HClO ③苛性钠 ④明矾 ⑤小苏打 ⑥氧化钠 ⑦Fe(OH) ⑧NaCl溶液
3
⑨HSO ⑩淀粉溶液 ⑪泥水
2 3
(2)交叉分类法应用举例
将下列氧化物与指定类别连线:
1.某物质经科学测定只含有一种元素,可以断定该物质一定是一种单质( )
2.Cu、NaCl、SiO、HSO 都称为分子式( )
2 2 4
3.金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物( )4.酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱( )
5.酸溶于水一定能电离出H+,但能电离出H+的不一定是酸( )
6.CO、NO 都能和水反应生成酸,故两者都是酸性氧化物( )
2 2
氧化物的再分类
(1)酸性氧化物。(2)碱性氧化物。(3)两性氧化物。(4)不成盐氧化物:既不能与酸反应,也不
能与碱反应生成(相应价态的)盐和水的氧化物。例如NO、CO等。(5)过氧化物:含有过氧
基(—O—O—)的化合物。例如:HO、NaO、CaO 等。
2 2 2 2 2
一、依据“标准”对常见无机物分类
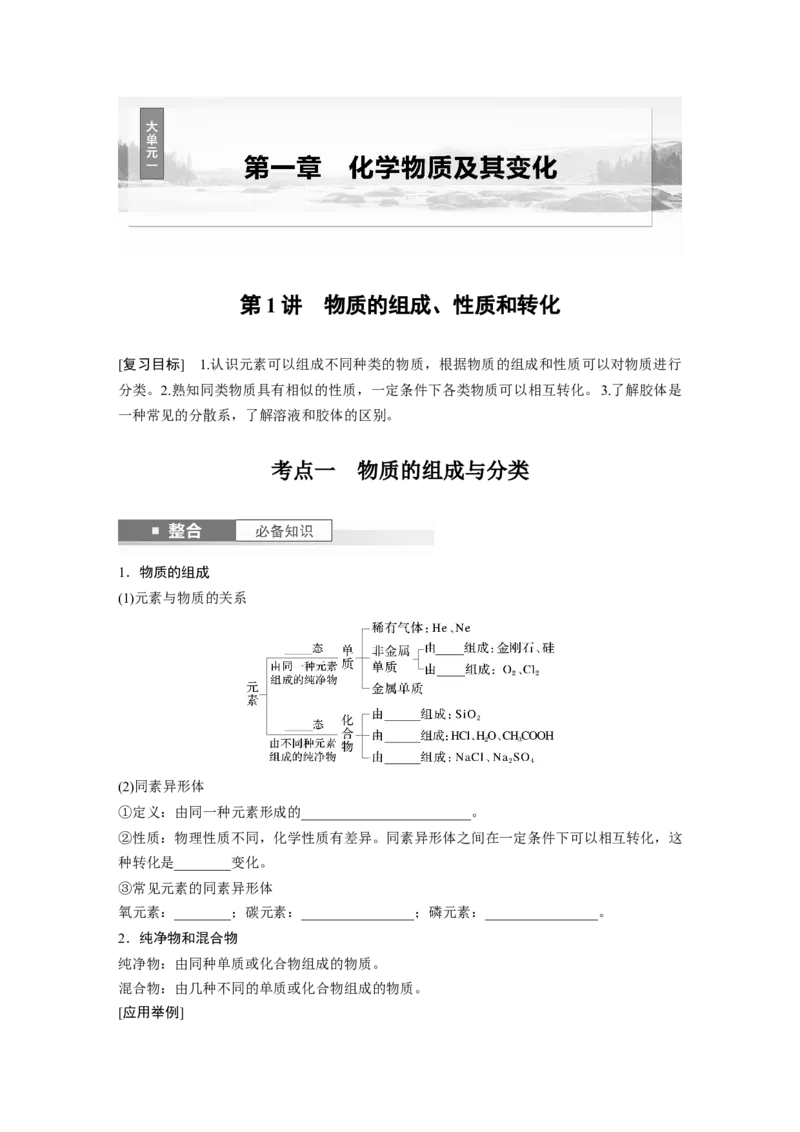
1.对下列物质分类,并完善表格内容
①HCl ② HNO ③ HSO ④ HS ⑤ HPO ⑥ HF ⑦ BaSO ⑧ NaHCO
3 2 4 2 3 4 4 3
⑨Cu (OH) CO ⑩FeSO
2 2 3 4
物质 分类依据 物质类别 实例
含氧酸
根据酸根离子是否含有氧元素
无氧酸
一元酸
根据一定条件下能电离出H+的数目 二元酸
酸 三元酸
强酸
根据电离程度
弱酸
高沸点酸
根据沸点高低
低沸点酸
正盐
盐 根据生成盐时酸、碱中和反应进行的程度 酸式盐
碱式盐
二、各物质类别包含关系判断
2.下列各组物质的分类都正确的是(括号里的是类别)________,都不正确的是________。
A.NaClO(碱式盐)、C HOH(碱)、HSO (离子化合物)、玻璃钢(金属材料)
2 5 2 4
B.液氨(氢化物)、NH Cl(铵盐)、HNO(含氧酸)、NaOH(强碱)
4 3
C.HCl(共价化合物)、CHCOOH(羧酸)、NaO(碱性氧化物)、CHI(卤代烃)
3 2 2 3
D.NO (酸性氧化物)、CHCHO(有机物)、CO(有机物)、CHCOOCH (酯)
2 3 3 3
3.如图表示了一些概念之间的从属关系,下列各项不符合图示关系的是( )选项 X Y Z
A 硫酸铜 盐 纯净物
B 碱性氧化物 金属氧化物 氧化物
C 酸性氧化物 非金属氧化物 氧化物
D 强电解质 电解质 化合物
考点二 物质的性质与转化
1.多角度认识物理变化与化学变化
(1)通过对比物理变化和化学变化的不同,回答下列问题:
①石油的分馏 ②煤的干馏 ③钠的焰色试验 ④碘的升华 ⑤氯化铵分解 ⑥蛋白质的变
性 ⑦蛋白质的显色反应 ⑧电解食盐水 ⑨CaCl 的潮解 ⑩冰的融化 ⑪FeCl 的水解
2 3
⑫石油的裂化、裂解 ⑬蛋白质的盐析 ⑭食物的缓慢氧化 ⑮同素异形体间的转化
其中属于物理变化的是__________________(填序号,下同);属于化学变化的是
________________________________________________________________________。
(2)分别从物质变化(宏观)和化学键变化(微观)的视角说明化学变化的特征。
________________________________________________________________________
________________________________________________________________________
2.不同类别的无机物之间的转化
(1)金属单质及其化合物的转化
金属单质――→碱性氧化物――→碱――→盐
如:Na――→NaO――→NaOH――→NaSO
2 2 4
符合上述转化关系的常见金属有Na、K、Ca、Ba等,但Mg、Fe、Al、Cu等不符合上述转
化关系。
(2)非金属单质及其化合物的转化
非金属单质――→酸性氧化物――→酸――→盐
如:S――→SO ――→HSO ――→NaSO
2 2 3 2 3
符合上述转化关系的常见非金属有C、S、P等,但N、Si等不符合上述转化关系。
1.从海水中提取物质都必须通过化学反应才能实现( )2.点燃爆竹后,硫燃烧生成SO ( )
3
3.232Th转化成233Th是化学变化( )
4.石墨在一定条件下转化为金刚石是化学变化( )
5.判断下列转化能否实现,能实现的打“√”,不能实现的打“×”。
①SiO――→HSiO( )
2 2 3
②SO ――→HSO ( )
3 2 4
③Fe O――→Fe(OH) ( )
2 3 3
④BaO――→Ba(OH) ( )
2
一、不同类别物质的转化
1.含碳元素的常见物质有CH 、单质碳(C)、CO、CO 、HCO 、NaCO 、NaHCO ,下面
4 2 2 3 2 3 3
是这些物质的“价—类”二维图及它们的转化关系:
请用化学方程式表示标有序号的物质间的转化(写出一个即可)。
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________;
⑤________________________________________________________________________;
⑥________________________________________________________________________;
⑦________________________________________________________________________。
二、物质性质与转化
2.铜器久置于空气中会和空气中的水蒸气、CO 、O 作用产生“绿锈”,该“绿锈”俗称
2 2
“铜绿”,又称“孔雀石”[化学式为Cu (OH) CO],“铜绿”能与酸反应生成铜盐、CO
2 2 3 2
和HO。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
2
铜――→铜绿――→A――→Cu(OH) ――→B――→Cu
2
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:________________________。
(2)请写出“铜绿”与盐酸反应的化学方程式:
________________________________________________________________________。(3)写出④⑤的化学方程式:
④________________________________________________________________________;
⑤________________________________________________________________________。
(4)上述转化过程中属于化合反应的是______(填序号,下同),属于复分解反应的是______,
属于分解反应的是________。
三、基于物质类别预测陌生物质的性质
3.已知次磷酸(H PO )是一元中强酸,请写出其与足量氢氧化钠反应的化学方程式:
3 2
________________________________________________________________________
________________________________________________________________________。
4.已知Be(OH) 与Al(OH) 都属于两性氢氧化物,写出Be(OH) 分别溶于NaOH溶液、盐酸
2 3 2
的化学方程式:
(1)________________________________________________________________________。
(2)________________________________________________________________________。
考点三 分散系 胶体
1.分散系
(1)组成
(2)分类:根据____________________________________________________________的大小。
2.胶体
(1)分类
请把下列物质的序号填到对应的横线上:
①Fe(OH) 胶体 ②云 ③烟水晶 ④雾 ⑤蛋白质溶液 ⑥烟 ⑦有色玻璃
3
气溶胶:____________;液溶胶:____________;固溶胶:________。
(2)性质与应用使胶体聚沉的常见方法:①加入电解质溶液,②加入与胶粒带相反电荷的胶体,③加热、搅
拌。
3.三种分散系的比较
分散系 溶液 胶体 浊液
巨大分子或离子
分散质微粒成分 离子或小分子 大分子或离子集合体
集合体
分散质粒子直径大小
外观特征
稳定性 稳定 介稳定 不稳定
分散质能否透过滤纸 能透过滤纸,不能透
均能 均不能
或半透膜 过半透膜
鉴别
1.可用过滤的方法将胶体粒子与分散剂分开( )
2.胶体不一定是液态,胶体的丁达尔效应属于物理变化( )
3.将1 mL 1 mol·L-1 FeCl 溶液滴入沸水中制备Fe(OH) 胶体,若FeCl 完全水解,则可制
3 3 3
得的Fe(OH) 胶体粒子数少于0.001N ( )
3 A
4.利用丁达尔效应可区分蛋白质溶液和食盐水( )
Fe(OH) 胶体的制备
3
(1)制备方法:向沸水中逐滴加入__________________________,继续煮沸至液体呈
________,停止加热,即制得Fe(OH) 胶体。
3
(2)制备原理:__________________________________________________________________
____________________________________________________________(用化学方程式表示)。
(3)Fe(OH) 胶体区别于FeCl 溶液最本质的特征是______(填字母)。
3 3
A.Fe(OH) 胶体分散质粒子的直径在1~100 nm之间
3
B.Fe(OH) 胶体具有丁达尔效应
3
C.Fe(OH) 胶体是均一的分散系
3
D.Fe(OH) 胶体的分散质能透过滤纸
3
(4)问题讨论①可以利用______________证明Fe(OH) 胶体已经制成。
3
②在制备Fe(OH) 胶体时,某些同学没有按要求进行,结果没有观察到胶体产生,请预测现
3
象并分析原因:甲同学在做实验时没有使用蒸馏水,而用自来水,结果会
__________________ , 其 原 因 可 能 是
__________________________________________________________________;乙同学在制备
Fe(OH) 胶 体 时 长 时 间 加 热 , 结 果 会 __________________ , 原 因 可 能 是
3
________________________________________________________________________。
1.(2023·新课标卷,7)化学在文物的研究和修复中有重要作用。下列说法错误的是( )
A.竹简的成分之一纤维素属于天然高分子
B.龟甲的成分之一羟基磷灰石属于无机物
C.古陶瓷修复所用的熟石膏,其成分为Ca(OH)
2
D.古壁画颜料中所用的铁红,其成分为Fe O
2 3
2.(2023·浙江6月选考,1)材料是人类赖以生存和发展的物质基础,下列材料主要成分属于
有机物的是( )
A.石墨烯 B.不锈钢
C.石英光导纤维 D.聚酯纤维
3.(2023·辽宁,1)科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的
是( )
A.利用CO 合成了脂肪酸:实现了无机小分子向有机高分子的转变
2
B.发现了月壤中的“嫦娥石[(Ca Y)Fe(PO)]”:其成分属于无机盐
8 4 7
C.研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
D.革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
4.(2022·湖北,1)化学与生活密切相关,下列不涉及化学变化的是( )
A.加入明矾后泥水变澄清
B.北京冬奥会用水快速制冰
C.炖排骨汤时加点醋味道更鲜
D.切开的茄子放置后切面变色