文档内容
第 1 讲 物质的组成、性质和转化
[复习目标] 1.认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行
分类。2.熟知同类物质具有相似的性质,一定条件下各类物质可以相互转化。3.了解胶体是
一种常见的分散系,了解溶液和胶体的区别。
考点一 物质的组成与分类
1.物质的组成
(1)元素与物质的关系
(2)同素异形体
①定义:由同一种元素形成的几种性质不同的单质。
②性质:物理性质不同,化学性质有差异。同素异形体之间在一定条件下可以相互转化,这
种转化是化学变化。
③常见元素的同素异形体
氧元素:O 、 O ;碳元素: 金刚石、石墨、 C ;磷元素:白磷、红磷。
2 3 60
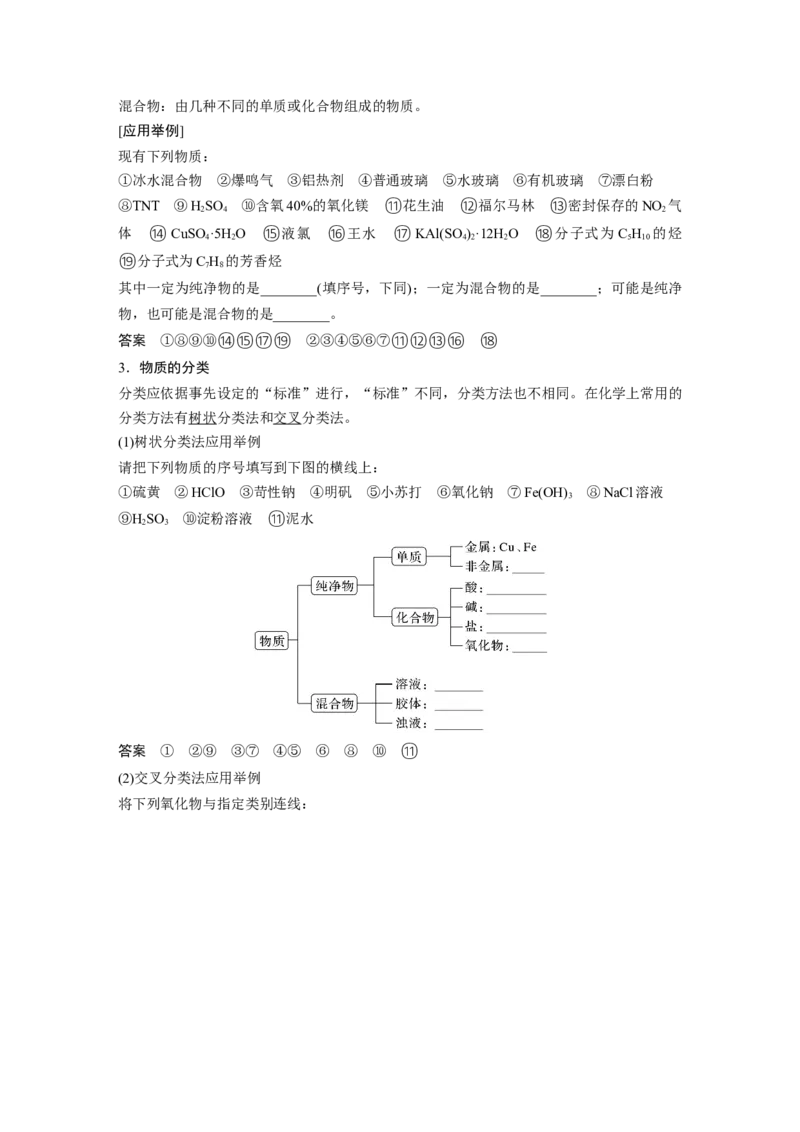
2.纯净物和混合物
纯净物:由同种单质或化合物组成的物质。混合物:由几种不同的单质或化合物组成的物质。
[应用举例]
现有下列物质:
①冰水混合物 ②爆鸣气 ③铝热剂 ④普通玻璃 ⑤水玻璃 ⑥有机玻璃 ⑦漂白粉
⑧TNT ⑨HSO ⑩含氧40%的氧化镁 ⑪花生油 ⑫福尔马林 ⑬密封保存的NO 气
2 4 2
体 ⑭CuSO ·5H O ⑮液氯 ⑯王水 ⑰KAl(SO )·12H O ⑱分子式为 C H 的烃
4 2 4 2 2 5 10
⑲分子式为C H 的芳香烃
7 8
其中一定为纯净物的是________(填序号,下同);一定为混合物的是________;可能是纯净
物,也可能是混合物的是________。
答案 ①⑧⑨⑩⑭⑮⑰⑲ ②③④⑤⑥⑦⑪⑫⑬⑯ ⑱
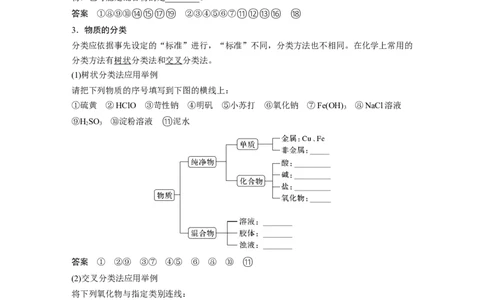
3.物质的分类
分类应依据事先设定的“标准”进行,“标准”不同,分类方法也不相同。在化学上常用的
分类方法有树状分类法和交叉分类法。
(1)树状分类法应用举例
请把下列物质的序号填写到下图的横线上:
①硫黄 ②HClO ③苛性钠 ④明矾 ⑤小苏打 ⑥氧化钠 ⑦Fe(OH) ⑧NaCl溶液
3
⑨HSO ⑩淀粉溶液 ⑪泥水
2 3
答案 ① ②⑨ ③⑦ ④⑤ ⑥ ⑧ ⑩ ⑪
(2)交叉分类法应用举例
将下列氧化物与指定类别连线:1.某物质经科学测定只含有一种元素,可以断定该物质一定是一种单质( )
2.Cu、NaCl、SiO、HSO 都称为分子式( )
2 2 4
3.金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物( )
4.酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱( )
5.酸溶于水一定能电离出H+,但能电离出H+的不一定是酸( )
6.CO、NO 都能和水反应生成酸,故两者都是酸性氧化物( )
2 2
答案 1.× 2.× 3.× 4.√ 5.√ 6.×
氧化物的再分类
(1)酸性氧化物。(2)碱性氧化物。(3)两性氧化物。(4)不成盐氧化物:既不能与酸反应,也不
能与碱反应生成(相应价态的)盐和水的氧化物。例如NO、CO等。(5)过氧化物:含有过氧
基(—O—O—)的化合物。例如:HO、NaO、CaO 等。
2 2 2 2 2
一、依据“标准”对常见无机物分类
1.对下列物质分类,并完善表格内容
①HCl ② HNO ③ HSO ④ HS ⑤ HPO ⑥ HF ⑦ BaSO ⑧ NaHCO
3 2 4 2 3 4 4 3
⑨Cu (OH) CO ⑩FeSO
2 2 3 4
物质 分类依据 物质类别 实例
根据酸根离子是否含有氧 含氧酸 ②③⑤
元素 无氧酸 ①④⑥
酸
一元酸 ①②⑥
根据一定条件下能电离出
二元酸 ③④三元酸 ⑤
H+的数目
强酸 ①②③
根据电离程度
弱酸 ④⑤⑥
高沸点酸 ③⑤
根据沸点高低
低沸点酸 ①②④⑥
正盐 ⑦⑩
根据生成盐时酸、碱中和
盐 酸式盐 ⑧
反应进行的程度
碱式盐 ⑨
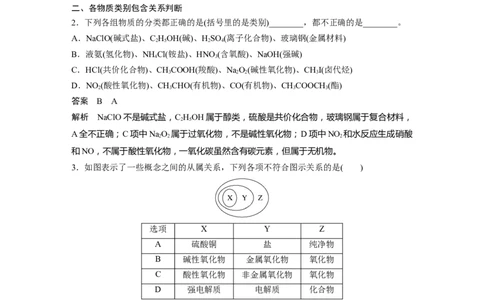
二、各物质类别包含关系判断
2.下列各组物质的分类都正确的是(括号里的是类别)________,都不正确的是________。
A.NaClO(碱式盐)、C HOH(碱)、HSO (离子化合物)、玻璃钢(金属材料)
2 5 2 4
B.液氨(氢化物)、NH Cl(铵盐)、HNO(含氧酸)、NaOH(强碱)
4 3
C.HCl(共价化合物)、CHCOOH(羧酸)、NaO(碱性氧化物)、CHI(卤代烃)
3 2 2 3
D.NO (酸性氧化物)、CHCHO(有机物)、CO(有机物)、CHCOOCH (酯)
2 3 3 3
答案 B A
解析 NaClO不是碱式盐,C HOH属于醇类,硫酸是共价化合物,玻璃钢属于复合材料,
2 5
A全不正确;C项中NaO 属于过氧化物,不是碱性氧化物;D项中NO 和水反应生成硝酸
2 2 2
和NO,不属于酸性氧化物,一氧化碳虽然含有碳元素,但属于无机物。
3.如图表示了一些概念之间的从属关系,下列各项不符合图示关系的是( )
选项 X Y Z
A 硫酸铜 盐 纯净物
B 碱性氧化物 金属氧化物 氧化物
C 酸性氧化物 非金属氧化物 氧化物
D 强电解质 电解质 化合物
答案 C
解析 从组成上分类,氧化物包括金属氧化物和非金属氧化物,但酸性氧化物不一定是非金
属氧化物,如MnO 等,C项错误。
2 7考点二 物质的性质与转化
1.多角度认识物理变化与化学变化
(1)通过对比物理变化和化学变化的不同,回答下列问题:
①石油的分馏 ②煤的干馏 ③钠的焰色试验 ④碘的升华 ⑤氯化铵分解 ⑥蛋白质的变
性 ⑦蛋白质的显色反应 ⑧电解食盐水 ⑨CaCl 的潮解 ⑩冰的融化 ⑪FeCl 的水解
2 3
⑫石油的裂化、裂解 ⑬蛋白质的盐析 ⑭食物的缓慢氧化 ⑮同素异形体间的转化
其中属于物理变化的是_____________________________(填序号,下同);属于化学变化的
是________________________________________________________________________。
答案 ①③④⑨⑩⑬ ②⑤⑥⑦⑧⑪⑫⑭⑮
(2)分别从物质变化(宏观)和化学键变化(微观)的视角说明化学变化的特征。
答案
宏观 有新物质生成的是化学变化,反之是物理变化
微观 有旧化学键断裂,同时有新化学键形成的是化学变化,本质是原子的重新组合
2.不同类别的无机物之间的转化
(1)金属单质及其化合物的转化
金属单质――→碱性氧化物――→碱――→盐
如:Na――→NaO――→NaOH――→NaSO
2 2 4
符合上述转化关系的常见金属有Na、K、Ca、Ba等,但Mg、Fe、Al、Cu等不符合上述转
化关系。
(2)非金属单质及其化合物的转化
非金属单质――→酸性氧化物――→酸――→盐
如:S――→SO ――→HSO ――→NaSO
2 2 3 2 3
符合上述转化关系的常见非金属有C、S、P等,但N、Si等不符合上述转化关系。
1.从海水中提取物质都必须通过化学反应才能实现( )
2.点燃爆竹后,硫燃烧生成SO ( )
3
3.232Th转化成233Th是化学变化( )
4.石墨在一定条件下转化为金刚石是化学变化( )
5.判断下列转化能否实现,能实现的打“√”,不能实现的打“×”。
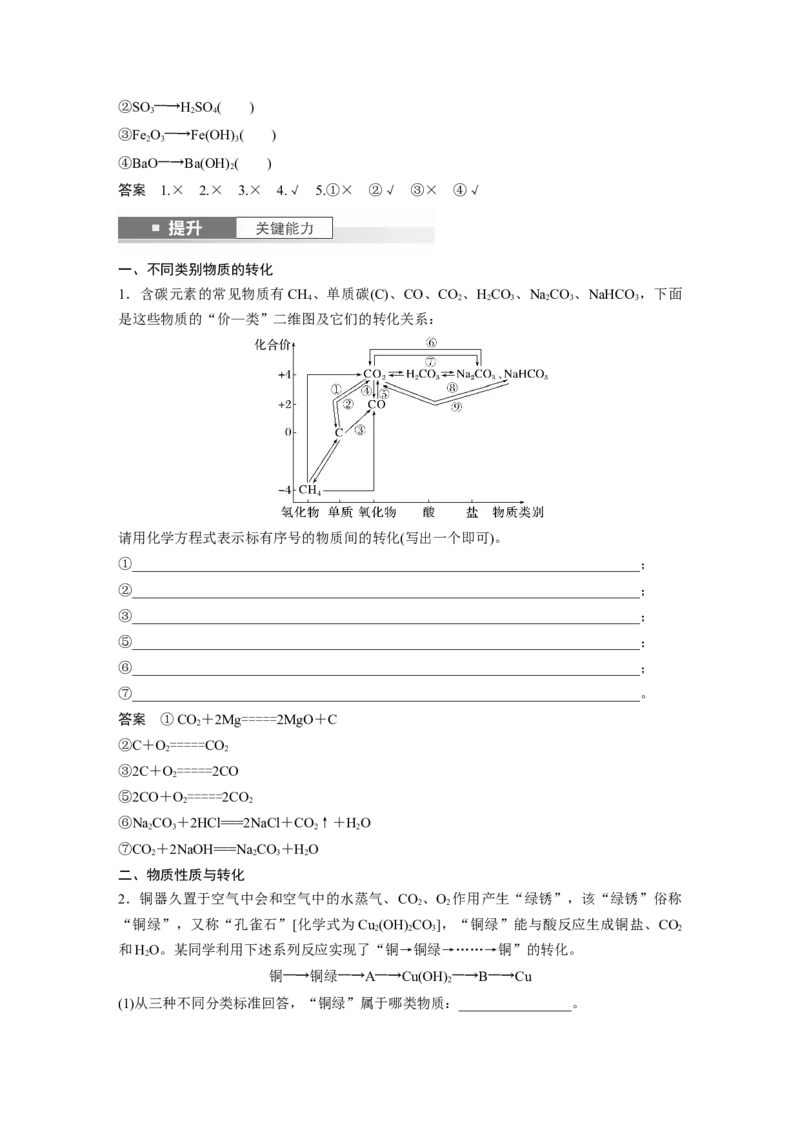
①SiO――→HSiO( )
2 2 3②SO ――→HSO ( )
3 2 4
③Fe O――→Fe(OH) ( )
2 3 3
④BaO――→Ba(OH) ( )
2
答案 1.× 2.× 3.× 4.√ 5.①× ②√ ③× ④√
一、不同类别物质的转化
1.含碳元素的常见物质有CH 、单质碳(C)、CO、CO 、HCO 、NaCO 、NaHCO ,下面
4 2 2 3 2 3 3
是这些物质的“价—类”二维图及它们的转化关系:
请用化学方程式表示标有序号的物质间的转化(写出一个即可)。
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________;
⑤________________________________________________________________________;
⑥________________________________________________________________________;
⑦________________________________________________________________________。
答案 ①CO+2Mg=====2MgO+C
2
②C+O=====CO
2 2
③2C+O=====2CO
2
⑤2CO+O=====2CO
2 2
⑥NaCO+2HCl===2NaCl+CO↑+HO
2 3 2 2
⑦CO+2NaOH===NaCO+HO
2 2 3 2
二、物质性质与转化
2.铜器久置于空气中会和空气中的水蒸气、CO 、O 作用产生“绿锈”,该“绿锈”俗称
2 2
“铜绿”,又称“孔雀石”[化学式为Cu (OH) CO],“铜绿”能与酸反应生成铜盐、CO
2 2 3 2
和HO。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
2
铜――→铜绿――→A――→Cu(OH) ――→B――→Cu
2
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:________________。(2)请写出“铜绿”与盐酸反应的化学方程式:
________________________________________________________________________。
(3)写出④⑤的化学方程式:
④________________________________________________________________________;
⑤________________________________________________________________________。
(4)上述转化过程中属于化合反应的是______(填序号,下同),属于复分解反应的是______,
属于分解反应的是________。
答案 (1)盐、铜盐、碱式盐(或碳酸盐)
(2)Cu (OH) CO +4HCl===2CuCl +3HO+CO↑ (3)Cu(OH) =====CuO+HO CuO+
2 2 3 2 2 2 2 2
H=====Cu+HO (4)① ②③ ④
2 2
三、基于物质类别预测陌生物质的性质
3.已知次磷酸(H PO )是一元中强酸,请写出其与足量氢氧化钠反应的化学方程式:
3 2
________________________________________________________________________
________________________________________________________________________。
答案 HPO +NaOH===NaH PO +HO
3 2 2 2 2
4.已知Be(OH) 与Al(OH) 都属于两性氢氧化物,写出Be(OH) 分别溶于NaOH溶液、盐酸
2 3 2
的化学方程式:
(1)Be(OH) + 2NaOH == = N aBeO + 2H O。
2 2 2 2
(2)Be(OH) + 2HC l == = BeC l + 2H O。
2 2 2
考点三 分散系 胶体
1.分散系
(1)组成
(2)分类:根据分散质粒子直径的大小。
2.胶体
(1)分类
请把下列物质的序号填到对应的横线上:
①Fe(OH) 胶体 ②云 ③烟水晶 ④雾
3⑤蛋白质溶液 ⑥烟 ⑦有色玻璃
气溶胶:②④⑥;液溶胶:①⑤;固溶胶:③⑦。
(2)性质与应用
使胶体聚沉的常见方法:①加入电解质溶液,②加入与胶粒带相反电荷的胶体,③加热、搅
拌。
3.三种分散系的比较
分散系 溶液 胶体 浊液
分散质微粒成分 离子或小分子 大分子或离子集合体 巨大分子或离子集合体
分散质粒子直径大小 < 1 nm 1 ~ 100 nm >100 nm
外观特征 均一、透明 均一、透明 不均一、不透明
稳定性 稳定 介稳定 不稳定
分散质能否透过滤纸 能透过滤纸,不能透过
均能 均不能
或半透膜 半透膜
鉴别 无丁达尔效应 有丁达尔效应 静置沉淀或分层
1.可用过滤的方法将胶体粒子与分散剂分开( )
2.胶体不一定是液态,胶体的丁达尔效应属于物理变化( )
3.将1 mL 1 mol·L-1 FeCl 溶液滴入沸水中制备Fe(OH) 胶体,若FeCl 完全水解,则可制
3 3 3
得的Fe(OH) 胶体粒子数少于0.001N ( )
3 A
4.利用丁达尔效应可区分蛋白质溶液和食盐水( )
答案 1.× 2.√ 3.√ 4.√
Fe(OH) 胶体的制备
3
(1)制备方法:向沸水中逐滴加入____________________________,继续煮沸至液体呈
________,停止加热,即制得Fe(OH) 胶体。
3
(2) 制 备 原 理 :
____________________________________________________________________
________________________________________________________________________(用化学
方程式表示)。(3)Fe(OH) 胶体区别于FeCl 溶液最本质的特征是______(填字母)。
3 3
A.Fe(OH) 胶体分散质粒子的直径在1~100 nm之间
3
B.Fe(OH) 胶体具有丁达尔效应
3
C.Fe(OH) 胶体是均一的分散系
3
D.Fe(OH) 胶体的分散质能透过滤纸
3
(4)问题讨论
①可以利用__________________证明Fe(OH) 胶体已经制成。
3
②在制备Fe(OH) 胶体时,某些同学没有按要求进行,结果没有观察到胶体产生,请预测现
3
象并分析原因:甲同学在做实验时没有使用蒸馏水,而用自来水,结果会________________,
其原因可能是___________________________________________________________________;
乙同学在制备 Fe(OH) 胶体时长时间加热,结果会____________________,原因可能是
3
_______________________________________________________________________________。
答案 (1)饱和FeCl 溶液 红褐色 (2)FeCl +3HO=====Fe(OH) (胶体)+3HCl (3)A
3 3 2 3
(4)①丁达尔效应 ②生成红褐色沉淀 自来水中含有电解质,使胶体发生聚沉 生成红褐
色沉淀 长时间加热使胶体发生聚沉
1.(2023·新课标卷,7)化学在文物的研究和修复中有重要作用。下列说法错误的是( )
A.竹简的成分之一纤维素属于天然高分子
B.龟甲的成分之一羟基磷灰石属于无机物
C.古陶瓷修复所用的熟石膏,其成分为Ca(OH)
2
D.古壁画颜料中所用的铁红,其成分为Fe O
2 3
答案 C
解析 羟基磷灰石的化学式为[Ca (PO )OH],属于无机物,B正确;熟石膏的主要成分为
5 4 3
2CaSO·H O,C错误。
4 2
2.(2023·浙江6月选考,1)材料是人类赖以生存和发展的物质基础,下列材料主要成分属于
有机物的是( )
A.石墨烯 B.不锈钢
C.石英光导纤维 D.聚酯纤维
答案 D
解析 石墨烯是一种由单层碳原子构成的平面结构新型碳材料,为碳的单质,属于无机物,
A不符合题意;不锈钢是Fe、Cr、Ni等的合金,属于金属材料,B不符合题意;石英光导
纤维的主要成分为SiO,属于无机非金属材料,C不符合题意。
2
3.(2023·辽宁,1)科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的
是( )A.利用CO 合成了脂肪酸:实现了无机小分子向有机高分子的转变
2
B.发现了月壤中的“嫦娥石[(Ca Y)Fe(PO)]”:其成分属于无机盐
8 4 7
C.研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
D.革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
答案 A
解析 脂肪酸不属于有机高分子,A错误;聚四氟乙烯塑料被称为塑料王,耐酸、耐碱,不
会被海水腐蚀,D正确。
4.(2022·湖北,1)化学与生活密切相关,下列不涉及化学变化的是( )
A.加入明矾后泥水变澄清
B.北京冬奥会用水快速制冰
C.炖排骨汤时加点醋味道更鲜
D.切开的茄子放置后切面变色
答案 B
解析 明矾净水的原理为Al3++3HOAl(OH) (胶体)+3H+,Al(OH) 胶体具有吸附性,
2 3 3
可以使泥水变澄清,涉及化学变化,A错误;水快速制冰为物理变化,B正确;炖排骨汤时
放点醋,可使骨头中的钙、磷、铁等矿物质溶解出来,此外,醋还可以防止食物中的维生素
被破坏,涉及化学变化,C错误;茄子中存在一类叫“酚氧化酶”的物质,遇到氧气之后,
发生化学反应产生一些有色的物质,反应时间越长,颜色越深,涉及化学变化,D错误。
课时精练
1.(2022·浙江6月选考,1)下列消毒剂的有效成分属于盐的是( )
A.高锰酸钾溶液 B.过氧乙酸溶液
C.双氧水 D.医用酒精
答案 A
2.(2022·广东,2)北京冬奥会成功举办、神舟十三号顺利往返、“天宫课堂”如期开讲及
“华龙一号”核电海外投产等,均展示了我国科技发展的巨大成就。下列相关叙述正确的是
( )
A.冬奥会“飞扬”火炬所用的燃料H 为氧化性气体
2
B.飞船返回舱表层材料中的玻璃纤维属于天然有机高分子
C.乙酸钠过饱和溶液析出晶体并放热的过程仅涉及化学变化
D.核电站反应堆所用铀棒中含有的U与U互为同位素
答案 D
解析 H 作为燃料在反应中被氧化,体现还原性,故A项错误;玻璃纤维是一种性能优异
2
的无机非金属材料,故B项错误。3.(2023·山东枣庄统考二模)二十大报告提出加快科技创新、构建新能源体系,推进生态优
先、绿色低碳发展。下列说法错误的是( )
A.“奋斗者”号深海载人潜水器采用的Ti62A新型钛合金材料硬度大、韧性好
B.推动大型风电、水电、太阳光伏等可再生能源发展
C.保护和治理山水林田湖草有利于实现碳中和
D.使用聚乙烯制作的塑料包装袋物美价廉,符合绿色低碳发展理念
答案 D
4.(2022·湖南,1)化学促进了科技进步和社会发展,下列叙述中没有涉及化学变化的是(
)
A.《神农本草经》中记载的“石胆能化铁为铜”
B.利用“侯氏联合制碱法”制备纯碱
C.科学家成功将CO 转化为淀粉或葡萄糖
2
D.北京冬奥会场馆使用CO 跨临界直冷制冰
2
答案 D
解析 CO 跨临界直冷制冰是利用液态CO 汽化吸热导致环境温度下降,从而使水结冰,属
2 2
于物理变化,D符合题意。
5.(2023·湖北校联考模拟)茶多酚是茶叶中多酚类物质的总称,具有抗癌、抗衰老等功能。
茶叶的手工制作过程非常复杂:“采回的鲜茶叶,要及时、均匀地薄摊在洁净的竹匾上……
要用火力均匀的木炭火……在锅内手工翻炒、烘焙……”。下列有关说法正确的是( )
A.“翻炒”时,木炭火的温度越高越好
B.用开水刚泡制的茶水pH=7
C.瓷器茶杯属于新型的无机非金属材料
D.茶多酚能有效清除人体的活性氧自由基,起到抗衰老作用
答案 D
解析 茶多酚的性质不稳定,在高温下易被空气中的氧气氧化,故“翻炒”时,木炭火的温
度不是越高越好,A错误;100 ℃时水的离子积K =10-12,此时中性溶液的pH=6,且酚
w
羟基具有弱酸性,茶叶中含有茶多酚,故用开水刚泡制的茶水pH应该小于6,B错误;瓷
器茶杯是陶瓷制品,是无机硅酸盐材料,属于传统的无机非金属材料,C错误。
6.澳大利亚科学家发现了纯碳新材料“碳纳米泡沫”,每个泡沫含有约4 000个碳原子,
直径约6~9 nm,在低于-183 ℃时,泡沫具有永久磁性,下列叙述正确的是( )
A.“碳纳米泡沫”与石墨互为同位素
B.把“碳纳米泡沫”分散到适当的溶剂中,能产生丁达尔效应
C.“碳纳米泡沫”是一种新型的碳化合物
D.“碳纳米泡沫”和金刚石的性质相同
答案 B
解析 “碳纳米泡沫”属于碳单质,与石墨互为同素异形体,A、C错误;在低于-183 ℃时,泡沫具有永久磁性,金刚石没有磁性,二者性质不同,D错误。
7.分类法是一种行之有效、简单易行的科学方法,某同学用如表所示的形式对所学知识进
行分类,其中甲与乙、丙、丁、戊是包含关系。
序号 甲 乙、丙、丁、戊
① 常见干燥剂 浓硫酸、石灰石、碱石灰、五氧化二磷
② 常见合金 不锈钢、青铜、硬铝、生铁
③ 基本营养物质 油脂、蛋白质、纤维素、无机盐
④ 腐蚀品 盐酸、浓硫酸、烧碱、硝酸
⑤ 碱性氧化物 过氧化钠、氧化镁、氧化铝、氧化铁
⑥ 弱电解质 次氯酸、一水合氨、水、醋酸
正确的组合是( )
A.①② B.④⑤⑥
C.②④⑥ D.①⑤⑥
答案 C
解析 ①中,石灰石不具备吸水性,不能作干燥剂;③中,纤维素不能被人体吸收,不属于
营养物质;⑤中,过氧化钠不是碱性氧化物,氧化铝是两性氧化物。
8.近日,科学研究发现液态水或存在第二形态,当水被加热到40~60 ℃时,它的导热性、
折射率、导电性等属性也会发生改变。下列说法正确的是( )
A.氢、氧两种元素只能组成HO
2
B.导热性、折射率、导电性属于水的化学性质
C.0 ℃时冰的密度比液态水的密度小
D.液态水两种形态间的转化属于化学变化
答案 C
解析 A项,氢、氧两种元素除组成HO外还可以组成HO ,错误;B项,导热性、折射
2 2 2
率、导电性属于水的物理性质,错误;C项,冰浮在水上,说明冰的密度小于液态水,正确;
D项,液态水两种形态间的转化属于物理变化,错误。
9.(2023·湖北,3)工业制备高纯硅的主要过程如下:
石英砂―――――→粗硅――→SiHCl ――→高纯硅
3
下列说法错误的是( )
A.制备粗硅的反应方程式为SiO+2C=====Si+2CO↑
2
B.1 mol Si含Si—Si的数目约为4×6.02×1023
C.原料气HCl和H 应充分去除水和氧气
2
D.生成SiHCl 的反应为熵减过程
3
答案 B
解析 在晶体硅中,每个Si与其周围的4个Si形成共价键并形成空间网状结构,因此,平均每个Si形成2个共价键, 1 mol Si含Si—Si的数目约为2×6.02×1023,B说法错误;
SiHCl 易水解,氢气中混有氧气易爆炸,原料气HCl和H 应充分去除水和氧气 ,C说法正
3 2
确;Si+3HCl=====SiHCl +H ,该反应是气体分子数减少的反应,因此,生成SiHCl 的反
3 2 3
应为熵减过程,D说法正确。
10.我国古代发明或技术应用中,其工作原理不涉及化学反应的是( )
①指南针 ②黑火药 ③转轮排字 ④黏土制陶瓷 ⑤用玻璃瓶盛装“强水”(古书中记载
一种能腐蚀五金的液体) ⑥用明矾溶液清洗铜镜表面的铜锈 ⑦湿法炼铜
A.①③④⑤ B.①③⑤
C.①③④⑦ D.①③⑤⑥
答案 B
解析 ⑤用玻璃瓶盛装“强水”(古书中记载一种能腐蚀五金的液体),这里所说的强水应该
是硝酸,硝酸不会和玻璃(主要成分是二氧化硅)发生反应,没有发生化学变化,正确。
11.下列说法在一定条件下可以实现的是( )
①酸性氧化物与碱反应 ②弱酸与盐溶液反应可生成强酸 ③没有水生成,也没有沉淀和气
体生成的复分解反应 ④两种酸溶液充分反应后的溶液呈中性 ⑤有单质参加的非氧化还原
反应 ⑥两种含氧化合物反应的产物有气体
A.全部 B.只有②④⑤⑥
C.只有①②③⑤ D.只有③④⑤⑥
答案 A
解析 SO 可与NaOH溶液反应,①可以实现;HS+CuSO ===CuS↓+HSO ,②可以实现
2 2 4 2 4
HSO +2CHCOONa===2CHCOOH+NaSO ,没有水、沉淀和气体生成,③可以实现;
2 4 3 3 2 4
HSO +2HS===3S↓+3HO,④可以实现;同素异形体之间的转化不属于氧化还原反应,
2 3 2 2
但有单质参加,⑤可以实现;2NaO+2HO===4NaOH+O↑,⑥可以实现。
2 2 2 2
12.在一定条件下进行的如图化学反应,已知 A、B、C中均含有同种元素,则下列对应物
质不正确的是( )
选项 A物质 B物质 C物质 D物质
A NaOH溶液 NaCO 溶液 NaHCO 溶液 CO
2 3 3 2
B Fe FeCl FeCl Cl
2 3 2
C AlCl 溶液 Al(OH) NaAlO 溶液 NaOH溶液
3 3 2
D HS S SO O
2 2 2
答案 B
解析 若A为Fe,D为Cl,Fe与Cl 反应生成FeCl 而不是FeCl ,B错误。
2 2 3 213.胶体金即金溶胶,其具有光吸收性、呈色性和胶体性等特点。免疫胶体金技术作为胶体
金标记物, 可实现对抗原抗体的测定。
用白磷还原法可制得一种金的分散系,该分散系在临床诊断及药物检测等方面有着广泛的应
用。
其操作步骤如下:
a.取20%白磷(①)的乙醚溶液0.5 mL,加蒸馏水(②)60 mL
b.先滴加1%氯化金水溶液(③)0.75 mL,再滴加0.1 mol·L-1 KCO(④)溶液0.6 mL,振荡
2 3
变成棕红色
c.加热煮沸至溶液变成透明红色
d.分离提纯,除去无机溶质
所得分散系中,金颗粒直径在5~12 nm。
请回答下列问题:
(1)上述物质①②③④中属于单质的是__________(填序号,下同),属于化合物的是________,
属于盐的是______。
(2)该分散系属于________,其分散质是________。
答案 (1)① ②④ ④ (2)胶体 金颗粒
14.(2023·青岛模拟)铁广泛应用于人类的生产、生活。
Ⅰ.铁及其化合物存在如图甲转化关系(部分反应物和反应条件已略去),回答下列问题。
(1)a、b、c三种物质中属于电解质的是________(填化学式)。
(2)①~⑤反应中,既是化合反应又是氧化还原反应的有________(填序号)。写出⑤的化学方
程式:________________________________________________________________________
______________________________________________________________________________。
(3)将e的浓溶液滴加到沸水中可得到红褐色液体,该液体属于一种特殊的分散系。该分散
系中分散质的微粒直径为___________________。鉴别e的浓溶液与该分散系所用方法的原
理 为
______________________________________________________________________________。
Ⅱ.明代《徐光启手迹》记载了以绿矾(FeSO ·7H O)和硝(KNO)为原料制备硝酸的方法,其
4 2 3
主要流程如图乙:(4)X为铁的氧化物,X的化学式可能为__________________________________,判断依据
为
________________________________________________________________________________
_______________________________________________________________________________
。
(5)③利用浓硫酸的性质为________(填字母)。
a.强氧化性 b.高沸点
c.酸性 d.脱水性
答案 (1)FeCl 、Fe(OH) (2)②③⑤ 4Fe(OH) +O +2HO===4Fe(OH) (3)1~100 nm
2 2 2 2 2 3
丁达尔效应 (4)Fe O 或Fe O FeSO 分解生成SO 和SO ,部分S元素被还原,则Fe元素
2 3 3 4 4 2 3
应被氧化,所以X为Fe O 或Fe O (5)bc
2 3 3 4
解析 (1)根据物质类别和铁元素的化合价可知,a 为 Fe,b 为 FeCl ,e 为 FeCl ,c 为
2 3
Fe(OH) ,d为Fe(OH) 。a、b、c三种物质中属于电解质的是FeCl 、Fe(OH) 。(2)①置换反
2 3 2 2
应;②氯气与氯化亚铁反应生成氯化铁;③铁在氯气中点燃生成氯化铁;④反应中Fe的化
合价没有发生变化;⑤氢氧化亚铁与氧气、水反应生成氢氧化铁;故①~⑤反应中,既是化
合反应又是氧化还原反应的有②③⑤。(5)③中浓硫酸与硝酸钾发生复分解反应生成硝酸,
硝酸沸点低,易挥发,浓硫酸的沸点高,难挥发,利用了浓硫酸的高沸点和酸性。