文档内容
第 7 讲 化学计算的常用方法
[复习目标] 1.进一步理解物质的量在化学计算中的“桥梁”作用。2.了解化学计算的常用
方法。3.初步建立化学计算的思维模型。
类型一 差量法计算及应用
1.差量法是指根据化学反应前后有关物理量发生的变化找出“理论差量”。 这种差量可以
是质量、物质的量、气态物质的体积或压强、反应过程中的热效应等。
2.差量法解题的关键是找准“理论差量”, 把化学方程式中的对应差量(理论差量)跟差量
(实际差量)列成比例,然后求解。如:
2C(s)+O(g)===2CO(g) Δm(固)/Δn(气)/ΔV(气)
2
2 mol 1 mol 2 mol 24 g 1 mol 22.4 L(标况)
[应用举例]
为了检验某含有NaHCO 杂质的NaCO 样品的纯度,现将 w g样品加热,其质量变为 w
3 2 3 1 2
g,请列式计算该样品中NaCO 的质量分数。
2 3
_______________________________________________________________________________
_______________________________________________________________________________
一、气体差量法应用
1.标准状况下,将20 L CO 和CO的混合气体全部通过足量的NaO 粉末,在相同状况下,
2 2 2
气体体积减少到16 L,则原混合气体中CO的体积为( )
A.4 L B.8 L C.12 L D.16 L
2.在一个容积为6 L的密闭容器中,放入3 L X(g)和2 L Y(g),在一定条件下发生反应:
4X(g)+nY(g)2Q(g)+6R(g),反应达到平衡后,容器内温度不变,混合气体的压强比原
来增大了5%,X的浓度减小,则该反应中的 n值为( )
A.2 B.3 C.4 D.5
二、热重差量法的应用
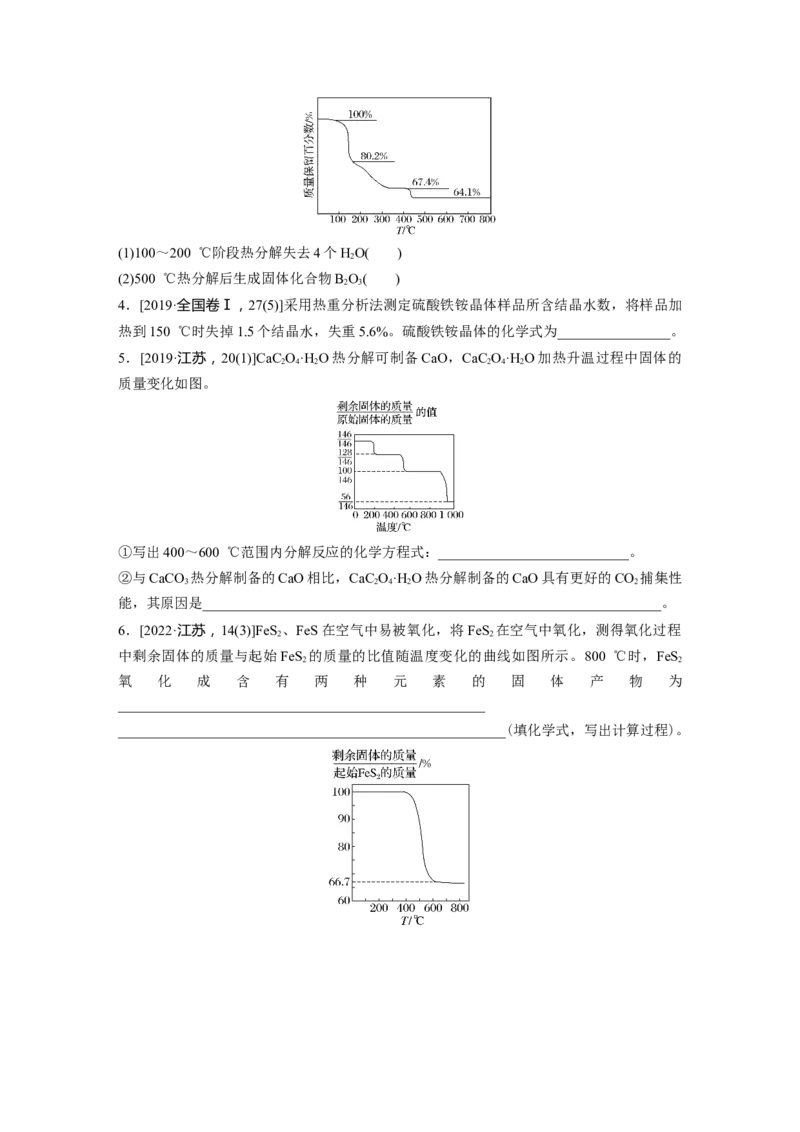
3.(2022·全国乙卷,11改编)NH B O·4H O的热重曲线如图,在200 ℃以下热分解时无刺
4 5 8 2
激性气体逸出。请判断下列说法的正误。(1)100~200 ℃阶段热分解失去4个HO( )
2
(2)500 ℃热分解后生成固体化合物B O( )
2 3
4.[2019·全国卷Ⅰ,27(5)]采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加
热到150 ℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为________________。
5.[2019·江苏,20(1)]CaC O·H O热分解可制备CaO,CaC O·H O加热升温过程中固体的
2 4 2 2 4 2
质量变化如图。
①写出400~600 ℃范围内分解反应的化学方程式:___________________________。
②与CaCO 热分解制备的CaO相比,CaC O·H O热分解制备的CaO具有更好的CO 捕集性
3 2 4 2 2
能,其原因是_________________________________________________________________。
6.[2022·江苏,14(3)]FeS 、FeS在空气中易被氧化,将FeS 在空气中氧化,测得氧化过程
2 2
中剩余固体的质量与起始FeS 的质量的比值随温度变化的曲线如图所示。800 ℃时,FeS
2 2
氧 化 成 含 有 两 种 元 素 的 固 体 产 物 为
____________________________________________________
_______________________________________________________(填化学式,写出计算过程)。类型二 关系式法计算及应用
1.关系式法是物质间的一种简化的式子,它可以把始态的反应物与终态的生成物之间
“量”的关系表示出来,把多步计算简化成一步计算。
2.关系式法解题的关键是建立关系式,建立关系式的方法有:①利用化学方程式中化学计
量数间的关系;②利用原子守恒关系;③利用得失电子守恒关系;④利用化学方程式的加和
等。
[应用举例]
200吨含硫40%的黄铁矿,用接触法可以制得95%的硫酸(不考虑中间过程的损耗)的质量为
多少吨?
________________________________________________________________________________
________________________________________________________________________________
关系式法在滴定计算中的应用
1.[2020·海南,15(5)]用KCr O 滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样
2 2 7
品,用过量稀硫酸溶解,用标准 K Cr O 溶液滴定其中的Fe2+。反应式:Cr O+6Fe2++
2 2 7 2
14H+===2Cr3++6Fe3++7HO;某次实验称取0.280 0 g样品,滴定时消耗浓度为0.030 00
2
mol·
L-1的KCr O 溶液25.10 mL,则样品中铁含量为________%。
2 2 7
2.[2017·全国卷Ⅱ,26(4)]草酸钙沉淀经稀HSO 处理后,用KMnO 标准溶液滴定,通过测
2 4 4
定草酸的量可间接获知钙的含量,滴定反应为MnO+H++HC O―→Mn2++CO +HO。
2 2 4 2 2
实验中称取0.400 g水泥样品,滴定时消耗了0.050 0 mol·L-1的KMnO 溶液36.00 mL,则该
4
水泥(主要成分为Co、SiO 等)样品中钙的质量分数为________。
2
3.[2017·北京,27(1)④]尿素溶液的浓度影响NO 的转化,测定溶液中尿素(M=60 g·mol-1)
2
含量的方法如下:取a g尿素溶液,将所含氮完全转化为 NH ,所得NH 用过量的V mL
3 3 1
c mol·L-1 HSO 溶液吸收完全,剩余HSO 用V mL c mol·L-1 NaOH溶液恰好中和,则
1 2 4 2 4 2 2
尿素溶液中溶质的质量分数是________________(已知尿素[CO(NH)]水溶液热分解为NH
2 2 3
和CO)。
2
4.[2021·山东,18(3)节选]利用碘量法测定WCl 产品纯度,实验如下:
6
①称量:将足量CS(易挥发)加入干燥的称量瓶中,盖紧称重为 m g;开盖并计时1分钟,
2 1
盖紧称重为 m g;再开盖加入待测样品并计时1分钟,盖紧称重为m g,则样品质量为
2 3
____________g(不考虑空气中水蒸气的干扰)。
②滴定:先将 WCl 转化为可溶的 NaWO ,通过 IO 离子交换柱发生反应:WO+
6 2 4Ba(IO)===BaWO +2IO;交换结束后,向所得含IO的溶液中加入适量酸化的KI溶液,发
3 2 4
生反应:IO+5I-+6H+===3I +3HO;反应完全后,用NaSO 标准溶液滴定,发生反应:
2 2 2 2 3
I +2SO===2I-+SO。滴定达终点时消耗 c mol·L-1的NaSO 溶液 V mL,则样品中
2 2 4 2 2 3
WCl(摩尔质量为M g·mol-1)的质量分数为____________________。
6
类型三 守恒法计算及应用
1.守恒法是一种整合的思维方法,就是物质在发生“变化”或两物质在发生“相互作用”
的过程中某些物理量的总量保持“不变”,分析时淡化中间过程,关注最终组成,利用守恒
关系进行整体分析。
2.守恒法解题的关键是找准研究对象的始态和终态或相互间的关系,列出对应守恒表达式,
常见守恒关系有元素守恒、电荷守恒、得失电子守恒等。
注:得失电子守恒见第4讲考点二 电子守恒法计算及应用。
一、元素守恒
1.(2022·浙江1月选考,27)某同学设计实验确定Al(NO )·xHO的结晶水数目。称取样品
3 3 2
7.50 g,经热分解测得气体产物中有NO 、O 、HNO 、HO,其中HO的质量为3.06 g;残
2 2 3 2 2
留的固体产物是Al O,质量为1.02 g。计算:
2 3
(1)x=________________________________________________________________________(写
出计算过程)。
________________________________________________________________________________
________________________________________________________________________________
(2)气体产物中n(O )=__________mol。
2
2.[2022·福建,11(2)]取5.0 g某粉煤灰(其中含质量分数为30%的Al O),加硫酸酸浸Al3
2 3
+,一段时间后,过滤、干燥后得到3.0 g浸渣(分析知含质量分数为8%的Al O),Al O 的
2 3 2 3
浸出率为__________。
3.[2022·湖南,15(6)]某实验小组以BaS溶液为原料制备BaCl ·2H O,并用重量法测定产品
2 2
中BaCl ·2H O的含量。设计了如下实验方案:
2 2
①称取产品0.500 0 g,用100 mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的0.100 mol·L-1 HSO 溶液;
2 4
③沉淀完全后,60 ℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
0.466 0 g。
产品中BaCl ·2H O的质量分数为________(保留三位有效数字)。
2 2二、电荷守恒(电中性原则)
4.对PM 样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分
2.5
及其平均浓度如下表:
离子 K+ Na+ NH SO NO Cl-
浓度/ (mol·L-1) 4×10-6 6×10-6 2×10-5 4×10-5 3×10-5 2×10-5
根据表中数据判断PM 的酸碱性为______,试样的pH=________。
2.5
5.在a L Al (SO ) 和(NH )SO 的混合溶液中加入b mol BaCl ,恰好使溶液中的SO完全沉
2 4 3 4 2 4 2
淀;加入足量强碱并加热可得到c mol NH ,则原溶液中Al3+的浓度(mol·L-1)为( )
3
A. B.
C. D.
类型四 列方程组进行二元混合物的计算
计算中的数学思想:在两种物质组成的混合物中,一般可设两个未知数 x、y,题目中通常
也会给出两个已知量(设为A、B),寻找x、y与A、B的数学关系,由此建立二元一次方程
组进行联解:。
1.取10.80 g某无机矿物盐X(仅含四种元素),将X在惰性气流中加热至完全分解,得到
6.40 g固体FeO、CaO的混合物和气体CO ,且无机矿物盐X能与稀盐酸反应生成CO 气体。
2 2
X 的化学式是________________,在惰性气流中加热 X 至完全分解的化学方程式为
______________________________________________________________________________
______________________________________________________________________________。
2.(2018·浙江11月选考,29)某红色固体粉末可能是Fe O 、Cu O或二者混合物,为探究其
2 3 2
组成,称取m g该固体粉末样品,用足量的稀HSO 充分反应后,称得固体质量为a g。
2 4
已知:Cu O+2H+===Cu+Cu2++HO
2 2
(1)若a=________(用含m的最简式表示),则红色固体粉末为纯净物。
(2)若a=,则红色固体粉末中Fe O 的物质的量为______ mol(用含m的最简式表示)。
2 3