文档内容
第 53 讲 酸碱中和滴定及拓展应用
[复习目标] 1.了解酸碱中和滴定的原理和滴定终点的判断方法,知道指示剂选择的方法。
2.掌握酸碱中和滴定的操作和数据处理误差分析的方法。3.掌握滴定法在定量测定中的应用。
考点一 酸碱中和滴定的原理与操作
1.原理
利用酸碱中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的方法。以标准HCl
溶液滴定待测的 NaOH 溶液,待测的 NaOH 溶液的物质的量浓度为 c(NaOH)=
________________________。
2.酸碱指示剂
(1)熟记:常见酸碱指示剂的变色范围
指示剂 变色范围
石蕊
甲基橙
酚酞
(2)中和滴定时指示剂的选择原则
滴定终点前后溶液的颜色变化对比明显。
①强酸与强碱的中和滴定,到达终点时,pH变化范围很大,可用酚酞,也可用甲基橙;
②强酸滴定弱碱,恰好完全反应时,溶液呈酸性,应选择在酸性范围内变色的指示剂——甲
基橙;
③强碱滴定弱酸,恰好完全反应时,溶液呈碱性,应选择在碱性范围内变色的指示剂——酚
酞;
④一般不用石蕊溶液,原因是其溶液颜色变化对比不明显,且变色范围较大。
3.实验操作与仪器的选择
(1)主要仪器(2)滴定前准备
滴定管:________→洗涤→________→装液→排气泡调液面→记录。
锥形瓶:洗涤→装待测液→加指示剂。
(3)滴定操作
(4)滴定终点
滴入最后半滴标准液,指示剂变色,且在半分钟内不恢复原来的颜色,停止滴定,并记录标
准溶液的体积。
(5)数据处理
按上述操作重复________次,根据每次所用标准液的体积计算待测液的物质的量浓度,最后
求出待测液的物质的量浓度的________。
1.将液面在0 mL处的25 mL的酸式滴定管中的液体全部放出,液体的体积为25 mL( )
2.滴定终点就是酸碱恰好中和的点( )
3.滴定管和锥形瓶在滴定前都应该用待装溶液润洗( )
4.酸碱指示剂越多变色越明显,指示剂至少加入2~3 mL( )
5.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁( )
一、酸碱中和滴定注意事项与数据处理
1.现用中和滴定来测定某NaOH溶液的浓度。
(1)滴定:用________式滴定管盛装c mol·L-1盐酸标准液。如图表示某次滴定时50 mL滴定
管中前后液面的位置。滴定前,读数为________ mL,此次滴定结束后的读数为
________mL,滴定管中剩余液体的体积__________(填“等于”“小于”或“大于”)25.10
mL,可用________________作指示剂。(2)排出碱式滴定管中气泡的方法应采用下图______(填“甲”“乙”或“丙”)的操作,然后
挤压玻璃球使尖嘴部分充满碱液。
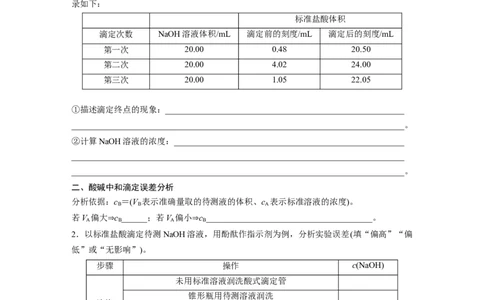
(3)若以酚酞溶液为指示剂,用0.100 0 mol·L-1的标准盐酸测定NaOH溶液的浓度,数据记
录如下:
标准盐酸体积
滴定次数 NaOH溶液体积/mL 滴定前的刻度/mL 滴定后的刻度/mL
第一次 20.00 0.48 20.50
第二次 20.00 4.02 24.00
第三次 20.00 1.05 22.05
①描述滴定终点的现象:________________________________________________________
______________________________________________________________________________。
②计算NaOH溶液的浓度:______________________________________________________
______________________________________________________________________________
______________________________________________________________________________。
二、酸碱中和滴定误差分析
分析依据:c =(V 表示准确量取的待测液的体积、c 表示标准溶液的浓度)。
B B A
若V 偏大⇒c ______;若V 偏小⇒c _______________________________________。
A B A B
2.以标准盐酸滴定待测NaOH溶液,用酚酞作指示剂为例,分析实验误差(填“偏高”“偏
低”或“无影响”)。
步骤 操作 c(NaOH)
未用标准溶液润洗酸式滴定管
锥形瓶用待测溶液润洗
洗涤
未用待测溶液润洗取用待测液的滴定管
锥形瓶洗净后瓶内还残留少量蒸馏水
取液 取碱液的滴定管尖嘴部分有气泡且取液结束前气泡消失
滴定完毕后立即读数,半分钟后颜色又变红
滴定前滴定管尖嘴部分有气泡,滴定后消失
滴定
滴定过程中振荡锥形瓶时有液滴溅出
滴定过程中,向锥形瓶内加少量蒸馏水
读数 滴定前仰视读数或滴定后俯视读数滴定前俯视读数或滴定后仰视读数
滴定管读数要领
以凹液面的最低点为基准,正确读数(虚线部分)和错误读数(实线部分)如图
考点二 酸碱中和滴定曲线的分析
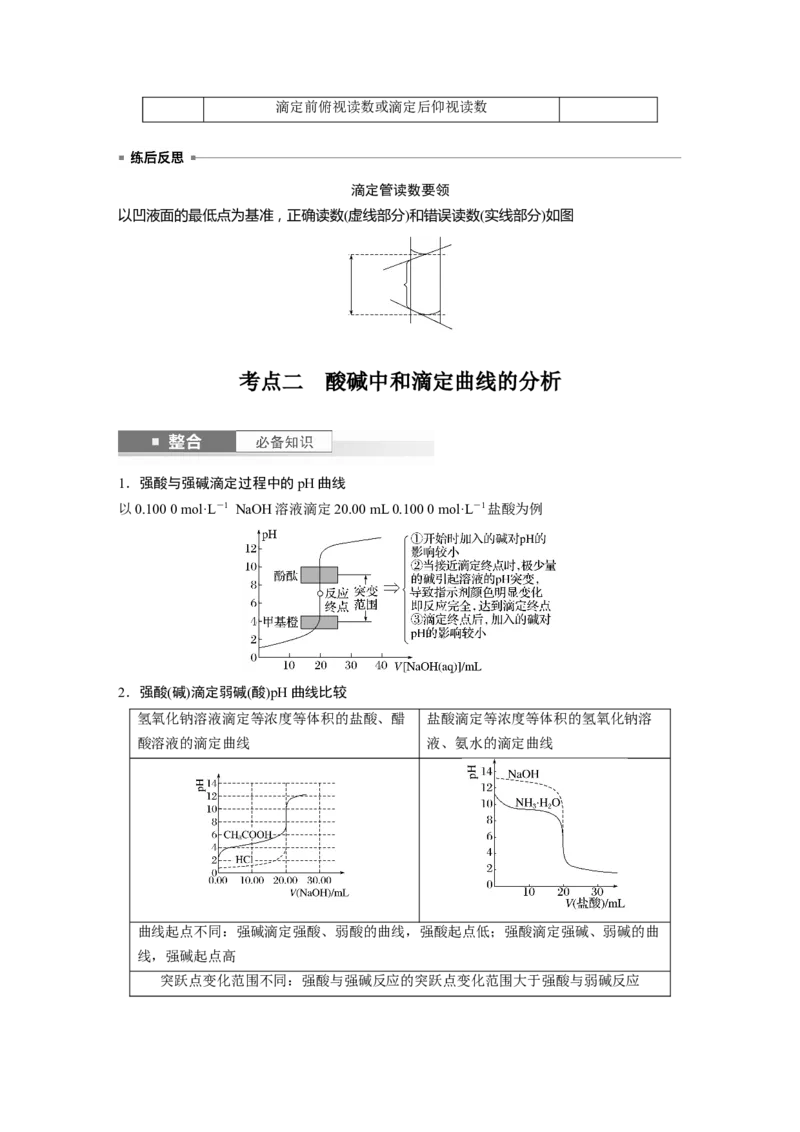
1.强酸与强碱滴定过程中的pH曲线
以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸为例
2.强酸(碱)滴定弱碱(酸)pH曲线比较
氢氧化钠溶液滴定等浓度等体积的盐酸、醋 盐酸滴定等浓度等体积的氢氧化钠溶
酸溶液的滴定曲线 液、氨水的滴定曲线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲
线,强碱起点高
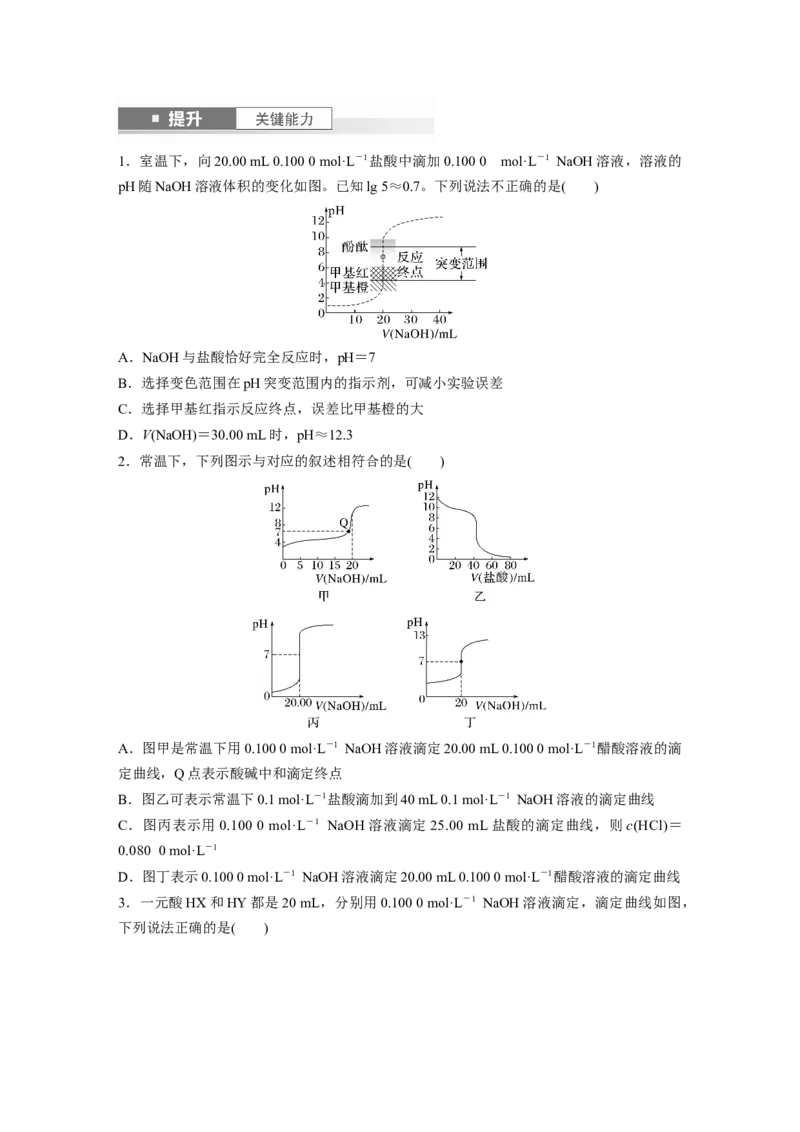
突跃点变化范围不同:强酸与强碱反应的突跃点变化范围大于强酸与弱碱反应1.室温下,向20.00 mL 0.100 0 mol·L-1盐酸中滴加0.100 0 mol·L-1 NaOH溶液,溶液的
pH随NaOH溶液体积的变化如图。已知lg 5≈0.7。下列说法不正确的是( )
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH≈12.3
2.常温下,下列图示与对应的叙述相符合的是( )
A.图甲是常温下用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1醋酸溶液的滴
定曲线,Q点表示酸碱中和滴定终点
B.图乙可表示常温下0.1 mol·L-1盐酸滴加到40 mL 0.1 mol·L-1 NaOH溶液的滴定曲线
C.图丙表示用0.100 0 mol·L-1 NaOH溶液滴定25.00 mL盐酸的滴定曲线,则c(HCl)=
0.080 0 mol·L-1
D.图丁表示0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1醋酸溶液的滴定曲线
3.一元酸HX和HY都是20 mL,分别用0.100 0 mol·L-1 NaOH溶液滴定,滴定曲线如图,
下列说法正确的是( )A.用0.100 0 mol·L-1 NaOH溶液滴定HX时,选用甲基橙作指示剂,测定结果偏低
B.HX可能是HCl,HY可能是CHCOOH
3
C.HX和HY的物质的量浓度可能都为1.000 mol·L-1
D.a点和b点对应溶液的导电性相同
4.室温下,向a点(pH=a)的20.00 mL 1.000 mol·L-1氨水中滴入1.000 mol·L-1盐酸,溶液
pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法错误的是( )
A.将此氨水稀释,溶液的导电能力减弱
B.b点溶液中离子浓度大小可能存在:c(NH)>c(Cl-)>c(OH-)>c(H+)
C.c点时消耗盐酸体积小于20.00 mL
D.a、d两点的溶液,水的离子积K (a)>K (d)
w w
答题规范(7) 滴定终点判断
当滴入最后半滴×××标准溶液后,溶液变成×××色,且半分钟内不恢复原来的颜色。
解答此类题目注意三个关键点:
(1)最后半滴:必须说明是滴入“最后半滴”溶液。
(2)颜色变化:必须说明滴入“最后半滴”溶液后溶液“颜色的变化”。
(3)半分钟:必须说明溶液颜色变化后“半分钟内不再恢复原来的颜色”。
1.用a mol·L-1的盐酸滴定未知浓度的NaOH溶液,用酚酞作指示剂,达到滴定终点的现
象 是
__________________________________________________________________________________________________________________________________________________________;
若用甲基橙作指示剂,滴定终点现象是___________________________________________
_____________________________________________________________________________。
2.用标准碘溶液滴定溶有SO 的水溶液,以测定水中SO 的含量,应选用__________作指
2 2
示剂,达到滴定终点的现象是___________________________________________________
_____________________________________________________________________________。
3.用标准酸性KMnO 溶液滴定溶有SO 的水溶液,以测定水中SO 的含量,是否需要选用
4 2 2
指示剂________(填“是”或“否”),达到滴定终点的现象是________________________
_____________________________________________________________________________。
4.用氧化还原滴定法测定TiO 的质量分数:一定条件下,将TiO 溶解并还原为Ti3+,再用
2 2
KSCN溶液作指示剂,用NH Fe(SO ) 标准溶液滴定Ti3+至全部生成Ti4+,滴定Ti3+时发生
4 4 2
反应的离子方程式为____________________________________________________________,
达到滴定终点的现象是___________________________________________________________
______________________________________________________________________________。
5.用标准KI溶液滴定含有Fe3+的溶液,应选用__________作指示剂,滴定终点现象是
_____________________________________________________________________________
_____________________________________________________________________________。
1.正误判断,正确的打“√”,错误的打“×”。
(1)可用“图1”测定醋酸浓度(2021·河北,3A)( )
(2)可用“图2”量取一定体积的KMnO 溶液(2021·天津,6B)( )
4
(3)碱式滴定管排气泡的操作如“图3”(2022·湖南,4A)( )
(4)用标准液润洗滴定管后,应将润洗液从滴定管上口倒出(2022·浙江6月选考,11A)( )
2.(2023·山东,8~10)一定条件下,乙酸酐[(CH CO) O]醇解反应[(CH CO) O+
3 2 3 2
ROH―→CHCOOR+CHCOOH]可进行完全,利用此反应定量测定有机醇(ROH)中的羟基
3 3
含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入m g ROH样品,充分反应后,加适量水
使剩余乙酸酐完全水解:(CHCO) O+HO―→2CHCOOH。
3 2 2 3③加指示剂并用c mol·L-1 NaOH-甲醇标准溶液滴定至终点,消耗标准溶液V mL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示
剂并用c mol·L-1 NaOH-甲醇标准溶液滴定至终点,消耗标准溶液V mL。
2
(1)对于上述实验,下列做法正确的是( )
A.进行容量瓶检漏时,倒置一次即可
B.滴入半滴标准溶液,锥形瓶中溶液变色,即可判定达滴定终点
C.滴定读数时,应单手持滴定管上端并保持其自然垂直
D.滴定读数时,应双手一上一下持滴定管
(2)ROH样品中羟基含量(质量分数)计算正确的是( )
A.×100%
B.×100%
C.×100%
D.×100%
(3)根据上述实验原理,下列说法正确的是( )
A.可以用乙酸代替乙酸酐进行上述实验
B.若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D.步骤④中,若加水量不足,将导致测定结果偏大
3.[2022·广东,17(4)①]准确测定HAc溶液的浓度。25 ℃时,HAc的K=1.75×10-5≈10-
a
4.76。
查阅资料获悉:一定条件下,按=1配制的溶液中,c(H+)的值等于HAc的K。
a
移取20.00 mL HAc溶液,加入2滴酚酞溶液,用0.100 0 mol·L-1NaOH溶液滴定至终点,消
耗体积为22.08 mL,则该HAc溶液的浓度为________ mol·L-1。
请画出上述过程的滴定曲线示意图并标注滴定终点。
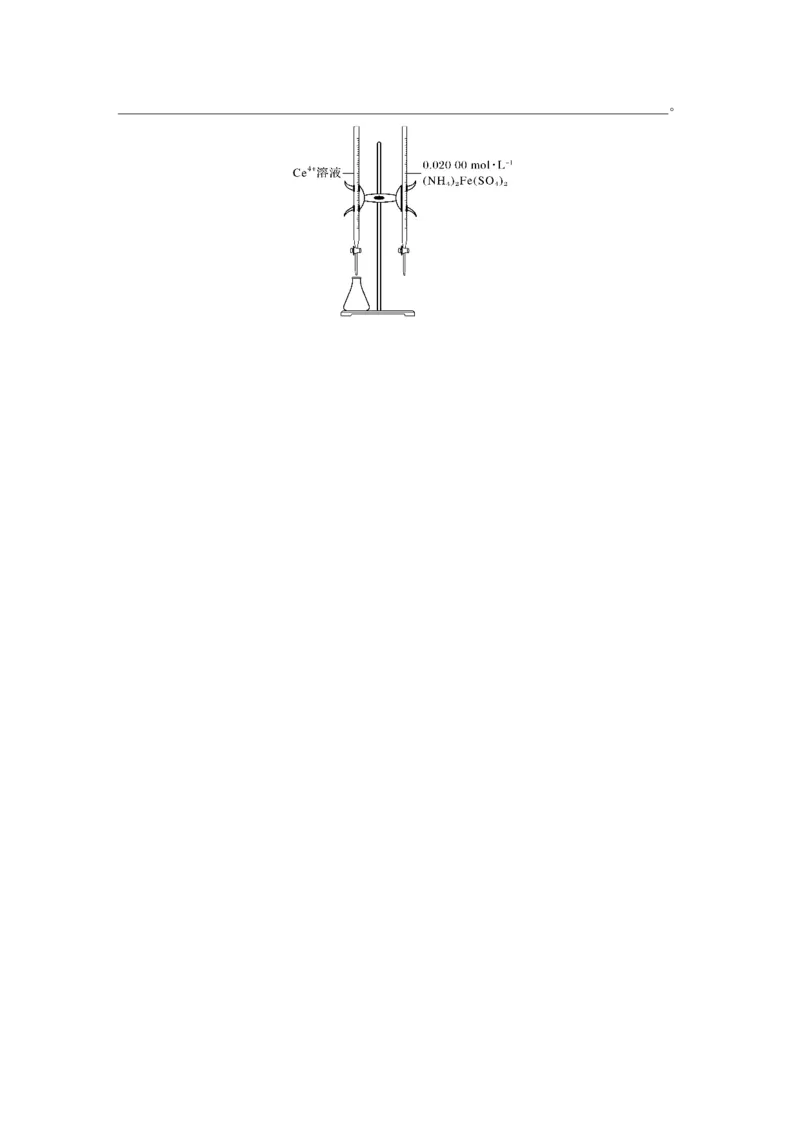
4.[2022·江苏,16(4)]实验中需要测定溶液中Ce3+的含量。已知水溶液中Ce4+可用准确浓度
的(NH )Fe(SO ) 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为
4 2 4 2
亮黄色,滴定反应为Fe2++Ce4+===Fe3++Ce3+。请补充完整实验方案:①准确量取25.00
mL Ce3+溶液[c(Ce3+)约为0.2 mol·L-1],加氧化剂将Ce3+完全氧化并去除多余氧化剂后,用
稀硫酸酸化,将溶液完全转移到 250 mL容量瓶中后定容;②按规定操作分别将0.020 00
mol·L-1
(NH )Fe(SO ) 和待测Ce4+溶液装入如图所示的滴定管中;③_________________________
4 2 4 2______________________________________________________________________________。