文档内容
绝密★启用前 试卷类型:A
2023 届高三年级第一次阶段测试
化学
命题人:江学勇 审题人:梅强
本试卷共8 页,共 20小题,满分100分, 考试用时75分钟。
注意事项:
1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名和考生号、试室号、座位
号填写在答题卡上。用2B铅笔将试卷类型和考生号填涂在答题卡相应位置上。
2.选择题每小题选出答案后,用2B铅笔把答题卡上对应的题目选项的答案信息点涂黑;
如需改动,用橡皮擦干净后,再填涂其他答案。答案不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区
域内相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案,不准使用
铅笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Mn-55
一、单项选择题(共16小题,每小题3分,共48分)
1.中华传统文化博大精深,也蕴含着许多化学知识。下列说法正确的是
A.“四海盛赞铜奔马,人人争说金缕衣”中的“铜奔马”主要是纯铜制品
B.“千淘万漉虽辛苦,吹尽黄沙始到金”中的淘金原理与化学上的萃取一致
C.“以芒硝 (Na SO •10H O) 于风日中消尽水气”得到的是Na SO
2 4 2 2 4
D.“红柿摘下未熟,每蓝用木瓜三枚放入,得气即发,并无涩味”中的“气”是指甲烷
2.下列“劳动小妙招”及其涉及的原理均正确的是
劳动小妙招 原理
A “洁厕灵”和“84消毒液”混合使用 使次氯酸浓度增大
B 在温水中加入含酶洗衣粉洗涤毛衣 适当升温和加酶可增强去污效果
C 用风油精拭去门上的胶印 风油精与胶水发生化学反应
D 用白醋去除铁栏杆上的锈迹 乙酸可与铁锈(Fe O )反应
3 4
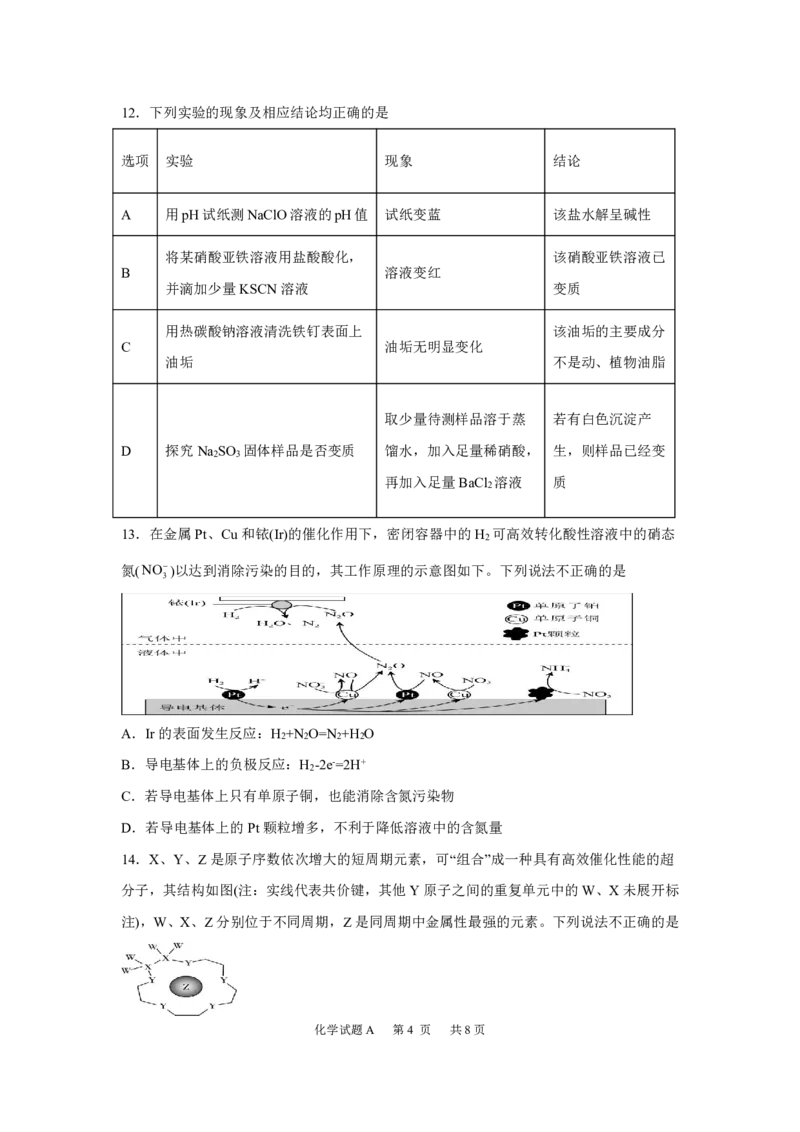
化学试题A 第1 页 共8页3.下列有关物质性质与用途对应关系不正确的是
A.NaHCO 受热不稳定,可用作焙制糕点的膨松剂
3
B.CaO能与SO 反应,可作为工业废气处理时的脱硫剂
2
C.氢气热值高,液氢可作运载火箭的高能清洁燃料
D.Al表面有致密的氧化铝保护层,可用铝制餐具存放酸性及碱性食物
4.亚铁氰化铁又名普鲁士蓝,化学式为Fe
4
FeCN
6
3
,是一种配位化合物,可以用来上
釉、用作油画染料等。下列有关普鲁士蓝构成微粒的符号表征正确的是
A.基态Fe3的价电子排布图为
B.氮原子的结构示意图为
C.CN的电子式为 CN
D.阴离子的结构式为
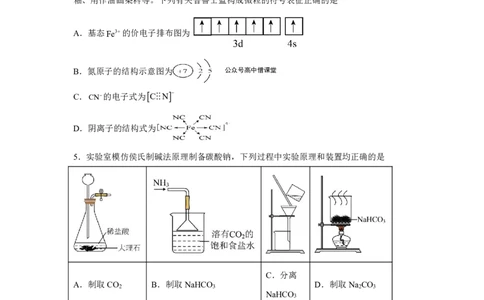
5.实验室模仿侯氏制碱法原理制备碳酸钠,下列过程中实验原理和装置均正确的是
C.分离
A.制取CO B.制取NaHCO D.制取Na CO
2 3 2 3
NaHCO
3
6.在给定条件下,下列选项所示的物质间转化均能实现的是
A.AlCl aq电解AlsNaOHNaAlO aq
3 2
B.Cu S(s) O 2 (g) SO (g) H 2 O 2 ( aq) H SO (aq)
2 高温 2 2 4
C.
FeO sAlFesCl 2FeCl
2 3 高温 点燃 2
D.SO(g)CaCl2 (aq)CaSO(s)O2CaSO(s)
2 3 4
化学试题A 第2 页 共8页7.设N 表示阿伏加德罗常数的值。下列叙述正确的是
A
A.71gCl 溶于适量水中,所得溶液中Cl 和ClO-微粒总数为N
2 2 A
B.1L1mol/LH O 溶液完全反应,转移的电子数目一定为2N
2 2 A
C.标准状况下,22.4LCCl 中含有C—Cl键的个数为4N
4 A
D.7.8gNa S和Na O 的混合物中,含有的离子总数为0.3N
2 2 2 A
8.下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是
A 少量SO 通入Ba(OH) 溶液 过量SO 通入少量Ba(OH) 溶液
2 2 2 2
B 少量浓氨水滴入Al (SO ) 溶液 少量Al (SO ) 溶液滴入浓氨水
2 4 3 2 4 3
C 0.1molCl 通入含0.2molFeBr 的溶液 0.3molCl 通入含0.2molFeBr 溶液中
2 2 2 2
D Na CO 溶液与少量H SO 溶液相混合 Na CO 溶液与过量稀H SO 相混合
2 3 2 4 2 3 2 4
9.下列指定反应的离子方程式正确的是
A.向Ba(HCO ) 溶液中加入少量KOH溶液:Ba2++2HCO-+2OH-=BaCO ↓+CO2-+2H O
3 2 3 3 3 2
B.向Fe(SCN) 溶液中滴入几滴0.01mol·L-1NaOH溶液:Fe3++3OH−=Fe(OH) ↓
3 3
C.已知次磷酸钠(NaH PO )属于正盐,向次磷酸(H PO 为弱酸)溶液中加入足量NaOH
2 2 3 2
溶液:H PO +3OH−=PO3-+3H O
3 2 2 2
D.K S溶液久置于空气中会变浑浊:2S2−+2H O+O = 2S↓+4OH−
2 2 2
10.神舟十二号与天和一号成功对接是对美国科技霸凌的一次大突围。神舟十二号全面使用
国产芯片,其中制作芯片刻蚀液为硝酸与氢氟酸的混合溶液,其工艺涉及的反应为:
Si+HNO +6HF=H SiF +HNO +H ↑+H O,下列说法正确的是
3 2 6 2 2 2
A.H SiF 中Si元素的化合价为+6价
2 6
B.该反应中,HNO 仅作氧化剂
3
C.该反应中,生成2.24LH 时,被氧化的Si为0.1mol
2
D.芯片刻蚀液可用稀硝酸代替
11.下列各组离子,在指定溶液中可以大量共存的是
A.无色透明溶液中:Ca2+、H+、Cl-、Cu2+
B.NO-大量存在的溶液中:Fe2+、Cl-、NH +、K+
3 4
C.碱性溶液中:Al3+、Mg2+、HCO-、SO2-
3 4
D.能使甲基橙变红的溶液中:Na+、NH +、SO 2-、Fe3+
4 3
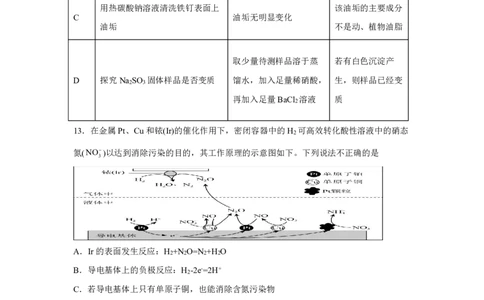
化学试题A 第3 页 共8页12.下列实验的现象及相应结论均正确的是
选项 实验 现象 结论
A 用pH试纸测NaClO溶液的pH值 试纸变蓝 该盐水解呈碱性
将某硝酸亚铁溶液用盐酸酸化, 该硝酸亚铁溶液已
B 溶液变红
并滴加少量KSCN溶液 变质
用热碳酸钠溶液清洗铁钉表面上 该油垢的主要成分
C 油垢无明显变化
油垢 不是动、植物油脂
取少量待测样品溶于蒸 若有白色沉淀产
D 探究Na SO 固体样品是否变质 馏水,加入足量稀硝酸, 生,则样品已经变
2 3
再加入足量BaCl 溶液 质
2
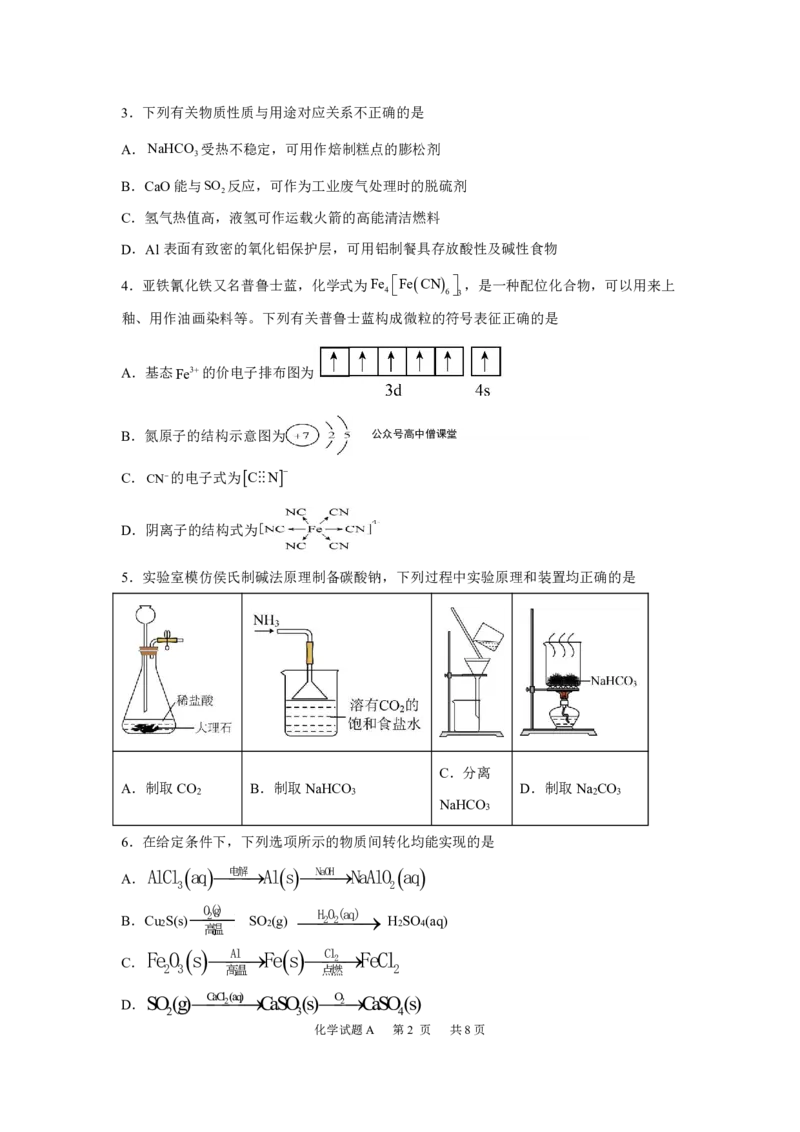
13.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H 可高效转化酸性溶液中的硝态
2
氮(NO)以达到消除污染的目的,其工作原理的示意图如下。下列说法不正确的是
3
A.Ir的表面发生反应:H +N O=N +H O
2 2 2 2
B.导电基体上的负极反应:H -2e-=2H+
2
C.若导电基体上只有单原子铜,也能消除含氮污染物
D.若导电基体上的Pt颗粒增多,不利于降低溶液中的含氮量
14.X、Y、Z是原子序数依次增大的短周期元素,可“组合”成一种具有高效催化性能的超
分子,其结构如图(注:实线代表共价键,其他Y原子之间的重复单元中的W、X未展开标
注),W、X、Z分别位于不同周期,Z是同周期中金属性最强的元素。下列说法不正确的是
化学试题A 第4 页 共8页A.X单质不存在能导电的晶体
B.W、X、Y可形成多种弱酸
C.Y与Z可组成阴阳离子数之比为1∶2的离子晶体
D.ZW与水发生反应,生成1mol W 时转移1mol电子
2
15.LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:
提示:已知滤渣中含有固体硫 。下列说法不正确的是
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序
2
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为Li CO +2HBr=CO +2LiBr+H O
2 3 2 2
D.参与反应的nBr :n(BaS):nH SO 为1∶1∶1
2 2 4
16.将SO 分别通入无氧、有氧的浓度均为0.1mol•L-1的BaCl 溶液和Ba(NO ) 溶液中,除
2 2 3 2
BaCl 溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图。下列说法不正确
2
的是
A.曲线a所示溶液pH降低的原因:SO +H O H SO
2 2 2 3
B.依据曲线b可推知0.2mol•L-1KNO 溶液(无氧)能氧化SO
3 2
C.曲线d所表示的过程中NO是氧化SO 的主要微粒
3 2
D.曲线c所示溶液中发生反应的离子方程式为:2Ba2++2SO +O +2H O=BaSO ↓+4H+
2 2 2 4
二、非选择题(共4题,共52分)
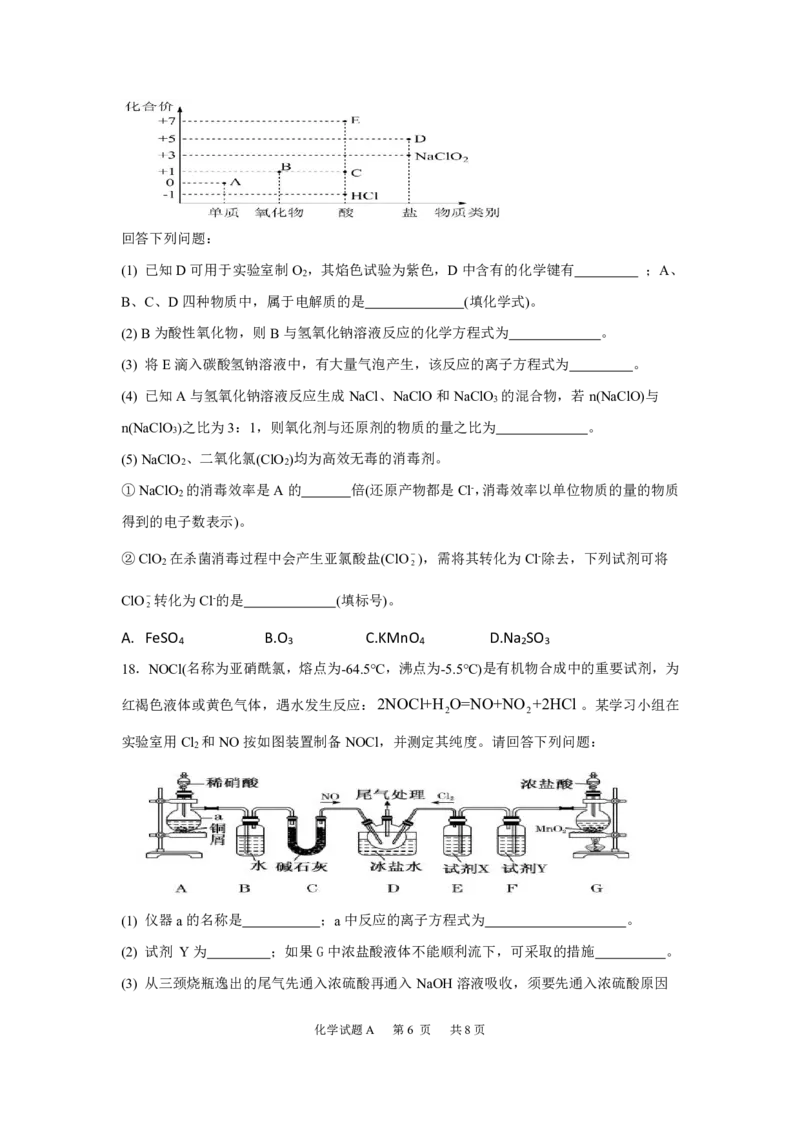
17.利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部
分物质类别的对应关系。
化学试题A 第5 页 共8页回答下列问题:
(1) 已知D可用于实验室制O ,其焰色试验为紫色,D中含有的化学键有 ;A、
2
B、C、D四种物质中,属于电解质的是 (填化学式)。
(2)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为 。
(3) 将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为 。
(4) 已知A与氢氧化钠溶液反应生成NaCl、NaClO和NaClO 的混合物,若n(NaClO)与
3
n(NaClO )之比为3:1,则氧化剂与还原剂的物质的量之比为 。
3
(5)NaClO 、二氧化氯(ClO )均为高效无毒的消毒剂。
2 2
①NaClO 的消毒效率是A的 倍(还原产物都是Cl-,消毒效率以单位物质的量的物质
2
得到的电子数表示)。
②ClO 在杀菌消毒过程中会产生亚氯酸盐(ClO),需将其转化为Cl-除去,下列试剂可将
2 2
ClO转化为Cl-的是 (填标号)。
2
A. FeSO B.O C.KMnO D.Na SO
4 3 4 2 3
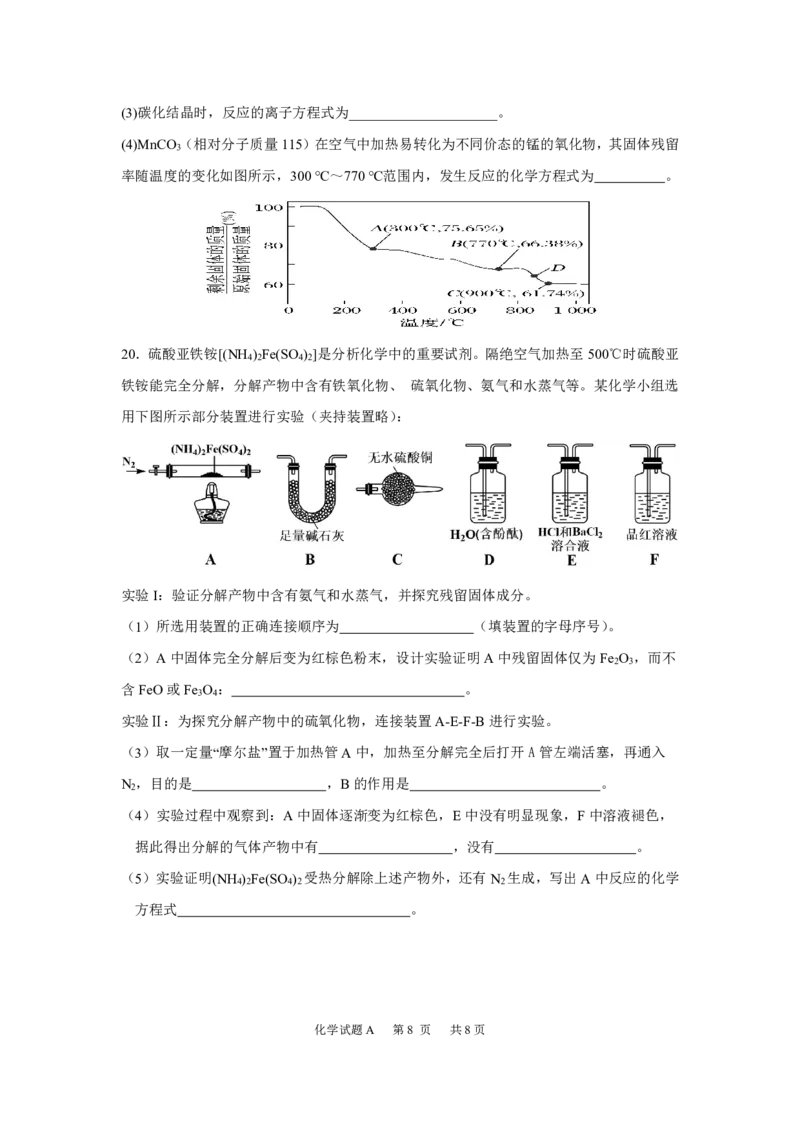
18.NOCl(名称为亚硝酰氯,熔点为-64.5℃,沸点为-5.5℃)是有机物合成中的重要试剂,为
红褐色液体或黄色气体,遇水发生反应:2NOCl+H O=NO+NO +2HCl 。某学习小组在
2 2
实验室用Cl 和NO按如图装置制备NOCl,并测定其纯度。请回答下列问题:
2
(1) 仪器a的名称是 ;a中反应的离子方程式为 。
(2) 试剂 Y为 ;如果G中浓盐酸液体不能顺利流下,可采取的措施 。
(3) 从三颈烧瓶逸出的尾气先通入浓硫酸再通入NaOH溶液吸收,须要先通入浓硫酸原因
化学试题A 第6 页 共8页是 。
(4)NOCl与NaOH溶液反应的化学方程式为 。
(已知:NO+NO+2NaOH=2NaNO+HO)
2 2 2
(5)测量产物NOCl纯度:取三颈烧瓶中所得产物mg溶于水,配制成250mL溶液,取出
25.00mL,用cmol·L-1AgNO 标准溶液滴定至终点,消耗标准溶液的体积为VmL,产物中
3
NOCl纯度的计算式为 。
19.氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下:
已知:① 菱锰矿的主要成分是MnCO ,还含少量Fe、Al、Ca、Mg等元素。
3
② 相关金属离子[c (Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Al3+ Fe3+ Fe2+ Ca2+ Mn2+ Mg2+
开始沉淀的pH 3.8 1.5 6.3 10.6 8.8 9.6
沉淀完全的pH 5.2 2.8 8.3 12.6 10.8 11.6
③ 常温下,CaF 、MgF 的溶度积分别为1.46×10-10、7.42×10-11。
2 2
回答下列问题:
(1)“焙烧”时发生的主要反应的化学方程式为 。
分析图1,氯化铵焙烧菱锰矿的最佳条件是:焙烧温度为500℃。分析选择反应温度不高于
500℃的原因是______________________________。
(2)浸出液“净化除杂”过程如下:首先加入MnO 将Fe2+氧化为Fe3+,反应的离子方程式
2
为 ;再调节溶液的pH将Al3+、Fe3+变为沉淀除去,溶液pH的范围
为__________;然后加入NH F 除去 。
4
化学试题A 第7 页 共8页(3)碳化结晶时,反应的离子方程式为_____________________。
(4)MnCO(相对分子质量115)在空气中加热易转化为不同价态的锰的氧化物,其固体残留
3
率随温度的变化如图所示,300℃~770℃范围内,发生反应的化学方程式为 。
20.硫酸亚铁铵[(NH ) Fe(SO ) ]是分析化学中的重要试剂。隔绝空气加热至500℃时硫酸亚
4 2 4 2
铁铵能完全分解,分解产物中含有铁氧化物、 硫氧化物、氨气和水蒸气等。某化学小组选
用下图所示部分装置进行实验(夹持装置略):
实验I:验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
(1)所选用装置的正确连接顺序为 (填装置的字母序号)。
(2)A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe O ,而不
2 3
含FeO或Fe O : 。
3 4
实验Ⅱ:为探究分解产物中的硫氧化物,连接装置A-E-F-B进行实验。
(3)取一定量“摩尔盐”置于加热管A中,加热至分解完全后打开A管左端活塞,再通入
N ,目的是 ,B的作用是 。
2
(4)实验过程中观察到:A中固体逐渐变为红棕色,E中没有明显现象,F中溶液褪色,
据此得出分解的气体产物中有 ,没有 。
(5)实验证明(NH ) Fe(SO ) 受热分解除上述产物外,还有N 生成,写出A中反应的化学
4 2 4 2 2
方程式 。
化学试题A 第8 页 共8页