文档内容
微专题17 金属及其化合物制备流程(Ti)
钛:元素符号Ti,原子序数22,原子量47.90,外围电子排布3d24s2,位于第四周期ⅣB
族,主要化合价+2、+3、+4。
一、物理性质:
银白色有光泽金属,有良好的延展性,密度4.54克/厘米3,熔点1660±10℃,沸点
3287℃。
二、化学性质:
表面易形成致密氧化物保护层,使化学性质变得不活动。加热时,在空气中燃烧生成
TiO2。室温时不与水、稀盐酸、稀硫酸和硝酸反应。但能被氢氟酸,熔融碱侵蚀。也能
跟热浓盐酸和王水反应。有良好的抗腐蚀性能。
三、用途:
钛和钛的合金广泛用于制造飞机、火箭、卫星、宇宙飞船、舰艇、汽轮机、化工设备、
电讯器材、人造骨骼等。1791年英国人格列高尔发现钛。在地壳中丰度0.42%,主要矿
物有金红石TiO,钛铁矿FeTiO 等。用镁、钠还原四氯化钛制得。
3
*最后附钛的化合物
四、工业制备:
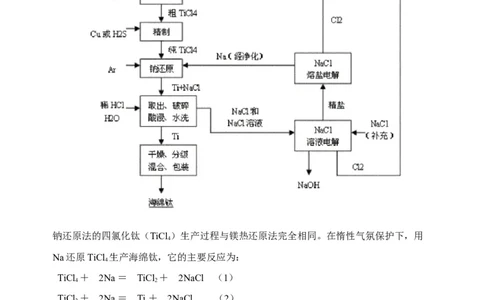
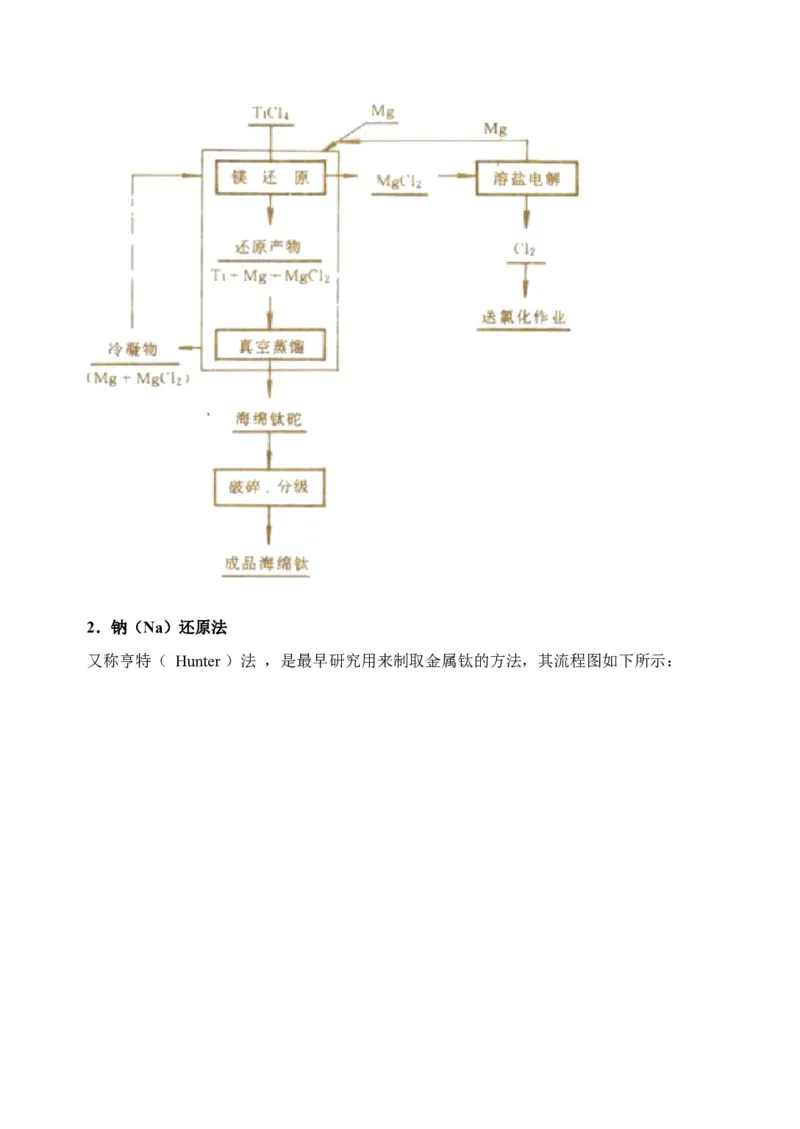
1.海绵钛冶炼工艺
用镁还原四氯化钛(TiCl )制取金属钛的过程,是金属钛生产的主要方法之一。还原作
4
业在高温、惰性气体保护气氛中进行,还原产物主要采用真空蒸馏法分离出剩余的金属
镁和MgCl ,获得海绵状金属钛。其工艺特征是在镁热还原TiCl 结束后,便将热态还原
2 4
产物在高温下直接转入真空蒸馏分离金属镁和MgCl ,这是镁热还原法工业化以来的重大
2
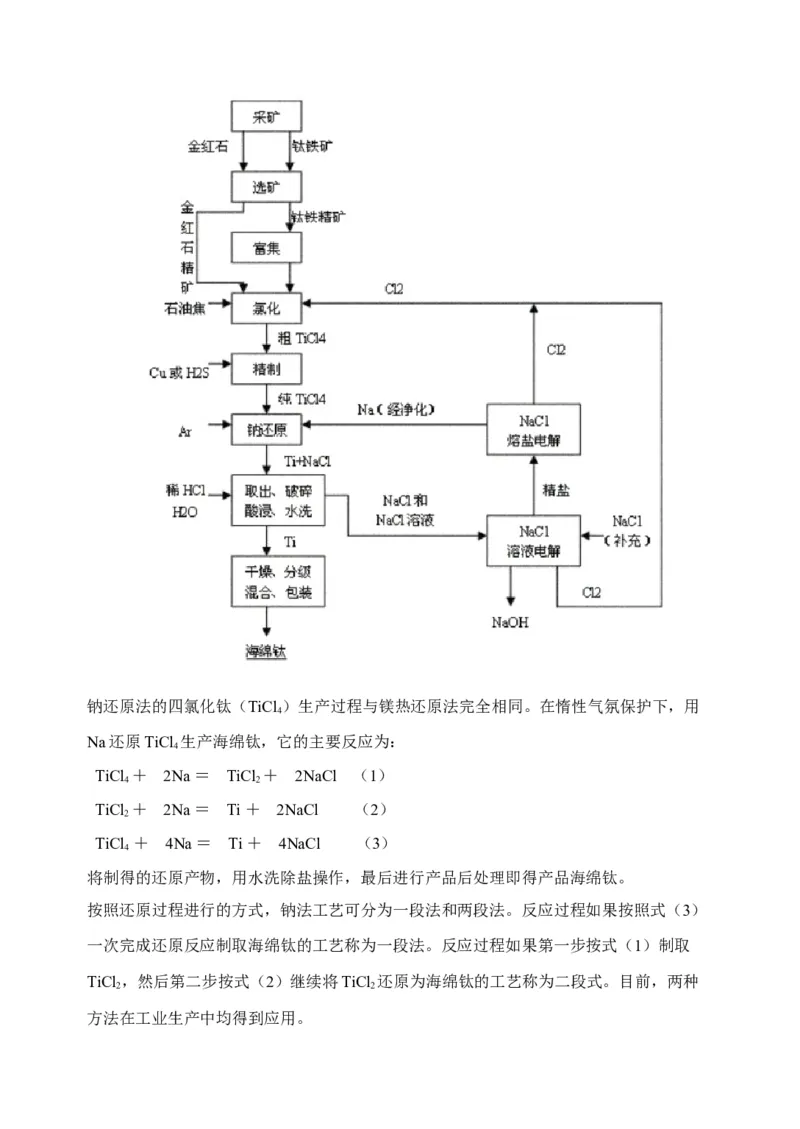
技术进步。工艺流程如下:2.钠(Na)还原法
又称亨特( Hunter )法 ,是最早研究用来制取金属钛的方法,其流程图如下所示:钠还原法的四氯化钛(TiCl )生产过程与镁热还原法完全相同。在惰性气氛保护下,用
4
Na还原TiCl 生产海绵钛,它的主要反应为:
4
TiCl + 2Na = TiCl + 2NaCl (1)
4 2
TiCl + 2Na = Ti + 2NaCl (2)
2
TiCl + 4Na = Ti + 4NaCl (3)
4
将制得的还原产物,用水洗除盐操作,最后进行产品后处理即得产品海绵钛。
按照还原过程进行的方式,钠法工艺可分为一段法和两段法。反应过程如果按照式(3)
一次完成还原反应制取海绵钛的工艺称为一段法。反应过程如果第一步按式(1)制取
TiCl ,然后第二步按式(2)继续将TiCl 还原为海绵钛的工艺称为二段式。目前,两种
2 2
方法在工业生产中均得到应用。【专题精练】
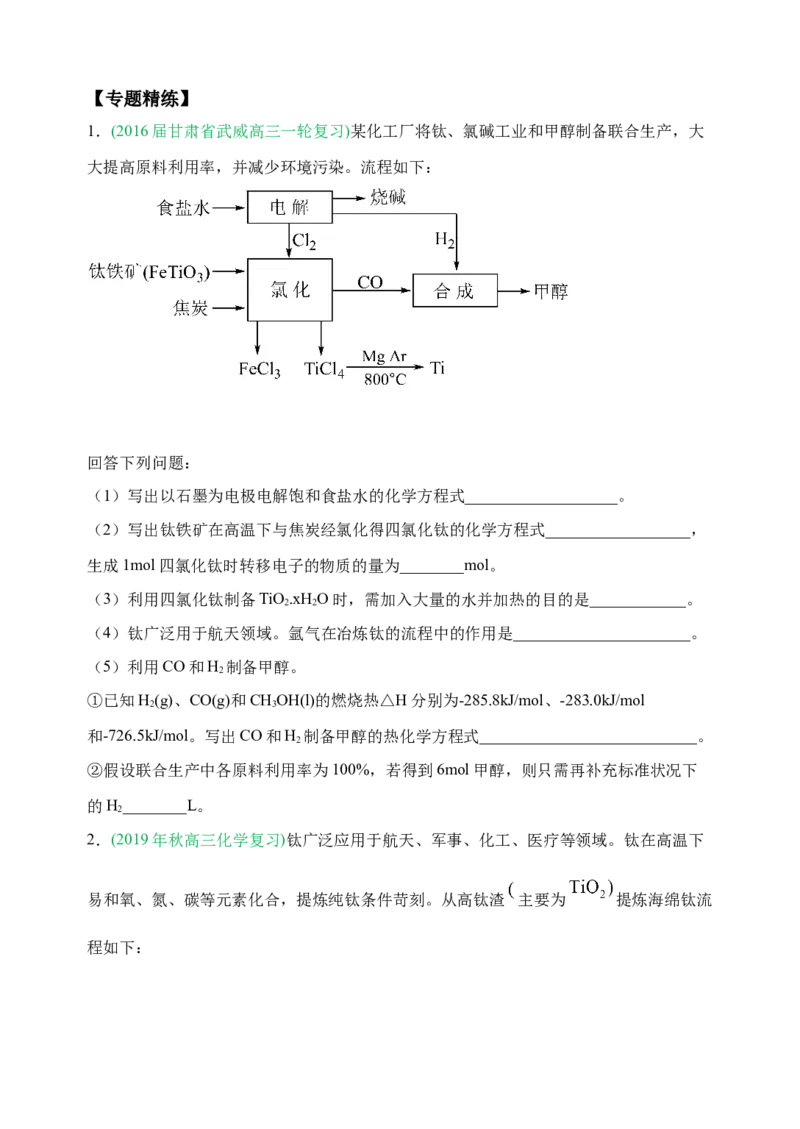
1.(2016届甘肃省武威高三一轮复习)某化工厂将钛、氯碱工业和甲醇制备联合生产,大
大提高原料利用率,并减少环境污染。流程如下:
回答下列问题:
(1)写出以石墨为电极电解饱和食盐水的化学方程式___________________。
(2)写出钛铁矿在高温下与焦炭经氯化得四氯化钛的化学方程式__________________,
生成1mol四氯化钛时转移电子的物质的量为________mol。
(3)利用四氯化钛制备TiO.xH O时,需加入大量的水并加热的目的是____________。
2 2
(4)钛广泛用于航天领域。氩气在冶炼钛的流程中的作用是______________________。
(5)利用CO和H 制备甲醇。
2
①已知H(g)、CO(g)和CHOH(l)的燃烧热△H分别为-285.8kJ/mol、-283.0kJ/mol
2 3
和-726.5kJ/mol。写出CO和H 制备甲醇的热化学方程式___________________________。
2
②假设联合生产中各原料利用率为100%,若得到6mol甲醇,则只需再补充标准状况下
的H________L。
2
2.(2019年秋高三化学复习)钛广泛应用于航天、军事、化工、医疗等领域。钛在高温下
易和氧、氮、碳等元素化合,提炼纯钛条件苛刻。从高钛渣 主要为 提炼海绵钛流
程如下:氯化后的粗 中含有 、 、 、 等杂质,相关物质的沸点如下
表:
化合物
沸点 136 310 180 138
回答下列问题:
(1)高钛渣经过破碎、磁选、磨粉后送氯化车间,磨粉的目的是________。
(2) “分馏”得到的低沸点物是________。分馏难以除去 ,原因是________。加入
铝粉使 转化为 便于除去,写出铝粉与 反应的化学方程式:
________。
(3) “除铝”的方法是用水湿润的活性炭加入到粗 ,使 转化为________而除去。
(4) “还原”需要在Ar的气氛中进行,原因是________。副产物经电解生成________可循
环使用。
(5)制备钛的一种新型方法是:将 粉末浇注成形,烧结后作阴极,以石墨为阳极,
为熔盐进行电解 熔盐不参与电极反应,起溶解和传导 的作用 。
阳极生成的气体除 外,还有________ 填化学式 。
阴极的电极反应式为________。3.(2020届高三化学二轮大题必练)二氧化钛是制取航天航空工业钛合金的重要原料.用
钛铁矿 主要成分是钛酸亚铁 ,含少量 、MgO、 等杂质 作原料生
产金属钛和绿矾 等产品的一种工艺流程如下:已知:Ti有两种价态,在
水溶液中主要以 无色 、 紫色 形式存在.
请回答下列问题:
(1)硫酸与 反应生成 的化学方程式是______.
(2)滤液1中加入适量铁粉,至刚好出现紫色为止,此时溶液仍呈强酸性.
已知:氧化性: 则加入铁粉的作用是______.
(3)滤液2中加入适量的试剂A,可选用______ 填编号 .
稀 通入 鼓入空气
(4)已知 ,101kPa时,由二氧化钛制取四氯化钛所涉及的反应有:
,
,反应 ______.
(5)用石墨作阳极、钛网作阴极、熔融 作电解质,利用如图所示装置获得金属
钙,并以钙为还原剂还原二氧化钛制备金属钛.写出阴极区反应的电极总反应式是
______.
(6)假如 中的铁元素占矿物中铁元素总量的 ;某次生产中,向滤液1中加入纯
铁粉为b kg,得到绿矾晶体的质量为cKg,整个过程中铁元素的总利用率为 ,Ti元
素的转化率为 ,其他损失忽略不计.按上述流程,得到 ______ 用数字和字
母表示 已知:
4.(2018届绵阳高三一诊)钛及其合金具有密度小,强度高,耐腐蚀等优良性能,被广泛
用于航天、航空、航海、石油化工、医药等部门,因此,钛被誉为第三金属和战略金属。
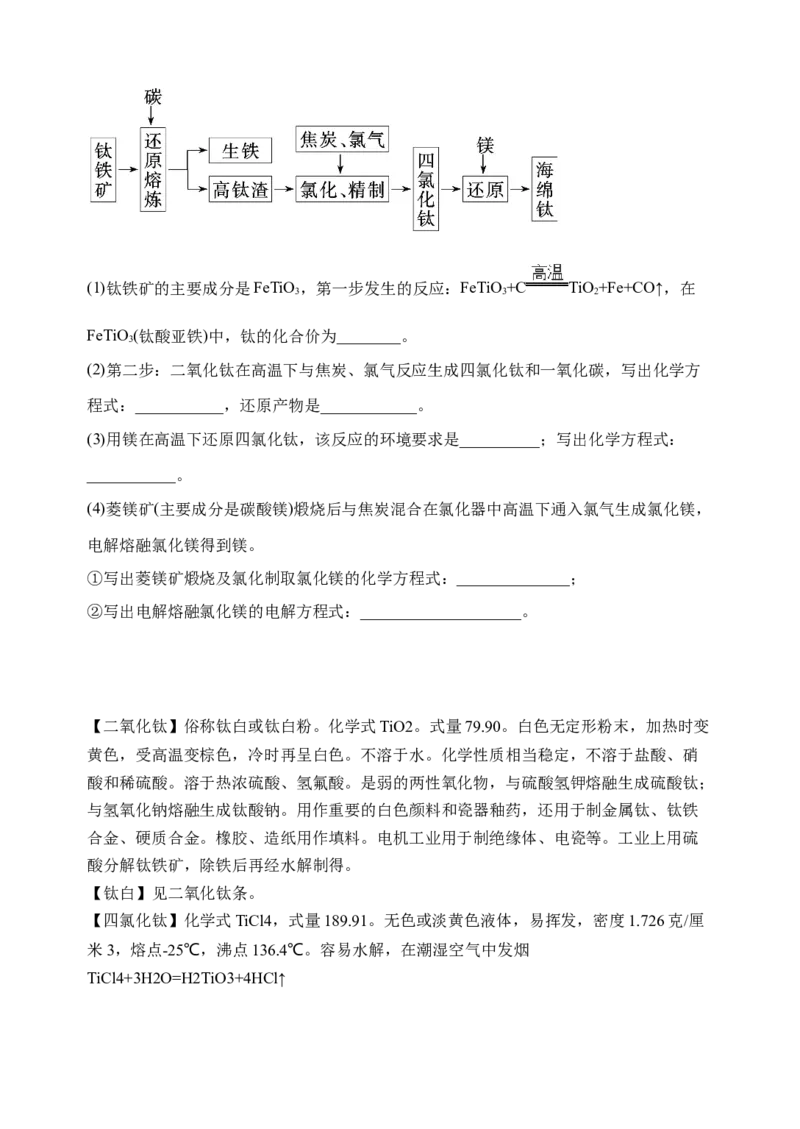
从钛铁矿提取金属钛(海绵钛)的主要工艺过程如下:(1)钛铁矿的主要成分是FeTiO,第一步发生的反应:FeTiO+C TiO+Fe+CO↑,在
3 3 2
FeTiO(钛酸亚铁)中,钛的化合价为________。
3
(2)第二步:二氧化钛在高温下与焦炭、氯气反应生成四氯化钛和一氧化碳,写出化学方
程式:___________,还原产物是____________。
(3)用镁在高温下还原四氯化钛,该反应的环境要求是__________;写出化学方程式:
___________。
(4)菱镁矿(主要成分是碳酸镁)煅烧后与焦炭混合在氯化器中高温下通入氯气生成氯化镁,
电解熔融氯化镁得到镁。
①写出菱镁矿煅烧及氯化制取氯化镁的化学方程式:______________;
②写出电解熔融氯化镁的电解方程式:____________________。
【二氧化钛】俗称钛白或钛白粉。化学式TiO2。式量79.90。白色无定形粉末,加热时变
黄色,受高温变棕色,冷时再呈白色。不溶于水。化学性质相当稳定,不溶于盐酸、硝
酸和稀硫酸。溶于热浓硫酸、氢氟酸。是弱的两性氧化物,与硫酸氢钾熔融生成硫酸钛;
与氢氧化钠熔融生成钛酸钠。用作重要的白色颜料和瓷器釉药,还用于制金属钛、钛铁
合金、硬质合金。橡胶、造纸用作填料。电机工业用于制绝缘体、电瓷等。工业上用硫
酸分解钛铁矿,除铁后再经水解制得。
【钛白】见二氧化钛条。
【四氯化钛】化学式TiCl4,式量189.91。无色或淡黄色液体,易挥发,密度1.726克/厘
米3,熔点-25℃,沸点136.4℃。容易水解,在潮湿空气中发烟
TiCl4+3H2O=H2TiO3+4HCl↑是制备金属钛的中间产物,在797℃时用熔融镁跟四氯化钛蒸气反应可得海绵状钛。还可
用作天然纤维和合成纤维的防水剂。将二氧化钛和碳粉混合加热至800℃左右,用氯处理,
可制得:
TiO2+2C+2Cl2=TiCl4+2CO2↑