文档内容
微专题突破1 化学用语 化学与STSE
我唯一知道的就是自己无知。——苏格拉底
目标定位
1.知道常用的化学用语及表示的意义。
2.能准确判断给定的化学用语是否正确。
教学重点难点
1.电子式的书写。
2.电子排布式的书写。
教学方法
讨论、归纳
教学过程
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
1.化学用语
核素与结构示意图 核素:上标与下标防写反了;结构示意图:分清原子或离子
电子式 一理清是离子键或共价键,二注意粒子排列顺序,三不漏写孤电子对
比例与球棍模型 一看清模型类型,二注意原子的大小
物质结构式 一注意原子连接顺序正确,二对于有机物氢原子不漏写或多写
方程式书写 一产物正确,二符号使用规范,三须配平,四要写反应条件
2.原子或离子结构的几种表示方法
(1)表示方法归纳
表示方法 举例
核素符号 中子数为10的氧原子为 O;中子数为18的氯原子为 Cl
188 3157
原子及离子结构示意图 S: S2-:
基态原子或离子电子排布式 S:1s22s22p63s23p4 Fe3+:1s22s22p63s23p63d5
简化电子排布式 S:[Ne]3s23p4 Fe3+:[Ar]3d5
外围电子排布式 S:3s23p4 Fe3+:3d5
电子排布图(或轨道表示式) S:
(2)注意事项
①3d能级的半充满、全充满状态更稳定。基态Cr、Cu原子的核外电子排布式分别为1s22s22p63s23p63d54s1、
1s22s22p63s23p63d104s1,而非1s22s22p63s23p63d44s2、1s22s22p63s23p63d94s2。
②虽然电子是按照4s、3d的顺序填充的,但书写电子排布式时仍按照3d、4s的顺序书写。
③虽然基态原子电子填充按照构造原理是4s、3d的顺序,但失去电子时先失4s电子,再失3d电子。
如Fe:1s22s22p63s23p63d64s2,失去电子形成Fe2+:1s22s22p63s23p63d6或Fe3+:1s22s22p63s23p63d5。
3.化学与生活
应用 原理解释或示例
食品干燥剂 生石灰、硅胶、氯化钙等
防腐剂——苯甲酸及其钠盐、亚硝酸钠等
食品添加剂 抗氧化剂——维生素C、还原铁粉、多酚类等
加碘食盐——添加KIO
3
阿司匹林——解热镇痛作用
常用药物
胃酸中和剂——碳酸氢钠、氢氧化铝、碳酸镁等
明矾净水 明矾电离出的Al3+水解生成Al(OH) 胶体,Al(OH) 胶体可吸附水中的悬浮物而沉降
3 3
灭火器 干粉灭火器内装的一般是磷酸铵盐干粉灭火剂微专题突破1 化学用语 化学与STSE 问题的态度:问则少;辩则明
泡沫灭火器利用Al (SO ) 溶液和饱和NaHCO 溶液的水解原理
2 4 3 3
钡餐 硫酸钡难溶于水和酸,可作X光透视肠胃时的药剂
含氯消毒剂:ClO 、84消毒液(NaClO)、漂粉精[Ca(ClO)]等
2 2
消毒剂 过氧化物:HO、过氧乙酸(CHCOOOH)等
2 2 3
其他:臭氧、SO 、KMnO 、75%的酒精、苯酚等
2 4
考考位位位
(2024·江苏卷)反应PbS+4HO=PbSO +4HO可用于壁画修复。下列说法正确的是
2 2 4 2
A.S2-的结构示意图为 B.HO 中既含离子键又含共价键
2 2
C.SO 2-中S元素的化合价为+6 D.HO的空间构型为直线形
4 2
【答案】C
【解析】A项,S2-核外有18个电子,其结构示意图为 ,错误;B项,HO 是共价化合物,其中只
2 2
含共价键,错误;C项,SO 2-中O元素化合价为-2,S元素的化合价为+6,正确;D项,HO中的O的杂化
4 2
类型为sp3,O有2个孤电子对,因此HO的空间构型为V形,错误。
2
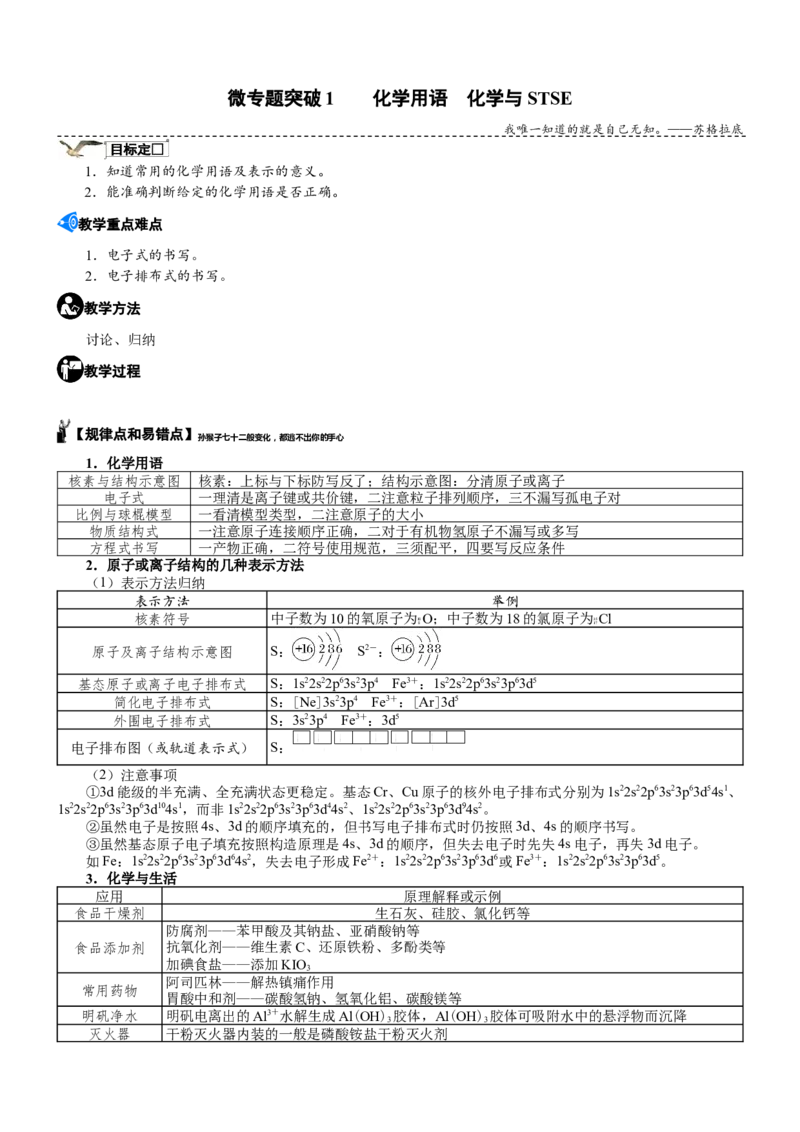
【问题解决1】
(2023·江苏省决胜新高考)基态P原子的外围电
(2023·湖南卷)中子数为 10 的氧原
×
① √ ④
子:188O 子的轨道表示式:
(2023·扬州市开学考)中子数为36的
② × ⑤ (2024·南通一模)P原子的结构示意图为 √
铜原子为3269 Cu
(2023·浙江卷)碳的基态原子轨道表示 (2023·泰州市期中)氯的基态原子的轨道表示
③ 式: × ⑥ 式: ×
【解析】①中子数为10的氧原子,质量数为18,可表示为188O,正确;②Cu是第29号元素,质子数为
29,中子数为36的铜原子为6259 Cu,不正确;③基态碳原子的核外电子排布式为1s22s22p2,根据洪特规则,2p轨
道上的2个电子应该分别在2个轨道上,且自旋方向相同,轨道表示式: ,错误;④基态P原子的
外围电子排布式为3s23p3,轨道表示式为 ,错误;⑤P是15号元素,原子的结构示意图为 ,
正确;⑥基态原子的轨道表示式应表示所有核外电子,而不只是价电子,错误。
核素与微粒的电子排布
1.核素表示为:_________AX
Z
2.粒子示意图:一圆圈中不要漏画_____“+”,二注意是原子还是离子
3.电子排布式:一电子排布式与价电子排布式写法不同,二第四周期不要漏写____3d上的电子
考点精练
① (2023·浙江卷)中子数为18的氯原子: Cl ×
3177
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找② (2023·南京师范大学附属中学)氧原子的结构示意图为 ×
③ (2024·淮安市高三上学期开学考)基态O2-的核外电子排布式:1s22s22p6 √
④ (2023·辽宁卷)基态Ni原子价电子排布式:3d10 ×
⑤ (2023·北京卷)基态 原子的价层电子轨道表示式为 ×
⑥ (2024·南通一模)Fe2+基态核外电子排布式为[Ar]3d54s1 ×
⑦ (2023·南通市海门市第一次调研)基态N原子的轨道表示式: ×
⑧ (2023·北京西城期末)基态Cr原子的价层电子排布式:3d44s2 ×
【答案】①质量数=质子数+中子数,质量数标注于元素符号左上角,质子数标注于左下角,中子数为 18
的氯原子的质量数为17+18=35,核素符号为3157 Cl,错误;②O原子的质子数和电子数都是8,核外电子分层排
布,其结构示意图为 ,错误;③基态O2-的核外电子排布式:1s22s22p6,正确;④Ni原子的原子序数为
28,其基态原子的价电子排布式为3d84s2,错误;⑤基态铬原子的价层电子轨道表示式是 ,
错误;⑥Fe2+基态核外电子排布式为[Ar]3d6,错误;⑦N的电子排布式为1s22s22p3,根据洪特规则,电子先占
满2p上的3个轨道, ,错误;⑧基态Cr原子的价层电子排布式为:3d54s1,错误。
【问题解决2】
① (2023·北京卷) 的电子式为 × ④ (2024·南通一模)HO的电子式为 ×
2
(2024·连云港一模)CS 的电子式为
2
② × ⑤ (2023·泰州市期中)N 的电子式:N N ×
2
(2023· 湖 南 卷 )HClO 的 电 子 式 : (2023· 浙 江 卷 )HCl 的 形 成 过 程 :
③ √ ⑥ ×
【解析】①NaCl为离子化合物,错误;②CS 与CO 为等电子体,电子式为 ,错误;③HClO
2 2
的电子式为 ,正确;④HO的电子式为 ,错误;⑤漏写了N原子上的孤电子对,错误;⑥HCl
2
是共价化合物,不存在电子得失,其形成过程应为 ,错误。
电子式书写
1.书写电子式需注意的问题
① 搞清是离子化合物还是共价化合物,确定粒子是原子还是离子
② 最外层上没有参与成键的孤电子对,也要画出来
③ 离子(或根)带电荷,基团不显电性,如OH-的电子式为[∶O∶H]-,—OH的电子式为·O∶H
④ 不能错误合并离子,如NaO 的电子式写成2Na+[∶O∶O∶]2-是错误的
2 2
⑤ 分子式中原子的排列顺序与实际原子的结合顺序不一定相同,如次氯酸(HClO):H∶O∶Cl∶
2.用电子式表示两类化学键的形成过程
化学键 用电子式表示形成过程
共价键 不标出弯箭头及电子的转移,表示出共用电子对,如:
用弯箭头表示电子转移,用中括号将接受电子的原子括起来并标上电荷数,如:
离子键
考点精练
1.按要求书写下列微粒的电子式:
C O NaCN NaBH COCl —OH NH
4 2 2微专题突破1 化学用语 化学与STSE 问题的态度:问则少;辩则明
[∶C C∶]2- [∶O∶O∶]2- Na+[C⋮⋮N]- ·O∶H
⋮⋮
2.判断以下化学用语是否正确:
① (2023·扬州市开学考)NH 3 的电子式为 ×
② (2024·淮安市高三上学期开学考)CsCl的电子式: ×
③ (2023·南通市海门市第一次调研)NH 4 Cl的电子式为 ×
④ (2023·湖北卷)用电子式表示KS的形成: √
2
⑤ (2023·江苏卷)NH的电子式为 ×
⑥
(2024·安徽统考模拟预测)CN
2
2-的电子式为
√
⑦ (2023·湖南长沙高三雅礼中学)BaC 2 的电子式: √
⑧ (2024·甘肃·模拟预测)硫酸钾的电子式 ×
【解析】①NH 的电子式为 ,不正确;②CsCl属于离子化合物,即电子式为 ,错误;
3
③NH Cl为离子化合物 ,错误;④钾原子失去电子,硫原子得到电子形成硫化钾,硫化钾为
4
离子化合物,用电子式表示KS的形成: ,正确;⑤NH的电子式为 ,
2
错误;⑥CN2-的电子式为 ,每个原子均达到了8电子稳定结构,正确;⑦BaC 为离子化合物,
2 2
其电子式为 ,正确;⑧硫酸钾的电子式为K+ K+,错误。
【问题解决3】
① (2023·泰州市)NH 3 的VSEPR模型名称: √ ④ (2024·淮安市高三上学期开学考)CO 3 2- ×
四面体形 的空间构型:三角锥形
(2023·浙江卷) 分子的球棍模型:
② × ⑤ (2023·辽宁卷)BeCl 的空间结构:V形 ×
2
(2023·北京卷)NH 的 VSEPR 模型为 (2023·海安高级中学高三下学期模拟)ClO
3 2
③ × ⑥ ×
的空间填充模型:
【解析】①NH 的价电子对为4,VSEPR模型名称为四面体形,正确;②HS分子是“V”形结构,因此
3 2
该图不是HS分子的球棍模型,错误;③氨分子的VSEPR模型是四面体结构,错误;④CO2-的空间构型为平
2 3
面三角形,错误;⑤BeCl 的中心原子为Be,根据VSEPR模型可以计算,BeCl 中不含有孤电子对,因此BeCl
2 2 2
为直线形分子,错误;⑥ClO 的价电子对数为4,含孤电子对,不是直线形,错误。
2
模型与空间构型判断
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找1.分清比例模型、球棍模型,关注原子大小及键角、分子空间构型等。
2.根据价层电子对互斥理论或杂化轨道理论,判断粒子空间构型。
考点精练
① (2023·浙江卷)AlCl 的价层电子对互斥模型: ×
3
②
(2024•南通市如皋市高三上学期开学考)NH的空间结构为正四面体形
√
③
(2023·天津静海一中)四氯化碳分子空间填充模型:
×
④ (2023·浙江卷)BF 3 的空间结构: (平面三角形) √
⑤ (2023·江苏省决胜新高考)PO的空间填充模型: ×
⑥
(2023··南京师范大学附属中)FNO的空间结构为直线形
×
⑦ (2023·湖南长沙高三雅礼中学校)SO 3 2-的VSEPR模型: ×
⑧ (2023·天津静海一中)NH 的VSEPR模型为 √
3
【解析】①AlCl 中心原子价层电子对数为3+=3,其价层电子对互斥模型为平面三角形,错误;②NH中
3
氮原子价层电子对数=4+=4且不含孤电子对,所以该微粒为正四面体形,正确;③四氯化碳分子的空间构型
为正四面体形,但氯原子的原子半径大于碳原子,所以空间填充模型为 ,错误;④BF 的中心原子B原子
3
价层电子对数为3+=3,空间构型为平面三角形,空间结构模型为: ,正确;⑤PO的中心原子的价电子对
数为=4,没有孤电子对,空间结构为正四面体,空间填充模型为 ,错误;⑥FNO中心原子N原子价电子
对数为2+=3,空间结构为V形,错误;⑦SO2-的中心原子S价层电子对数为3+=4,有一对孤电子对,其
3
VSEPR模型为四面体形,错误;⑧氨分子中氮原子的价层电子对数为 4、孤对电子对数为1,VSEPR模型为
,正确。
【问题解决4】
(2023·辽宁卷)顺-2-丁烯的结构简
① 对硝基甲苯的结构简式: × ④ ×
式:
聚 苯 乙 烯 结 构 简 式 :
对氯甲苯的结构简式:
② × ⑤ ×
③ CS 的结构式:S—C—S × ⑥ 次氯酸的结构式:H—Cl—O ×
2
【解析】①—NO 中的N原子应与苯环连接,错误;②聚苯乙烯结构简式为 ,错误;③CS
2 2
的结构式:S=C=S,错误;④顺-2-丁烯的结构中两个甲基在双键的同一侧,其结构简式为微专题突破1 化学用语 化学与STSE 问题的态度:问则少;辩则明
,错误;④对氯甲苯的结构简式为 ,错误;⑥次氯酸结构式为H—O—Cl,错误。
物质结构的判断
关注物质的结构式、结构简式以及基团原子的连接方式等。
考点精练
① (2024·南通市如皋市高三上学期开学考)N 2 的结构式为N=N ×
② 聚乙炔的结构简式: √
③ (2024·青海西宁高三统考期末)HO的结构式: √
2
【解析】①N 中N和N原子共用3对电子对,结构式为N≡N,错误;②CH≡CH结构中断一根共价键,
2
生成的聚乙炔为 ,正确;③已知HO为V形结构,故HO的结构式为: ,正确。
2 2
【问题解决5】
① (2023·南通市海门市第一次调研)NH 为非极性分子 ×
3
② (2023·南通市海门市第一次调研)CO(NH ) 中只含共价键 √
2 2
③ (2024•南通市如皋市高三上学期开学考)HO中含有非极性共价键 ×
2
④ (2023·扬州市开学考)NH F中含有离子键和共价键 √
4
⑤ (2024·镇江市丹阳市上学期开学考)NaClO既含离子键又含共价键 √
【解析】①氨气为共价化合物,分子中N、H共用1对电子,N原子还有1对孤电子,氨气为极性分子,错
误;②CO(NH ) 是共价化合物,含有极性共价键,正确;③HO中含有2个O-H极性共价键,而不是非极性
2 2 2
键,错误;④NH F中铵根中N原子和H原子之间通过共价键结合,铵根离子和F-通过离子键结合,正确;⑤
4
钠离子和次氯酸根离子之间存在离子键,次氯酸根离子中存在Cl-O共价键,正确。
化学键与分子的极性
1.化学键:熟知常见物质的类别及物质中存在的粒子是原子、离子,注意活泼金属与活泼的非金属元素间
不一定是离子键。
2.分子的极性:一是看空间结构是否高度对称,二如是AB 分子看A元素的价态。
n
考点精练
① (2023·辽宁卷)P 中的共价键类型:非极性键 ×
4
② (2023·泰州市期中)NH 4 Cl仅含共价键 ×
③ (2024·镇江市丹阳市上学期开学考)N 2 H 4 的结构式为: ×
(2023·湖北卷)用电子云轮廓图表示H—H的s-s σ键形成的示意图:
④ √
⑤ (2023·南京二模)OF 是非极性分子 ×
2
【解析】①P 中磷磷间共用电子对不发生偏移,为非极性键,正确;②NH Cl含有离子键和极性共价键,
4 4
错误;③肼为共价化合物,氮原子间形成一对共用电子对,每个氮原子和两个氢原子形成两个共价键,结构式
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找为 ,错误;④两个氢原子1s轨道电子云重叠,形成s-s σ键,正确;⑤OF 中的O原子为sp3杂
2
化,存在2对孤对电子,为V形结构,是极性分子,错误.
【问题解决6】
① NaHCO 的电离方程式:NaHCO =Na++H++CO2- ×
3 3 3
② ×
+HO +HO+是苯酸的水解方程式
2 3
(2024·河北石家庄第九中学校)用离子方程式表示氨水中滴入少量硝酸银溶液:Ag++
③ √
2NH ·HO=[Ag(NH ) ]++2HO
3 2 3 2 2
【解析】①HCO -对应的为弱酸,不可拆;错误;②HO+拆成HO与H+,方程式两边各去掉一个HO,实
3 3 2 2
为苯酚的电离,错误;③由于氨水是过量的,则生成了稳定的[Ag(NH )]+,其离子方程式为Ag++2NH ·HO
3 2 3 2
=[Ag(NH )]++2HO,正确。
3 2 2
涉及基本原理的考查
依据有关原理,认识水解与电离方程式的不同,判断离子方程式的正误。
考点精练
① 纯碱溶液呈碱性的原理:CO 3 2-+2H 2 O H 2 CO 3 +2OH- ×
②
熔融状态下,KHSO
4
的电离方程式:KHSO
4
=K++HSO
4
-
√
(2024·辽宁朝阳期末)用离子方程式表示 Cu(OH) 溶于氨水:Cu2++4NH ·HO=
③ 2 3 2 √
[Cu(NH )]2++4HO
3 4 2
【解析】①多元弱酸(HS、HCO 、HSO )的电离、多元弱酸根离子(S2-、CO2-、SO 2-)的水解都是分步
2 2 3 2 3 3 3
进行的且以第一步为主,错误;②特殊盐(如KHSO 、NaHSO)的电离条件不同电离方式不同如:在水溶液中
4 4
KHSO=K++H++SO 2-,而熔融状态下为KHSO=K++HSO -,正确;③Cu(OH) 难溶于水,用离子方程
4 4 4 4 2
式表示Cu(OH) 溶于氨水为Cu(OH)+4NH ·HO=[Cu(NH )]2++2OH-+4HO,错误。
2 2 3 2 3 4 2
【问题解决6】
(2022•江苏卷)下列物质性质与用途具有对应关系的是
A.石墨能导电,可用作润滑剂
B.单晶硅熔点高,可用作半导体材料
C.青铜比纯铜熔点低、硬度大,古代用青铜铸剑
D.含铅化合物颜色丰富,可用作电极材料
【答案】C
【解析】A项,石墨是混合型晶体,质软,可用作润滑剂,错误;B项,单晶硅可用作半导体材料与空穴
可传递电子有关,与熔点高无关,错误;C项,青铜是铜合金,比纯铜熔点低、硬度大,易于锻造,古代用青
铜铸剑,正确;D项,含铅化合物可在正极得到电子发生还原反应,所以可用作电极材料,与含铅化合物颜色
丰富无关,错误。
化学与STSE
命题载体是与社会、生活联系紧密的科学、技术、社会和环境问题,高起点、低落点。
一般选择最新科技成果(最近诺贝尔成果、科技新发现新进展),知识源于教材,最终都是用化学知识解决
问题。
考点精练
1.(2024·南京、盐城模拟)“神舟飞船”接力腾飞、“太空之家”遨游苍穹、“福建号”航母下水、国
产“C919”大飞机正式交付都彰显了中国力量。下列成果所涉及的材料为金属材料的是
A.“神舟十五”号飞船使用的耐辐照光学窗材料——石英玻璃
B.“天宫”空间站使用的太阳能电池板材料——砷化镓
C.“福建号”航母使用的高强度甲板材料——合金钢
D.“C919”大飞机使用的机身复合材料——碳纤维和环氧树脂
【答案】C
【解析】A项,石英玻璃主要成分为SiO,SiO 为新型无机非金属材料,不属于金属材料,错误;B项,
2 2
砷化镓为是一种无机化合物,属于半导体材料,不属于金属材料,错误;C项,合金钢是指钢里除了铁、碳外,微专题突破1 化学用语 化学与STSE 问题的态度:问则少;辩则明
加入其他金属元素,所以属于金属材料,正确;D项,碳纤维指的是含碳量在百分之九十以上的高强度高模量
纤维,不属于金属材料,环氧树脂是一种高分子聚合物,也不属于金属材料,错误。
2.(2024·南京考前模拟)化学知识与科技、生产和生活有密切的关系。下列叙述不正确的是
A.ClO 是一种绿色消毒剂,可用于自来水杀菌消毒
2
B.红酒中添加SO ,利用了SO 的还原性和杀菌消毒的能力
2 2
C.利用NH HPO 作灭火剂,是因为其易分解且吸热,分解产物不支持燃烧
4 2 4
D.利用Na+KCl======K↑+NaCl制取K,该反应可以说明Na的金属性强于K
【答案】D
【解析】A项,ClO 具有强氧化性,ClO 是一种绿色消毒剂,常用于自来水杀菌消毒,正确;B项,在严
2 2
格控制用量的情况下,红酒中添加SO 作抗氧剂,主要利用了SO 的还原性和杀菌消毒的能力,正确;C项,
2 2
NH HPO 是一种铵盐,受热易分解且吸热,分解产物不支持燃烧,因此NH HPO 常用作灭火剂,正确;D项,
4 2 4 4 2 4
利用Na+KCl======K↑+NaCl制取K,在该条件下钾为气体,利用平衡移动原理,与元素的金属性强弱无关,
错误。
成功体验
1.(2024·泰州市下学期一模)超硬陶瓷材料氮化硅可由反应3SiH +4NH =Si N +12H 制得。下列说
4 3 3 4 2
法正确的是
A.NH 的电子式为 B.SiH 为平面正方形结构
3 4
C.H 是非极性分子 D.Si N 属于分子晶体
2 3 4
【答案】C
【解析】A项,NH 的电子式为 ,错误;B项,SiH 的价层电子对数为4,为正四面体结构,错误;
3 4
C项,H 的正电荷中心与负电荷中心重合,是非极性分子,正确;D项,Si N 属于共价晶体,错误。
2 3 4
2.(2024·苏锡常镇二模)催化热解HS可同时回收S(结构为 )和H 。下列说法正确的
2 8 2
是
A.中子数为17的硫原子为17S B.HS的电子式为H∶S∶H
2
C.S 固态时为共价晶体 D.H 分子中含有p-p σ键
8 2
【答案】B
【解析】A项,在表示原子组成时,将质量数写在左上方,质子数写在左下方,S为第16号元素因此质子
数为16,可知中子数为17的硫原子的质量数为33,故表示为:3136 S,错误;B项,H
2
S为共价化合物,其电子式
为H∶S∶H,正确;C项,固态S是由S 构成的,可知该晶体中存在的微粒是分子,属于分子晶体,错误;D
8
项,基态H原子为1s1,形成的H 分子中含有s-s σ键,错误。
2
3.(2023·江苏卷)反应NH Cl+NaNO =NaCl+N↑+2HO应用于石油开采。下列说法正确的是
4 2 2 2
A.NH的电子式为 B.NO中N元素的化合价为+5
C.N 分子中存在N≡N键 D.HO为非极性分子
2 2
【答案】C
【解析】A项,NH的电子式为 ,错误;B项,NO中N元素的化合价为+3,错误;C项,N
2
分子存在氮氮三键,正确;D项,HO为V形分子,分子中正负电荷中心未重合,为极性分子,错误。
2
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找4.(2024·泰州市下学期一模)利用反应LiH+NH ====H+LiNH 可制备化工试剂LiNH。下列说法正确
3 2 2 2
的是
A.LiH的电子式为
B.基态N原子的价电子排布图为
C.H 为共价化合物
2
D.NH2-的VSEPR模型为平面三角形
【答案】B
【解析】A项,H-的核外只有两个电子,LiH的电子式为 ,错误;B项,依据基态氮原子的价电
子排布式2s22p3,价电子排布图为 ,正确;C项,H 不是化合物,错误;D项,NH2-的价层电子
2
对数为2+=4,VSEPR模型为四面体形,错误。
5.(2025·扬州市开学考)检验微量砷的原理为2AsH+12AgNO+3HO=As O↓+12HNO+
3 3 2 2 3 3
12Ag↓。AsH 常温下为无色气体。下列说法正确的是
3
A.基态O原子的轨道表示式为: B.NO -的空间构型为平面三角形
3
C.固态AsH 属于共价晶体 D.HNO 既含离子键又含共价键
3 3
【答案】B
【解析】A项,O原子核外有8个电子,基态O原子的轨道表示式为 ,错误;B项,
NO -中N原子价电子对数为3,无孤电子对,空间构型为平面三角形,正确;C项,AsH 常温下为无色气体,
3 3
沸点低,固态AsH 属于分子晶体,错误;D项,HNO 是共价化合物,只含共价键,错误。
3 3