文档内容
押江苏卷第 15 题
有机推断与有机合成
核心考点 考情统计 考向预测 备考策略
2023·江苏卷,15 1.重点关注与其他模块交叉知
结合药物的合成考查有机物的结 识,高考题经常综合考查;
有机推断与有
2022·江苏卷,15
构、有机反应类型、限定条件的同
机合成 分异构体书写、有机合成路线设计 2.难点是限定条件同分异构体结
2021·江苏卷,16
等知识点 构简式的书写以及有机合成路线的
设计
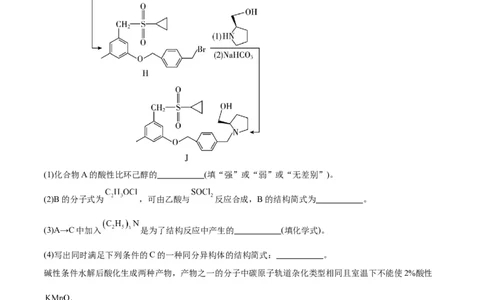
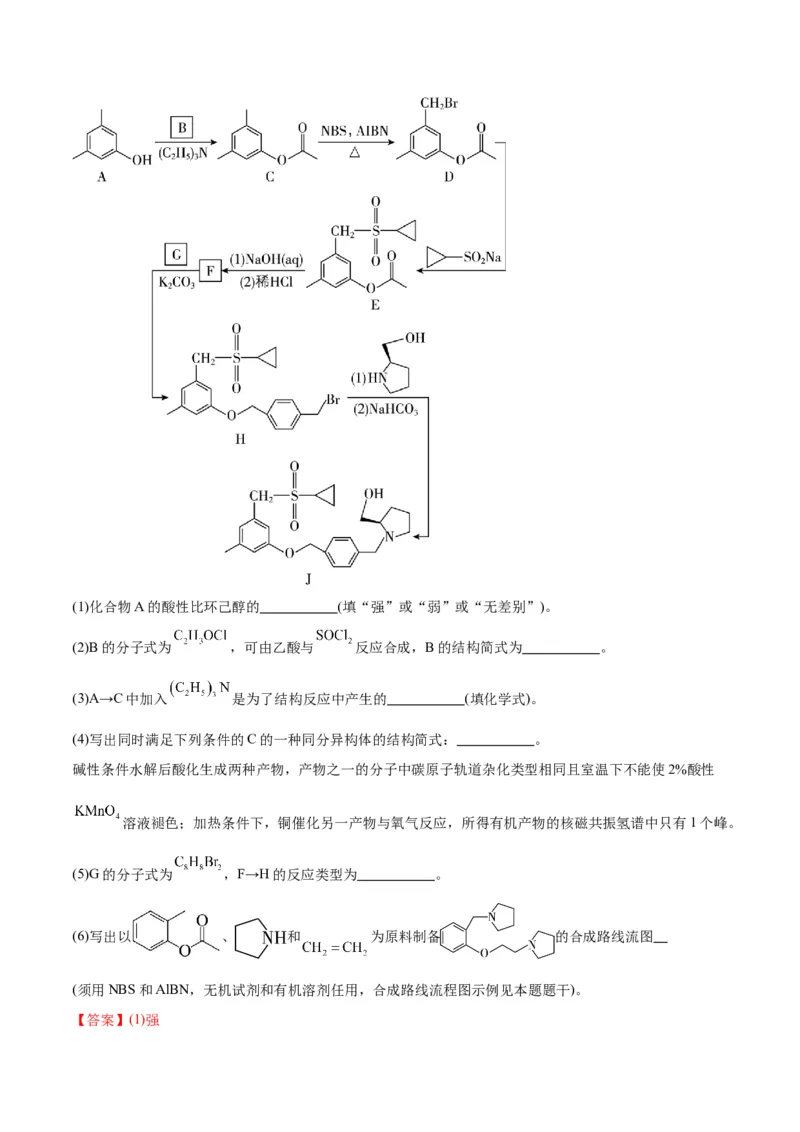
1.(2023·江苏卷,15)化合物I是鞘氨醇激酶抑制剂,其合成路线如下:(1)化合物A的酸性比环己醇的 (填“强”或“弱”或“无差别”)。
(2)B的分子式为 ,可由乙酸与 反应合成,B的结构简式为 。
(3)A→C中加入 是为了结构反应中产生的 (填化学式)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式: 。
碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%酸性
溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个峰。
(5)G的分子式为 ,F→H的反应类型为 。
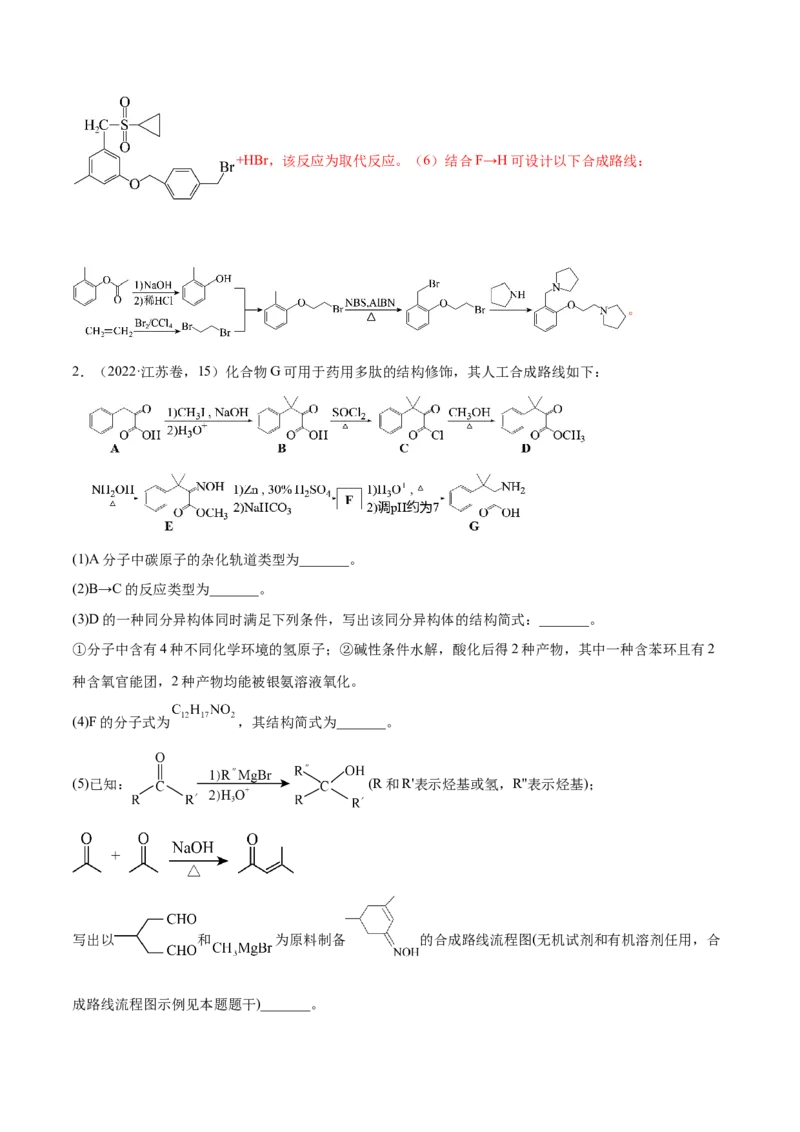
(6)写出以 、 和 为原料制备 的合成路线流图
(须用NBS和AlBN,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
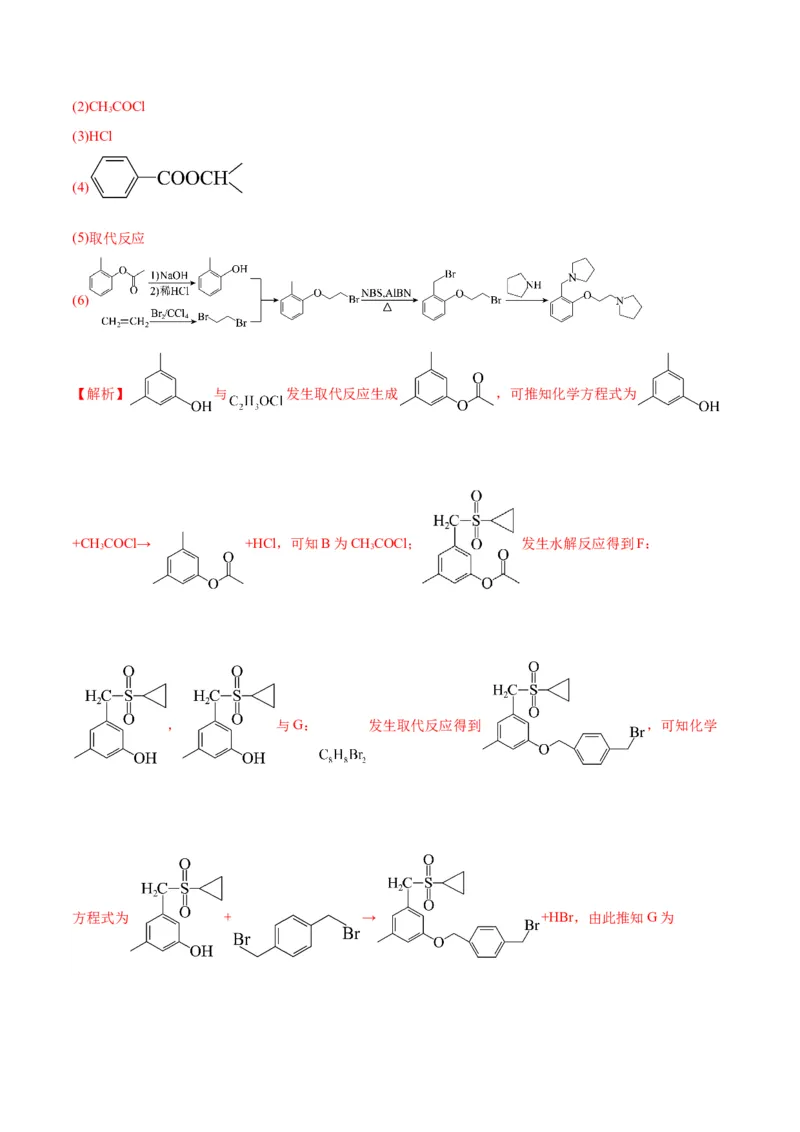
【答案】(1)强(2)CH COCl
3
(3)HCl
(4)
(5)取代反应
(6)
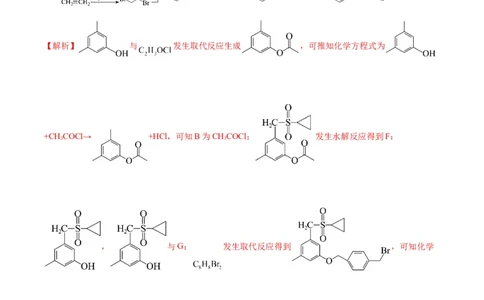
【解析】 与 发生取代反应生成 ,可推知化学方程式为
+CH COCl→ +HCl,可知B为CHCOCl; 发生水解反应得到F:
3 3
, 与G: 发生取代反应得到 ,可知化学
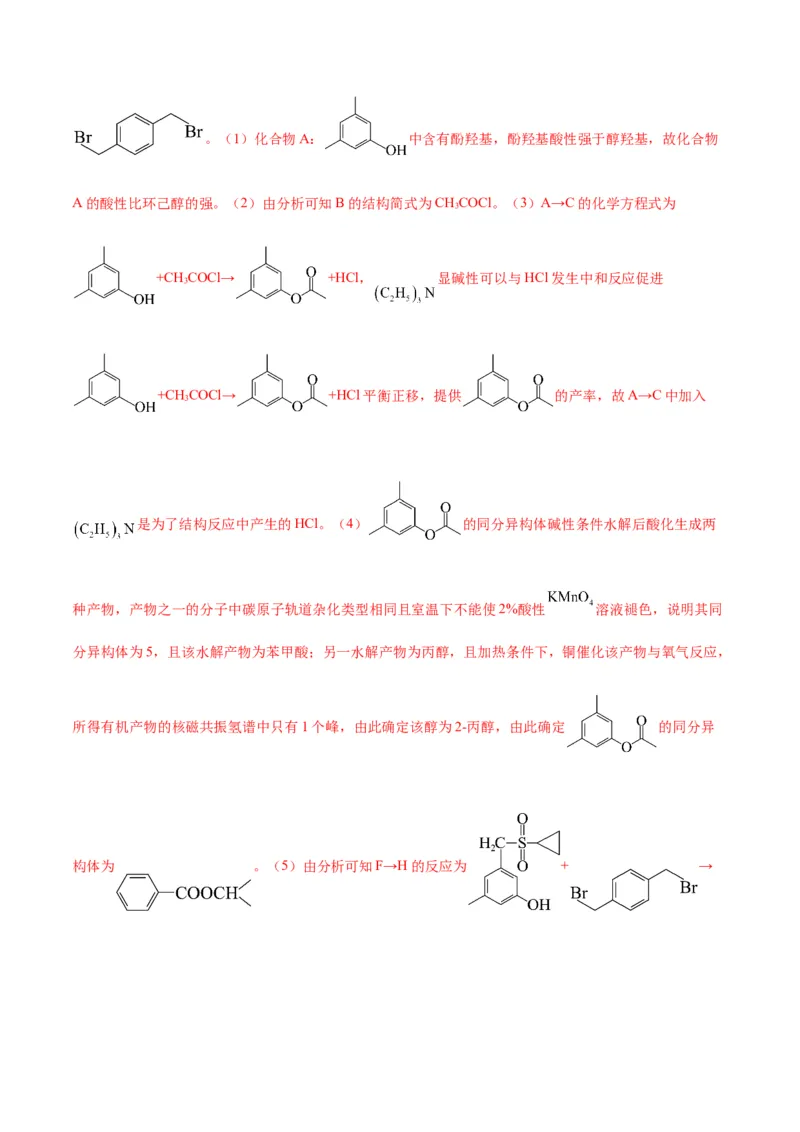
方程式为 + → +HBr,由此推知G为。(1)化合物A: 中含有酚羟基,酚羟基酸性强于醇羟基,故化合物
A的酸性比环己醇的强。(2)由分析可知B的结构简式为CHCOCl。(3)A→C的化学方程式为
3
+CH COCl→ +HCl, 显碱性可以与HCl发生中和反应促进
3
+CH COCl→ +HCl平衡正移,提供 的产率,故A→C中加入
3
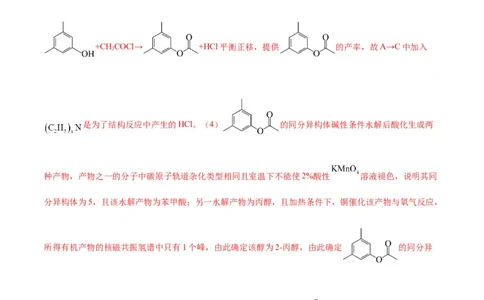
是为了结构反应中产生的HCl。(4) 的同分异构体碱性条件水解后酸化生成两
种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%酸性 溶液褪色,说明其同
分异构体为5,且该水解产物为苯甲酸;另一水解产物为丙醇,且加热条件下,铜催化该产物与氧气反应,
所得有机产物的核磁共振氢谱中只有1个峰,由此确定该醇为2-丙醇,由此确定 的同分异
构体为 。(5)由分析可知F→H的反应为 + →+HBr,该反应为取代反应。(6)结合F→H可设计以下合成路线:
。
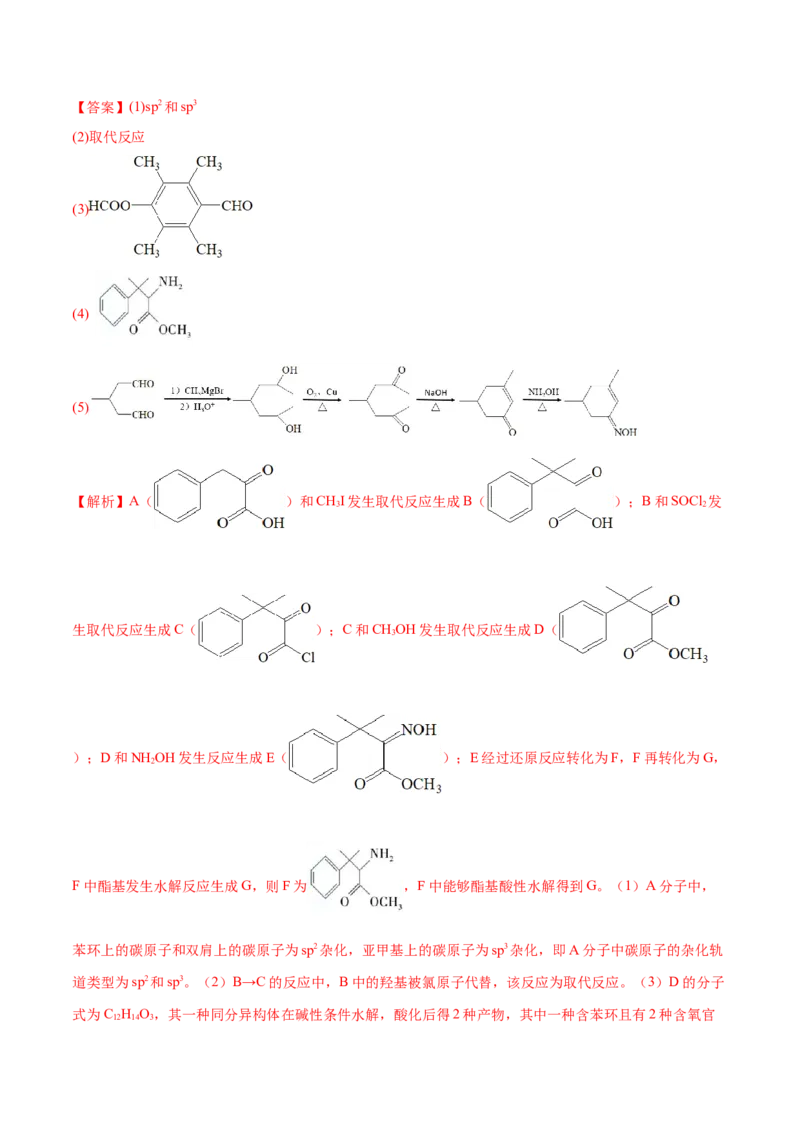
2.(2022·江苏卷,15)化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
(1)A分子中碳原子的杂化轨道类型为_______。
(2)B→C的反应类型为_______。
(3)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______。
①分子中含有4种不同化学环境的氢原子;②碱性条件水解,酸化后得2种产物,其中一种含苯环且有2
种含氧官能团,2种产物均能被银氨溶液氧化。
(4)F的分子式为 ,其结构简式为_______。
(5)已知: (R和R'表示烃基或氢,R''表示烃基);
写出以 和 为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合
成路线流程图示例见本题题干)_______。【答案】(1)sp2和sp3
(2)取代反应
(3)
(4)
(5)
【解析】A( )和CHI发生取代反应生成B( );B和SOCl 发
3 2
生取代反应生成C( );C和CHOH发生取代反应生成D(
3
);D和NH OH发生反应生成E( );E经过还原反应转化为F,F再转化为G,
2
F中酯基发生水解反应生成G,则F为 ,F中能够酯基酸性水解得到G。(1)A分子中,
苯环上的碳原子和双肩上的碳原子为sp2杂化,亚甲基上的碳原子为sp3杂化,即A分子中碳原子的杂化轨
道类型为sp2和sp3。(2)B→C的反应中,B中的羟基被氯原子代替,该反应为取代反应。(3)D的分子
式为C H O,其一种同分异构体在碱性条件水解,酸化后得2种产物,其中一种含苯环且有2种含氧官
12 14 3能团,2种产物均能被银氨溶液氧化,说明该同分异构体为酯,且水解产物都含有醛基,则水解产物中,
有一种是甲酸,另外一种含有羟基和醛基,该同分异构体属于甲酸酯;同时,该同分异构体分子中含有4
种不同化学环境的氢原子,则该同分异构体的结构简式为 。(4)由分析可知,
F的结构简式为 。(5)根据已知的第一个反应可知, 与CHMgBr
3
反应生成 , 再被氧化为 ,根据已知的第二个反应可知,
可以转化为 ,根据流程图中D→E的反应可知, 和NH OH反
2
应生成 。
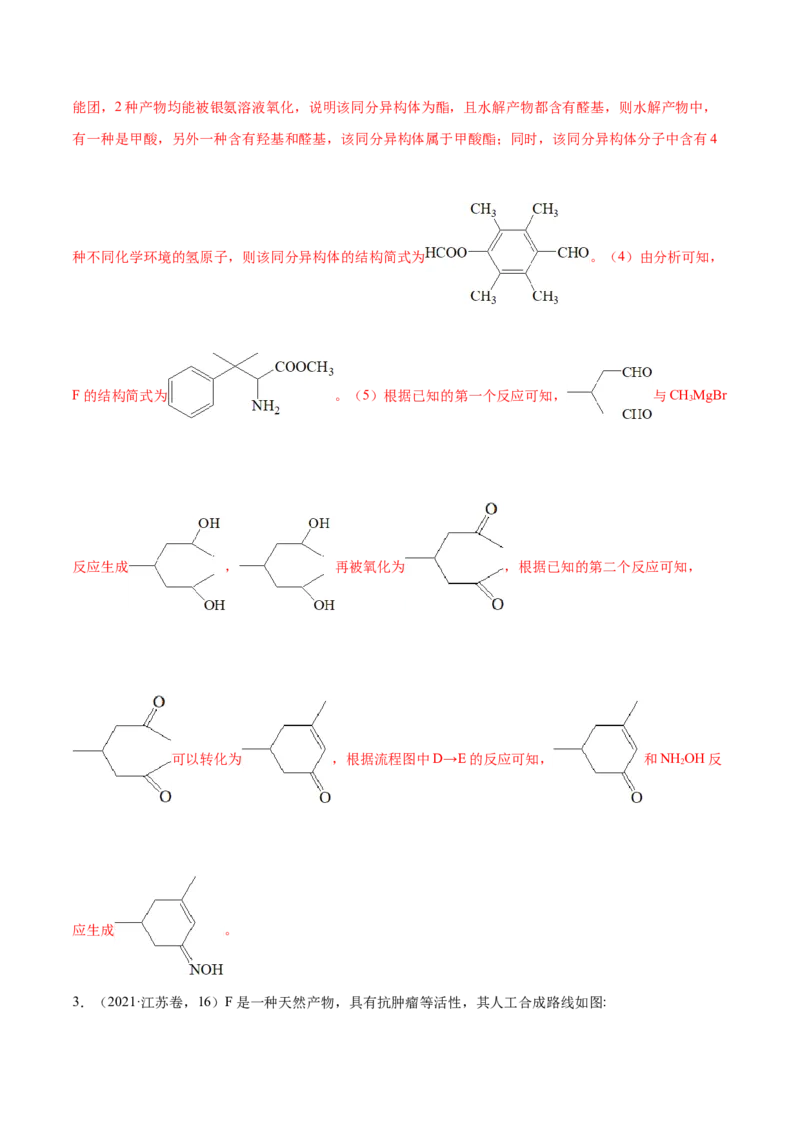
3.(2021·江苏卷,16)F是一种天然产物,具有抗肿瘤等活性,其人工合成路线如图:(1)A分子中采取sp2杂化的碳原子数目是___。
(2)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___。
①分子中不同化学环境的氢原子个数比是2:2:2:1。
②苯环上有4个取代基,且有两种含氧官能团。
(3)A+B→C的反应需经历A+B→X→C的过程,中间体X的分子式为C H NO 。X→C的反应类型为___。
17 17 6
(4)E→F中有一种分子式为C H O 的副产物生成,该副产物的结构简式为___。
15 14 4
(5)写出以 CH 和F CHOH为原料制备
3 2
的合成路线流程图___(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
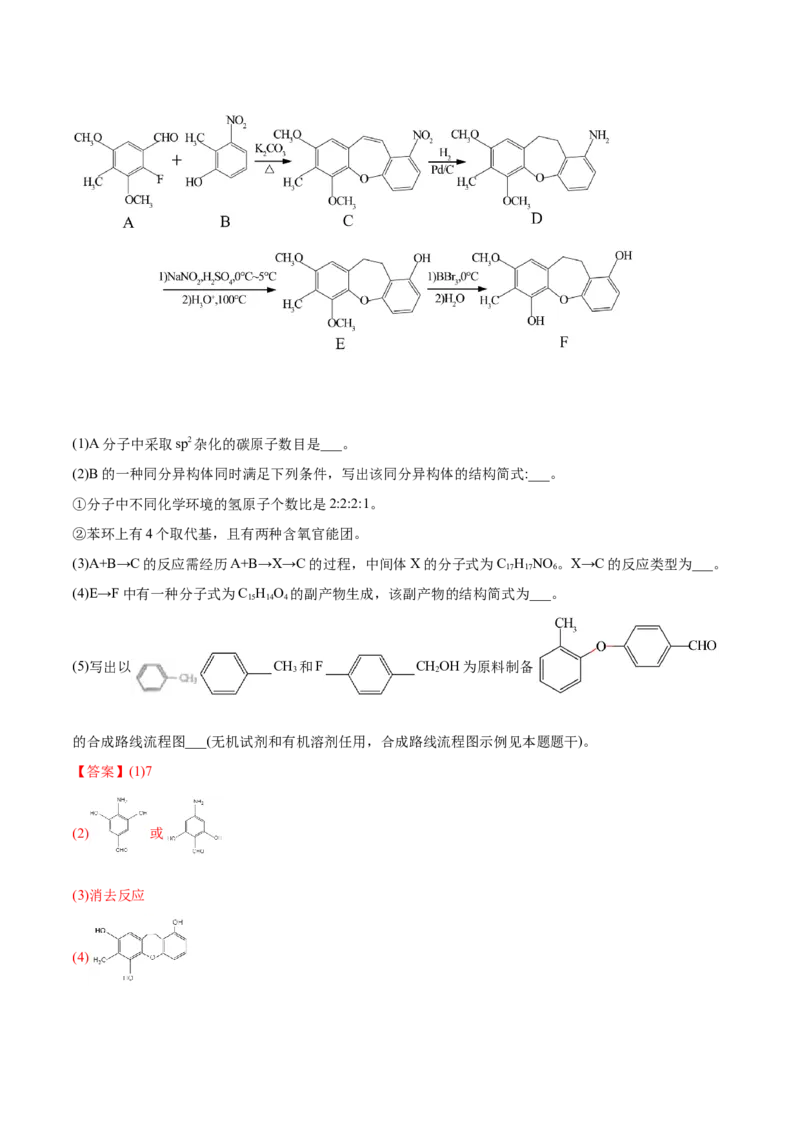
【答案】(1)7
(2) 或
(3)消去反应
(4)(5)
【解析】A和B在KCO 作用、加热条件反应得到C、HF和HO,C和H 发生还原反应得到D,D发生取
2 3 2 2
代反应生成E,E发生取代反应得到F。(1)从成键方式看,形成双键的中心原子通常采用sp2杂化,醛基和
苯环中的碳原子为sp2杂化,饱和C为sp3杂化,故共有7个碳原子采取sp2杂化;故答案为:7。(2)B的一种
同分异构体,环上有4个取代基,且有两种含氧官能团,根据其不饱和度可知,这两种含氧官能团为羟基
和含羰基的官能团;分子中不同化学环境的氢原子个数比是2:2:2:1,说明分子结构具有一定的对称性,则
该物质可能为 或 ;故答案为: 或 。(3)由题给C
结构式可知,C的分子式为C H NO ;中间体X的分子式为C H NO ;结合C的结构简式可知X→C生
17 15 5 17 17 6
成碳碳双键,反应类型为消去反应;故答案为:消去反应。(4)由E与F结构简式可知,E→F为甲氧基被-
OH取代,则可能另一个甲氧基也被-OH取代,副产物的分子式为C H O,则其结构简式为:
15 14 4
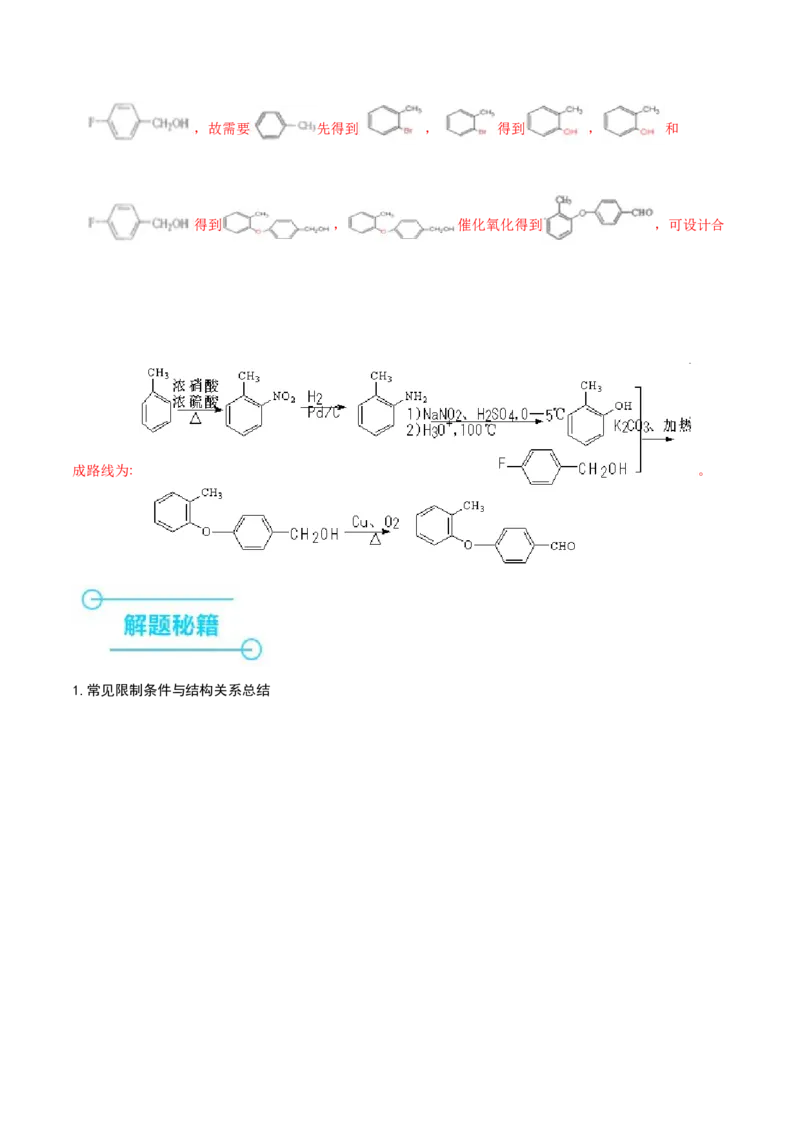
;故答案为: 。(5)以 和 为原料制备
,两个碳环以-O-连接在一起,则一定会发生类似A+B→C的反应,则需要 和,故需要 先得到 , 得到 , 和
得到 , 催化氧化得到 ,可设计合
成路线为: 。
1.常见限制条件与结构关系总结2. 常见含氧官能团的结构与性质
官能团 结构 性质
易取代、易消去(如乙醇在浓硫酸、170 ℃条件下生
醇羟基 —OH 成乙烯)、易催化氧化、易被强氧化剂氧化(如乙醇被
酸性KCr O、KMnO 溶液氧化)
2 2 7 4
极弱酸性(酚羟基中的氢能与NaOH溶液反应,但酸
性极弱,不能使石蕊变色)、易氧化(如无色的苯酚晶
酚羟基 —OH
体易被空气中的氧气氧化为红色)、显色反应(如苯酚
遇FeCl 溶液呈紫色)
3
易被氧化(如乙醛与银氨溶液共热生成银镜)、可被还
醛基
原为醇
可被还原(如 在Ni催化、加热条件下加氢生成
酮羰基
)
酸性(如乙酸的酸性强于碳酸)、易取代(如发生酯化
羧基
反应)
易水解 (如乙酸乙酯在稀硫酸、加热条件下发生酸性
酯基 水解;乙酸乙酯在NaOH溶液、加热条件下发生碱
性水解;碱性条件下,乙酸乙酯水解更彻底)醚键
可水解(如 )
3. 有机反应类型与常见的有机反应
反应类型 重要的有机反应
烷烃的卤代(以CH 为例):
4
CH+Cl――→CHCl+HCl(可继续反应生成CHCl、CHCl 、CCl )
4 2 3 2 2 3 4
丙烯、甲苯在光照条件下分别与氯气发生取代反应:
CH===CH—CH+Cl――→CH===CH—CHCl+HCl、
2 3 2 2 2
苯的取代反应:
苯环上的定位效应:
①邻、对位取代基:—R、—OH、—NH 、—OR、—X(Cl、Br、I)等;
2
②间位取代基:—NO 、—SO H、—CHO、—COOH、—COOR 等(为吸
2 3
电子基)
卤代烃的水解:CHCHBr+NaOH――→CHCHOH+NaBr
3 2 3 2
取代 醇分子间脱水:CHCH—OH+HO—CH CH――→CHCH—O—CH CH
3 2 2 3 3 2 2 3
反应
+HO
2
酯化反应:CHCOOH+C HOHCHCOOC H+HO、
3 2 5 3 2 5 2
酯 的 水 解 反 应 ( 含 皂 化 反 应 ) :
C H O 蔗糖+HO――→C H O 葡萄糖+C H O 果糖
12 22 11 2 6 12 6 6 12 6
二肽水解:CH≡CH+Br ―→CHBr===CHBr、CHBr===CHBr+Br ―→CHBr —CHBr
2 2 2 2
加
CH—CH===CH +HBr――→CH—CHBr—CH (马氏规则)、
3 2 3 3
成
CH—CH===CH +HBr――→CH—CH—CHBr(反马氏规则)
3 2 3 2 2
反
1,3-丁二烯的加成反应:
应
CH===CH—CH===CH +Cl―→CHCl—CHCl—CH===CH (1,2-加成)、
2 2 2 2 2
CH===CH—CH===CH +Cl―→CHCl—CH===CH—CHCl(1,4-加成)
2 2 2 2 2
Diels-Alder反应:
醇分子内脱水生成烯烃:C HOH――→CH===CH ↑+HO
2 5 2 2 2
消去
卤代烃脱HX生成烯烃:CHCHBr+NaOH――→CH===CH ↑+NaBr+
3 2 2 2
反应
HO
2
加
聚
共轭二烯烃的加聚:
反
应
二元醇与二元羧酸之间的缩聚:
缩
聚
反
应
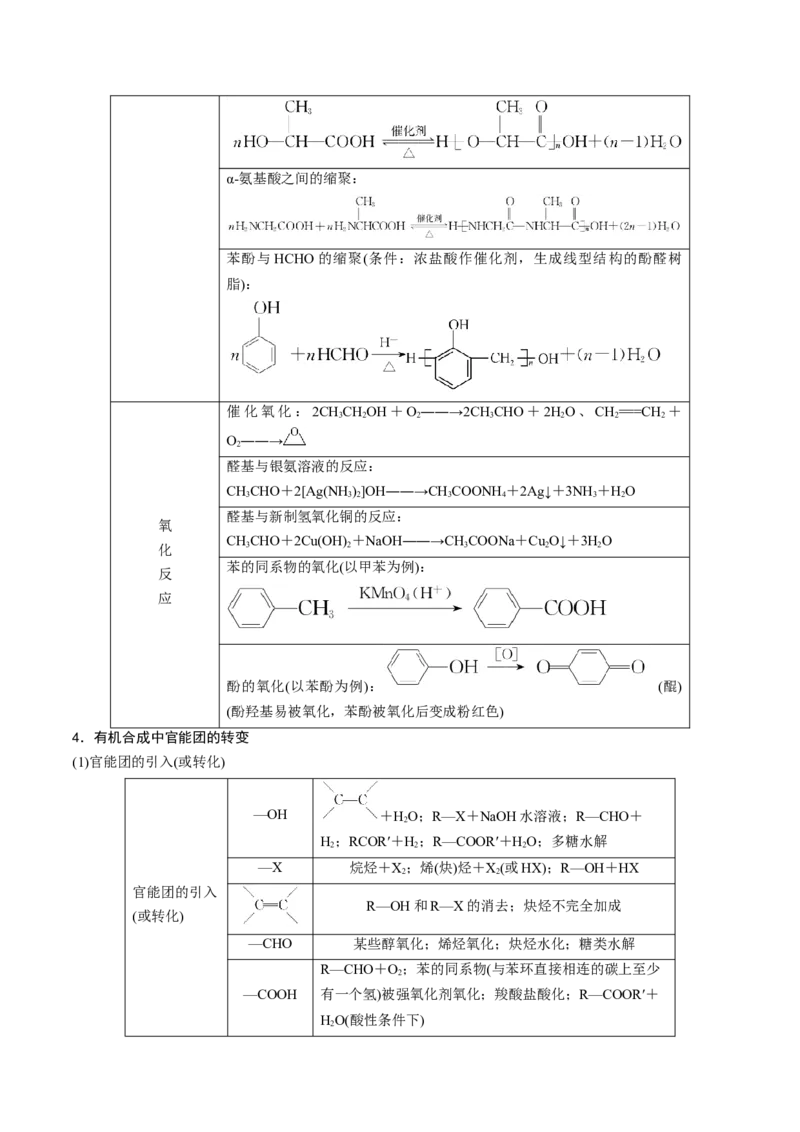
α-羟基酸之间的缩聚:α-氨基酸之间的缩聚:
苯酚与HCHO的缩聚(条件:浓盐酸作催化剂,生成线型结构的酚醛树
脂):
催化氧化:2CHCHOH+O――→2CHCHO+2HO、CH===CH +
3 2 2 3 2 2 2
O――→
2
醛基与银氨溶液的反应:
CHCHO+2[Ag(NH)]OH――→CHCOONH+2Ag↓+3NH +HO
3 3 2 3 4 3 2
醛基与新制氢氧化铜的反应:
氧
CHCHO+2Cu(OH) +NaOH――→CHCOONa+Cu O↓+3HO
化 3 2 3 2 2
苯的同系物的氧化(以甲苯为例):
反
应
酚的氧化(以苯酚为例): (醌)
(酚羟基易被氧化,苯酚被氧化后变成粉红色)
4.有机合成中官能团的转变
(1)官能团的引入(或转化)
—OH +HO;R—X+NaOH水溶液;R—CHO+
2
H;RCOR′+H;R—COOR′+HO;多糖水解
2 2 2
—X 烷烃+X;烯(炔)烃+X(或HX);R—OH+HX
2 2
官能团的引入
R—OH和R—X的消去;炔烃不完全加成
(或转化)
—CHO 某些醇氧化;烯烃氧化;炔烃水化;糖类水解
R—CHO+O;苯的同系物(与苯环直接相连的碳上至少
2
—COOH 有一个氢)被强氧化剂氧化;羧酸盐酸化;R—COOR′+
HO(酸性条件下)
2—COOR 酯化反应
(2)官能团的消除
①消除碳碳双键:加成反应、氧化反应。
②消除羟基:消去反应、氧化反应、酯化反应、取代反应。
③消除醛基:还原反应、氧化反应。
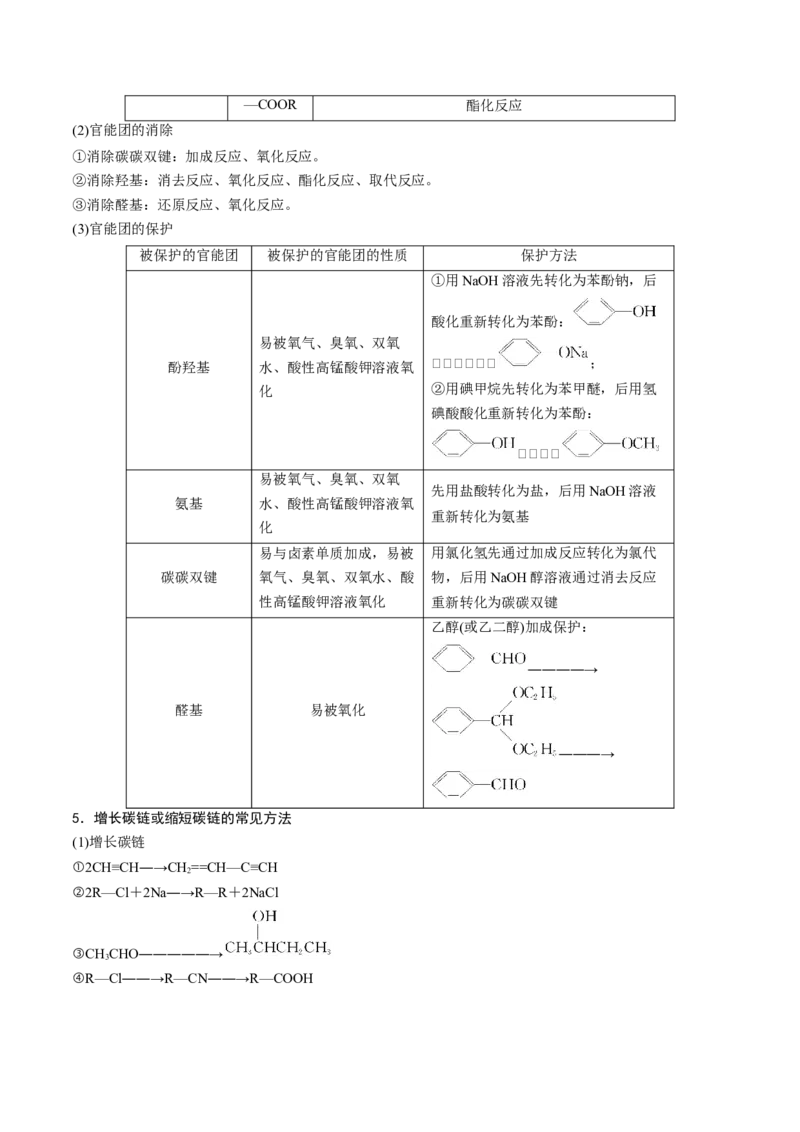
(3)官能团的保护
被保护的官能团 被保护的官能团的性质 保护方法
①用NaOH溶液先转化为苯酚钠,后
酸化重新转化为苯酚:
易被氧气、臭氧、双氧
酚羟基 水、酸性高锰酸钾溶液氧 ;
化 ②用碘甲烷先转化为苯甲醚,后用氢
碘酸酸化重新转化为苯酚:
易被氧气、臭氧、双氧
先用盐酸转化为盐,后用NaOH溶液
氨基 水、酸性高锰酸钾溶液氧
重新转化为氨基
化
易与卤素单质加成,易被 用氯化氢先通过加成反应转化为氯代
碳碳双键 氧气、臭氧、双氧水、酸 物,后用NaOH醇溶液通过消去反应
性高锰酸钾溶液氧化 重新转化为碳碳双键
乙醇(或乙二醇)加成保护:
――――→
醛基 易被氧化
―――→
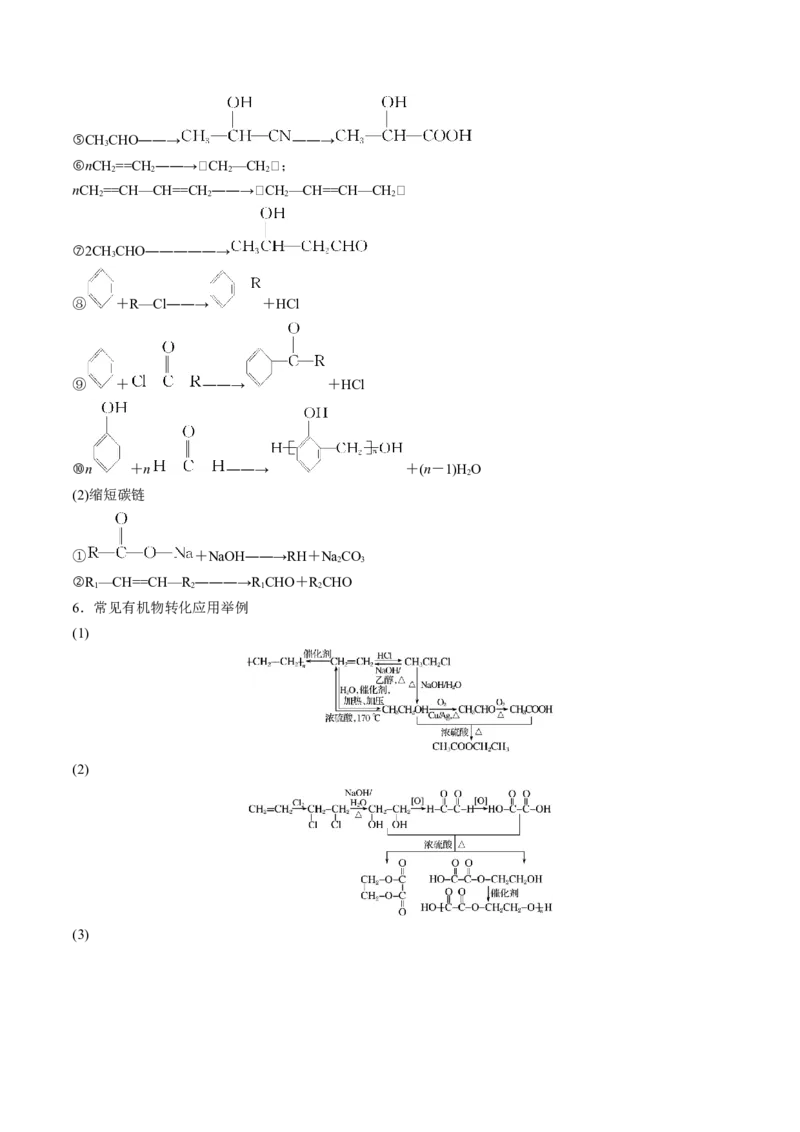
5.增长碳链或缩短碳链的常见方法
(1)增长碳链
①2CH≡CH―→CH==CH—C≡CH
2
②2R—Cl+2Na―→R—R+2NaCl
③CH CHO―――――→
3
④R—Cl――→R—CN――→R—COOH⑤CHCHO――→ ――→
3
⑥nCH==CH ――→CH —CH;
2 2 2 2
nCH==CH—CH==CH ――→CH —CH==CH—CH
2 2 2 2
⑦2CH CHO―――――→
3
⑧ +R—Cl――→ +HCl
⑨ + ――→ +HCl
⑩n +n ――→ +(n-1)H O
2
(2)缩短碳链
① +NaOH――→RH+NaCO
2 3
②R —CH==CH—R ―――→R CHO+R CHO
1 2 1 2
6.常见有机物转化应用举例
(1)
(2)
(3)(4)CH CHO―――――→ ――→
3
7.依据合成框图及相关信息设计有机合成路线
表达方式 A――→B――→C……―→D
总体思路 根据目标分子与原料分子的差异构建碳骨架和实现官能团转化
设计关键 信息及框图流程的运用
从某种原料分子开始,对比目标分子与原料分子的结构(碳骨架及
官能团),对该原料分子进行碳骨架的构建和官能团的引入(或者官
能团的转化),从而设计出合理的合成路线,其思维程序为
正向合
成法
从目标分子着手,分析目标分子的结构,然后由目标分子逆推出原
料分子,并进行合成路线的设计,其思维程序为
常用
逆向合
方法
成法
采用正推和逆推相结合的方法,是解决合成路线题的最实用的方
法,其思维程序为
正逆双
向合
成法
考点 有机推断与有机合成
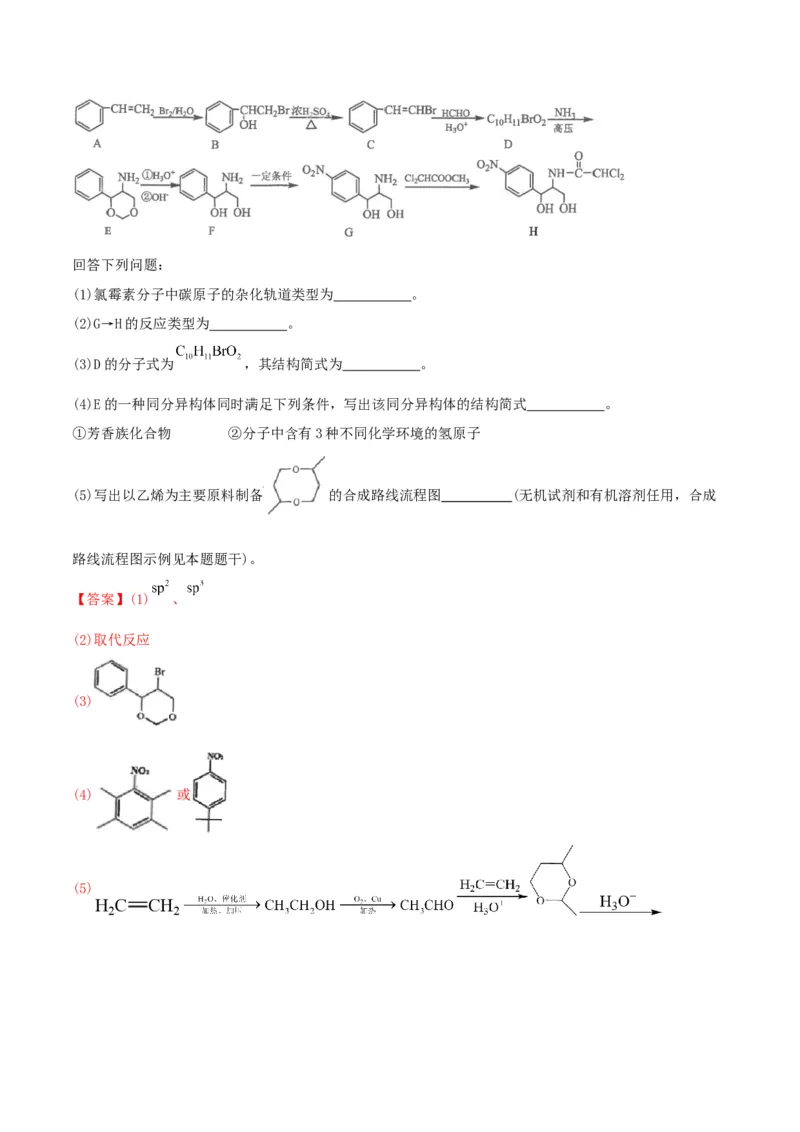
1.(2024·江苏扬州中学高三上学期开学考试,15)氯霉素(H)的一种合成路线如下:回答下列问题:
(1)氯霉素分子中碳原子的杂化轨道类型为 。
(2)G→H的反应类型为 。
(3)D的分子式为 ,其结构简式为 。
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式 。
①芳香族化合物 ②分子中含有3种不同化学环境的氢原子
(5)写出以乙烯为主要原料制备 的合成路线流程图 (无机试剂和有机溶剂任用,合成
路线流程图示例见本题题干)。
【答案】(1) 、
(2)取代反应
(3)
(4) 或
(5)。
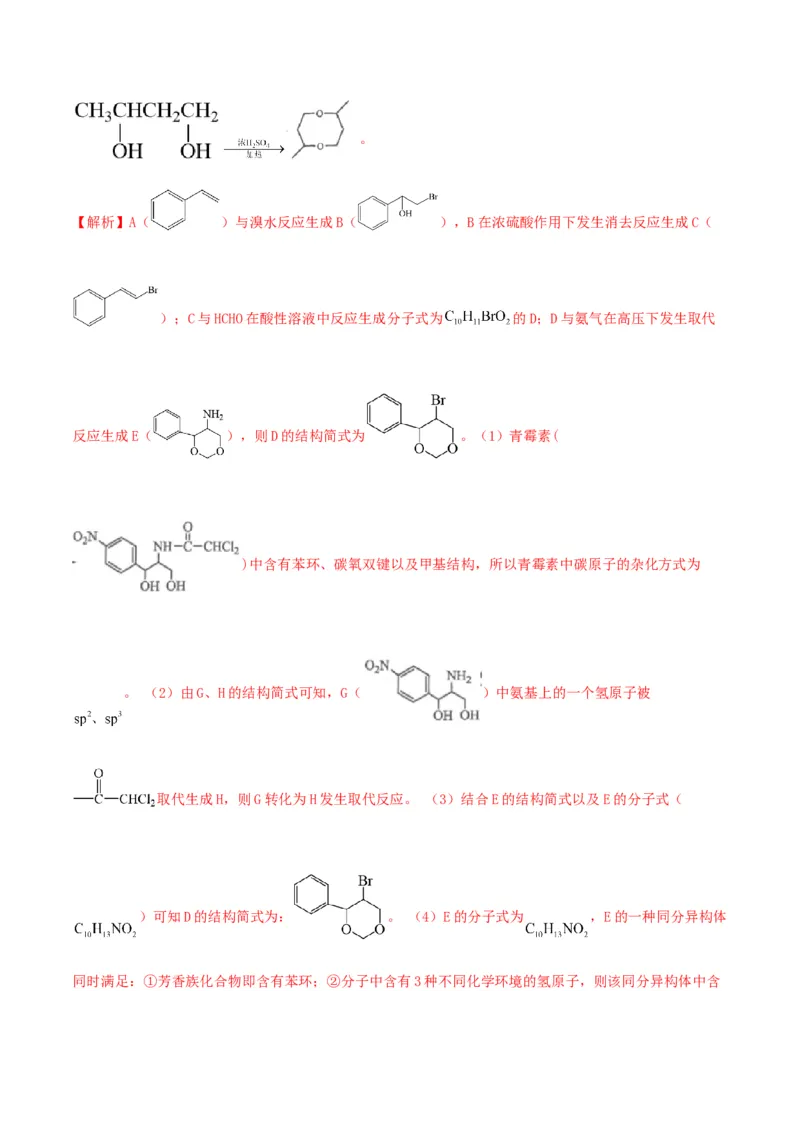
【解析】A( )与溴水反应生成B( ),B在浓硫酸作用下发生消去反应生成C(
);C与HCHO在酸性溶液中反应生成分子式为 的D;D与氨气在高压下发生取代
反应生成E( ),则D的结构简式为 。(1)青霉素(
)中含有苯环、碳氧双键以及甲基结构,所以青霉素中碳原子的杂化方式为
。 (2)由G、H的结构简式可知,G( )中氨基上的一个氢原子被
取代生成H,则G转化为H发生取代反应。 (3)结合E的结构简式以及E的分子式(
)可知D的结构简式为: 。 (4)E的分子式为 ,E的一种同分异构体
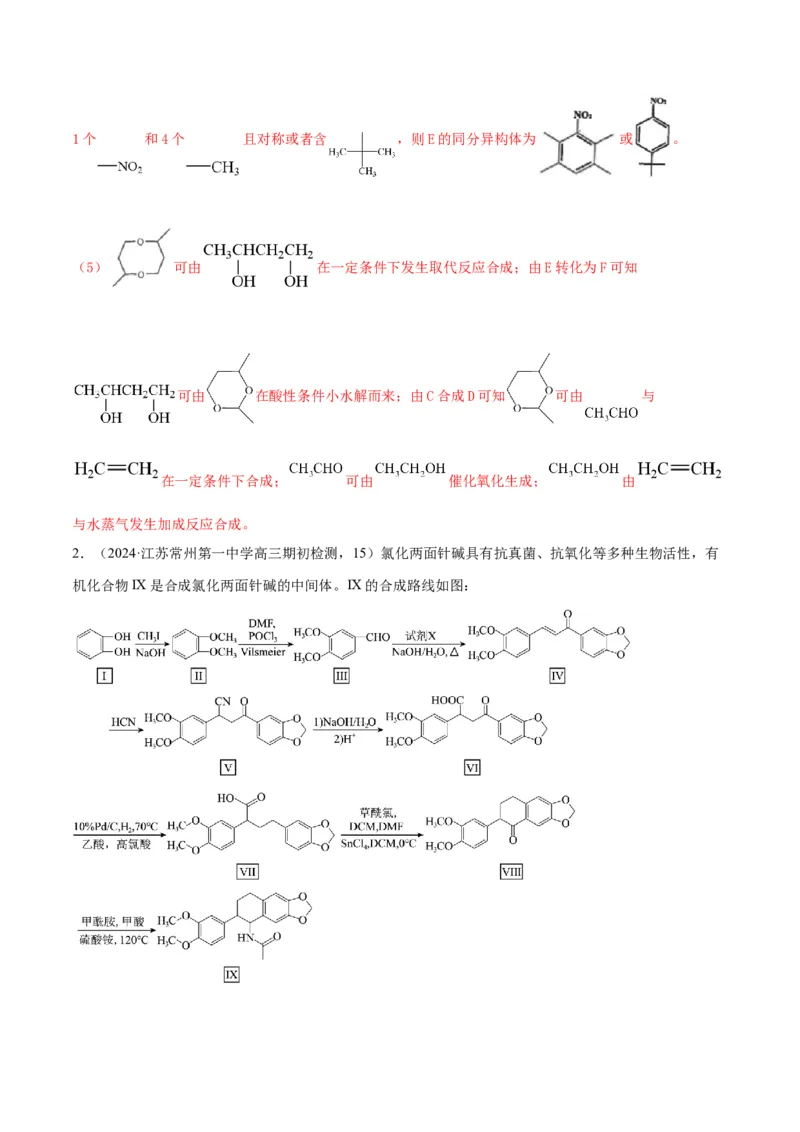
同时满足:①芳香族化合物即含有苯环;②分子中含有3种不同化学环境的氢原子,则该同分异构体中含1个 和4个 且对称或者含 ,则E的同分异构体为 或 。
(5) 可由 在一定条件下发生取代反应合成;由E转化为F可知
可由 在酸性条件小水解而来;由C合成D可知 可由 与
在一定条件下合成; 可由 催化氧化生成; 由
与水蒸气发生加成反应合成。
2.(2024·江苏常州第一中学高三期初检测,15)氯化两面针碱具有抗真菌、抗氧化等多种生物活性,有
机化合物IX是合成氯化两面针碱的中间体。IX的合成路线如图:已知:i.RCHO+ +H O
2
ii.
回答下列问题:
(1)Ⅳ中的含氧官能团的名称为 ,Ⅵ→Ⅶ的反应类型为 。
(2)X的结构简式为 。
(3)Ⅳ的同分异构体中,满足下列条件的是 。
①结构中含有3个六元环;
②核磁共振共有6组峰;
③不能发生银镜反应,且酸性环境能发生水解反应,所得产物遇 变色。
(4)写出以 为主要原料制备 的合成路线流程图 (无机试剂和有机溶
剂任用)。
【答案】(1) 醚键、酮羰基 还原反应
(2)
(3) 、 、 、
(4)【解析】由有机物的转化关系可知,氢氧化钠作用下 与一碘甲烷发生取代反应生成
, 一定条件下转化为 , 与
发生信息i反应生成 ,则X为 ;
与氢氰酸发生加成反应生成 ,
碱性条件下发生水解反应后,酸化得到
; 一定条件下发生还原反应生
成 , 一定条件下发生分子内取代反应生成 , 一定条件下转化为
。(1)由结构简式可知, 的含氧
官能团为醚键、酮羰基;Ⅵ→Ⅶ的反应为 一定条件下发生还原反应生
成 。(2)由分析可知,X的结构简式为 。(3)Ⅳ的
同分异构体的结构中含有3个六元环,核磁共振共有6组峰说明同分异构体分子结构对称,不能发生银镜
反应,且酸性环境能发生水解反应,所得产物遇氯化铁变色说明分子中不含有甲酸酯基,含有酚酯基和醚
键,符合条件的结构简式为 、 、
、 。(4)由题给信息可知,以为主要原料制备 的合成步骤为 与氰化钠发生取
代反应生成 , 碱性条件下发生水解反应后,酸化生成
, 一定条件下转化为 , 一
定条件下发生还原反应生成 。
3.(2024·江苏海安高级中学高三12月月考,15)奥培米芬(化合物I)是一种雌激素受体调节剂,以下是一
种合成路线。
已知:Ⅰ.
Ⅱ.
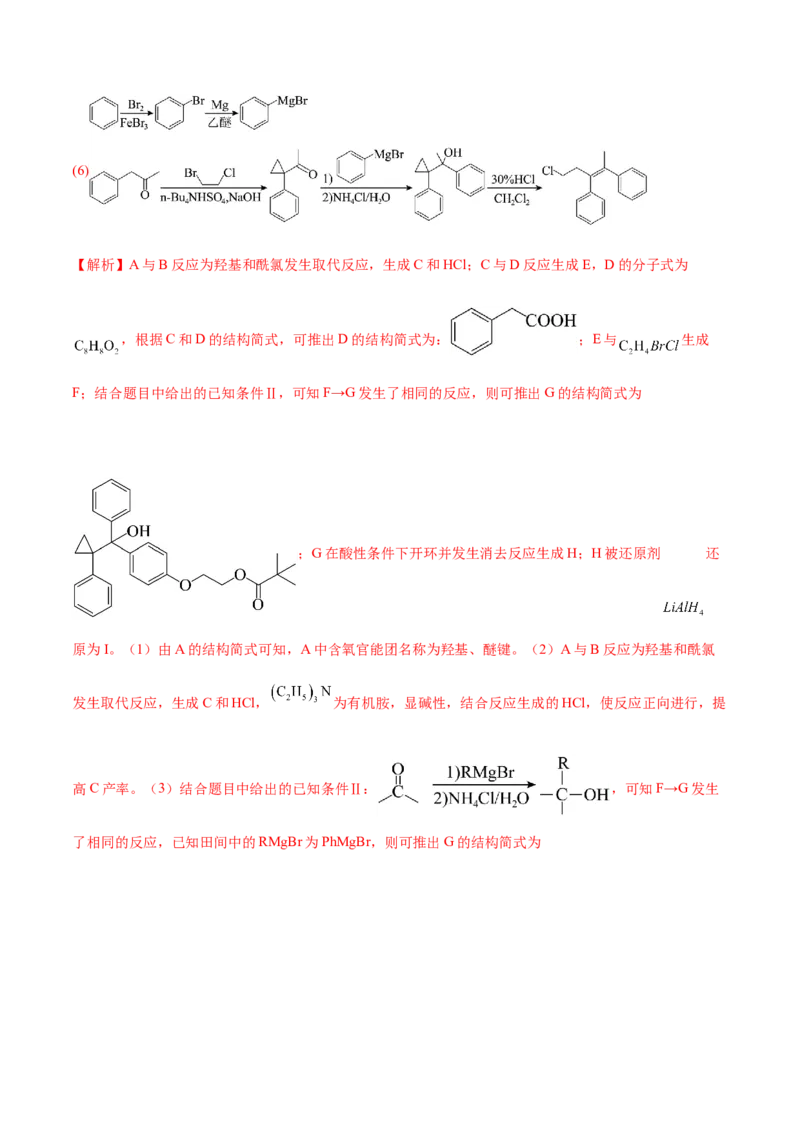
Ⅲ.Ph为苯环(1)A中含氧官能团名称为 。
(2) 过程中加入 的目的是 。
(3)G的结构简式为 。
(4) 的反应类型为 。
(5)写出同时满足下列条件的C的一种同分异构体的结构简式 。
①能发生水解反应;
②遇 溶液显紫色;
③含有苯环;
④核磁共振氢谱显示为四组峰、且峰面积比为9:6:2:1
(6)综合上述信息,写出由 , , 为原料制备 的
合成路线流程图 (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
【答案】(1)羟基、醚键
(2)结合反应生成的HCl,提高C产率
(3)
(4)还原反应
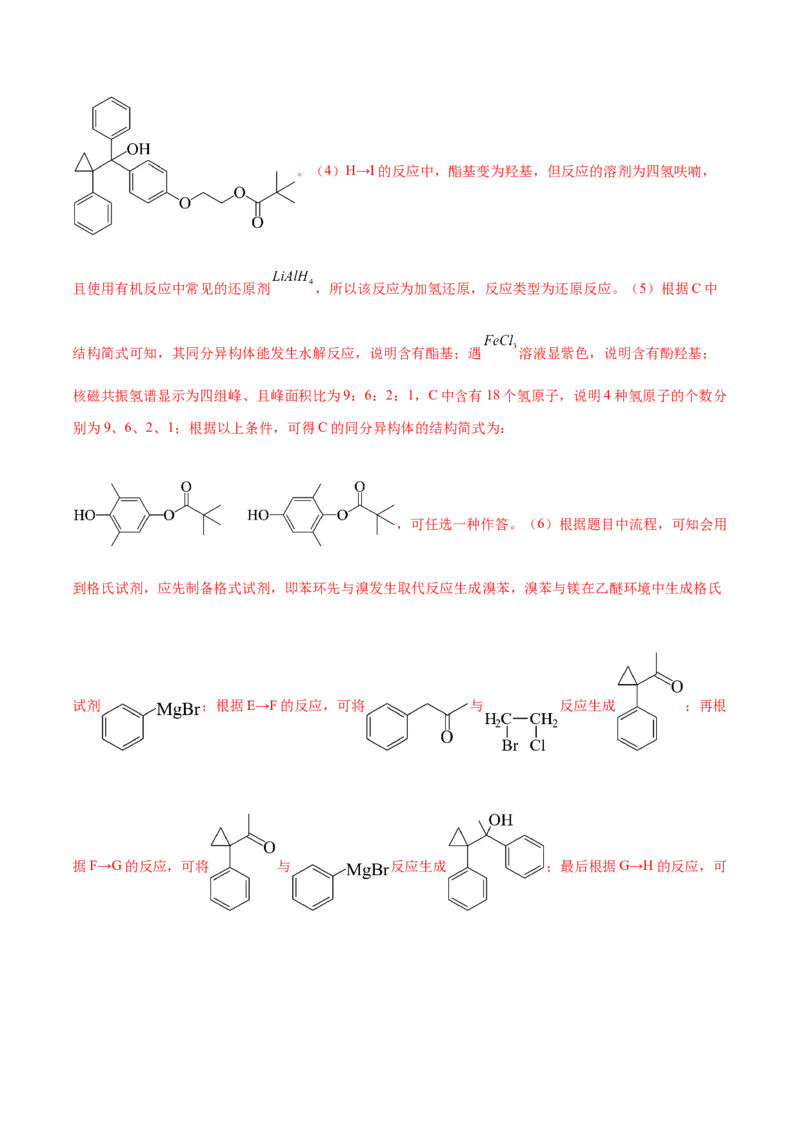
(5)(6)
【解析】A与B反应为羟基和酰氯发生取代反应,生成C和HCl;C与D反应生成E,D的分子式为
,根据C和D的结构简式,可推出D的结构简式为: ;E与 生成
F;结合题目中给出的已知条件Ⅱ,可知F→G发生了相同的反应,则可推出G的结构简式为
;G在酸性条件下开环并发生消去反应生成H;H被还原剂 还
原为I。(1)由A的结构简式可知,A中含氧官能团名称为羟基、醚键。(2)A与B反应为羟基和酰氯
发生取代反应,生成C和HCl, 为有机胺,显碱性,结合反应生成的HCl,使反应正向进行,提
高C产率。(3)结合题目中给出的已知条件Ⅱ: ,可知F→G发生
了相同的反应,已知田间中的RMgBr为PhMgBr,则可推出G的结构简式为。(4)H→I的反应中,酯基变为羟基,但反应的溶剂为四氢呋喃,
且使用有机反应中常见的还原剂 ,所以该反应为加氢还原,反应类型为还原反应。(5)根据C中
结构简式可知,其同分异构体能发生水解反应,说明含有酯基;遇 溶液显紫色,说明含有酚羟基;
核磁共振氢谱显示为四组峰、且峰面积比为9:6:2:1,C中含有18个氢原子,说明4种氢原子的个数分
别为9、6、2、1;根据以上条件,可得C的同分异构体的结构简式为:
,可任选一种作答。(6)根据题目中流程,可知会用
到格氏试剂,应先制备格式试剂,即苯环先与溴发生取代反应生成溴苯,溴苯与镁在乙醚环境中生成格氏
试剂 ;根据E→F的反应,可将 与 反应生成 ;再根
据F→G的反应,可将 与 反应生成 ;最后根据G→H的反应,可将 在酸性条件下开环并发生消去反应,生成 。
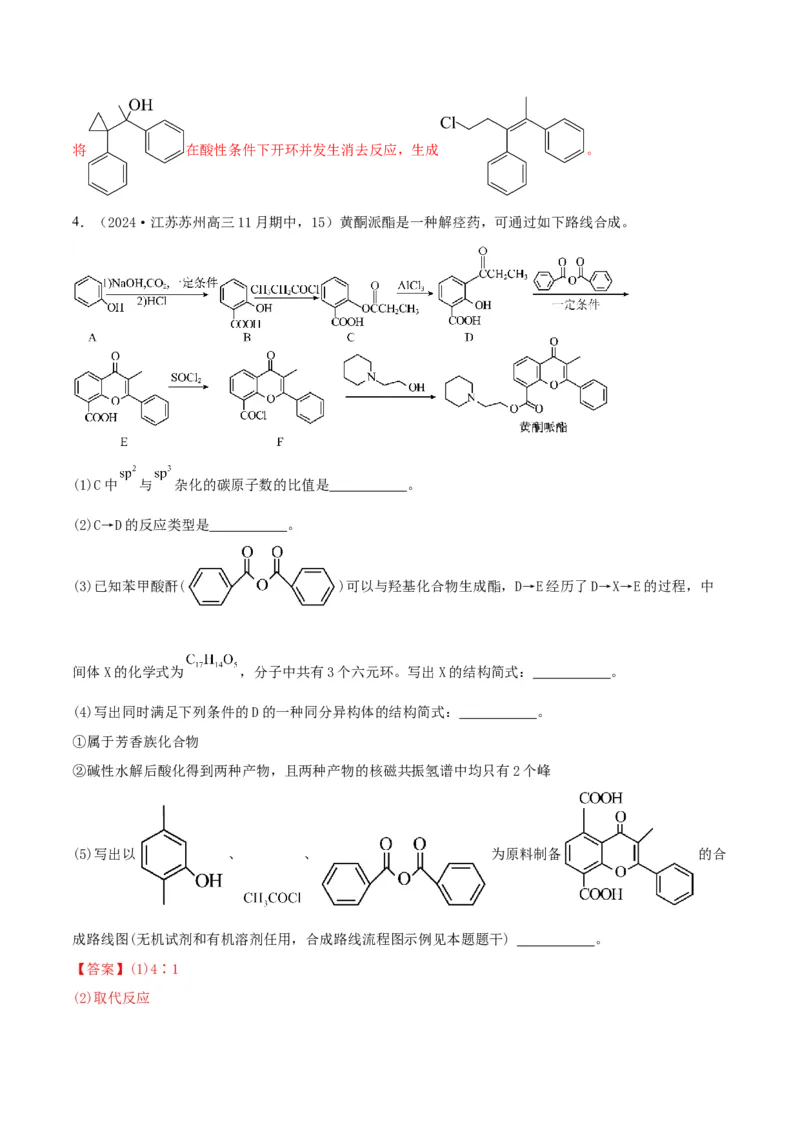
4.(2024·江苏苏州高三11月期中,15)黄酮派酯是一种解痉药,可通过如下路线合成。
(1)C中 与 杂化的碳原子数的比值是 。
(2)C→D的反应类型是 。
(3)已知苯甲酸酐( )可以与羟基化合物生成酯,D→E经历了D→X→E的过程,中
间体X的化学式为 ,分子中共有3个六元环。写出X的结构简式: 。
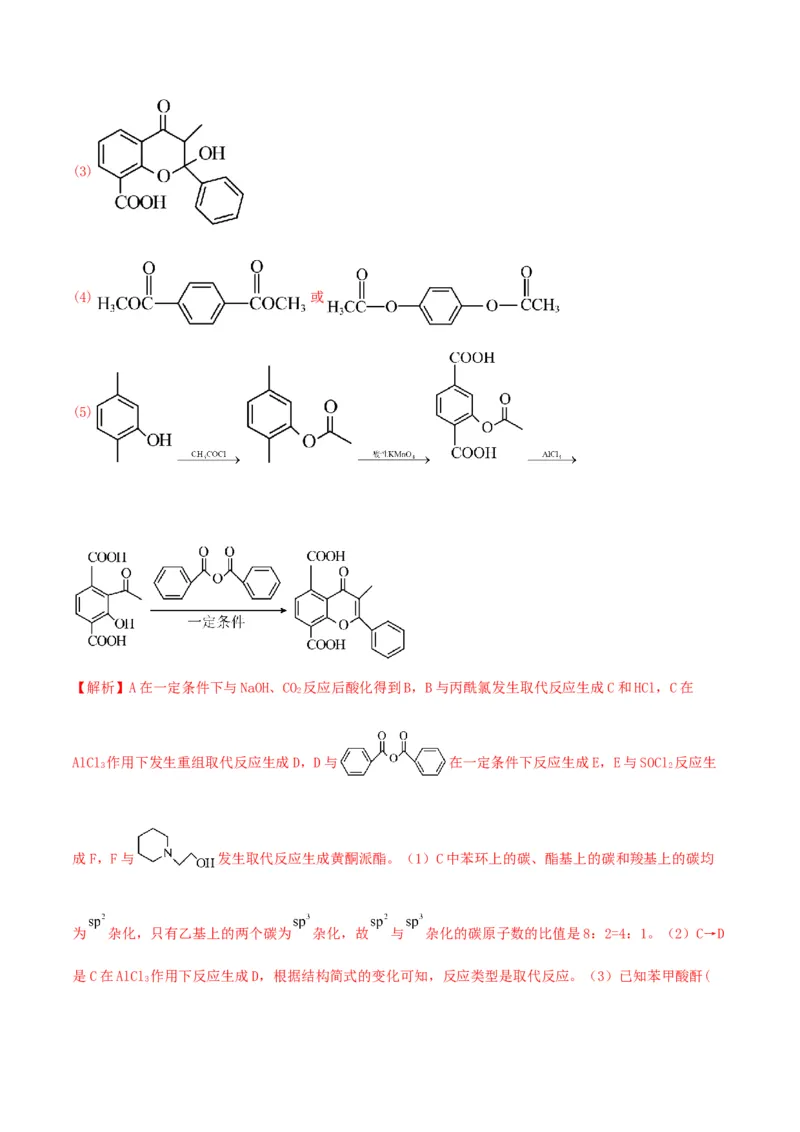
(4)写出同时满足下列条件的D的一种同分异构体的结构简式: 。
①属于芳香族化合物
②碱性水解后酸化得到两种产物,且两种产物的核磁共振氢谱中均只有2个峰
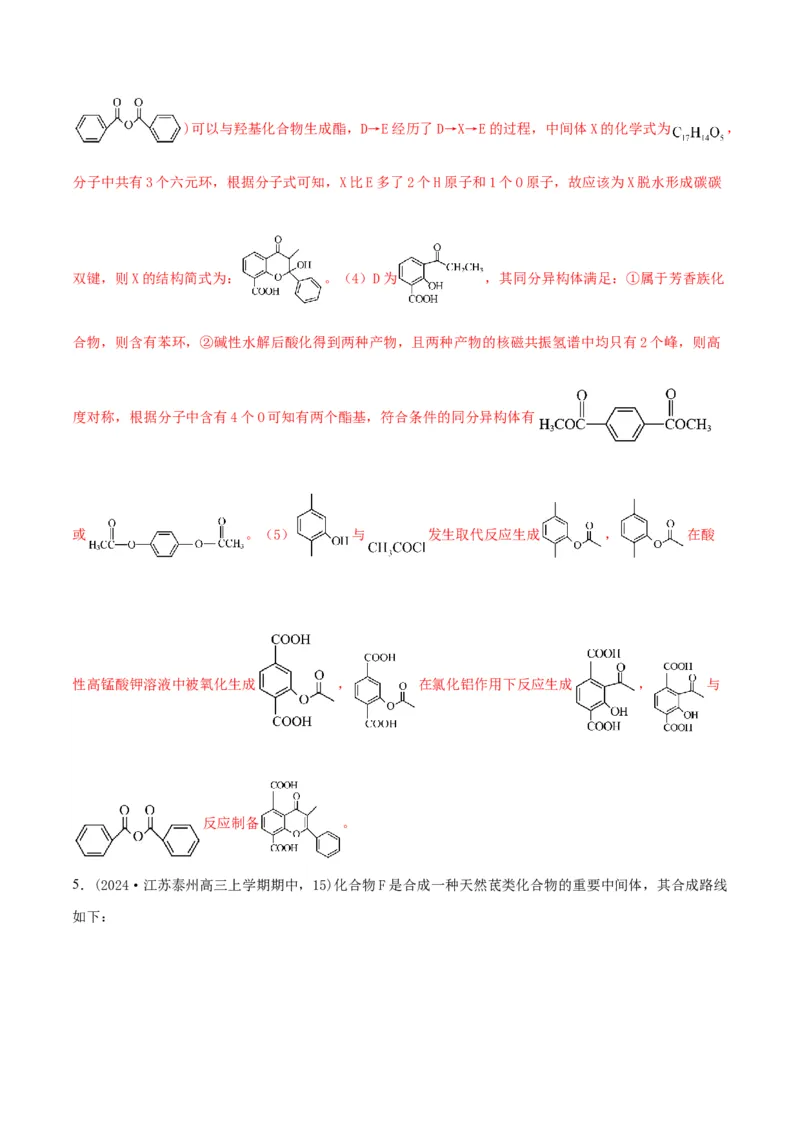
(5)写出以 、 、 为原料制备 的合
成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干) 。
【答案】(1)4∶1
(2)取代反应(3)
(4) 或
(5)
【解析】A在一定条件下与NaOH、CO 反应后酸化得到B,B与丙酰氯发生取代反应生成C和HCl,C在
2
AlCl 作用下发生重组取代反应生成D,D与 在一定条件下反应生成E,E与SOCl 反应生
3 2
成F,F与 发生取代反应生成黄酮派酯。(1)C中苯环上的碳、酯基上的碳和羧基上的碳均
为 杂化,只有乙基上的两个碳为 杂化,故 与 杂化的碳原子数的比值是8:2=4:1。(2)C→D
是C在AlCl 作用下反应生成D,根据结构简式的变化可知,反应类型是取代反应。(3)已知苯甲酸酐(
3)可以与羟基化合物生成酯,D→E经历了D→X→E的过程,中间体X的化学式为 ,
分子中共有3个六元环,根据分子式可知,X比E多了2个H原子和1个O原子,故应该为X脱水形成碳碳
双键,则X的结构简式为: 。(4)D为 ,其同分异构体满足:①属于芳香族化
合物,则含有苯环,②碱性水解后酸化得到两种产物,且两种产物的核磁共振氢谱中均只有2个峰,则高
度对称,根据分子中含有4个O可知有两个酯基,符合条件的同分异构体有
或 。(5) 与 发生取代反应生成 , 在酸
性高锰酸钾溶液中被氧化生成 , 在氯化铝作用下反应生成 , 与
反应制备 。
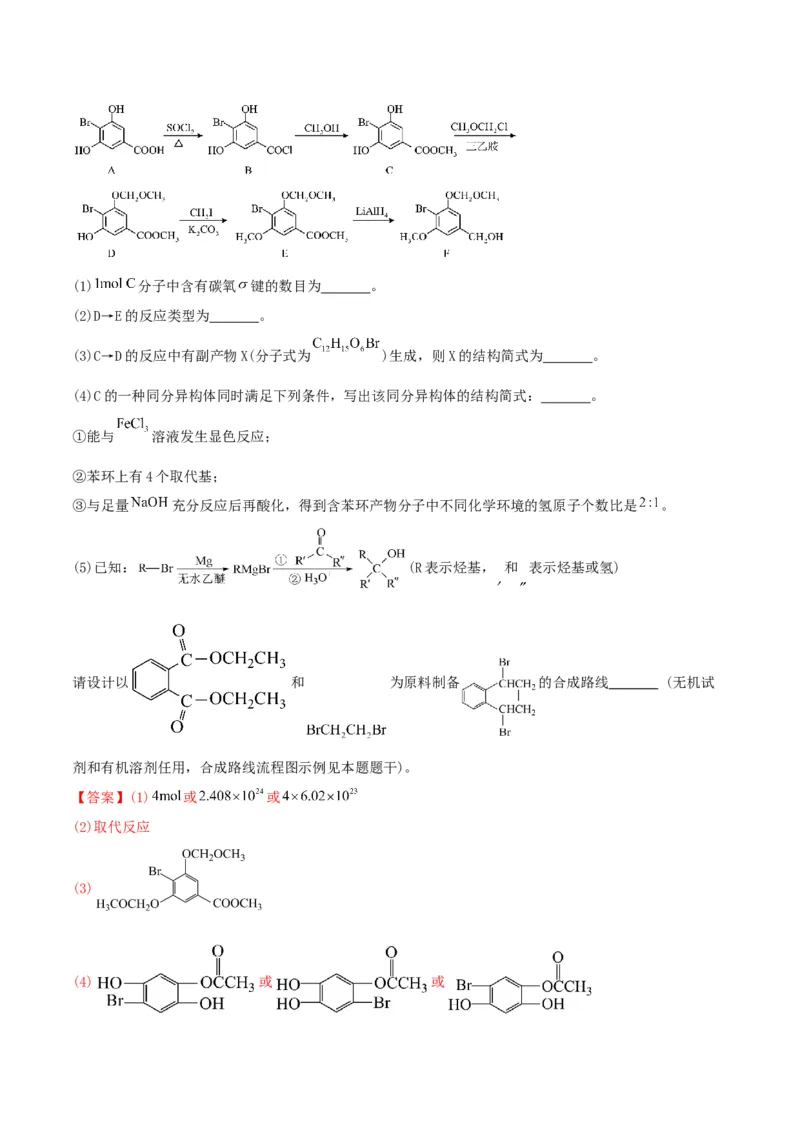
5.(2024·江苏泰州高三上学期期中,15)化合物F是合成一种天然茋类化合物的重要中间体,其合成路线
如下:(1) 分子中含有碳氧 键的数目为 。
(2)D→E的反应类型为 。
(3)C→D的反应中有副产物X(分子式为 )生成,则X的结构简式为 。
(4)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: 。
①能与 溶液发生显色反应;
②苯环上有4个取代基;
③与足量 充分反应后再酸化,得到含苯环产物分子中不同化学环境的氢原子个数比是 。
(5)已知: (R表示烃基, 和 表示烃基或氢)
请设计以 和 为原料制备 的合成路线 (无机试
剂和有机溶剂任用,合成路线流程图示例见本题题干)。
【答案】(1) 或 或
(2)取代反应
(3)
(4) 或 或(5)
【解析】A到B为羧基被亚硫酰氯酰化;B到C为酰氯和醇发生的取代反应;C到D是C分子苯环上的酚羟
基发生了取代反应;D到E是D分子苯环上的酚羟基发生了取代反应;E到F是酯基被还原为醇羟基。
(1)分析C的结构简式可知,1个C分子中含有4个碳氧 键,所以1molC分子中含有碳氧σ键的数目为
4mol。(2)D到E是一碘甲烷中的甲基取代了D分子中羟基上的氢原子,属于取代反应。(3)副产物X比
D多两个碳原子,说明D中剩下的羟基也被取代,则X的结构简式为: 。(4)条件
①说明分子中有酚羟基,条件②必须有4个取代基,条件③说明最后产物只有两种环境下的氢原子,且数
目比为2:1,根据以上条件,可得到该同分异构体的结构简式: 、 、
。(5)根据题目中的E到F的反应,酯基可以直接还原为醇羟基,
可直接转化为 ,醇羟基可进一步氧化为醛,即 ,题目给出的已知是卤代烃转化为格氏试剂的反应,然后再与醛反应,所以 可以转化为格氏试
剂 ,与 进一步反应可以生成 ,再与溴化氢发生取代,
得到 。
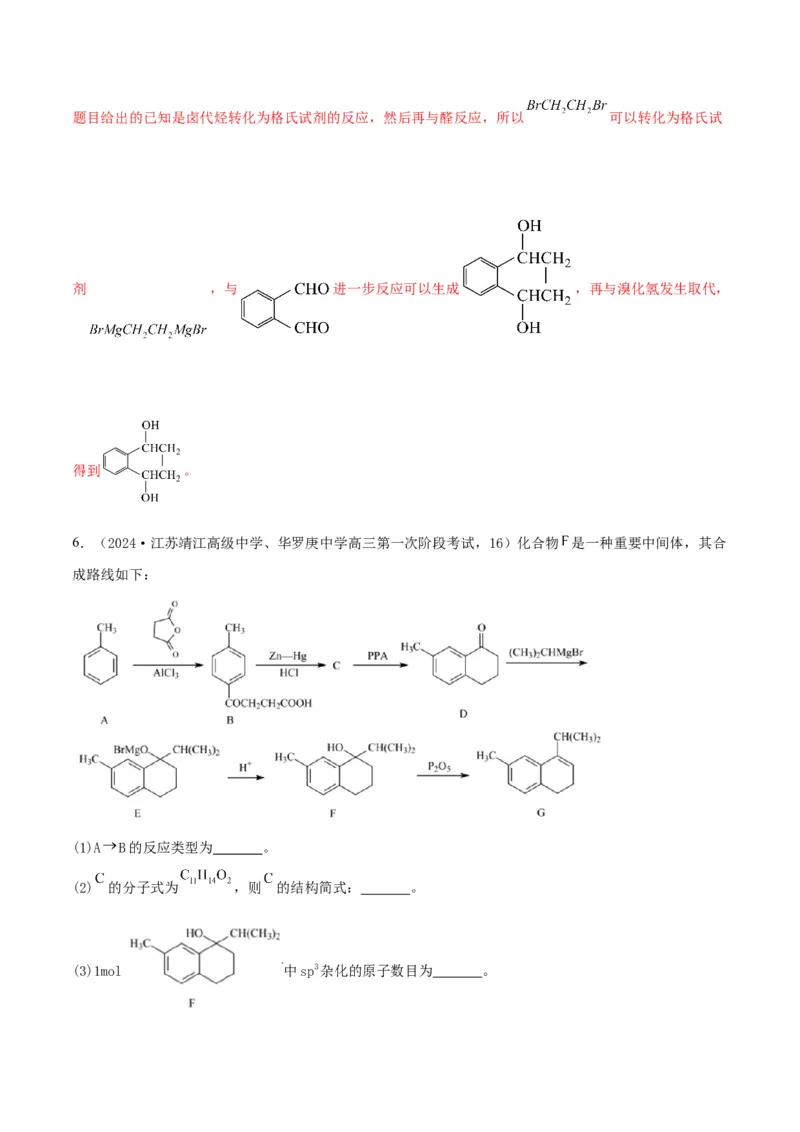
6.(2024·江苏靖江高级中学、华罗庚中学高三第一次阶段考试,16)化合物 是一种重要中间体,其合
成路线如下:
(1)A B的反应类型为 。
(2) 的分子式为 ,则 的结构简式: 。
(3)1mol 中sp3杂化的原子数目为 。(4) 的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式 。
①能发生银镜反应;
②能与 溶液发生显色反应;
③分子中只有4种不同化学环境的氢。
(5)已知: 。设计以 原料制备 的合成路线(无机试剂和
有机溶剂任用,合成路线示例见本题题干)。
【答案】(1)加成反应
(2)
(3)9N
A
(4) 或
(5) 【解析】
与 在氯化铝催化作用下发生开环加成反应生成B,B在Zn-Hg/HCl作用下发生还原反应,结合
D的结构简式及C的分子式可知该过程中羰基被还原为-CH-,则C的结构简式为: ;C在PPA
2
作用下发生分子内脱水反应生成D,D与格式试剂发生加成反应生成E,E水解得到F,F发生消去反应生成G。(3)由F的结构简式可知F中单键C和单键O原子均采用sp3杂化,个数为9,则1molF中含9Nsp3杂
A
化的原子。(4)B的一种同分异构体同时满足下①能发生银镜反应,说明有醛基;②能与 溶液发生
显色反应;说明有酚羟基;根据B的结构分析,该同分异构体中应含有两个醛基和一个酚羟基;③分子中
只有4种不同化学环境的氢,说明苯环上连接的取代基后有对称性,酚羟基在对称轴上,两个醛基位于对
称位置。则结构可能为: 、 。(5)卤代烃和镁在乙醚条件下反应,
另外还需要将卤代烃变成碳氧双键的结构,即先水解生成羟基,再氧化生成醛基,醛类与格式试剂发生加
成再水解得到目标产物。
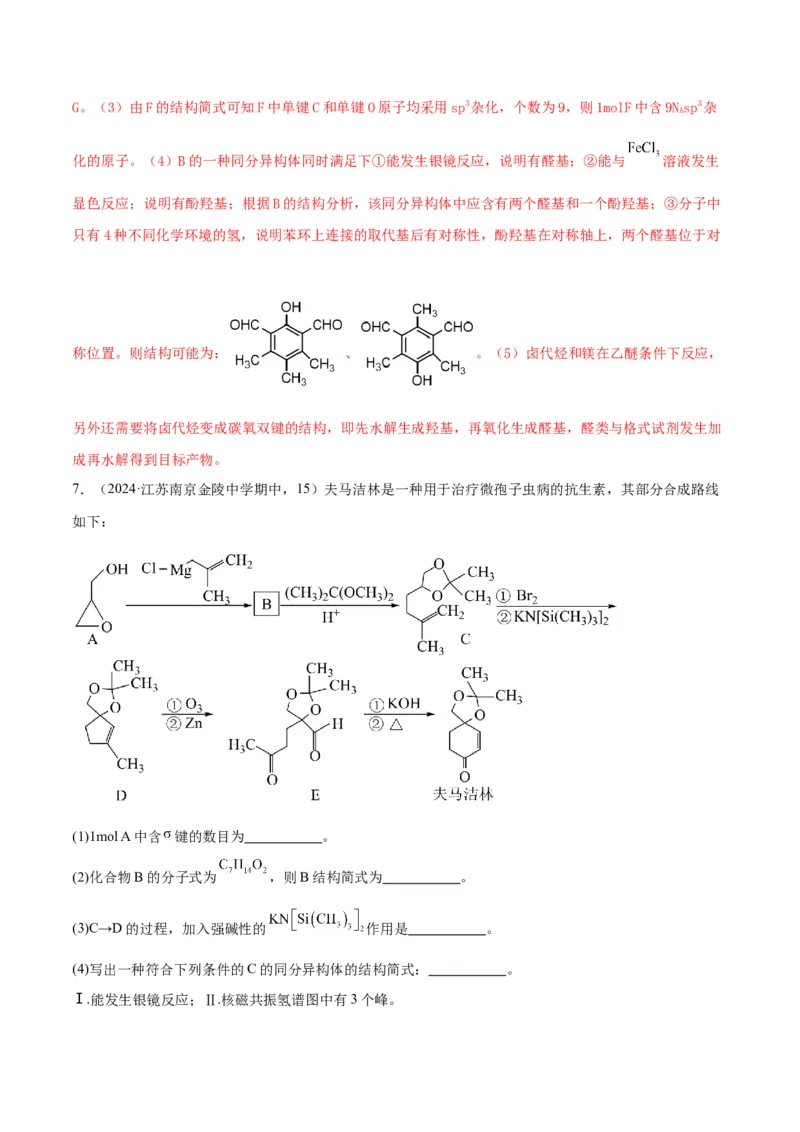
7.(2024·江苏南京金陵中学期中,15)夫马洁林是一种用于治疗微孢子虫病的抗生素,其部分合成路线
如下:
(1)1mol A中含 键的数目为 。
(2)化合物B的分子式为 ,则B结构简式为 。
(3)C→D的过程,加入强碱性的 作用是 。
(4)写出一种符合下列条件的C的同分异构体的结构简式: 。
Ⅰ.能发生银镜反应;Ⅱ.核磁共振氢谱图中有3个峰。(5)写出以 为原料制备 的合成路线流程图(无机试剂任用,合成路线流程图示例见本
题题干) 。
【答案】(1)11N
A
(2)
(3)使卤素原子充分被消去形成双键,闭合成环
(4)
(5)
【解析】对比A、C结构简式,结合B分子式可推出B结构简式: ;B发生取代反应生成C,C在
强碱性条件下使卤素原子充分被消去形成双键,闭合成环生成D;D在臭氧和Zn作用下先开环,在KOH
加热条件下再闭环生成夫马洁林。(1)根据A物质结构可知1mol A中含 键的数目为11N 。(2)化合
A
物B的分子式为 ,结合A、C结构简式对比可知B结构简式: 。(3)加入强碱性的作用:使卤素原子充分被消去形成双键,闭合成环。(4)C分子式 ,符合下列条
件:Ⅰ.能发生银镜反应,说明有醛基;Ⅱ.核磁共振氢谱图中有3个峰,说明为对称结构;则符合要求的同
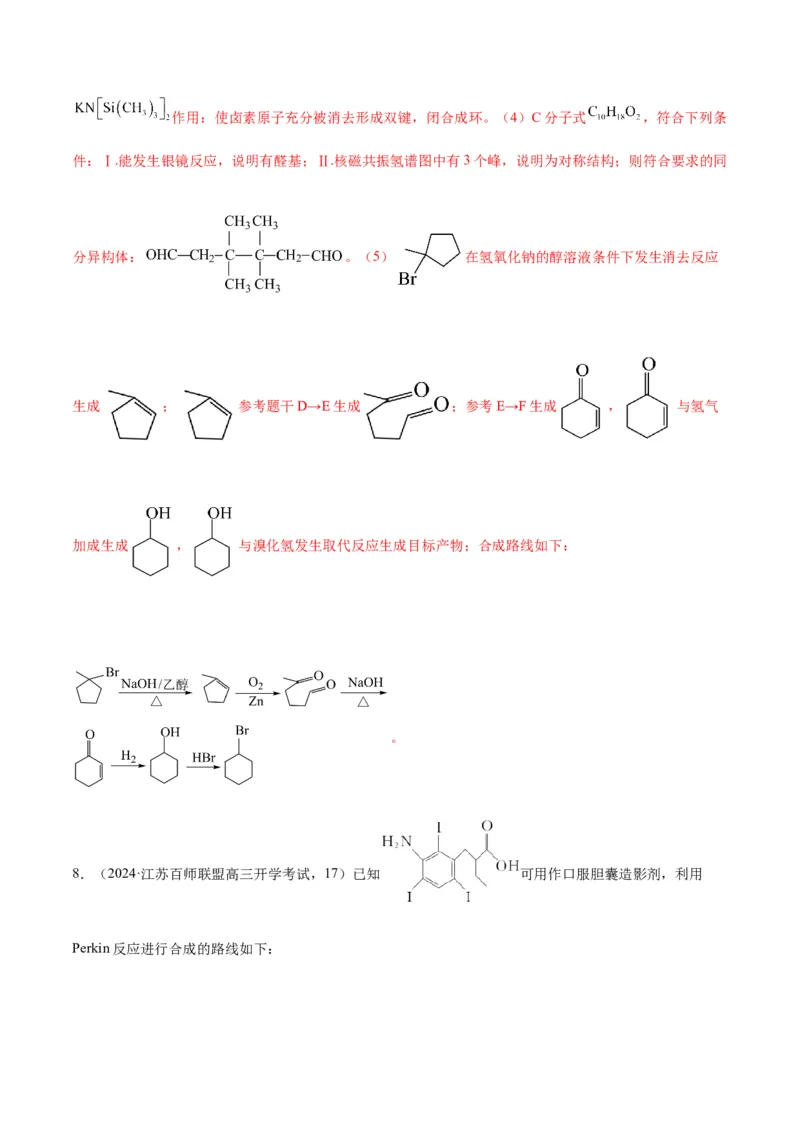
分异构体: 。(5) 在氢氧化钠的醇溶液条件下发生消去反应
生成 ; 参考题干D→E生成 ;参考E→F生成 , 与氢气
加成生成 , 与溴化氢发生取代反应生成目标产物;合成路线如下:
。
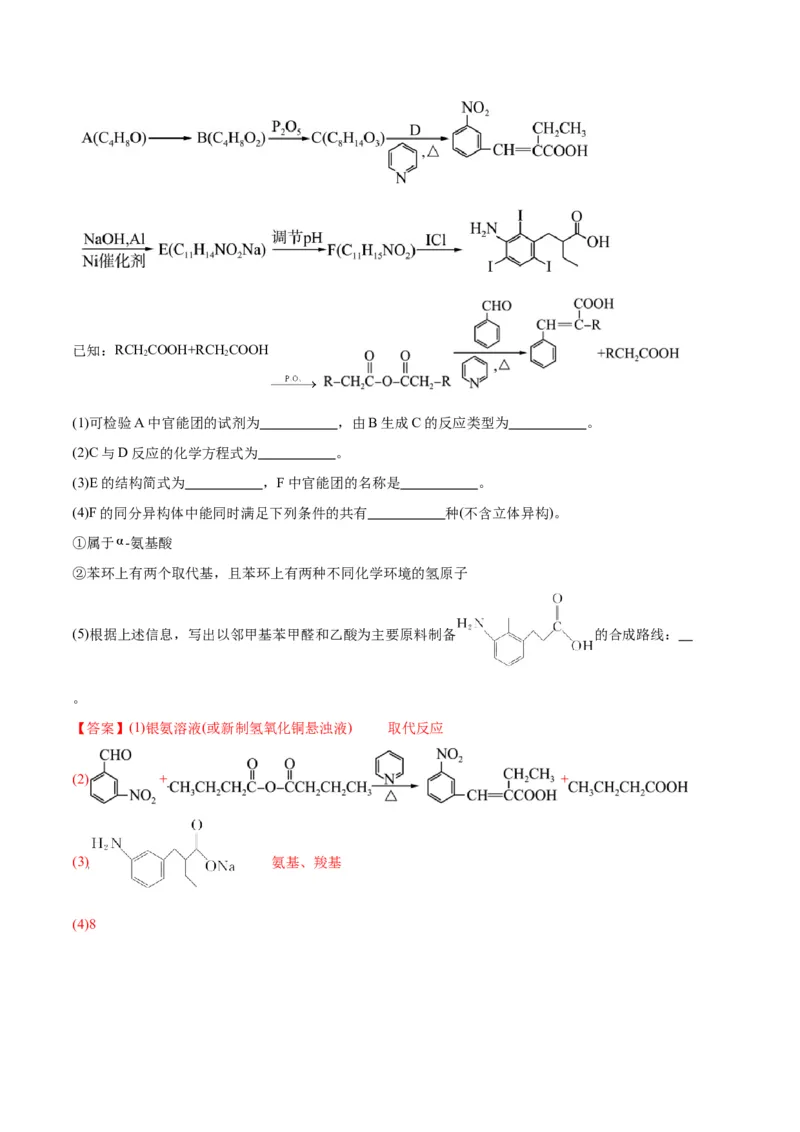
8.(2024·江苏百师联盟高三开学考试,17)已知 可用作口服胆囊造影剂,利用
Perkin反应进行合成的路线如下:已知:RCHCOOH+RCH COOH
2 2
(1)可检验A中官能团的试剂为 ,由B生成C的反应类型为 。
(2)C与D反应的化学方程式为 。
(3)E的结构简式为 ,F中官能团的名称是 。
(4)F的同分异构体中能同时满足下列条件的共有 种(不含立体异构)。
①属于 -氨基酸
②苯环上有两个取代基,且苯环上有两种不同化学环境的氢原子
(5)根据上述信息,写出以邻甲基苯甲醛和乙酸为主要原料制备 的合成路线:
。
【答案】(1)银氨溶液(或新制氢氧化铜悬浊液) 取代反应
(2) + +
(3) 氨基、羧基
(4)8(5)
【解析】B发生信息中第一步反应生成C,C与D发生信息中第二步反应生成 ,
结合B、C的分子式,推知B为CHCHCHCOOH、C为 ,则D为
3 2 2
,结合A的分子式推知A为CHCHCHCHO,结合E的分子式,对比
3 2 2
、目标产物的结构变化,结合E、F的分子式与反应条件,可知硝基还原为氨基、
羧基与氢氧化钠发生中和反应、碳碳双键与氢气加成生成E,E中-COONa转化为-COOH生成F,F与ICl
发生取代反应生成目标产物,故E为 、F为 。(1)根据
已知信息的条件,结合流程图的条件和分子式,A、B的不饱和度均为1,可推知B为 ,
A为 ,检验醛基用银氨溶液或新制氢氧化铜悬浊液。由 生成 的反应为两分子丁酸脱水生成的酸酐, 的结构简式为 ,反应类型为取代反应。(2)结合流
程图C和D反应生成 ,推知则 为 ,C与D反应的化学方程
式为 。(3)由流程图逆
推可知,E的结构简式为 ,F的结构简式为 ,其
官能团的名称是氨基、羧基。(4)F的同分异构体中要求属于 -氨基酸,即氨基和羧基连在同一个碳原子
上,苯环上有两个取代基且苯环上有两种不同化学环境的氢原子,则两个取代基处于苯环的对位,还有三
个饱和碳原子,可能的结构为 、 、 、、 、 、 、 共8
种。(5)CHCOOH在PO 条件下转化为 ,邻甲基苯甲醛 发生硝化反应生成
3 2 5
,然后与 在催化剂条件下生成 ,然后在NaOH、
Al、Ni催化剂条件下生成 ,最后调节pH生成 ,合成路
线为 。
9.(2024·江苏连云港高三期中,15)化合物H可以用于治疗皮炎,其合成路线如下:(1)化合物B的熔点比化合物A的高,主要原因是 。
(2)D的分子式为 ,则D的结构简式可能为 。
(3)E中含有的官能团名称为 。
(4)F→G的反应类型为 。
(5)写出同时满足下列条件的G的一种同分异构体的结构简式: 。
①分子中存在2个六元环状结构;
②碱性条件下水解得到2种有机物,其核磁共振氢谱均只有2个峰。
(6)写出以 为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流
程图示例见本题题干) 。
【答案】(1)化合物B分子间能形成氢键,分子间作用力较大,所以熔点比化合物A高
(2)
(3)羰基、碳氯键
(4)取代反应
(5) 或(6) ,
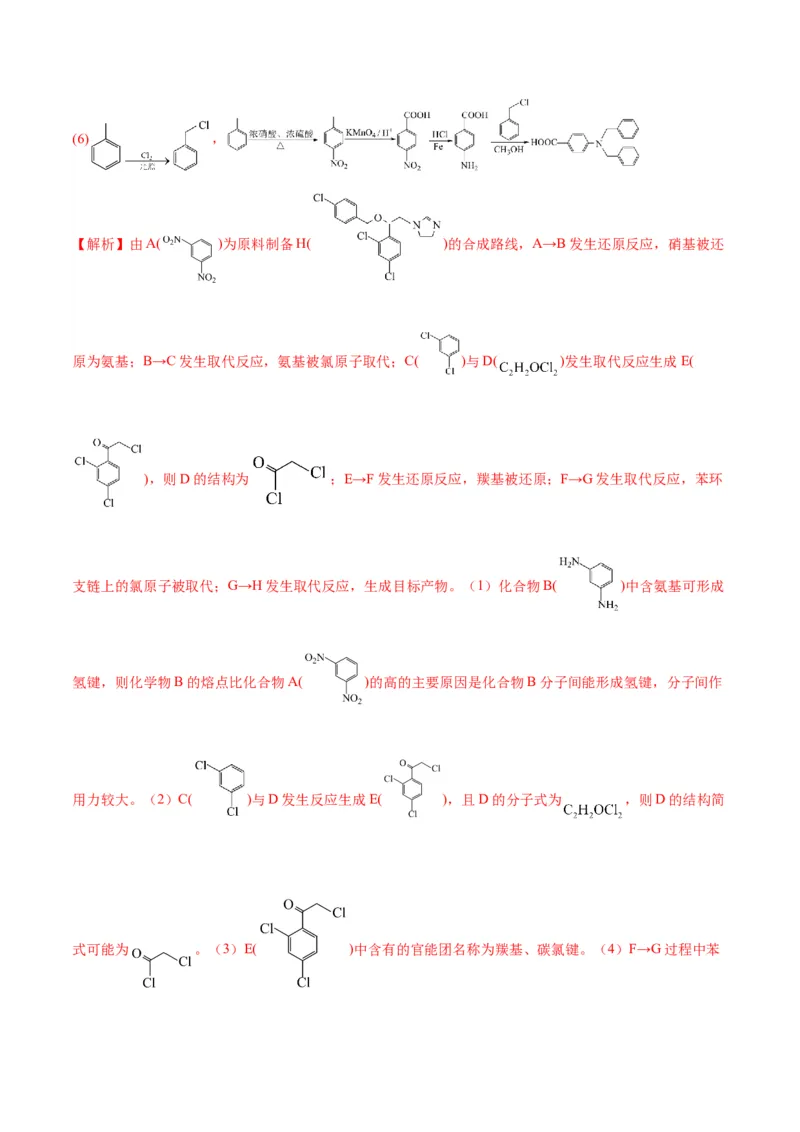
【解析】由A( )为原料制备H( )的合成路线,A→B发生还原反应,硝基被还
原为氨基;B→C发生取代反应,氨基被氯原子取代;C( )与D( )发生取代反应生成E(
),则D的结构为 ;E→F发生还原反应,羰基被还原;F→G发生取代反应,苯环
支链上的氯原子被取代;G→H发生取代反应,生成目标产物。(1)化合物B( )中含氨基可形成
氢键,则化学物B的熔点比化合物A( )的高的主要原因是化合物B分子间能形成氢键,分子间作
用力较大。(2)C( )与D发生反应生成E( ),且D的分子式为 ,则D的结构简
式可能为 。(3)E( )中含有的官能团名称为羰基、碳氯键。(4)F→G过程中苯环支链上的氯原子被取代,则F→G的反应类型为取代反应;(5)G( )同分异构体满足①分子
中存在2个六元环状结构②碱性条件下水解得到2种有机物,其核磁共振氢谱均只有2个峰,则该同分异
构体含酰胺基,则可能的结构为 或 。(6)以 为原料制
备 ,需要由 合成 和 。
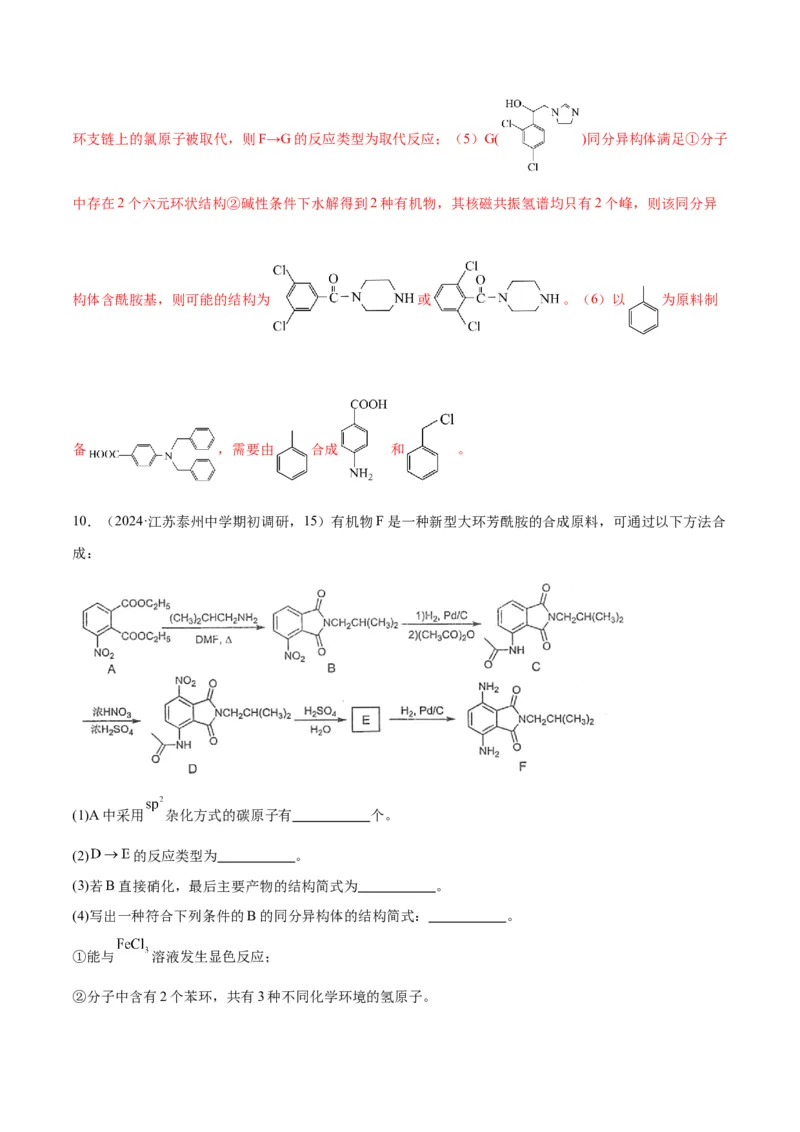
10.(2024·江苏泰州中学期初调研,15)有机物F是一种新型大环芳酰胺的合成原料,可通过以下方法合
成:
(1)A中采用 杂化方式的碳原子有 个。
(2) 的反应类型为 。
(3)若B直接硝化,最后主要产物的结构简式为 。
(4)写出一种符合下列条件的B的同分异构体的结构简式: 。
①能与 溶液发生显色反应;
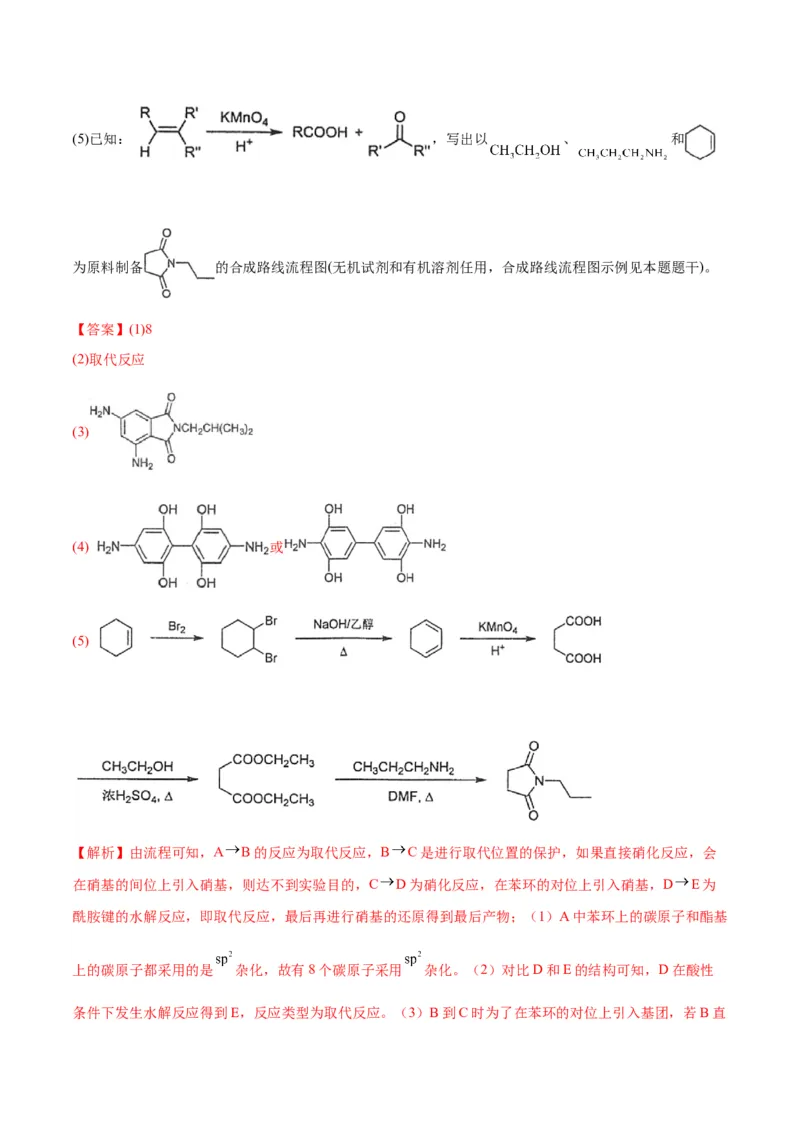
②分子中含有2个苯环,共有3种不同化学环境的氢原子。(5)已知: ,写出以 、 和
为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
【答案】(1)8
(2)取代反应
(3)
(4) 或
(5)
【解析】由流程可知,A B的反应为取代反应,B C是进行取代位置的保护,如果直接硝化反应,会
在硝基的间位上引入硝基,则达不到实验目的,C D为硝化反应,在苯环的对位上引入硝基,D E为
酰胺键的水解反应,即取代反应,最后再进行硝基的还原得到最后产物;(1)A中苯环上的碳原子和酯基
上的碳原子都采用的是 杂化,故有8个碳原子采用 杂化。(2)对比D和E的结构可知,D在酸性
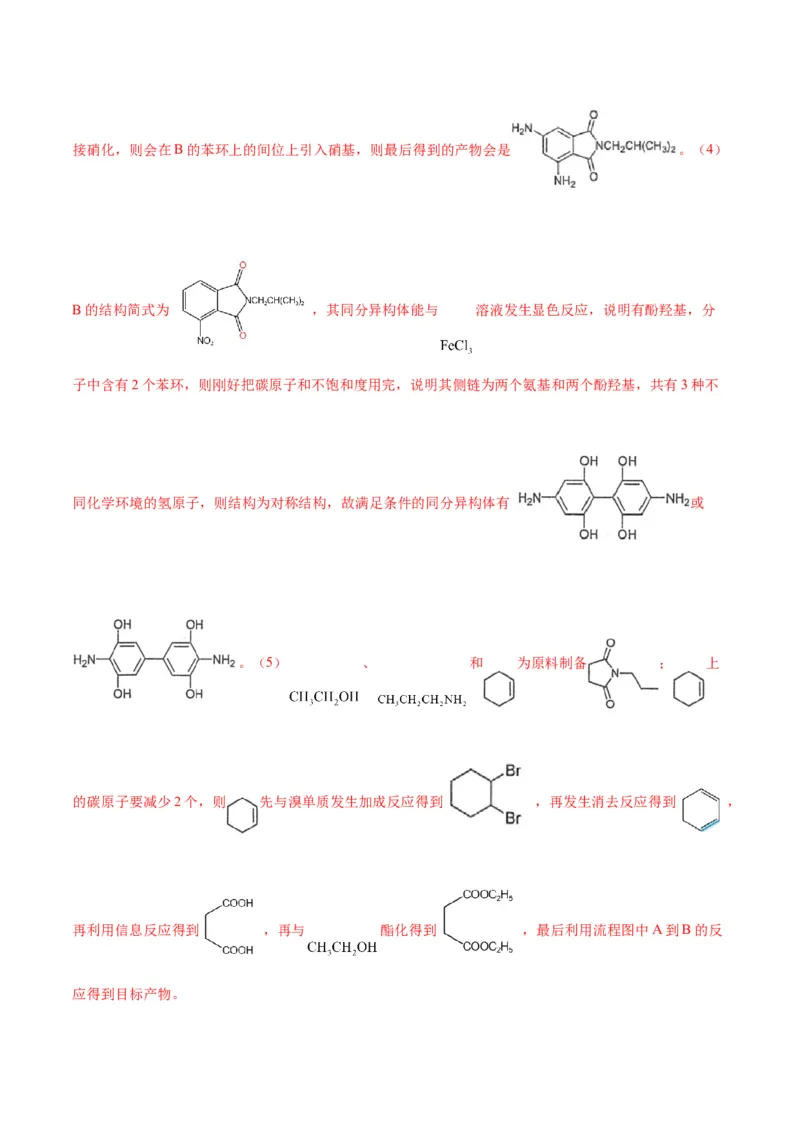
条件下发生水解反应得到E,反应类型为取代反应。(3)B到C时为了在苯环的对位上引入基团,若B直接硝化,则会在B的苯环上的间位上引入硝基,则最后得到的产物会是 。(4)
B的结构简式为 ,其同分异构体能与 溶液发生显色反应,说明有酚羟基,分
子中含有2个苯环,则刚好把碳原子和不饱和度用完,说明其侧链为两个氨基和两个酚羟基,共有3种不
同化学环境的氢原子,则结构为对称结构,故满足条件的同分异构体有 或
。(5) 、 和 为原料制备 ; 上
的碳原子要减少2个,则 先与溴单质发生加成反应得到 ,再发生消去反应得到 ,
再利用信息反应得到 ,再与 酯化得到 ,最后利用流程图中A到B的反
应得到目标产物。