文档内容
收官测试押题卷1(15+4)
(考试时间:75分钟 试卷满分:100分)
可能用到的相对分子质量:H 1 C 12 O 16 Cl 35.5 Fe 56
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.科学、安全、有效、合理地使用化学品是每一位生产者和消费者的要求和责任,下列有关说法错误的
是
A.聚四氟乙烯可作化工反应器的内壁涂层,该材料属于合成高分子材料
B.铁强化酱油中的添加剂乙二胺四乙酸铁钠属于增味剂
C.非处方药有“OTC”标识,消费者无需凭医生处方,即可购买和使用
D.硝酸铵是一种高效氮肥,但受热或撞击易爆炸,故必须作改性处理后才能施用
【答案】B
【解析】A.聚四氟乙烯可作化工反应器的内壁涂层,该材料属于合成高分子材料,A正确;B.补铁酱
油在酱油中加入一种新型铁强化剂乙二胺四乙酸铁钠,使普通酱油在添加了这种铁强化剂之后具有补充铁
元素的功效,属于营养强化剂,B错误;C.包装上有“OTC”标识是非处方药,无需凭医生处方购买和使
用,C正确;D.硝酸铵是一种高效氮肥,性质不稳定,受热遇到撞击容易分解,故必须作改性处理后才
能施用,D正确;故选B。
2.实验室可用反应 制取少量 。下列说法正确的是
A. 的空间填充模型为 B. 的空间结构为V形
C. 的结构示意图为 D. 的电子式为
【答案】B
【解析】A. 是 的球棍模型,A错误;B. 的价层电子对数为3,有1对孤电子对,
中的空间构型为V形,B正确;C. 的核电荷数为17,不是18,C错误;D. 的电子式为:
,D错误;故选B。
3.硫代硫酸钠( )在酸性环境中易发生歧化反应: 。
设 为阿伏加德罗常数的值,下列说法正确的是
A.18g 中含有质子的数目为
B.每生成32g S,转移电子的数目为
C.1mol 固体中含有离子的数目为
D.常温常压下,22.4L 中含有 键的数目为
【答案】C
【解析】A.18g 是1mol,含有质子的数目为 ,A错误;B.每生成32g S,即有1mol的硫元素从平均价态+2价降到0价,所以转移电子的数目为 ,B错误;C.1mol 固体中含有2mol钠
离子,1mol ,含有离子的数目为 ,C正确;D.常温常压下,气体摩尔体积不是22.4L/mol,所
以22.4L 不是1mol,则含有 键的数目不是 ,D错误;故选C。
4.下列有关电极方程式或离子方程式错误的是
A.向次氯酸钙溶液中通入足量二氧化碳:
B.铅酸蓄电池充电时,阳极发生反应:
C.将 溶液滴入 溶液中:
D.锌锰碱性干电池的负极反应:
【答案】B
【解析】A.向次氯酸钙溶液中通入足量二氧化碳生成碳酸氢钙和次氯酸:
,A正确;B.铅酸蓄电池充电时,阳极发生氧化反应,硫酸铅不能拆成
离子形式: ,B错误;C.将 溶液滴入 溶液中产生蓝
色沉淀: ,C正确;D.锌锰碱性干电池的负极为锌失去电子发
生氧化反应: ,D正确;故选B。
5.下列有关仪器的名称、示意图与用途或使用操作的叙述均正确的是
选项 A B C D
名称 坩埚 蒸馏烧瓶 分液漏斗 球形干燥管
示意图
用途或
可用于对固体 可用于制 分液时将磨口瓶塞上的凹槽 洗气除杂实验中将
使用操
进行高温加热 备蒸馏水 对准漏斗口颈上的小孔 气体从小口通入
作
【答案】C
【解析】A. 该仪器为蒸发皿,不是坩埚,故A错误;B. 该仪器为圆底烧瓶,不是蒸馏烧瓶,蒸馏烧瓶带
支管,故B错误;C. 该仪器为分液漏斗,分液时将磨口瓶塞上的凹槽对准漏斗口颈上的小孔,故C正
确;D. 该仪器为球形干燥管,洗气除杂实验中将气体从大口通入,故D错误;选C。
6.某液晶分子结构如图所示,X、Y、Z、W为原子序数依次增大的短周期非金属元素,基态X原子的电
子只有一种自旋取向,基态W原子核外s能级上的电子总数与p能级上的电子总数相等,Y与W的质子
数之和等于Z的质子数的2倍。下列说法错误的是A.电负性:W>Z>Y B.第一电离能:Z>W>Y
C.常见单质分子键能:X>W>Z D.简单氢化物沸点:W>Z>Y
【答案】C
【分析】基态X原子的电子只有一种自旋取向,则X为H元素;基态W原子核外s能级上的电子总数与
p能级上的电子总数相等,电子排布为1s22s22p4 或1s22s22p63s2 ,则W为O或Mg元素,由于W是非金属
元素,故W是O元素;Y与W的质子数之和等于Z的质子数的2倍,Y、Z、W为原子序数依次增大的
非金属元素,则Y为C元素,Z为N元素。据此作答。
【解析】A.同周期元素从左向右电负性依次增大,故O>N>C,A正确;B.同周期元素从左向右第一电
离能呈增大趋势,其中N原子的2p电子半满为较稳定结构,第一电离能大于相邻元素的第一电离能,则
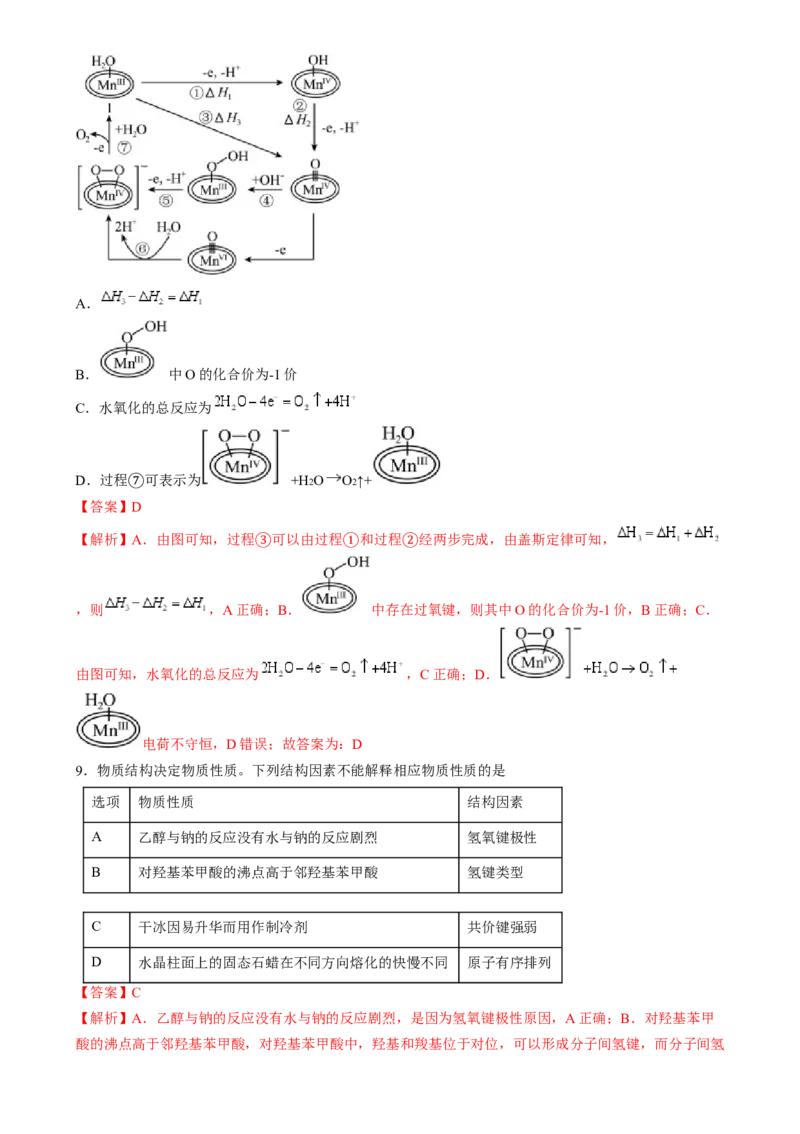
第一电离能大小顺序为:N>O>C,B正确;C .X、W、Z的单质分子分别为H2 、N2 、O2 ,对应的化学
键分别是单键、三键、双键,故键能大小关系为H2Ksp(AgSCN)=2×10-12 ,硝基苯的作用为防止AgCl转化为AgSCN,B正确;C.取消步骤Ⅲ,
则AgCl转化为AgSCN,所需NH4SCN体积V偏大,可知Cl%偏小,C错误;D.Ag+ 总物质的量为
0.1000mol·L-1×50.00mL=5.0×10-3mol,NH4SCN的物质的量为cmol·L-1×VmL=cV×10-3mol,设三氯氧磷
(POCl3)样品中Cl元素的物质的量为x,结合关系式POCl3~3Cl-~3AgNO3~3Ag+ 、Ag+~NH4SCN可知有x+
cV×10-3=5.0×10-3mol,解得x=(5.0-cV)×10-3mol,因此三氯氧磷(POCl3)样品中Cl元素的质量为(5.0-cV)×10-
3mol×35.5g/mol=3.55(5.0-cV) ×10-2g,因此Cl元素的质量分数为 ,D错误;故选B。
11.锌-空气电池被认为是替代锂离子电池、满足电动汽车爆炸性需求的下一代候选电池。用光照充电的
锌-空气电池的工作原理如图所示。光照时,光电极 (空穴),驱动阴极和阳极反应。下列叙述
不正确的是
A.放电时, 向光电极迁移 B.充电时的阳极反应为C.放电时,光电子经电解液向 极移动 D. 是配离子,配位数是4
【答案】C
【分析】光照充电时 转化为 ,故充电时 为阴极,光电极为阳极;放电时 为负极,光
电极为正极;总反应为 。
【解析】A.放电时,阳离子向正极(光电极)迁移, 项正确;B.充电时, 失去的电子填入正电
空穴, 项正确;C.光电子只能在外电路中通过, 项错误;D.从 结构可以看出其配位数
是4,D项正确;故选C。
12.葡萄糖水溶液中,存在链状和环状结构间的平衡。常温下,各种葡萄糖结构及其所占百分含量如下图
所示。已知各种葡萄糖结构中链状结构的熵最大,下列说法不正确的是
A.葡萄糖由链状转化为环状结构发生了加成反应
B. 吡喃葡萄糖的稳定性大于 吡喃葡萄糖
C.葡萄糖链状和环状结构中均有4个手性碳原子
D.葡萄糖由链状转化为环状结构 ,
【答案】C
【解析】A.葡萄糖由链状转化为环状结构,—CHO与—OH加成,A正确;B.因为α−D−吡喃葡萄糖的
羟基离环面更近,使得羟基与环面形成了较强的氢键作用,从而增加了分子的 稳定性,B正确;C.葡
萄糖链状结构中有4个手性碳原子,环状结构中有5个手性碳原子,C错误;D.葡萄糖结构中链状结构
的熵最大,葡萄糖由链状转化为环状结构ΔS<0,ΔH<0,D正确;故选C。
13.实验室可以通过以下反应和操作制取肉桂酸:
已知:苯甲醛、肉桂酸均难溶于水,苯甲醛的熔点-26 ,肉桂酸的熔点133 ,乙酸酐(CH3CO)2O易水
解。
℃ ℃
操作:
将5.3g苯甲醛(M=106g/mol)、6.12g乙酸酐(M=102g/mol)、K2CO3 混合加热回流0.5h
①
向回流后的混合液中加入K2CO3 溶液调节溶液至碱性
将“ ”中溶液装入下图的Ⅱ装置中,并通入水蒸气,Ⅲ中收集到苯甲醛和水
②
③ ②……,得到纯净的肉桂酸(M=148g/mol)6.2g。
④
下列有关说法错误的是
A.当馏出液无油珠时,即可停止通入水蒸气
B.操作 结束时,应先打开弹簧夹再移去热源
C.向Ⅱ中残余溶液中加入盐酸酸化,再过滤、洗涤、干燥可以获得肉桂酸粗品
③
D.肉桂酸的产率为69.8%
【答案】D
【分析】将一定量苯甲醛、乙酸酐、K2CO3 在圆底烧瓶中混合均匀,然后加热回流0.5h;向回流后的混合
液中加入K2CO3 溶液调节溶液至碱性,将肉桂酸、乙酸、乙酸酐等转化为盐;通入水蒸气进行蒸馏,收
集苯甲醛;将蒸馏后剩余溶液中加入酸,重新生成肉桂酸等,肉桂酸难溶于水,过滤后洗涤、干燥,便可
获得肉桂酸。
【解析】A.苯甲醛难溶于水,当馏出液无油珠时,表明苯甲醛已全部蒸出,此时可停止通入水蒸气,A
正确;B.操作 结束时,为防止发生倒吸,应先打开弹簧夹使系统与大气相通,再移去热源,B正确;
C.向Ⅱ中残余
③
溶液中加入盐酸酸化,使肉桂酸钾转化为肉桂酸,肉桂酸难溶于水,生成沉淀,再过滤、
洗
涤、干燥可以获得肉桂酸粗品,C正确;D.5.3g苯甲醛的物质的量为0.05mol,6.12g乙酸酐的物质的量
为0.06mol,理论上生成肉桂酸的物质的量为0.05mol,质量为0.05mol×148g/mol=7.4g,则肉桂酸的产率
为 ≈83.8%,D错误;故选D。
14. 是某些太阳能薄膜电池的材料。下图所示为 的晶胞结构,已知晶胞参数为apm,2号
氧原子的分数坐标为 ,下列说法不正确的是
A.1号氧原子的分数坐标为
B.晶胞中与Ca等距离且最近的O有4个
C.元素 在元素周期表中处于d区D.Ti和Ca原子间的最短距离为
【答案】B
【解析】A.根据空间直角坐标系以及2号氧原子的分数坐标,可以得到1号氧原子的分数坐标为
,故A正确;B.以顶点的钙原子分析,该晶胞中与Cu等距离且最近的O有12个,故B错误;
C.钛元素位于元素周期表中第四周期ⅡB族,其价电子排布式为3d24s2 ,最后一个电子填充在d轨道,
属于元素周期表中d区元素,故C正确;D.根据晶胞结构可知,钙原子和钛原子之间的距离为体对角线
的一半即 ,故D正确;故答案选B;
15.某温度下, 与不同pH的 体系反应可生成不同的沉淀。下面图1表示 体系中各
含碳粒子的物质的量分数与pH的关系。图2表示 与不同pH的 体系反应生成沉淀的情况,
其中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 molL ,不同pH下 由图1得到]。
⋅
下列说法正确的是
A.上述 体系呈中性时, 一定是
B.符合 的pH范围:
C. , molL 时,溶液中存在 和 两种沉淀
⋅
D. , molL 时可发生反应:
【答案】D
⋅
【分析】图1中pH越大,碳酸根物质的量分数越大,碳酸物质的量分数越小,碳酸氢根物质的量分数先
增大后减小;图2中已知曲线Ⅰ代表的是氢氧化镁,曲线Ⅱ代表的是碳酸镁。。
【解析】A.温度不一定是常温,因此中性体系pH不一定是7, 也就不确定,A错误;B.由图1可知, , , 。若 ,则满足下
列两个关系: , 。将 代入 表达式,可得 ,即
① ② ①
;将 代入 表达式,可得 ,即 。因此,符合条件的pH范围是
②,B错误;C.分析图2, , 浓度为0.01 mol/L时,溶液中只存在 沉
淀,C错误;D.分析图1和图2, 时,溶液中主要含碳离子为 , 浓度为0.1 mol/L时,
只产生 沉淀,因此可以发生 ,D正确;故选D。
二、非选择题:本题共4小题,共55分。
16.(13分)铁铬废泥是FeCl3 蚀刻废液经还原、碱沉淀后产生的固体废泥(铁质量分数约为15%,铬质
量分数约为2%,不溶物含量为5%~10%,含水率为40%~50%),可用酸洗废液(所含酸主要是盐酸)酸溶
后,再经过下列方式处理获得FeCl3 和PbCrO4 两种产品,变废为宝。
Ⅰ.部分含铬微粒的颜色状态如下表所示:
物质 Cr(OH)3 PbCrO4
颜色状态 绿色沉淀 绿色溶液 黄色溶液 橙色溶液 黄色沉淀
Ⅱ.几种金属离子开始沉淀和完全沉淀的pH如表所示:
金属离子 Fe3+ Fe2+ Cr3+
开始沉淀的
2.3 7.6 4.5
pH
完全沉淀的
3.3 9.1 5.6
pH
回答下列问题:
(1)基态Cr原子的价层电子排布式为 。
(2)铁铬废泥中铁元素和铬元素的存在形式是 (填化学式)。
(3)用酸洗废液酸溶时,反应温度为65 ,此时铁铬废泥的浸出效果较佳。但实际生产中,只需要将溶
液预热到60 左右即可,原因是 。
℃
(4)加入C
℃
a(OH)2 时,应调节的pH范围为 。
(5)试剂A的最佳选择是 (填字母)。a.酸性KMnO4 溶液 b.HNO3 c.Cl2
(6)绿色溶液转化为黄色溶液过程的离子方程式是 。
(7)FeCl3 的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,再转移到100mL容量
瓶;用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液;充分反应后,滴入淀粉指示剂并用
cmol·L-1Na2S2O3 溶液滴定用去VmL。样品中氯化铁的质量分数为 (用字母m、c、V来表示)。已
知:I2+2 =2I-+ 。
【答案】(1)3d54s1 (1分)
(2)Fe(OH)3 、Cr(OH)3 (2分)
(3)Fe(OH)3 、Cr(OH)3 与盐酸反应会放出一定的热量(2分)
(4)5.6 pH<7.6(2分)
(5)c(2分)
(6) +2H2O2+Pb+=PbCrO4↓+2H2O(2分)
(7) (2分)
【分析】铁铬废泥是FeCl3 蚀刻废液经还原、碱沉淀后产生的固体废泥(铁质量分数约为15%,铬质量分数
约为2%,不溶物含量为5%~10%,含水率为40%~50%),可用酸洗废液(所含酸主要是盐酸)酸溶后,滤渣
为不溶物,滤液1中含有Fe3+ 与Cr3+ ,加入铁片后Fe3+ 还原为Fe2+ ,加入Ca(OH)2 ,应调节pH在5.6 pH
<7.6,Gr3+ 既完全沉淀,Fe2+ 也不会产生沉淀,滤液3中Fe2+ 经过氯气氧化得到FeCl3 ;高铬滤渣为
Cr(OH)3 ,与氢氧化钠反应生成NaCrO2 , 氧化为 , 的溶液中加酸,溶液变为橙黄色,说
明单聚的 转化为二聚的 , 与醋酸铅反应生成PbCrO4 ,据此分析解题。
【解析】(1)Cr为第24号元素, 基态Cr原子的价层电子排布式为3d54s1 。
(2)铁铬废泥是FeCl3 蚀刻废液经还原、碱沉淀后产生的固体废泥,铁铬废泥中铁元素和铬元素的存在
形式是Fe(OH)3 、Cr(OH)3 。
(3)Fe(OH)3 、Cr(OH)3 与盐酸反应会放出一定的热量,故实际生产中,只需要将溶液预热到60 左右即
可。
℃
(4)加入Ca(OH)2 时,应调节的pH的范围在5.6 pH<7.6,Gr3+ 既完全沉淀,Fe2+ 也不会产生沉淀。
(5)试剂A的最佳选择是Cl2 ,因为最后的目标产物为FeCl3 ,既可以达到将Fe2+ 氧化为Fe3+ 的目的,也
不引入新的杂质离子,故选c。
(6)绿色溶液转化为黄色溶液过程的离子方程式是: +2H2O2+Pb+=PbCrO4↓+2H2O。
(7)I2+2 =2I-+ ,2Fe3++2I-=2Fe2++I2 ,可知关系式2Fe3+- I2-2 ,cmol·L-1Na2S2O3 溶液滴定用
去VmL,所需物质的量为cV×10-3mol,消耗Fe3+ 的物质的量为cV×10-3mol,从100mL容量瓶取出
10.00mL样品,样品中氯化铁的质量分数为 。
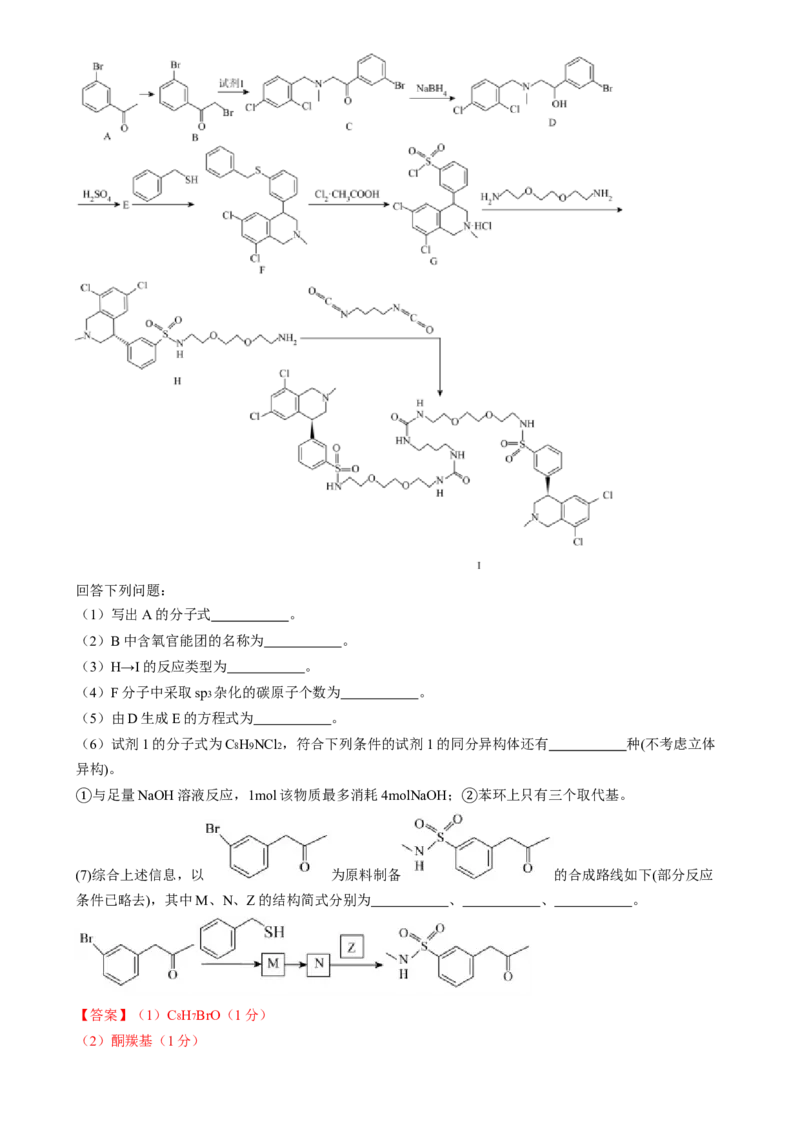
17.(14分)替纳帕诺片可用于控制正在接受血液透析治疗的慢性肾脏病(CKD)成人患者的高磷血症。替
纳帕诺片的有效成分I的合成路线如下:回答下列问题:
(1)写出A的分子式 。
(2)B中含氧官能团的名称为 。
(3)H→I的反应类型为 。
(4)F分子中采取sp3 杂化的碳原子个数为 。
(5)由D生成E的方程式为 。
(6)试剂1的分子式为C8H9NCl2 ,符合下列条件的试剂1的同分异构体还有 种(不考虑立体
异构)。
与足量NaOH溶液反应,1mol该物质最多消耗4molNaOH; 苯环上只有三个取代基。
① ②
(7)综合上述信息,以 为原料制备 的合成路线如下(部分反应
条件已略去),其中M、N、Z的结构简式分别为 、 、 。
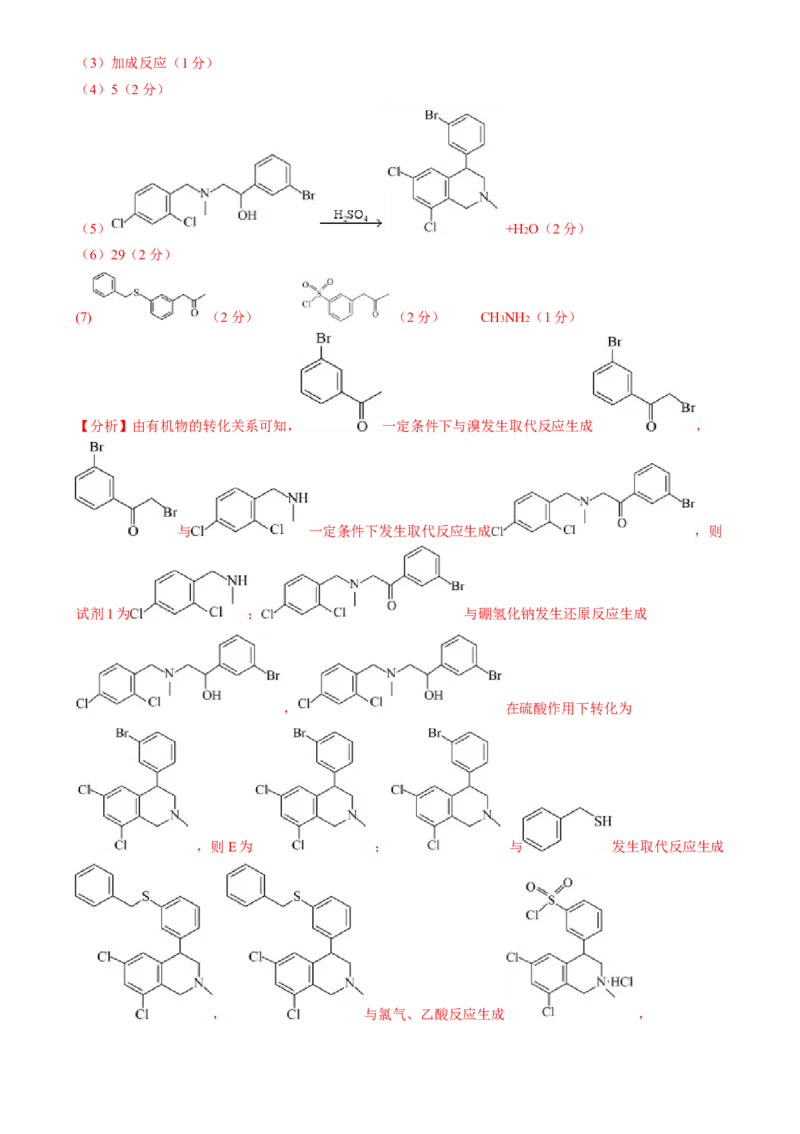
【答案】(1)C8H7BrO(1分)
(2)酮羰基(1分)(3)加成反应(1分)
(4)5(2分)
(5) +H2O(2分)
(6)29(2分)
(7) (2分) (2分) CH3NH2 (1分)
【分析】由有机物的转化关系可知, 一定条件下与溴发生取代反应生成 ,
与 一定条件下发生取代反应生成 ,则
试剂1为 ; 与硼氢化钠发生还原反应生成
, 在硫酸作用下转化为
,则E为 ; 与 发生取代反应生成
, 与氯气、乙酸反应生成 ,与 发生取代反应生成
, 与
发生加成反应生成
。
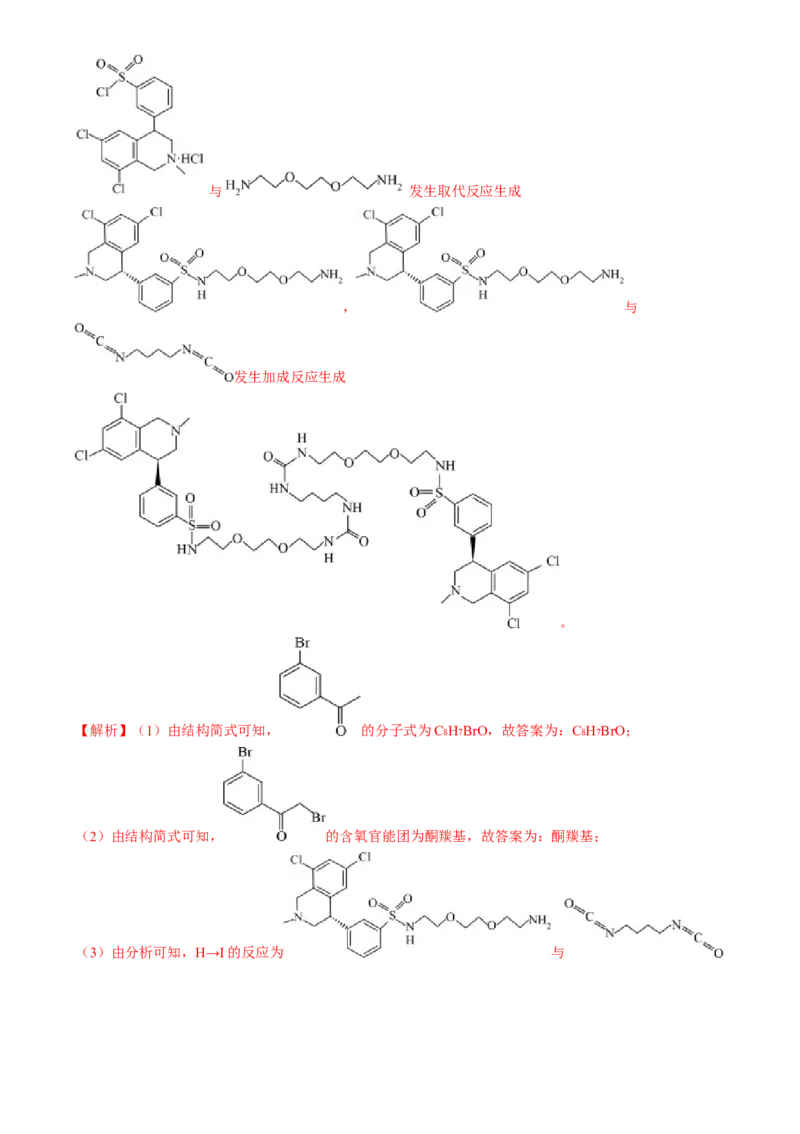
【解析】(1)由结构简式可知, 的分子式为C8H7BrO,故答案为:C8H7BrO;
(2)由结构简式可知, 的含氧官能团为酮羰基,故答案为:酮羰基;
(3)由分析可知,H→I的反应为 与发生加成反应生成 ,故答案为:加成反应;
(4)由结构简式可知, 分子中含有5个杂化方式为sp3 杂化的饱和碳原子,故答案为:5;
(5)由分析可知,由D生成E的反应为 在硫酸作用下转化为 和
水,反应的化学方程式为 +H2O,故答案为:
+H2O;
(6) 的同分异构体与足量氢氧化钠溶液反应,1 mol试剂1最多消耗4 mol氢氧化钠说
明2个氯原子原子直接与苯环相连,苯环上只有三个取代基说明同分异构体分子的结构可以视作邻二氯
苯、间二氯苯、对二氯苯分子中苯环上的氢原子被—CH2CH2NH2 、或 、或—NH—CH2CH3 ,或
—CH2—NH—CH3 、或—N(CH3)2 取代所得结构,其中邻二氯苯、间二氯苯、对二氯苯分子中苯环上的氢
原子被取代基取代所得结构分别有2种、3种、1种,则符合条件的结构简式共有5×6—1=29种,故答案
为:29;
(7)由有机物的转化关系可知, 与 发生取代反应生成 ,则M为
; 与氯气、乙酸反应生成 ,则N为
; 与CH3NH2 发生取代反应生成 ,故答案为:; ;CH3NH2 。
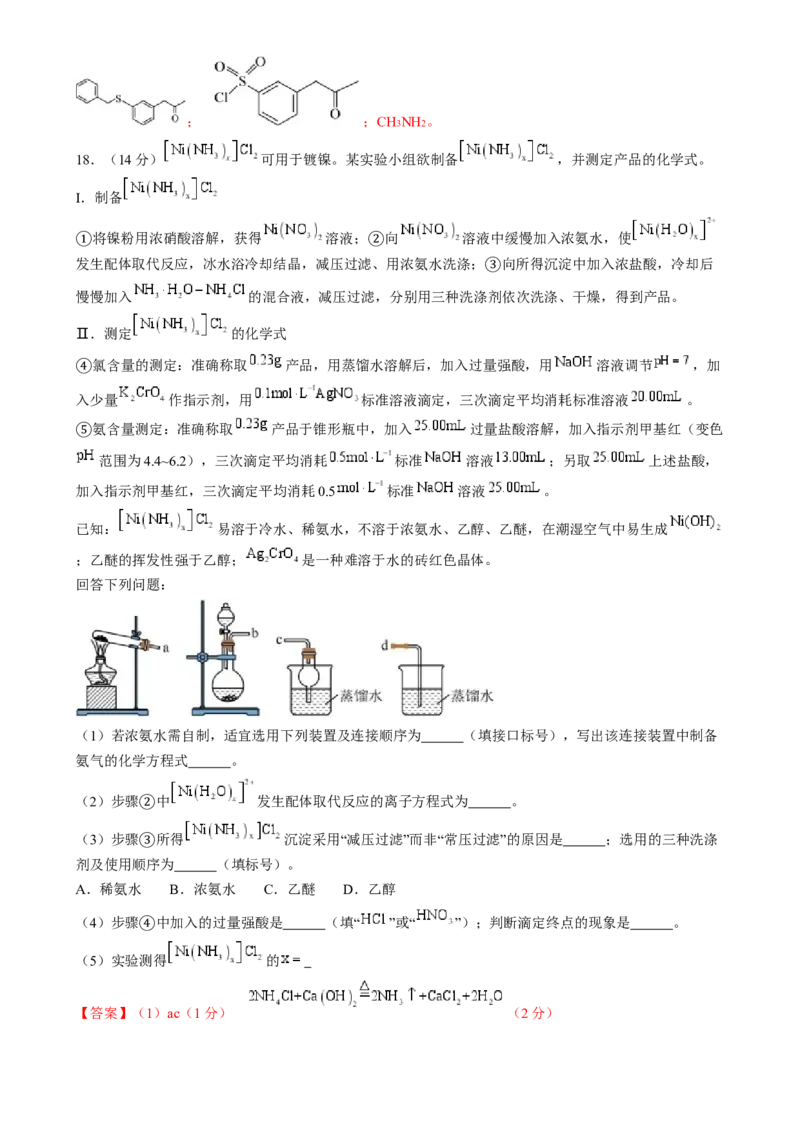
18.(14分) 可用于镀镍。某实验小组欲制备 ,并测定产品的化学式。
I.制备
将镍粉用浓硝酸溶解,获得 溶液; 向 溶液中缓慢加入浓氨水,使
发生配体取代反应,冰水浴冷却结晶,减压过滤、用浓氨水洗涤; 向所得沉淀中加入浓盐酸,冷却后
① ②
慢慢加入 的混合液,减压过滤,分别用三种洗涤③剂依次洗涤、干燥,得到产品。
Ⅱ.测定 的化学式
氯含量的测定:准确称取 产品,用蒸馏水溶解后,加入过量强酸,用 溶液调节 ,加
④入少量 作指示剂,用 标准溶液滴定,三次滴定平均消耗标准溶液 。
氨含量测定:准确称取 产品于锥形瓶中,加入 过量盐酸溶解,加入指示剂甲基红(变色
⑤ 范围为4.4~6.2),三次滴定平均消耗 标准 溶液 ;另取 上述盐酸,
加入指示剂甲基红,三次滴定平均消耗0.5 标准 溶液 。
已知: 易溶于冷水、稀氨水,不溶于浓氨水、乙醇、乙醚,在潮湿空气中易生成
;乙醚的挥发性强于乙醇; 是一种难溶于水的砖红色晶体。
回答下列问题:
(1)若浓氨水需自制,适宜选用下列装置及连接顺序为 (填接口标号),写出该连接装置中制备
氨气的化学方程式 。
(2)步骤 中 发生配体取代反应的离子方程式为 。
②
(3)步骤 所得 沉淀采用“减压过滤”而非“常压过滤”的原因是 ;选用的三种洗涤
剂及使用顺序为 (填标号)。
③
A.稀氨水 B.浓氨水 C.乙醚 D.乙醇
(4)步骤 中加入的过量强酸是 (填“ ”或“ ”);判断滴定终点的现象是 。
④
(5)实验测得 的
【答案】(1)ac(1分) (2分)(2) (2分)
(3)利于盐酸、氨水挥发得到较为纯净的产品(2分) BDC(2分)
(4) (1分) 最后半滴标准液加入后,产生砖红色沉淀且半分钟内沉淀不溶解(2分)
(5)6(2分)
【分析】镍粉用浓硝酸溶解,获得 溶液;向 溶液中缓慢加入浓氨水,使
发生配体取代反应生成 ,冰水浴冷却结晶,减压过滤、用浓氨水洗涤;向所
得沉淀中加入浓盐酸,冷却后加入 的混合液,减压过滤,洗涤、干燥,得到产品;
【解析】(1)氯化铵和氢氧化钙加热生成氯化钙、水和氨气,
,反应为固体加热反应且生成氨气极易溶于水,需要使用防倒
吸装置,故浓氨水自制,适宜选用下列装置及连接顺序为ac;
(2) 溶液中缓慢加入浓氨水,使 发生配体取代反应生成 ,反应为
;
(3)浓盐酸、氨水均具有挥发性,使用采用“减压过滤”而非“常压过滤”可以利于盐酸、氨水挥发得到较
为纯净的产品;已知: 易溶于冷水、稀氨水,不溶于浓氨水、乙醇、乙醚,在潮湿空气中
易生成 ,乙醚的挥发性强于乙醇,则洗涤过程中不能使用稀氨水,且应该逐步使用挥发性的物
质,更利
于得到干燥的 ,故答案为:BDC;
(4)加入盐酸会引入氯离子,和银离子生成氯化银沉淀,则步骤 中加入的过量强酸是HCl;
是一种难溶于水的砖红色晶体,则判断滴定终点的现象是:最后半滴标准液加入后,产生砖红色沉淀且半
④
分钟内沉淀不溶解;
(5)由题干可知, 产品中氯的物质的量为 , 产品中 的物质
的量为 ,则x:2=0.006:0.002,则 的
x=6。
19.(14分)对氮氧化物 的资源化利用,运用多种方式促进氮的循环转化,具有重要的研究意义。
(1)已知a:
b:C的燃烧热为 ;c:
请写出 与 反应生成两种无污染性气体的热化学方程式: 。
①将等物质的量的 与 混合气体分别通入体积均为 的恒温密闭容器Ⅰ和绝热密闭容器Ⅱ中,反
应一段时间后两容器内达到平衡状态,下列说法正确的是 。
②
A.两容器内混合气体密度相等
B. 转化率C.反应平衡常数
(2)可利用钴氨配合物吸收 对 的配合能力很强,而 对 的配合能
力极低。
已知 的结构如图所示 , 中含有 键的数目
是 。
①
有氧和无氧条件下, 溶液脱除 的效率如图1所示,有氧环境下,发生总反应:
②
,在 的有氧环境下,往
溶液中持续通入试样气体 脱除率为60%(假设溶液体积不发生改变),结
合图1信息,计算此时钴氨溶液中 有效含钴率为 。
(有效含钴率 )
钴氨溶液经过多次循环吸收 后,其吸收 的能力变化如图2所示,前 内钴氨溶液吸收 的
能力不断下降的原因是 。
③
(3)催化电解 吸收液可将 还原为 ,其催化机理如图3所示,在相同条件下,恒定通过电解
池的电量,电解得到部分还原产物的法拉第效率 随电解电压的变化如图4所示。已知
表示电解生还原产物X所转移电子的物质的量,F表示法拉第常数; 表示电解过
程中通过的总电量。当电解电压为 时,催化电解 生成 的电极反应式为 。
①当电解电压为 时,电解生成的 和 的物质的量之比为 。
②
【答案】(1) 2NO(g)+ 2CO(g)=N2(g)+2CO2(g) H=—748kJ/mol(2分) AC(2分)
(2) 24NA ( ① 2分) 85.6%(2分) [ △ Co(NH3)6]2+ 被氧化为[Co(NH3)6] ②3+ ,[Co(NH3)6]3+ 对NO
的配位能力极低(2分)
① ② ③
(3) NO+5e—+5H+=NH3+H2O(2分) 15:2(2分)
【解析
①
】(1) 由题意可知,碳燃烧的热化学
②
方程式为C(s) +O2(g)= CO2(g) H=—393kJ/mol,由盖斯定
律可知,反应b
①
—a—c得到反应2NO(g)+ 2CO(g)=N2(g)+2CO2(g),则反应
△
H=(—393kJ/mol)—(+182.6kJ/mol)—(+172.4kJ/mol)=—748kJ/mol,故答案为:2NO(g)+ 2CO(g)=N2(g)
△
+2CO2(g) H=—748kJ/mol; A.由质量守恒定律可知,反应前后气体的质量相等,则1L的恒温密闭
容器Ⅰ和绝
△
热密闭容器Ⅱ中混
②
合气体密度相等,故正确;B.该反应为放热反应,则恒温密闭容器Ⅰ中反
应温度小于绝热密闭容器Ⅱ,升高温度,平衡向逆反应方向移动,一氧化氮的转化率减小,则一氧化氮转
化率α
Ⅰ
大于α
Ⅱ
,故错误;C.该反应为放热反应,则恒温密闭容器Ⅰ中反应温度小于绝热密闭容器Ⅱ,
升高
温度,平衡向逆反应方向移动,化学平衡常数减小,则反应平衡常数K 大于K ,故正确;故选AC;
Ⅰ Ⅱ
(2) [Co(NH3)6]3+ 离子中配位键属于σ键、氮氢键属于σ键,则1mol[Co(NH3)6]3+ 离子中含有σ键的数
目1mo
①
l×24×NAmol—1=24NA ,故答案为:24NA ; 由题给信息可知,反应消耗一氧化氮的物质的量为
2×10—4m3/min×300min×2×10—2mol/m3×60%=0.00
②
072mol,则钴氨溶液中[Co(NH3)6]2+ 有效含钴率为
×100%=85.6%,故答案为:85.6%; 由图可知,前16h内钴氨溶液吸收
NO的能力不断下降的原因是[Co(NH3)6]2+ 被氧化为[Co(NH3)6]3+ ,[
③
Co(NH3)6]3+ 对NO的配位能力极低,故
答案为:[Co(NH3)6]2+ 被氧化为[Co(NH3)6]3+ ,[Co(NH3)6]3+ 对NO的配位能力极低;
(3) 由图可知,当电解电压为U2 时,催化电解一氧化氮生成氨气的电极为阴极,酸性条件下一氧化
氮在阴
①
极得到电子发生还原反应生成氨气和水,电极反应式为NO+5e—+5H+=NH3+H2O,故答案为:
NO+5e—+5H+=NH3+H2O; 由图可知,当电解电压为U1 时,氢气和氨气的法拉第效率分别为60%和
②
20%,则电解生成的氢气和氨气的物质的量之比为 : =15:2,故答案为:15:2。