文档内容
易错专题 13 化学平衡图像和计算
聚焦易错点:
►易错点一 化学平衡图像
►易错点二 化学平衡计算
典例精讲
易错点一 化学平衡图像
【易错典例】
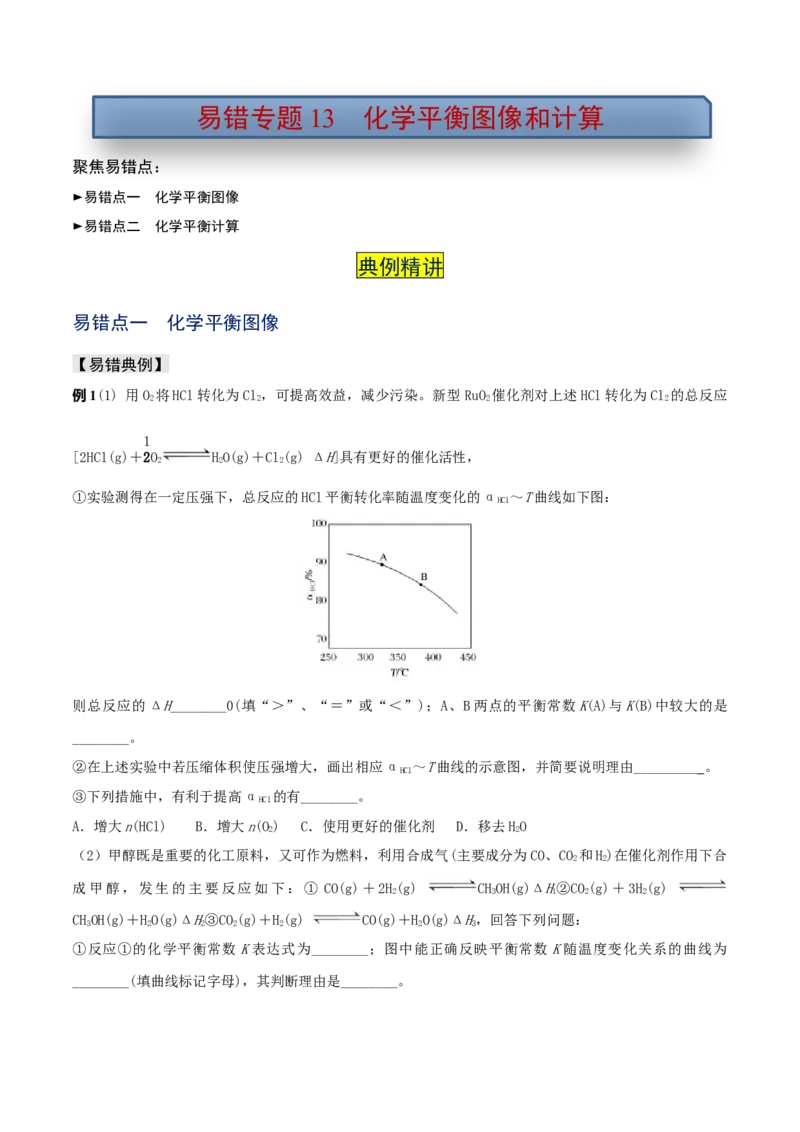
例1(1) 用O 将HCl转化为Cl ,可提高效益,减少污染。新型RuO 催化剂对上述HCl转化为Cl 的总反应
2 2 2 2
1
[2HCl(g)+2O HO(g)+Cl(g) ΔH]具有更好的催化活性,
2 2 2
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的α ~T曲线如下图:
HCl
则总反应的ΔH________0(填“>”、“=”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是
________。
②在上述实验中若压缩体积使压强增大,画出相应α ~T曲线的示意图,并简要说明理由_________ 。
HCl
③下列措施中,有利于提高α 的有________。
HCl
A.增大n(HCl) B.增大n(O) C.使用更好的催化剂 D.移去HO
2 2
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO 和H)在催化剂作用下合
2 2
成甲醇,发生的主要反应如下:① CO(g)+2H(g) CHOH(g)ΔH②CO(g)+3H(g)
2 3 1 2 2
CHOH(g)+HO(g)ΔH③CO(g)+H(g) CO(g)+HO(g)ΔH,回答下列问题:
3 2 2 2 2 2 3
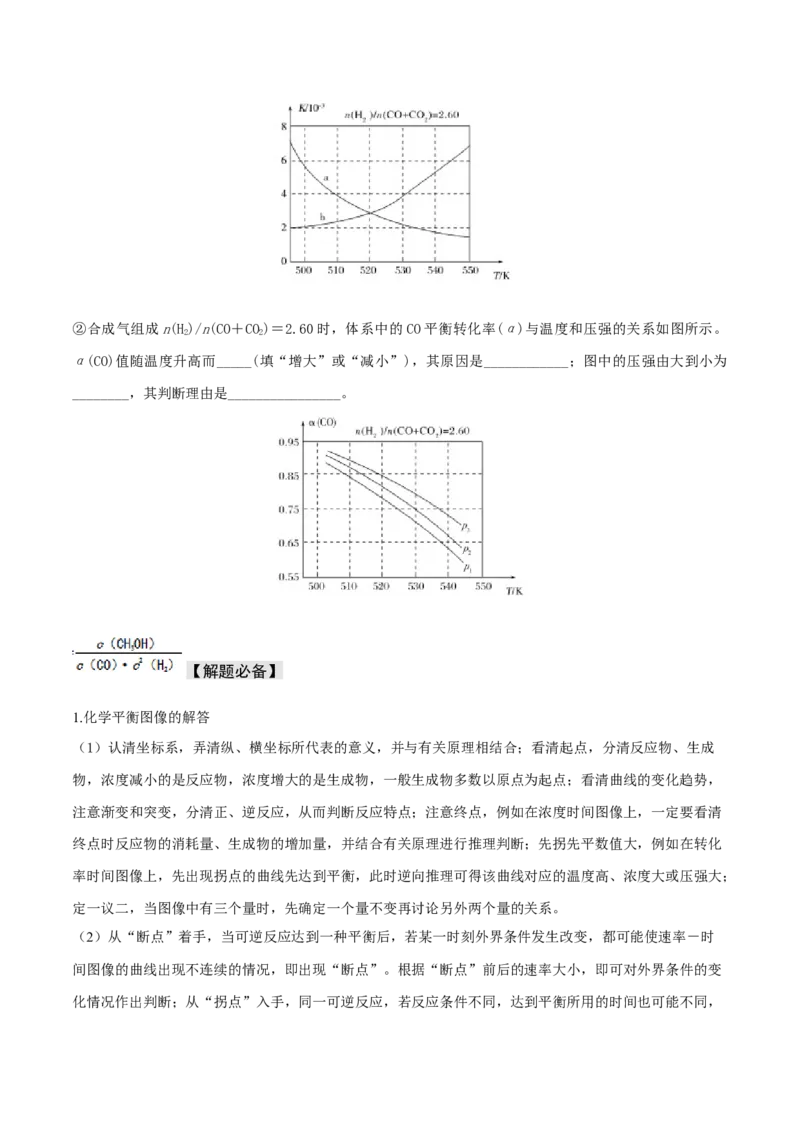
①反应①的化学平衡常数K表达式为________;图中能正确反映平衡常数K随温度变化关系的曲线为
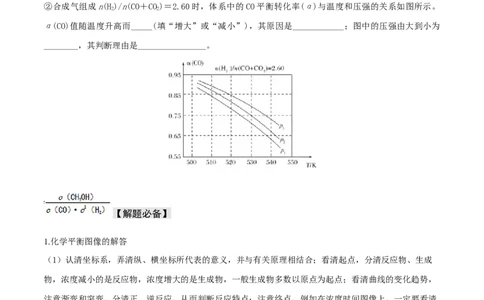
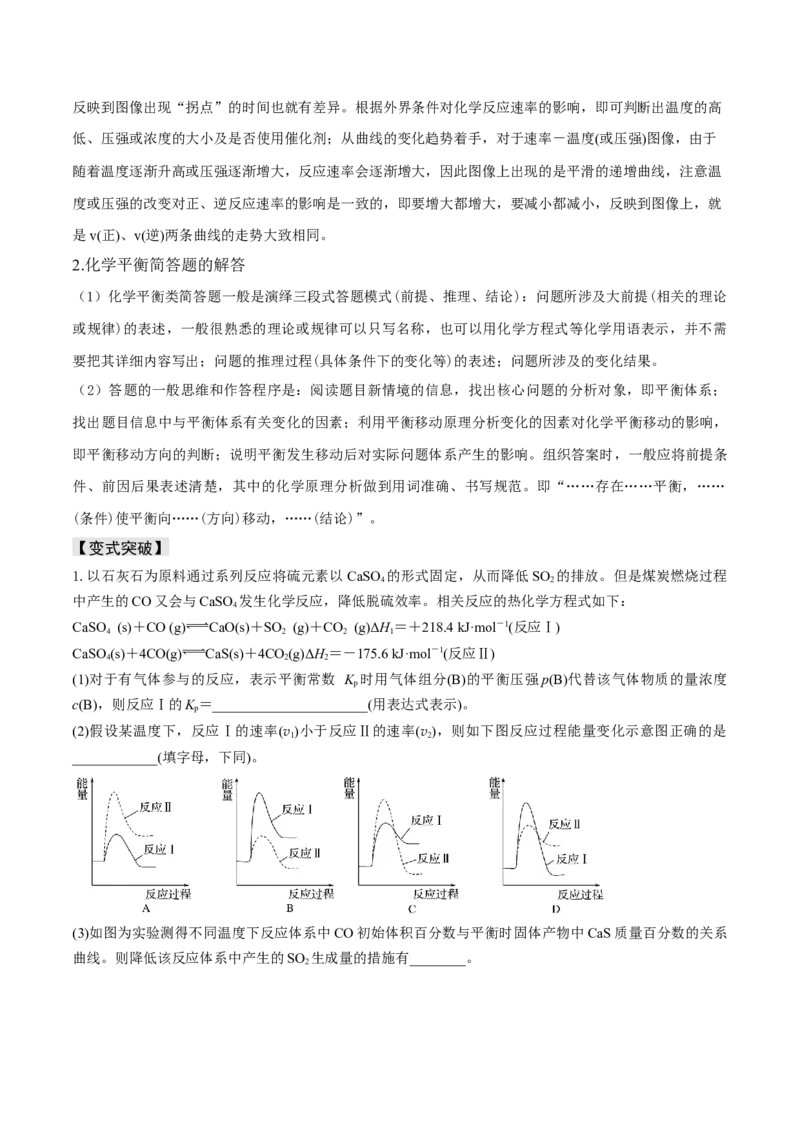
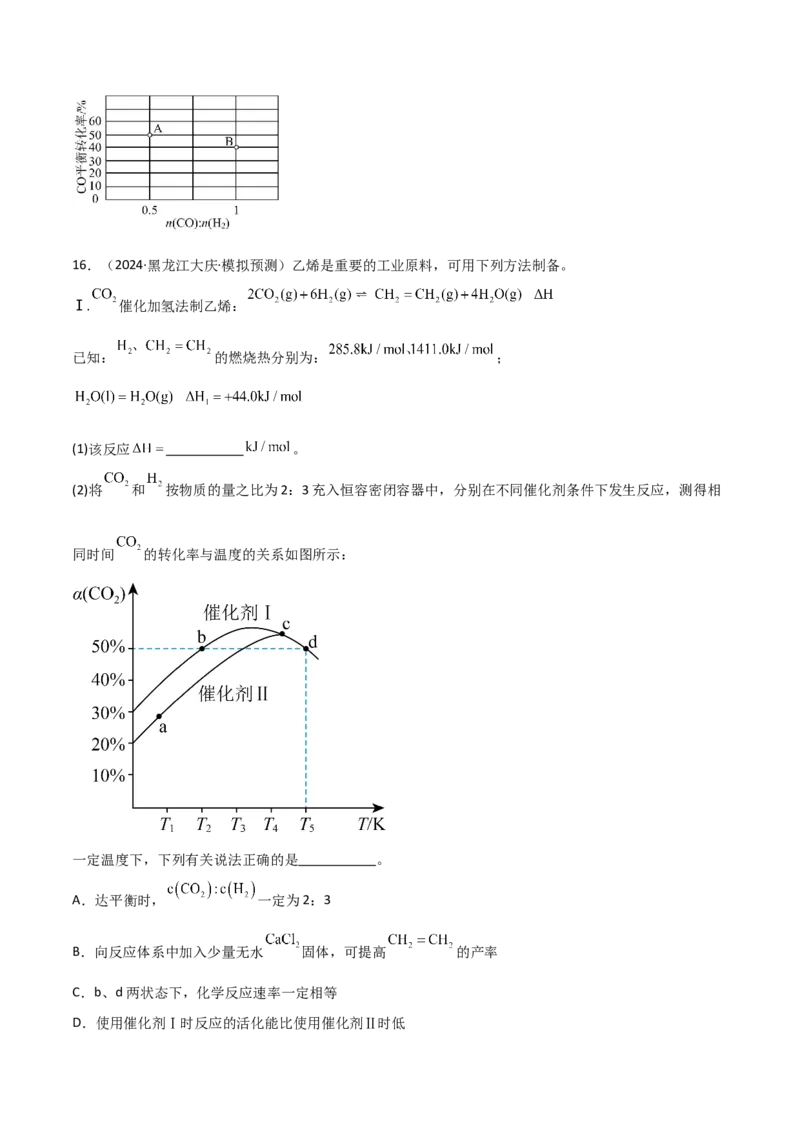
________(填曲线标记字母),其判断理由是________。②合成气组成n(H)/n(CO+CO)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图所示。
2 2
α(CO)值随温度升高而_____(填“增大”或“减小”),其原因是____________;图中的压强由大到小为
________,其判断理由是________________。
【解题必备】
1.化学平衡图像的解答
(1)认清坐标系,弄清纵、横坐标所代表的意义,并与有关原理相结合;看清起点,分清反应物、生成
物,浓度减小的是反应物,浓度增大的是生成物,一般生成物多数以原点为起点;看清曲线的变化趋势,
注意渐变和突变,分清正、逆反应,从而判断反应特点;注意终点,例如在浓度时间图像上,一定要看清
终点时反应物的消耗量、生成物的增加量,并结合有关原理进行推理判断;先拐先平数值大,例如在转化
率时间图像上,先出现拐点的曲线先达到平衡,此时逆向推理可得该曲线对应的温度高、浓度大或压强大;
定一议二,当图像中有三个量时,先确定一个量不变再讨论另外两个量的关系。
(2)从“断点”着手,当可逆反应达到一种平衡后,若某一时刻外界条件发生改变,都可能使速率-时
间图像的曲线出现不连续的情况,即出现“断点”。根据“断点”前后的速率大小,即可对外界条件的变
化情况作出判断;从“拐点”入手,同一可逆反应,若反应条件不同,达到平衡所用的时间也可能不同,反映到图像出现“拐点”的时间也就有差异。根据外界条件对化学反应速率的影响,即可判断出温度的高
低、压强或浓度的大小及是否使用催化剂;从曲线的变化趋势着手,对于速率-温度(或压强)图像,由于
随着温度逐渐升高或压强逐渐增大,反应速率会逐渐增大,因此图像上出现的是平滑的递增曲线,注意温
度或压强的改变对正、逆反应速率的影响是一致的,即要增大都增大,要减小都减小,反映到图像上,就
是v(正)、v(逆)两条曲线的走势大致相同。
2.化学平衡简答题的解答
(1)化学平衡类简答题一般是演绎三段式答题模式(前提、推理、结论):问题所涉及大前提(相关的理论
或规律)的表述,一般很熟悉的理论或规律可以只写名称,也可以用化学方程式等化学用语表示,并不需
要把其详细内容写出;问题的推理过程(具体条件下的变化等)的表述;问题所涉及的变化结果。
(2)答题的一般思维和作答程序是:阅读题目新情境的信息,找出核心问题的分析对象,即平衡体系;
找出题目信息中与平衡体系有关变化的因素;利用平衡移动原理分析变化的因素对化学平衡移动的影响,
即平衡移动方向的判断;说明平衡发生移动后对实际问题体系产生的影响。组织答案时,一般应将前提条
件、前因后果表述清楚,其中的化学原理分析做到用词准确、书写规范。即“……存在……平衡,……
(条件)使平衡向……(方向)移动,……(结论)”。
【变式突破】
1.以石灰石为原料通过系列反应将硫元素以CaSO 的形式固定,从而降低SO 的排放。但是煤炭燃烧过程
4 2
中产生的CO又会与CaSO 发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
4
CaSO (s)+CO (g) CaO(s)+SO (g)+CO (g)ΔH=+218.4 kJ·mol-1(反应Ⅰ)
4 2 2 1
CaSO(s)+4CO(g) CaS(s)+4CO(g)ΔH=-175.6 kJ·mol-1(反应Ⅱ)
4 2 2
(1)对于有气体参与的反应,表示平衡常数 K 时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度
p
c(B),则反应Ⅰ的K =______________________(用表达式表示)。
p
(2)假设某温度下,反应Ⅰ的速率(v)小于反应Ⅱ的速率(v),则如下图反应过程能量变化示意图正确的是
1 2
____________(填字母,下同)。
(3)如图为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系
曲线。则降低该反应体系中产生的SO 生成量的措施有________。
2A.向该反应体系中投入生石灰 B.在合适的温度区间内控制较低的反应温度
C.降低CO的初始体积百分数 D.提高反应体系的温度
2.①将一定量的CO(g)和CH(g)通入一恒容密闭容器中发生反应:CO(g)+CH(g) 2CO(g)+2H(g)。其他
2 4 2 4 2
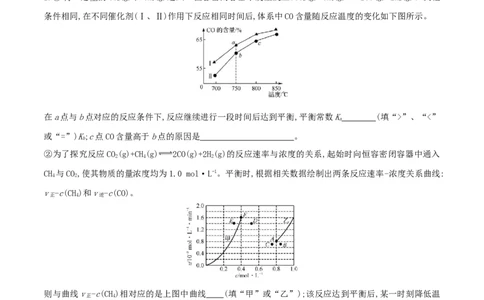
条件相同,在不同催化剂(Ⅰ、Ⅱ)作用下反应相同时间后,体系中CO含量随反应温度的变化如下图所示。
在a点与b点对应的反应条件下,反应继续进行一段时间后达到平衡,平衡常数K (填“>”、“<”
a
或“=”)K;c点CO含量高于b点的原因是 。
b
②为了探究反应CO(g)+CH(g) 2CO(g)+2H(g)的反应速率与浓度的关系,起始时向恒容密闭容器中通入
2 4 2
CH 与CO,使其物质的量浓度均为1.0 mol·L-1。平衡时,根据相关数据绘制出两条反应速率-浓度关系曲线:
4 2
v -c(CH)和v -c(CO)。
正 4 逆
则与曲线v -c(CH)相对应的是上图中曲线 (填“甲”或“乙”);该反应达到平衡后,某一时刻降低温
正 4
度,反应重新达到平衡,平衡常数减小,则此时曲线甲对应的平衡点可能为 (填字母,下同),曲线乙
对应的平衡点可能为 。
3.SO 经过净化后与空气混合进行催化氧化后制取硫酸或者硫酸铵,其中SO 发生催化氧化的反应为2SO(g)
2 2 2
+O(g) 2SO(g)。若在T ℃、0.1 MPa条件下,往一密闭容器通入SO 和O[其中n(SO)∶n(O)=2∶1],测
2 3 1 2 2 2 2
得容器内总压强与反应时间如右上图所示。①该反应的化学平衡常数表达式:K= 。
②图中A点时,SO 的转化率为 。
2
③计算SO 催化氧化反应在图中B点的压强平衡常数K= (用平衡分压代替平衡浓度计算,
2 p
分压=总压×物质的量分数)。
④若在T ℃、其他条件不变的情况下测得压强的变化曲线如上图所示,则T (填“>”、“<”或
2 1
“=”)T;其中C点的正反应速率v(正)与A点的逆反应速率v(逆)的大小关系为v(正) (填“>”、
2 C A C
“<”或“=”)v(逆)。
A
易错点二 化学平衡计算
【易错典例】
例2(Ⅰ.二甲醚是一种重要的清洁燃料,可以通过CHOH分子间脱水制得:2CHOH(g) CHOCH(g)+
3 3 3 3
HO(g) ΔH=-23.5kJ·mol-1。在t℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化
2 1
如图所示。
(1)该条件下反应平衡常数表达式 K=___________________________;在t ℃时,反应的平衡常数为
1
________,达到平衡时n(CHOCH):n(CHOH): n(HO)=_____________________。
3 3 3 2
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为:c(CHOH)=0.4 mol·L-1、c(HO)=0.6
3 2
mol·L-1、c(CHOCH)=2.4mol·L-1,此时正、逆反应速率的大小:v ________v (填“>”、“<”或
3 3 正 逆
“=”),反应向______反应方向进行(填“正”或“逆”)。
Ⅱ.已知可逆反应:M(g)+N(g) P(g)+Q(g) ΔH>0,请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为c(M)=1 mol·L-1,c(N)=2.4 mol·L-1。达到平衡后,M的转
化率为60%,此时N的转化率为____________。
(2)若反应温度升高,M的转化率__________(填“增大”、“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为c(M)=4mol·L-1,c(N)=a mol·L-1;达到平衡后,c(P)=2 mol·L-1,a=____________。
【解题必备】
1.化学平衡常数
(1)在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度化学计量数次幂的乘积与其反应物浓
度化学计量数次幂的乘积的比值是一个常数,即平衡常数,用符号K表示。对一般可逆反应mA(g)+nB(g)
pC(g)+qD(g),当在一定温度下达平衡状态时,可以得出:K= ,K值越大,说明平衡体
系中生成物所占的比例越大,反应物的转化率越大,K只受温度影响,与反应物或生成物的浓度变化无关,
即在一定温度下,平衡常数保持不变。
(2)化学平衡常数的应用:根据平衡常数可判断可逆反应进行的程度,平衡常数越大,正反应进行的程
度越大,反应物的转化率越高,平衡后生成物的浓度越大,反应物的浓度越小;利用化学平衡常数可判断
化学平衡移动的方向,对于可逆反应aA(g)+bB(g) cC(g)+dD(g),在一定温度下的任意时刻,反应
物与生成物浓度有如下关系: =Q,称为浓度商: ;
c
利用化学平衡常数判断可逆反应的热效应: 。
2.化学平衡的计算
“三段式”法是有效解答化学平衡计算题的“万能钥匙”。解题时,要注意清楚条理地列出起始量、
转化量、平衡量,按题目要求进行计算,同时还要注意单位的统一。举例如下:
(1)则A的转化率α(A)=×100%。
(2)D的物质的量分数=×100%。
(3)起始与平衡时的压强比:=。
(4)平衡时混合气体的平均相对分子质量=。
【变式突破】
4.亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl 反应得到,化学方程式为2NO(g)+Cl(g)
2 2
2NOCl(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO(g)+NaCl(s) NaNO(s)+NOCl(g)
2 3
②4NO(g)+2NaCl(s) 2NaNO(s)+2NO(g)+Cl(g)
2 3 2
③2NO(g)+Cl(g) 2NOCl(g)
2设反应①②③对应的平衡常数依次为K、K、K,则K、K、K之间的关系为____________。
1 2 3 1 2 3
(2)300 ℃时,2NOCl(g) 2NO(g)+Cl(g)。
2
正反应速率的表达式为v =k·cn(NOCl)(k为速率常数,只与温度有关),测得速率与浓度的关系如表所
正
示:
v/mol·L-1·s
序号 c(NOCl)/mol·L-1
-1
① 0.30 3.60×10-9
② 0.60 1.44×10-8
③ 0.90 3.24×10-8
n=________,k=________。
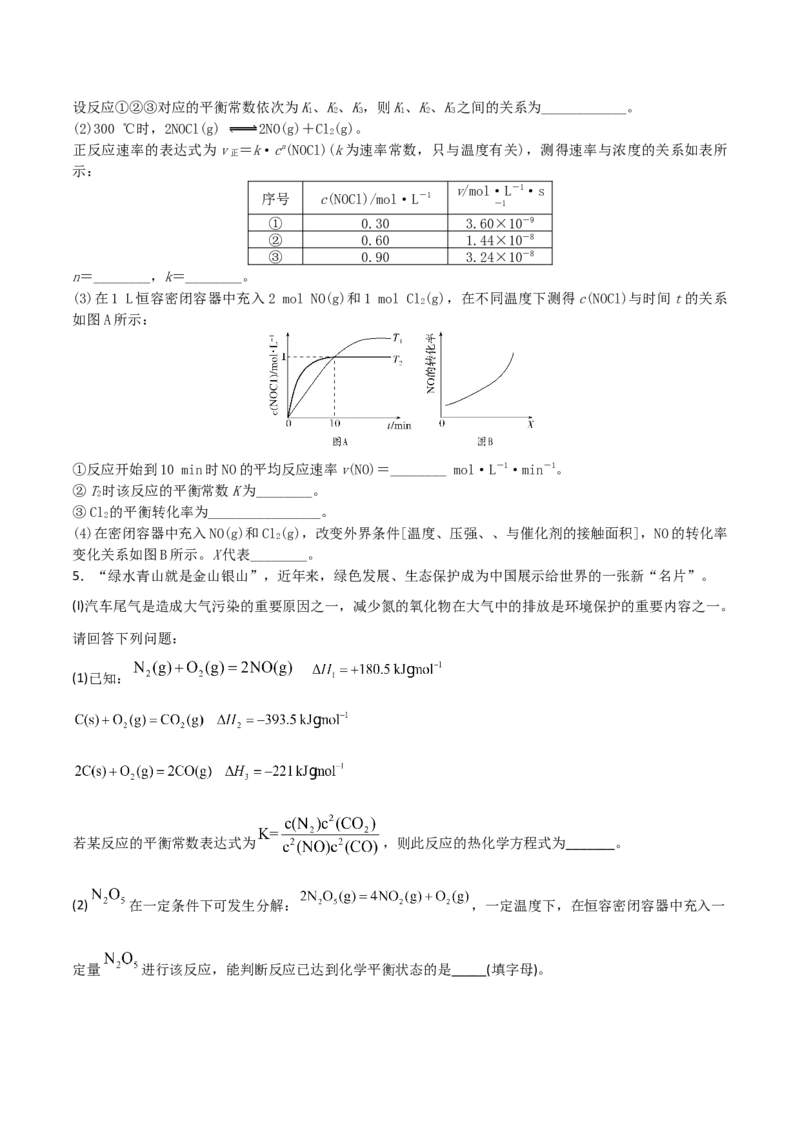
(3)在1 L恒容密闭容器中充入2 mol NO(g)和1 mol Cl(g),在不同温度下测得c(NOCl)与时间t的关系
2
如图A所示:
①反应开始到10 min时NO的平均反应速率v(NO)=________ mol·L-1·min-1。
②T时该反应的平衡常数K为________。
2
③Cl 的平衡转化率为________________。
2
(4)在密闭容器中充入NO(g)和Cl(g),改变外界条件[温度、压强、、与催化剂的接触面积],NO的转化率
2
变化关系如图B所示。X代表________。
5.“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。
(I)汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
请回答下列问题:
(1)已知:
若某反应的平衡常数表达式为 ,则此反应的热化学方程式为_______。
(2) 在一定条件下可发生分解: ,一定温度下,在恒容密闭容器中充入一
定量 进行该反应,能判断反应已达到化学平衡状态的是_____(填字母)。A. 和 的浓度比保持不变 B.容器中压强不再变化
C. D.气体的密度保持不变
(Ⅱ)甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都是重要的化工原料,有着重要的用途和应用前景,
可以用多种方法合成。 CO (g) + 3H (g) CH OH(g) + H O(g)
2 2 3 2
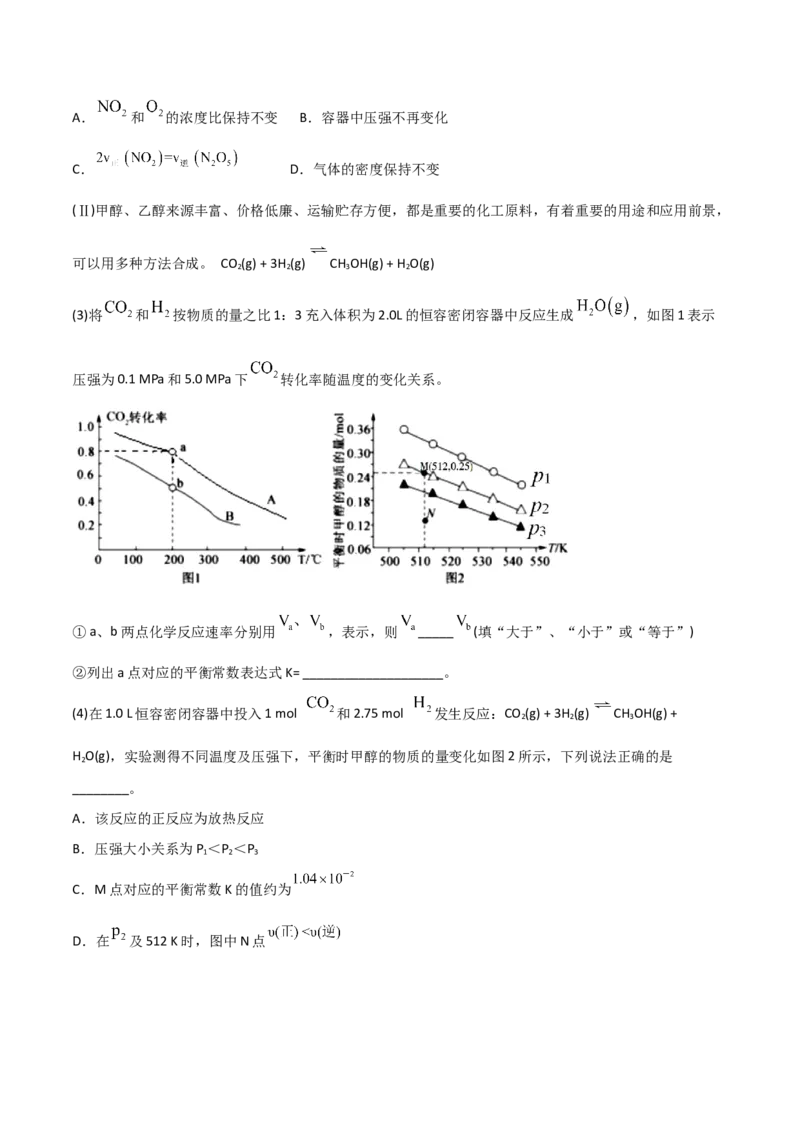
(3)将 和 按物质的量之比1:3充入体积为2.0L的恒容密闭容器中反应生成 ,如图1表示
压强为0.1 MPa和5.0 MPa下 转化率随温度的变化关系。
①a、b两点化学反应速率分别用 ,表示,则 _____ (填“大于”、“小于”或“等于”)
②列出a点对应的平衡常数表达式K= ____________________。
(4)在1.0 L恒容密闭容器中投入1 mol 和2.75 mol 发生反应:CO (g) + 3H (g) CH OH(g) +
2 2 3
H O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是
2
________。
A.该反应的正反应为放热反应
B.压强大小关系为P <P <P
1 2 3
C.M点对应的平衡常数K的值约为
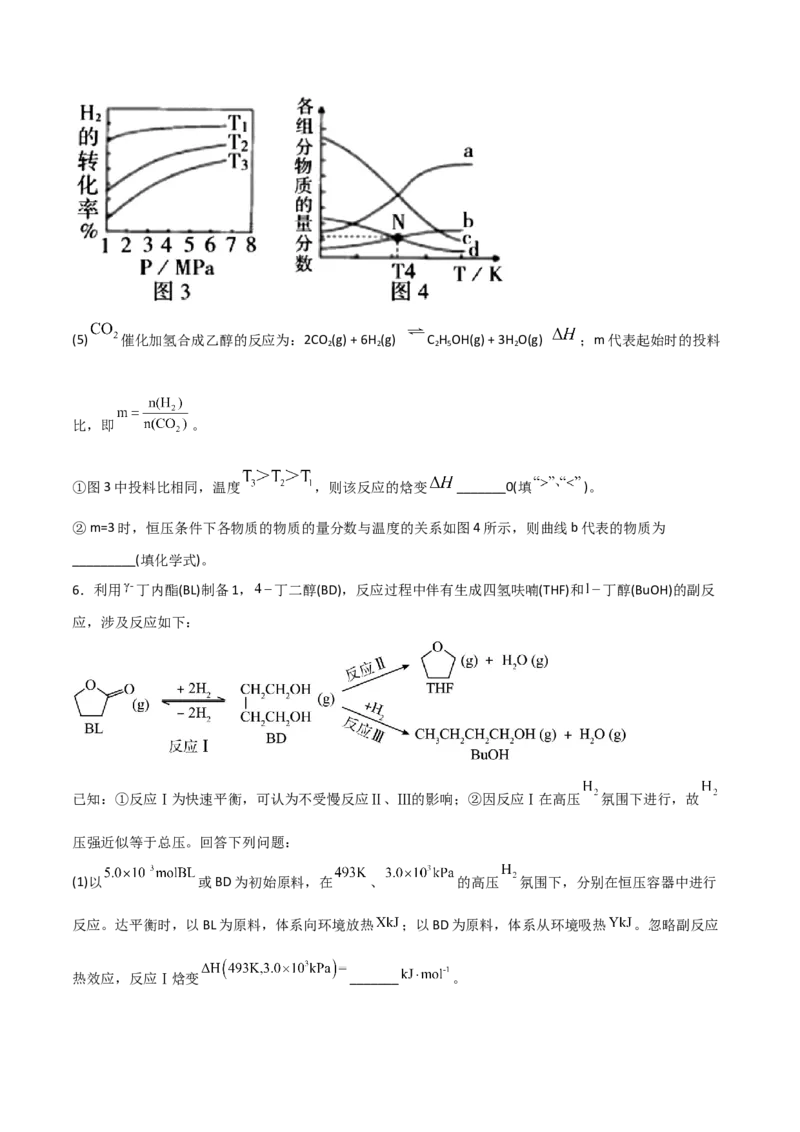
D.在 及512 K时,图中N点(5) 催化加氢合成乙醇的反应为:2CO (g) + 6H (g) C H OH(g) + 3H O(g) ;m代表起始时的投料
2 2 2 5 2
比,即 。
①图3中投料比相同,温度 ,则该反应的焓变 _______0(填 )。
②m=3时,恒压条件下各物质的物质的量分数与温度的关系如图4所示,则曲线b代表的物质为
_________(填化学式)。
6.利用 丁内酯(BL)制备1, 丁二醇(BD),反应过程中伴有生成四氢呋喃(THF)和 丁醇(BuOH)的副反
应,涉及反应如下:
已知:①反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响;②因反应Ⅰ在高压 氛围下进行,故
压强近似等于总压。回答下列问题:
(1)以 或BD为初始原料,在 、 的高压 氛围下,分别在恒压容器中进行
反应。达平衡时,以BL为原料,体系向环境放热 ;以BD为原料,体系从环境吸热 。忽略副反应
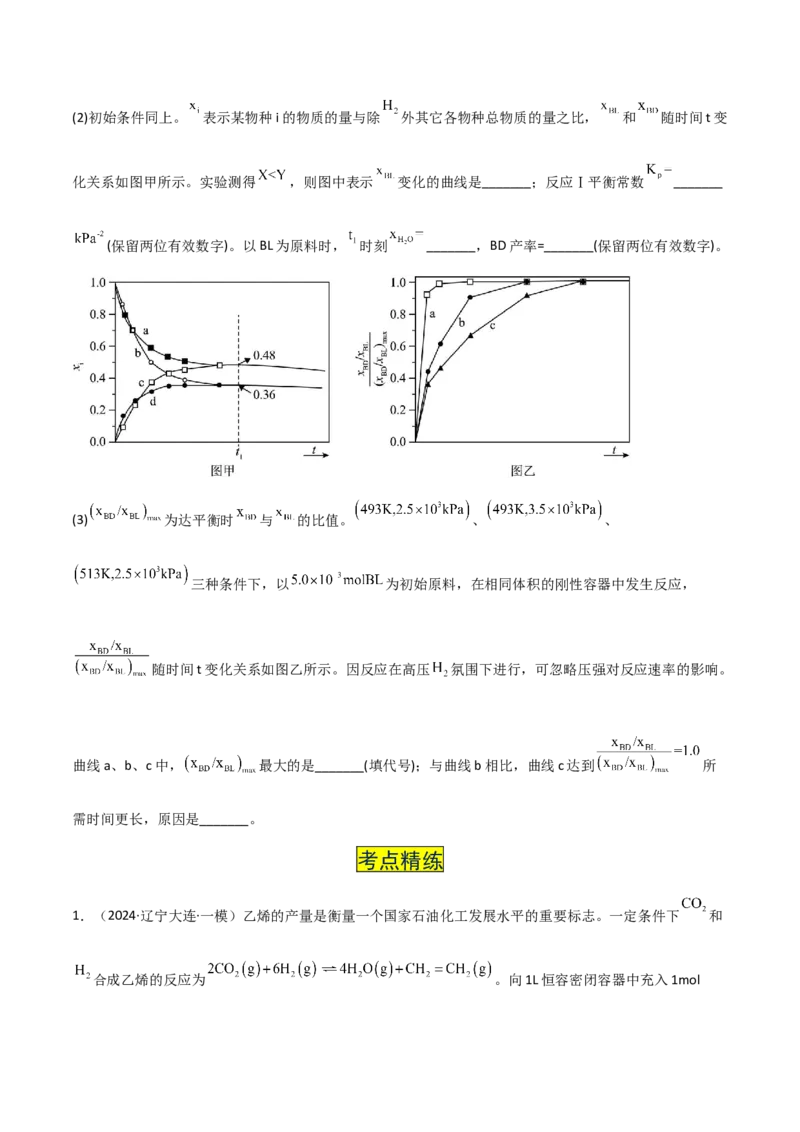
热效应,反应Ⅰ焓变 _______ 。(2)初始条件同上。 表示某物种i的物质的量与除 外其它各物种总物质的量之比, 和 随时间t变
化关系如图甲所示。实验测得 ,则图中表示 变化的曲线是_______;反应Ⅰ平衡常数 _______
(保留两位有效数字)。以BL为原料时, 时刻 _______,BD产率=_______(保留两位有效数字)。
(3) 为达平衡时 与 的比值。 、 、
三种条件下,以 为初始原料,在相同体积的刚性容器中发生反应,
随时间t变化关系如图乙所示。因反应在高压 氛围下进行,可忽略压强对反应速率的影响。
曲线a、b、c中, 最大的是_______(填代号);与曲线b相比,曲线c达到 所
需时间更长,原因是_______。
考点精练
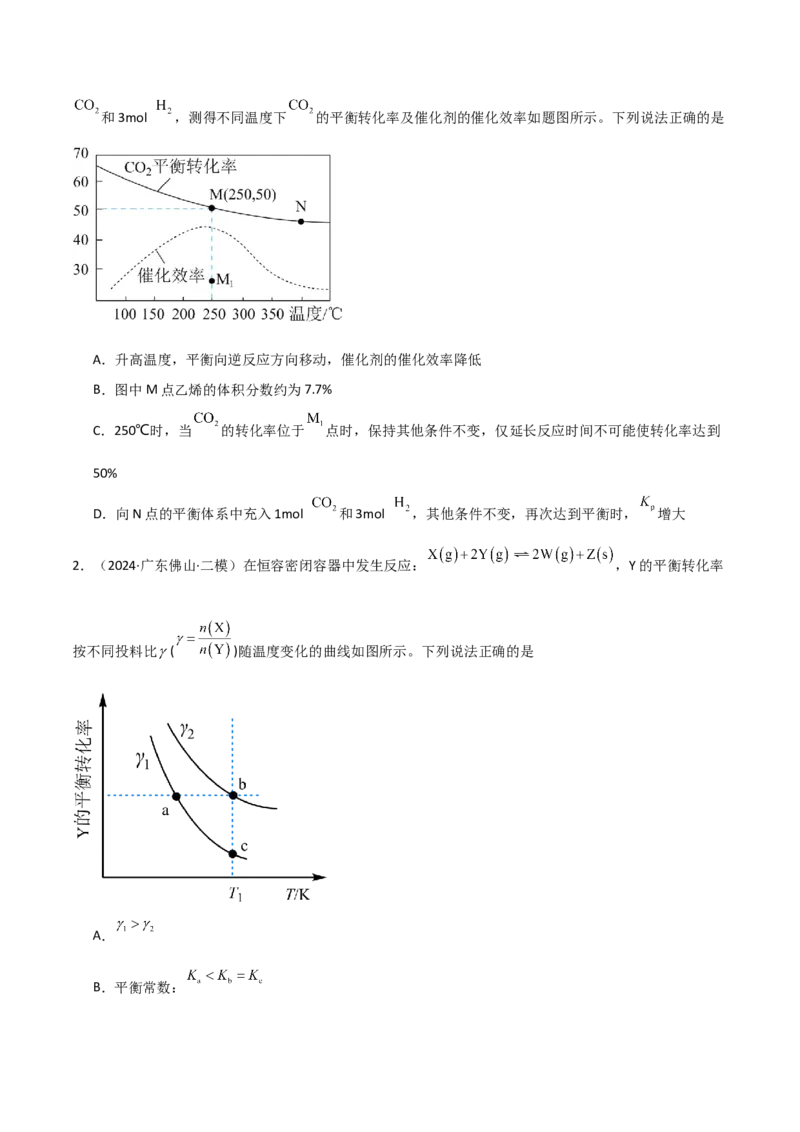
1.(2024·辽宁大连·一模)乙烯的产量是衡量一个国家石油化工发展水平的重要标志。一定条件下 和
合成乙烯的反应为 。向1L恒容密闭容器中充入1mol和3mol ,测得不同温度下 的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是
A.升高温度,平衡向逆反应方向移动,催化剂的催化效率降低
B.图中M点乙烯的体积分数约为7.7%
C.250℃时,当 的转化率位于 点时,保持其他条件不变,仅延长反应时间不可能使转化率达到
50%
D.向N点的平衡体系中充入1mol 和3mol ,其他条件不变,再次达到平衡时, 增大
2.(2024·广东佛山·二模)在恒容密闭容器中发生反应: ,Y的平衡转化率
按不同投料比 ( )随温度变化的曲线如图所示。下列说法正确的是
A.
B.平衡常数:C.当容器内气体密度不变时,反应达到平衡
D. 温度下增大压强,c点向a点方向移动
3.(2024·黑龙江·二模)中国积极推动技术创新,力争2060年实现碳中和。CO 催化还原的主要反应有:
2
①
②
向恒温恒压的密闭容器中通入1 mol CO 和3 mol H 进行上述反应。CH OH的平衡产率、CO 的平衡转化率
2 2 3 2
随温度变化关系如图。下列说法错误的是
A.反应②的
B.若气体密度不再变化,反应①和②均达到平衡状态
C.任一温度下的平衡转化率:
D.平衡时 随温度升高先增大后减小
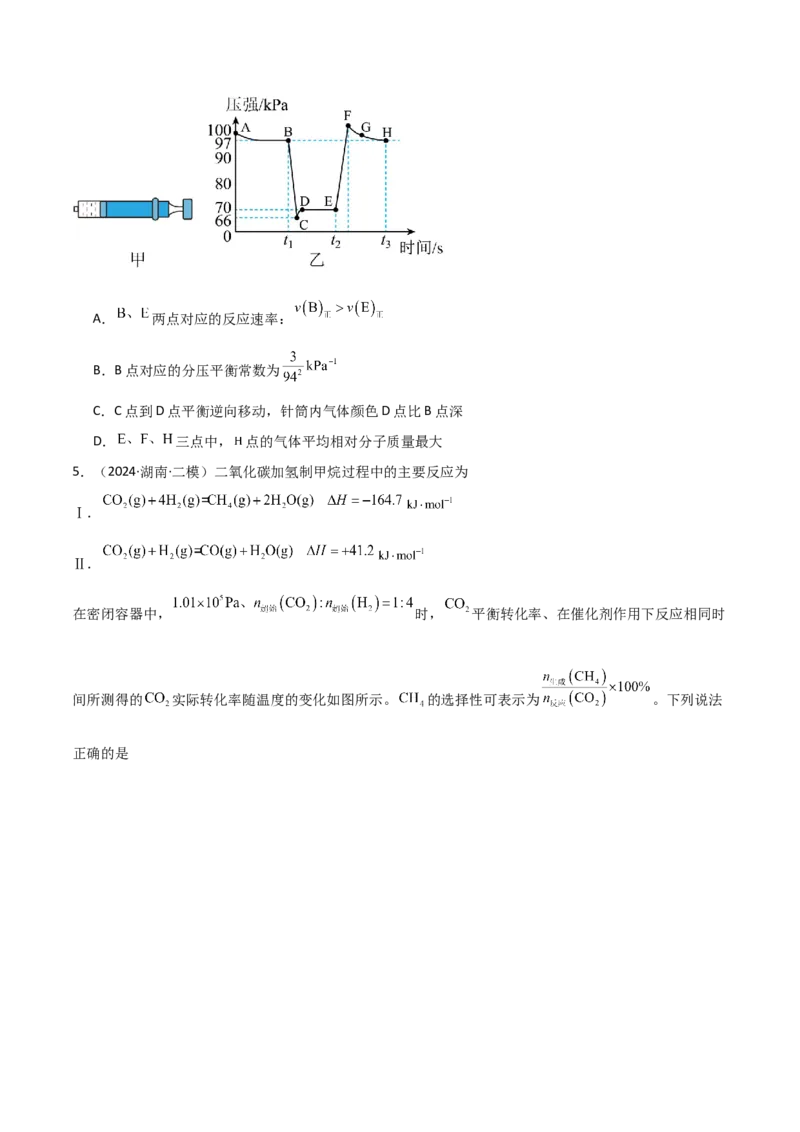
4.(2024·重庆·一模)利用传感技术可探究压强对化学平衡 的影响。往注射器中充
入适量 气体保持活塞位置不变达到平衡(图甲);恒定温度下,分别在 时快速移动注射器活塞后保
持活塞位置不变,测得注射器内气体总压强随时间变化如图乙。下列说法错误的是A. 两点对应的反应速率:
B.B点对应的分压平衡常数为
C.C点到D点平衡逆向移动,针筒内气体颜色D点比B点深
D. 三点中, 点的气体平均相对分子质量最大
5.(2024·湖南·二模)二氧化碳加氢制甲烷过程中的主要反应为
Ⅰ.
Ⅱ.
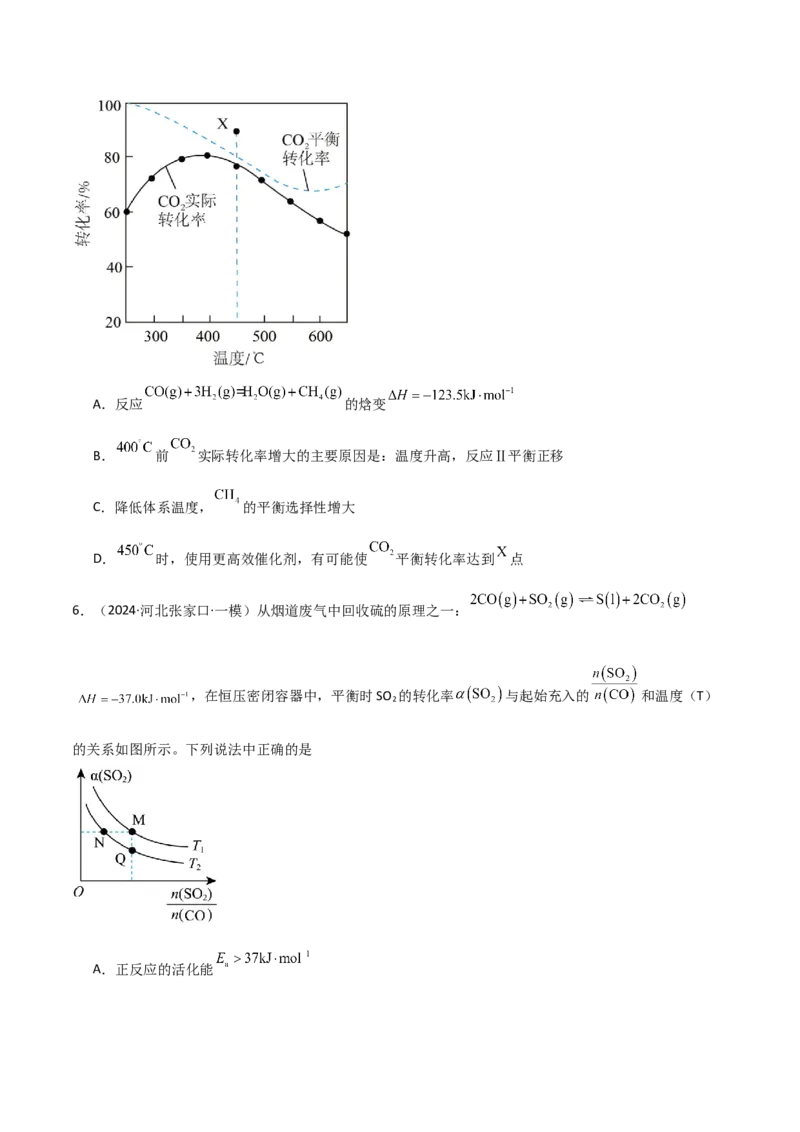
在密闭容器中, 时, 平衡转化率、在催化剂作用下反应相同时
间所测得的 实际转化率随温度的变化如图所示。 的选择性可表示为 。下列说法
正确的是A.反应 的焓变
B. 前 实际转化率增大的主要原因是:温度升高,反应Ⅱ平衡正移
C.降低体系温度, 的平衡选择性增大
D. 时,使用更高效催化剂,有可能使 平衡转化率达到 点
6.(2024·河北张家口·一模)从烟道废气中回收硫的原理之一:
,在恒压密闭容器中,平衡时SO 的转化率 与起始充入的 和温度(T)
2
的关系如图所示。下列说法中正确的是
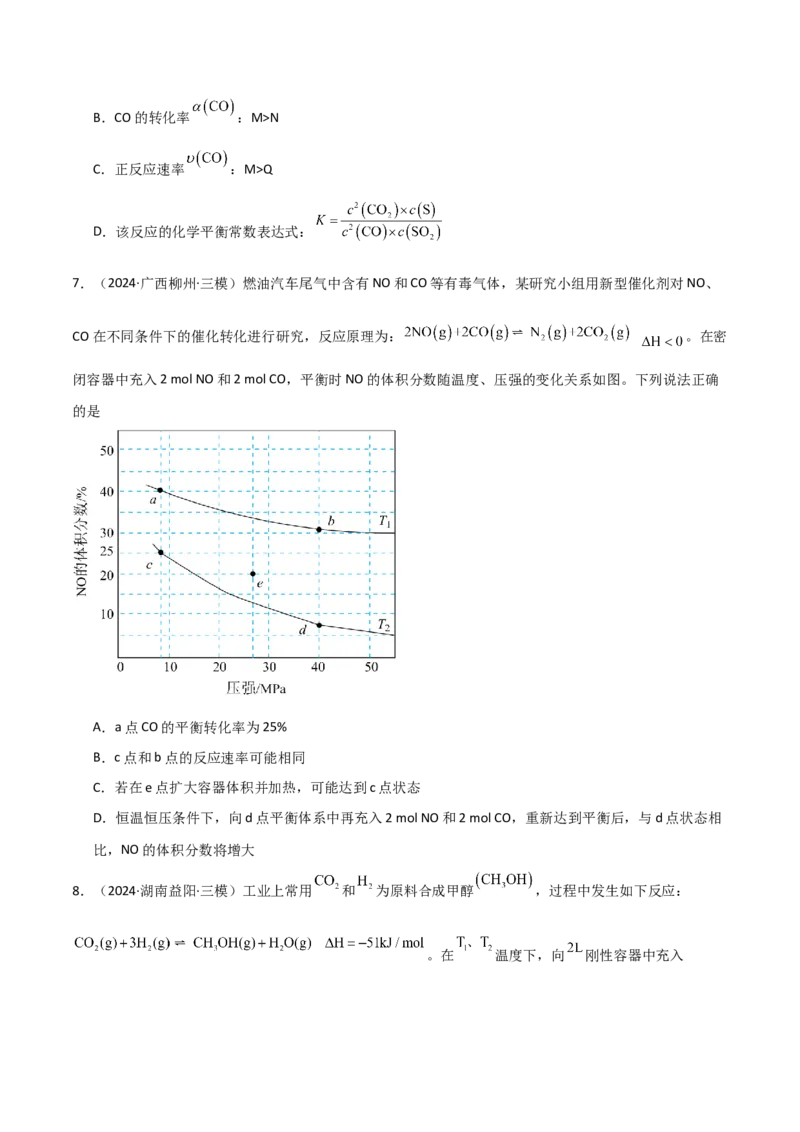
A.正反应的活化能B.CO的转化率 :M>N
C.正反应速率 :M>Q
D.该反应的化学平衡常数表达式:
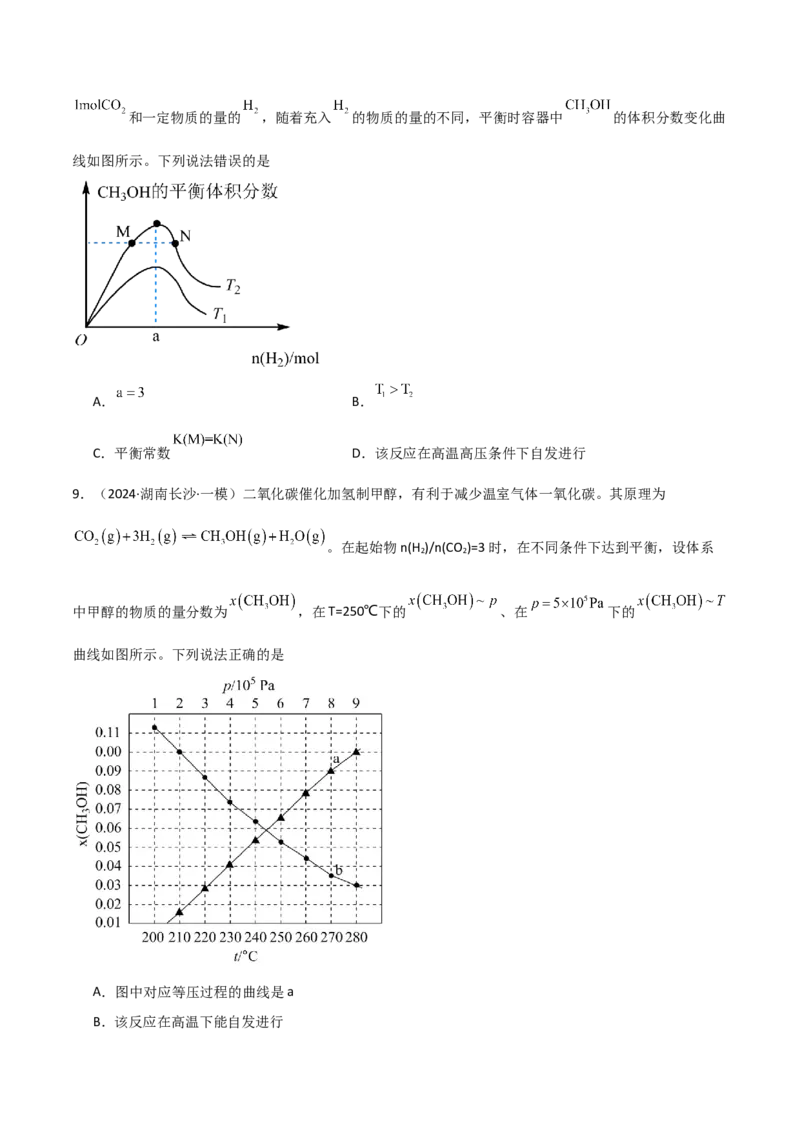
7.(2024·广西柳州·三模)燃油汽车尾气中含有NO和CO等有毒气体,某研究小组用新型催化剂对NO、
CO在不同条件下的催化转化进行研究,反应原理为: 。在密
闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确
的是
A.a点CO的平衡转化率为25%
B.c点和b点的反应速率可能相同
C.若在e点扩大容器体积并加热,可能达到c点状态
D.恒温恒压条件下,向d点平衡体系中再充入2 mol NO和2 mol CO,重新达到平衡后,与d点状态相
比,NO的体积分数将增大
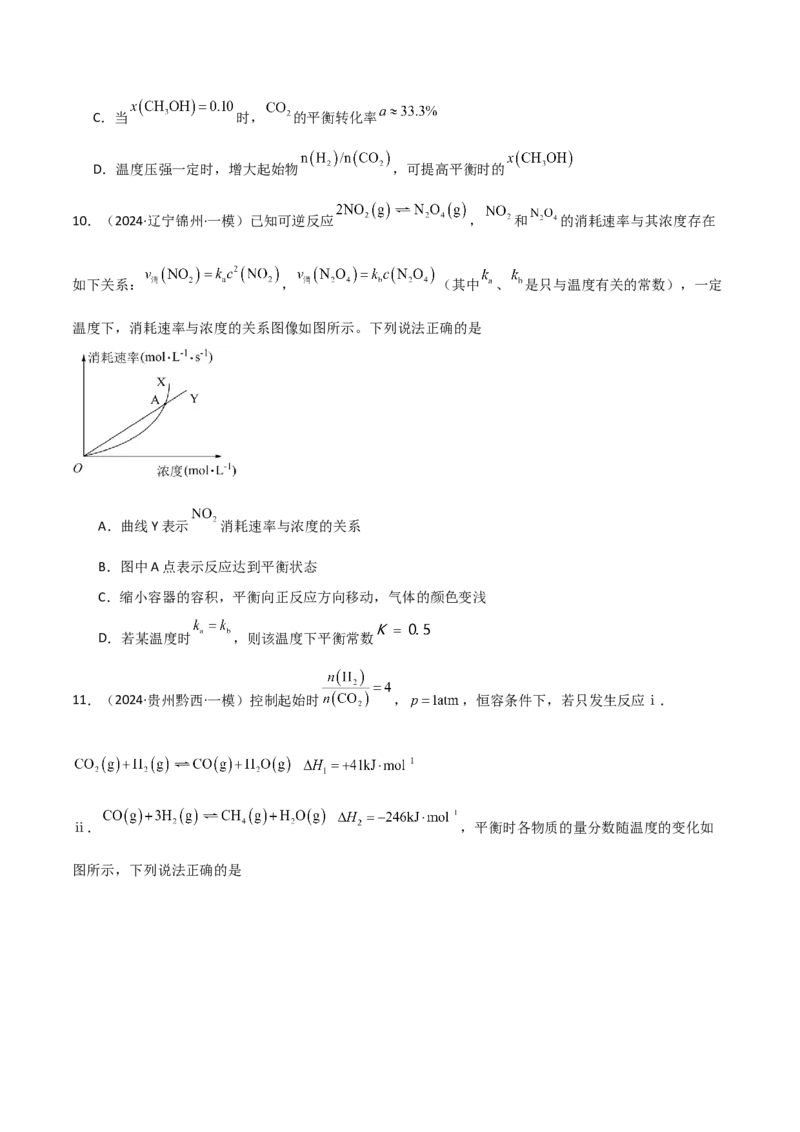
8.(2024·湖南益阳·三模)工业上常用 和 为原料合成甲醇 ,过程中发生如下反应:
。在 温度下,向 刚性容器中充入和一定物质的量的 ,随着充入 的物质的量的不同,平衡时容器中 的体积分数变化曲
线如图所示。下列说法错误的是
A. B.
C.平衡常数 D.该反应在高温高压条件下自发进行
9.(2024·湖南长沙·一模)二氧化碳催化加氢制甲醇,有利于减少温室气体一氧化碳。其原理为
。在起始物n(H )/n(CO )=3时,在不同条件下达到平衡,设体系
2 2
中甲醇的物质的量分数为 ,在T=250℃下的 、在 下的
曲线如图所示。下列说法正确的是
A.图中对应等压过程的曲线是a
B.该反应在高温下能自发进行C.当 时, 的平衡转化率
D.温度压强一定时,增大起始物 ,可提高平衡时的
10.(2024·辽宁锦州·一模)已知可逆反应 , 和 的消耗速率与其浓度存在
如下关系: , (其中 、 是只与温度有关的常数),一定
温度下,消耗速率与浓度的关系图像如图所示。下列说法正确的是
A.曲线Y表示 消耗速率与浓度的关系
B.图中A点表示反应达到平衡状态
C.缩小容器的容积,平衡向正反应方向移动,气体的颜色变浅
D.若某温度时 ,则该温度下平衡常数
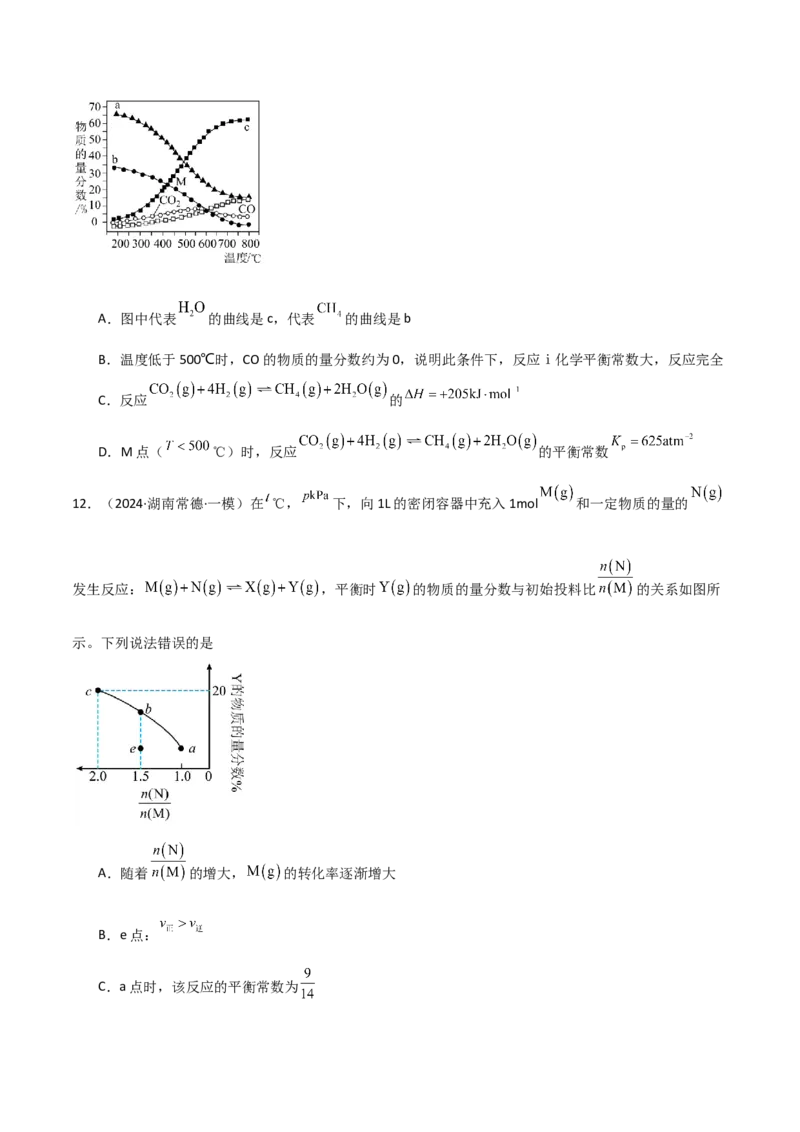
11.(2024·贵州黔西·一模)控制起始时 , ,恒容条件下,若只发生反应ⅰ.
ⅱ. ,平衡时各物质的量分数随温度的变化如
图所示,下列说法正确的是A.图中代表 的曲线是c,代表 的曲线是b
B.温度低于500℃时,CO的物质的量分数约为0,说明此条件下,反应ⅰ化学平衡常数大,反应完全
C.反应 的
D.M点( ℃)时,反应 的平衡常数
12.(2024·湖南常德·一模)在 ℃, 下,向1L的密闭容器中充入1mol 和一定物质的量的
发生反应: ,平衡时 的物质的量分数与初始投料比 的关系如图所
示。下列说法错误的是
A.随着 的增大, 的转化率逐渐增大
B.e点:
C.a点时,该反应的平衡常数为D.a点,平衡后再投入1mol 和1mol ,达到新平衡时, 的产率增大
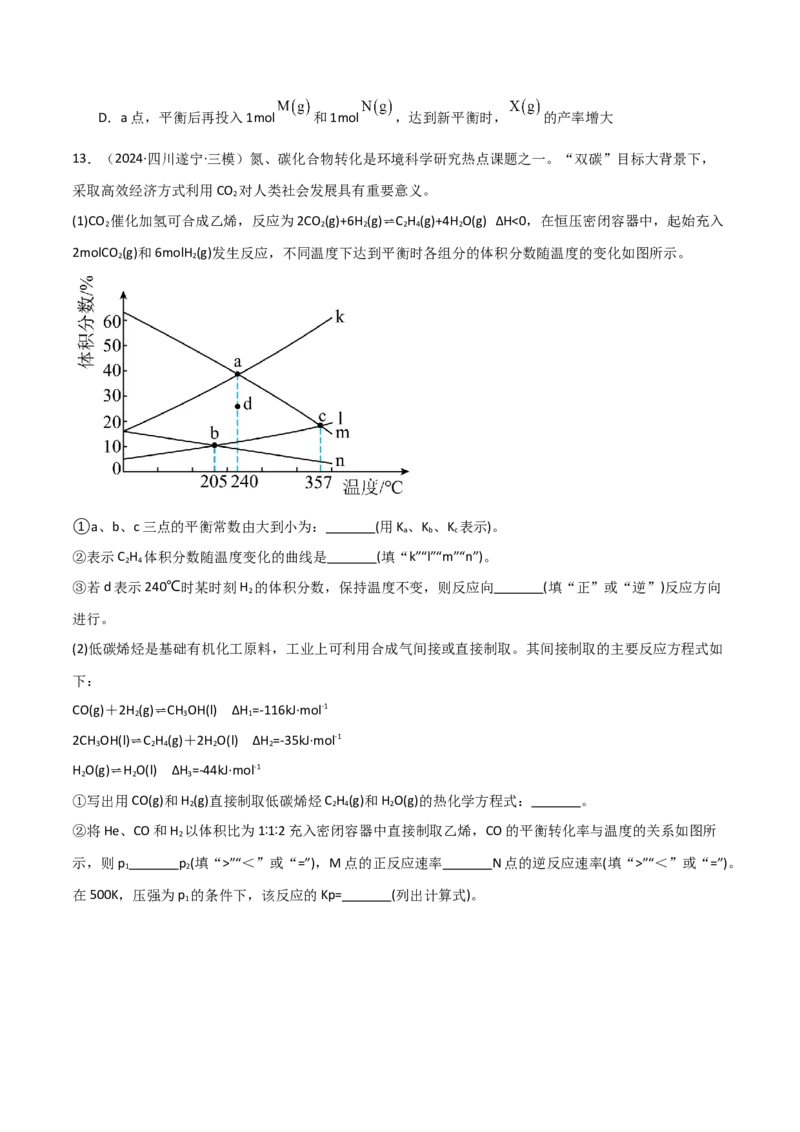
13.(2024·四川遂宁·三模)氮、碳化合物转化是环境科学研究热点课题之一。“双碳”目标大背景下,
采取高效经济方式利用CO 对人类社会发展具有重要意义。
2
(1)CO
2
催化加氢可合成乙烯,反应为2CO
2
(g)+6H
2
(g)⇌C
2
H
4
(g)+4H
2
O(g) ΔH<0,在恒压密闭容器中,起始充入
2molCO (g)和6molH (g)发生反应,不同温度下达到平衡时各组分的体积分数随温度的变化如图所示。
2 2
①a、b、c三点的平衡常数由大到小为: (用K、K 、K 表示)。
a b c
②表示C H 体积分数随温度变化的曲线是 (填“k”“l”“m”“n”)。
2 4
③若d表示240℃时某时刻H 的体积分数,保持温度不变,则反应向 (填“正”或“逆”)反应方向
2
进行。
(2)低碳烯烃是基础有机化工原料,工业上可利用合成气间接或直接制取。其间接制取的主要反应方程式如
下:
CO(g)+2H
2
(g)⇌CH
3
OH(l) ΔH
1
=-116kJ·mol-1
2CH
3
OH(l)⇌C
2
H
4
(g)+2H
2
O(l) ΔH
2
=-35kJ·mol-1
H
2
O(g)⇌H
2
O(l) ΔH
3
=-44kJ·mol-1
①写出用CO(g)和H (g)直接制取低碳烯烃C H (g)和H O(g)的热化学方程式: 。
2 2 4 2
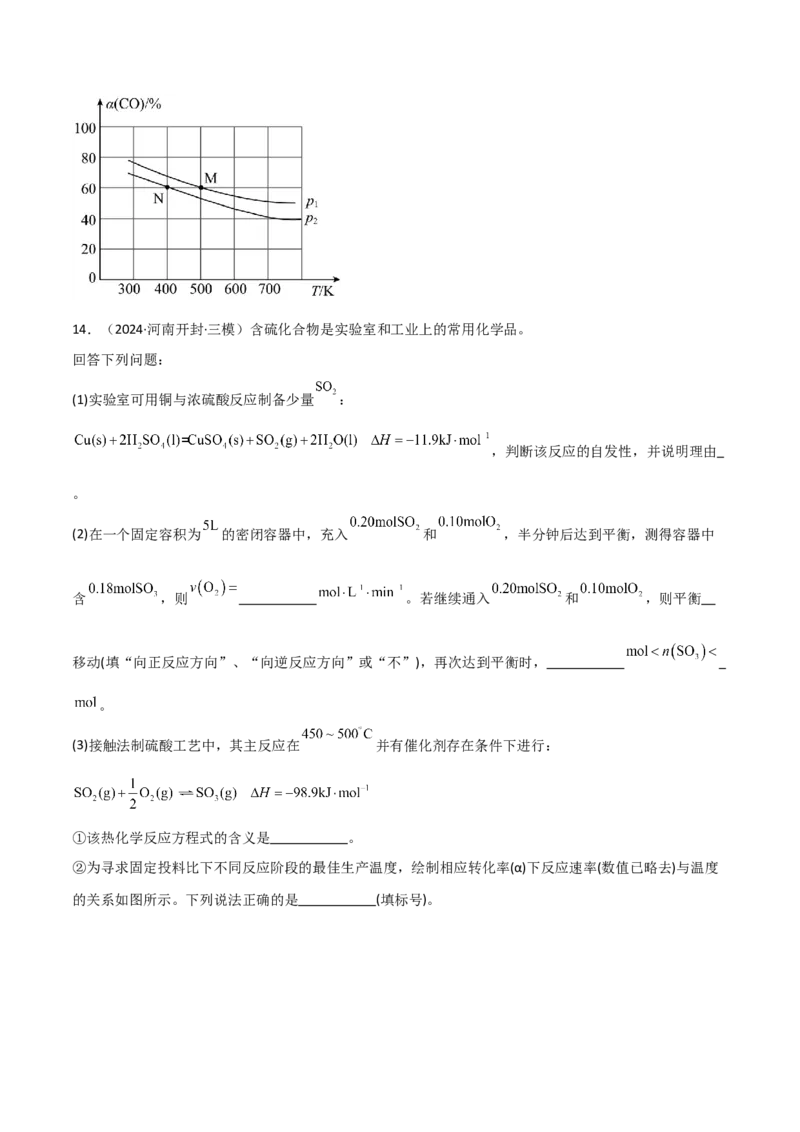
②将He、CO和H 以体积比为1∶1∶2充入密闭容器中直接制取乙烯,CO的平衡转化率与温度的关系如图所
2
示,则p p (填“>”“<”或“=”),M点的正反应速率 N点的逆反应速率(填“>”“<”或“=”)。
1 2
在500K,压强为p 的条件下,该反应的Kp= (列出计算式)。
114.(2024·河南开封·三模)含硫化合物是实验室和工业上的常用化学品。
回答下列问题:
(1)实验室可用铜与浓硫酸反应制备少量 :
,判断该反应的自发性,并说明理由
。
(2)在一个固定容积为 的密闭容器中,充入 和 ,半分钟后达到平衡,测得容器中
含 ,则 。若继续通入 和 ,则平衡
移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡时,
。
(3)接触法制硫酸工艺中,其主反应在 并有催化剂存在条件下进行:
①该热化学反应方程式的含义是 。
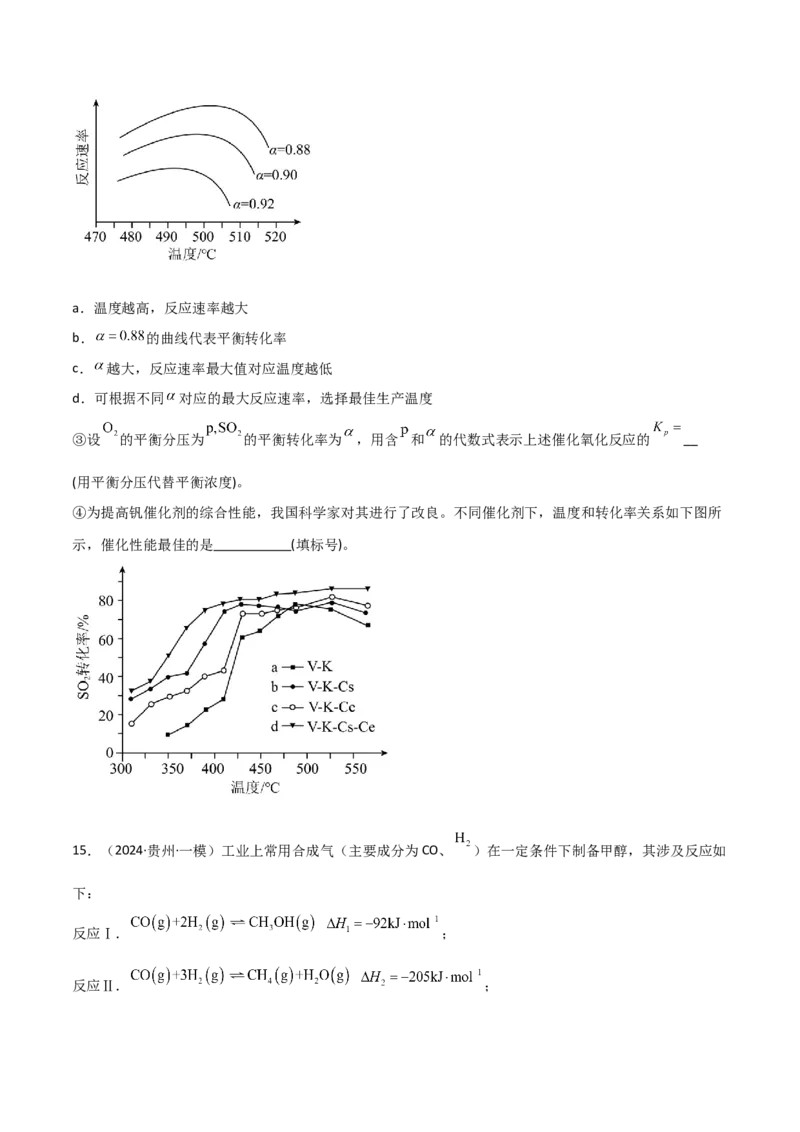
②为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度
的关系如图所示。下列说法正确的是 (填标号)。a.温度越高,反应速率越大
b. 的曲线代表平衡转化率
c. 越大,反应速率最大值对应温度越低
d.可根据不同 对应的最大反应速率,选择最佳生产温度
③设 的平衡分压为 的平衡转化率为 ,用含 和 的代数式表示上述催化氧化反应的
(用平衡分压代替平衡浓度)。
④为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所
示,催化性能最佳的是 (填标号)。
15.(2024·贵州·一模)工业上常用合成气(主要成分为CO、 )在一定条件下制备甲醇,其涉及反应如
下:
反应Ⅰ. ;
反应Ⅱ. ;反应Ⅲ. 。
回答下列问题:
(1)在催化剂作用下也可以由CO 制备甲醇: ,则
2
;该反应在 (填“高温”“低温”或“任意温度”)下可自发进行。
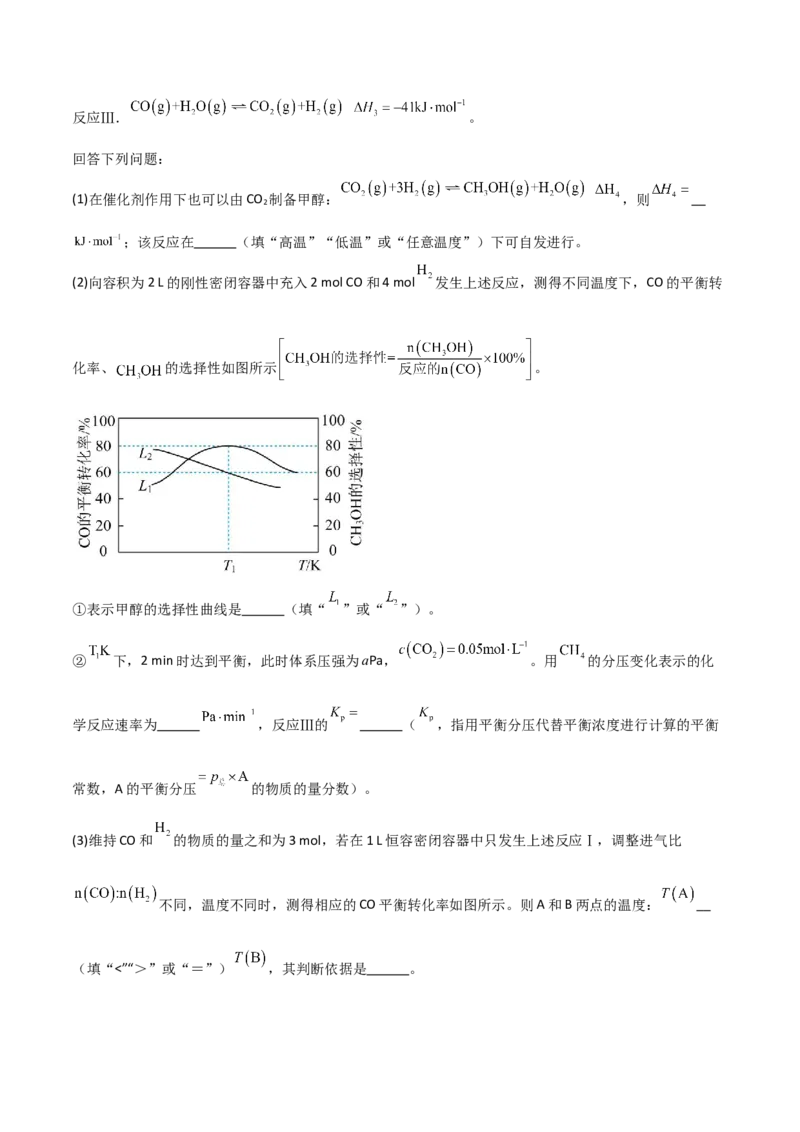
(2)向容积为2 L的刚性密闭容器中充入2 mol CO和4 mol 发生上述反应,测得不同温度下,CO的平衡转
化率、 的选择性如图所示 。
①表示甲醇的选择性曲线是 (填“ ”或“ ”)。
② 下,2 min时达到平衡,此时体系压强为aPa, 。用 的分压变化表示的化
学反应速率为 ,反应Ⅲ的 ( ,指用平衡分压代替平衡浓度进行计算的平衡
常数,A的平衡分压 的物质的量分数)。
(3)维持CO和 的物质的量之和为3 mol,若在1 L恒容密闭容器中只发生上述反应Ⅰ,调整进气比
不同,温度不同时,测得相应的CO平衡转化率如图所示。则A和B两点的温度:
(填“<”“>”或“=”) ,其判断依据是 。16.(2024·黑龙江大庆·模拟预测)乙烯是重要的工业原料,可用下列方法制备。
Ⅰ. 催化加氢法制乙烯:
已知: 的燃烧热分别为: ;
(1)该反应 。
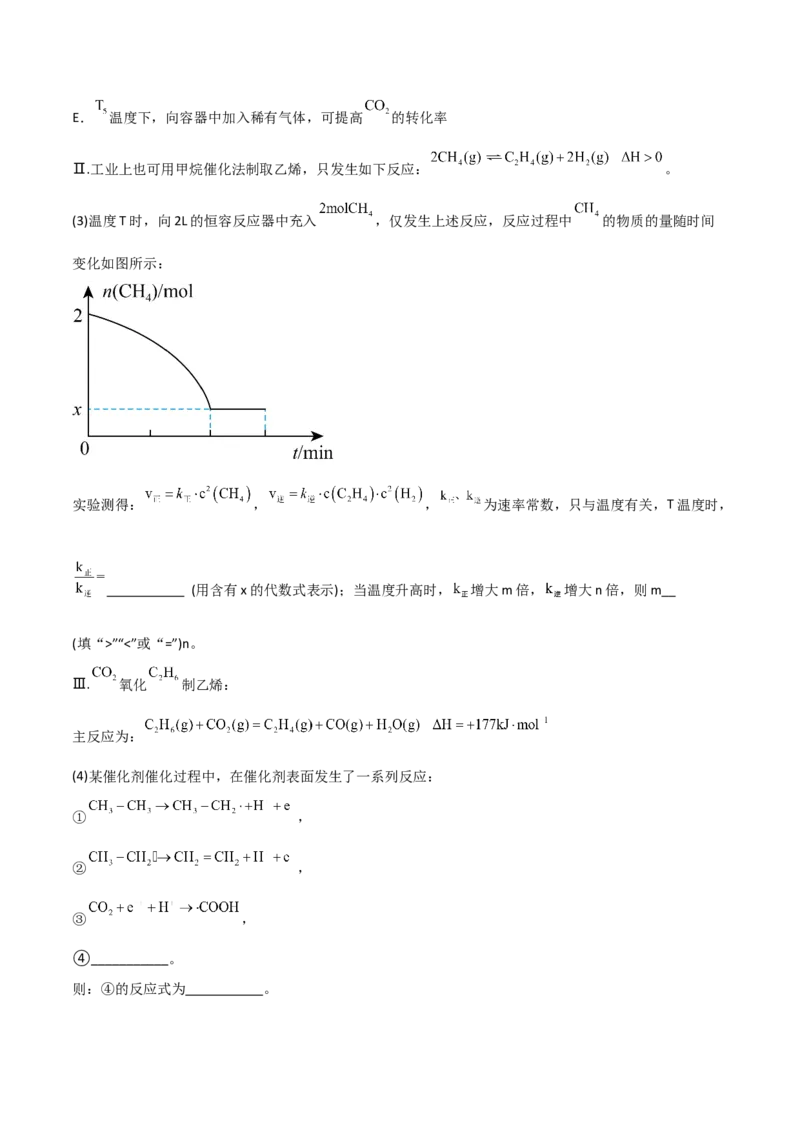
(2)将 和 按物质的量之比为2:3充入恒容密闭容器中,分别在不同催化剂条件下发生反应,测得相
同时间 的转化率与温度的关系如图所示:
一定温度下,下列有关说法正确的是 。
A.达平衡时, 一定为2:3
B.向反应体系中加入少量无水 固体,可提高 的产率
C.b、d两状态下,化学反应速率一定相等
D.使用催化剂Ⅰ时反应的活化能比使用催化剂Ⅱ时低E. 温度下,向容器中加入稀有气体,可提高 的转化率
Ⅱ.工业上也可用甲烷催化法制取乙烯,只发生如下反应: 。
(3)温度T时,向2L的恒容反应器中充入 ,仅发生上述反应,反应过程中 的物质的量随时间
变化如图所示:
实验测得: , , 为速率常数,只与温度有关,T温度时,
(用含有x的代数式表示);当温度升高时, 增大m倍, 增大n倍,则m
(填“>”“<”或“=”)n。
Ⅲ. 氧化 制乙烯:
主反应为:
(4)某催化剂催化过程中,在催化剂表面发生了一系列反应:
① ,
② ,
③ ,
④___________。
则:④的反应式为 。(5)在 与 反应制 的过程中,
还会发生副反应:
①其他条件相同时, 与 经相同反应时间测得如表实验数据:
实验 温度/K 催化剂 的产率%
400 催化剂1 55.0
实验1
400 催化剂2 62.3
500 催化剂1 68.5
实验2
500 催化剂2 80.1
相同温度时,催化剂2催化下 产率更高的原因是 。
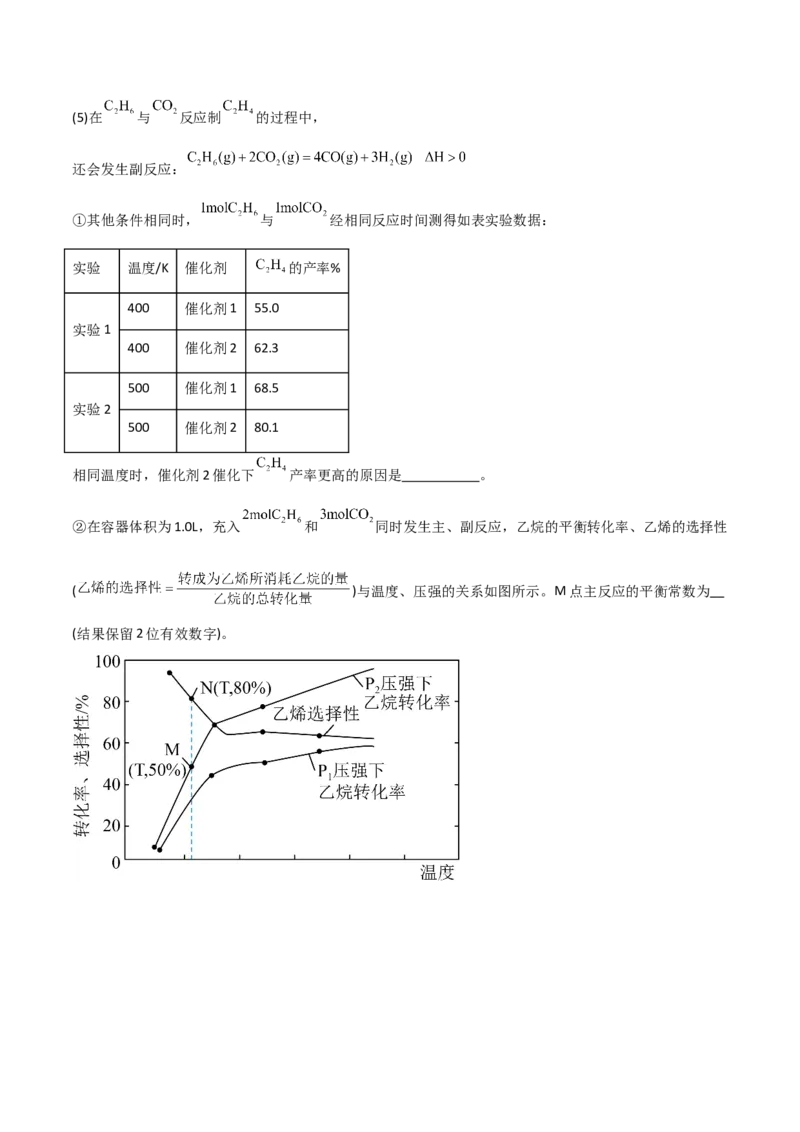
②在容器体积为1.0L,充入 和 同时发生主、副反应,乙烷的平衡转化率、乙烯的选择性
( )与温度、压强的关系如图所示。M点主反应的平衡常数为
(结果保留2位有效数字)。