文档内容
2022~2023学年度第一学期高三期初试卷
化 学
可能用到的相对原子质量:
选择题
单项选择题:本题包括13小题,每小题3分,共计39分。每小题只有一个选项最符合题意。
1.从烟道气分离回收硫的基本反应: 。下列说法正确的是()。
A.该反应属于置换反应 B.铝土矿的主要成分为
C. 在该反应中表现出氧化性 D. 、CO和 均属于酸性氧化物
2.乙醛常用于有机合成,可由乙醇氧化得到。乙醇催化氧化制取乙醛的反应如下:
下列说法正确的是()。
A.CuO晶体是共价晶体
B. 的电子式:
C. 的沸点低于
D. 中所含 键的数目为6mol
3.白云土是一种硅酸盐,用氢氟酸处理白云土生成一种水溶性很低的物质 。下列
说法正确的是()。
A.电负性大小: B.半径大小:
C.电离能大小: D.碱性强弱:
4.下图为实验室制备 并验证其氧化性的实验装置,实验过程中控制甲装置滴加硫酸溶
液的量,其中表述不正确的是()。
A.用装置甲产生 气体
B.装置乙中应通入过量的
C.装置丙中溶液颜色发生变化,体现了 具有氧化性
D.用装置丁吸收尾气
阅读下列材料,完成5~7题:黄铁矿 是一种重要的含铁矿物,在潮湿空气中会被缓
慢氧化: 。工业上常选择黄铁矿为原料制备
硫酸,其中发生的反应有: ;。
5.下列物质性质与用途具有对应关系的是()。
A. 溶液显酸性,可用作自来水厂的净水剂
B. 属于碱性氧化物,可用作粉刷墙壁的红色涂料
C. 具有还原性,可用于葡萄酒的保存
D.浓硫酸具有脱水性,可干燥氯气
6.下列说法正确的是()。
A. 的价电子排布式为 B. 晶体中存在离子键和非极性共
价键
C. 与 都是非极性分子 D. 与 的空间构型相同
7. 的反应机理如下:
反应Ⅰ:
反应Ⅱ:
反应中的能量变化如题图,下列说法不正确的是()。
A.
B.反应Ⅰ的
C.通入过量空气,可提高 的平衡转化率
D.反应速率由反应Ⅰ决定
8.某同学按题图装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物质
组合不符合要求的是()。
气体 液体 固体粉末
A 饱和 溶液
B 溶液 Fe
C HCl 溶液 CuD AgCl
9.异黄酮类是药用植物的有效成分之一。一种异黄酮类化合物Z的部分合成路线如图:
下列有关化合物X、Y和Z的说法正确的是()。
A.1molX与足量溴水反应消耗
B.1molY最多能与3molNaOH反应
C.Z分子中存在顺反异构体
D.Z与足量 加成所得有机物中含6个手性碳原子
10.弱碱性条件下,利用含砷氧化铜矿(含CuO、 及少量不溶性杂质)制备
的工艺流程如下。下列说法不正确的是()。
A.“氨浸”时 发生的离子反应为
B.“氨浸”后的滤液中存在的阳离子主要有: 、
C.“氧化除 ”时生成 ,消耗 为1.5mol
D.“蒸氨”后的滤液中含有
11.室温下,下列实验探究方案不能达到探究目的的是()。
选项 探究方案及现象 探究目的
向KBr溶液中加入少量苯,通入适量
A 氧化性:
后充分振荡,观察有机层颜色变化
向盛有 溶液的试管中滴加几滴
B KSCN溶液,振荡,再滴加几滴新制氯水, 具有还原性
观察溶液颜色变化
向蛋白质溶液中滴加饱和 溶液,
C 蛋白质发生了变性
有固体析出,再加水观察固体是否溶解
用pH计测量浓度均为 的
D 和 溶液的pH,
后者大于前者
12.室温下,通过下列实验探究邻苯二甲酸氢钾( ,以KHA表示)溶液的性质。
实验1:用pH计测定 溶液的pH,测得pH约为4.01
实验2:向 溶液中滴加 溶液实验3:向 溶液中加入过量澄清石灰水,产生白色沉淀
下列有关说法正确的是()。
A.由实验1可得出:
B.实验2滴加过程中: 逐渐减小
C.实验2所得的溶液中:
D.实验3中反应的离子方程式为:
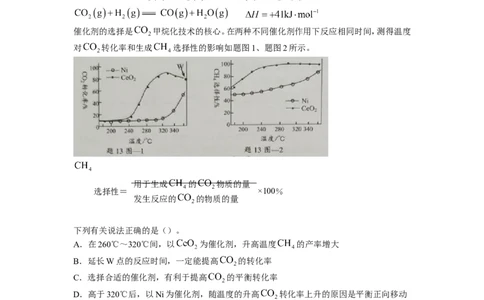
13.在一定的温度和压强下,将按一定比例混合的 和 通过装有催化剂的反应器可得
到甲烷。已知:
催化剂的选择是 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测得温度
对 转化率和生成 选择性的影响如题图1、题图2所示。
用于生成 的 物质的量
选择性= ×100%
发生反应的 的物质的量
下列有关说法正确的是()。
A.在260℃~320℃间,以 为催化剂,升高温度 的产率增大
B.延长W点的反应时间,一定能提高 的转化率
C.选择合适的催化剂,有利于提高 的平衡转化率
D.高于320℃后,以Ni为催化剂,随温度的升高 转化率上升的原因是平衡正向移动
非选择题(共4题,共61分)
14.(16分)氧化亚铜是一种重要的无机化工原料,在工农业生产等领域有广泛的用途。
的制备有电解法、湿法还原法和水解法等。
(1)电解法
以含NaOH的碱性NaCl为电解质溶液,纯铜为阴、阳极电解制备 。写出电解的总反应
式______。
(2)湿法还原法
水合肼 还原碱性的铜氨离子 ,可得到 和 。①写出上述反应的离子方程式______。
②不考虑空间构型, 结构的示意图可表示为______。
③保持其它条件不变,水合肼浓度对 的产率有影响。当水合肼浓度过高时,
的转化率增大,但 的产率却下降,可能的原因是______。
(3)水解法
已知:CuCl为白色粉末,微溶于水,不溶于乙醇。
以CuCl为前驱体水解也可制得 ,前驱体CuCl可由 与 、NaCl在溶液
中反应,过滤制得。
①写出生成CuCl的离子方程式______。
②用“醇洗”可快速去除滤渣表面的水,并能防止滤渣被空气氧化为 。CuCl
被氧化为 的化学方程式为______。
15.(15分)SCR催化制广泛应用于燃煤烟气的处理,其主要成分为 、 、 ,还
含有少量CaO、 、 等。一种从废SCR催化剂中回收钨的工艺如下:
(1)“酸浸还原”中 转化成可溶于水的 ,该反应的化学方程式为______。
(2)“碱浸”时 转化为 的离子方程式为______。
(3)“滤渣”的主要成分是______。
(4)常温下 , 。“沉钨”过程中不断
加入石灰乳,当“滤液”的 时, 为______ 。
(5)“熔融电解”过程中阴极反应为 。电解过程中作阳极的石
墨易消耗,原因是______。
(6)钛渣经处理可得到粗 。将 氯化为 是冶炼金属钛的主要反应之一。工业
上常采用“加碳氯化”的方法生产 ,同时得到CO,相应的化学方程式为
①
②
结合数据说明氯化过程中加碳的理由______。
16.(15分)采用沉淀-氧化法处理含铬(Ⅲ)废水,并回收制备重铬酸钾 的流程如
下:已知:① ,溶液 时,主要以 存在;在
时,主要以 存在。
②酸性条件下, 氧化性强于 。
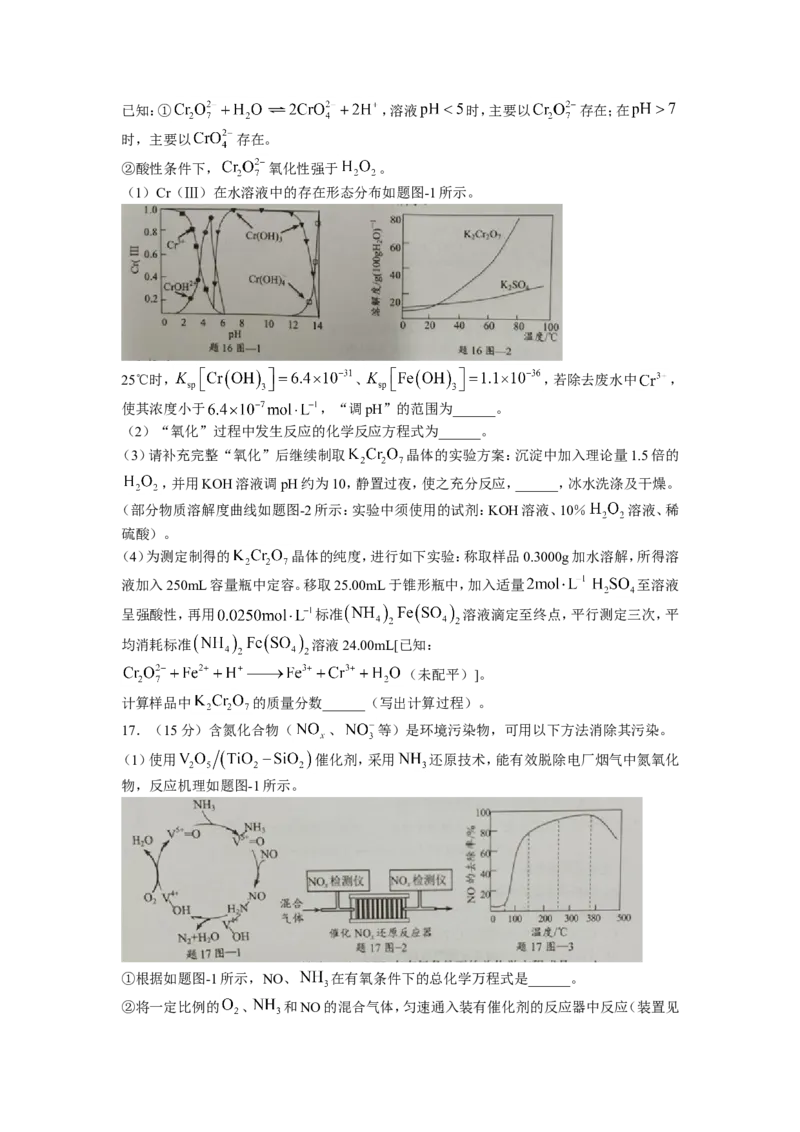
(1)Cr(Ⅲ)在水溶液中的存在形态分布如题图-1所示。
25℃时, 、 ,若除去废水中 ,
使其浓度小于 ,“调pH”的范围为______。
(2)“氧化”过程中发生反应的化学反应方程式为______。
(3)请补充完整“氧化”后继续制取 晶体的实验方案:沉淀中加入理论量1.5倍的
,并用KOH溶液调pH约为10,静置过夜,使之充分反应,______,冰水洗涤及干燥。
(部分物质溶解度曲线如题图-2所示:实验中须使用的试剂:KOH溶液、10% 溶液、稀
硫酸)。
(4)为测定制得的 晶体的纯度,进行如下实验:称取样品0.3000g加水溶解,所得溶
液加入250mL容量瓶中定容。移取25.00mL于锥形瓶中,加入适量 至溶液
呈强酸性,再用 标准 溶液滴定至终点,平行测定三次,平
均消耗标准 溶液24.00mL[已知:
(未配平)]。
计算样品中 的质量分数______(写出计算过程)。
17.(15分)含氮化合物( 、 等)是环境污染物,可用以下方法消除其污染。
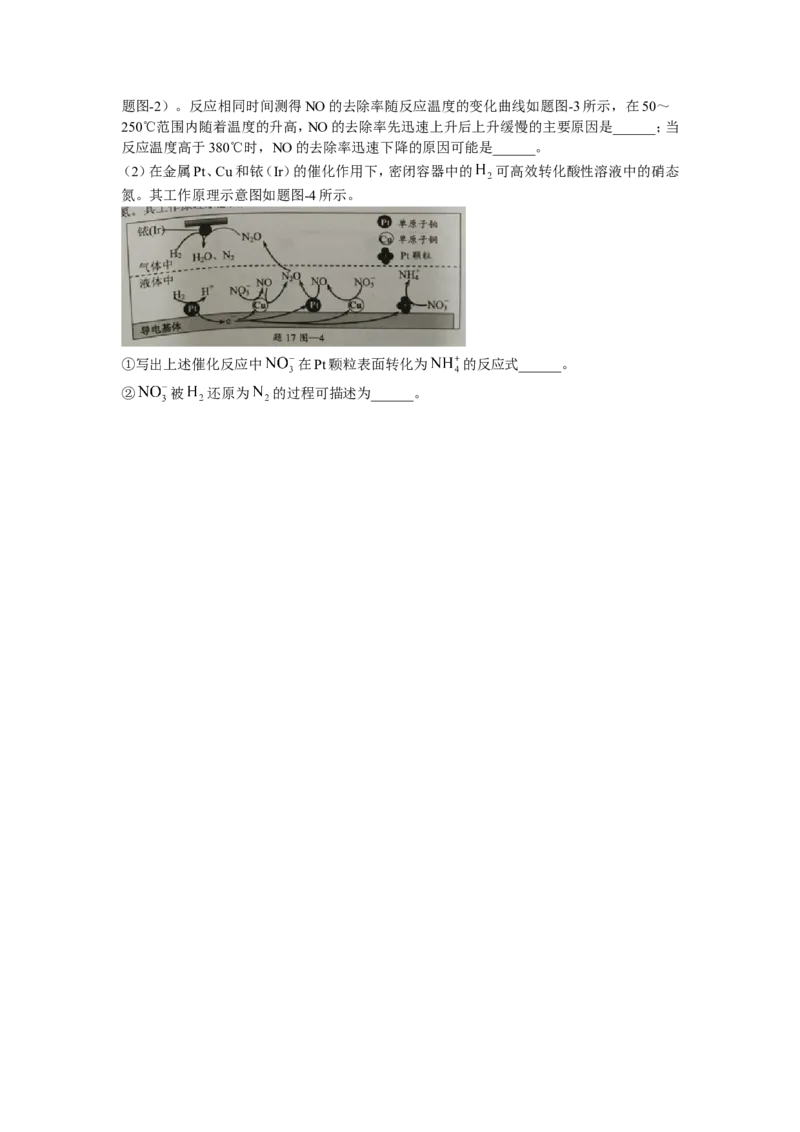
(1)使用 催化剂,采用 还原技术,能有效脱除电厂烟气中氮氧化
物,反应机理如题图-1所示。
①根据如题图-1所示,NO、 在有氧条件下的总化学万程式是______。
②将一定比例的 、 和NO的混合气体,匀速通入装有催化剂的反应器中反应(装置见题图-2)。反应相同时间测得NO的去除率随反应温度的变化曲线如题图-3所示,在50~
250℃范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是______;当
反应温度高于380℃时,NO的去除率迅速下降的原因可能是______。
(2)在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的 可高效转化酸性溶液中的硝态
氮。其工作原理示意图如题图-4所示。
①写出上述催化反应中 在Pt颗粒表面转化为 的反应式______。
② 被 还原为 的过程可描述为______。