文档内容
热点强化练 17 物质的分离提纯在实验、流程中的应用
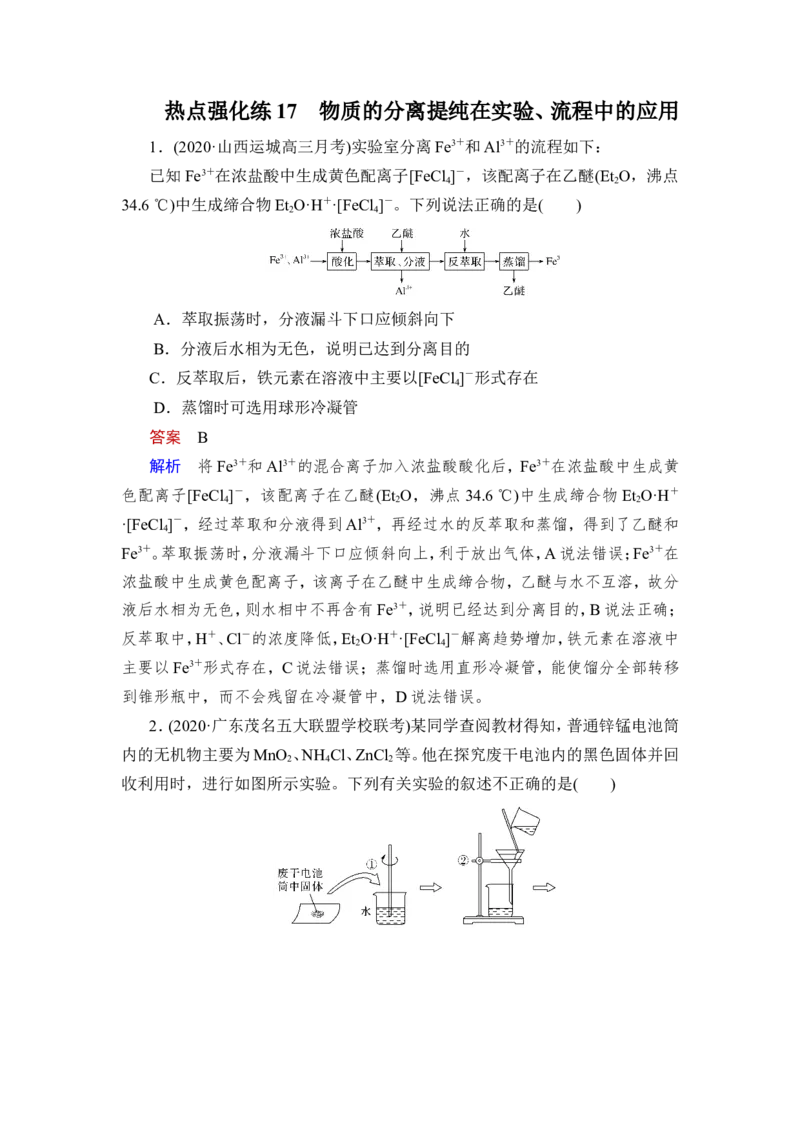
1.(2020·山西运城高三月考)实验室分离Fe3+和Al3+的流程如下:
已知Fe3+在浓盐酸中生成黄色配离子[FeCl ]-,该配离子在乙醚(Et O,沸点
4 2
34.6 ℃)中生成缔合物Et O·H+·[FeCl ]-。下列说法正确的是( )
2 4
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液后水相为无色,说明已达到分离目的
C.反萃取后,铁元素在溶液中主要以[FeCl ]-形式存在
4
D.蒸馏时可选用球形冷凝管
答案 B
解析 将Fe3+和Al3+的混合离子加入浓盐酸酸化后,Fe3+在浓盐酸中生成黄
色配离子[FeCl ]-,该配离子在乙醚(Et O,沸点34.6 ℃)中生成缔合物Et O·H+
4 2 2
·[FeCl ]-,经过萃取和分液得到Al3+,再经过水的反萃取和蒸馏,得到了乙醚和
4
Fe3+。萃取振荡时,分液漏斗下口应倾斜向上,利于放出气体,A说法错误;Fe3+在
浓盐酸中生成黄色配离子,该离子在乙醚中生成缔合物,乙醚与水不互溶,故分
液后水相为无色,则水相中不再含有Fe3+,说明已经达到分离目的,B说法正确;
反萃取中,H+、Cl-的浓度降低,Et O·H+·[FeCl ]-解离趋势增加,铁元素在溶液中
2 4
主要以Fe3+形式存在,C说法错误;蒸馏时选用直形冷凝管,能使馏分全部转移
到锥形瓶中,而不会残留在冷凝管中,D说法错误。
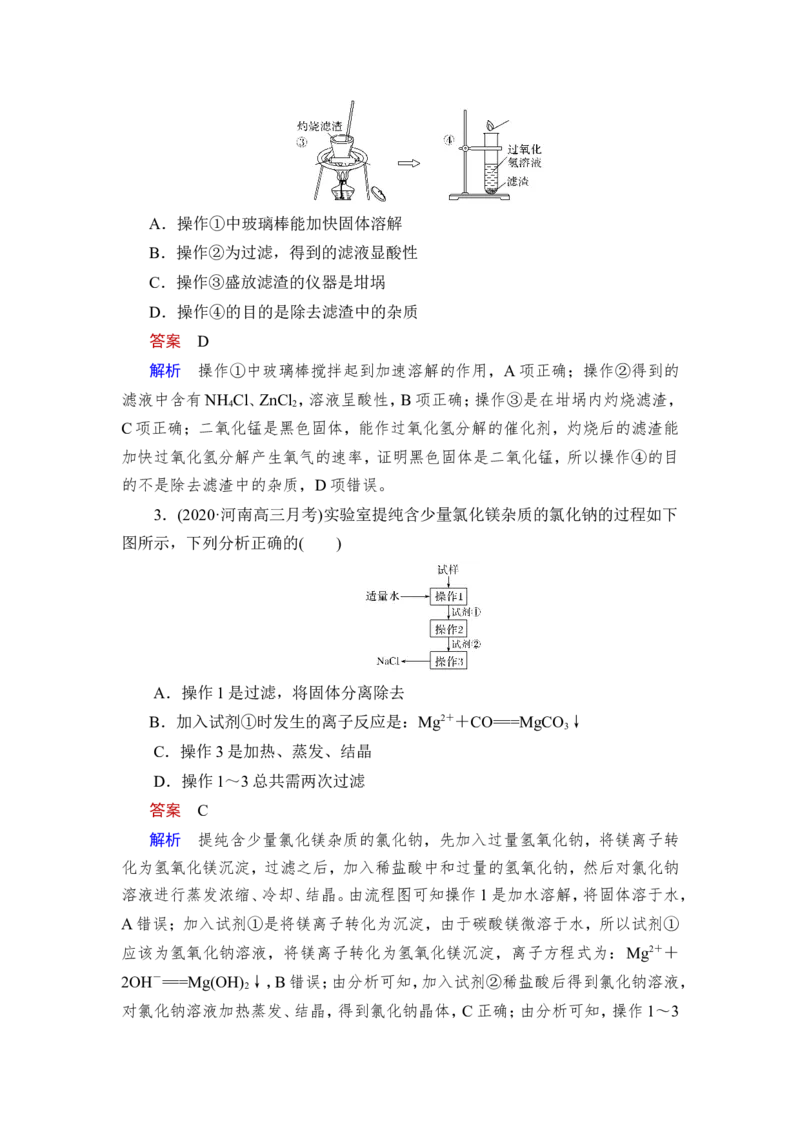
2.(2020·广东茂名五大联盟学校联考)某同学查阅教材得知,普通锌锰电池筒
内的无机物主要为MnO 、NH Cl、ZnCl 等。他在探究废干电池内的黑色固体并回
2 4 2
收利用时,进行如图所示实验。下列有关实验的叙述不正确的是( )A.操作①中玻璃棒能加快固体溶解
B.操作②为过滤,得到的滤液显酸性
C.操作③盛放滤渣的仪器是坩埚
D.操作④的目的是除去滤渣中的杂质
答案 D
解析 操作①中玻璃棒搅拌起到加速溶解的作用,A项正确;操作②得到的
滤液中含有NH Cl、ZnCl ,溶液呈酸性,B项正确;操作③是在坩埚内灼烧滤渣,
4 2
C项正确;二氧化锰是黑色固体,能作过氧化氢分解的催化剂,灼烧后的滤渣能
加快过氧化氢分解产生氧气的速率,证明黑色固体是二氧化锰,所以操作④的目
的不是除去滤渣中的杂质,D项错误。
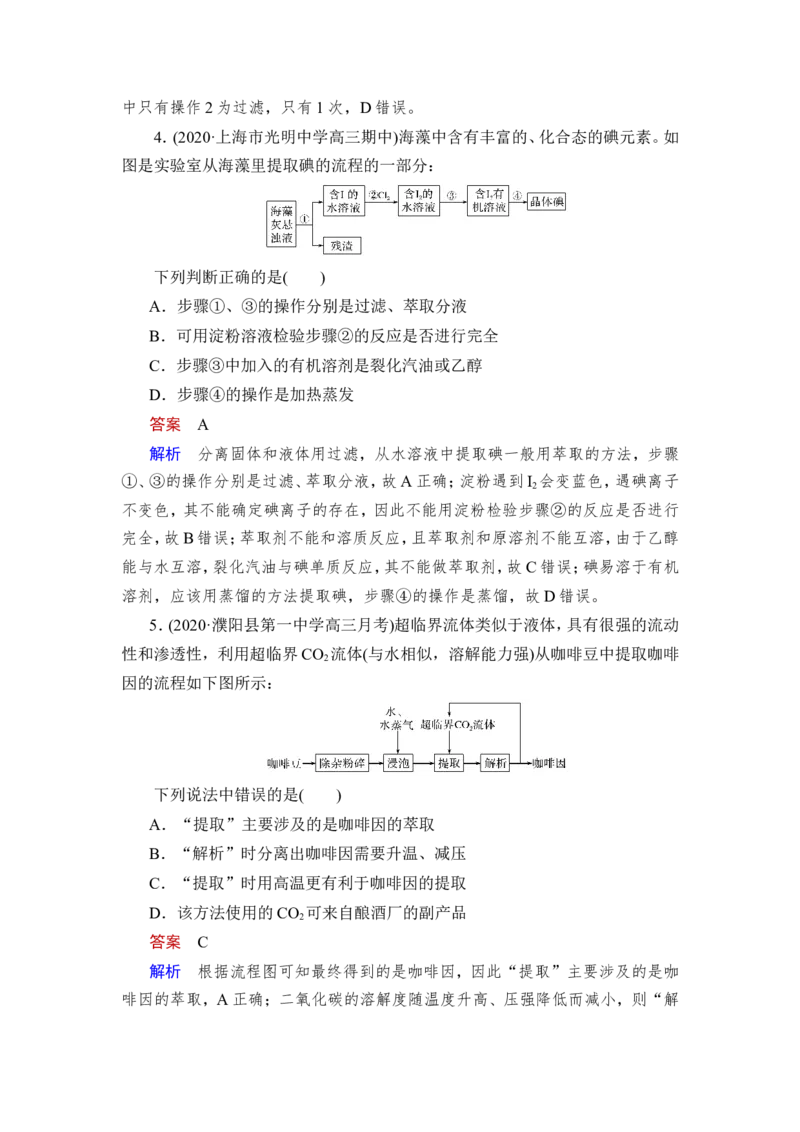
3.(2020·河南高三月考)实验室提纯含少量氯化镁杂质的氯化钠的过程如下
图所示,下列分析正确的( )
A.操作1是过滤,将固体分离除去
B.加入试剂①时发生的离子反应是:Mg2++CO===MgCO ↓
3
C.操作3是加热、蒸发、结晶
D.操作1~3总共需两次过滤
答案 C
解析 提纯含少量氯化镁杂质的氯化钠,先加入过量氢氧化钠,将镁离子转
化为氢氧化镁沉淀,过滤之后,加入稀盐酸中和过量的氢氧化钠,然后对氯化钠
溶液进行蒸发浓缩、冷却、结晶。由流程图可知操作1是加水溶解,将固体溶于水,
A错误;加入试剂①是将镁离子转化为沉淀,由于碳酸镁微溶于水,所以试剂①
应该为氢氧化钠溶液,将镁离子转化为氢氧化镁沉淀,离子方程式为:Mg2++
2OH-===Mg(OH) ↓,B错误;由分析可知,加入试剂②稀盐酸后得到氯化钠溶液,
2
对氯化钠溶液加热蒸发、结晶,得到氯化钠晶体,C正确;由分析可知,操作1~3中只有操作2为过滤,只有1次,D错误。
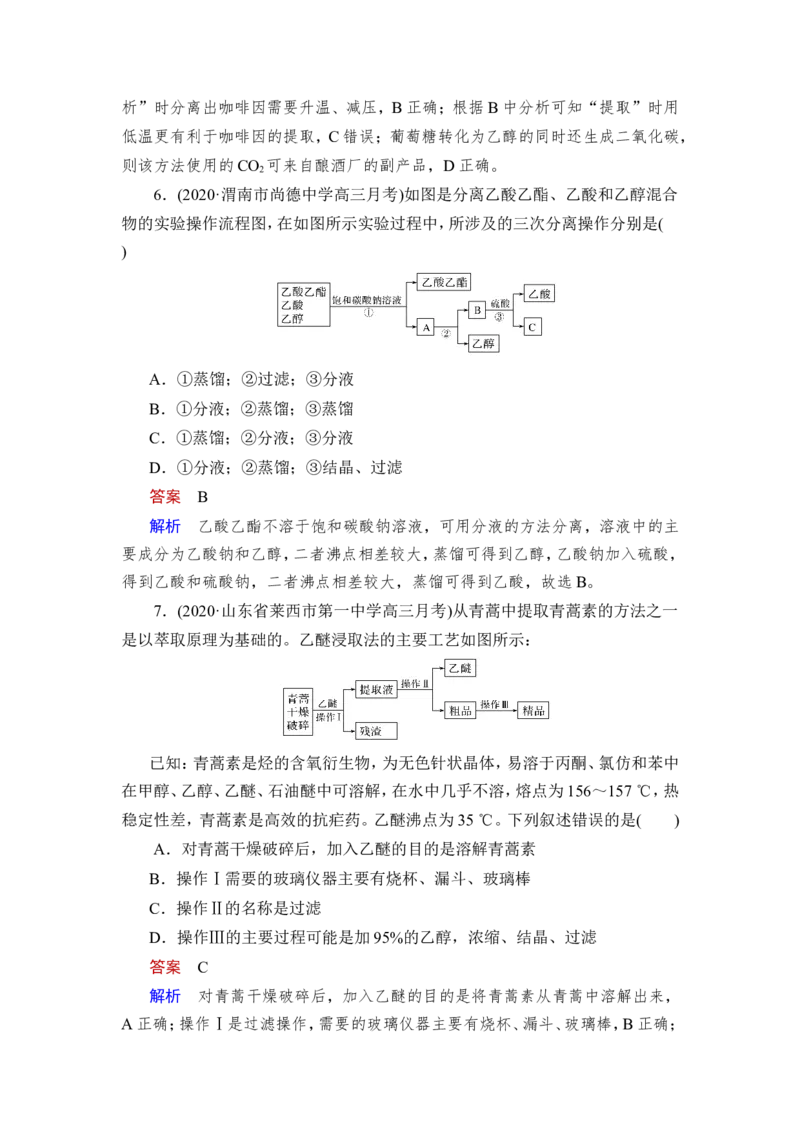
4.(2020·上海市光明中学高三期中)海藻中含有丰富的、化合态的碘元素。如
图是实验室从海藻里提取碘的流程的一部分:
下列判断正确的是( )
A.步骤①、③的操作分别是过滤、萃取分液
B.可用淀粉溶液检验步骤②的反应是否进行完全
C.步骤③中加入的有机溶剂是裂化汽油或乙醇
D.步骤④的操作是加热蒸发
答案 A
解析 分离固体和液体用过滤,从水溶液中提取碘一般用萃取的方法,步骤
①、③的操作分别是过滤、萃取分液,故A正确;淀粉遇到I 会变蓝色,遇碘离子
2
不变色,其不能确定碘离子的存在,因此不能用淀粉检验步骤②的反应是否进行
完全,故B错误;萃取剂不能和溶质反应,且萃取剂和原溶剂不能互溶,由于乙醇
能与水互溶,裂化汽油与碘单质反应,其不能做萃取剂,故C错误;碘易溶于有机
溶剂,应该用蒸馏的方法提取碘,步骤④的操作是蒸馏,故D错误。
5.(2020·濮阳县第一中学高三月考)超临界流体类似于液体,具有很强的流动
性和渗透性,利用超临界CO 流体(与水相似,溶解能力强)从咖啡豆中提取咖啡
2
因的流程如下图所示:
下列说法中错误的是( )
A.“提取”主要涉及的是咖啡因的萃取
B.“解析”时分离出咖啡因需要升温、减压
C.“提取”时用高温更有利于咖啡因的提取
D.该方法使用的CO 可来自酿酒厂的副产品
2
答案 C
解析 根据流程图可知最终得到的是咖啡因,因此“提取”主要涉及的是咖
啡因的萃取,A正确;二氧化碳的溶解度随温度升高、压强降低而减小,则“解析”时分离出咖啡因需要升温、减压,B正确;根据B中分析可知“提取”时用
低温更有利于咖啡因的提取,C错误;葡萄糖转化为乙醇的同时还生成二氧化碳,
则该方法使用的CO 可来自酿酒厂的副产品,D正确。
2
6.(2020·渭南市尚德中学高三月考)如图是分离乙酸乙酯、乙酸和乙醇混合
物的实验操作流程图,在如图所示实验过程中,所涉及的三次分离操作分别是(
)
A.①蒸馏;②过滤;③分液
B.①分液;②蒸馏;③蒸馏
C.①蒸馏;②分液;③分液
D.①分液;②蒸馏;③结晶、过滤
答案 B
解析 乙酸乙酯不溶于饱和碳酸钠溶液,可用分液的方法分离,溶液中的主
要成分为乙酸钠和乙醇,二者沸点相差较大,蒸馏可得到乙醇,乙酸钠加入硫酸,
得到乙酸和硫酸钠,二者沸点相差较大,蒸馏可得到乙酸,故选B。
7.(2020·山东省莱西市第一中学高三月考)从青蒿中提取青蒿素的方法之一
是以萃取原理为基础的。乙醚浸取法的主要工艺如图所示:
已知:青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中
在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157 ℃,热
稳定性差,青蒿素是高效的抗疟药。乙醚沸点为35 ℃。下列叙述错误的是( )
A.对青蒿干燥破碎后,加入乙醚的目的是溶解青蒿素
B.操作Ⅰ需要的玻璃仪器主要有烧杯、漏斗、玻璃棒
C.操作Ⅱ的名称是过滤
D.操作Ⅲ的主要过程可能是加95%的乙醇,浓缩、结晶、过滤
答案 C
解析 对青蒿干燥破碎后,加入乙醚的目的是将青蒿素从青蒿中溶解出来,
A正确;操作Ⅰ是过滤操作,需要的玻璃仪器主要有烧杯、漏斗、玻璃棒,B正确;操作Ⅱ是蒸馏,C错误;操作Ⅲ的主要过程是加95%的乙醇溶解,浓缩、结晶、过
滤得到精品,D正确。
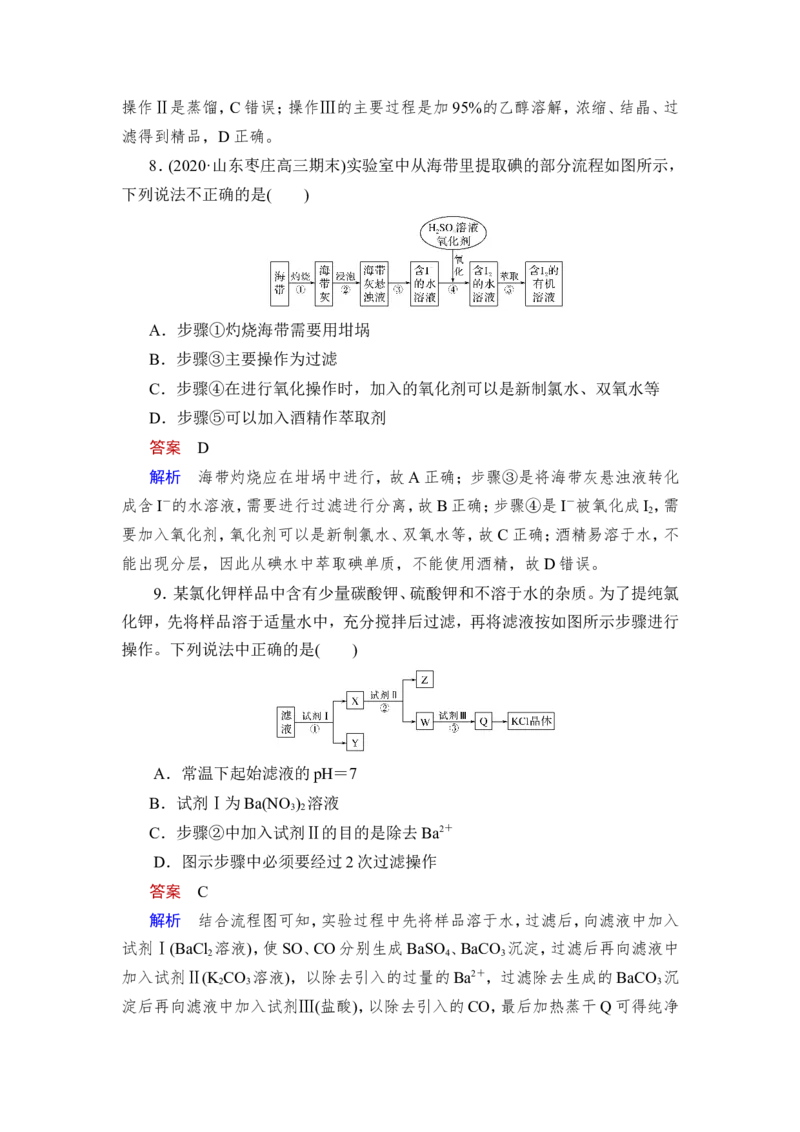
8.(2020·山东枣庄高三期末)实验室中从海带里提取碘的部分流程如图所示,
下列说法不正确的是( )
A.步骤①灼烧海带需要用坩埚
B.步骤③主要操作为过滤
C.步骤④在进行氧化操作时,加入的氧化剂可以是新制氯水、双氧水等
D.步骤⑤可以加入酒精作萃取剂
答案 D
解析 海带灼烧应在坩埚中进行,故A正确;步骤③是将海带灰悬浊液转化
成含I-的水溶液,需要进行过滤进行分离,故B正确;步骤④是I-被氧化成I ,需
2
要加入氧化剂,氧化剂可以是新制氯水、双氧水等,故C正确;酒精易溶于水,不
能出现分层,因此从碘水中萃取碘单质,不能使用酒精,故D错误。
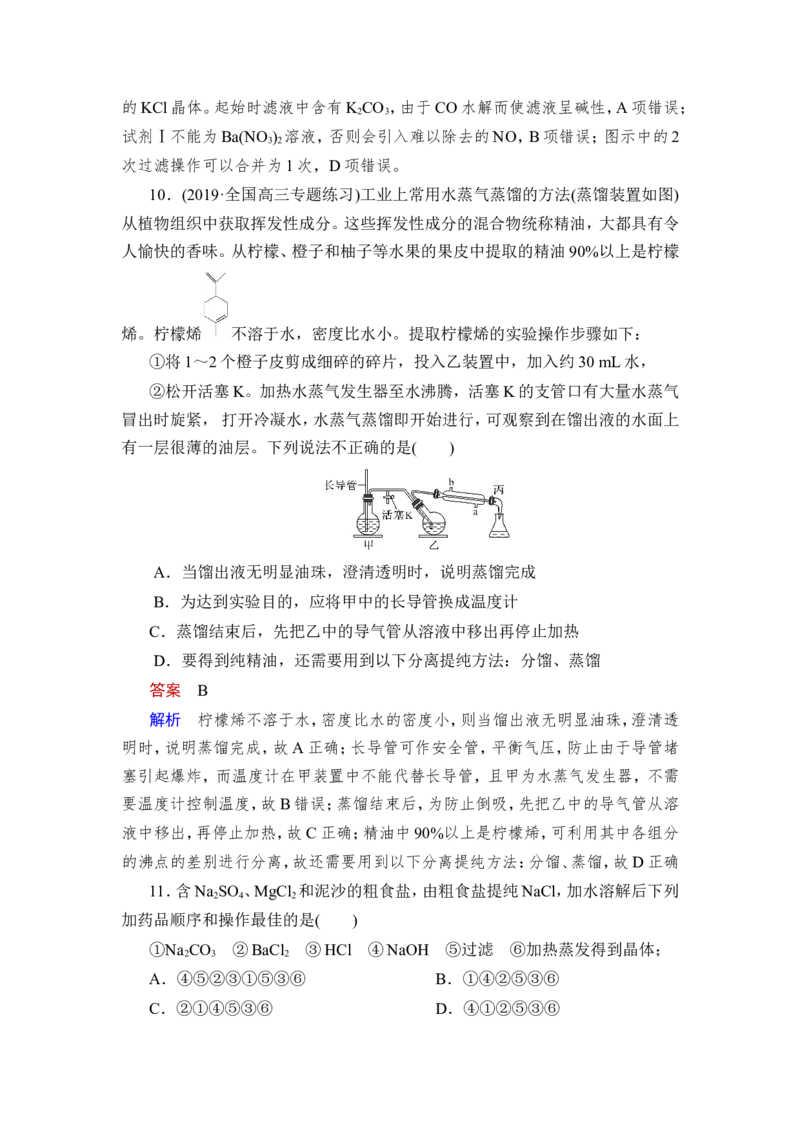
9.某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯
化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行
操作。下列说法中正确的是( )
A.常温下起始滤液的pH=7
B.试剂Ⅰ为Ba(NO ) 溶液
3 2
C.步骤②中加入试剂Ⅱ的目的是除去Ba2+
D.图示步骤中必须要经过2次过滤操作
答案 C
解析 结合流程图可知,实验过程中先将样品溶于水,过滤后,向滤液中加入
试剂Ⅰ(BaCl 溶液),使SO、CO分别生成BaSO 、BaCO 沉淀,过滤后再向滤液中
2 4 3
加入试剂Ⅱ(K CO 溶液),以除去引入的过量的Ba2+,过滤除去生成的BaCO 沉
2 3 3
淀后再向滤液中加入试剂Ⅲ(盐酸),以除去引入的CO,最后加热蒸干Q可得纯净的KCl晶体。起始时滤液中含有K CO ,由于CO水解而使滤液呈碱性,A项错误;
2 3
试剂Ⅰ不能为Ba(NO ) 溶液,否则会引入难以除去的NO,B项错误;图示中的2
3 2
次过滤操作可以合并为1次,D项错误。
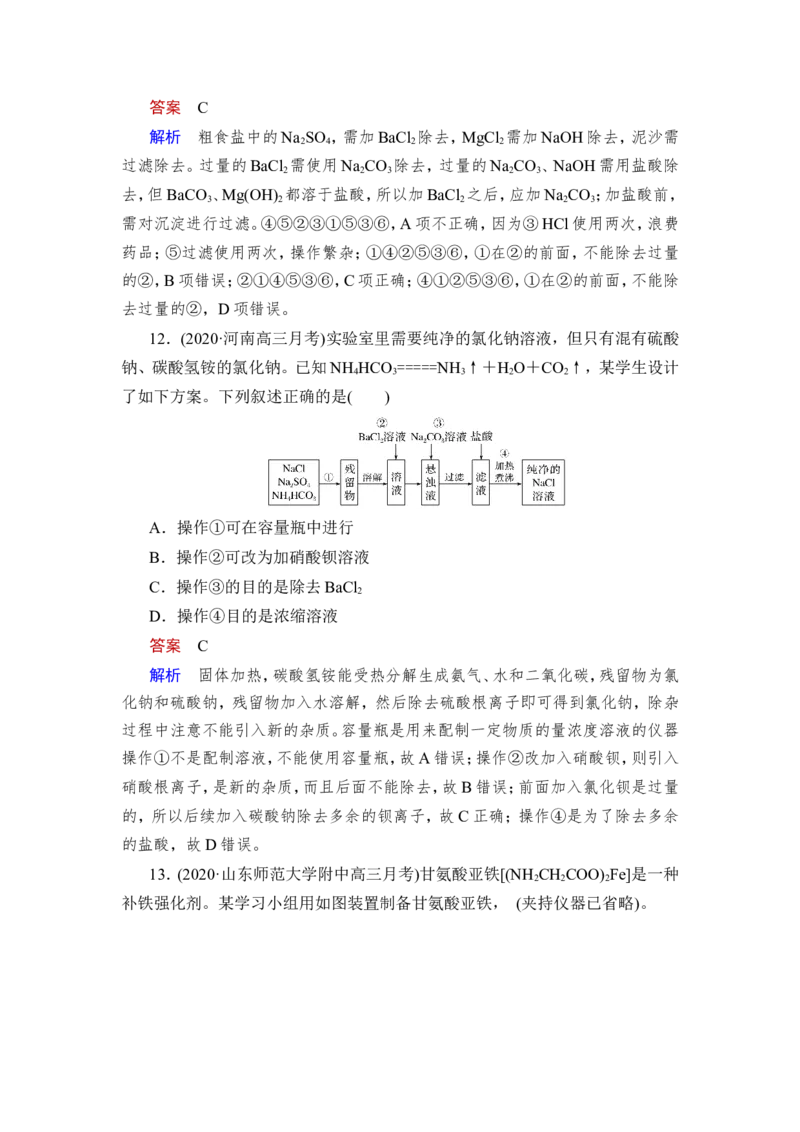
10.(2019·全国高三专题练习)工业上常用水蒸气蒸馏的方法(蒸馏装置如图)
从植物组织中获取挥发性成分。这些挥发性成分的混合物统称精油,大都具有令
人愉快的香味。从柠檬、橙子和柚子等水果的果皮中提取的精油90%以上是柠檬
烯。柠檬烯 不溶于水,密度比水小。提取柠檬烯的实验操作步骤如下:
①将1~2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30 mL水,
②松开活塞K。加热水蒸气发生器至水沸腾,活塞K的支管口有大量水蒸气
冒出时旋紧, 打开冷凝水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上
有一层很薄的油层。下列说法不正确的是( )
A.当馏出液无明显油珠,澄清透明时,说明蒸馏完成
B.为达到实验目的,应将甲中的长导管换成温度计
C.蒸馏结束后,先把乙中的导气管从溶液中移出再停止加热
D.要得到纯精油,还需要用到以下分离提纯方法:分馏、蒸馏
答案 B
解析 柠檬烯不溶于水,密度比水的密度小,则当馏出液无明显油珠,澄清透
明时,说明蒸馏完成,故A正确;长导管可作安全管,平衡气压,防止由于导管堵
塞引起爆炸,而温度计在甲装置中不能代替长导管,且甲为水蒸气发生器,不需
要温度计控制温度,故B错误;蒸馏结束后,为防止倒吸,先把乙中的导气管从溶
液中移出,再停止加热,故C正确;精油中90%以上是柠檬烯,可利用其中各组分
的沸点的差别进行分离,故还需要用到以下分离提纯方法:分馏、蒸馏,故D正确
11.含Na SO 、MgCl 和泥沙的粗食盐,由粗食盐提纯NaCl,加水溶解后下列
2 4 2
加药品顺序和操作最佳的是( )
①Na CO ②BaCl ③HCl ④NaOH ⑤过滤 ⑥加热蒸发得到晶体;
2 3 2
A.④⑤②③①⑤③⑥ B.①④②⑤③⑥
C.②①④⑤③⑥ D.④①②⑤③⑥答案 C
解析 粗食盐中的Na SO ,需加BaCl 除去,MgCl 需加NaOH除去,泥沙需
2 4 2 2
过滤除去。过量的BaCl 需使用Na CO 除去,过量的Na CO 、NaOH需用盐酸除
2 2 3 2 3
去,但BaCO 、Mg(OH) 都溶于盐酸,所以加BaCl 之后,应加Na CO ;加盐酸前,
3 2 2 2 3
需对沉淀进行过滤。④⑤②③①⑤③⑥,A项不正确,因为③HCl使用两次,浪费
药品;⑤过滤使用两次,操作繁杂;①④②⑤③⑥,①在②的前面,不能除去过量
的②,B项错误;②①④⑤③⑥,C项正确;④①②⑤③⑥,①在②的前面,不能除
去过量的②,D项错误。
12.(2020·河南高三月考)实验室里需要纯净的氯化钠溶液,但只有混有硫酸
钠、碳酸氢铵的氯化钠。已知NH HCO =====NH ↑+H O+CO ↑,某学生设计
4 3 3 2 2
了如下方案。下列叙述正确的是( )
A.操作①可在容量瓶中进行
B.操作②可改为加硝酸钡溶液
C.操作③的目的是除去BaCl
2
D.操作④目的是浓缩溶液
答案 C
解析 固体加热,碳酸氢铵能受热分解生成氨气、水和二氧化碳,残留物为氯
化钠和硫酸钠,残留物加入水溶解,然后除去硫酸根离子即可得到氯化钠,除杂
过程中注意不能引入新的杂质。容量瓶是用来配制一定物质的量浓度溶液的仪器
操作①不是配制溶液,不能使用容量瓶,故A错误;操作②改加入硝酸钡,则引入
硝酸根离子,是新的杂质,而且后面不能除去,故B错误;前面加入氯化钡是过量
的,所以后续加入碳酸钠除去多余的钡离子,故C正确;操作④是为了除去多余
的盐酸,故D错误。
13.(2020·山东师范大学附中高三月考)甘氨酸亚铁[(NH CH COO) Fe]是一种
2 2 2
补铁强化剂。某学习小组用如图装置制备甘氨酸亚铁, (夹持仪器已省略)。有关物质性质如表:
易溶于水,微溶于乙醇、冰醋酸,在冰醋酸中的溶
甘氨酸(H NCH COOH)
2 2
解度大于在乙醇中的溶解度
柠檬酸 易溶于水和乙醇,酸性较强,有强还原性
甘氨酸亚铁 易溶于水,难溶于乙醇、冰醋酸
实验步骤如下:
Ⅰ.打开K 和K ,向c中通入气体,待确定c中空气被排尽后,将b中溶液加
1 3
入到c中。
Ⅱ.在50 ℃恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加NaOH溶液,
调节溶液pH至5.5左右,使反应物充分反应。
Ⅲ.反应完成后,向c中反应混合物中加入无水乙醇,生成白色沉淀,将沉淀过
滤、洗涤得到粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器a的名称是________;与a相比,仪器A的优点是
_____________________________________________________________。
d装置的作用是________________________________________________。
(2)步骤Ⅰ中将b中溶液加入到c中的具体操作是
_____________________________________________________________。
步骤Ⅱ中若调节pH偏高,则所得粗产品中会混有的杂质________(写化学
式)。
(3)下列关于该实验的说法错误的是________(填写序号)。
a.步骤Ⅰ中可由d中导管冒出气泡的快慢来判断装置中的空气是否排尽
b.反应混合液中加入柠檬酸的作用是防止Fe2+被氧化
c.步骤Ⅲ中加入无水乙醇的作用是降低甘氨酸亚铁的溶解度
d.步骤Ⅲ中沉淀洗涤时,用蒸馏水作洗涤剂
答案 (1)分液漏斗 平衡气压,使液体顺利流下 防止空气进入装置c中氧
化甘氨酸亚铁
(2)关闭K ,打开K Fe(OH) (3)ad
3 2 2解析 由实验装置图可知,制备甘氨酸亚铁时应先打开K 、K ,铁屑与稀硫
1 3
酸反应生成硫酸亚铁同时产生氢气,将装置内的空气排尽;之后关闭 K ,打开
3
K ,通过产生的气体将b中溶液压入盛放甘氨酸和少量柠檬酸的c中;在50 ℃恒
2
温条件下用磁力搅拌器不断搅拌,然后向c中滴加NaOH溶液,调溶液pH至5.5
左右,使反应物充分反应,反应完成后加入无水乙醇,降低甘氨酸亚铁的溶解度,
从而使其析出得到的产品。
(1)根据仪器a的结构特点可知其为分液漏斗;仪器 A中分液漏斗中液体上
部和下部连通,可以平衡气压,使液体顺利流下;甘氨酸亚铁含有亚铁离子,易被
空气中的氧气氧化,装置d用水形成液封,可以防止空气进入装置c中氧化甘氨
酸亚铁;
(2)步骤Ⅰ中将b中溶液加入到c中的操作是:关闭K ,打开K ,铁屑与稀硫
3 2
酸反应生成的氢气使蒸馏烧瓶中的压强增大,将b中溶液压入c中;步骤Ⅱ中若
调节溶液pH偏高,硫酸亚铁可能与氢氧化钠溶液反应生成Fe(OH) 沉淀,导致粗
2
产品中会混有杂质;
(3)空气排尽后也会有氢气冒出,气泡产生的速率与空气是否排尽无关,故a
错误;根据题目信息可知柠檬酸具有还原性,可以防止亚铁离子被氧化,故b正
确;根据题目信息可知甘氨酸亚铁易溶于水,难溶于乙醇,所以加入乙醇可以降
低其溶解度,使其从溶液中析出,故c正确;甘氨酸亚铁易溶于水,用水洗涤会造
成大量产品损失,故d错误。