文档内容
第 01 讲 化学反应的热效应
目录
01 模拟基础练
【题型二】反应过程与能量变化
【题型二】反应热与能量变化图象分析
【题型二】反应热与键能
【题型二】热化学方程式书写及正误判断
【题型二】中和反应热测定
【题型二】盖斯定律及应用
02 重难创新练
03 真题实战练
题型一 反应过程与能量变化
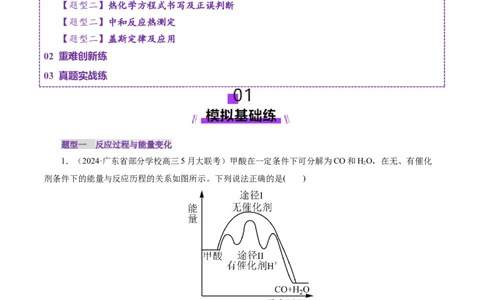
1.(2024·广东省部分学校高三5月大联考)甲酸在一定条件下可分解为CO和HO,在无、有催化
2
剂条件下的能量与反应历程的关系如图所示。下列说法正确的是( )
A.该反应的活化能为甲酸分子的键能之和
B.其他条件不变,按途径Ⅰ进行的反应热效应更大
C. 中键能之和比 中键能之和大
D.途径Ⅱ的决速步骤为放热过程
2.丙烷与溴原子能发生以下两种反应:
①CHCHCH(g)+Br·(g) CHCHCH·(g)+HBr(g)。
3 2 3 3 2 2②CHCHCH(g)+Br·(g) CHCH·CH (g)+HBr(g)。
3 2 3 3 3
反应过程的能量变化如图所示。下列说法正确的是( )
A.反应①是放热反应
B.反应②使用了催化剂
C.产物中 CHCHCH·(g)的含量比CHCH·CH (g)低
3 2 2 3 3
D.CHCHCH·(g)转变为 CHCH·CH (g)时需要吸热
3 2 2 3 3
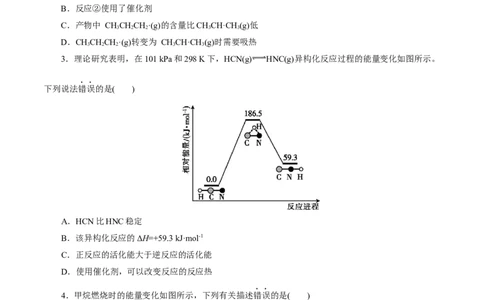
3.理论研究表明,在101 kPa和298 K下,HCN(g) HNC(g)异构化反应过程的能量变化如图所示。
下列说法错误的是( )
A.HCN比HNC稳定
B.该异构化反应的ΔH=+59.3 kJ·mol-1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
4.甲烷燃烧时的能量变化如图所示,下列有关描述错误的是( )
A.反应①和反应②均为放热反应
B.等物质的量时,CO 具有的能量比CO低
2C.由图像可以推得:2CO(g)+O(g)=2CO (g) ΔH=-283 kJ·mol-1
2 2
3
D.反应②的热化学方程式为CH(g)+ O(g)=CO(g)+2HO(l) ΔH=-607.3 kJ·mol-1
4 2 2 2
5.已知:①S(g) +O (g)=SO(g) ΔH,②S(s)+O (g)=SO(g) ΔH。下列说法正确的是( )
2 2 1 2 2 2
A.硫燃烧过程中将化学能全部转化为热能
B.相同条件下,1 mol S(s)比1 mol S(g) 燃烧更剧烈
C.两个过程的能量变化可用上图表示,ΔH<ΔH<0
1 2
D.两个反应中反应物的总键能都比生成物的总键能小
题型二 反应热与能量变化图象分析
6.某反应2A=3B,它的反应能量变化曲线如图所示,下列有关叙述正确的是( )
A.该反应为吸热反应 B.A比B更稳定
C.加入催化剂会改变反应的焓变 D.整个反应的ΔH=E -E
1 2
7.工业上常利用CO 和NH 合成尿素[CO(NH)],该可逆反应分两步进行,整个过程中的能量变化如
2 3 2 2
图所示。下列说法错误的是( )
A.NH COONH 为合成尿素反应的中间产物
2 4
B.反应Ⅰ逆反应的活化能>反应Ⅱ正反应的活化能
C.反应Ⅱ在热力学上进行趋势较小D.2NH (g)+CO (g) CO(NH)(l)+H O(l)的ΔH=E-E
3 2 2 2 2 1 2
8.H 与ICl的反应分①②两步进行,其能量曲线如图所示。下列有关说法错误的是( )
2
A.反应①、反应②均为放热反应
B.反应①、反应②均为氧化还原反应
C.反应①比反应②的速率慢,与相应正反应的活化能无关
D.反应①、反应②的焓变之和为ΔH=-218 kJ·mol-1
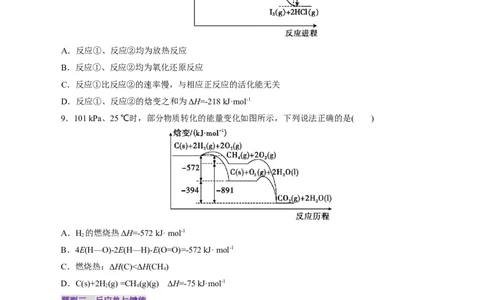
9.101 kPa、25 ℃时,部分物质转化的能量变化如图所示,下列说法正确的是( )
A.H 的燃烧热ΔH=-572 kJ· mol-1
2
B.4E(H—O)-2E(H—H)-E(O=O)=-572 kJ· mol-1
C.燃烧热:ΔH(C)<ΔH(CH)
4
D.C(s)+2H(g) =CH (g)(g) ΔH=-75 kJ·mol-1
2 4
题型三 反应热与键能
10.(2024·湖北省部分学校高三三模)如表所示为部分化学键的键能数据,由键能数据大小,不能解
释下列事实的是( )
化学键
键能/( kJ·mol−1) 413 348 745 326 318 226 452 347
A.硬度:金刚石 碳化硅
B.熔、沸点:金刚石>CO
2
C.SiH 的稳定性小于CH,更易生成氧化物
4 4D.硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多
11.已知H(g)+Br (l)=2HBr(g) ΔH=-72 kJ·mol-1。蒸发1 mol Br (l)需要吸收的能量为30 kJ,其他相关
2 2 2
数据如下表所示:
共价键 H—H H—Br
键能/(kJ·mol-1) 436 369
下列说法正确的是( )
A.Br (l)=Br (g) ΔH=-30kJ·mol-1
2 2
B.2Br(g)=Br (g) ΔH=230 kJ·mol-1
2
C.2HBr(g)=H (g)+Br (g) ΔH=+102 kJ·mol-1
2 2
D.H(g)+Br (l)=2HBr(g) ΔH=-72 kJ·mol-1表示一个氢气分子和一个液溴分子完全反应放出72 kJ热量
2 2
12.标准状态下,1mol纯物质的相对能量及解离为气态原子时所消耗的能量如下表所示:
物质 O(g) N(g) NO g) C(s,石墨) CH(g) CO(g)
2 2 2 4 2
相对能量/ kJ·mol−1 0 0 x 0 -75 -393.5
解离总耗能/kJ 498 946 632 717 1656 y
下列说法正确的是( )
A.x =180
B.逐级断开CH(g)中的每摩尔C—H所消耗的能量均为414kJ
4
C.解离每摩尔C(s,石墨)中的碳碳键平均耗能为239kJ
D.根据NO(g)+CH(g) CO(g)+N(g)+2H O(g)的ΔH可计算出H—O键能
4 2 2
13.(2024·浙江省义乌中学高三适应性考试)标准状态下,气态反应物、生成物及活化分子[A(B)表示
“A+B→产物”的活化分子]的相对能量如表所示:
物质 NO(g) NO (g) SO (g) SO (g) O(g) O(g) NO(O) SO (O )
2 2 3 2 3 3 2 3
相对能量/ 91.3 33.2 -296.8 -395.7 0 142.7 237.2 -96.1
下列说法不正确的是( )
A.NO (g)+SO (g) NO (g)+ SO (g) ΔH=-40.8 kJ·mol-1
2 2 3
B.3O(g) 2O(g)反应不能自发进行
2 3
C.相同条件下,SO (g)+O(g) O (g)+ SO (g)比NO (g)+O(g) O (g)+ NO (g)速率快
2 3 2 3 3 2 2
D.1mol NO (g)的总键能大于1mol NO(g)总键能
2
14.(2024·江西省九江市十校高三联考)有机物a、b、c、d分别与氢气发生加成反应生成1mol环己烷(
)的能量变化如图所示,下列推理正确的是( )A.由ΔH 的值可知,a分子中碳碳双键的键能为120kJ/mol
1
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,不利于物质稳定
2 3
C.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
题型四 热化学方程式书写及正误判断
15.已知一定温度和压强下:2H(g)+O(g)=2HO(g) ΔH=-a kJ·mol-1。下列叙述不正确的是( )
2 2 2
A.2 mol H (g)和1 mol O (g)完全反应生成2 mol H O(g)时放出a kJ的热量
2 2 2
B.2 mol H O(g)完全分解为2 mol H (g)和1 mol O (g)时吸收a kJ的热量
2 2 2
C.2 mol H (g)和1 mol O (g)完全反应生成2 mol H O(l)时放出的热量小于a kJ
2 2 2
D.1 mol H (g)和0.5 mol O(g)完全反应生成1 mol H O(g)时放出0.5a kJ的热量
2 2 2
16.工业生产硫酸过程中,SO 在接触室中被催化氧化为SO 气体,已知该反应为放热反应。现将2
2 3
mol SO 、1 mol O 充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO 的转化率为50%,则下列
2 2 2
热化学方程式正确的是( )
A.2SO (g)+O(g) 2SO (g) ΔH=+196.6 kJ·mol-1
2 2 3
B.2SO (g)+O(g) 2SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
C.SO (g)+ O(g) SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
D.SO (g)+ O(g) SO (g) ΔH=-196.6 kJ·mol-1
2 2 3
17.工业生产硫酸过程中,SO 在接触室中被催化氧化为SO 气体,已知该反应为放热反应。现将2
2 3
mol SO 、1 mol O 充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO 的转化率为50%,则下列
2 2 2
热化学方程式正确的是( )
A.2SO (g)+O(g) 2SO (g) ΔH=+196.6 kJ·mol-1
2 2 3
B.2SO (g)+O(g) 2SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
C.SO (g)+ O(g) SO (g) ΔH=-98.3 kJ·mol-1
2 2 3D.SO (g)+ O(g) SO (g) ΔH=-196.6 kJ·mol-1
2 2 3
18.根据如图所给信息,得出的结论正确的是( )
A.48 g碳完全燃烧放出热量为1 574 kJ/mol
B.2C(s)+O(g)===2CO(g) ΔH=-221.0 kJ/mol
2
C.2CO(g)===2CO(g)+O(g) ΔH=+283.0 kJ/mol
2 2
D.C(s)+O(g)===CO (s) ΔH=-393.5 kJ/mol
2 2
19.“嫦娥”五号预计在海南文昌发射中心发射,火箭的第一、二级发动机中,所用的燃料为偏二甲
肼和四氧化二氮,偏二甲肼可用肼来制备。用肼(N H)作燃料,四氧化二氮作氧化剂,二者反应生成氮气
2 4
和气态水。已知:
①N(g)+2O(g)===N O(g) ΔH=+10.7 kJ·mol-1
2 2 2 4
②NH(g)+O(g)===N (g)+2HO(g) ΔH=-543 kJ·mol-1
2 4 2 2 2
写出气态肼和NO 反应的热化学方程式: 。
2 4
20.(1)化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物
的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:
NO 和CO反应生成CO 和NO过程中能量变化示意图如图所示,请写出NO 和CO反应的热化学方程
2 2 2
式: 。
(2)CO 的回收与利用是科学家研究的热点课题,可利用CH 与CO 制备“合成气”(CO、H),还可制
2 4 2 2
备甲醇、二甲醚、碳基燃料等产品。
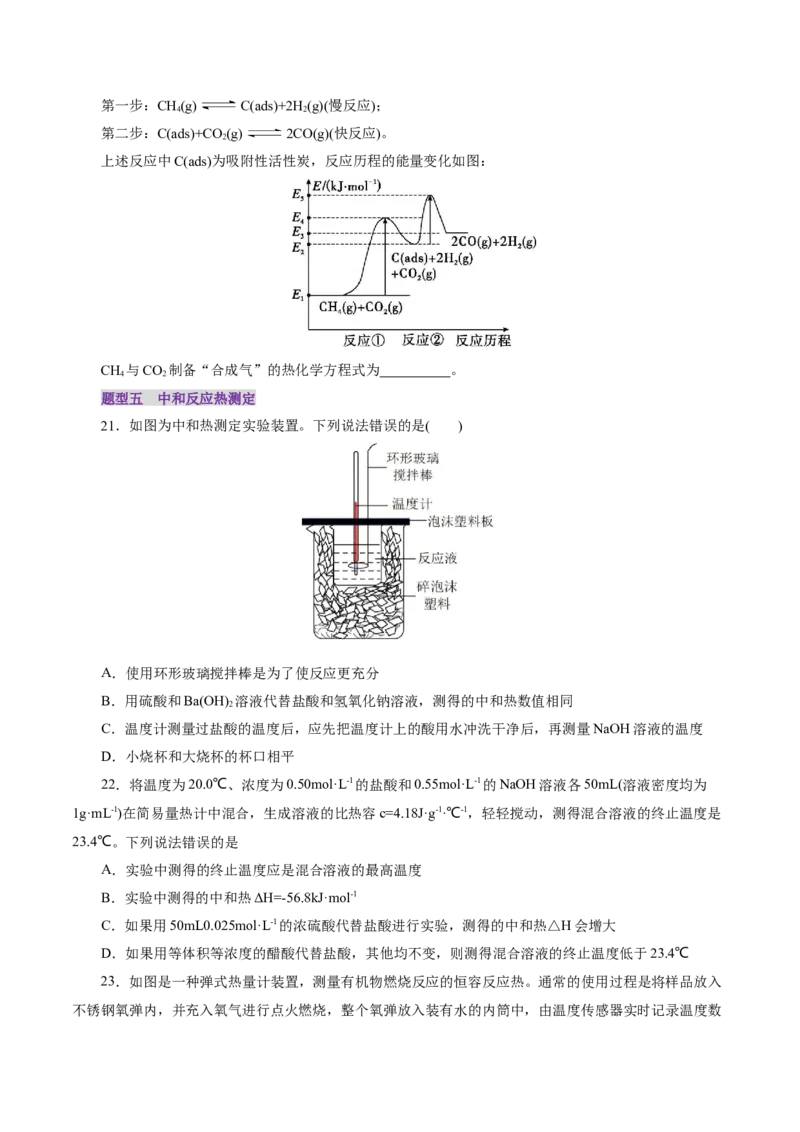
科学家提出制备“合成气”反应历程分两步:第一步:CH(g) C(ads)+2H(g)(慢反应);
4 2
第二步:C(ads)+CO (g) 2CO(g)(快反应)。
2
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
CH 与CO 制备“合成气”的热化学方程式为 。
4 2
题型五 中和反应热测定
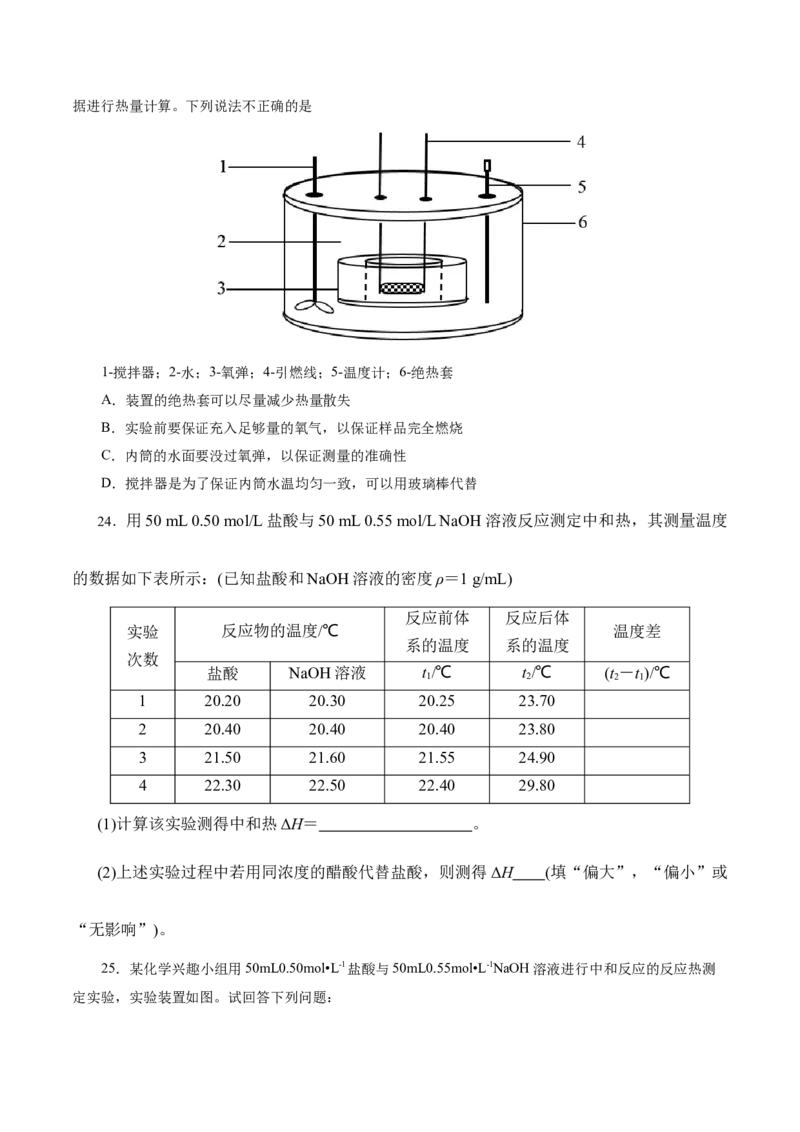
21.如图为中和热测定实验装置。下列说法错误的是( )
A.使用环形玻璃搅拌棒是为了使反应更充分
B.用硫酸和Ba(OH) 溶液代替盐酸和氢氧化钠溶液,测得的中和热数值相同
2
C.温度计测量过盐酸的温度后,应先把温度计上的酸用水冲洗干净后,再测量NaOH溶液的温度
D.小烧杯和大烧杯的杯口相平
22.将温度为20.0℃、浓度为0.50mol·L-1的盐酸和0.55mol·L-1的NaOH溶液各50mL(溶液密度均为
1g·mL-1)在简易量热计中混合,生成溶液的比热容c=4.18J·g-1·℃-1,轻轻搅动,测得混合溶液的终止温度是
23.4℃。下列说法错误的是
A.实验中测得的终止温度应是混合溶液的最高温度
B.实验中测得的中和热ΔH=-56.8kJ·mol-1
C.如果用50mL0.025mol·L-1的浓硫酸代替盐酸进行实验,测得的中和热△H会增大
D.如果用等体积等浓度的醋酸代替盐酸,其他均不变,则测得混合溶液的终止温度低于23.4℃
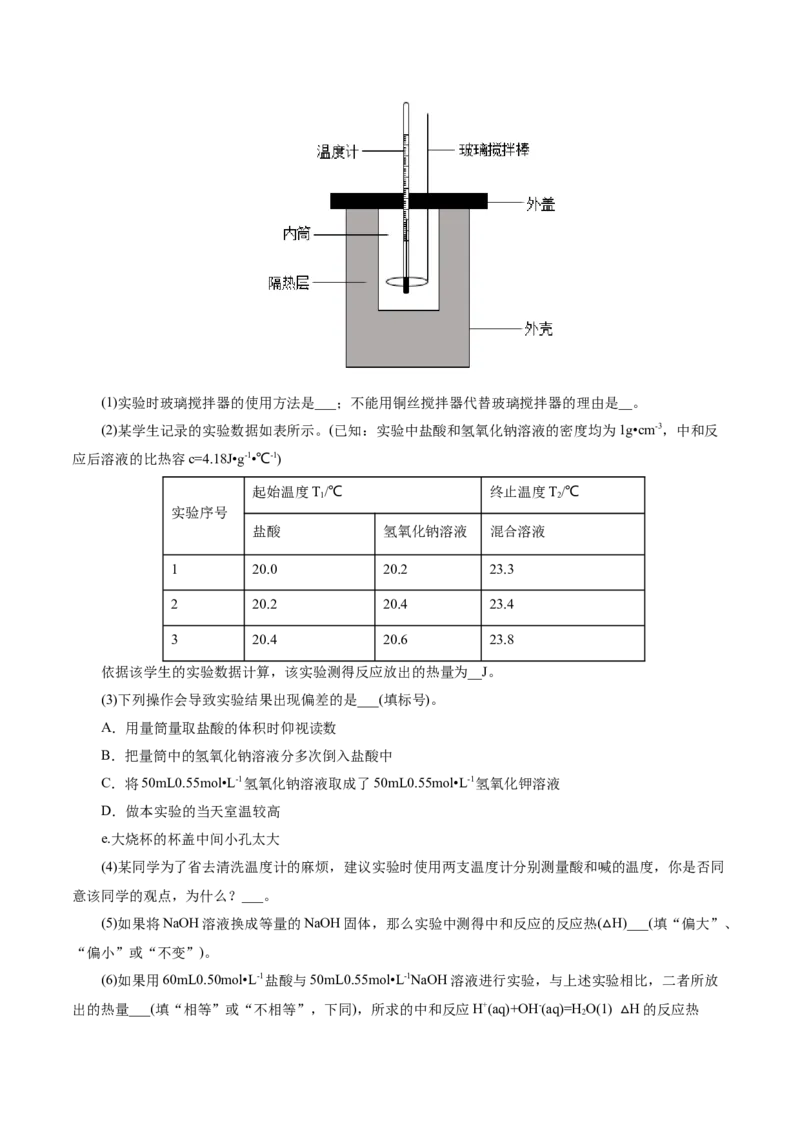
23.如图是一种弹式热量计装置,测量有机物燃烧反应的恒容反应热。通常的使用过程是将样品放入
不锈钢氧弹内,并充入氧气进行点火燃烧,整个氧弹放入装有水的内筒中,由温度传感器实时记录温度数据进行热量计算。下列说法不正确的是
1-搅拌器;2-水;3-氧弹;4-引燃线;5-温度计;6-绝热套
A.装置的绝热套可以尽量减少热量散失
B.实验前要保证充入足够量的氧气,以保证样品完全燃烧
C.内筒的水面要没过氧弹,以保证测量的准确性
D.搅拌器是为了保证内筒水温均匀一致,可以用玻璃棒代替
24.用50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液反应测定中和热,其测量温度
的数据如下表所示:(已知盐酸和NaOH溶液的密度ρ=1 g/mL)
反应前体 反应后体
实验 反应物的温度/℃ 温度差
系的温度 系的温度
次数
盐酸 NaOH溶液 t /℃ t /℃ (t -t )/℃
1 2 2 1
1 20.20 20.30 20.25 23.70
2 20.40 20.40 20.40 23.80
3 21.50 21.60 21.55 24.90
4 22.30 22.50 22.40 29.80
(1)计算该实验测得中和热ΔH= 。
(2)上述实验过程中若用同浓度的醋酸代替盐酸,则测得ΔH (填“偏大”,“偏小”或
“无影响”)。
25.某化学兴趣小组用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行中和反应的反应热测
定实验,实验装置如图。试回答下列问题:(1)实验时玻璃搅拌器的使用方法是___;不能用铜丝搅拌器代替玻璃搅拌器的理由是__。
(2)某学生记录的实验数据如表所示。(已知:实验中盐酸和氢氧化钠溶液的密度均为1g•cm-3,中和反
应后溶液的比热容c=4.18J•g-1•℃-1)
起始温度T/℃ 终止温度T/℃
1 2
实验序号
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.2 23.3
2 20.2 20.4 23.4
3 20.4 20.6 23.8
依据该学生的实验数据计算,该实验测得反应放出的热量为__J。
(3)下列操作会导致实验结果出现偏差的是___(填标号)。
A.用量筒量取盐酸的体积时仰视读数
B.把量筒中的氢氧化钠溶液分多次倒入盐酸中
C.将50mL0.55mol•L-1氢氧化钠溶液取成了50mL0.55mol•L-1氢氧化钾溶液
D.做本实验的当天室温较高
e.大烧杯的杯盖中间小孔太大
(4)某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和喊的温度,你是否同
意该同学的观点,为什么?___。
(5)如果将NaOH溶液换成等量的NaOH固体,那么实验中测得中和反应的反应热( H)___(填“偏大”、
“偏小”或“不变”)。 △
(6)如果用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行实验,与上述实验相比,二者所放
出的热量___(填“相等”或“不相等”,下同),所求的中和反应H+(aq)+OH-(aq)=H O(1) H的反应热
2
△( H)___。
△ 题型六 盖斯定律及应用
26.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为S(s)+2KNO (s)+3C(s)=K S(s)+N (g)
3 2 2
+3CO (g) ΔH=x kJ·mol-1。
2
已知:碳的燃烧热ΔH=a kJ·mol-1;
1
S(s)+2K(s)=K S(s) ΔH=b kJ·mol-1;
2 2
2K(s)+N (g)+3O(g)=2KNO (s) ΔH=c kJ·mol-1。
2 2 3 3
则x为 ( )
A.3a+b-c B.c+3a-b C.a+b-c D.c+a-b
27.通过以下反应可获得新型能源二甲醚(CHOCH )。下列说法不正确的是( )
3 3
①C(s)+HO(g)=CO(g)+H (g) ΔH=a kJ·mol-1
2 2 1
②CO(g)+HO(g)=CO(g)+H(g) ΔH=b kJ·mol-1
2 2 2 2
③CO(g)+3H(g)=CH OH(g)+H O(g) ΔH=c kJ·mol-1
2 2 3 2 3
④2CHOH(g)=CH OCH (g)+HO(g) ΔH=d kJ·mol-1
3 3 3 2 4
A.反应①②为反应③提供原料气
B.反应③也是CO 资源化利用的方法之一
2
1 1 d
C.反应CHOH(g)= CHOCH (g)+ HO(l)的ΔH= kJ·mol-1
3 2 3 3 2 2 2
D.反应2CO(g)+4H(g)=CH OCH (g)+HO(g)的ΔH=(2b+2c+d) kJ·mol-1
2 3 3 2
28.已知室温下,将 CuSO ·5H O(s)溶于水会使溶液温度降低, 将 CuSO (s)溶于水会使溶液温度升
4 2 4
高。则下列能量转化关系的判断不正确的是
A. △H>0 B. △H>△H C. △H>△H D. △H= H+ H
1 2 3 3 1 2 1 3
△ △
29.2 mol金属钠和l mol氯气反应的能量关系如图所示,下列说法不正确的是( )A.原子失电子为吸热过程,相同条件下,K(s)的( H'+△H')-( H+△H)
2 3 4 5 6 7
D.2Na(s)+Cl
2
(g)=2NaCl(s)在较低△温度下自发进行
1.(2024·河北省石家庄市高三模拟)化学反应在有新物质生成的同时,一定伴随有能量的变化。下
列说法正确的是( )
A.已知H 的燃烧热为285.8kJ/mol,则表示H 燃烧热的热化学方程式为H(g)+ O(g)=HO(l)
2 2 2 2 2
H=-285.8kJ/mol
B.已知H+(aq)+OH—(ag)=H O(l) H=—57.3kJ/mol,用含49.0gH SO 的浓硫酸与足量稀NaOH溶液反
△ 2 2 4
应,放出57.3kJ热量 △
C.H(g)与O(g)充分反应生成等量的气态水比液态水放出的热量更多
2 2
D.已知I(g)+H(g) 2HI(g) H=-11kJ/mol,现将1molI (g)和1molH (g)充入密闭容器中充分反应
2 2 2 2
后,放出的热量为11 kJ △
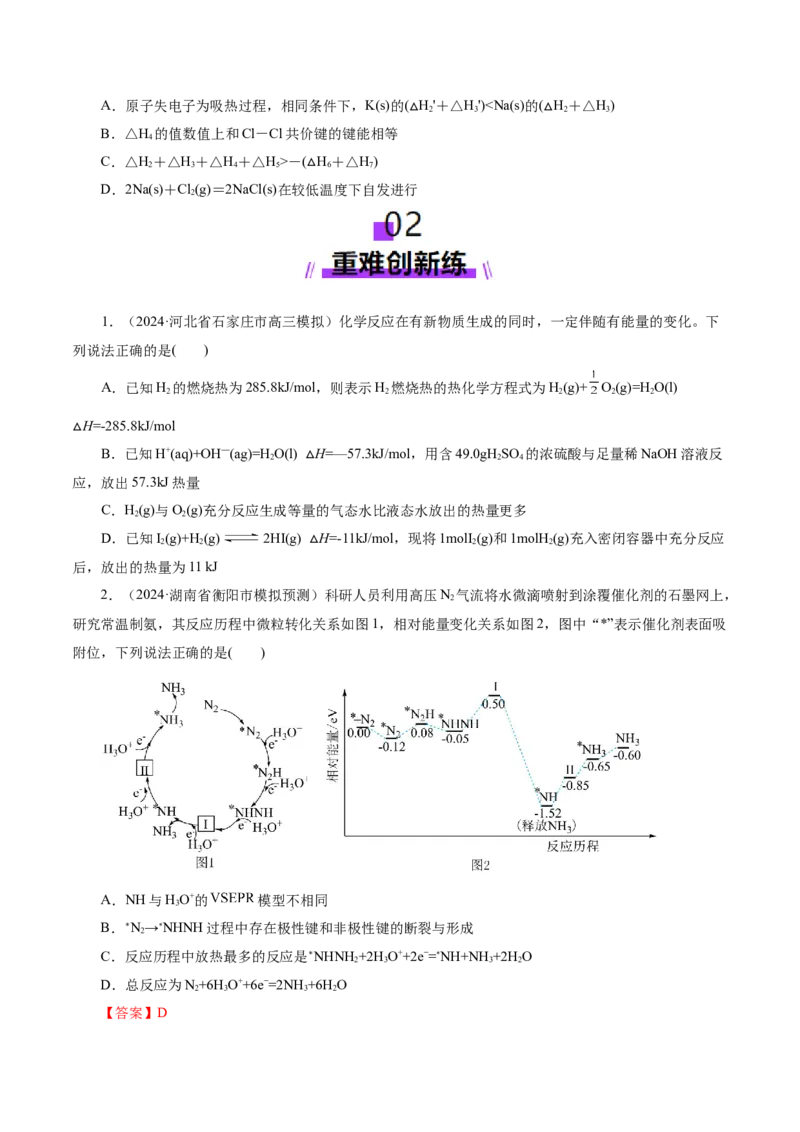
2.(2024·湖南省衡阳市模拟预测)科研人员利用高压N 气流将水微滴喷射到涂覆催化剂的石墨网上,
2
研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸
附位,下列说法正确的是( )
A.NH与HO+的 模型不相同
3
B.∗N→NHNH过程中存在极性键和非极性键的断裂与形成
2
∗
C.反应历程中放热最多的反应是∗NHNH +2H O++2e−=NH+NH +2H O
2 3 3 2
∗
D.总反应为N+6H O++6e−=2NH+6H O
2 3 3 2
【答案】D【解析】A项,NH 与HO+的中心原子N和O原子都是形成3根单键,并有一对孤对电子,价层电子
3 3
对数都是4,VSEPR模型,相同,A错误;B项,∗N→NHNH过程中,起始物质为∗N 和HO+,有非极性
2 2 3
∗
键氮氮三键和极性键氢氧键的断裂,氮氮三键未完全断开,故有极性键氮氢键的形成,但是没有非极性键
的形成,B错误;C项,由相对能量得,反应历程中放热最多的反应是∗NHNH +H O++e−=NH+NH +H O,
2 3 3 2
∗
C错误;D项,由图1知,总反应为N+6H O++6e−=2NH+6H O,D正确;故选D。
2 3 3 2
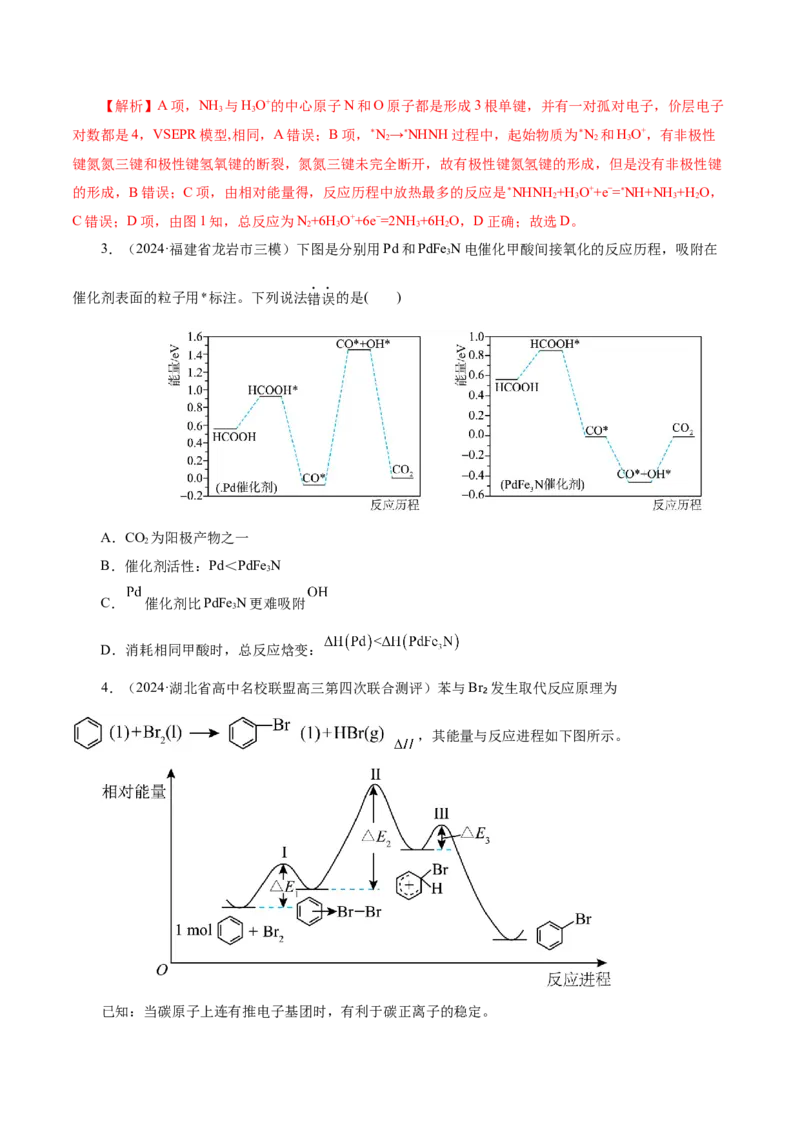
3.(2024·福建省龙岩市三模)下图是分别用Pd和PdFe N电催化甲酸间接氧化的反应历程,吸附在
3
催化剂表面的粒子用 标注。下列说法错误的是( )
A.CO 为阳极产物之一
2
B.催化剂活性:Pd<PdFe N
3
C. 催化剂比PdFe N更难吸附
3
D.消耗相同甲酸时,总反应焓变:
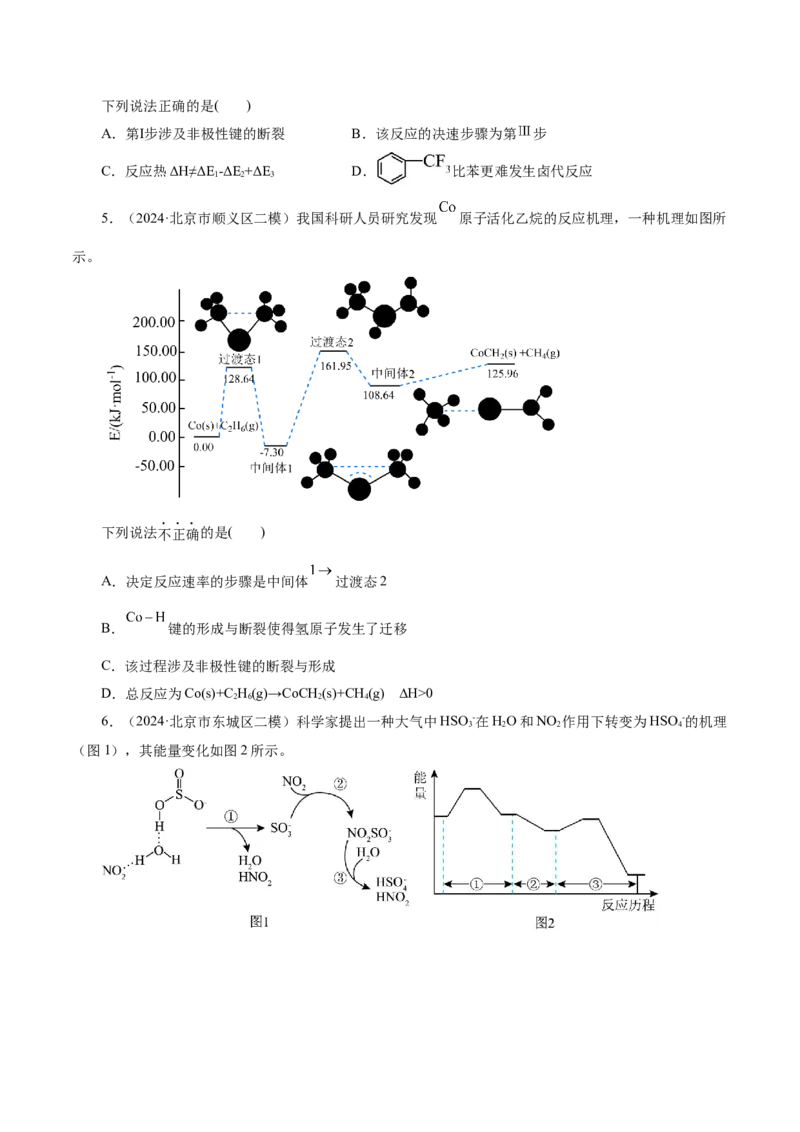
4.(2024·湖北省高中名校联盟高三第四次联合测评)苯与Br₂发生取代反应原理为
,其能量与反应进程如下图所示。
已知:当碳原子上连有推电子基团时,有利于碳正离子的稳定。下列说法正确的是( )
A.第I步涉及非极性键的断裂 B.该反应的决速步骤为第 步
C.反应热ΔH≠ΔE -ΔE +ΔE D. 比苯更难发生卤代反应
1 2 3
5.(2024·北京市顺义区二模)我国科研人员研究发现 原子活化乙烷的反应机理,一种机理如图所
示。
下列说法不正确的是( )
A.决定反应速率的步骤是中间体 过渡态2
B. 键的形成与断裂使得氢原子发生了迁移
C.该过程涉及非极性键的断裂与形成
D.总反应为Co(s)+C H(g)→CoCH(s)+CH(g) ∆H>0
2 6 2 4
6.(2024·北京市东城区二模)科学家提出一种大气中HSO -在HO和NO 作用下转变为HSO -的机理
3 2 2 4
(图1),其能量变化如图2所示。已知:NO SO -的结构式为
2 3
下列说法不正确的是( )
A.①中涉及O-H键的断裂与生成 B.②③均发生了氧化还原反应
C.由图2可知,该过程的决速步是① D.总反应中还原剂与氧化剂的物质的量之比为1:2
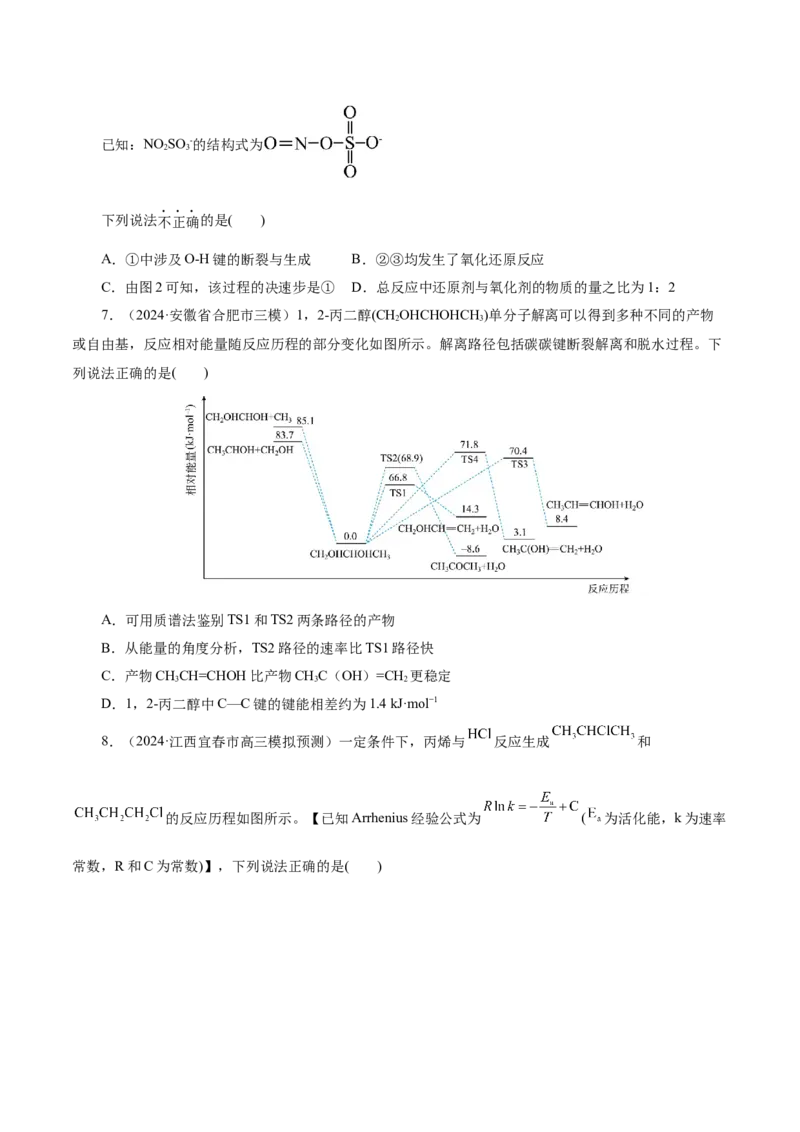
7.(2024·安徽省合肥市三模)1,2-丙二醇(CHOHCHOHCH )单分子解离可以得到多种不同的产物
2 3
或自由基,反应相对能量随反应历程的部分变化如图所示。解离路径包括碳碳键断裂解离和脱水过程。下
列说法正确的是( )
A.可用质谱法鉴别TS1和TS2两条路径的产物
B.从能量的角度分析,TS2路径的速率比TS1路径快
C.产物CHCH=CHOH比产物CHC(OH)=CH 更稳定
3 3 2
D.1,2-丙二醇中C—C键的键能相差约为1.4 kJ·mol−1
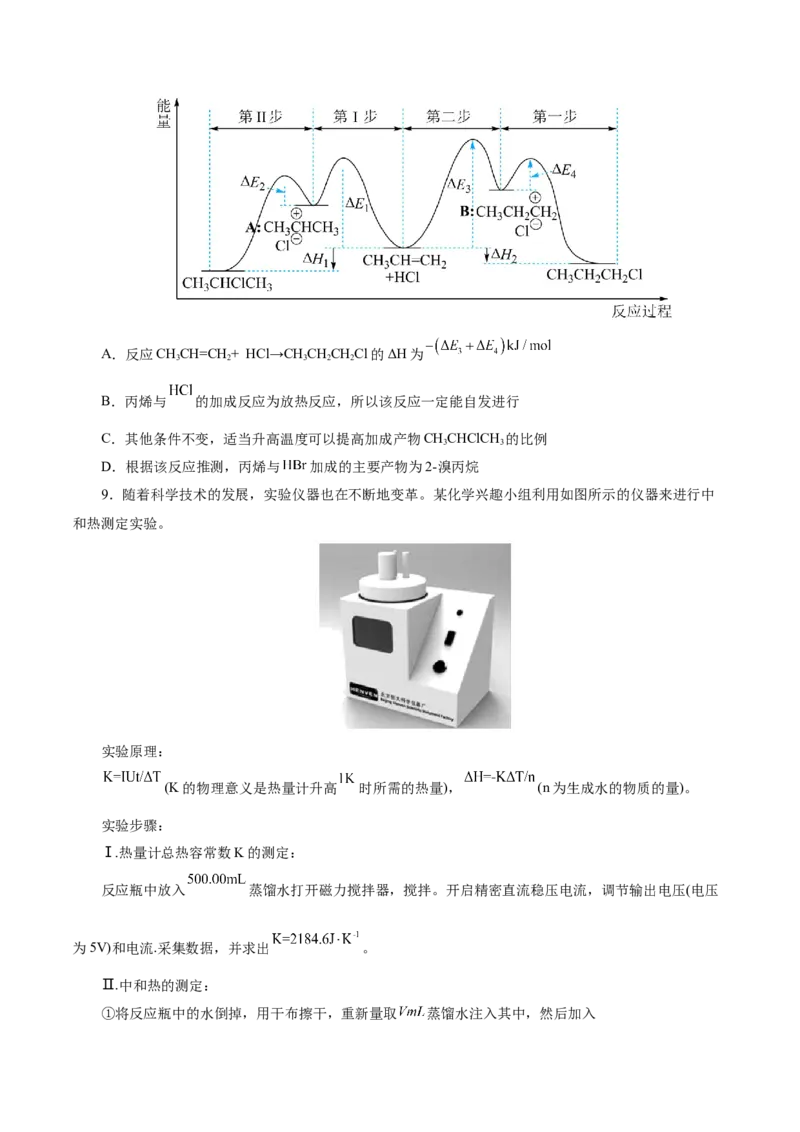
8.(2024·江西宜春市高三模拟预测)一定条件下,丙烯与 反应生成 和
的反应历程如图所示。【已知Arrhenius经验公式为 ( 为活化能,k为速率
常数,R和C为常数)】,下列说法正确的是( )A.反应CHCH=CH+ HCl→CHCHCHCl的ΔH为
3 2 3 2 2
B.丙烯与 的加成反应为放热反应,所以该反应一定能自发进行
C.其他条件不变,适当升高温度可以提高加成产物CHCHClCH 的比例
3 3
D.根据该反应推测,丙烯与 加成的主要产物为2-溴丙烷
9.随着科学技术的发展,实验仪器也在不断地变革。某化学兴趣小组利用如图所示的仪器来进行中
和热测定实验。
实验原理:
(K的物理意义是热量计升高 时所需的热量), (n为生成水的物质的量)。
实验步骤:
Ⅰ.热量计总热容常数K的测定:
反应瓶中放入 蒸馏水打开磁力搅拌器,搅拌。开启精密直流稳压电流,调节输出电压(电压
为5V)和电流.采集数据,并求出 。
Ⅱ.中和热的测定:
①将反应瓶中的水倒掉,用干布擦干,重新量取 蒸馏水注入其中,然后加入溶液,再取 溶液注入储液管中。
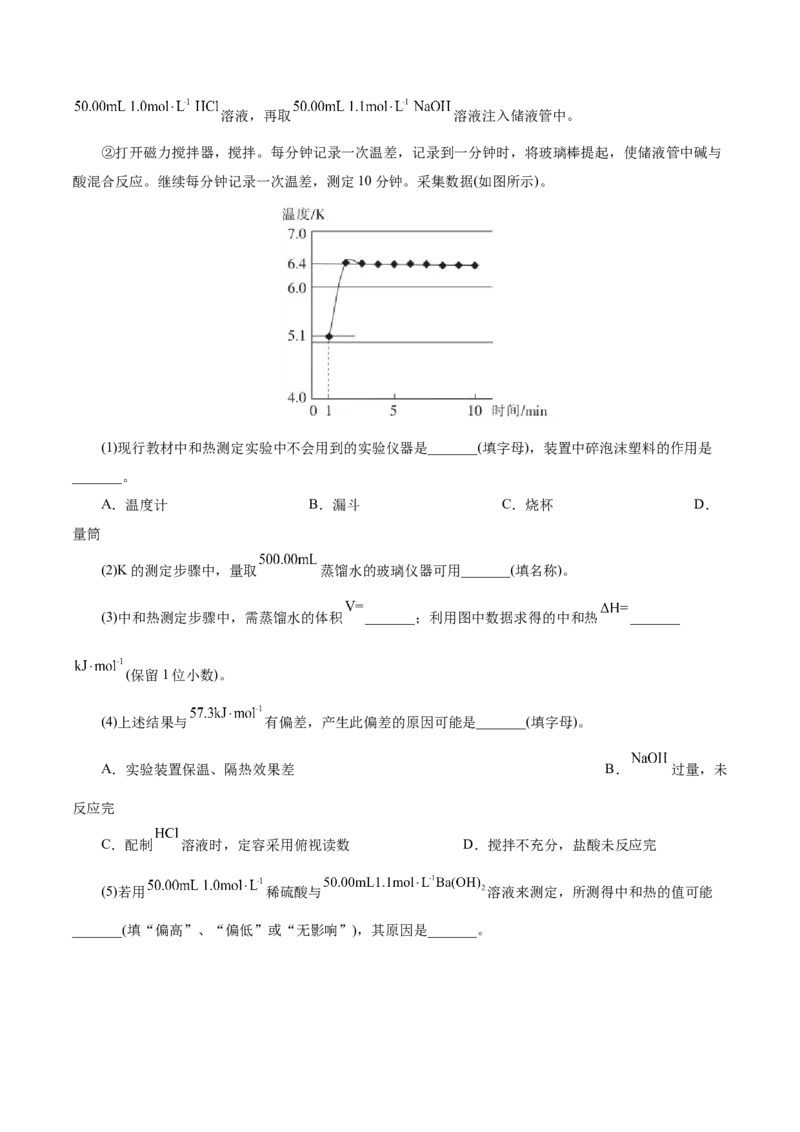
②打开磁力搅拌器,搅拌。每分钟记录一次温差,记录到一分钟时,将玻璃棒提起,使储液管中碱与
酸混合反应。继续每分钟记录一次温差,测定10分钟。采集数据(如图所示)。
(1)现行教材中和热测定实验中不会用到的实验仪器是_______(填字母),装置中碎泡沫塑料的作用是
_______。
A.温度计 B.漏斗 C.烧杯 D.
量筒
(2)K的测定步骤中,量取 蒸馏水的玻璃仪器可用_______(填名称)。
(3)中和热测定步骤中,需蒸馏水的体积 _______;利用图中数据求得的中和热 _______
(保留1位小数)。
(4)上述结果与 有偏差,产生此偏差的原因可能是_______(填字母)。
A.实验装置保温、隔热效果差 B. 过量,未
反应完
C.配制 溶液时,定容采用俯视读数 D.搅拌不充分,盐酸未反应完
(5)若用 稀硫酸与 溶液来测定,所测得中和热的值可能
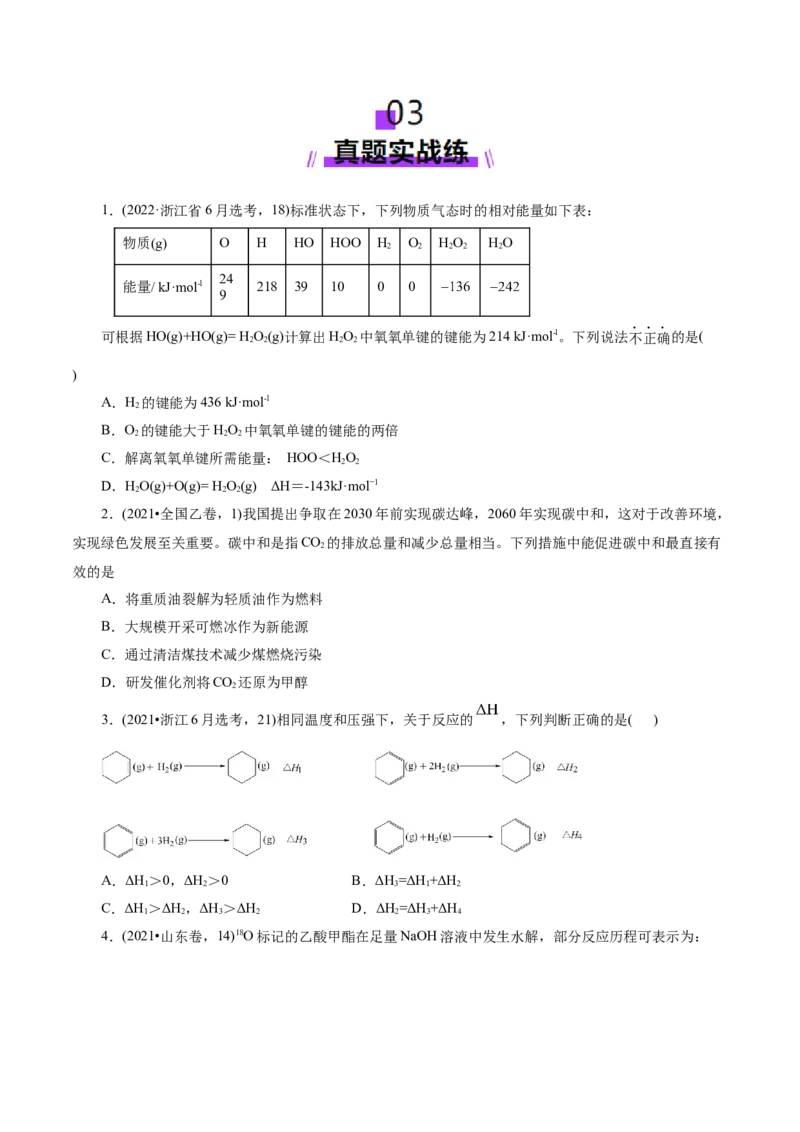
_______(填“偏高”、“偏低”或“无影响”),其原因是_______。1.(2022·浙江省6月选考,18)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O HO HO
2 2 2 2 2
24
能量/ kJ·mol-l 218 39 10 0 0
9
可根据HO(g)+HO(g)= H O(g)计算出HO 中氧氧单键的键能为214 kJ·mol-l。下列说法不正确的是(
2 2 2 2
)
A.H 的键能为436 kJ·mol-l
2
B.O 的键能大于HO 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量: HOO<HO
2 2
D.HO(g)+O(g)= H O(g) ΔH=-143kJ·mol−1
2 2 2
2.(2021•全国乙卷,1)我国提出争取在2030年前实现碳达峰,2060年实现碳中和,这对于改善环境,
实现绿色发展至关重要。碳中和是指CO 的排放总量和减少总量相当。下列措施中能促进碳中和最直接有
2
效的是
A.将重质油裂解为轻质油作为燃料
B.大规模开采可燃冰作为新能源
C.通过清洁煤技术减少煤燃烧污染
D.研发催化剂将CO 还原为甲醇
2
3.(2021•浙江6月选考,21)相同温度和压强下,关于反应的 ,下列判断正确的是( )
A.ΔH>0,ΔH>0 B.ΔH=ΔH+ΔH
1 2 3 1 2
C.ΔH>ΔH,ΔH>ΔH D.ΔH=ΔH+ΔH
1 2 3 2 2 3 4
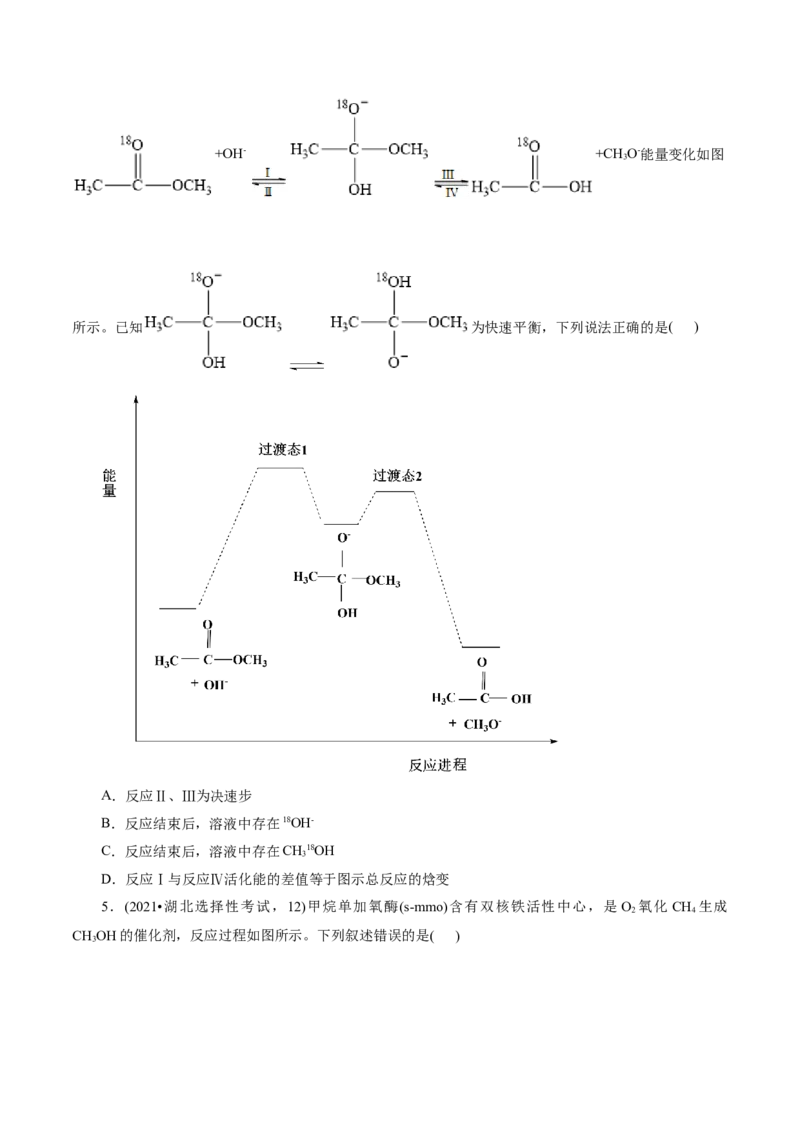
4.(2021•山东卷,14)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:+OH- +CH O-能量变化如图
3
所示。已知 为快速平衡,下列说法正确的是( )
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
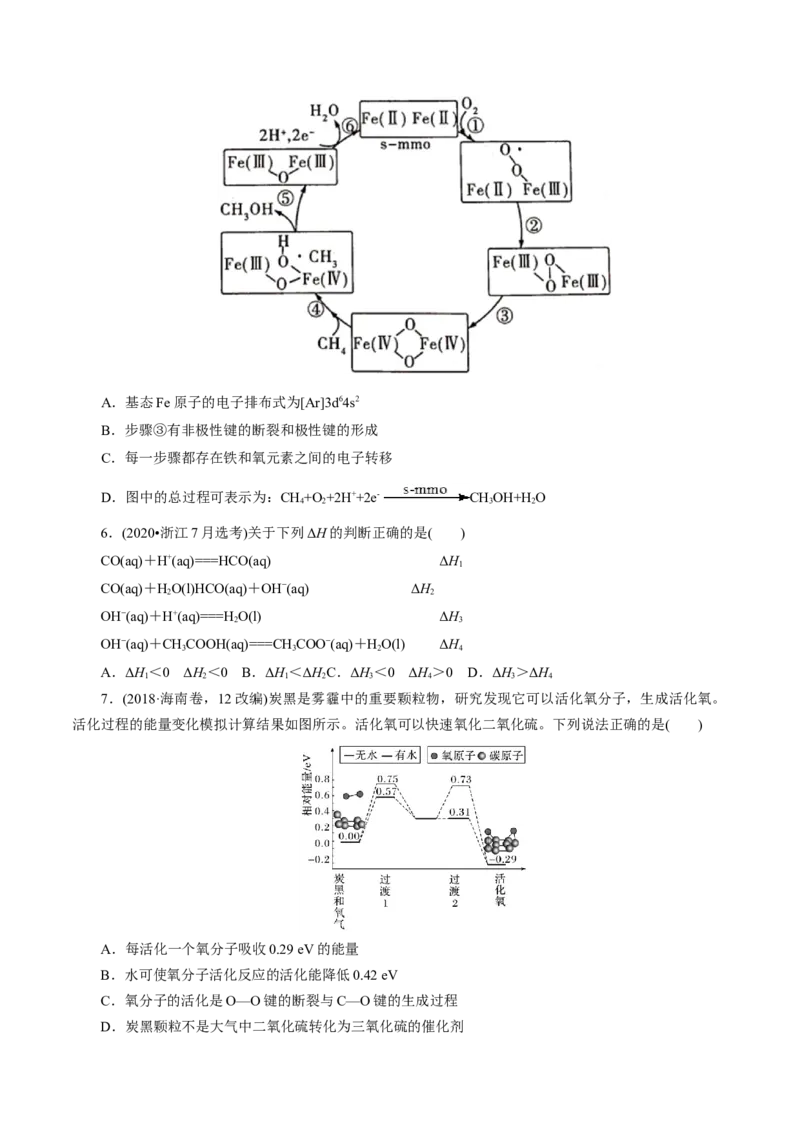
5.(2021•湖北选择性考试,12)甲烷单加氧酶(s-mmo)含有双核铁活性中心,是 O 氧化 CH 生成
2 4
CHOH的催化剂,反应过程如图所示。下列叙述错误的是( )
3A.基态Fe原子的电子排布式为[Ar]3d64s2
B.步骤③有非极性键的断裂和极性键的形成
C.每一步骤都存在铁和氧元素之间的电子转移
D.图中的总过程可表示为:CH+O +2H++2e- CHOH+H O
4 2 3 2
6.(2020•浙江7月选考)关于下列ΔH的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH
1
CO(aq)+HO(l)HCO(aq)+OH−(aq) ΔH
2 2
OH−(aq)+H+(aq)===HO(l) ΔH
2 3
OH−(aq)+CHCOOH(aq)===CHCOO−(aq)+HO(l) ΔH
3 3 2 4
A.ΔH<0 ΔH<0 B.ΔH<ΔH C.ΔH<0 ΔH>0 D.ΔH>ΔH
1 2 1 2 3 4 3 4
7.(2018·海南卷,12改编)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧。
活化过程的能量变化模拟计算结果如图所示。活化氧可以快速氧化二氧化硫。下列说法正确的是( )
A.每活化一个氧分子吸收0.29 eV的能量
B.水可使氧分子活化反应的活化能降低0.42 eV
C.氧分子的活化是O—O键的断裂与C—O键的生成过程
D.炭黑颗粒不是大气中二氧化硫转化为三氧化硫的催化剂