文档内容
专题 01 物质及其变化
第 03 练 氧化还原反应
1.(2020•浙江1月选考)反应MnO +4HCl(浓) ===MnCl +Cl↑+2HO中,氧化产物是( )
2 2 2 2
A.MnO B.HCl C.MnCl D.Cl
2 2 2
2.处理汽车尾气的反应2NO+2CO 2CO+N 中,氧化剂是( )
2 2
A.NO B.CO C.CO D.N
2 2
3.黑火药的反应原理为:2KNO+S+3C KS+N↑+3CO ↑,该反应中氧化产物是( )
3 2 2 2
A.KS B.N C.CO D.KS和N
2 2 2 2 2
9.反应8NH +3Cl=N +6NHCl中,还原产物是( )
3 2 2 4
A.N B.Cl C.NH Cl D.NH
2 2 4 3
4.(2020•北京卷)水与下列物质反应时,水表现出氧化性的是( )
A.Na B.Cl C.NO D.NaO
2 2 2
5.(2020•浙江7月选考)反应MnO +4HCl(浓) MnCl +Cl↑+2H O中,氧化产物与还原产物的物质的
2 2 2 2
量之比是( )
A.1:2 B.1:1 C.2:1 D.4:1
6.(2020•山东卷)下列叙述不涉及氧化还原反应的是( )
A.谷物发酵酿造食醋 B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒 D.大气中NO 参与酸雨形成
2
7.下列反应中,HO做氧化剂的是( )
2
A.SO +H O=HSO B.3NO +H O=2HNO +NO
3 2 2 4 2 2 3
C.Cl+H O HCl+HClO D.3Fe+4H O(g) Fe O+4H
2 2 2 3 4 2
8.下列变化过程中,加入氧化剂才能实现的是( )
A.Cl→Cl- B.I-→I C.SO →SO 2- D.CuO→Cu
2 2 2 3
9.下列物质的转化必须加入氧化剂才能实现的是( )
A.Cl→HClO B.HS→SO C.NO→HNO D.HNO→NO
2 2 2 2 5 3 3
10.下列变化需要加入还原剂才能实现的是( )
A.KClO→O B.Cl→HCl C.Fe→Fe3+ D.C→CO
3 2 2 211.下列反应中,氧化产物与还原产物为同一种物质的是( )
A.KClO + 6HCl = KCl+ 3Cl ↑+ 3H O B.2Na+2HO=2NaOH+H ↑
3 2 2 2 2
C.2NaO+2H O=4NaOH+O ↑ D.I+2NaSO = 2NaI + NaSO
2 2 2 2 2 2 2 3 2 4 6
12.关于反应8NH +3Cl=6NHCl+N ,下列说法正确的是( )
3 2 4 2
A.每生成1 molN,有8 molNH 被氧化
2 3
B.每3 mol Cl 反应,转移6N 个电子
2 A
C.氧化剂和还原剂的物质的量之比为3:8
D.还原产物为N
2
13.下列反应中,通入的气体只作还原剂的是( )
A.二氧化硫通入溴水中 B.氯气通入氢氧化钠溶液中
C.二氧化硫通入氢氧化钾溶液中 D.二氧化氮通入水中
14.下列化学反应中溴元素仅被氧化的是( )
A.2NaBr+Cl===2NaCl+Br B.Br +2NaI===2NaBr+I
2 2 2 2
C.3Br +6NaOH=====5NaBr+NaBrO +3HO D.HBr+NaOH===NaBr+HO
2 3 2 2
15.下列实验中,颜色的变化与氧化还原反应有关的是( )
A.往紫色石蕊试液中加入盐酸,溶液变红
B.饱和FeCl 溶液在沸水中变成红褐色胶体
3
C.向FeSO 溶液中滴加NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色
4
D.SO 使滴有酚酞的NaOH溶液褪色
2
1.(2021•浙江1月选考)关于反应8NH +6NO=7N +12H O,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化( )
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
2.(2021•浙江6月选考)关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是( )
2 3 6 2 2
A. KHIO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7g I 时,转移0.1mol电子 D.还原剂与氧化剂的物质的量之比为7:1
2
3.ClO 是一种高效水处理剂,实验室通过以下反应制得ClO :2KClO+H C O+H SO
2 2 3 2 2 4 2 4
2ClO ↑+K SO +2CO ↑+2H O,关于此反应的说法正确的是( )
2 2 4 2 2
A.KClO 中的Cl化合价降低,失电子 B.反应中HSO 体现了酸性和强氧化性
3 2 4C.反应中HC O 被氧化 D.产物中Cl与C化合价相同,因而氧化性一样强
2 2 4
4.OF 可以发生反应:HS+4OF===SF +2HF+4O,下列说法正确的是( )
2 2 2 2 2 6 2
A.氧气是氧化产物
B.OF 既是氧化剂又是还原剂
2 2
C.若生成4.48 L HF,则转移0.8 mol 电子
D.还原剂与氧化剂的物质的量之比为1∶4
5.已知反应 ,下列有关该反应的说法正确的是(
)
A.HO 发生还原反应 B.X是KO
2 2 2
C.MnSO 是氧化产物 D.
4
6.(NH )SO 具有强氧化性,在酸性溶液中,可将Mn2+氧化为MnO -,但一般情况下,该反应进行
4 2 2 8 4
地非常缓慢,而加入AgNO 溶液后,混合液迅速变为紫红色。下列说法错误的是( )
3
A.AgNO 为该反应的催化剂
3
B.该反应中的还原产物为SO 2-
4
C.反应中氧化剂与还原剂物质的量之比为2:5
D.SO2-中-1价O与-2价O的个数比为1:3
2 8
7.环保部门利用NaSO 处理含氰化钠废水,其反应原理为 NaCN+Na SO=NaSCN+Na SO (NaSCN
2 2 3 2 2 3 2 3
中S的化合价为-2价),下列有关说法正确的是( )
A.NaCN中C的化合价为+4价 B.NaSO 只作还原剂
2 2 3
C.NaSO 是氧化产物 D.该方法处理酸性废水效果更好
2 3
8.KFeO 是优良的水处理剂,一种制备方法是将 Fe O 、KNO 、KOH 混合共熔,反应为
2 4 2 3 3
Fe O+3KNO +4KOH =2KFeO+3 KNO+2H O,下列关于该反应的说法不正确的是( )
2 3 3 2 4 2 2
A.铁元素被氧化,氮元素被还原
B.KFeO 是氧化产物,KNO KNO 是还原产物
2 4 2 2
C.KFeO 在酸性条件下不稳定,会迅速分解并生成氢气
2 4
D.KFeO 具有强氧化性,因而有杀菌作用
2 4
9.制备氰氨基化钙的化学方程式为CaCO +2HCN===CaCN +CO↑+H↑+CO↑,下列说法正确的是(
3 2 2 2
)
A.氢元素被氧化,碳元素被还原 B.HCN是氧化剂,CaCO 是还原剂
3
C.CaCN 是氧化产物,H 为还原产物 D.CO为氧化产物,H 为还原产物
2 2 2
10.已知Co O 在酸性溶液中易被还原成Co2+,Co O 、Cl 、FeCl 、I 的氧化性依次减弱。下列反应
2 3 2 3 2 3 2
在水溶液中不可能发生的是( )A.3Cl+6FeI===2FeCl +4FeI B.Cl+FeI===FeCl +I
2 2 3 3 2 2 2 2
C.Co O+6HCl===2CoCl +Cl↑+3HO D.2Fe3++2I-===2Fe2++I
2 3 2 2 2 2
11.向FeBr 溶液中通入一定量的Cl,发生反应2Fe2++2Br-+2Cl→2Fe3++Br +4Cl-,下列关于该反应说
2 2 2 2
法错误的是( )
A.氧化性:Cl>Fe3+
2
B.还原性:Fe2+<Br-
C.参加反应的 与Cl 的物质的量之比为1:1
2
D.被氧化的 占 总量的一半
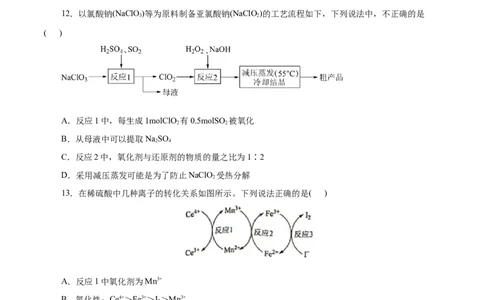
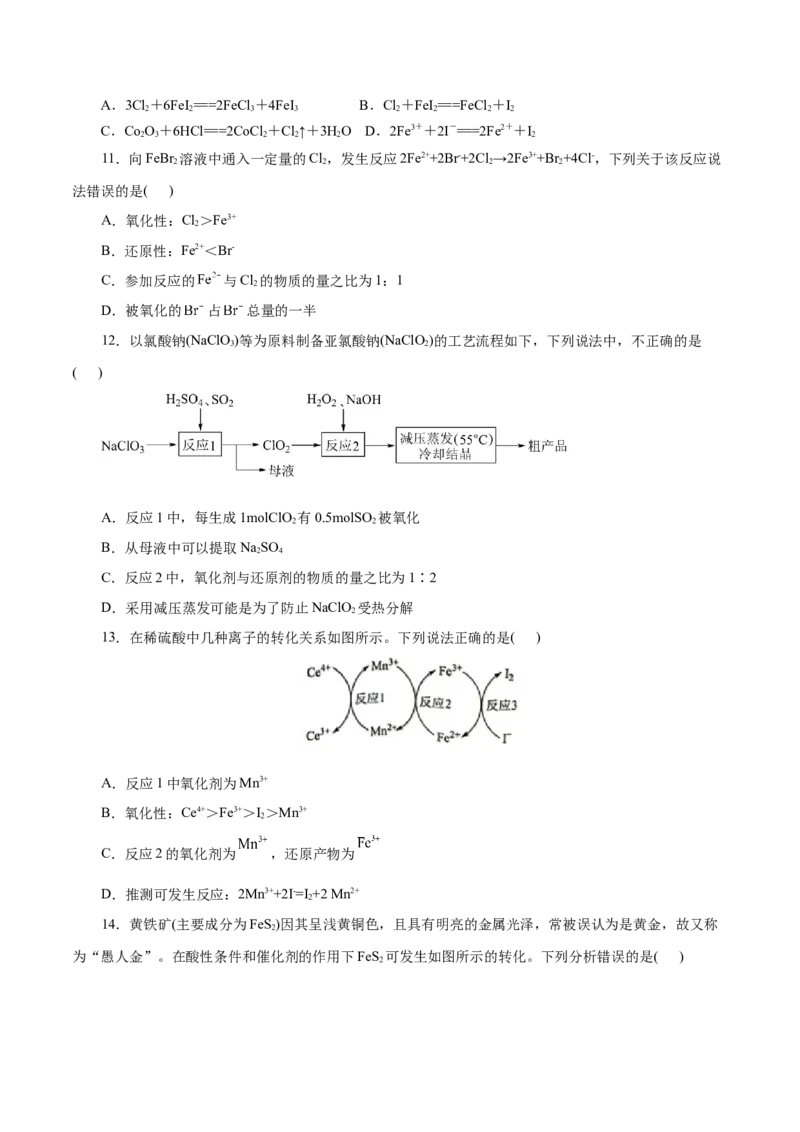
12.以氯酸钠(NaClO)等为原料制备亚氯酸钠(NaClO)的工艺流程如下,下列说法中,不正确的是
3 2
( )
A.反应1中,每生成1molClO 有0.5molSO 被氧化
2 2
B.从母液中可以提取NaSO
2 4
C.反应2中,氧化剂与还原剂的物质的量之比为1∶2
D.采用减压蒸发可能是为了防止NaClO 受热分解
2
13.在稀硫酸中几种离子的转化关系如图所示。下列说法正确的是( )
A.反应1中氧化剂为Mn3+
B.氧化性:Ce4+>Fe3+>I>Mn3+
2
C.反应2的氧化剂为 ,还原产物为
D.推测可发生反应:2Mn3++2I-=I +2 Mn2+
2
14.黄铁矿(主要成分为FeS)因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称
2
为“愚人金”。在酸性条件和催化剂的作用下FeS 可发生如图所示的转化。下列分析错误的是( )
2A.反应Ⅰ、Ⅱ为氧化还原反应
B.反应Ⅰ的离子方程式:4 Fe(NO)2++O +4H+═4Fe3++4NO+2HO
2 2
C.反应Ⅱ中,每消耗1mol FeS,转移电子的物质的量为
2
D.在酸性条件下,黄铁矿催化氧化中 和 均作催化剂
15.含氮化合物及其单质的“类别-价态”二维图如图,下列相关分析或预测错误的是( )
A.NaOH、NaNO 、NH Cl均属于强电解质
2 4
B.N→NO →HNO 的转化均能一步实现
2 2 3
C.反应NO +NO+2 NaOH =2NaNO +H O属于氧化还原反应
2 2 2
D.NO 溶于水的离子方程式为3NO +H O=2H++2NO-+NO
2 2 2 3
1.(2022•山东卷)古医典富载化学知识,下述之物见其氧化性者为( )
A.金(Au):“虽被火亦未熟"
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳(CaCO):“色黄,以苦酒(醋)洗刷则白”
32.洁厕灵和84消毒液混合使用时发生反应:NaC1O+2HCl=NaCl+Cl ↑+H O,生成有毒的氯气。下列
2 2
说法正确的是( )
A.84消毒液的有效成分是HCl
B.氯气既是氧化产物又是还原产物,氯化钠是还原产物
C.HCl只表现还原性
D.若有0.lmolHCl被氧化,生成的氯气在标准状况下的体积约为2.24L
3.(2022·浙江省1月选考)关于反应4CO+SiH 4CO+2HO+SiO,下列说法正确的是( )
2 4 2 2
A.CO是氧化产物
B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4
D.生成1molSiO 时,转移8mol电子
2
4.(2022·浙江省6月选考)关于反应NaSO+H SO =Na SO +S ↓+SO ↑ +H O,下列说法正确的是( )
2 2 3 2 4 2 4 2 2
A.HSO 发生还原反应
2 4
B.NaSO 既是氧化剂又是还原剂
2 2 3
C.氧化产物与还原产物的物质的量之比为2∶1
D.1mol Na SO 发生反应,转移4mol电子
2 2 3
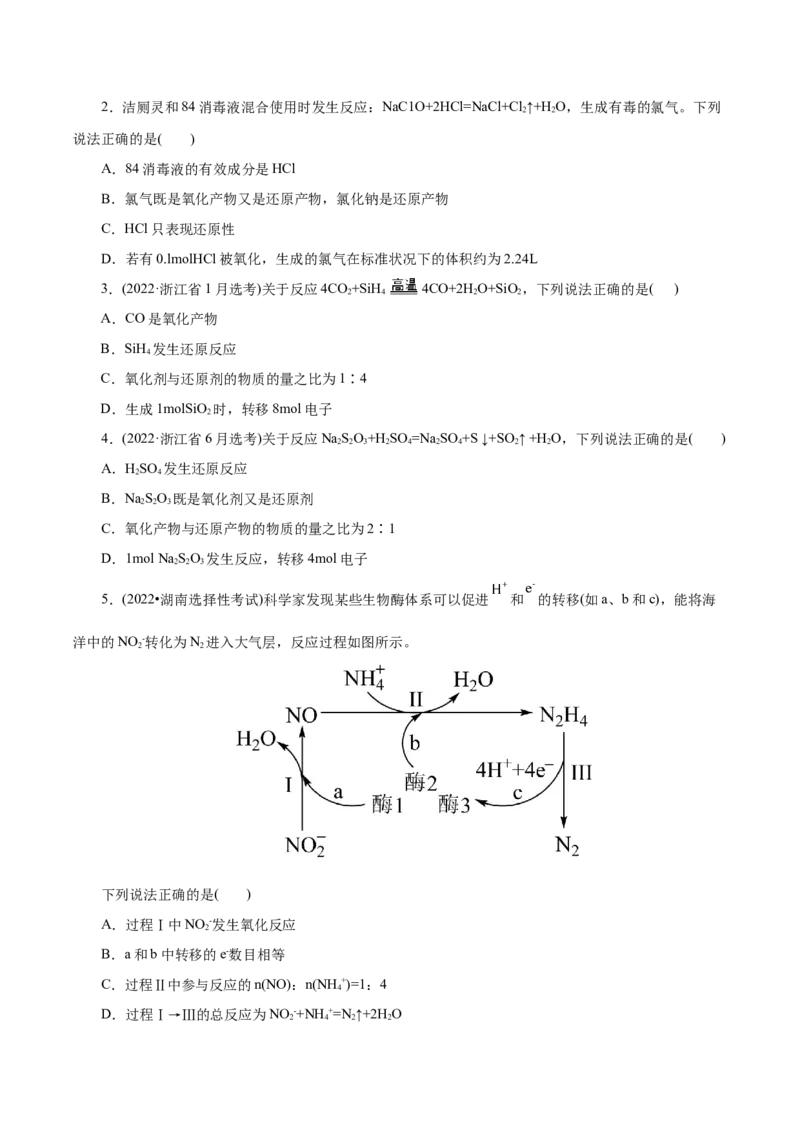
5.(2022•湖南选择性考试)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海
洋中的NO -转化为N 进入大气层,反应过程如图所示。
2 2
下列说法正确的是( )
A.过程Ⅰ中NO -发生氧化反应
2
B.a和b中转移的e-数目相等
C.过程Ⅱ中参与反应的n(NO):n(NH +)=1:4
4
D.过程Ⅰ→Ⅲ的总反应为NO -+NH+=N ↑+2H O
2 4 2 26.(2022•山东卷)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的
是( )
A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量,C H 的平衡转化率不变
3 8
D.当主要发生包含②的历程时,最终生成的水减少
7.(2021•湖南选择性考试)KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一
3
步反应为6I +11KClO +3H O 6KH(IO ) +5KCl+3Cl ↑。下列说法错误的是( )
2 3 2 3 2 2
A.产生22.4L(标准状况)Cl 时,反应中转移10mol e﹣
2
B.反应中氧化剂和还原剂的物质的量之比为11:6
C.可用石灰乳吸收反应产生的Cl 制备漂白粉
2
D.可用酸化的淀粉碘化钾溶液检验食盐中IO -的存在
3
8.(2021•北京卷)电石中混有CaS、Ca P 等杂质,用电石水解制备乙炔时,乙炔中常混有HS、PH ,
3 2 2 3
可用CuSO 溶液除去这两种杂质,相应的化学方程式是( )
4
i.CuSO +H S=CuS↓+H SO
4 2 2 4
ii.11PH+24CuSO+12H O=3HPO +24H SO +8Cu P↓
3 4 2 3 4 2 4 3
下列说法不正确的是
A.反应i不能说明HS的酸性强于HSO
2 2 4
B.24molCuSO 完全反应时,可氧化11molPH
4 3
C.HS、PH 会干扰KMnO 酸性溶液对乙炔性质的检验
2 3 4
D.CaS的水解方程式:CaS+2H O=Ca(OH) +H S↑;Ca P 水解方程式:Ca P+6H O=3Ca(OH) +2PH↑
2 2 2 3 2 3 2 2 2 3
9.工业接触法制备硫酸过程如下:将硫黄或其他含硫矿物(如黄铁矿,主要成分:FeS)在沸腾炉中与
2
氧气反应生成SO ;SO 在VO 催化作用下与空气中的O 在接触室中发生催化氧化反应;生成的SO 在吸
2 2 2 5 2 3
收塔中用98.3%的浓硫酸吸收得到发烟硫酸(H SO •SO )。下列关于反应4FeS+11O 2Fe O+8SO 说法
2 4 3 2 2 2 3 2
正确的是( )A.FeS 中S的化合价为
2
B.反应中铁元素被还原
C.产物Fe O 可用作食品保存的吸氧剂
2 3
D.反应中转移 ,生成 的SO
2
10.二氧化氯(ClO )是一种优良的消毒剂,可由氯酸钠和双氧水在酸性条件下反应制备,反应原理为
2
NaClO+H O+H SO →ClO ↑+Na SO +H O+O↑(未配平)。下列有关该反应的说法正确的是( )
3 2 2 2 4 2 2 4 2 2
A.HO 是氧化剂,发生氧化反应
2 2
B.HO是还原产物
2
C.产物中ClO 与O 的物质的量之比为
2 2
D.每转移 电子,生成标准状况下11.2L O
2
11.已知HSO +I+HO===H SO +2HI,将0.1 mol Cl 通入100 mL含等物质的量的HI与HSO 的混
2 3 2 2 2 4 2 2 3
合溶液中,有一半的HI被氧化,则下列说法正确的是( )
A.物质的还原性:HI>HSO >HCl
2 3
B.HSO 的物质的量浓度为0.6 mol·L-1
2 3
C.若再通入0.05 mol Cl ,则恰好能将HI和HSO 完全氧化
2 2 3
D.通入0.1 mol Cl 发生反应的离子方程式为5Cl+4HSO +2I-+4HO===4SO+I+10Cl-+16H+
2 2 2 3 2 2
12.将一定量的氯气通入30 mL浓度为10 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成
NaCl、NaClO、NaClO 共存体系。下列判断正确的是( )
3
A.与NaOH反应的氯气一定为0.3 mol
B.n(Na+)∶n(Cl-)可能为7∶3
C.n(NaCl)∶n(NaClO)∶n(NaClO)可能为11∶2∶1
3
D. 若反应中转移的电子为n mol,则0.15<n<0.25
13.已知氧化性:Fe3+>M2+(M为不活泼的常见金属),向物质的量浓度均为1mol•L-1的Fe (SO ) 和
2 4 3
MSO 的100mL混合液中加入amol铁粉,充分反应后,下列说法不正确的是( )
4
A.当a≤0.1时,发生的反应为2Fe3++Fe=3Fe2+
B.当0.1≤a<0.2时,溶液中n(Fe2+)=(0.2+a)mol
C.当a≥0.2时,发生的反应为2Fe3++M2++2Fe=4Fe2++M
D.若有固体剩余则可能是铁
14.三氟化氮(NF )(氟只有两种价态:-1,0)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环
3
境中能发生反应:3NF +5H O==2NO+HNO +9HF。下列有关该反应的说法正确的是( )
3 2 3
A.NF 是氧化剂,HO是还原剂
3 2B.若1mol NF 被氧化,反应转移电子数为2N
3 A
C.若生成0.4molHNO ,则转移0.4mol电子
3
D.氧化剂与还原剂的物质的量之比为1∶2
15.在有机碳源和微生物作用下,大气中氮可以实现平衡循环,过程如图所示。下列说法正确的是(
)
A.图示所有含氮微粒中N的化合价只有0、+3、+5
B.循环转化过程中NO -被甲醇氧化为N
3 2
C.温度越高,N 转化成NH +的速率越快
2 4
D.NH +与NO -反应的离子方程式为:NH ++NO-=N ↑+2H O
4 2 4 2 2 2