文档内容
第 06 讲 钠及其化合物
1.用光洁的铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察到火焰呈黄色,下列各判断正确的是(
)
A.只含有Na+
B.一定含有Na+,可能含有K+
C.既含有Na+,又含有K+
D.可能含有Na+,还可能含有K+
2.南朝陶弘景在《本草经集注》中记载有鉴别消石(KNO)与朴消(Na SO )之法:“以火烧之,紫青烟
3 2 4
起,云是真消石也”。该鉴别方法利用的原理是( )
A.受热升华 B.颜色反应
C.焰色试验 D.丁达尔效应
3.下列有关钠的说法中,不正确的是( )
A.工业上通过电解氯化钠溶液制取金属钠
B.高压钠灯常用于道路和广场的照明
C.钠钾合金可在快中子反应堆中作热交换剂
D.钠可用于从钛、铌等金属的氯化物中置换出金属单质
4.下列关于钠的氧化物的说法正确的是( )
A.NaO 是白色固体,与冷水作用放出氧气,生成氢氧化钠
2 2
B.在NaO 与CO 的反应中,氧化剂是NaO,还原剂是CO
2 2 2 2 2 2
C.Na和O 在加热时反应生成NaO,在常温下反应生成NaO
2 2 2 2
D.NaO 能与水反应,生成NaOH,所以NaO 是碱性氧化物
2 2 2 2
5.化学与科学、技术、社会、环境密切相关。下列有关说法中正确的是( )
A.小苏打可用于生产玻璃,也可用来除去物品表面的油污
B.过氧化钠可用于食品、羽毛和织物等的漂白
C.医用酒精、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的
D.使用含有氯化钠的融雪剂会加快桥梁的腐蚀
6.有两试管分别装有NaCO 和NaHCO 溶液,下列操作和判断均正确的是( )
2 3 3
选项 操作 判断
A 分别加入澄清石灰水 产生沉淀的为NaCO
2 3B 分别加入等浓度的稀盐酸 反应较剧烈的为NaCO
2 3
C 分别加入CaCl 溶液 产生沉淀的为NaCO
2 2 3
D 逐滴加入等浓度的盐酸 立即产生气泡的为NaCO
2 3
7.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气中在常温下充分反应,则下列说法
正确的是( )
A.第一块钠失去电子多
B.两块钠失去电子一样多
C.第二块钠的反应产物质量大
D.两块钠的反应产物质量一样大
8.为除去括号内的杂质,所选用的试剂或方法不正确的是( )
A.NaCO 溶液(NaHCO ),选用适量的NaOH溶液
2 3 3
B.NaHCO 溶液(Na CO),应通入过量的CO 气体
3 2 3 2
C.NaO 粉末(Na O),将混合物在氧气中加热
2 2 2
D.NaCO 溶液(Na SO ),加入适量Ba(OH) 溶液,过滤
2 3 2 4 2
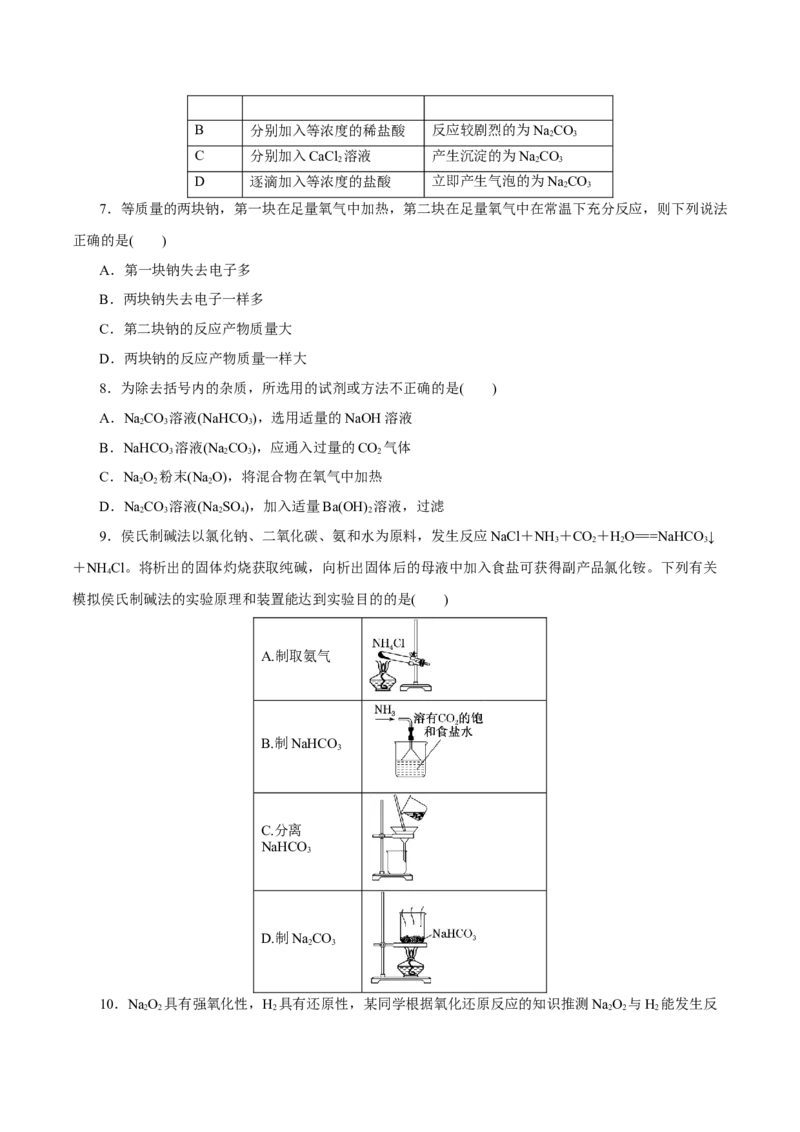
9.侯氏制碱法以氯化钠、二氧化碳、氨和水为原料,发生反应NaCl+NH +CO+HO===NaHCO↓
3 2 2 3
+NH Cl。将析出的固体灼烧获取纯碱,向析出固体后的母液中加入食盐可获得副产品氯化铵。下列有关
4
模拟侯氏制碱法的实验原理和装置能达到实验目的的是( )
A.制取氨气
B.制NaHCO
3
C.分离
NaHCO
3
D.制NaCO
2 3
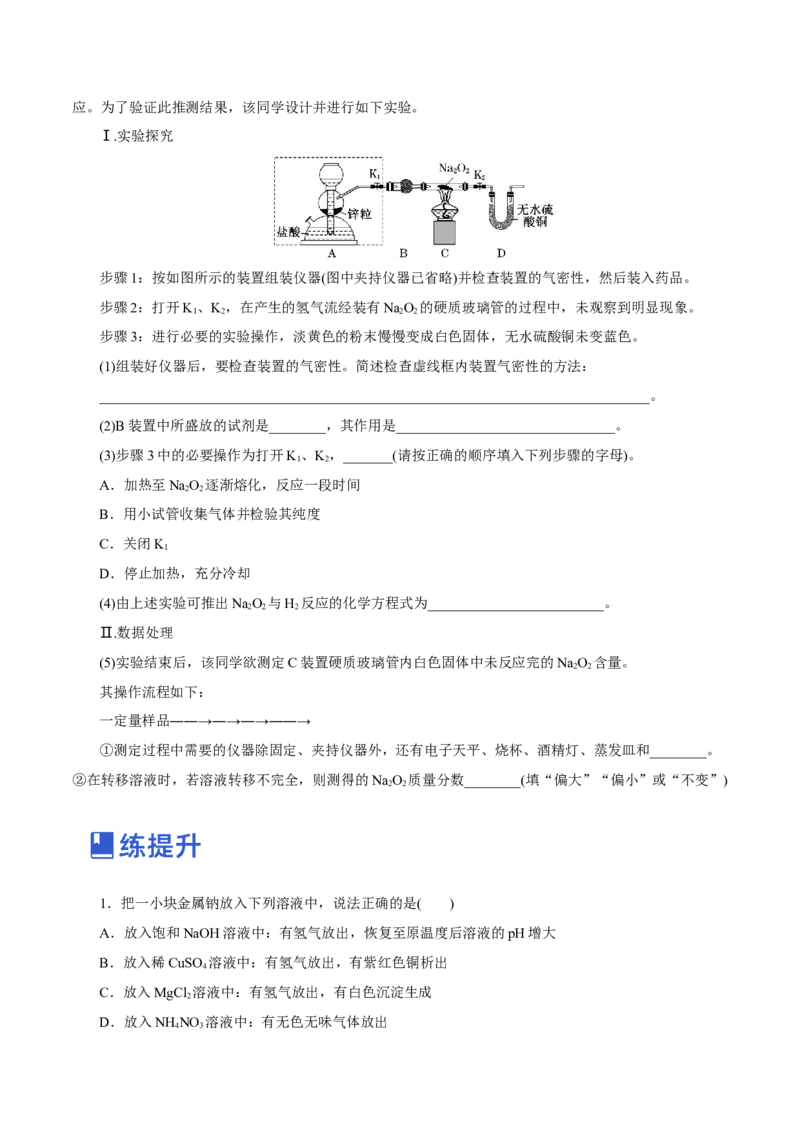
10.NaO 具有强氧化性,H 具有还原性,某同学根据氧化还原反应的知识推测NaO 与H 能发生反
2 2 2 2 2 2应。为了验证此推测结果,该同学设计并进行如下实验。
Ⅰ.实验探究
步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K、K,在产生的氢气流经装有NaO 的硬质玻璃管的过程中,未观察到明显现象。
1 2 2 2
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:
______________________________________________________________________________。
(2)B装置中所盛放的试剂是________,其作用是_______________________________。
(3)步骤3中的必要操作为打开K、K,_______(请按正确的顺序填入下列步骤的字母)。
1 2
A.加热至NaO 逐渐熔化,反应一段时间
2 2
B.用小试管收集气体并检验其纯度
C.关闭K
1
D.停止加热,充分冷却
(4)由上述实验可推出NaO 与H 反应的化学方程式为_________________________。
2 2 2
Ⅱ.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的NaO 含量。
2 2
其操作流程如下:
一定量样品――→―→―→――→
①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和________。
②在转移溶液时,若溶液转移不完全,则测得的NaO 质量分数________(填“偏大”“偏小”或“不变”)
2 2
1.把一小块金属钠放入下列溶液中,说法正确的是( )
A.放入饱和NaOH溶液中:有氢气放出,恢复至原温度后溶液的pH增大
B.放入稀CuSO 溶液中:有氢气放出,有紫红色铜析出
4
C.放入MgCl 溶液中:有氢气放出,有白色沉淀生成
2
D.放入NH NO 溶液中:有无色无味气体放出
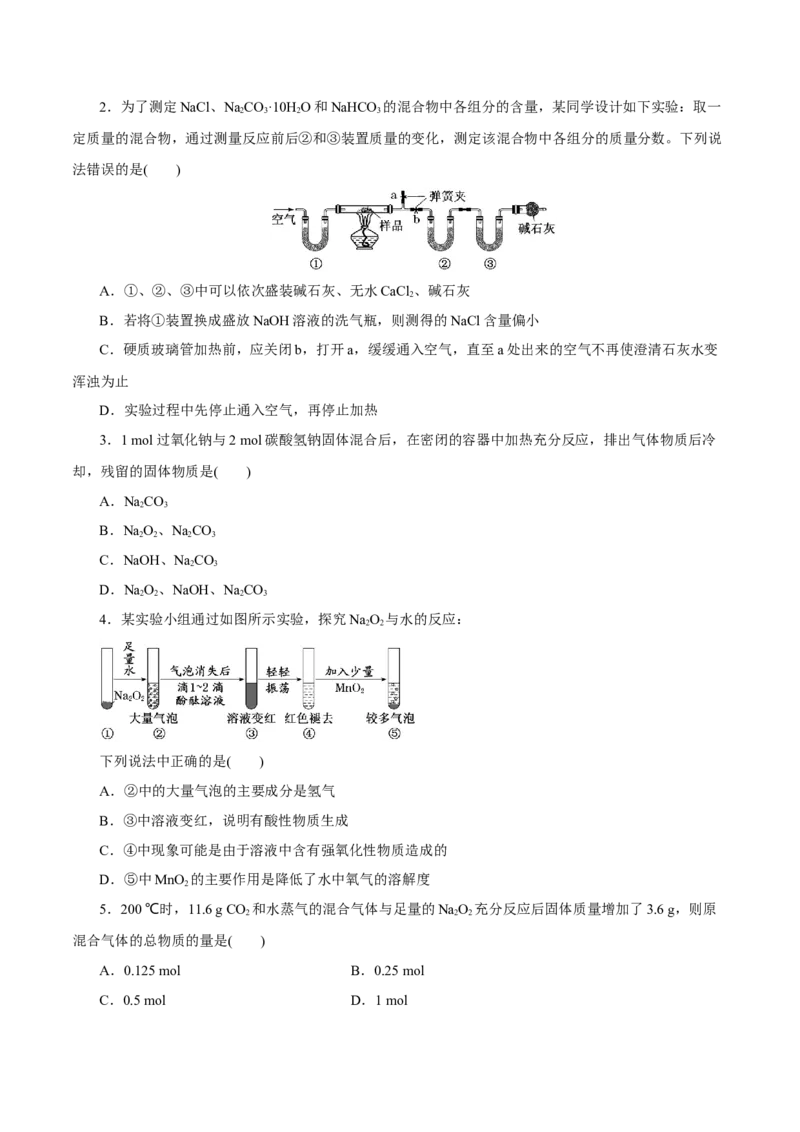
4 32.为了测定NaCl、NaCO·10H O和NaHCO 的混合物中各组分的含量,某同学设计如下实验:取一
2 3 2 3
定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说
法错误的是( )
A.①、②、③中可以依次盛装碱石灰、无水CaCl 、碱石灰
2
B.若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏小
C.硬质玻璃管加热前,应关闭b,打开a,缓缓通入空气,直至a处出来的空气不再使澄清石灰水变
浑浊为止
D.实验过程中先停止通入空气,再停止加热
3.1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷
却,残留的固体物质是( )
A.NaCO
2 3
B.NaO、NaCO
2 2 2 3
C.NaOH、NaCO
2 3
D.NaO、NaOH、NaCO
2 2 2 3
4.某实验小组通过如图所示实验,探究NaO 与水的反应:
2 2
下列说法中正确的是( )
A.②中的大量气泡的主要成分是氢气
B.③中溶液变红,说明有酸性物质生成
C.④中现象可能是由于溶液中含有强氧化性物质造成的
D.⑤中MnO 的主要作用是降低了水中氧气的溶解度
2
5.200 ℃时,11.6 g CO 和水蒸气的混合气体与足量的NaO 充分反应后固体质量增加了3.6 g,则原
2 2 2
混合气体的总物质的量是( )
A.0.125 mol B.0.25 mol
C.0.5 mol D.1 mol6.在120 ℃下,将V mL的CO 和HO(水蒸气),通入足量的过氧化钠,充分反应后发现电子转移为
2 2
1 mol,则下列说法正确的是( )
A.过氧化钠的摩尔质量为78
B.整个过程消耗的过氧化钠为156 g
C.充分反应后气体在120 ℃体积为0.4V mL
D.V mL的CO 和HO(水蒸气)质量可能为31 g
2 2
7.有关NaHCO 和NaCO 与盐酸的反应,以下叙述错误的是( )
3 2 3
A.等质量的NaHCO 和NaCO 与足量盐酸反应,在相同条件下NaCO 产生的CO 体积小
3 2 3 2 3 2
B.等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积NaCO 是NaHCO 的两倍
2 3 3
C.等质量的NaHCO 和NaCO 与盐酸完全反应,前者消耗盐酸较多
3 2 3
D.等物质的量的NaHCO 和NaCO 与足量盐酸反应,两者产生的CO 一样多
3 2 3 2
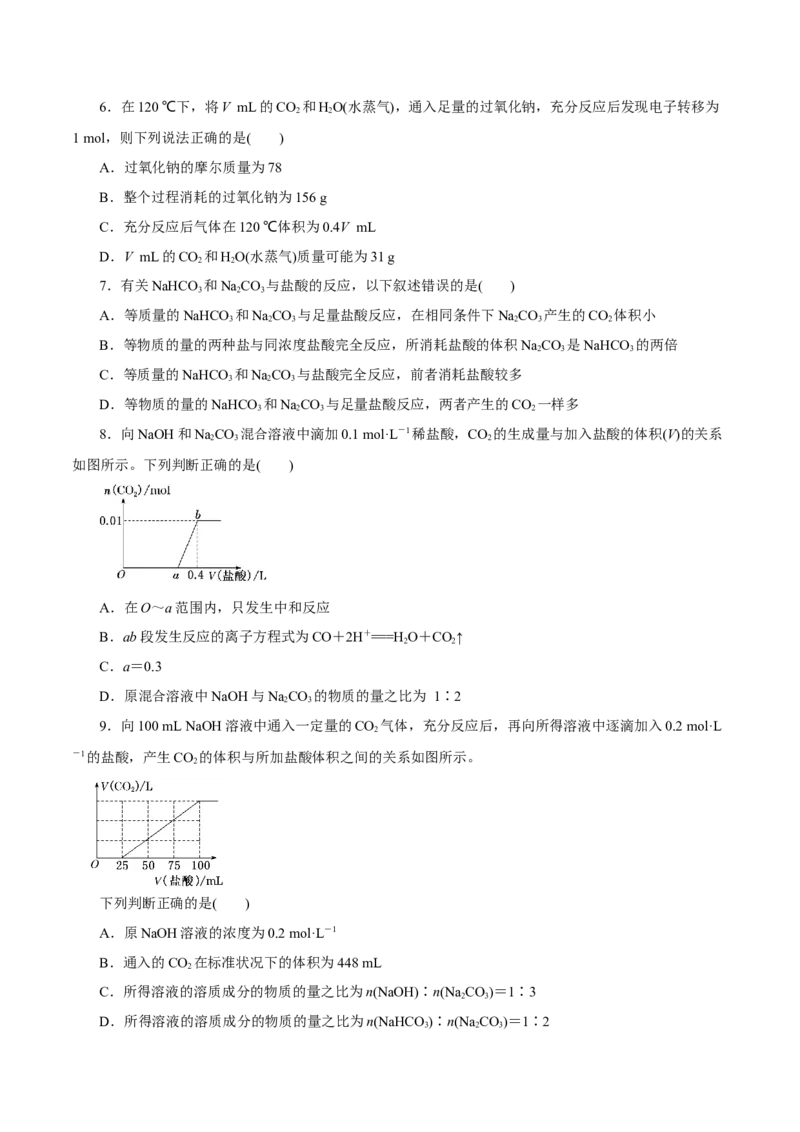
8.向NaOH和NaCO 混合溶液中滴加0.1 mol·L-1稀盐酸,CO 的生成量与加入盐酸的体积(V)的关系
2 3 2
如图所示。下列判断正确的是( )
A.在O~a范围内,只发生中和反应
B.ab段发生反应的离子方程式为CO+2H+===H O+CO↑
2 2
C.a=0.3
D.原混合溶液中NaOH与NaCO 的物质的量之比为 1∶2
2 3
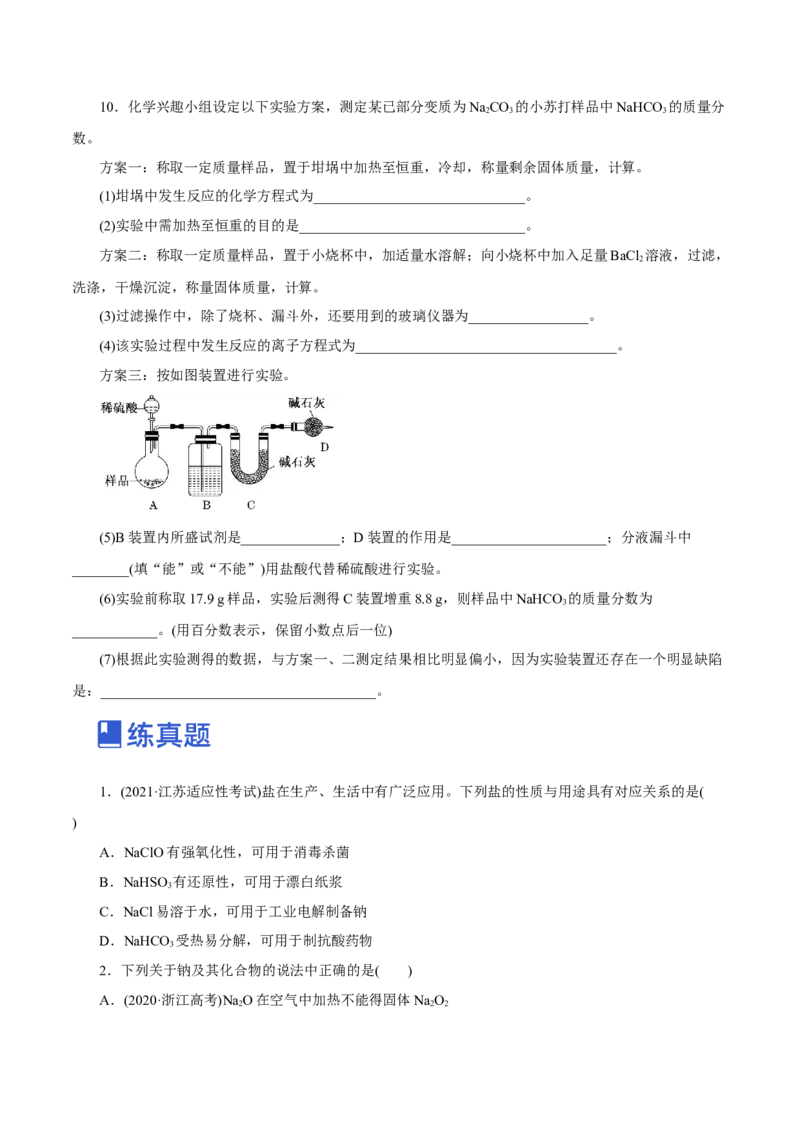
9.向100 mL NaOH溶液中通入一定量的CO 气体,充分反应后,再向所得溶液中逐滴加入0.2 mol·L
2
-1的盐酸,产生CO 的体积与所加盐酸体积之间的关系如图所示。
2
下列判断正确的是( )
A.原NaOH溶液的浓度为0.2 mol·L-1
B.通入的CO 在标准状况下的体积为448 mL
2
C.所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na CO)=1∶3
2 3
D.所得溶液的溶质成分的物质的量之比为n(NaHCO )∶n(Na CO)=1∶2
3 2 310.化学兴趣小组设定以下实验方案,测定某已部分变质为NaCO 的小苏打样品中NaHCO 的质量分
2 3 3
数。
方案一:称取一定质量样品,置于坩埚中加热至恒重,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为______________________________。
(2)实验中需加热至恒重的目的是________________________________。
方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量BaCl 溶液,过滤,
2
洗涤,干燥沉淀,称量固体质量,计算。
(3)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为_________________。
(4)该实验过程中发生反应的离子方程式为_____________________________________。
方案三:按如图装置进行实验。
(5)B装置内所盛试剂是______________;D装置的作用是______________________;分液漏斗中
________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(6)实验前称取17.9 g样品,实验后测得C装置增重8.8 g,则样品中NaHCO 的质量分数为
3
____________。(用百分数表示,保留小数点后一位)
(7)根据此实验测得的数据,与方案一、二测定结果相比明显偏小,因为实验装置还存在一个明显缺陷
是:_______________________________________。
1.(2021·江苏适应性考试)盐在生产、生活中有广泛应用。下列盐的性质与用途具有对应关系的是(
)
A.NaClO有强氧化性,可用于消毒杀菌
B.NaHSO 有还原性,可用于漂白纸浆
3
C.NaCl易溶于水,可用于工业电解制备钠
D.NaHCO 受热易分解,可用于制抗酸药物
3
2.下列关于钠及其化合物的说法中正确的是( )
A.(2020·浙江高考)Na O在空气中加热不能得固体NaO
2 2 2B.(2021·浙江高考)钠与水反应生成氢氧化钠和氢气
C.(2020·江苏高考) 室温下,Na在空气中反应生成NaO
2 2
D.(2019·江苏高考) NaHCO 受热易分解,所以可用于制胃酸中和剂
3
3.下列说法错误的是( )
A.(经典高考)碳酸钠可用于去除餐具的油污
B.(经典高考)用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+
C.(经典高考)Na O 可与CO 反应放出氧气,可用于制作呼吸面具
2 2 2
D.(2019·全国Ⅱ卷)Na O 在空气中放置后由淡黄色变为白色,反应的化学方程式为2NaO===2Na O
2 2 2 2 2
+O↑
2