文档内容
第 06 讲 钠及其化合物
1.向下列物质中加入NaOH溶液并加热,其成分不发生改变的是
A.用聚四氟乙烯制 B.用于通信的光 C.用于焙制糕点的 D.从餐厨废弃物中
成的实验仪器 导纤维 小苏打 提取的地沟油
2.氢氧化钠应用广泛,下列说法不正确的是
A.钠元素位于周期表s区 B. 属于强电解质
C.工业上常用 制备小苏打 D. 溶液能使蛋白质变性
3.关于实验室保存试剂的说法错误的是
A.实验室中金属钠通常保存在煤油里
B.液溴以少量水液封后用橡胶塞塞紧瓶口
C.盛放氢氧化钠溶液的试剂瓶不能使用玻璃塞
D.浓硝酸通常保存在棕色试剂瓶中
4.钠及其化合物应用广泛。下列说法正确的是
A.乙醇和二甲醚互为同系物,可用金属钠鉴别
B.过氧化钠中含有非极性键,属于非极性分子
C.工业上利用侯氏制碱法可以制备碳酸钠, 的空间构型为平面三角形
D.向 稀盐酸中逐滴加入含 的溶液,则混和液中:
5.氯化钠应用广泛,下列说法正确的是
A.侯氏制碱法是将足量CO 通入氨化的氯化钠饱和溶液中,析出NaCO 晶体
2 2 3
B.氯碱工业采用阴离子交换膜电解槽电解饱和食盐水获得氯气和氢氧化钠
C.用洗净的铂丝蘸取某样品在酒精灯上灼烧,火焰呈黄色,该样品一定是氯化钠
D.饱和氯化钠溶液能使蛋白质盐析
6.下列有关现象或事实正确且对应原理也正确的是选
现象或事实 对应的化学或离子方程式
项
A 利用一定浓度的盐酸在玻璃器皿上刻蚀标记
B 向 溶液中通入 ,产生白色沉淀
向 溶液中滴加氯水,溶液颜色变成棕黄
C
色
D 可在呼吸面具中作为氧气的来源
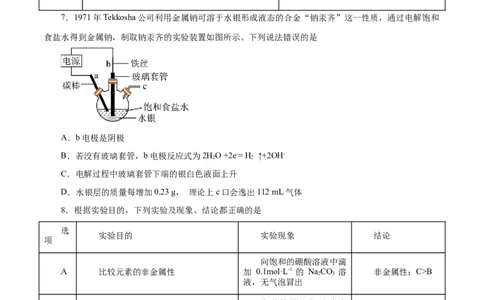
7.1971年Tekkosha公司利用金属钠可溶于水银形成液态的合金“钠汞齐”这一性质,通过电解饱和
食盐水得到金属钠,制取钠汞齐的实验装置如图所示。下列说法错误的是
A.b电极是阴极
B.若没有玻璃套管,b电极反应式为2HO +2e-= H ↑+2OH-
2 2
C.电解过程中玻璃套管下端的银白色液面上升
D.水银层的质量每增加0.23 g, 理论上c口会逸出112 mL气体
8.根据实验目的,下列实验及现象、结论都正确的是
选
实验目的 实验现象 结论
项
向饱和的硼酸溶液中滴
A 比较元素的非金属性 加 0.1mol·L-1 的 NaCO 溶 非金属性:C>B
2 3
液,无气泡冒出
向酸性 KMnO 溶液中
4
滴入FeCl 溶液,紫红色溶 氧 化 性 :
B 比较KMnO 、Cl 和Fe3+的氧化性 2
4 2 液变浅并伴有黄绿色气体产 KMnO > Cl > Fe3+
4 2
生
向1 mL 0.1 mol·L-1的MgCl 溶液中
2 白色沉淀转化成红褐色 K [Mg(OH) ]>
C 滴加 2mL0.2mol·L-1NaOH 溶液,再滴加 sp 2
沉淀 K [(Fe(OH) ]
2滴0.1mol·L-1FeCl 溶液 sp 3
3
用玻璃棒蘸取该溶液在
该溶液中含有钠
D 检验溶液中是否含有钠元素 酒精灯外焰上灼烧,火焰呈
元素
黄色9.下列方程式与所给事实不相符的是
A.硫酸铜溶液中加过量的氨水:
B.向 中投入 固体:
C . 侯 氏 制 碱 法 的 原 理 : 、
D.海水提溴工艺中,用纯碱溶液富集 :
10.已知甲、乙都为单质,丙为化合物,能实现下述转化关系。下列说法正确的是
A.若丙溶于水后得到强碱溶液,则甲可能是O
2
B.若溶液丙遇NaCO 放出气体CO,则甲不可能是H
2 3 2 2
C.若溶液丙中滴加NaOH溶液有蓝色沉淀生成,则甲一定为Cu
D.若溶液丙中滴加NaOH溶液有白色沉淀生成后沉淀溶解,则甲可能为Al
11.某同学在两个相同的特制容器中分别加入 溶液和
溶液,再分别用 盐酸滴定,利用 计和压强传感器检测,得到如图曲线。
已知:常温下,酚酞的变色范围是 ,甲基橙的变色范围是 。下列说法不正确
的是
A. 溶液或 溶液中
B.图中曲线甲和曲线丁表示向 溶液中滴加 盐酸C.在 点发生反应的离子方程式为
D.滴定分析时, 点可用酚酞、 点可用甲基橙作指示剂指示滴定终点
12.利用浓缩海水,模拟侯氏制碱法制备NaHCO ,进一步处理得到产品NaCO 和NH Cl,实验流程
3 2 3 4
如下。
下列说法错误的是
A.将饱和氨盐水雾化后与CO 反应可使反应更快更充分
2
B.制备 NaHCO 的化学方程式为NH +NaCl+HO+CO=NaHCO↓+NHCl
3 3 2 2 3 4
C.流程中“气体”可循环利用
D.将“母液”低温蒸发结晶可得纯净的NH Cl
4
13.已知 。下列说法不正确的是
A.钠在空气中燃烧,产生黄色火焰,生成淡黄色固体
B. 中含有离子键和非极性共价键
C. 中阴阳离子个数比为
D. 可作供氧制,与 反应过程中每生成 转移
14.为除去 溶液中的下列杂质,所选用的试剂正确的是
选
杂质 试剂
项
A 适量的NaOH溶液
B NaOH 适量的 溶液
C NaCl 适量的盐酸D 适量的 溶液
15.下列实验方案中,不能测定出 和 的混合物中 质量分数的是
A.取ag混合物充分加热,质量减少bg
B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体
C.取ag混合物与足量 溶液充分反应,过滤、洗涤、烘干、得到bg固体
D.取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg
16.图示为证明过氧化钠可在呼吸面具和潜水艇中做供氧剂的实验装置图,其中 a装置是实验室制备
二氧化碳的装置,c中盛放的是过氧化钠。下列说法正确的是
A.a中可以用NaCO 和稀盐酸来制备CO
2 3 2
B.b装置中是饱和NaCO 溶液,作用是除去a中产生的HCl
2 3
C.c中只发生2NaO +2CO =2Na CO+O
2 2 2 2 3 2
D.f中收集的气体是纯净的O
2
17.下列物质性质与用途具有对应关系的是
A. 呈淡黄色,可用作供氧剂 B.NaCl熔点较高,可用于制取NaOH
C. 溶液呈碱性,可用于除油污 D. 易分解,可用于治疗胃酸过多
18.氢化钠是一种重要的储氢试剂、缩合剂、还原剂、烷基化试剂,在有机合成中具有重要作用,某
学习小组利用如图装置制备少量氢化钠,下列说法错误的是
A.装置丙中将Na分散到NaCl晶体中可以增大接触面积,使反应更充分
B.装置乙和装置丁内盛放的试剂可以分别为无水氯化钙和碱石灰C.实验过程中应先打开K,一段时间后,尾端验纯后再点燃酒精灯
1
D.m gH 储存到NaH中,与足量水反应也释放m gH ,遵从质量守恒定律
2 2
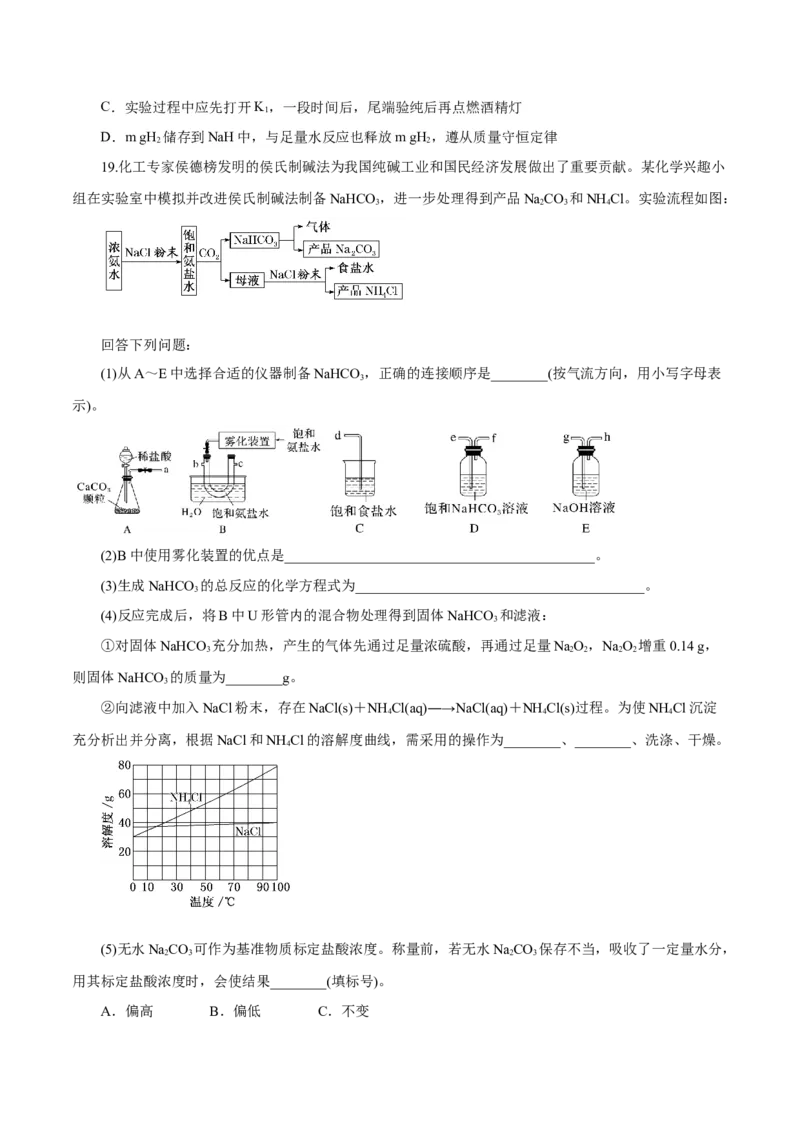
19.化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献。某化学兴趣小
组在实验室中模拟并改进侯氏制碱法制备NaHCO ,进一步处理得到产品NaCO 和NH Cl。实验流程如图:
3 2 3 4
回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO ,正确的连接顺序是________(按气流方向,用小写字母表
3
示)。
(2)B中使用雾化装置的优点是____________________________________________。
(3)生成NaHCO 的总反应的化学方程式为_________________________________________。
3
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO 和滤液:
3
①对固体NaHCO 充分加热,产生的气体先通过足量浓硫酸,再通过足量NaO,NaO 增重0.14 g,
3 2 2 2 2
则固体NaHCO 的质量为________g。
3
②向滤液中加入NaCl粉末,存在NaCl(s)+NH Cl(aq)―→NaCl(aq)+NH Cl(s)过程。为使NH Cl沉淀
4 4 4
充分析出并分离,根据NaCl和NH Cl的溶解度曲线,需采用的操作为________、________、洗涤、干燥。
4
(5)无水NaCO 可作为基准物质标定盐酸浓度。称量前,若无水NaCO 保存不当,吸收了一定量水分,
2 3 2 3
用其标定盐酸浓度时,会使结果________(填标号)。
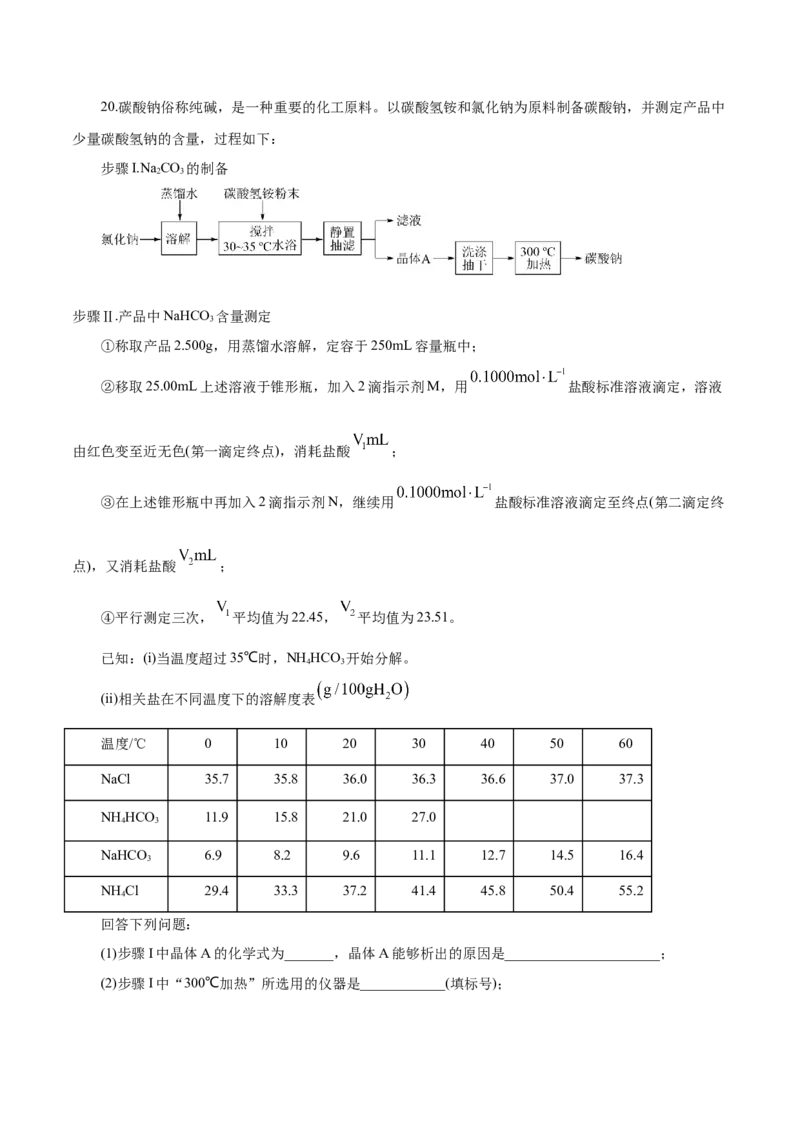
A.偏高 B.偏低 C.不变20.碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定产品中
少量碳酸氢钠的含量,过程如下:
步骤I.Na CO 的制备
2 3
步骤Ⅱ.产品中NaHCO 含量测定
3
①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 盐酸标准溶液滴定,溶液
由红色变至近无色(第一滴定终点),消耗盐酸 ;
③在上述锥形瓶中再加入2滴指示剂N,继续用 盐酸标准溶液滴定至终点(第二滴定终
点),又消耗盐酸 ;
④平行测定三次, 平均值为22.45, 平均值为23.51。
已知:(i)当温度超过35℃时,NH HCO 开始分解。
4 3
(ii)相关盐在不同温度下的溶解度表
温度/℃ 0 10 20 30 40 50 60
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
NH HCO 11.9 15.8 21.0 27.0
4 3
NaHCO 6.9 8.2 9.6 11.1 12.7 14.5 16.4
3
NH Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.2
4
回答下列问题:
(1)步骤I中晶体A的化学式为_______,晶体A能够析出的原因是______________________;
(2)步骤I中“300℃加热”所选用的仪器是____________(填标号);A. B. C. D.
(3)指示剂N为_______,描述第二滴定终点前后颜色变化______________________;
(4)产品中NaHCO 的质量分数为______________________(保留三位有效数字);
3
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则NaHCO 质量分数的计算结果
3
____________(填“偏大”“偏小”或“无影响”)。