文档内容
第 08 讲 金属材料
【化学学科素养】
1.宏观辨识与微观探析:认识金属材料的性能和应用,根据金属及其化合物的性质理解常见金属的冶
炼原理。
2.科学态度与社会责任:根据金属的冶炼原理及方法,认识开发利用金属矿物应具有可持续性,培养
绿色环保意识。
3.科学探究与创新意识:科学领悟铜、铝及其化合物的性质及探究方案并进行实验探究,得出其主要
性质。
【必备知识解读】
一、铝镁的性质及应用
1.金属铝的物理性质
银白色有金属光泽的固体,有良好的延展性、导电性和导热性等,密度较小,质地柔软。
2.金属铝的化学性质
①4Al+3O=====2Al O
2 2 3
②2Al+Fe O=====2Fe+Al O
2 3 2 3
③2Al+6H+===2Al3++3H↑
2
④2Al+2OH-+6HO===2[Al(OH) ]-+3H↑
2 4 2
3.铝热反应
实验装置
①镁带剧烈燃烧,放出大量的热,并发出耀眼的白光,氧化铁与铝粉在
实验现象
较高温度下发生剧烈的反应;②纸漏斗的下部被烧穿,有熔融物落入沙中
高温下,铝与氧化铁发生反应,放出大量的热:Fe O+2Al=====2Fe+
实验结论 2 3
Al O
2 3
①制取熔点较高、活动性弱于Al的金属,如铁、铬、锰、钨等,
原理应用 3MnO +4Al=====3Mn+2Al O;
2 2 3
②金属焊接,如野外焊接钢轨等
4.铝的制备和用途
(1)制备原理电解熔融Al O:2Al O(熔融)=====4Al+3O↑。
2 3 2 3 2
【特别提醒】工业上冶炼Al用电解熔融Al O 而不用AlCl 的原因是AlCl 是共价化合物,熔融态不导
2 3 3 3
电。
(2)铝的用途
纯铝用作导线,铝合金用于制造汽车、飞机、生活用品等。
二、铝的重要化合物
1.氧化铝
(1)物理性质:白色固体,难溶于水,熔点很高。
(2)化学性质
与H+反应Al O+6H+=2Al3++3H O
2 3 2
与强碱反应Al O+2OH-=2AlO-+H O
2 3 2 2
2.氢氧化铝
(1)物理性质:白色胶状不溶于水的固体,有较强的吸附性。
(2)化学性质(用化学方程式表示)
Al(OH) 的电离方程式为
3
酸式电离:Al(OH) +HO [Al(OH) ]-+H+
3 2 4
碱式电离:Al(OH) Al3++3OH-
3
写出图中有关反应的化学方程式或离子方程式:
①Al(OH) +3H+===Al3++3HO。
3 2
②Al(OH) +OH-===[Al(OH) ]-。
3 4
③2Al(OH) =====Al O+3HO。
3 2 3 2
(3)制备
①向铝盐中加入氨水,离子方程式为Al3++3NH ·H O ===Al(OH) ↓+3NH。
3 2 3
②Na[Al(OH) ]溶液中通入足量CO,离子方程式为
4 2
[Al(OH) ]-+CO===Al(OH) ↓+HCO。
4 2 3
③Na[Al(OH) ]溶液与AlCl 溶液混合:3[Al(OH) ]-+Al3+===4Al(OH) ↓。
4 3 4 3
3.常见的铝盐
(1)硫酸铝钾是由两种不同的金属离子和一种酸根离子组成的复盐。
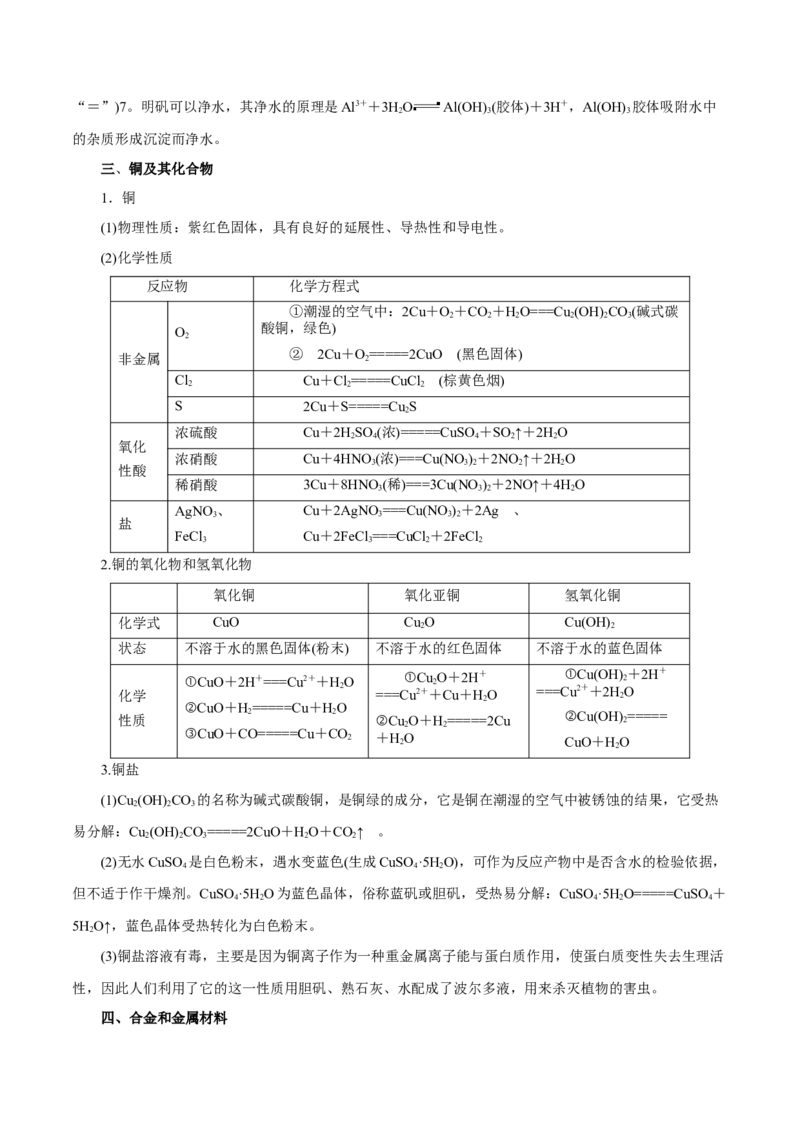
(2)明矾的化学式为KAl(SO )·12H O,它是无色晶体,可溶于水,水溶液pH<(填“<”“>”或
4 2 2“=”)7。明矾可以净水,其净水的原理是Al3++3HO Al(OH) (胶体)+3H+,Al(OH) 胶体吸附水中
2 3 3
的杂质形成沉淀而净水。
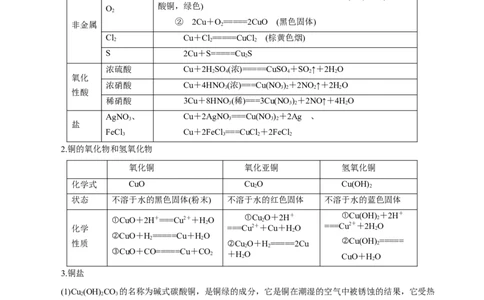
三、铜及其化合物
1.铜
(1)物理性质:紫红色固体,具有良好的延展性、导热性和导电性。
(2)化学性质
反应物 化学方程式
①潮湿的空气中:2Cu+O+CO+HO===Cu (OH) CO(碱式碳
2 2 2 2 2 3
O
酸铜,绿色)
2
非金属 ② 2Cu+O 2 =====2CuO (黑色固体)
Cl Cu+Cl=====CuCl (棕黄色烟)
2 2 2
S 2Cu+S=====Cu S
2
浓硫酸 Cu+2HSO (浓)=====CuSO +SO ↑+2HO
2 4 4 2 2
氧化
浓硝酸 Cu+4HNO(浓)===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
性酸
稀硝酸 3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO
3 3 2 2
AgNO、 Cu+2AgNO===Cu(NO )+2Ag 、
3 3 3 2
盐
FeCl Cu+2FeCl ===CuCl +2FeCl
3 3 2 2
2.铜的氧化物和氢氧化物
氧化铜 氧化亚铜 氢氧化铜
化学式 CuO Cu O Cu(OH)
2 2
状态 不溶于水的黑色固体(粉末) 不溶于水的红色固体 不溶于水的蓝色固体
①CuO+2H+===Cu2++HO ①Cu 2 O+2H+ ①Cu(OH) 2 +2H+
化学 2 ===Cu2++Cu+H 2 O ===Cu2++2H 2 O
②CuO+H=====Cu+HO
性质 2 2 ②Cu O+H=====2Cu ②Cu(OH) 2 =====
2 2
③CuO+CO=====Cu+CO
2 +H 2 O CuO+H 2 O
3.铜盐
(1)Cu (OH) CO 的名称为碱式碳酸铜,是铜绿的成分,它是铜在潮湿的空气中被锈蚀的结果,它受热
2 2 3
易分解:Cu (OH) CO=====2CuO+HO+CO↑ 。
2 2 3 2 2
(2)无水CuSO 是白色粉末,遇水变蓝色(生成CuSO ·5H O),可作为反应产物中是否含水的检验依据,
4 4 2
但不适于作干燥剂。CuSO ·5H O为蓝色晶体,俗称蓝矾或胆矾,受热易分解:CuSO ·5H O=====CuSO +
4 2 4 2 4
5HO↑,蓝色晶体受热转化为白色粉末。
2
(3)铜盐溶液有毒,主要是因为铜离子作为一种重金属离子能与蛋白质作用,使蛋白质变性失去生理活
性,因此人们利用了它的这一性质用胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的害虫。
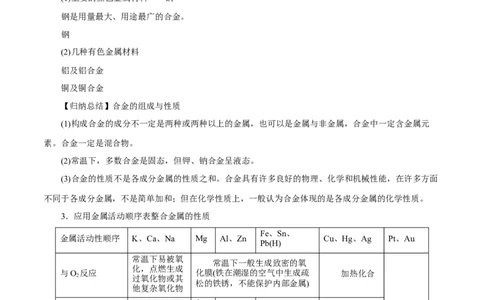
四、合金和金属材料1.合金
(1)概念:合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
(2)性能:合金具有不同于各成分金属的物理、化学性能或机械性能。
①熔点:一般比它的各成分金属的低;
②硬度和强度:一般比它的各成分金属的大。
2.常见金属材料及应用
金属材料—
(1)重要的黑色金属材料——钢
钢是用量最大、用途最广的合金。
钢
(2)几种有色金属材料
铝及铝合金
铜及铜合金
【归纳总结】合金的组成与性质
(1)构成合金的成分不一定是两种或两种以上的金属,也可以是金属与非金属,合金中一定含金属元
素。合金一定是混合物。
(2)常温下,多数合金是固态,但钾、钠合金呈液态。
(3)合金的性质不是各成分金属的性质之和。合金具有许多良好的物理、化学和机械性能,在许多方面
不同于各成分金属,不是简单加和;但在化学性质上,一般认为合金体现的是各成分金属的化学性质。
3.应用金属活动顺序表整合金属的性质
Fe、Sn、
金属活动性顺序 K、Ca、Na Mg Al、Zn Cu、Hg、Ag Pt、Au
Pb(H)
常温下易被氧
常温下一般生成致密的氧
化,点燃生成
与O 反应 化膜(铁在潮湿的空气中生成疏 加热化合
2 过氧化物或其
松的铁锈,不能保护内部金属)
他复杂氧化物
与
热 有碱存 不反应
常温下生 与高温水蒸气
与HO反应 水 在与水 不反应
2 成碱和氢气 反应
反 反应
应
与非氧化性酸反
生成盐和氢气 生成盐和氢气 不反应
应
先与水反应,
与盐溶液反应 生成的碱再与 排在前面的金属能把排在后面的金属从其盐溶液中置换出来
盐反应
【关键能力拓展】一、铝、镁的化学性质
铝 镁
2Mg+O=====2MgO
2
与非金属反应 能被Cl、O 氧化
2 2
3Mg+N=====MgN
2 3 2
能与沸水反应
与水反应 反应很困难
Mg+2HO=====Mg(OH) +H↑
2 2 2
与碱反应 能溶于强碱溶液 不反应
与某些氧化物 能与Fe O、MnO 、Cr O 等金
能在CO
2
中燃烧:
2 3 2 2 3
反应 属氧化物发生铝热反应 2Mg+CO=====2MgO+C
2
二、铝与酸或碱反应生成H 的量的关系
2
2Al+6HCl===2AlCl +3H↑
3 2
2Al+2NaOH+6HO===2Na[Al(OH) ]+3H↑
2 4 2
(1)等质量的铝与足量的盐酸、氢氧化钠溶液分别反应:
①产生H 的物质的量相等。
2
②消耗H+、OH-的物质的量之比为n(H+)∶n(OH-)=3∶1。
(2)足量的铝分别与等物质的量的HCl和NaOH反应:
①消耗Al的物质的量之比为1∶3。
②生成H 的物质的量之比为1∶3。
2
(3)一定量的铝分别与一定量的盐酸、氢氧化钠溶液反应:
若产生氢气的体积比为<<1,则必定
①铝与盐酸反应时,铝过量而HCl不足。
②铝与氢氧化钠溶液反应时,铝不足而NaOH过量。
三、数形结合与“铝三角”
1.Al3+、Al(OH) 、[Al(OH) ]-之间的转化关系
3 4
(1)①Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②Al3++3[Al(OH) ]-===4Al(OH) ↓
4 3
③Al3++3OH-===Al(OH) ↓
3(2)Al(OH) +3H+===Al3++3HO
3 2
(3)Al3++4OH-===[Al(OH) ]-
4
(4)[Al(OH)]-+4H+===Al3++4HO
4 2
(5)①[Al(OH) ]-+CO===Al(OH) ↓+HCO
4 2 3
②[Al(OH)]-+H+===Al(OH) ↓+HO
4 3 2
(6)Al(OH) +OH-===[Al(OH) ]-
3 4
2.铝三角的应用
(1)选择制备Al(OH) 的最佳途径
3
①由Al3+制备Al(OH) ,宜用Al3+与氨水反应:
3
Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②由NaAlO 制备Al(OH) 宜用CO 与AlO反应:
2 3 2
2HO+AlO+CO===Al(OH) ↓+HCO
2 2 3
③从节约原料角度,由Al制备Al(OH) ,宜用Al制备Al3+,Al制备AlO,然后将二者混合:
3
Al3++3AlO+6HO===4Al(OH) ↓
2 3
(2)有关离子共存问题
①与Al3+不能大量共存的(阴)离子有:OH-、AlO、HS-、SiO、CO、HCO、SO等。
②与AlO不能大量共存的(阳)离子有:H+、Al3+、NH、Fe2+、Fe3+等。
③AlO与HCO因发生(相对)强酸制弱酸的反应而不能共存。
(3)分析离子反应顺序
①向含有Al3+、NH、H+的混合溶液中逐滴加入NaOH溶液,反应顺序是:Ⅰ.H++OH-===HO;
2
Ⅱ.Al3++3OH-===Al(OH) ↓(若先与NH反应,则生成的NH ·H O又使Al3+沉淀且生成NH);Ⅲ.NH+OH-
3 3 2
===NH ·H O[若先溶解Al(OH) ,则产生的AlO又与NH反应生成沉淀];Ⅳ.Al(OH) +OH-===AlO+
3 2 3 3
2HO。
2
②向含有AlO、CO、OH-的混合溶液中逐滴加入盐酸,反应顺序是:Ⅰ.OH-+H+===HO;Ⅱ.AlO+
2
H++HO===Al(OH) ↓(AlO比CO先反应);Ⅲ.CO+H+===HCO;Ⅳ.HCO+H+===CO ↑+HO[HCO比
2 3 2 2
Al(OH) 先反应];Ⅴ.Al(OH) +3H+===Al3++3HO。
3 3 2
四、金属活动顺序与金属冶炼的关系
①热分解法:适用于不活泼的金属,如Hg和Ag。由HgO冶炼Hg的化学方程式:2HgO=====2Hg+
O↑;由Ag O冶炼Ag的化学方程式:2Ag O=====4Ag+O↑。
2 2 2 2②热还原法:用还原剂(C、CO、H、Al等)还原金属氧化物,适合较活泼的金属。
2
完成冶炼铁、锌、钨的化学方程式:
a.CO还原Fe O:Fe O+4CO=====3Fe+4CO;
3 4 3 4 2
b.C还原ZnO:ZnO+C=====Zn+CO↑;
c.H 还原WO:WO+3H=====W+3HO。
2 3 3 2 2
③电解法:适合冶炼金属活动性很强的金属(一般指在金属活动性顺序中排在锌前面的金属)。
工业上用电解法冶炼Na、Mg、Al的化学方程式分别为2NaCl(熔融)=====2Na+Cl↑、
2
MgCl (熔融)=====Mg+Cl↑、2Al O=====4Al+3O↑。
2 2 2 3 2
【方法技巧】有些很活泼的金属也可以用还原法来冶炼,如
Na+KCl=====K↑+NaCl
2RbCl+Mg========MgCl +2Rb↑等,
2
主要运用了化学平衡移动原理,利用K、Rb沸点低,汽化离开反应体系,使化学反应得以向正反应方
向进行。
五、铝与盐酸、NaOH溶液反应的应用与定量关系
2Al+6H+===2Al3++3H↑
2
2Al+2OH-+2HO===2AlO+3H↑
2 2
(1)等量的铝分别与足量的盐酸和氢氧化钠溶液反应,消耗HCl和NaOH的物质的量之比为3∶1。
(2)等量的铝分别与足量的盐酸和氢氧化钠溶液反应,产生氢气的体积比为V (H )∶V (H )=1∶1。
HCl 2 NaOH 2
(3)足量的铝分别与等物质的量的盐酸和氢氧化钠溶液反应,产生氢气的体积比为V (H )∶V (H )
HCl 2 NaOH 2
=1∶3。
(4)一定量的铝分别与一定量的盐酸和氢氧化钠溶液反应,若产生氢气的体积比为
1∶3