文档内容
第 15 讲 化学反应的热效应
1.下列过程所发生的反应中,属于吸热反应的是
A.木炭燃烧 B.酸碱中和
C.炸药爆炸 D.Ba(OH) ·8H O和NH Cl混合搅拌
2 2 4
2.下列有关反应 的说法正确的是
A.该反应是吸热反应
B.生成物的总键能小于反应物的总键能
C.反应物总能量高于生成物总能量
D.涉及的四种物质均属于电解质
3.下列反应中生成物总能量高于反应物总能量的是
A.碳酸钙受热分解 B.甲烷燃烧
C.铝粉与氧化铁粉末反应 D.铁粉与硫粉反应
4.下列说法或表示方法正确的是
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(s,石墨)=C(s,金刚石)ΔH=+1.90kJ·mol-1可知,金刚石比石墨稳定
C.在101kPa时,2gH 完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为
2
2H(g)+O(g)=2HO(l)ΔH=-285.8kJ·mol-1
2 2 2
D.在稀溶液中,H+(aq)+OH-(aq)=H O(l)ΔH=-57.3kJ·mol-1,若将含0.5molHSO 的浓硫酸与含
2 2 4
1molNaOH的溶液混合,放出的热量大于57.3kJ
5.热化学离不开实验,更离不开对反应热的研究。下列有关说法正确的是
A.向甲的试管A中加入某一固体和液体,若注射器的活塞右移,说明A中发生了吸热反应
B.将甲虚线框中的装置换为乙装置,若注射器的活塞右移,说明锌粒和稀硫酸的反应为放热反应C.用丙装置进行中和反应热的测定实验时,NaOH要缓缓倒入稀硫酸中
D.用丙装置进行中和反应热的测定实验时,每次实验要测量并记录三次温度数值
6.已知正丁烷、异丁烷燃烧的热化学方程式分别为:
下列说法不正确的是
A.正丁烷分子储存的能量大于异丁烷分子
B.正丁烷的稳定性大于异丁烷
C.异丁烷转化为正丁烷的过程是一个吸热过程
D.异丁烷和正丁烷属于同分异构体
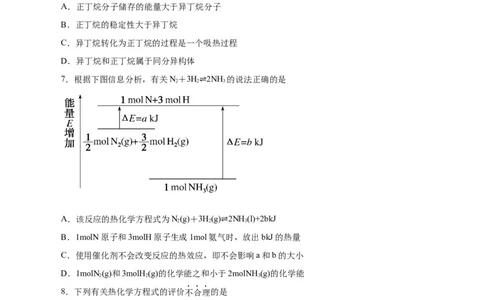
7.根据下图信息分析,有关N+3H 2NH 的说法正确的是
2 2 3
⇌
A.该反应的热化学方程式为N(g)+3H(g) 2NH (l)+2bkJ
2 2 3
B.1molN原子和3molH原子生成1mol氨气⇌时,放出bkJ的热量
C.使用催化剂不会改变反应的热效应,即不会影响a和b的大小
D.1molN (g)和3molH (g)的化学能之和小于2molNH (g)的化学能
2 2 3
8.下列有关热化学方程式的评价不合理的是
选
实验事实 热化学方程式 评价
项
与足量水完全反应生成
A 正确
,放出热量260.6kJ
B 热值为 正确
C
已知 不正确;因,将稀硫酸与稀氢氧 为同时还生成了
化钡溶液混合 硫酸钡沉淀
不正确;明
已知25℃、101kPa下,120g石墨 确的同素异形体
D
完全燃烧放出热量3935.1kJ 要注名称:C(s,
石墨)
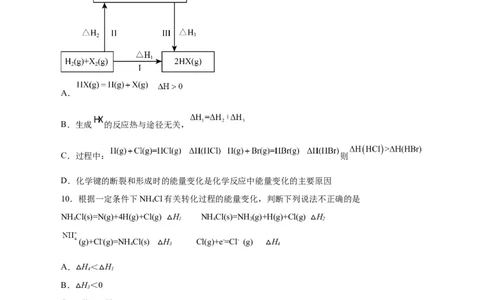
9.图为卤素单质( )和 反应的转化过程,相关说法不正确的是
A.
B.生成 的反应热与途径无关,
C.过程中: 则
D.化学键的断裂和形成时的能量变化是化学反应中能量变化的主要原因
10.根据一定条件下NH Cl有关转化过程的能量变化,判断下列说法不正确的是
4
NH Cl(s)=N(g)+4H(g)+Cl(g) H NH Cl(s)=NH (g)+H(g)+Cl(g) H
4 1 4 3 2
△ △
(g)+Cl-(g)=NH Cl(s) H Cl(g)+e-=Cl- (g) H
4 3 4
△ △
A. H< H
4 1
B.△H<0△
3
C.△H< H
1 2
D.△相同条△件下,NH Br和NH I也进行类似转化,NH Br的 H 比NH I的大
4 4 4 2 4
11.已知中和热的数值是57.3kJ/mol。下列反应物混合时,产△生的热量等于57.3kJ的是( )
A.1mol/L稀HCl(aq)和1mol/L稀NaOH(aq)
B.500mL2.0mol/L的HCl(aq)和500mL2.1mol/L的NaOH(aq)
C.500mL2.0mol/L的CHCOOH(aq)和500mL2.0mol/L的NaOH(aq)
3
D.1mol/L稀CHCOOH(aq)和1mol/L稀NaOH(aq)
312.根据能量变化示意图(如图所示),下列说法不正确的是
A.相同质量的 和 ,前者具有的能量较高
B.破坏相同物质的量的 和 中所有的化学键,后者所需的能量高
C.
D. ,则
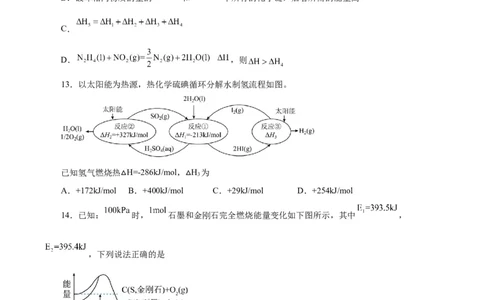
13.以太阳能为热源,热化学硫碘循环分解水制氢流程如图。
已知氢气燃烧热 H=-286kJ/mol, H 为
3
A.+172kJ/mol △B.+400kJ/mol△ C.+29kJ/mol D.+254kJ/mol
14.已知: 时, 石墨和金刚石完全燃烧能量变化如下图所示,其中 ,
,下列说法正确的是
A. C(s,金刚石)比C(s,石墨)更稳定
B. (s,石墨)转化为C(s,金刚石),放热
C. 时, 完全分解为 (s,石墨)和 吸热D.C(s,石墨)与C(s,金刚石)互为同分异构体
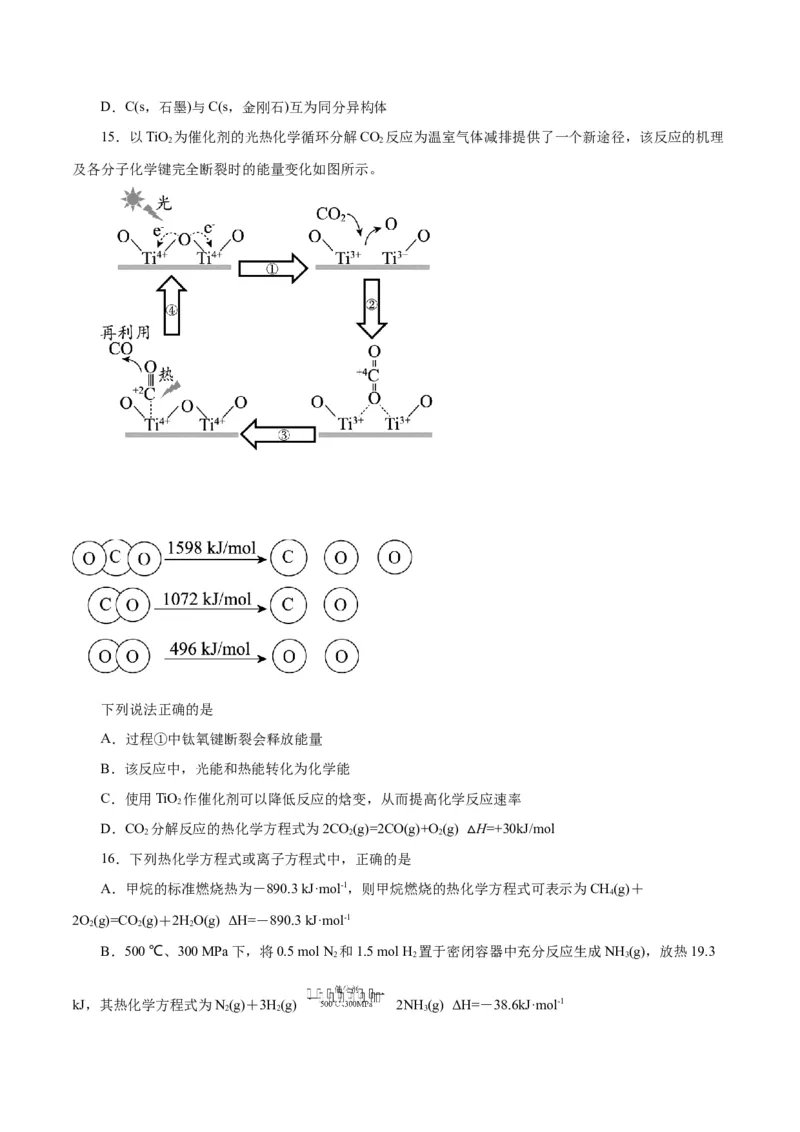
15.以TiO 为催化剂的光热化学循环分解CO 反应为温室气体减排提供了一个新途径,该反应的机理
2 2
及各分子化学键完全断裂时的能量变化如图所示。
下列说法正确的是
A.过程①中钛氧键断裂会释放能量
B.该反应中,光能和热能转化为化学能
C.使用TiO 作催化剂可以降低反应的焓变,从而提高化学反应速率
2
D.CO 分解反应的热化学方程式为2CO(g)=2CO(g)+O(g) H=+30kJ/mol
2 2 2
16.下列热化学方程式或离子方程式中,正确的是 △
A.甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH(g)+
4
2O(g)=CO (g)+2HO(g) ΔH=-890.3 kJ·mol-1
2 2 2
B.500 ℃、300 MPa下,将0.5 mol N 和1.5 mol H 置于密闭容器中充分反应生成NH (g),放热19.3
2 2 3
kJ,其热化学方程式为N(g)+3H(g) 2NH (g) ΔH=-38.6kJ·mol-1
2 2 3C.氯化镁溶液与氨水反应:Mg2++2OH-=Mg(OH) ↓
2
D.氧化铝溶于NaOH溶液:A1 O+2OH-=2AlO +HO
2 3 2
17.N(g)与H(g)化合生成NH (g)的过程能量变化如下图所示,有关说法正确的是
2 2 3
A.使用催化剂会改变反应的热效应
B.反应的热化学方程式为:N(g)+3H(g) 2NH (g)+2bkJ
2 2 3
C.1molN(g)和3molH(g)生成1molNH (g)时,放出bkJ热量
3
D.1molN (g)和3molH (g)的能量之和小于2molNH (g)的能量
2 2 3
18.下列依据热化学方程式得出的结论正确的是
A.若2H(g)+O(g)=2HO(g) ΔH=-483.6kJ·mol-1,则H 的标准燃烧热为-241.8kJ·mol-1
2 2 2 2
B.若C(石墨;s)=C(金刚石,s) ΔH>0,则石墨比金刚石稳定
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H O(l) ΔH=-57.4kJ·mol-1,则20.0gNaOH固体与稀盐酸完全中
2
和,放出28.7kJ的热量
D.已知2C(s)+2O(g)=2CO (g) ΔH;2C(s)+O(g)=2CO(g) ΔH,则ΔH>ΔH
2 2 l 2 2 l 2
19.利用化学反应为人类生产生活提供能量。
(1)下列反应中,属于放热反应的是 (填序号)。
①生石灰和水反应②二氧化碳与炽热的炭反应③氢氧化钠溶于水④炸药爆炸⑤碳酸钙高温分解⑥葡萄
糖的缓慢氧化⑦ 和 反应
(2)①在如图所示的量热计中,将100mL0.50mol·L-1CHCOOH溶液与100mL0.55mol·L-1NaOH溶液混
3
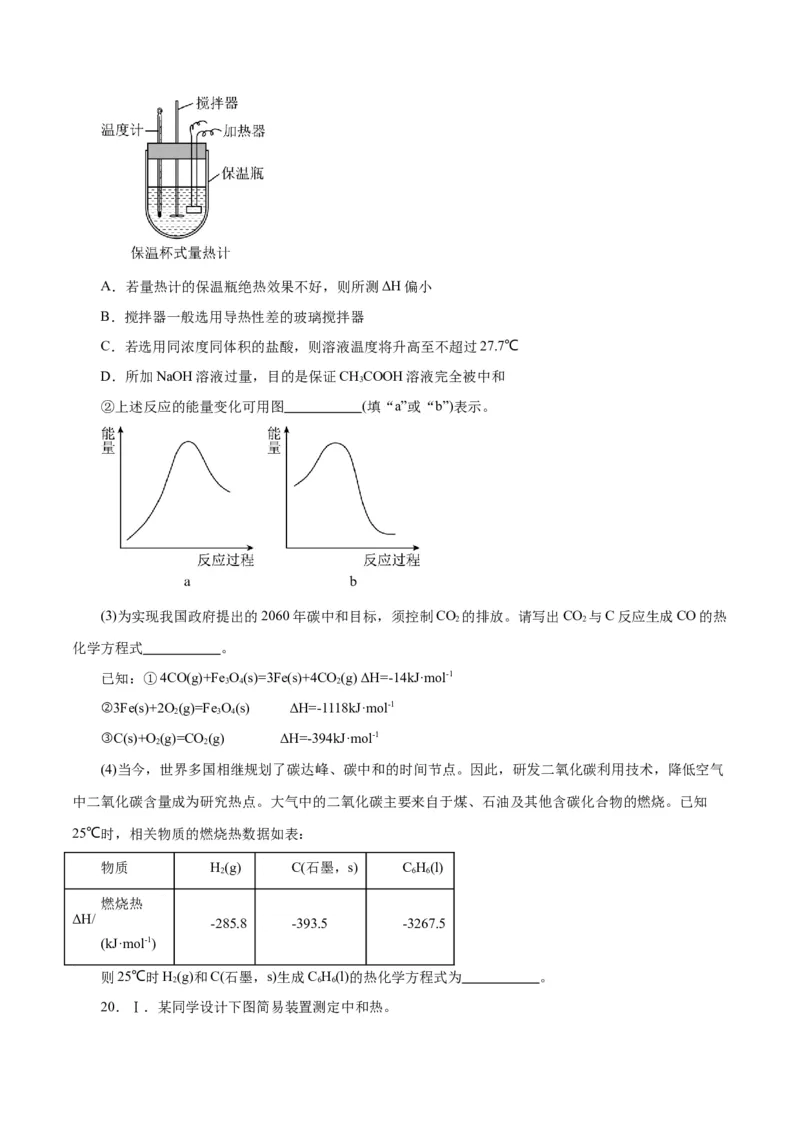
合,温度从25.0℃升高到27.7℃。下列说法错误的是A.若量热计的保温瓶绝热效果不好,则所测ΔH偏小
B.搅拌器一般选用导热性差的玻璃搅拌器
C.若选用同浓度同体积的盐酸,则溶液温度将升高至不超过27.7℃
D.所加NaOH溶液过量,目的是保证CHCOOH溶液完全被中和
3
②上述反应的能量变化可用图 (填“a”或“b”)表示。
(3)为实现我国政府提出的2060年碳中和目标,须控制CO 的排放。请写出CO 与C反应生成CO的热
2 2
化学方程式 。
已知:①4CO(g)+Fe O(s)=3Fe(s)+4CO (g) ΔH=-14kJ·mol-1
3 4 2
②3Fe(s)+2O (g)=Fe O(s) ΔH=-1118kJ·mol-1
2 3 4
③C(s)+O (g)=CO (g) ΔH=-394kJ·mol-1
2 2
(4)当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气
中二氧化碳含量成为研究热点。大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知
25℃时,相关物质的燃烧热数据如表:
物质 H(g) C(石墨,s) C H(l)
2 6 6
燃烧热
ΔH/
-285.8 -393.5 -3267.5
(kJ·mol-1)
则25℃时H(g)和C(石墨,s)生成C H(l)的热化学方程式为 。
2 6 6
20.Ⅰ.某同学设计下图简易装置测定中和热。回答下列问题:
(1)该装置中缺少的仪器是 。
(2)50mL0.10mol/L的盐酸与50mL0.11mol/L的NaOH溶液混合后,测得反应放出的热量为285J,则中
和热 。若将环形玻璃搅拌棒换为金属搅拌棒,则测得反应放出的热量将 (填
“偏多”“偏少”或“不变”)。
Ⅱ.2021年世界环境日中国主题:人与自然和谐共生。
(3)以 为催化剂的光热化学循环分解 反应为温室气体的减排提供了一个新途径,断开各分子中
1mol化学键吸收的能量如下表所示,则以 为催化剂分解 生成 和 的热化学方程式
为 。
化学键 C=O C≡O(CO) O=O
能量/ 799 1072 496
(4)以太阳能为热源,金属氧化物为催化剂可以分解水制 和 ,实现能源绿色化,其过程如下:
过程Ⅰ: ,
过程Ⅱ: ,
总反应: ,
则过程Ⅱ的 。
Ⅲ.(5)已知强酸与强碱在稀溶液中反应的中和热可表示为: ,对于下列反应:
,
,
, 上述反应均在溶液中进行,则下列
、 、 的关系正确的是_______。
A. B. C. D.