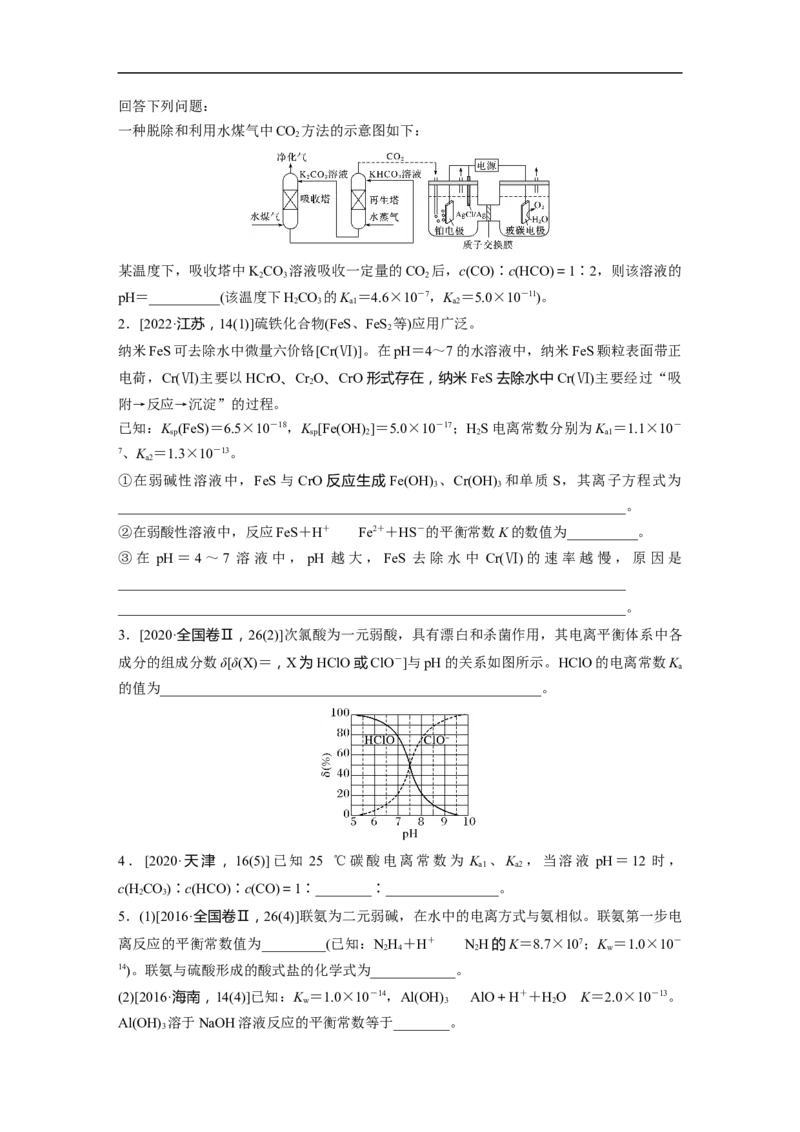
文档内容
[复习目标] 1.理解电离常数、水解常数、溶度积常数的概念及影响因素。2.掌握电离常数、
水解常数、溶度积常数的相关计算。
1.电离常数(K )与电离度(α)的关系(以一元弱酸HA为例)
电离
HA H+ + A-
起始浓度: c 0 0
酸
平衡浓度: c ·(1-α) c ·α c ·α
酸 酸 酸
K ==。
电离
若α很小,可认为1-α≈1,则K =c ·α2(或α=)。
电离 酸
2.电离常数与水解常数的关系
(1)对于一元弱酸HA,K 与K 的关系
a h
HAH++A-,K(HA)=;A-+HOHA+OH-,K (A-)=。则K·K =c(H+)·c(OH-)=
a 2 h a h
K ,故K =。
w h
常温时K·K =K =1.0×10-14,K =。
a h w h
(2)对于二元弱酸HB,K (H B)、K (H B)与K (HB-)、K (B2-)的关系
2 a1 2 a2 2 h h
HB-+HOHB+OH-,K (HB-)===。
2 2 h
B2-+HOHB-+OH-,K (B2-)===。
2 h
考向拓展 常温时,对于一元弱酸HA,当K>1.0×10-7时,K <1.0×10-7,此时将等物质
a h
的量浓度的HA溶液与NaA溶液等体积混合,HA的电离程度大于A-的水解程度,溶液呈
酸性;同理,当K<1.0×10-7时,K >1.0×10-7,A-的水解程度大于HA的电离程度,溶液
a h
呈碱性。对于多元弱酸,K =,K 是其阴离子结合一个H+所形成的粒子的电离常数。
h a
[实例]
按要求回答下列问题。
(1)已知在25 ℃时,碳酸和亚硫酸的电离平衡常数如表所示:
电解质 碳酸 亚硫酸
K =4.30×10-7 K =1.00×10-2
a1 a1
电离常数
K =5.61×10-11 K =1.02×10-7
a2 a2
①NaHSO 水解反应的平衡常数K =_______________________________________。
3 h②HSO 溶液和NaHCO 溶液反应的主要离子方程式为__________________________
2 3 3
________________________________________________________________________。
(2)已知HNO 的电离常数K=7.1×10-4;NH ·H O的电离常数K =1.7×10-5;则0.1 mol·L-1
2 a 3 2 b
NH NO 溶液中离子浓度由大到小的顺序是_____________________________________。
4 2
常温下NO水解反应的平衡常数K =______(结果保留两位有效数字)。
h
3.溶度积常数(K )的相关计算
sp
(1)M(OH) 悬浊液中K 、K 、pH间的关系
n sp w
M(OH) (s)Mn+(aq)+nOH-(aq)
n
K =c(Mn+)·cn(OH-)=·cn(OH-)==()n+1。
sp
(2)K 与溶解度(S)之间的计算关系
sp
对于AB型物质,其K =2。
sp
如60 ℃时溴酸银(AgBrO )的溶解度为0.6 g,则K 约等于________________。
3 sp
(3)K 与沉淀转化平衡常数K的计算关系
sp
建立K 与K的关系,一般是在K的表达式分子分母中同乘以某个离子的浓度,将分子分母
sp
转化为不同物质的K 。
sp
如在1.0 L Na CO 溶液中溶解0.01 mol BaSO ,列式计算,NaCO 溶液的最初浓度不得低于
2 3 4 2 3
______ mol·L-1[忽略溶液体积变化,已知:K (BaSO)=1.1×10-10、K (BaCO)=5.1×10-
sp 4 sp 3
9]。
(4)K 与电离常数K 的计算关系
sp a
根据电离常数计算出各离子浓度,进而计算K 。
sp
如汽车尾气中的SO 可用石灰水吸收,生成亚硫酸钙浊液。常温下,测得 CaSO 与水形成的
2 3
浊液pH为9,忽略SO的第二步水解,则K (CaSO)=________(结果保留3位有效数字)。
sp 3
[已知:K (H SO )=1.54×10-2,K (H SO )=1.02×10-7]
a1 2 3 a2 2 3
(5)判断沉淀转化能否进行
已知:常温下,ZnS和CuS的K 分别为1.6×10-24和6.4×10-36,判断常温下反应ZnS+
sp
CuSO ===CuS+ZnSO 能否进行。
4 4
该反应的平衡常数
K==
==
=2.5×1010>105,故该反应能完全转化。
若计算沉淀转化的平衡常数K<10-5,则转化反应不能进行,若10-5