文档内容
第 24 讲 沉淀溶解平衡
1.下列对“难溶”的理解正确的是
A.“难溶”是指物质常温时在水中溶解的质量小于0.01g
B.在水中难溶的物质,也难溶于其他溶剂
C.只有难溶的物质才能建立溶解平衡
D.相同条件下,难溶的物质更容易形成饱和溶液
2.在一定温度下,当Mg(OH) 固体在水溶液中达到下列平衡时:Mg(OH) (s) Mg2+(aq)+2OH-(aq),要
2 2
使Mg(OH) 固体减少而c(Mg2+)不变,可采取的措施是
2
A.加MgSO 固体 B.通HCl气体 C.加NaOH固体 D.加少量水
4
3.在一定温度下,氯化银在水中存在如下沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl—(aq),若把AgCl分别
放入①100mL0.1mol/LNaNO 溶液中;②100mL0.1mol/LNaCl溶液中;③100mL0.1mol/LAlCl 溶液中;
3 3
④100mL0.1mol/LMgCl 溶液中,搅拌后在相同的温度下Ag+浓度由大到小的顺序是:
2
A.①>②>④>③ B.②>①>④>③
C.④>③>②>① D.①>④>③>②
4.室温下,用饱和 溶液浸泡 粉末,一段时间后过滤,向滤渣中加入足量稀盐酸、产生气
泡,固体未完全溶解。已知 , 。下列说法正确的是
A.滤渣中加入醋酸发生反应的离子方程式:
B.饱和 溶液中存在:
C.反应 正向进行,需满足
D.过滤后所得溶液中一定存在 且
5.下列对沉淀溶解平衡的描述正确的是
A.达到平衡时,沉淀溶解和离子沉淀停止
B.达到平衡时,溶液中溶质的离子浓度相等
C.加水时,溶解平衡向溶解方向移动D.升高温度,溶解平衡向溶解方向移动
6.在FeS悬浊液中,存在平衡FeS(s) Fe2+(aq)+S2-(aq)。欲使FeS固体质量减少,Fe2+浓度不变,可向悬
浊液中加入的试剂是 ⇌
A.CuSO 溶液 B.盐酸 C.蒸馏水 D.NaS
4 2
7.t℃时, 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.t℃时, 的Ksp数量级是10-9
B.t℃时:的平衡常数 (t℃时 )
C.t℃时,用 液滴定 和 的混合液, 先沉
淀
D.在饱和 溶液中加入 固体可使溶液由Y点到X点
8.某兴趣小组进行下列实验:
①将0.1 mol·L-1 MgCl 溶液和0.5 mol·L-1 NaOH溶液等体积混合得到浊液
2
②取少量①中浊液,滴加0.1 mol·L-1 FeCl 溶液,出现红褐色沉淀
3
③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1 FeCl 溶液,白色沉淀变为红褐色沉淀
3
④另取少量白色沉淀,滴加饱和NH Cl溶液,沉淀溶解
4
下列说法中不正确的是
A.将①中所得浊液过滤,所得滤液中含少量Mg2+
B.①中浊液中存在沉淀溶解平衡:
Mg(OH) (s) Mg2+(aq)+2OH-(aq)
2
C.实验②和⇌③均能说明Fe(OH)
3
比Mg(OH)
2
难溶
D.NH Cl溶液中的NH 可能是④中沉淀溶解的原因
49.根据下列图示,相应叙述正确的是
A.图甲表示一定温度下,CHCOOH稀溶液加水时溶液导电性变化,a点pH值大于b点
3
B.图乙表示一定温度下,MCO (M:Mg2+、Ca2+)的沉淀溶解平衡曲线,则K (MgCO )<K (CaCO)
3 sp 3 sp 3
C.图丙是稀释相同体积、相同pH的HNO 和CHCOOH稀溶液时,溶液的pH随加水体积的变化,所含
2 3
溶质的物质的量浓度x点小于y点
D.图丁中,曲线B对应温度下,将0.02mol·L-1Ba(OH) 溶液与等物质的量浓度的NaHSO 溶液等体积混合
2 4
后,混合溶液的pH=12
10.已知25 ℃时,AgCl的溶度积K =1.8×10-10 mol2·L-2,则下列说法正确的是
sp
A.向饱和AgCl水溶液中加入盐酸,K 值变大
sp
B.AgNO 溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-)
3
C.温度一定,当溶液中c(Ag+)·c(Cl-)=K 时,此溶液为AgCl饱和溶液
sp
D.将固体AgCl加入到KI溶液中,固体由白色变为黄色,AgCl完全转化为AgI,AgCl的溶解度小于AgI
的溶解度
11.下列有关AgCl沉淀的溶解平衡说法正确的是
A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.继续加水,AgCl沉淀的溶解度增大
D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度不变
12.已知几种难溶电解质的溶度积常数K (25℃)见表,下列叙述不正确的是
sp
难溶电解
AgCl AgBr AgI Ag SO Ag CrO
质 2 4 2 4
K 1.8×10-10 5.4×10-13 8.5×10-17 1.4×10-5 1.12×10-12
sp
A.由溶度积常数可判断在相同条件下一些同类型物质的溶解性大小
B.将浓度均为4×10-3mol·L-1的AgNO 溶液和KCrO 溶液等体积混合,有Ag CrO 沉淀产生
3 2 4 2 4
C.向AgCl的悬浊液中滴加饱和NaBr溶液可以得到黄色AgBr悬浊液
D.向100mL0.1mol·L-1的NaSO 溶液中加入1mL0.lmol·L-1的AgNO 溶液,有白色沉淀生成
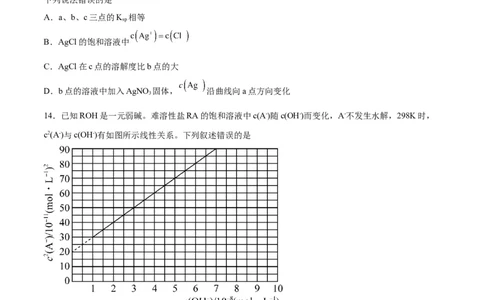
2 4 313.一定温度下, 体系中, 和 的关系如图所示。
下列说法错误的是
A.a、b、c三点的K 相等
sp
B.AgCl的饱和溶液中
C.AgCl在c点的溶解度比b点的大
D.b点的溶液中加入AgNO 固体, 沿曲线向a点方向变化
3
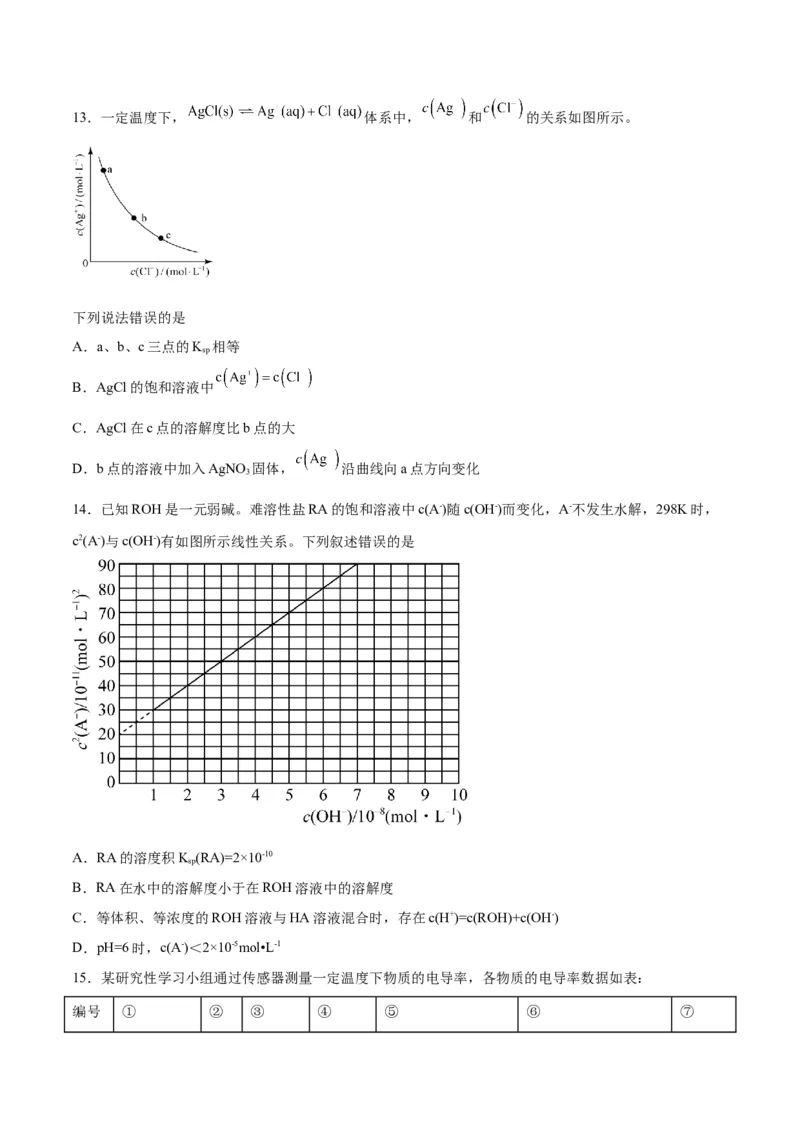
14.已知ROH是一元弱碱。难溶性盐RA的饱和溶液中c(A-)随c(OH-)而变化,A-不发生水解,298K时,
c2(A-)与c(OH-)有如图所示线性关系。下列叙述错误的是
A.RA的溶度积K (RA)=2×10-10
sp
B.RA在水中的溶解度小于在ROH溶液中的溶解度
C.等体积、等浓度的ROH溶液与HA溶液混合时,存在c(H+)=c(ROH)+c(OH-)
D.pH=6时,c(A-)<2×10-5mol•L-1
15.某研究性学习小组通过传感器测量一定温度下物质的电导率,各物质的电导率数据如表:
编号 ① ② ③ ④ ⑤ ⑥ ⑦CaCO CaSO AgCl
3 4
CaCO (固 0.001mol·L-1NaCl溶 0.001mol·L-1AgNO 溶
物质 3 HO 3
体) 2 饱和溶 饱和溶 液 液 饱和溶
液 液 液
电导
0 7 37 389 1989 1138 13
率
下列分析不正确的是
A.依据表中数据分析,CaCO 固体中不存在能自由移动的离子
3
B.对比②和⑦,说明⑦中存在:AgCl=Ag++Cl-
C.对比③和④,可推出该温度下,K (CaCO <K (CaSO)
sp 3) sp 4
D.⑤、⑥等体积混合后过滤,推测滤液的电导率等于13
16.某污水处理厂用“ 沉淀法”处理含铬废水(主要含 以及少量 、 )的工艺流程如图所
示:
已知:①金属离子 、 、 沉淀完全时( )pH分别为6.7、5.6、2.8。
② 。
下列说法错误的是
A.“氧化”时生成 的离子方程式为
B.“沉降”过程中加入NaOH溶液,调节溶液pH>6.7
C.加入 生成 ,说明
D.“沉铬”过程中,增大溶液的pH,沉铬率提高
17.某温度下,向体积均为20.00 mL、浓度均为0.1 mol·L-1的NaCl、NaCrO 溶液中分别滴加0.1 mol·L-1
2 4
的AgNO 溶液,滴定过程中的pX(pX=-lgX,X=Cl-、CrO )与滴加AgNO 溶液体积关系如图所示
3 3
(lg3=0.47)。下列说法错误的是A.a=1 B.曲线I表示NaCl溶液
C.K (Ag CrO)=1.0×10-2b D.M约为2c-1.47
sp 2 4
18.25 ℃和100 ℃两种情况下,碳酸钙在水中的溶解平衡曲线如图所示。下列说法正确的是
A.100℃时,d点已经饱和,会有沉淀析出
B.25℃时,CaCO 的K =2.8×10-9
3 sp
C.25℃时加入NaCO,可以使溶液由c点变为d点
2 3
D.升高温度可以使溶液由a点变为曲线上的任一点
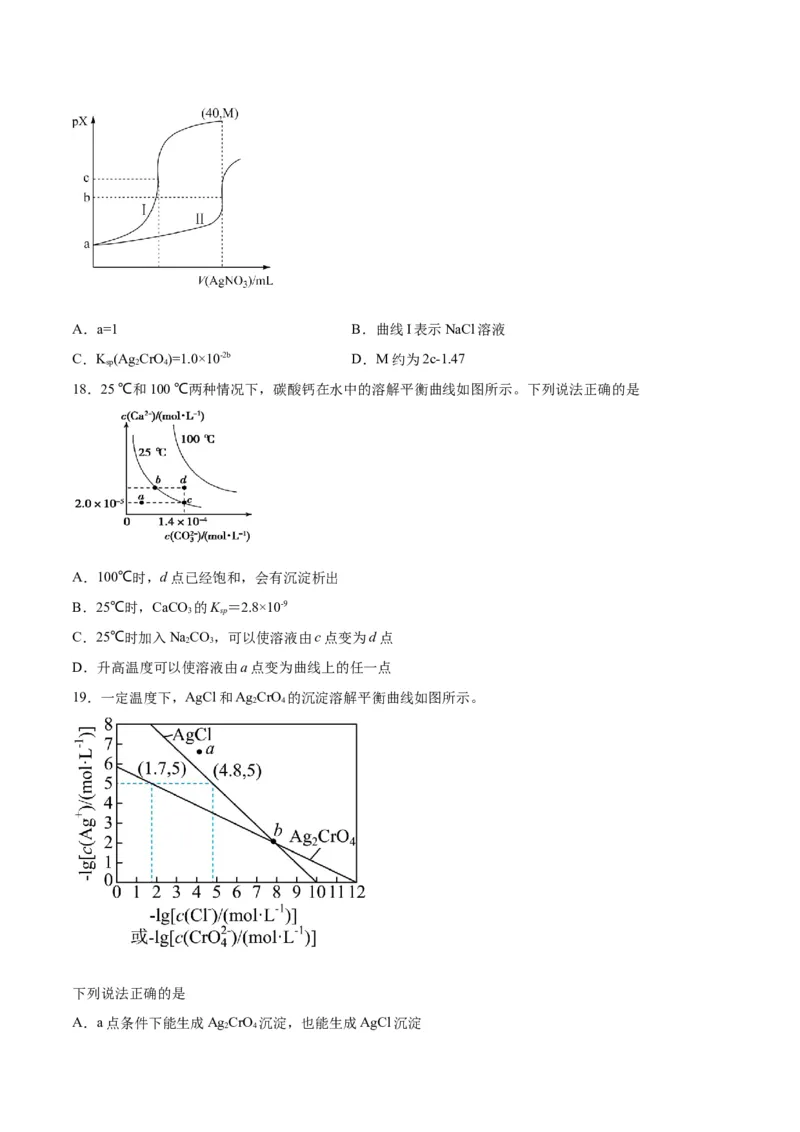
19.一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所示。
2 4
下列说法正确的是
A.a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4B.b点时,c(Cl-)=c(CrO ),K (AgCl)=K (Ag CrO)
sp sp 2 4
C.Ag CrO+2Cl- 2AgCl+CrO 的平衡常数K=107.9
2 4
D.向NaCl、NaCrO 均为0.1mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO 沉淀
2 4 3 2 4
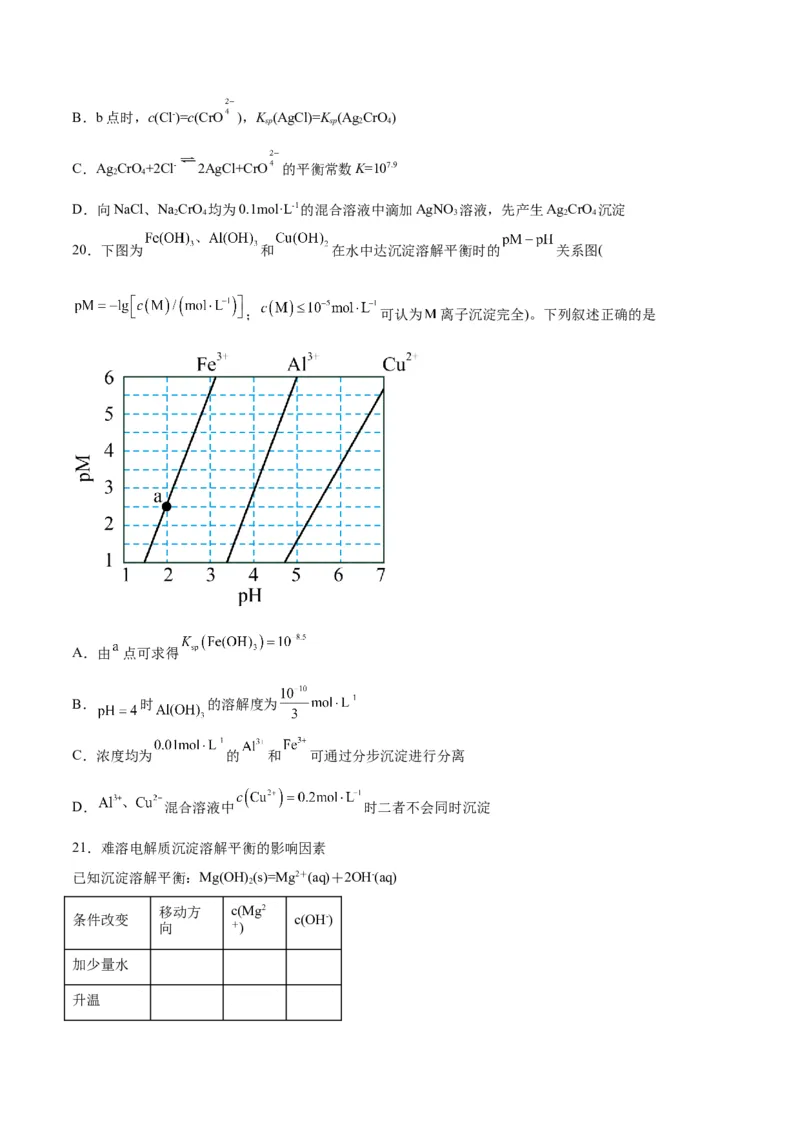
20.下图为 和 在水中达沉淀溶解平衡时的 关系图(
; 可认为 离子沉淀完全)。下列叙述正确的是
A.由 点可求得
B. 时 的溶解度为
C.浓度均为 的 和 可通过分步沉淀进行分离
D. 混合溶液中 时二者不会同时沉淀
21.难溶电解质沉淀溶解平衡的影响因素
已知沉淀溶解平衡:Mg(OH) (s)=Mg2+(aq)+2OH-(aq)
2
移动方 c(Mg2
条件改变 c(OH-)
向 +)
加少量水
升温加MgCl (s)
2
加盐酸
加NaOH(s)
Q:离子积对于A B (s)=mAn+(aq)+nBm-(aq)任意时刻Q=cm(An+)·cn(Bm-)。
m n
(1)Q>K ,溶液过饱和,有 析出,直至溶液 ,达到新的平衡。
sp
(2)Q=K ,溶液饱和,沉淀与溶解处于 。
sp
(3)Q”“=”或“<”) 。
③当向含有相同浓度的 、 、 的溶液中滴加 溶液时, (填离子符号)先沉淀。④要使0.2 溶液中 沉淀完全,则应向溶液中加入 溶液使溶液的 不低于
(保留1位小数)。