文档内容
第 24 讲 沉淀溶解平衡
【化学学科素养】
1.变化观念与平衡思想:认识难溶电解质的溶解有一定限度,是可以调控的。能多角度、动态地分析
难溶电解质的沉淀溶解平衡,并运用难溶电解质的沉淀溶解平衡原理解决实际问题(如利用生成沉淀处理
污水等)。
2.科学研究与创新意识:能发现和提出有关难溶电解质的沉淀溶解平衡的判断问题;能从问题和假设
出发,确定探究目的,设计探究方案,进行沉淀转化等实验探究。
【必备知识解读】
一、沉淀溶解平衡的基本概念
1.溶解平衡的定义
杨sir化学,侵权必究
在一定温度下,当难溶电解质溶于水形成饱和溶液时,溶质的离子与该固态溶质之间建立的动态平
衡,叫作沉淀溶解平衡。
2. 沉淀溶解平衡方程式
M A(s) mMn+(aq) + nAm-(aq)
m n
如AgCl沉淀溶解平衡:AgCl(s) Ag+(aq) + Cl-(aq)
二、沉淀溶解平衡及应用
1.难溶、可溶、易溶界定:
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:
2.沉淀溶解平衡
(1)溶解平衡的建立
(2)特点(同其他化学平衡):逆、等、定、动、变(适用平衡移动原理)
3.影响沉淀溶解平衡的因素
(1)内因难溶电解质本身的性质,这是决定因素。
(2)外因
①浓度:加水稀释,平衡向沉淀溶解的方向移动;
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向沉淀溶解的方向移动;
③同离子效应:向平衡体系中加入难溶物溶解产生的离子,平衡向生成沉淀的方向移动;
④其他:向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡向
沉淀溶解的方向移动。
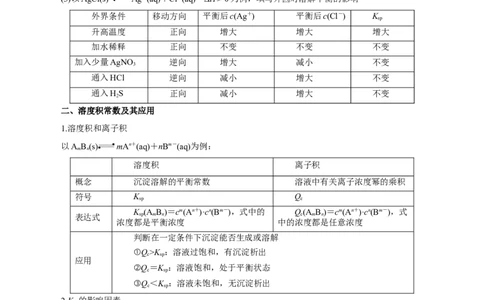
(3)以AgCl(s) Ag+(aq)+Cl-(aq) ΔH>0为例,填写外因对溶解平衡的影响
外界条件 移动方向 平衡后c(Ag+) 平衡后c(Cl-) K
sp
升高温度 正向 增大 增大 增大
加水稀释 正向 不变 不变 不变
加入少量AgNO 逆向 增大 减小 不变
3
通入HCl 逆向 减小 增大 不变
通入HS 正向 减小 增大 不变
2
二、溶度积常数及其应用
1.溶度积和离子积
以A B (s ) mAn+(aq)+nBm-(aq)为例:
m n
溶度积 离子积
概念 沉淀溶解的平衡常数 溶液中有关离子浓度幂的乘积
符号 K Q
sp c
K (A B )=cm(An+)·cn(Bm-),式中的 Q(A B )=cm(An+)·cn(Bm-),式
表达式 sp m n c m n
浓度都是平衡浓度 中的浓度都是任意浓度
判断在一定条件下沉淀能否生成或溶解
①Q>K :溶液过饱和,有沉淀析出
c sp
应用
②Q=K :溶液饱和,处于平衡状态
c sp
③Q<K :溶液未饱和,无沉淀析出
c sp
2.K 的影响因素
sp
(1)内因:难溶物质本身的性质,这是主要决定因素。
(2)外因
①浓度:加水稀释,平衡向溶解方向移动,但K 不变。
sp
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向溶解方向移动,K 增大。
sp
③其他:向平衡体系中加入可与体系中某些离子反应生成更难溶物质或更难电离物质或气体的离子时,
平衡向溶解方向移动,但K 不变。
sp
3. 意义对于相同类型的难溶电解质,K 越大,说明难溶电解质在水中的溶解能力越大。
sp
如:K (AgCl) > K (AgBr) > K (AgI),则溶解度:S (AgCl) > S (AgBr) > S (AgI)。
sp sp sp
4.应用
① M m A n (s) ⇌ mMn+(aq) + nAm-(aq),任意时刻的离子积:Q = cm(Mn+)·cn(Am-)
② 根据K 和Q的相对大小,可以判断给定条件下溶液中难溶电解质的沉淀或溶解情况:
sp
Q > K ,溶液中有沉淀析出
sp 杨sir化学,侵权必究
Q = K ,沉淀与溶解处于平衡状态
sp
Q < K ,溶液中无沉淀析出
sp
【关键能力拓展】
一、沉淀的生成
1.应用
在无机物的制备和提纯、废水处理等领域,常利用生成沉淀来达到分离或除去某些离子的目的。
杨sir化学,侵权必究
2.方法
(1)调节pH法
如:除去NH Cl溶液中的FeCl 杂质,可加入氨水调节pH至7~8,离子方程式为
4 3
Fe3++3NH ·H O===Fe(OH) ↓+3NH。
3 2 3
(2)沉淀剂法
如:用HS沉淀Cu2+,离子方程式为HS+Cu2+===CuS↓+2H+。
2 2
二、沉淀的溶解
1.原理
根据平衡移动原理,对于在水中难溶的电解质,如果能设法不断地移去平衡体系中的相应离子,使平
衡向沉淀溶解的方向移动,就可以使沉淀溶解。
(1)酸溶解法
如:CaCO 溶于盐酸,离子方程式为CaCO +2H+===Ca2++HO+CO↑。
3 3 2 2
(2)盐溶液溶解法
如:Mg(OH) 溶于NH Cl溶液,离子方程式为Mg(OH) +2NH===Mg2++2NH ·H O。
2 4 2 3 2
(3)氧化还原溶解法
如:不溶于盐酸的硫化物CuS溶于稀HNO。3CuS + 8HNO === 3Cu(NO ) + 3S + 2NO↑+ 4H O
3 3 3 2 2
(4)配位溶解法
如:AgCl溶于氨水,离子方程式为AgCl+2NH ·H O===[Ag(NH)]++Cl-+2HO。
3 2 3 2 2
三、沉淀的转化
1. AgCl、AgI、Ag S的转化
2 杨sir化学,侵权必究
如:AgNO 溶液――→AgCl(白色沉淀)――→AgBr(浅黄色沉淀)――→AgI(黄色沉淀)――→Ag S(黑色
3 2沉淀)。
2. 实质、条件、规律
① 实质:沉淀溶解平衡的移动(沉淀的溶解度差别越大,越容易转化)。
② 条件:两种沉淀的溶解度不同。
② 规律:溶解度小的沉淀转化为溶解度更小的沉淀容易实现,溶解度相差越大,转化越容易。
3. 沉淀转化的应用
(1)锅炉除水垢(含有CaSO)
4 杨sir化学,侵权必究
① 操作:先加NaCO 溶液,再加稀盐酸
2 3
② 原理:CaSO 4 (s) + Na 2 CO 3 ⇌ CaCO 3 (s) + Na 2 SO 4 CaCO 3 + 2HCl===CaCl 2 + H 2 O + CO 2 ↑
(2)自然界中矿物的转化
氧化、淋滤 渗透、遇闪锌矿(ZnS)和方铅矿(PbS)
原生铜的硫化物 CuSO 溶液 铜蓝(CuS)
4
CuSO (aq) + ZnS (s) CuS(s) + ZnSO (aq);CuSO (aq) + PbS(s) CuS (s) + PbSO (s)
4 ⇌ 4 4 ⇌ 4
(3)氟化物预防龋齿
① 牙齿表面的釉质层,只要成分是难溶的羟基磷灰石[Ca (PO )(OH)]。
5 4 3
② 口腔中的有机酸使釉质层溶解:Ca (PO )(OH) + 4H+ === 5Ca2+ + 3HPO2- + HO
5 4 3 4 2
③ 氟离子能与羟基磷灰石反应,生成溶解度更小的氟磷灰石,更能抵抗酸的腐蚀。
【核心题型例解】
高频考点一 沉淀溶解平衡
【例1】(2023·全国甲卷第7题)下图为 和 在水中达沉淀溶解平衡时
的 关系图( ; 可认为 离子沉淀完全)。下
列叙述正确的是A. 由 点可求得
B. 时 的溶解度为
C. 浓度均为 的 和 可通过分步沉淀进行分离
D. 混合溶液中 时二者不会同时沉淀
【变式探究】下列有关BaSO 沉淀的溶解平衡状态的说法中,正确的是
4
A.BaSO 沉淀的生成和溶解不断进行,但速率相等
4
B.BaSO 难溶于水,溶液中没有Ba2+和SO
4
C.升高温度,BaSO 的溶解度不变
4
D.向BaSO 沉淀的溶解平衡体系中加入NaSO 固体,BaSO 的溶解度不变
4 4 4
高频考点二 影响沉淀溶解平衡的因素
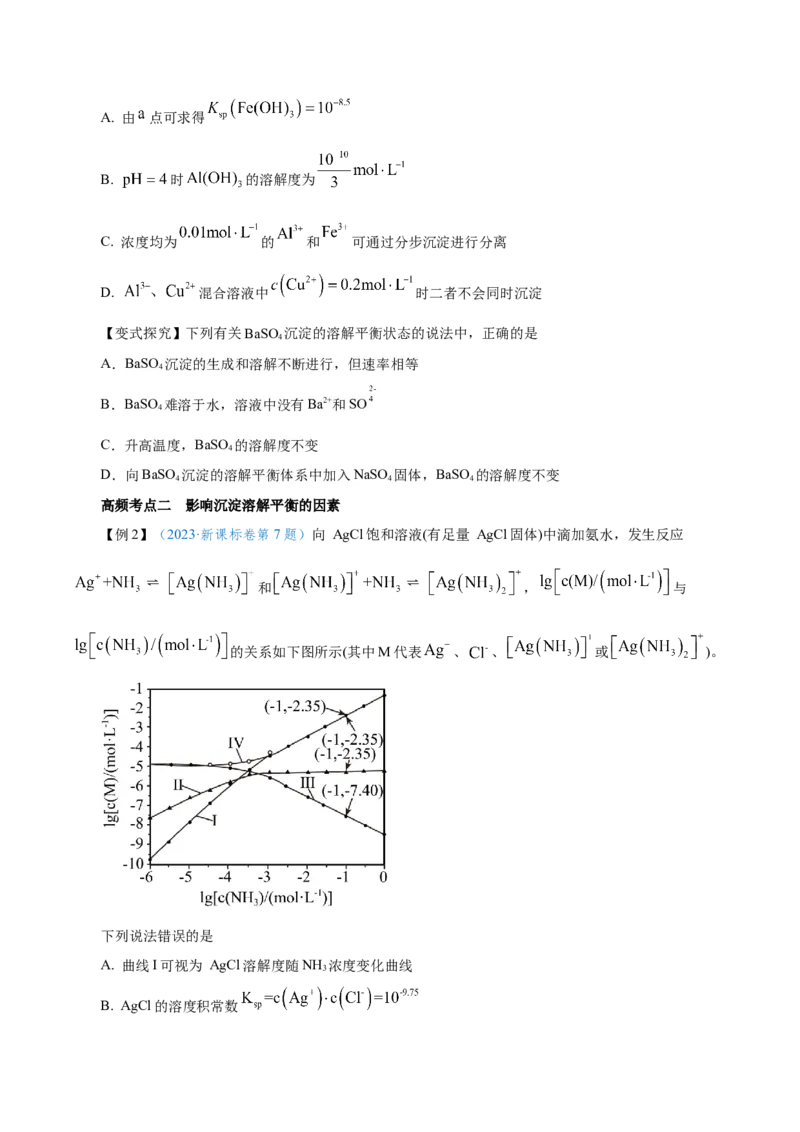
【例2】(2023·新课标卷第7题)向 AgCl饱和溶液(有足量 AgCl固体)中滴加氨水,发生反应
和 , 与
的关系如下图所示(其中M代表 、 、 或 )。
下列说法错误的是
A. 曲线I可视为 AgCl溶解度随NH 浓度变化曲线
3
B. AgCl的溶度积常数C. 反应 的平衡常数K的值为
D. 时,溶液中
【变式探究】某兴趣小组进行下列实验:
①将0.1 mol·L-1 MgCl 溶液和0.5 mol·L-1 NaOH溶液等体积混合得到浊液
2
②取少量①中的浊液,滴加0.1 mol·L-1 FeCl 溶液,出现红褐色沉淀
3
③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1 FeCl 溶液,白色沉淀变为红褐色沉淀
3
④另取少量白色沉淀,滴加饱和NH Cl溶液,沉淀溶解
4
下列说法中不正确的是 ( )
A.将①中所得浊液过滤,所得滤液中含少量Mg2+
B.①中浊液中存在沉淀溶解平衡:Mg(OH) (s ) Mg2+(aq)+2OH-(aq)
2
C.实验②和③均能说明Fe(OH) 比Mg(OH) 难溶
3 2
D.NH Cl溶液中的NH可能是④中沉淀溶解的原因
4
高频考点二 沉淀溶解平衡的应用
【例2】(2023·浙江选考1月第15题)碳酸钙是常见难溶物,将过量碳酸钙粉末置于水中达到溶解平
衡: [已知 , ,
的电离常数 ],下列有关说法正确的是( )
A. 上层清液中存在
B. 上层清液中含碳微粒最主要以 形式存在
C. 向体系中通入CO 气体,溶液中 保持不变
2
D. 通过加 溶液可实现 向 的有效转化
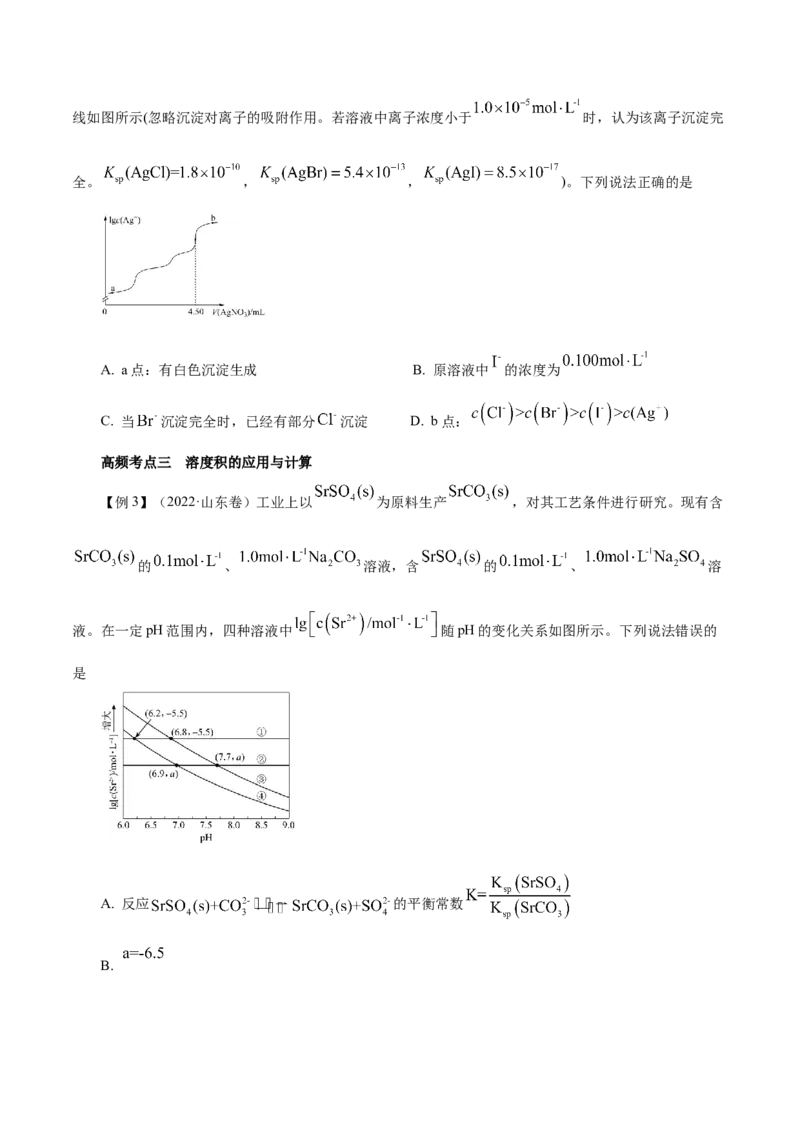
【变式探究】(2022·湖南卷)室温时,用 的标准 溶液滴
定 浓度相等的 、 和 混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作用。若溶液中离子浓度小于 时,认为该离子沉淀完
全。 , , )。下列说法正确的是
A. a点:有白色沉淀生成 B. 原溶液中 的浓度为
C. 当 沉淀完全时,已经有部分 沉淀 D. b点:
高频考点三 溶度积的应用与计算
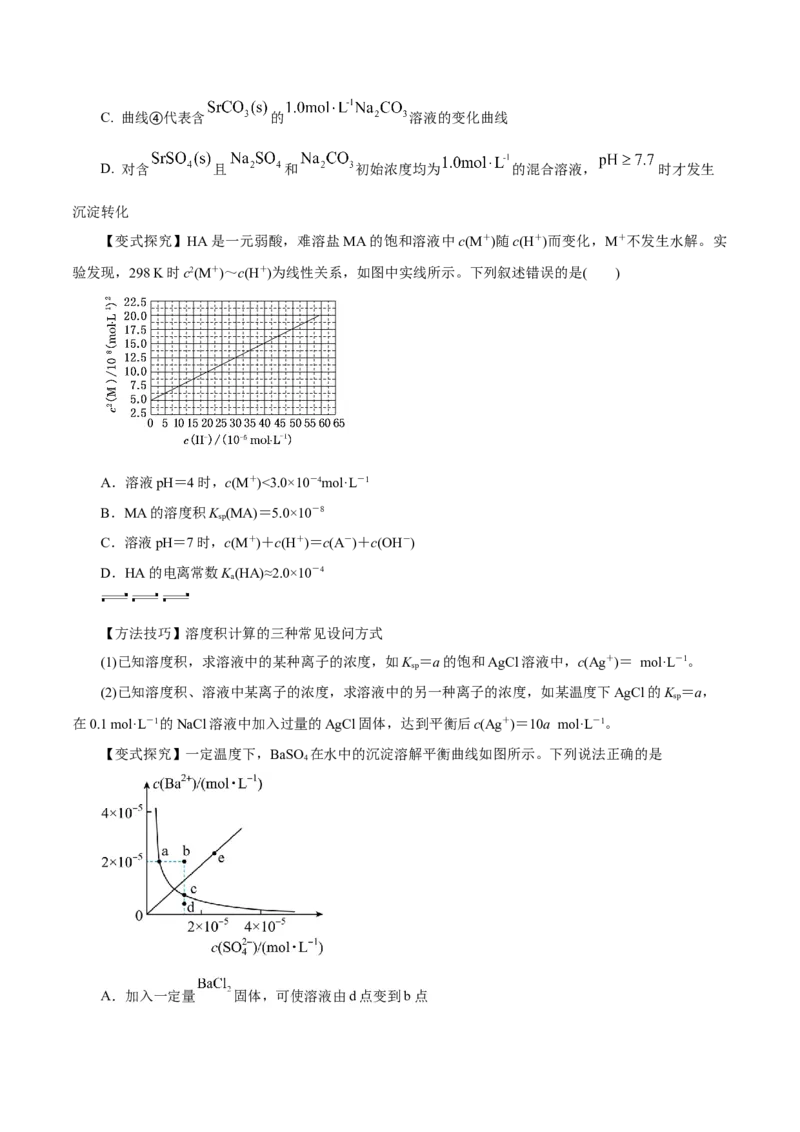
【例3】(2022·山东卷)工业上以 为原料生产 ,对其工艺条件进行研究。现有含
的 、 溶液,含 的 、 溶
液。在一定pH范围内,四种溶液中 随pH的变化关系如图所示。下列说法错误的
是
A. 反应 的平衡常数
B.C. 曲线④代表含 的 溶液的变化曲线
D. 对含 且 和 初始浓度均为 的混合溶液, 时才发生
沉淀转化
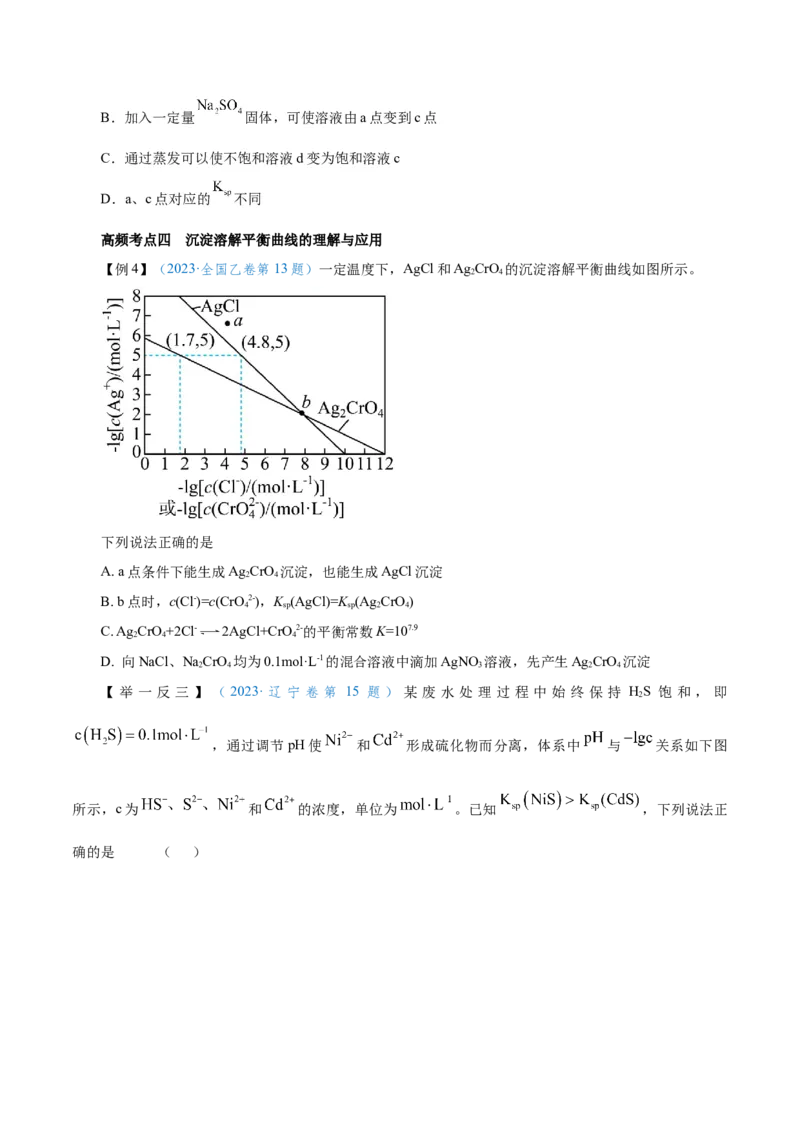
【变式探究】HA是一元弱酸,难溶盐MA的饱和溶液中c(M+)随c(H+)而变化,M+不发生水解。实
验发现,298 K时c2(M+)~c(H+)为线性关系,如图中实线所示。下列叙述错误的是( )
A.溶液pH=4时,c(M+)<3.0×10-4mol·L-1
B.MA的溶度积K (MA)=5.0×10-8
sp
C.溶液pH=7时,c(M+)+c(H+)=c(A-)+c(OH-)
D.HA的电离常数K(HA)≈2.0×10-4
a
【方法技巧】溶度积计算的三种常见设问方式
(1)已知溶度积,求溶液中的某种离子的浓度,如K =a的饱和AgCl溶液中,c(Ag+)= mol·L-1。
sp
(2)已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度,如某温度下AgCl的K =a,
sp
在0.1 mol·L-1的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=10a mol·L-1。
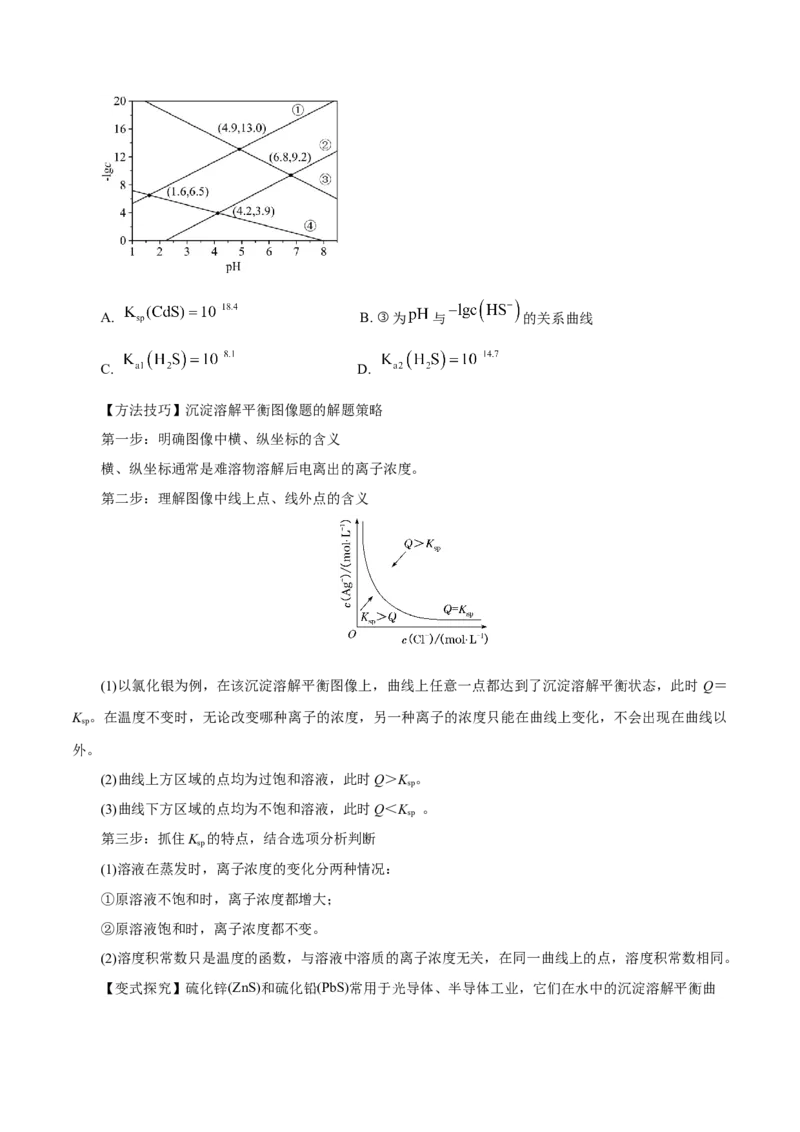
【变式探究】一定温度下,BaSO 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
4
A.加入一定量 固体,可使溶液由d点变到b点B.加入一定量 固体,可使溶液由a点变到c点
C.通过蒸发可以使不饱和溶液d变为饱和溶液c
D.a、c点对应的 不同
高频考点四 沉淀溶解平衡曲线的理解与应用
【例4】(2023·全国乙卷第13题)一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所示。
2 4
下列说法正确的是
A. a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4
B. b点时,c(Cl-)=c(CrO 2-),K (AgCl)=K (Ag CrO)
4 sp sp 2 4
C. Ag CrO+2Cl- 2AgCl+CrO 2-的平衡常数K=107.9
2 4 4
D. 向NaCl、NaCrO 均为0.1mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO 沉淀
2 4 3 2 4
【 举 一 反 三 】 ( 2023· 辽 宁 卷 第 15 题 ) 某 废 水 处 理 过 程 中 始 终 保 持 HS 饱 和 , 即
2
,通过调节pH使 和 形成硫化物而分离,体系中 与 关系如下图
所示,c为 和 的浓度,单位为 。已知 ,下列说法正
确的是 ( )A. B. ③为 与 的关系曲线
C. D.
【方法技巧】沉淀溶解平衡图像题的解题策略
第一步:明确图像中横、纵坐标的含义
横、纵坐标通常是难溶物溶解后电离出的离子浓度。
第二步:理解图像中线上点、线外点的含义
(1)以氯化银为例,在该沉淀溶解平衡图像上,曲线上任意一点都达到了沉淀溶解平衡状态,此时 Q=
K 。在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变化,不会出现在曲线以
sp
外。
(2)曲线上方区域的点均为过饱和溶液,此时Q>K 。
sp
(3)曲线下方区域的点均为不饱和溶液,此时Q<K 。
sp
第三步:抓住K 的特点,结合选项分析判断
sp
(1)溶液在蒸发时,离子浓度的变化分两种情况:
①原溶液不饱和时,离子浓度都增大;
②原溶液饱和时,离子浓度都不变。
(2)溶度积常数只是温度的函数,与溶液中溶质的离子浓度无关,在同一曲线上的点,溶度积常数相同。
【变式探究】硫化锌(ZnS)和硫化铅(PbS)常用于光导体、半导体工业,它们在水中的沉淀溶解平衡曲线如图所示。已知: ,M为Zn或Pb,pM表示 。下列说法正确的是
A.曲线Ⅱ代表PbS的沉淀溶解平衡曲线
B.n、q两点溶液中的 :n