文档内容
第 25 讲 常见仪器使用和实验基本操作
1.某试剂瓶标签上安全标志如图,该试剂是( )
A.氨水 B.乙酸
C.氢氧化钠 D.硝酸
【答案】D
【解析】氨水具有腐蚀性,但不具有氧化性,A不符合题意;乙酸具有腐蚀性,但不具有氧化性,B
不符合题意;氢氧化钠具有腐蚀性,但不具有氧化性,C不符合题意;硝酸具有腐蚀性,同时具有氧化
性,D符合题意。
2.下列有关仪器的名称、图形、用途与使用操作的叙述均正确的是( )
选项 A B C D
名称 250 mL容量瓶 长颈漏斗 酸式滴定管 冷凝管
图形
配制1.0 mol·L-1 NaCl 用酒精萃取碘水
可用于量取
用途与使 溶液,定容时仰视刻 中的碘,分液 蒸馏实验中将蒸
10.00 mL高锰酸
用操作 度线,则配得的溶液 时,碘层需从下 气冷凝为液体
钾溶液
浓度大于1.0 mol·L-1 口放出
【答案】C
【解析】定容时仰视刻度线,溶液体积偏大致使溶液的浓度偏低,A项错误;该仪器为分液漏斗且酒
精不能萃取碘水中的碘,B项错误;高锰酸钾具有强氧化性,能腐蚀橡胶,可用酸式滴定管量取,C项正
确;蒸馏实验中水从冷凝管的下口进上口出,D项错误。
3.球形干燥管是中学化学常用的一种玻璃仪器。下列有关球形干燥管的创新用途,错误的是( )
选项 装置 用途A 用于尾气处理,防倒吸
B 用于铜丝与Cl 反应,防污染
2
C 简易的天然水净化过滤器
D 用NaCO 固体与稀硫酸反应制备CO 气体,可随制随停
2 3 2
【答案】D
【解析】球形干燥管的球形结构在尾气处理时可以防倒吸,A、B正确;活性炭具有吸附性,装置可
作简易的天然水净化过滤器,C正确;NaCO 固体易溶于水和稀硫酸,与稀硫酸接触后,关闭活塞不能使
2 3
固液分离,则制备CO 气体时不能随制随停,D错误。
2
4.下列实验操作或实验仪器使用正确的是( )
A.将高锰酸钾溶液盛装在碱式滴定管中
B.容量瓶、滴定管使用前均需用蒸馏水洗净并烘干
C.用10 mL量筒量取2.5 mL浓硫酸用于配制一定浓度的稀硫酸
D.溶液蒸发浓缩时,用坩埚钳夹持蒸发皿直接加热
【答案】C
【解析】高锰酸钾溶液应盛装在酸式滴定管中,故A错误;容量瓶使用前不需要烘干,滴定管使用前
需用蒸馏水洗净然后再用待装溶液润洗,不需要烘干,故B错误;可用10 mL量筒量取2.5 mL浓硫酸用于
配制一定浓度的稀硫酸,操作正确,故C正确;溶液蒸发浓缩时,蒸发皿应放置在三角架或泥三角上加
热,不能直接用坩埚钳夹持加热,故D错误。
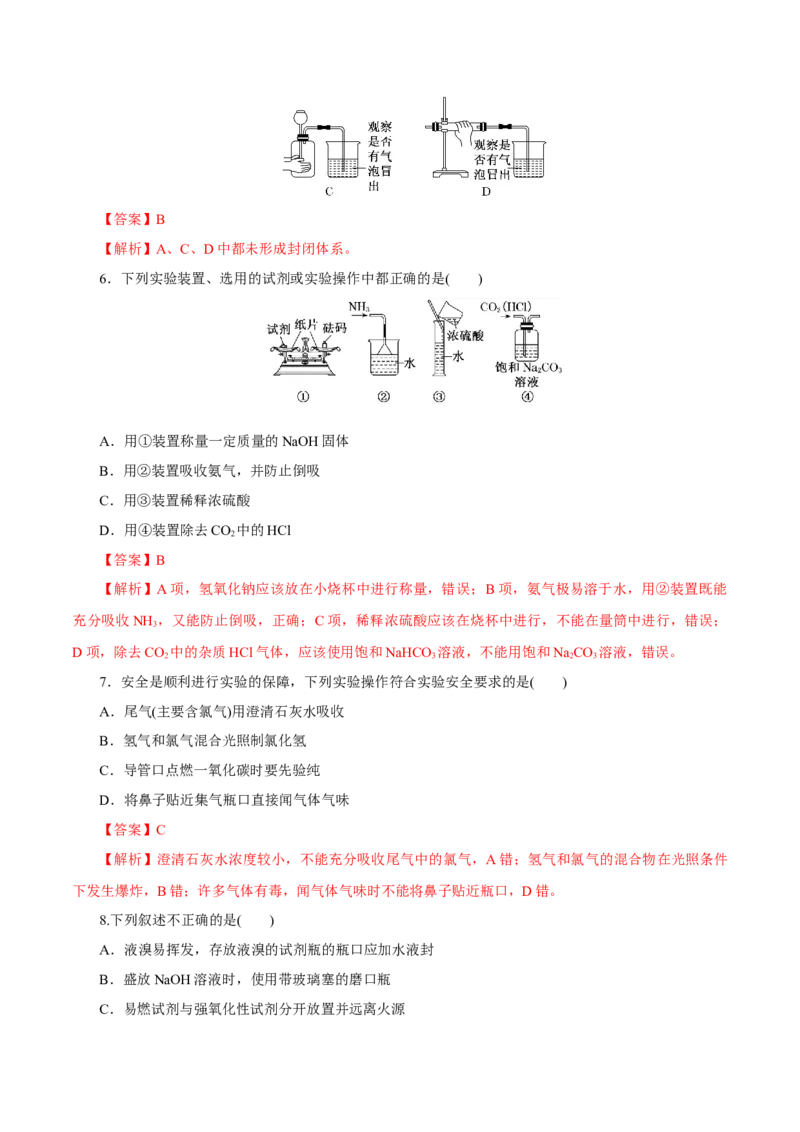
5.下列是一些装置气密性检查的方法,其中正确的是( )【答案】B
【解析】A、C、D中都未形成封闭体系。
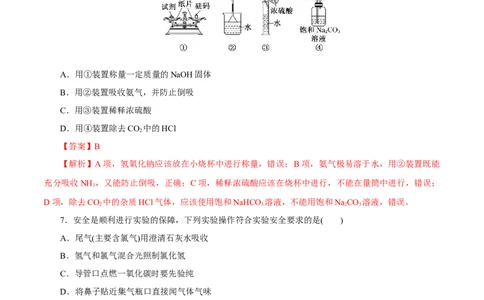
6.下列实验装置、选用的试剂或实验操作中都正确的是( )
A.用①装置称量一定质量的NaOH固体
B.用②装置吸收氨气,并防止倒吸
C.用③装置稀释浓硫酸
D.用④装置除去CO 中的HCl
2
【答案】B
【解析】A项,氢氧化钠应该放在小烧杯中进行称量,错误;B项,氨气极易溶于水,用②装置既能
充分吸收NH ,又能防止倒吸,正确;C项,稀释浓硫酸应该在烧杯中进行,不能在量筒中进行,错误;
3
D项,除去CO 中的杂质HCl气体,应该使用饱和NaHCO 溶液,不能用饱和NaCO 溶液,错误。
2 3 2 3
7.安全是顺利进行实验的保障,下列实验操作符合实验安全要求的是( )
A.尾气(主要含氯气)用澄清石灰水吸收
B.氢气和氯气混合光照制氯化氢
C.导管口点燃一氧化碳时要先验纯
D.将鼻子贴近集气瓶口直接闻气体气味
【答案】C
【解析】澄清石灰水浓度较小,不能充分吸收尾气中的氯气,A错;氢气和氯气的混合物在光照条件
下发生爆炸,B错;许多气体有毒,闻气体气味时不能将鼻子贴近瓶口,D错。
8.下列叙述不正确的是( )
A.液溴易挥发,存放液溴的试剂瓶的瓶口应加水液封
B.盛放NaOH溶液时,使用带玻璃塞的磨口瓶
C.易燃试剂与强氧化性试剂分开放置并远离火源D.用棕色试剂瓶存放浓硝酸
【答案】B
【解析】盛放液溴的试剂瓶瓶口应加少量水液封,以减少溴的挥发,A项正确;NaOH能与玻璃成分
中的SiO 反应,生成具有黏性的硅酸钠,使瓶口不易打开,所以盛放NaOH溶液时应使用带橡胶塞的试剂
2
瓶,B项不正确;易燃试剂与强氧化剂混在一起容易引起火灾或爆炸,故应分开放置并远离火源,C项正
确;浓硝酸见光易分解,应盛放在棕色试剂瓶中,D项正确。
9.下列实验基本操作或对事故的处理方法不正确的是( )
A.给盛有液体的烧瓶加热时,需要加碎瓷片或沸石
B.发现实验室中有大量的可燃性气体泄漏时,应立即开窗通风
C.酒精灯内的酒精不能超过酒精灯容积的
D.不慎将少量浓硫酸溅到皮肤上,应立即用水冲洗,然后涂抹10%的NaOH溶液
【答案】D
【解析】给盛有液体的烧瓶加热时,需要加碎瓷片或沸石以防暴沸,A正确;开窗通风以减小可燃性
气体的浓度以防爆炸,B正确;酒精灯内酒精量过多,易造成酒精灯内酒精被引燃,出现酒精灯内发生剧
烈燃烧而爆炸的现象,C正确;NaOH具有强腐蚀性,会造成二次伤害,应涂抹 3%~5%的NaHCO 溶
3
液,D错误。
10.下列操作表示过滤的是( )
【答案】C
【解析】A项为萃取操作,B项为一定物质的量浓度溶液配制过程中的定容操作,C项为过滤操作,D
项为一定物质的量浓度溶液配制过程中的移液操作。
1.仅用下表提供的玻璃仪器(非玻璃仪器任选)就能实现相应实验目的的是( )
选项 实验目的 玻璃仪器
A 分离水和食用油 长颈漏斗、烧杯、玻璃棒
B 配制100 mL 0.2 mol·L-1的NaOH溶液 100 mL容量瓶、烧杯、玻璃棒
C 从食盐水中提取NaCl 酒精灯、蒸发皿、玻璃棒
D 分离水与泥沙 分液漏斗、烧杯【答案】C
【解析】A项中应用分液漏斗,不能用长颈漏斗;B项中缺胶头滴管;D项中应用普通漏斗,不能用
分液漏斗,缺玻璃棒。
2.下列实验操作能达到目的的是( )
【答案】D
【解析】滴加液体时胶头滴管通常不能伸到试管内,A错误;稀释浓硫酸时应该将浓硫酸注入到水
中,B错误;从食盐水中提取氯化钠晶体需要蒸发浓缩,需用蒸发皿,不能用坩埚,C错误;该滴定管是
碱式滴定管,可以用来量取15.00 mL氢氧化钠溶液,D正确。
3.下列实验仪器或装置的使用正确的是( )
A.装置甲洗气 B.装置乙过滤
C.装置丙盛装NaSiO 溶液 D.装置丁加热固体
2 3
【答案】D
【解析】洗气装置应长导管进气,短导管出气,故A错误;过滤装置中漏斗下端尖嘴处应紧贴烧杯内
壁,故B错误;硅酸钠溶液是一种矿物胶、无机黏合剂,会把玻璃塞和瓶子黏在一起,故C错误;试管加
热固体时管口应略向下倾斜,故D正确。
4.茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )A.将茶叶灼烧灰化,选用①②和⑨
B.用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④⑥和⑦
C.过滤得到滤液,选用④⑤和⑦
D.检验滤液中的Fe3+,选用③⑧和⑩
【答案】B
【解析】灼烧茶叶需用的仪器有坩埚、泥三角、酒精灯等,A项正确;溶解茶叶灰的过程中会用到烧
杯、玻璃棒等仪器,容量瓶是配制一定体积、一定物质的量浓度溶液时的主要仪器,B项错误;过滤需用
的仪器有漏斗、烧杯、玻璃棒等,C项正确;检验Fe3+可用KSCN溶液,仪器为胶头滴管和试管,D项正
确。
5.菠菜中富含铁元素,实验室可以检验菠菜中的铁元素,实验过程中涉及的下列操作及相关叙述错误
的是( )
A B C D
往滤液中滴加
在通风橱中,用稀硝
将菠菜叶剪碎后灼烧 过滤 K[Fe(CN) ]溶液检验
酸浸取菠菜灰 3 6
Fe3+
【答案】D
【解析】将菠菜叶剪碎后灼烧,在坩埚中进行,操作合理,选项A正确;在通风橱中,用稀硝酸浸取
菠菜灰,防止产生的有毒气体使人中毒,操作合理,选项 B正确;通过过滤操作将溶解后的固体与溶液分
离开来,操作合理,选项C正确;往滤液中滴加K[Fe(CN) ]溶液可以检验的是Fe2+而不是Fe3+,操作不合
3 6
理,选项D错误。
6.水合肼(N H·H O)是重要的氢能源稳定剂,其制备的反应原理为 NaClO+2NH ===N H·H O+
2 4 2 3 2 4 2
NaCl。下列装置和操作不能达到实验目的的是( )A.在装置甲的圆底烧瓶中加入碱石灰制取NH
3
B.用装置乙作为反应过程的安全瓶
C.制备水合肼时从装置丙的b口通入NH
3
D.用装置丁吸收反应中过量的NH
3
【答案】C
【解析】浓氨水遇碱放出氨气,在装置甲的圆底烧瓶中加入碱石灰可以制取NH ,故A正确;氨气极
3
易溶于水,为防止倒吸,用装置乙作为反应过程的安全瓶,故 B正确;氨气密度比空气小,为有利于氨气
和NaClO溶液反应,制备水合肼时应从装置丙的a口通入NH ,故C错误;氨气会污染环境,用装置丁可
3
以吸收反应中过量的NH ,并能防止倒吸,故D正确。
3
7.下列实验操作规范且能达到实验目的的是( )
操作 目的
称取5.0 g CuSO ·5H O加入27.0 g水中,搅拌
A 4 2 配制10% CuSO 溶液
溶解 4
B 先用稀盐酸洗涤,再用水清洗 洗涤分解KMnO 制O 的试管
4 2
用玻璃棒蘸取溶液,点在干燥的pH试纸上,
C 测定0.05 mol·L-1 NaClO溶液的pH
片刻后与标准比色卡比较并读数
将粗碘放入烧杯中,烧杯口放一盛满冷水的烧
D 瓶,隔石棉网对烧杯加热,然后收集烧瓶外壁 提纯混有NH Cl的粗碘
4
的固体
【答案】A
【解析】5.0 g CuSO ·5H O中含3.2 g CuSO ,加入27.0 g水中,搅拌溶解得到32 g CuSO 溶液,溶质
4 2 4 4
的质量分数为×100%=10%,故A正确;洗涤分解KMnO 制O 的试管,试管内壁附着MnO 需要先用浓盐
4 2 2
酸并加热洗涤,再用水洗涤,故B错误;测定0.05 mol·L-1 NaClO溶液的pH,由于NaClO具有强氧化
性,能使试纸褪色,故不能用pH试纸测其pH,故C错误;因NH Cl受热分解生成氨气和氯化氢,冷却后
4
又结合成NH Cl,故不能用加热的方法提纯混有NH Cl的粗碘,故D错误。
4 4
8.安全是顺利进行实验及避免伤害的保障。下列实验操作正确但不是从实验安全角度考虑的是( )A.操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B.操作②:使用CCl 萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出
4
C.操作③:吸收氨气或氯化氢气体并防止倒吸
D.操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
【答案】D
【解析】A项,由于连通氢气发生装置的导管在液面以下,燃烧的氢气在液面上,所以该装置可以防
止点燃不纯氢气时发生爆炸,该操作是从安全角度考虑的,错误;B项,打开活塞使漏斗内气体放出以防
止分液漏斗内压强过大引起危险,该操作是从安全角度考虑的,错误;C项,水层在下层不能防止倒吸,
应该使用四氯化碳和水,该操作不正确,错误;D项,检查容量瓶是否漏水操作正确,但这不是从实验安
全角度考虑的,正确。
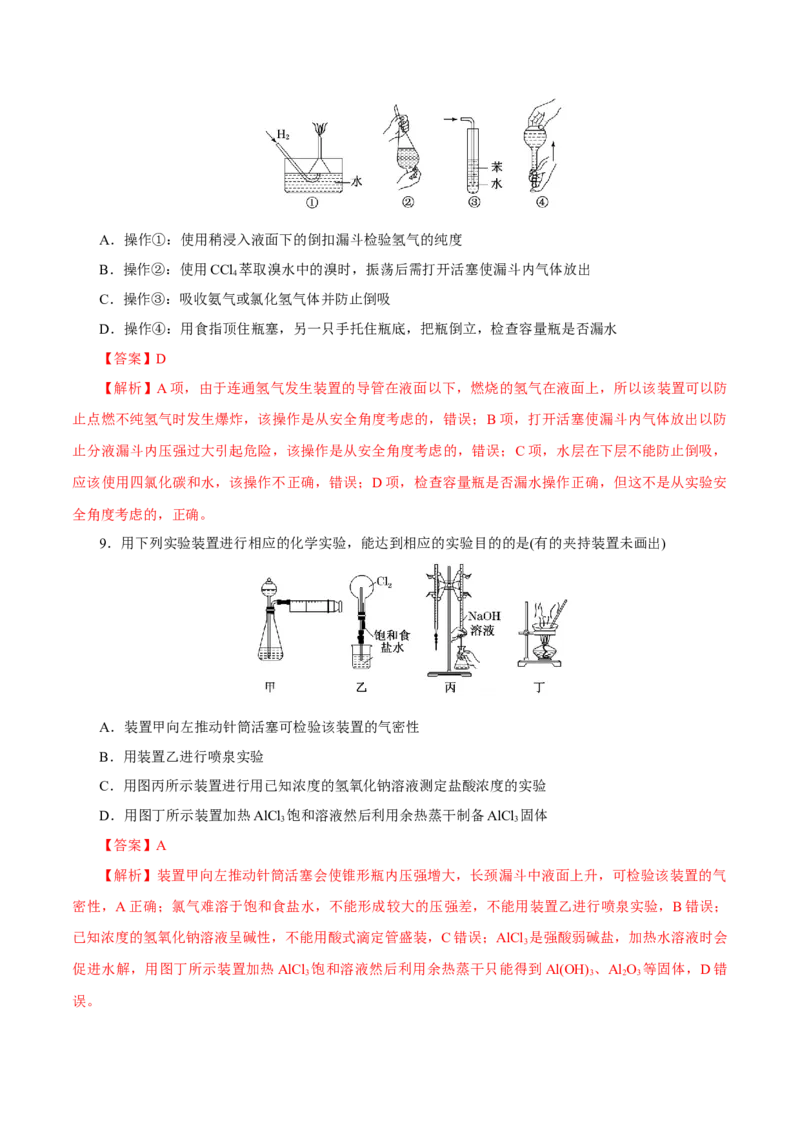
9.用下列实验装置进行相应的化学实验,能达到相应的实验目的的是(有的夹持装置未画出)
A.装置甲向左推动针筒活塞可检验该装置的气密性
B.用装置乙进行喷泉实验
C.用图丙所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验
D.用图丁所示装置加热AlCl 饱和溶液然后利用余热蒸干制备AlCl 固体
3 3
【答案】A
【解析】装置甲向左推动针筒活塞会使锥形瓶内压强增大,长颈漏斗中液面上升,可检验该装置的气
密性,A正确;氯气难溶于饱和食盐水,不能形成较大的压强差,不能用装置乙进行喷泉实验,B错误;
已知浓度的氢氧化钠溶液呈碱性,不能用酸式滴定管盛装,C错误;AlCl 是强酸弱碱盐,加热水溶液时会
3
促进水解,用图丁所示装置加热AlCl 饱和溶液然后利用余热蒸干只能得到Al(OH) 、Al O 等固体,D错
3 3 2 3
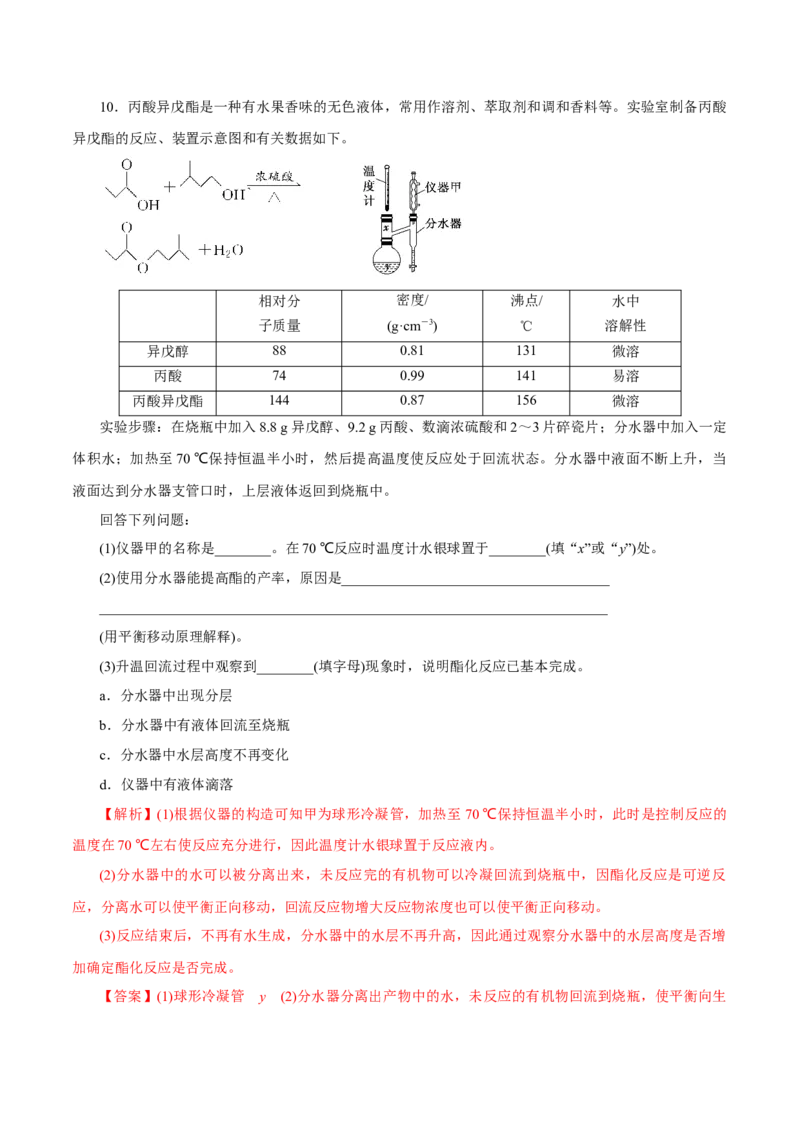
误。10.丙酸异戊酯是一种有水果香味的无色液体,常用作溶剂、萃取剂和调和香料等。实验室制备丙酸
异戊酯的反应、装置示意图和有关数据如下。
相对分 密度/ 沸点/ 水中
子质量 (g·cm-3) ℃ 溶解性
异戊醇 88 0.81 131 微溶
丙酸 74 0.99 141 易溶
丙酸异戊酯 144 0.87 156 微溶
实验步骤:在烧瓶中加入8.8 g异戊醇、9.2 g丙酸、数滴浓硫酸和2~3片碎瓷片;分水器中加入一定
体积水;加热至70 ℃保持恒温半小时,然后提高温度使反应处于回流状态。分水器中液面不断上升,当
液面达到分水器支管口时,上层液体返回到烧瓶中。
回答下列问题:
(1)仪器甲的名称是________。在70 ℃反应时温度计水银球置于________(填“x”或“y”)处。
(2)使用分水器能提高酯的产率,原因是______________________________________
________________________________________________________________________
(用平衡移动原理解释)。
(3)升温回流过程中观察到________(填字母)现象时,说明酯化反应已基本完成。
a.分水器中出现分层
b.分水器中有液体回流至烧瓶
c.分水器中水层高度不再变化
d.仪器中有液体滴落
【解析】(1)根据仪器的构造可知甲为球形冷凝管,加热至70 ℃保持恒温半小时,此时是控制反应的
温度在70 ℃左右使反应充分进行,因此温度计水银球置于反应液内。
(2)分水器中的水可以被分离出来,未反应完的有机物可以冷凝回流到烧瓶中,因酯化反应是可逆反
应,分离水可以使平衡正向移动,回流反应物增大反应物浓度也可以使平衡正向移动。
(3)反应结束后,不再有水生成,分水器中的水层不再升高,因此通过观察分水器中的水层高度是否增
加确定酯化反应是否完成。
【答案】(1)球形冷凝管 y (2)分水器分离出产物中的水,未反应的有机物回流到烧瓶,使平衡向生成酯的方向移动,提高酯的产率 (3)c
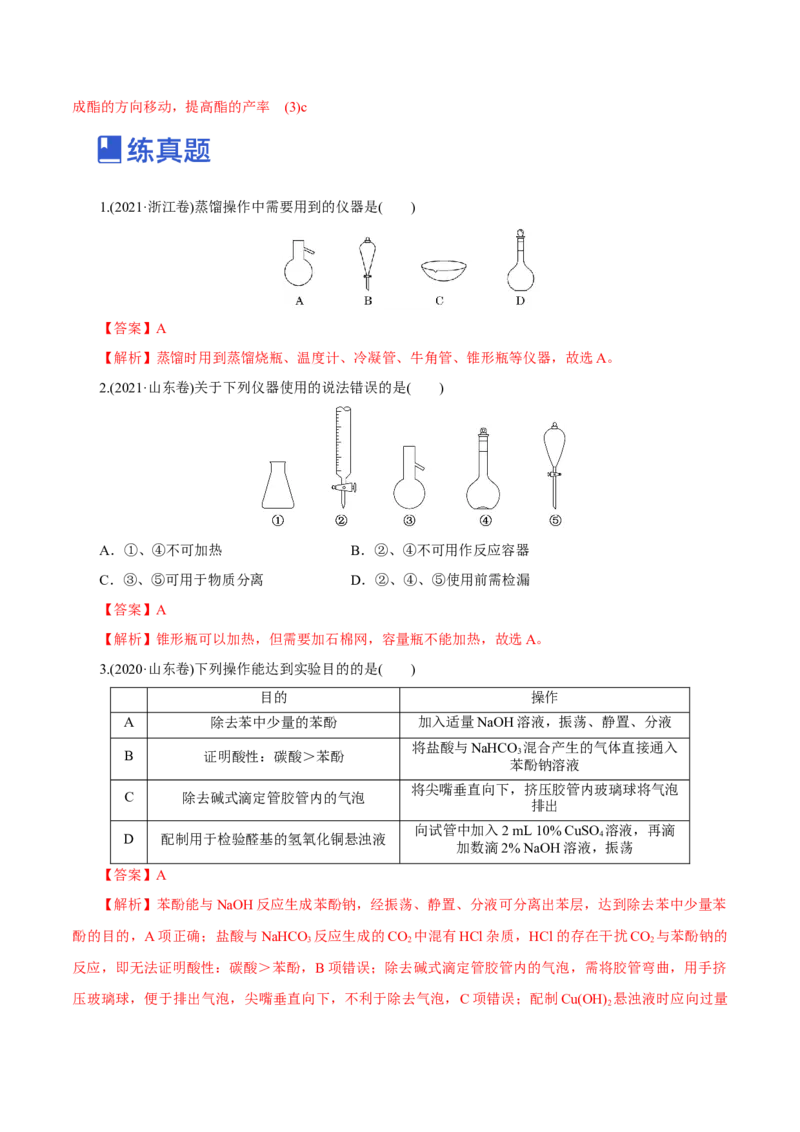
1.(2021·浙江卷)蒸馏操作中需要用到的仪器是( )
【答案】A
【解析】蒸馏时用到蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶等仪器,故选A。
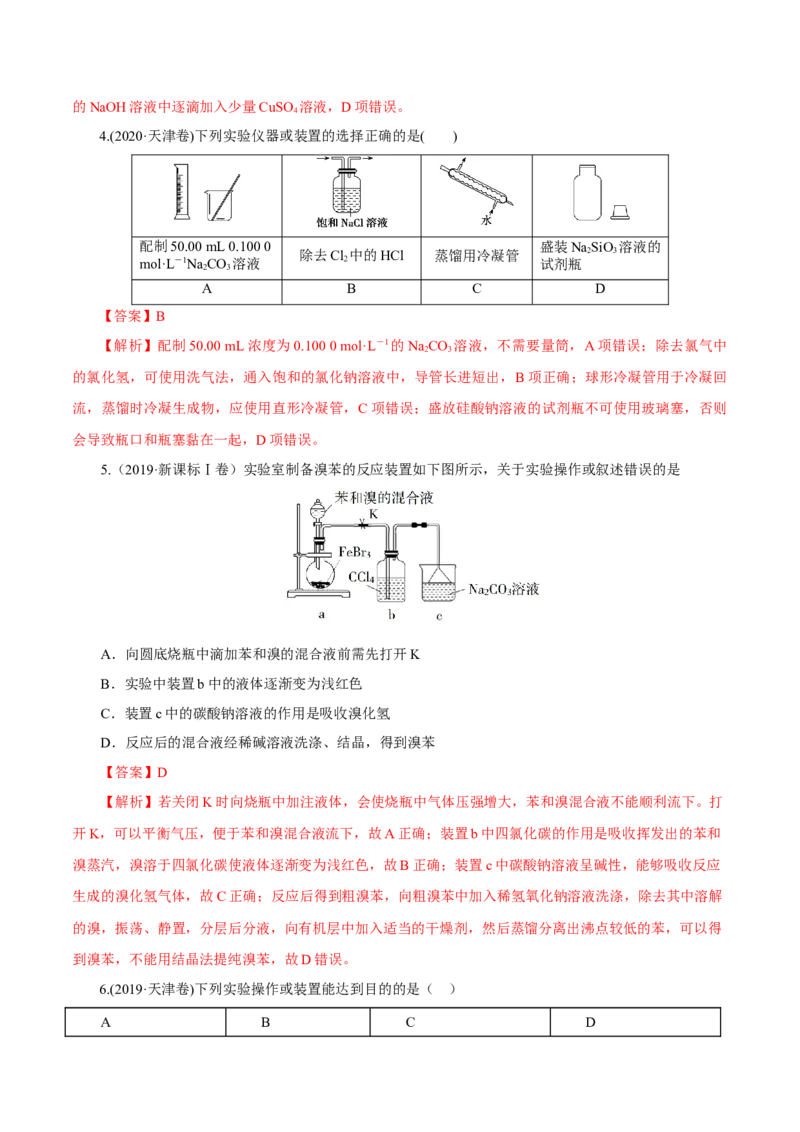
2.(2021·山东卷)关于下列仪器使用的说法错误的是( )
A.①、④不可加热 B.②、④不可用作反应容器
C.③、⑤可用于物质分离 D.②、④、⑤使用前需检漏
【答案】A
【解析】锥形瓶可以加热,但需要加石棉网,容量瓶不能加热,故选A。
3.(2020·山东卷)下列操作能达到实验目的的是( )
目的 操作
A 除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
将盐酸与NaHCO 混合产生的气体直接通入
B 证明酸性:碳酸>苯酚 3
苯酚钠溶液
将尖嘴垂直向下,挤压胶管内玻璃球将气泡
C 除去碱式滴定管胶管内的气泡
排出
向试管中加入2 mL 10% CuSO 溶液,再滴
D 配制用于检验醛基的氢氧化铜悬浊液 4
加数滴2% NaOH溶液,振荡
【答案】A
【解析】苯酚能与NaOH反应生成苯酚钠,经振荡、静置、分液可分离出苯层,达到除去苯中少量苯
酚的目的,A项正确;盐酸与NaHCO 反应生成的CO 中混有HCl杂质,HCl的存在干扰CO 与苯酚钠的
3 2 2
反应,即无法证明酸性:碳酸>苯酚,B项错误;除去碱式滴定管胶管内的气泡,需将胶管弯曲,用手挤
压玻璃球,便于排出气泡,尖嘴垂直向下,不利于除去气泡,C项错误;配制Cu(OH) 悬浊液时应向过量
2的NaOH溶液中逐滴加入少量CuSO 溶液,D项错误。
4
4.(2020·天津卷)下列实验仪器或装置的选择正确的是( )
配制50.00 mL 0.100 0 盛装NaSiO 溶液的
除去Cl 中的HCl 蒸馏用冷凝管 2 3
mol·L-1NaCO 溶液 2 试剂瓶
2 3
A B C D
【答案】B
【解析】配制50.00 mL浓度为0.100 0 mol·L-1的NaCO 溶液,不需要量筒,A项错误;除去氯气中
2 3
的氯化氢,可使用洗气法,通入饱和的氯化钠溶液中,导管长进短出,B项正确;球形冷凝管用于冷凝回
流,蒸馏时冷凝生成物,应使用直形冷凝管,C项错误;盛放硅酸钠溶液的试剂瓶不可使用玻璃塞,否则
会导致瓶口和瓶塞黏在一起,D项错误。
5.(2019·新课标Ⅰ卷)实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中装置b中的液体逐渐变为浅红色
C.装置c中的碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
【答案】D
【解析】若关闭K时向烧瓶中加注液体,会使烧瓶中气体压强增大,苯和溴混合液不能顺利流下。打
开K,可以平衡气压,便于苯和溴混合液流下,故A正确;装置b中四氯化碳的作用是吸收挥发出的苯和
溴蒸汽,溴溶于四氯化碳使液体逐渐变为浅红色,故B正确;装置c中碳酸钠溶液呈碱性,能够吸收反应
生成的溴化氢气体,故C正确;反应后得到粗溴苯,向粗溴苯中加入稀氢氧化钠溶液洗涤,除去其中溶解
的溴,振荡、静置,分层后分液,向有机层中加入适当的干燥剂,然后蒸馏分离出沸点较低的苯,可以得
到溴苯,不能用结晶法提纯溴苯,故D错误。
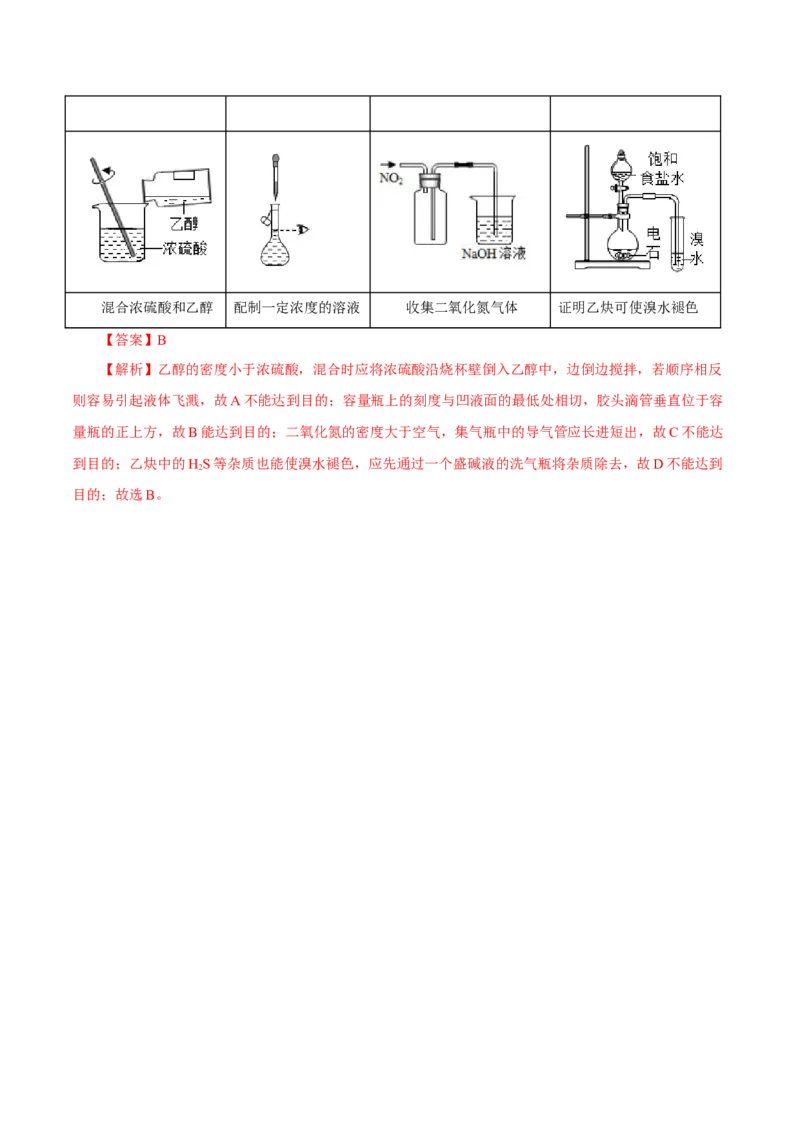
6.(2019·天津卷)下列实验操作或装置能达到目的的是( )
A B C D混合浓硫酸和乙醇 配制一定浓度的溶液 收集二氧化氮气体 证明乙炔可使溴水褪色
【答案】B
【解析】乙醇的密度小于浓硫酸,混合时应将浓硫酸沿烧杯壁倒入乙醇中,边倒边搅拌,若顺序相反
则容易引起液体飞溅,故A不能达到目的;容量瓶上的刻度与凹液面的最低处相切,胶头滴管垂直位于容
量瓶的正上方,故B能达到目的;二氧化氮的密度大于空气,集气瓶中的导气管应长进短出,故C不能达
到目的;乙炔中的HS等杂质也能使溴水褪色,应先通过一个盛碱液的洗气瓶将杂质除去,故D不能达到
2
目的;故选B。