文档内容
第 34 讲 生物大分子 与合成高分子
【化学学科素养】
1.宏观辨识与微观探析:能从官能团角度认识生活中常见的有机化合物的组成、结构和性质,形成
“结构决定性质”的观念,并能从宏观和微观相结合的视角分析与解决实际问题。
2.证据推理与模型认知:具有证据意识,能对生活中常见的有机化合物的组成、结构及其变化提出可
能的假设,并能解释某些化学现象,揭示现象的本质和规律。
3.科学态度与社会责任:通过高分子材料的合成等了解化学对社会发展的重大贡献:通过分析高分子
材料的利弊建立可持续发展意识和绿色化学观念,并能对与此有关的社会热点问题做出正确的价值判断。
【必备知识解读】
一、糖类、油脂、蛋白质的组成、结构和性质
1.糖类
(1)糖类的概念和分类。
①概念:从分子结构上看,糖类可以定义为多羟基醛、多羟基酮和它们的脱水缩合物。
②组成:碳、氢、氧三种元素。大多数糖类化合物的通式为C (H O) ,所以糖类也叫碳水化合物。
n 2 m
③分类:
(2)单糖——葡萄糖与果糖
①组成和分子结构
分子式 结构简式 官能团 二者关系
CHOH(CHOH) —OH、
2 4
葡萄糖
CHO —CHO
C H O 同分异构体
6 12 6
CHOH(CHOH)
果糖 2 3
COCH OH
2 、—OH
②葡萄糖的化学性质
—能发生银镜反应,能与新制Cu(OH) 悬浊液反应
2
|—与H 发生加成反应生成己六醇
2
|
—\s\up7(C6H12O6)――→2C HOH+2CO↑
2 5 2
|
—C H O+6O―→6CO+6HO+能量
6 12 6 2 2 2
(3)二糖——蔗糖与麦芽糖
比较项目 蔗糖 麦芽糖
分子式 均为C H O
12 22 11
相同点
性质 都能发生水解反应
是否含醛基 不含 含有
不同点
水解产物 葡萄糖和果糖 葡萄糖
相互关系 互为同分异构体
(4)多糖——淀粉与纤维素
①相似点:
a.都属于天然有机高分子化合物,属于多糖,分子式都可表示为(C H O)。
6 10 5 n
b.都能发生水解反应,如淀粉水解的化学方程式为\s\up7(C6H10O5n)+
nHO――→\s\up7(nC6H12O6)。
2
c.都不能发生银镜反应。
②不同点:
a.通式中n值不同。
b.淀粉遇碘呈现特殊的蓝色。
2.油脂
(1)组成和结构
油脂是高级脂肪酸与甘油反应所生成的酯,由C、H、O三种元素组成,其结构可表示为
(2)分类(3)物理性质
性质 特点
密度 密度比水小
溶解性 难溶于水,易溶于有机溶剂
含有不饱和脂肪酸成分较多的甘油酯,常温下一般呈液态;
状态
含有饱和脂肪酸成分较多的甘油酯,常温下一般呈固态
熔、沸点 天然油脂都是混合物,没有固定的熔、沸点
(4)化学性质
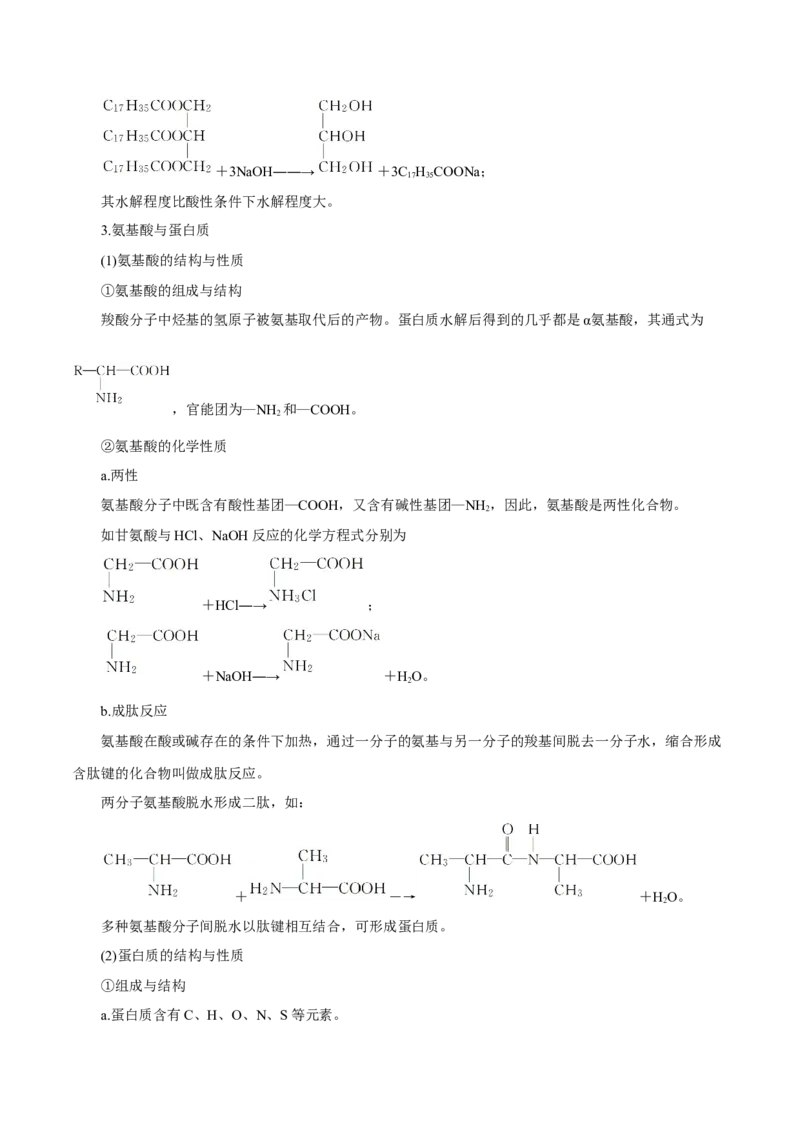
①油脂的氢化(油脂的硬化)
烃基上含有碳碳双键,能与H 发生加成反应。如油酸甘油酯与H 发生加成反应的化学方程式为
2 2
+3H――→ 。
2
经硬化制得的油脂叫人造脂肪,也称硬化油。
②水解反应
a.酸性条件下
如硬脂酸甘油酯的水解反应方程式为 +3HO
2
+3C H COOH。
17 35
b.碱性条件下——皂化反应
如硬脂酸甘油酯的水解反应方程式为+3NaOH――→ +3C H COONa;
17 35
其水解程度比酸性条件下水解程度大。
3.氨基酸与蛋白质
(1)氨基酸的结构与性质
①氨基酸的组成与结构
羧酸分子中烃基的氢原子被氨基取代后的产物。蛋白质水解后得到的几乎都是α氨基酸,其通式为
,官能团为—NH 和—COOH。
2
②氨基酸的化学性质
a.两性
氨基酸分子中既含有酸性基团—COOH,又含有碱性基团—NH ,因此,氨基酸是两性化合物。
2
如甘氨酸与HCl、NaOH反应的化学方程式分别为
+HCl―→ ;
+NaOH―→ +HO。
2
b.成肽反应
氨基酸在酸或碱存在的条件下加热,通过一分子的氨基与另一分子的羧基间脱去一分子水,缩合形成
含肽键的化合物叫做成肽反应。
两分子氨基酸脱水形成二肽,如:
+ ―→ +HO。
2
多种氨基酸分子间脱水以肽键相互结合,可形成蛋白质。
(2)蛋白质的结构与性质
①组成与结构
a.蛋白质含有C、H、O、N、S等元素。b.蛋白质是由氨基酸通过缩聚反应生成的,蛋白质属于天然有机高分子化合物。
②性质
(3)酶
①大部分酶是一种蛋白质,具有蛋白质的性质。
②酶是一种生物催化剂,催化作用具有以下特点:
a.条件温和,不需加热
b.具有高度的专一性
c.具有高效催化作用
二、合成有机高分子
1.基本概念
(1)单体:能够进行聚合反应形成高分子化合物的低分子化合物。
(2)链节:高分子化合物中化学组成相同、可重复的最小单位。
(3)聚合度:高分子链中含有链节的数目。
如:
2.合成高分子化合物的两个基本反应
(1)加聚反应:小分子物质以加成反应形式生成高分子化合物的反应。
(2)缩聚反应:单体分子间缩合脱去小分子(如HO、HX等)生成高分子化合物的反应。
2
3.高分子化合物的分类及性质特点高分子化合物
――→
其中,塑料、合成纤维、合成橡胶又被称为“三大合成材料”。
4.加聚反应、缩聚反应方程式的书写方法
(1)加聚反应的书写方法
①单烯烃型单体加聚时,“断开双键,键分两端,添上括号,右下写n”。例如:
nCH==CH—CH ――→
2 3
②二烯烃型单体加聚时,“单变双,双变单,破两头,移中间,添上括号,右下写n”。
③含有一个双键的两种单体聚合时,“双键打开,中间相连,添上括号,右下写n”。例如:
――→
(2)缩聚反应的书写方法
书写缩合聚合物(简称缩聚物)结构式时,与加成聚合物(简称加聚物)结构式写法有点不同,缩聚物结构
式要在方括号外侧写出链节余下的端基原子或原子团,而加聚物的端基不确定,通常用横线“—”表示。
例如:
a.聚酯类:—OH与—COOH间的缩聚
nHOCH —CHOH+nHOOC—COOH
2 2
+(2n-1)H O。
2
nHOCH —CH—COO H +(n-1)H O。
2 2 2
b.聚氨基酸类:—NH 与—COOH间的缩聚
2
nHN—CH COOH――→ +(n-1)H O。
2 2 2
nHNCH COOH+ ――→ +(2n-
2 2
1)H O]。
2c.酚醛树脂类:
nHCHO+ ――→(n-1)H O+ 。
2
【关键能力拓展】
一、有机合成的思路与方法
1.有机合成题的解题思路
2.有机合成中碳骨架的构建
(1)碳链增长的反应
①加聚反应;
②缩聚反应;
③酯化反应;
④利用题目信息所给反应,如:醛酮中的羰基与HCN加成。
CHCHO+HCN――→ ――→
3
(2)碳链减短的反应
①烷烃的裂化反应;
②酯类、糖类、蛋白质等的水解反应;
③利用题目信息所给反应,如:烯烃、炔烃的氧化反应,羧酸及其盐的脱羧反应……
(3)常见由链成环的方法
①二元醇成环:
如:HOCH CHOH――→ +HO;
2 2 2
②羟基酸酯化成环:如: +HO;
2
③氨基酸成环:
如:HNCH CHCOOH―→ +HO;
2 2 2 2
④二元羧酸成环:
如:HOOCCH CHCOOH――→ +HO;
2 2 2
⑤利用题目所给信息成环,如常给信息二烯烃与单烯烃的聚合成环:
+ ――→ 。
3.有机合成中官能团的转化
(1)官能团的引入
引入官能团 引入方法
①烃、酚的取代;
引入卤素原子 ②不饱和烃与HX、X 的加成;
2
③醇与氢卤酸(HX)反应
①烯烃与水加成;
②醛酮与氢气加成;
引入羟基
③卤代烃在碱性条件下水解;
④酯的水解
①某些醇或卤代烃的消去;
引入碳碳双键 ②炔烃不完全加成;
③烷烃裂化
①醇的催化氧化;
引入碳氧双键 ②连在同一个碳上的两个羟基脱水;
③含碳碳三键的物质与水加成
引入羧基 ①醛基氧化;②酯、肽、蛋白质、羧酸盐的水解
(2)官能团的消除
①通过加成反应可以消除不饱和键(双键、三键、苯环);
②通过消去、氧化或酯化反应等消除羟基;
③通过加成或氧化反应等消除醛基;
④通过水解反应消除酯基、肽键、卤素原子。
(3)官能团的改变
①利用官能团的衍生关系进行衍变,如
R—CHO H R—CHO――→R—COOH;
2
②通过某种化学途径使一个官能团变为两个,如
CHCHOH――――→CH==CH ――→Cl—CH —CHCl――→HO—CH —CH—OH;
3 2 2 2 2 2 2 2
③通过某种手段改变官能团的位置,如
。
【核心题型例解】
高频考点一 糖类、油脂、蛋白质的组成、性质及应用
例1.(2023·湖北卷第7题)中科院院士研究发现,纤维素可在低温下溶于NaOH溶液,恢复至室温后
不稳定,加入尿素可得到室温下稳定的溶液,为纤维素绿色再生利用提供了新的解决方案。下列说法错误
的是( )
A. 纤维素是自然界分布广泛的一种多糖
B. 纤维素难溶于水的主要原因是其链间有多个氢键
C. NaOH提供OH-破坏纤维素链之间的氢键
D. 低温降低了纤维素在NaOH溶液中的溶解性
【答案】B
【解析】纤维素属于多糖,大量存在于我们吃的蔬菜水果中,在自然界广泛分布,A正确;纤维素难
溶于水,一是因为纤维素不能跟水形成氢键,二是因为碳骨架比较大,B错误;纤维素在低温下可溶于氢氧化钠溶液,是因为碱性体系主要破坏的是纤维素分子内和分子间的氢键促进其溶解,C正确;温度越
低,物质的溶解度越低,所以低温下,降低了纤维素在氢氧化钠溶液中的溶解性,D正确;故选B。
【变式探究】(2023·海南卷第2题)化学实验中的颜色变化,可将化学抽象之美具体为形象之美。下
列叙述错误的是
A. 土豆片遇到碘溶液,呈蓝色
B. 蛋白质遇到浓硫酸,呈黄色
C. 溶液( )中滴加乙醇,呈绿色
D. 苯酚溶液( )中滴加 溶液( ),呈紫色
【答案】B
【解析】土豆片中含有淀粉,淀粉遇到碘单质会变蓝,A正确;结构中含苯环的蛋白质遇到浓硝酸,
呈黄色,B错误; 会被乙醇还原为三价铬,呈绿色,C正确;苯酚遇到氯化铁会有显色反应,生成紫
色的配合物,D正确; 故选B。
【变式探究】(2022·江苏卷)我国为人类科技发展作出巨大贡献。下列成果研究的物质属于蛋白质的
是
A. 陶瓷烧制 B. 黑火药 C. 造纸术 D. 合成结晶牛胰岛素
【答案】D
【解析】陶瓷的主要成分是硅酸盐,陶瓷烧制研究的物质是硅的化合物,A不符合题意;黑火药研究
的物质是硫、碳和硝酸钾,B不符合题意;造纸术研究的物质是纤维素,C不符合题意;胰岛素的主要成
分是蛋白质,故合成结晶牛胰岛素研究的物质是蛋白质,D符合题意;故选D。
【变式探究】(2022·浙江卷)下列说法不正确的是
A.油脂属于高分子化合物,可用于制造肥皂和油漆
B.福尔马林能使蛋白质变性,可用于浸制动物标本
C.天然气的主要成分是甲烷,是常用的燃料
D.中国科学家在世界上首次人工合成具有生物活性的蛋白质——结晶牛胰岛素
【答案】A
【解析】油脂的相对分子质量虽然较大,但比高分子化合物的相对分子质量小的多,油脂不是高分子
化合物,A错误;福尔马林是甲醛的水溶液,能使蛋白质发生变性,可用于浸制动物标本,B正确;天然
气是三大化石燃料之一,其主要成分是甲烷,是生产生活中常用的一种清洁燃料,C正确;我国科学家合成的结晶牛胰岛素,是世界上首次人工合成的具有活性的蛋白质,蛋白质的基本组成单位是氨基酸,D正
确;故选A。
高频考点二 糖类、油脂、蛋白质与有机推断
【例2】(2023·广东卷第10题)部分含 或含 物质的分类与相应化合价关系如图所示。下列推
断不合理的是( )
A. 可存在c→d→e的转化
B. 能与 反应生成c的物质只有b
C. 新制的d可用于检验葡萄糖中的醛基
D. 若b能与 反应生成 ,则b中含共价键
【答案】B
【解析】由图可知a、b、c对应物质分别为:钠、氧化钠(过氧化钠)、氢氧化钠或a、b、e 、d对
应物质分别为:铜、氧化亚铜、氧化铜、氢氧化铜。由分析可知氢氧化钠和硫酸铜反应生成氢氧化铜,氢
氧化铜受热分解生成氧化铜所以存在c→d→e的转化,A合理;钠和氧化钠(过氧化钠)都能与HO反应
2
都能生成氢氧化钠,B不合理;新制氢氧化铜可用于检验葡萄糖中的醛基,C合理;若b能与HO反应生
2
成O,则b为过氧化钠,结构中含共价键和离子键,D合理;故选B。
2
【变式探究】(2022·广东卷)我国科学家进行了如图所示的碳循环研究。下列说法正确的是
A. 淀粉是多糖,在一定条件下能水解成葡萄糖
B. 葡萄糖与果糖互为同分异构体,都属于烃类
C. 中含有 个电子D. 被还原生成
【答案】A
【解析】淀粉是由葡萄糖分子聚合而成的多糖,在一定条件下水解可得到葡萄糖,故A正确;葡萄糖
与果糖的分子式均为C H O,结构不同,二者互为同分异构体,但含有O元素,不是烃类,属于烃的衍
6 12 6
生物,故B错误;一个CO分子含有14个电子,则1molCO中含有14×6.02×1023=8.428×1024个电子,故C
错误;未指明气体处于标况下,不能用标况下的气体摩尔体积计算其物质的量,故D错误;答案选A。
【变式探究】(2022·湖北卷)化学物质与生命过程密切相关,下列说法错误的是
A. 维生素C可以还原活性氧自由基 B. 蛋白质只能由蛋白酶催化水解
C. 淀粉可用 为原料人工合成 D. 核酸可视为核苷酸的聚合产物
【答案】B
【解析】维生素C具有还原性,可以还原活性氧自由基,故A正确;蛋白质在酸、碱的作用下也能发
生水解,故B错误;将二氧化碳先还原生成甲醇,再转化为淀粉,实现用 为原料人工合成淀粉,故C
正确;核苷酸通过聚合反应制备核酸,故D正确;故选B。
【变式探究】(2022·浙江卷)下列说法不正确的是
A.植物油含有不饱和高级脂肪酸甘油酯,能使溴的四氯化碳溶液褪色
B.向某溶液中加入茚三酮溶液,加热煮沸出现蓝紫色,可判断该溶液含有蛋白质
C.麦芽糖、葡萄糖都能发生银镜反应
D.将天然的甘氨酸、丙氨酸、苯丙氨酸混合,在一定条件下生成的链状二肽有9种
【答案】B
【解析】植物油中含有不饱和高级脂肪酸甘油酯,能与溴发生加成反应,因此能使溴的四氯化碳溶液
褪色,A正确;某溶液中加入茚三酮试剂,加热煮沸后溶液出现蓝紫色,氨基酸也会发生类似颜色反应,
则不可判断该溶液含有蛋白质,B错误;麦芽糖、葡萄糖均含有醛基,所以都能发生银镜反应,C正确;
羧基脱羟基,氨基脱氢原子形成链状二肽,形成1个肽键;甘氨酸、丙氨酸、苯丙氨酸相同物质间共形成
3种二肽,甘氨酸、丙氨酸、苯丙氨酸不同物质间形成6种二肽,所以生成的链状二肽共有9种,D正确;
故选B。
高频考点三 合成有机高分子的结构、性质及应用
例3.(2023·浙江卷1月第10题)丙烯可发生如下转化,下列说法不正确的是A. 丙烯分子中最多7个原子共平面
B. X的结构简式为 CH-CH=CHBr
3
C. Y与足量KOH醇溶液共热可生成丙炔
D. 聚合物Z的链节为
【答案】B
【解析】CH-CH=CH 与Br 的CCl 溶液发生加成反应,生成 (Y);CH-CH=CH 与Br 在
3 2 2 4 3 2 2
光照条件下发生甲基上的取代反应,生成 (X);CH-CH=CH 在催化剂作用下发生加聚反
3 2
应,生成 (Z)。乙烯分子中有6个原子共平面,甲烷分子中最多有3个原子共平面,则丙烯
分子中,两个框内的原子可能共平面,所以最多7个原子共平面,A正确;由分析可知,
X的结构简式为 ,B不正确;Y( )与足量KOH醇溶液共热,发生消去反应,可生成丙炔(CHC≡CH)和KBr等,C正确;聚合物Z为 ,则其链节为 ,D正
3
确;故选B。
【变式探究】(2023·北京卷第9题)一种聚合物PHA的结构简式如下,下列说法不正确的是
A. PHA的重复单元中有两种官能团
B. PHA通过单体 缩聚合成
C. PHA在碱性条件下可发生降解
D. PHA中存在手性碳原子
【答案】A
【解析】PHA的重复单元中只含有酯基一种官能团,A项错误;由PHA的结构可知其为聚酯,由单
体 缩聚合成,B项正确;PHA为聚酯,碱性条件下可发生降解,C项正确;PHA的重复单元
中只连有1个甲基的碳原子为手性碳原子,D项正确;故选A。
【变式探究】(2022·湖南卷)聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法错误的是
A. B. 聚乳酸分子中含有两种官能团
C. 乳酸与足量的 反应生成 D. 两分子乳酸反应能够生成含六元环的分子
【答案】B
【解析】根据氧原子数目守恒可得:3n=2n+1+m,则m=n-1,A正确;聚乳酸分子中含有三种官能
团,分别是羟基、羧基、酯基,B错误;1个乳酸分子中含有1个羟基和1个羧基,则1mol乳酸和足量的Na反应生成1mol H,C正确;1个乳酸分子中含有1个羟基和1个羧基,则两分子乳酸可以缩合产生含六
2
元环的分子( ),D正确;故选B。
【变式探究】(2022·山东卷)下列高分子材料制备方法正确的是
A. 聚乳酸( )由乳酸经加聚反应制备
B. 聚四乙烯( )由四氟乙烯经加聚反应制备
C. 尼龙 ( )由己胺和己酸经缩聚反应制备
D. 聚乙烯醇( )由聚乙酸乙烯酯( )经消去反应制备
【答案】B
【解析】聚乳酸( )是由乳酸[HOCH(CH )COOH]分子间脱水缩聚而得,即发
3
生缩聚反应,A错误;聚四氟乙烯( )是由四氟乙烯(CF=CF )经加聚反应制备,B正
2 2
确;尼龙-66( )是由己二胺和己二酸经过缩聚反应制得,C错误;聚乙烯醇( )由聚乙酸乙烯醇酯( )发生水解反应制
得,D错误;故答案为B。
【举一反三】(2022·北京卷)高分子Y是一种人工合成的多肽,其合成路线如下。
下列说法不正确的是
A. F中含有2个酰胺基 B. 高分子Y水解可得到E和G
C. 高分子X中存在氢键 D. 高分子Y的合成过程中进行了官能团保护
【答案】B
【解析】由结构简式可知,F中含有2个酰胺基,故A正确,由结构简式可知,高分子Y一定条件下
发生水解反应生成 和 ,故B错误;由结构简式可知,高分子X中含有的
酰胺基能形成氢键,故C正确;由结构简式可知,E分子和高分子Y中都含有氨基,则高分子Y的合成过
程中进行了官能团氨基的保护,故D正确;故选B。
高频考点四 有机合成路线的设计
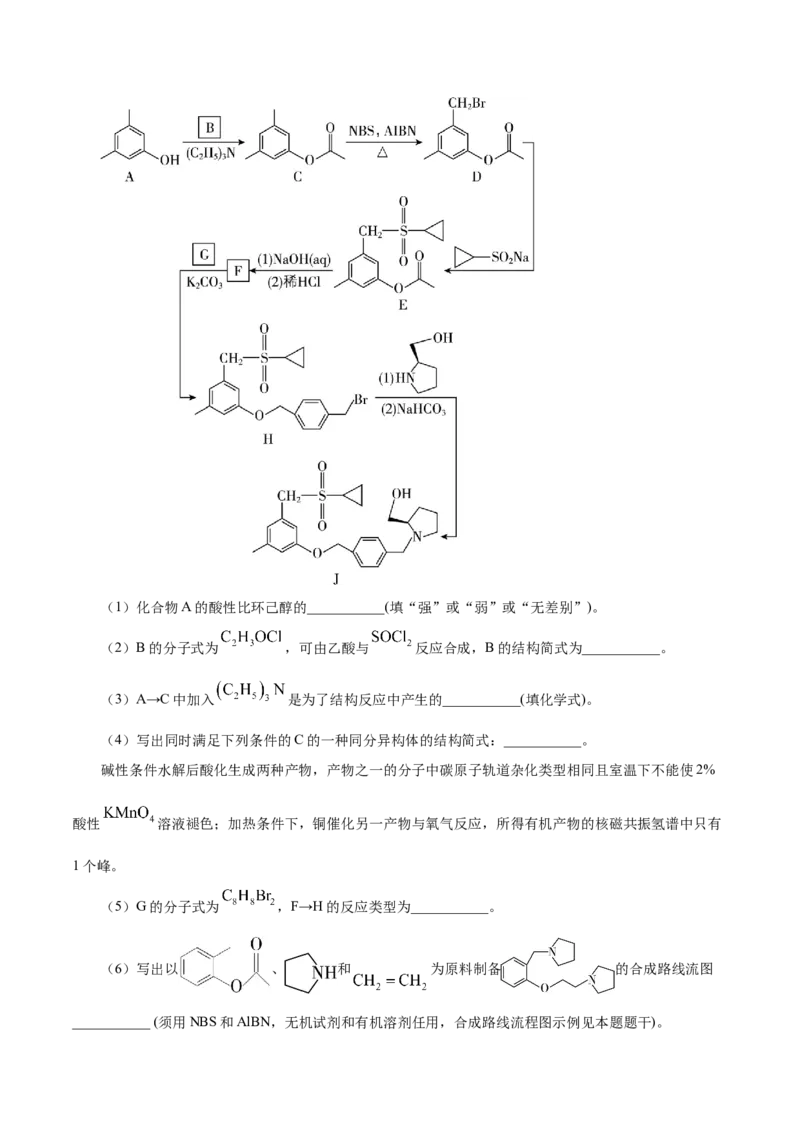
例4.(2023·江苏卷第15题)化合物I是鞘氨醇激酶抑制剂,其合成路线如下:(1)化合物A的酸性比环己醇的___________(填“强”或“弱”或“无差别”)。
(2)B的分子式为 ,可由乙酸与 反应合成,B的结构简式为___________。
(3)A→C中加入 是为了结构反应中产生的___________(填化学式)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:___________。
碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%
酸性 溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有
1个峰。
(5)G的分子式为 ,F→H的反应类型为___________。
(6)写出以 、 和 为原料制备 的合成路线流图
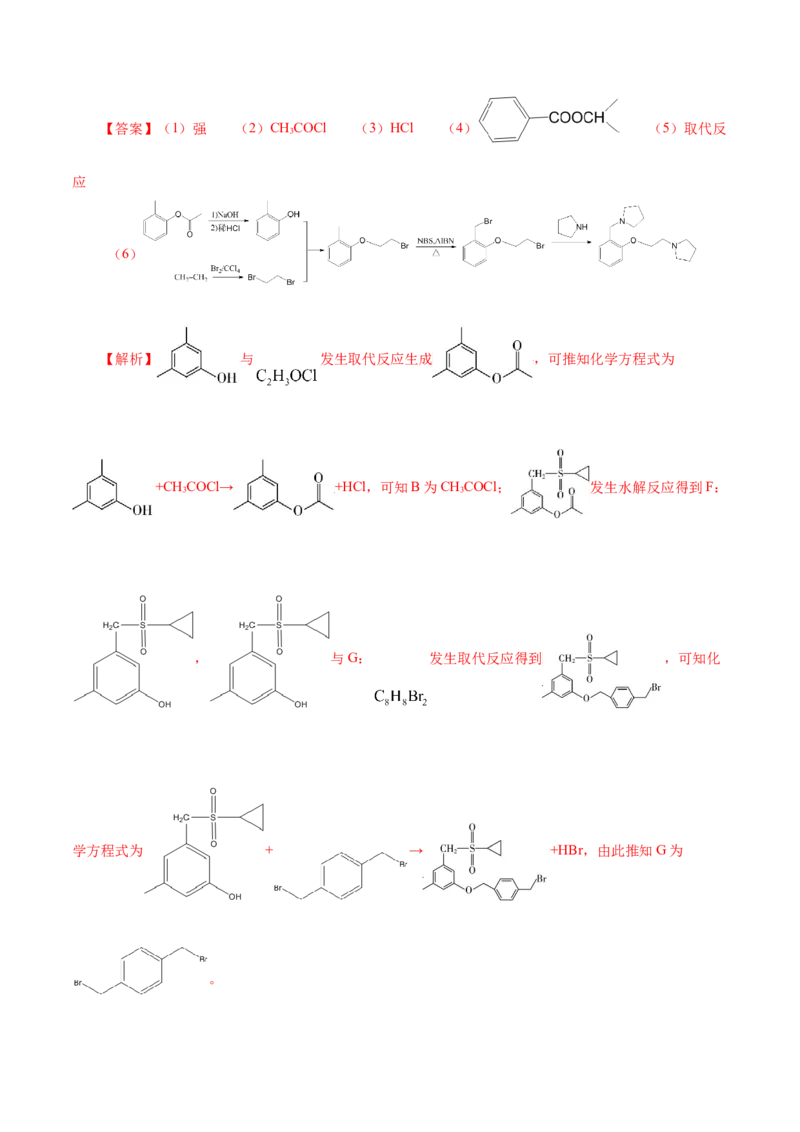
___________ (须用NBS和AlBN,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。【答案】(1)强 (2)CHCOCl (3)HCl (4) (5)取代反
3
应
(6)
【解析】 与 发生取代反应生成 ,可推知化学方程式为
+CH COCl→ +HCl,可知B为CHCOCl; 发生水解反应得到F:
3 3
, 与G: 发生取代反应得到 ,可知化
学方程式为 + → +HBr,由此推知G为
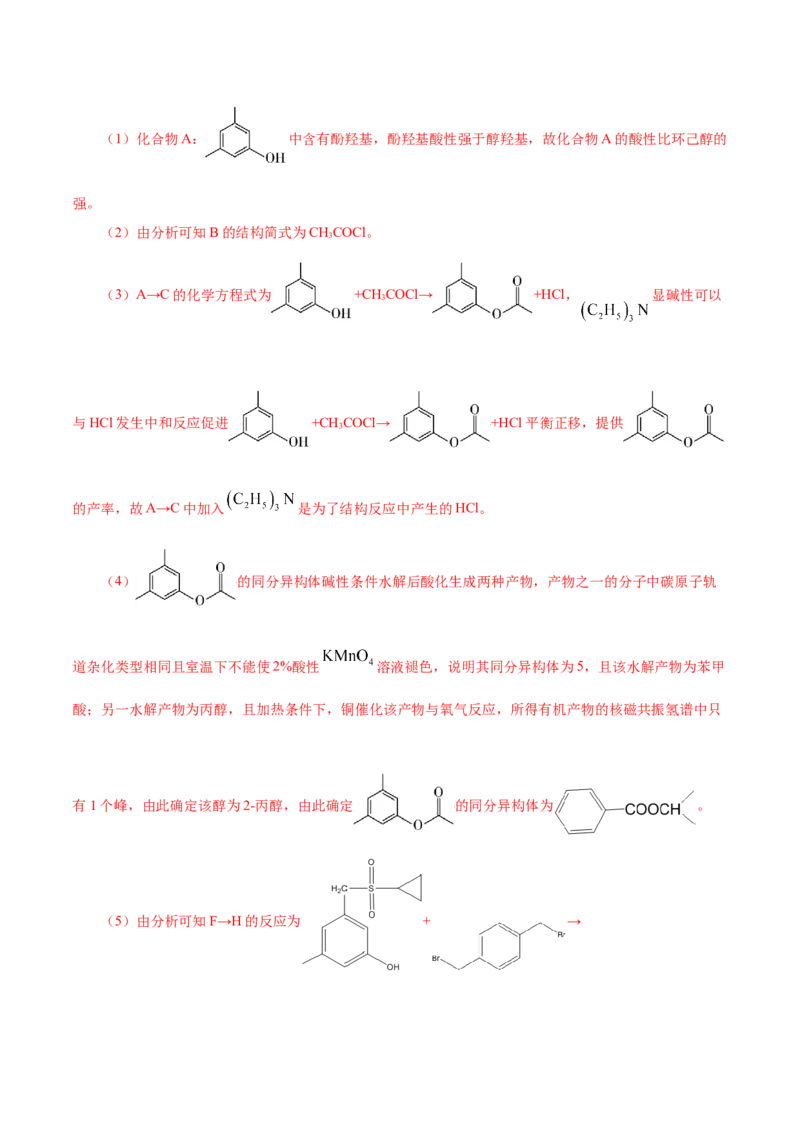
。(1)化合物A: 中含有酚羟基,酚羟基酸性强于醇羟基,故化合物A的酸性比环己醇的
强。
(2)由分析可知B的结构简式为CHCOCl。
3
(3)A→C的化学方程式为 +CH COCl→ +HCl, 显碱性可以
3
与HCl发生中和反应促进 +CH COCl→ +HCl平衡正移,提供
3
的产率,故A→C中加入 是为了结构反应中产生的HCl。
(4) 的同分异构体碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨
道杂化类型相同且室温下不能使2%酸性 溶液褪色,说明其同分异构体为5,且该水解产物为苯甲
酸;另一水解产物为丙醇,且加热条件下,铜催化该产物与氧气反应,所得有机产物的核磁共振氢谱中只
有1个峰,由此确定该醇为2-丙醇,由此确定 的同分异构体为 。
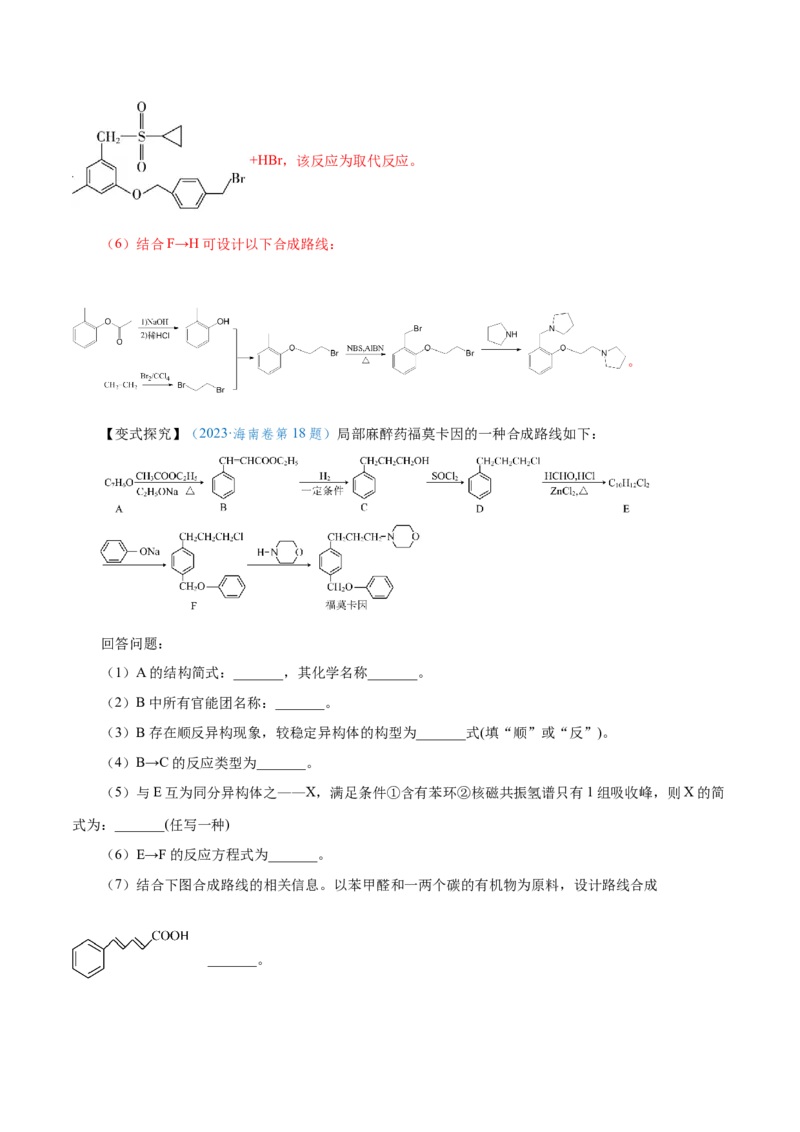
(5)由分析可知F→H的反应为 + →+HBr,该反应为取代反应。
(6)结合F→H可设计以下合成路线:
。
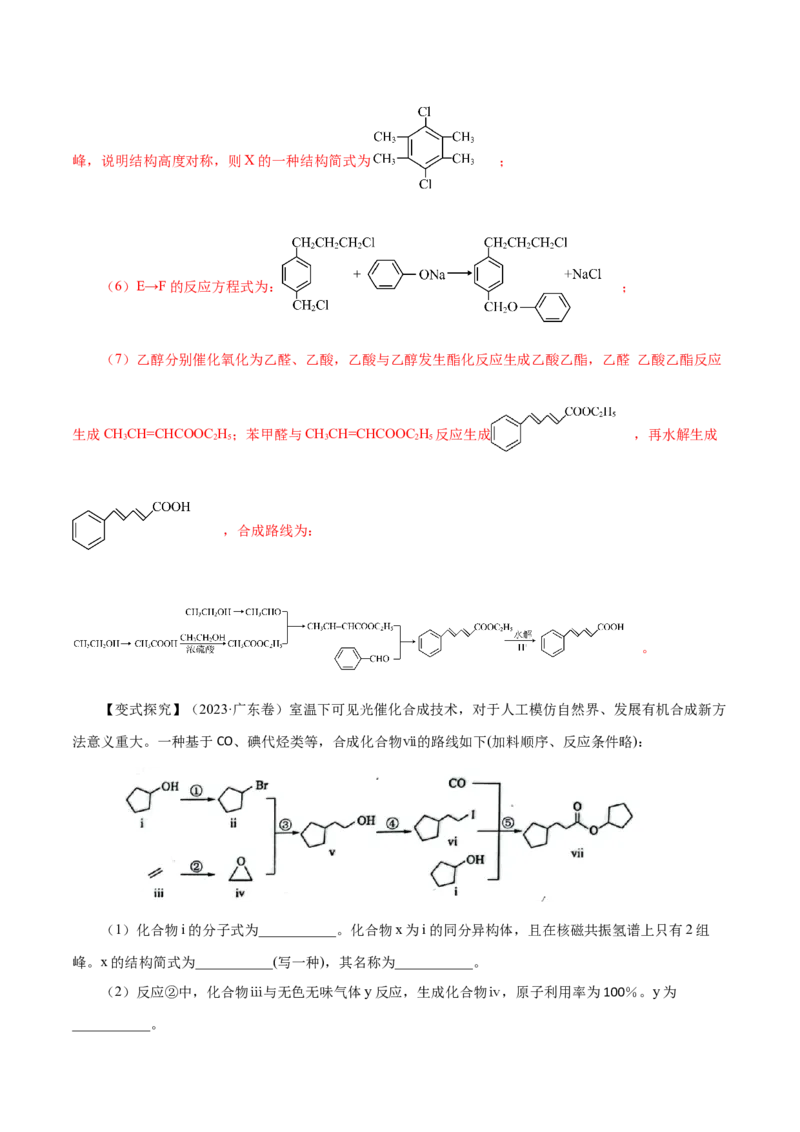
【变式探究】(2023·海南卷第18题)局部麻醉药福莫卡因的一种合成路线如下:
回答问题:
(1)A的结构简式:_______,其化学名称_______。
(2)B中所有官能团名称:_______。
(3)B存在顺反异构现象,较稳定异构体的构型为_______式(填“顺”或“反”)。
(4)B→C的反应类型为_______。
(5)与E互为同分异构体之——X,满足条件①含有苯环②核磁共振氢谱只有1组吸收峰,则X的简
式为:_______(任写一种)
(6)E→F的反应方程式为_______。
(7)结合下图合成路线的相关信息。以苯甲醛和一两个碳的有机物为原料,设计路线合成
_______。【答案】(1) 苯甲醛 (2)碳碳双键、酯基 (3)反 (4)还原反应
(5) (6)
(7)
【解析】结合B的结构式,可逆向推得A的结构为 ,B与氢气一定条件下反应还原
生成C,C在SOCl2条件下发生取代反应生成D,D在HCHO、HCl、ZnCl,发生取代反应生成E(
2
),E与 发生取代生成F,F与 发生取代反应生成
福莫卡因。
(1)结合上述分析可知,A的结构简式: ,其化学名称苯甲醛;
(2)结合题干信息中B的结构式,B中所有官能团名称碳碳双键、酯基;
(3)顺式中的两个取代基处于同一侧,空间比较拥挤,范德华力较大,分子内能较高,不稳定,反
式较顺式稳定;
(4)结合上述分析,B→C的反应类型为还原反应;
(5)E的结构为 ,同分异构体满足①含有苯环②核磁共振氢谱只有1组吸收峰,说明结构高度对称,则X的一种结构简式为 ;
(6)E→F的反应方程式为: ;
(7)乙醇分别催化氧化为乙醛、乙酸,乙酸与乙醇发生酯化反应生成乙酸乙酯,乙醛 乙酸乙酯反应
生成CHCH=CHCOOC H;苯甲醛与CHCH=CHCOOC H 反应生成 ,再水解生成
3 2 5 3 2 5
,合成路线为:
。
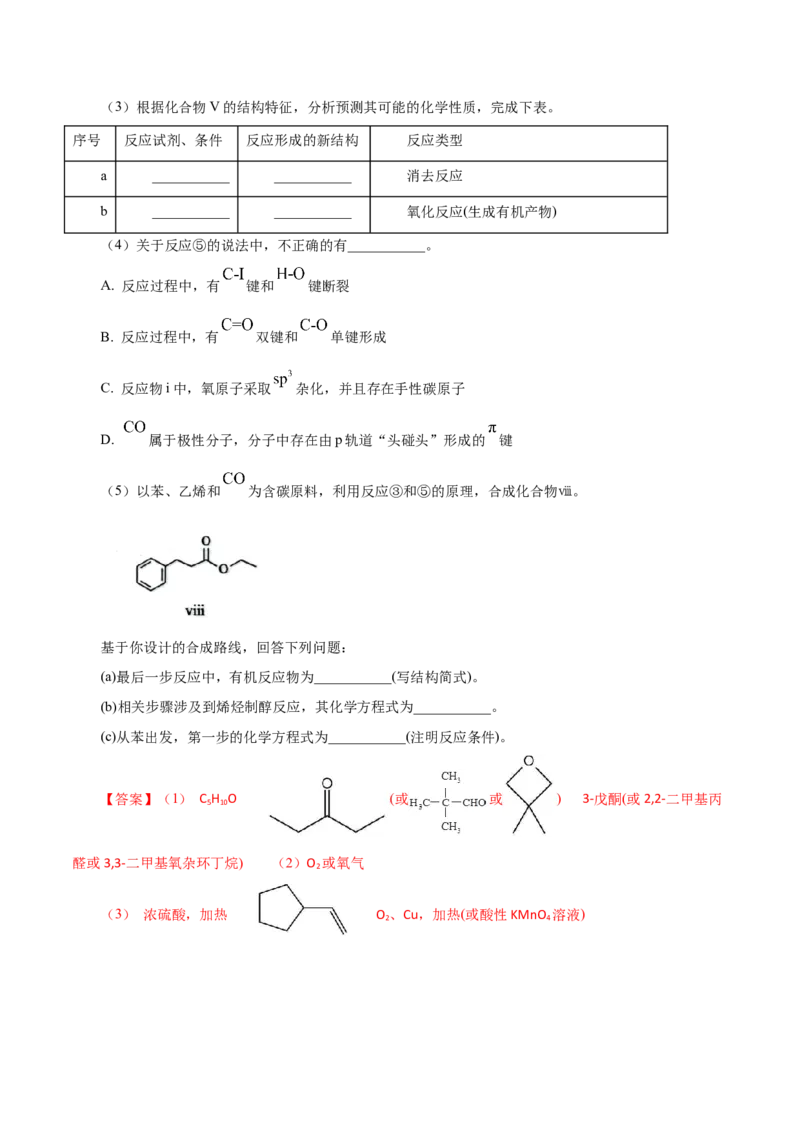
【变式探究】(2023·广东卷)室温下可见光催化合成技术,对于人工模仿自然界、发展有机合成新方
法意义重大。一种基于CO、碘代烃类等,合成化合物ⅶ的路线如下(加料顺序、反应条件略):
(1)化合物i的分子式为___________。化合物x为i的同分异构体,且在核磁共振氢谱上只有2组
峰。x的结构简式为___________(写一种),其名称为___________。
(2)反应②中,化合物ⅲ与无色无味气体y反应,生成化合物ⅳ,原子利用率为100%。y为
___________。(3)根据化合物V的结构特征,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
a ___________ ___________ 消去反应
b ___________ ___________ 氧化反应(生成有机产物)
(4)关于反应⑤的说法中,不正确的有___________。
A. 反应过程中,有 键和 键断裂
B. 反应过程中,有 双键和 单键形成
C. 反应物i中,氧原子采取 杂化,并且存在手性碳原子
D. 属于极性分子,分子中存在由p轨道“头碰头”形成的 键
(5)以苯、乙烯和 为含碳原料,利用反应③和⑤的原理,合成化合物ⅷ。
基于你设计的合成路线,回答下列问题:
(a)最后一步反应中,有机反应物为___________(写结构简式)。
(b)相关步骤涉及到烯烃制醇反应,其化学方程式为___________。
(c)从苯出发,第一步的化学方程式为___________(注明反应条件)。
【答案】(1) C H O (或 或 ) 3-戊酮(或2,2-二甲基丙
5 10
醛或3,3-二甲基氧杂环丁烷) (2)O 或氧气
2
(3) 浓硫酸,加热 O 、Cu,加热(或酸性KMnO 溶液)
2 4(或 ) (4)CD
(5) 和CH CH OH
3 2
【解析】 与HBr加热发生取代反应生成 ,②乙烯在催化剂作用下氧化生成
,③ 与 发生开环加成生成 ,④ 发生取代反应生成
,⑤ 与 及CO反应生成 。
(1)化合物i 的分子式为C H O。 不饱和度为1,x可形成碳碳双键或碳氧双
5 10
键或一个圆环,化合物x为i的同分异构体,且在核磁共振氢谱上只有2组峰,说明分子中有对称结构,不
对称的部分放在对称轴上,x的结构简式含酮羰基时为 (或含醛基时为 或含圆环
是为 ),其名称为3-戊酮(或2,2-二甲基丙醛或3,3-二甲基氧杂环丁烷)。
(2)反应②中,化合物ⅲ与无色无味气体y反应,生成化合物ⅳ,原子利用率为100%,②乙烯在催化剂作用下氧化生成 ,y为O 或氧气。
2
(3)根据化合物V 的结构特征,分析预测其可能的化学性质:含有羟基,且与羟基
相连的碳的邻碳上有氢,可在浓硫酸、加热条件下发生消去反应生成 ,与羟基相连的碳上有
氢,可在铜或银催化作用下氧化生成 ,或酸性KMnO 溶液中氧化生成
4
,见下表:
序号 反应试剂、条件 反应形成的新结构 反应类型
a 浓硫酸,加热 消去反应
O 、Cu,,
2 氧化反应(生成有机
b 加热(或酸性 (或 )
产物)
KMnO 溶液)
4
(4)从产物中不存在C-I键和H-O键可以看出,反应过程中,有C-I键和H-O键断裂,故A正确;反
应物中不存在CCOO双键,酰碘基中碘原子离去与羟基中氢离去,余下的部分结合形成酯基中C-O单键,
所以反应过程中,有C=O双键和C-O单键形成,故B正确;反应物i 中,氧原子采取sp3杂化,
但与羟基相连的碳有对称轴,其它碳上均有2个氢,分子中不存在手性碳原子,故C错误;CO属于极性分
子,分子中存在由p轨道“肩并肩”形成的π键,故D错误;故答案为CD;
(5)以苯、乙烯和CO为含碳原料,利用反应③和⑤的原理,合成化合物ⅷ。乙烯与水在催化剂加热
加压条件下合成乙醇;乙烯在银催化作用下氧化生成环氧乙醚;苯在铁催化作用下与溴生成溴苯,溴苯与
环氧乙醚生成 ,与HI反应合成 ,最后根据反应⑤的原理, 与乙醇、CO合成化合物ⅷ。(a)最后一步反应中,有机反应物为 和CH CH OH。 (b)相关步骤
3 2
涉及到烯烃制醇反应,其化学方程式为 。 (c)从苯出发,第一
步的化学方程式为 。
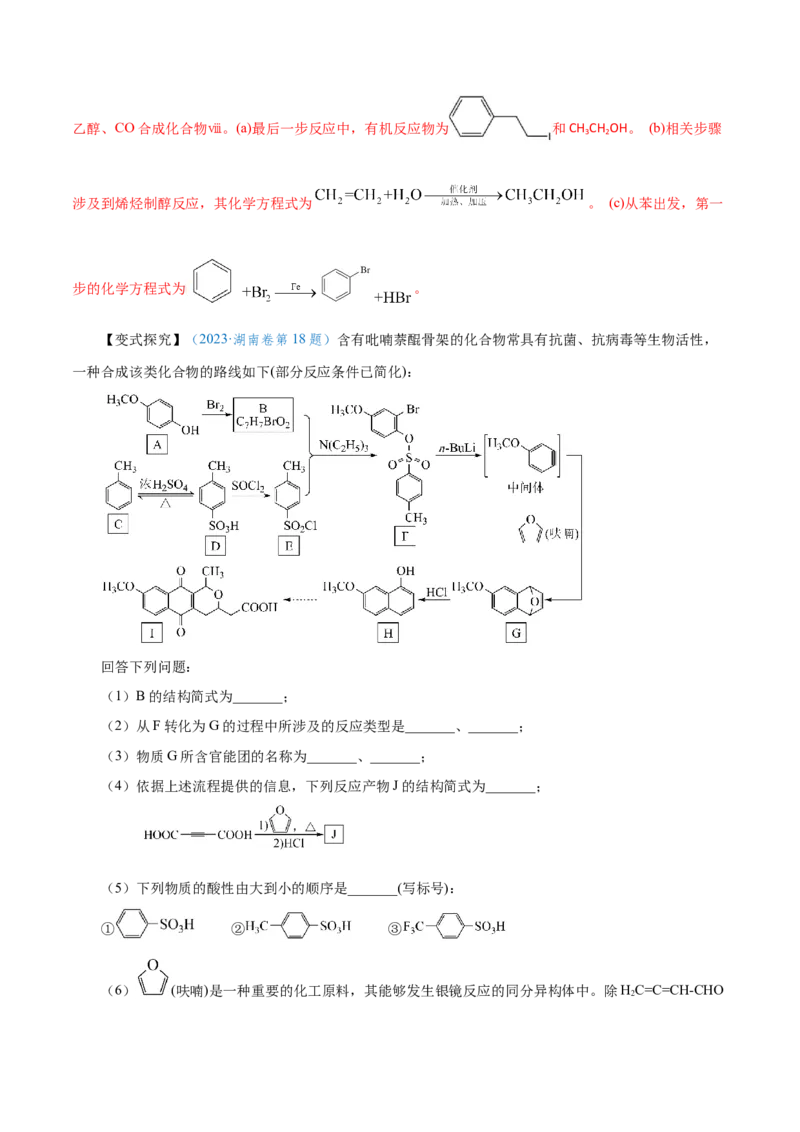
【变式探究】(2023·湖南卷第18题)含有吡喃萘醌骨架的化合物常具有抗菌、抗病毒等生物活性,
一种合成该类化合物的路线如下(部分反应条件已简化):
回答下列问题:
(1)B的结构简式为_______;
(2)从F转化为G的过程中所涉及的反应类型是_______、_______;
(3)物质G所含官能团的名称为_______、_______;
(4)依据上述流程提供的信息,下列反应产物J的结构简式为_______;
(5)下列物质的酸性由大到小的顺序是_______(写标号):
① ② ③
(6) (呋喃)是一种重要的化工原料,其能够发生银镜反应的同分异构体中。除HC=C=CH-CHO
2外,还有_______种;
(7)甲苯与溴在FeBr 催化下发生反应,会同时生成对溴甲苯和邻溴甲苯,依据由C到D的反应信
3
息,设计以甲苯为原料选择性合成邻溴甲苯的路线_______(无机试剂任选)。
【答案】(1) (2)消去反应 加成反应 (3)碳碳双键 醚键
(4) (5)②>③>① (6)4
(7)
【解析】
(1)有机物A与Br 反应生成有机物B,有机物B与有机物E发生取代反应生成有机物F,结合有机
2
物A、F的结构和有机物B的分子式可以得到有机物B的结构式,即 。
(2)有机物F转化为中间体时消去的是-Br和 ,发生的是消去反应,中间体与呋喃反应生成有机
物G时,中间体中的碳碳三键发生断裂与呋喃中的两个双键发生加成反应,故答案为消去反应、加成反
应。
(3)根据有机物G的结构,有机物G中的官能团为碳碳双键、醚键。
(4)根据上述反应流程分析, 与呋喃反应生成 ,
继续与HCl反应生成有机物J,有机物J的结构为 。
(5)苯环上带有甲基时,甲基增强了苯环上的电子云密度,导致磺酸根离子中的氧原子电子云密度
降低,使其更容易失去质子,但当甲基上的H原子被F原子代替时,三氟甲基对苯环上电子的吸引力有所
降低,因此对甲基苯磺酸的酸性强于对三氟甲基苯磺酸的酸性,但没有甲基时的苯磺酸,由于没有其他基团对苯环上电子的吸引导致磺根中S对H的吸引力增强,使H的电子程度减弱,故酸性大小为②>③>①。
(6)呋喃是一种重要的化工原料,其同分异构体中可以发生银镜反应,说明其同分异构体中含有醛
基,这样的同分异构体共有4种,分别为:CH-C≡C-CHO、CH≡C-CH -CHO、 、 。
3 2
(7)甲苯和溴在FeBr 的条件下生成对溴甲苯和邻溴甲苯,因题目中欲合成邻溴甲苯,因此需要对甲
3
基的对位进行处理,利用题目中流程所示的步骤将甲苯与硫酸反应生成对甲基苯磺酸,再将对甲基苯磺酸
与溴反应生成 ,再将 中的磺酸基水解得到目标化合物,具体的合成流程为:
。