文档内容
第3课时 必备知识——原电池和常见化学电源
[重要概念]①原电池;②一次电池;③二次电池;④燃料电池
知识清单 [基本规律]①原电池的构成条件;②原电池的工作原理;③原电池工作原理
的应用
知识点1 原电池的构成及工作原理
1.原电池的概念
原电池是把化学能转化为电能的装置,其反应本质是发生了氧化还原反应。
2.原电池的形成条件
形成
具体分析
条件
反应 能自发进行的氧化还原反应(一般是活泼性强的金属与电解质溶液反应)
电极 一般是活泼性不同的两个电极
闭合 形成闭合回路的两个条件:①电解质溶液(或熔融电解质);②两电极直接或间
回路 接接触,并插入电解质溶液(或熔融电解质)中
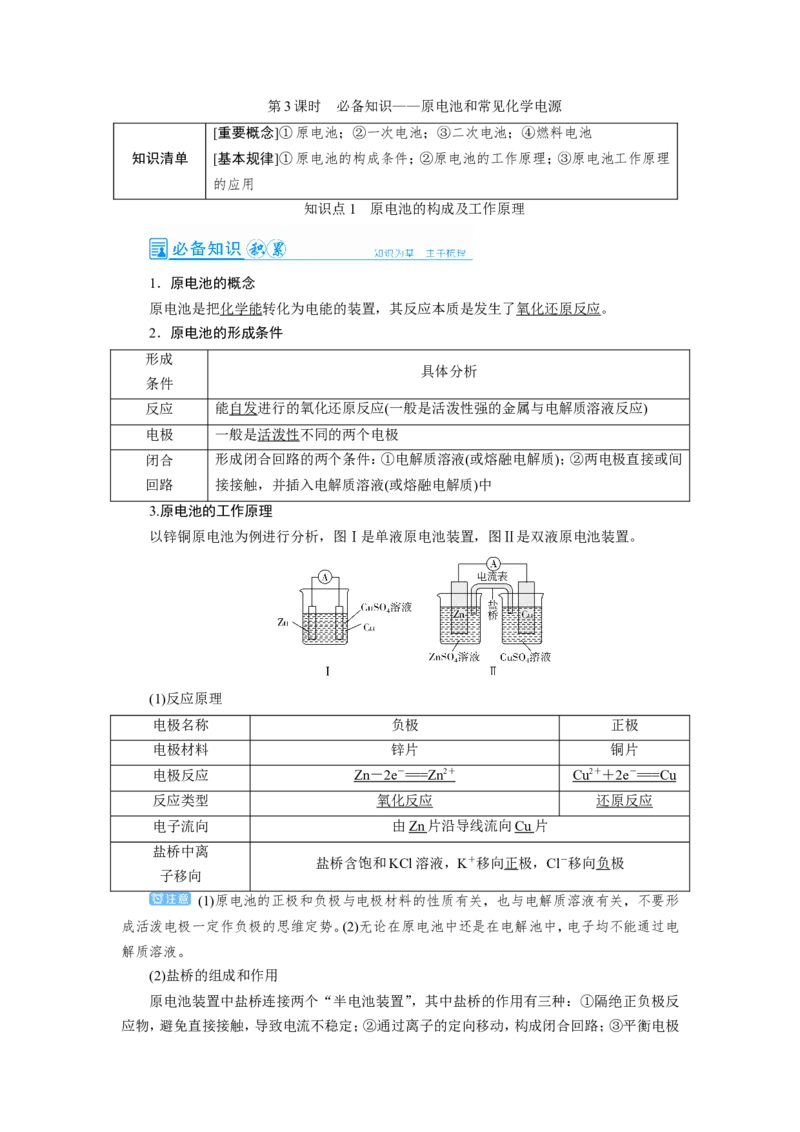
3.原电池的工作原理
以锌铜原电池为例进行分析,图Ⅰ是单液原电池装置,图Ⅱ是双液原电池装置。
(1)反应原理
电极名称 负极 正极
电极材料 锌片 铜片
电极反应 Zn - 2e - == =Zn 2 + Cu 2 + + 2e - == =Cu
反应类型 氧化反应 还原反应
电子流向 由Zn 片沿导线流向Cu 片
盐桥中离
盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极
子移向
(1)原电池的正极和负极与电极材料的性质有关,也与电解质溶液有关,不要形
成活泼电极一定作负极的思维定势。(2)无论在原电池中还是在电解池中,电子均不能通过电
解质溶液。
(2)盐桥的组成和作用
原电池装置中盐桥连接两个“半电池装置”,其中盐桥的作用有三种:①隔绝正负极反
应物,避免直接接触,导致电流不稳定;②通过离子的定向移动,构成闭合回路;③平衡电极区的电荷。
[通关1] (易错排查)判断正误
(1)理论上,任何自发的氧化还原反应都可设计成原电池(√)
(2)在原电池中,发生氧化反应的一极一定是负极(√)
(3)在锌铜原电池中,因为有电子通过电解质溶液形成闭合回路,所以有电流产生(×)
(4)原电池工作时,溶液中的阳离子向负极移动,盐桥中的阳离子向正极移动(×)
(5)两种活泼性不同的金属组成原电池的两极,活泼金属一定作负极(×)
(6)实验室制备H 时,用粗锌(含Cu、Fe等)代替纯锌与盐酸反应效果更佳(√)
2
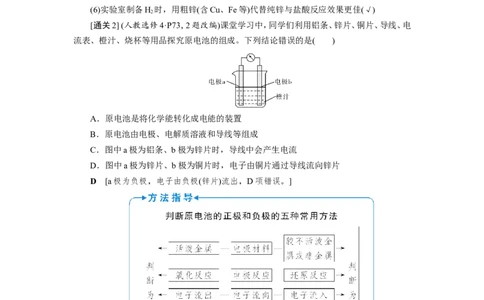
[通关2] (人教选修4·P73,2题改编)课堂学习中,同学们利用铝条、锌片、铜片、导线、电
流表、橙汁、烧杯等用品探究原电池的组成。下列结论错误的是( )
A.原电池是将化学能转化成电能的装置
B.原电池由电极、电解质溶液和导线等组成
C.图中a极为铝条、b极为锌片时,导线中会产生电流
D.图中a极为锌片、b极为铜片时,电子由铜片通过导线流向锌片
D [a极为负极,电子由负极(锌片)流出,D项错误。]
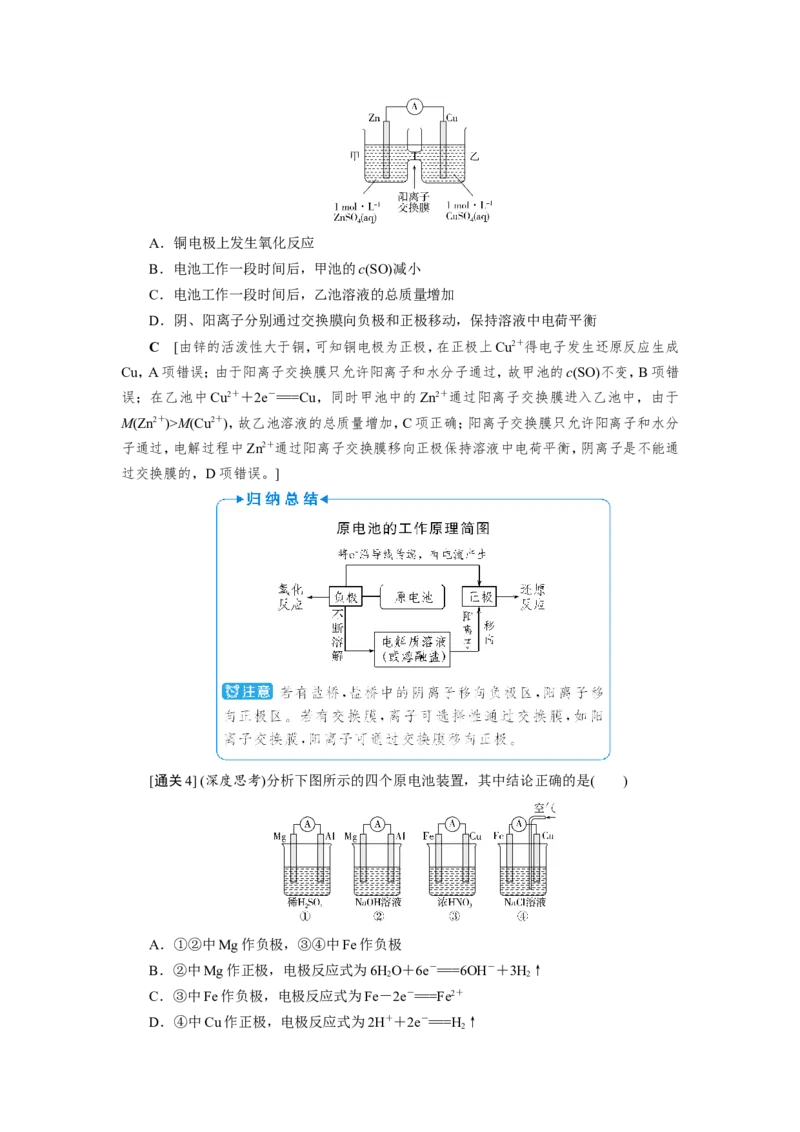
[通关3] (2021·安徽合肥检测)锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离
子和水分子通过,下列有关叙述正确的是( )A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
C [由锌的活泼性大于铜,可知铜电极为正极,在正极上Cu2+得电子发生还原反应生成
Cu,A项错误;由于阳离子交换膜只允许阳离子和水分子通过,故甲池的c(SO)不变,B项错
误;在乙池中Cu2++2e-===Cu,同时甲池中的Zn2+通过阳离子交换膜进入乙池中,由于
M(Zn2+)>M(Cu2+),故乙池溶液的总质量增加,C项正确;阳离子交换膜只允许阳离子和水分
子通过,电解过程中Zn2+通过阳离子交换膜移向正极保持溶液中电荷平衡,阴离子是不能通
过交换膜的,D项错误。]
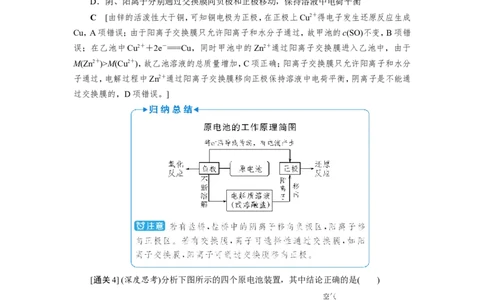
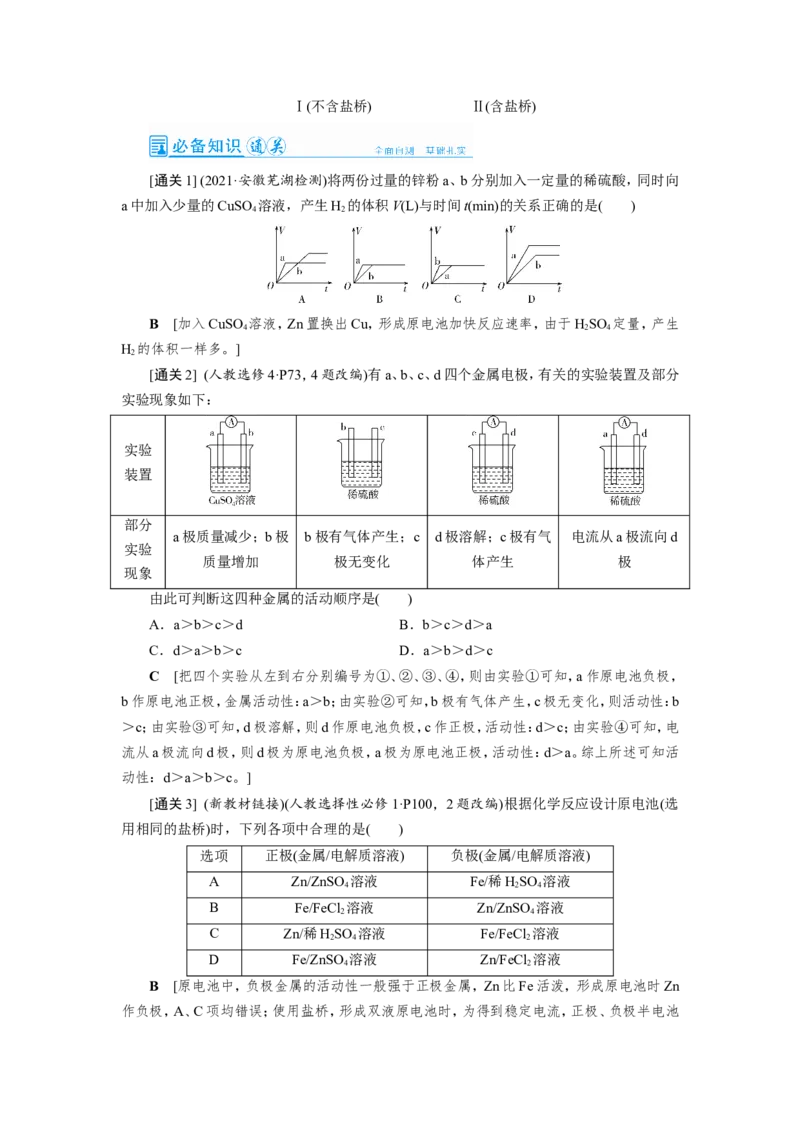
[通关4] (深度思考)分析下图所示的四个原电池装置,其中结论正确的是( )
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6HO+6e-===6OH-+3H↑
2 2
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H ↑
2B [②中Mg不与NaOH溶液反应,而Al能和NaOH溶液反应失去电子,故Al是负极;
③中Fe在浓硝酸中钝化,Cu和浓HNO 反应失去电子作负极,A、C错;②中电池总反应为
3
2Al+2NaOH+2HO===2NaAlO +3H↑,负极反应式为 2Al+8OH--6e-===2AlO+
2 2 2
4HO,二者相减得到正极反应式为6HO+6e-===6OH-+3H↑,B正确;④中Cu是正极,
2 2 2
电极反应式为O+2HO+4e-===4OH-,D错。]
2 2
知识点2 原电池原理的应用
1.加快氧化还原反应的速率
一个自发进行的氧化还原反应,形成原电池时会使反应速率加快。例如,在锌粉与稀
HSO 反应制取H 时,加入少量CuSO 溶液,置换出的Cu能与Zn形成原电池,使产生H 的
2 4 2 4 2
反应速率加快。
2.比较金属的活动性强弱
原电池中,负极一般是活动性较强的金属,正极一般是活动性较弱的金属(或非金属)。例
如,用导线将金属A和B连接后,插入到稀硫酸中,一段时间后,观察到A溶解,而B上有气
体放出,则说明A作负极,B作正极,据此推知金属活动性:A>(填“>”或“<”)B。
3.用于金属的防护
被保护的金属制品作原电池的正极而得到保护。例如,要保护钢铁水闸,可用导线将其
与锌块相连,使锌作原电池的负极,铁闸作正极而受到保护。
4.设计制作原电池装置
例如,根据反应Cu+2Ag+===Cu2++2Ag设计原电池:Ⅰ(不含盐桥) Ⅱ(含盐桥)
[通关1] (2021·安徽芜湖检测)将两份过量的锌粉a、b分别加入一定量的稀硫酸,同时向
a中加入少量的CuSO 溶液,产生H 的体积V(L)与时间t(min)的关系正确的是( )
4 2
B [加入CuSO 溶液,Zn置换出Cu,形成原电池加快反应速率,由于HSO 定量,产生
4 2 4
H 的体积一样多。]
2
[通关2] (人教选修4·P73,4题改编)有a、b、c、d四个金属电极,有关的实验装置及部分
实验现象如下:
实验
装置
部分
a极质量减少;b极 b极有气体产生;c d极溶解;c极有气 电流从a极流向d
实验
质量增加 极无变化 体产生 极
现象
由此可判断这四种金属的活动顺序是( )
A.a>b>c>d B.b>c>d>a
C.d>a>b>c D.a>b>d>c
C [把四个实验从左到右分别编号为①、②、③、④,则由实验①可知,a作原电池负极,
b作原电池正极,金属活动性:a>b;由实验②可知,b极有气体产生,c极无变化,则活动性:b
>c;由实验③可知,d极溶解,则d作原电池负极,c作正极,活动性:d>c;由实验④可知,电
流从a极流向d极,则d极为原电池负极,a极为原电池正极,活动性:d>a。综上所述可知活
动性:d>a>b>c。]
[通关3] (新教材链接)(人教选择性必修1·P100,2题改编)根据化学反应设计原电池(选
用相同的盐桥)时,下列各项中合理的是( )
选项 正极(金属/电解质溶液) 负极(金属/电解质溶液)
A Zn/ZnSO 溶液 Fe/稀HSO 溶液
4 2 4
B Fe/FeCl 溶液 Zn/ZnSO 溶液
2 4
C Zn/稀HSO 溶液 Fe/FeCl 溶液
2 4 2
D Fe/ZnSO 溶液 Zn/FeCl 溶液
4 2
B [原电池中,负极金属的活动性一般强于正极金属,Zn比Fe活泼,形成原电池时Zn
作负极,A、C项均错误;使用盐桥,形成双液原电池时,为得到稳定电流,正极、负极半电池中电解质溶液一般是电极金属材料形成的盐溶液,D项错误,B项正确。]
[通关4] (深度思考)某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,完
成有关实验项目:
方案Ⅰ:有人提出将大小相等的铁片和铜片,分别同时放入稀硫酸(或稀盐酸)中,观察产
生气泡的快慢,据此确定它们的活动性。该原理的离子方程式为___________。
方案Ⅱ:有人利用Fe、Cu做电极设计成原电池,以确定它们的活动性。试在下面的方框
内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出电极反应式。
正极反应式:_____________________________________________________。
负极反应式:_____________________________________________________。
方案Ⅲ:结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案:
________________________________________________________________________
________________________________________________________________________
(与方案Ⅰ、Ⅱ不能雷同),用离子方程式表示其反应原理:
________________________________________________________________________。
解析 方案Ⅰ:铁与酸反应产生气泡,Fe+2H+===Fe2++H↑,而铜与酸不反应。
2
方案Ⅱ:设计原电池时以铁、铜为电极,电解质溶液为稀硫酸或盐酸等溶液。实验现象是
铁溶解,而铜极上有无色气泡产生。
在负极:Fe失去电子变为Fe2+,Fe-2e-===Fe2+;在正极,溶液中的H+获得电子变为
H 2H++2e-===H ↑。
2, 2
方案Ⅲ:设计简单实验时注意原理与方案Ⅰ及方案Ⅱ的原理不同,且现象明显,操作简
单。
将铁片置于CuSO 溶液,若铁片表面覆盖一层铜,说明Fe比Cu活动性强,离子方程式
4
为Fe+Cu2+===Fe2++Cu。(合理即可)
答案 方案Ⅰ:Fe+2H+===Fe2++H↑
2
方案Ⅱ:装置如图所示
2H++2e-===H ↑ Fe-2e-===Fe2+
2方案Ⅲ:将铁片置于CuSO 溶液,若铁片表面覆盖一层铜,说明Fe比Cu活动性强 Fe
4
+Cu2+===Fe2++Cu
知识点3 常见化学电源
1.一次电池(只使用一次,不能重复使用)
负极材料:Zn
电极反应: Zn + 2OH - - 2e - == =Zn (OH)
2
碱性 正极材料:碳棒
锌锰 电极反应:2MnO +2HO+2e-
2 2
电池 ===2MnOOH+2OH-
总反应:Zn+2MnO +
2
2HO===2MnOOH+Zn(OH)
2 2
负极材料:Zn
电极反应: Zn + 2OH - - 2e - == =Zn (OH)
2
正极材料:Ag O
2
锌银
电极反应:Ag O+HO+2e-===2Ag+
2 2
电池
2OH-
总反应:Zn+Ag O+HO===Zn(OH) +
2 2 2
2Ag
2.二次电池(放电后充电复原继续使用)
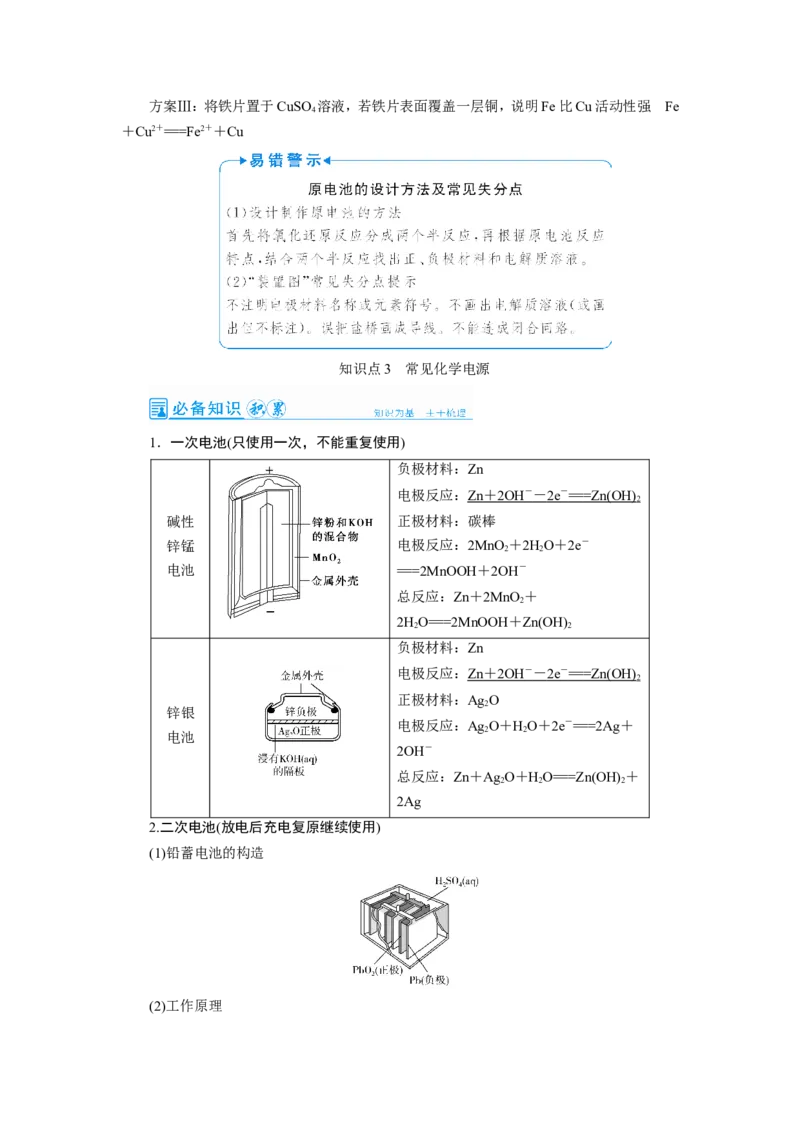
(1)铅蓄电池的构造
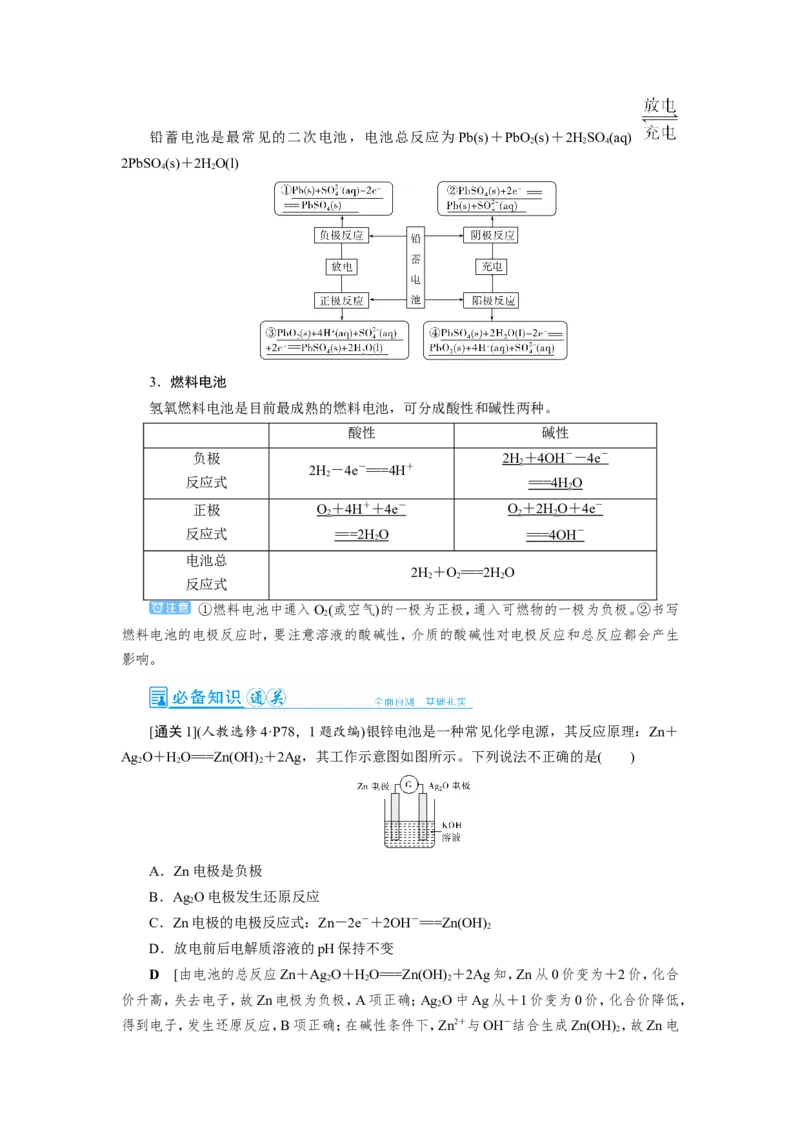
(2)工作原理铅蓄电池是最常见的二次电池,电池总反应为 Pb(s)+PbO (s)+2HSO (aq)
2 2 4
2PbSO (s)+2HO(l)
4 2
3.燃料电池
氢氧燃料电池是目前最成熟的燃料电池,可分成酸性和碱性两种。
酸性 碱性
负极 2H + 4OH - - 4 e -
2
2H-4e-===4H+
2
反应式 == =4H O
2
正极 O + 4H + + 4 e - O + 2H O + 4e -
2 2 2
反应式 == =2H O == =4OH -
2
电池总
2H+O===2H O
2 2 2
反应式
①燃料电池中通入O(或空气)的一极为正极,通入可燃物的一极为负极。②书写
2
燃料电池的电极反应时,要注意溶液的酸碱性,介质的酸碱性对电极反应和总反应都会产生
影响。
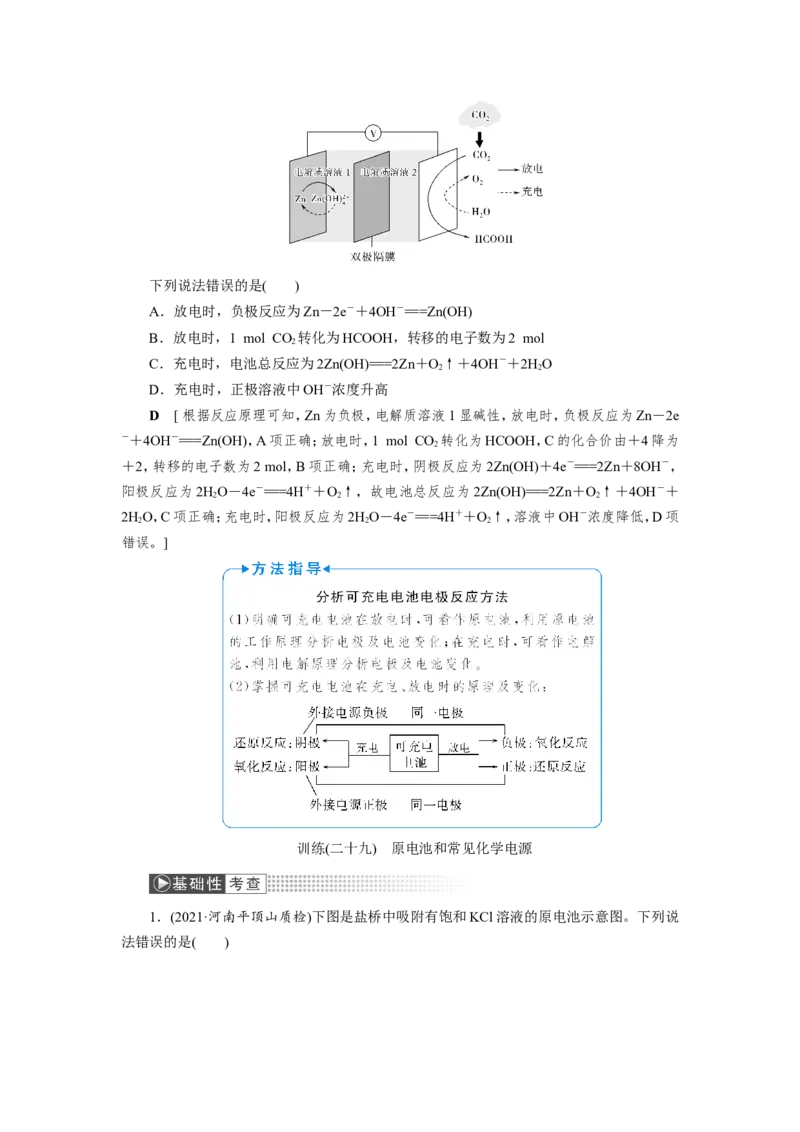
[通关1](人教选修4·P78,1题改编)银锌电池是一种常见化学电源,其反应原理:Zn+
Ag O+HO===Zn(OH) +2Ag,其工作示意图如图所示。下列说法不正确的是( )
2 2 2
A.Zn电极是负极
B.Ag O电极发生还原反应
2
C.Zn电极的电极反应式:Zn-2e-+2OH-===Zn(OH)
2
D.放电前后电解质溶液的pH保持不变
D [由电池的总反应Zn+Ag O+HO===Zn(OH) +2Ag知,Zn从0价变为+2价,化合
2 2 2
价升高,失去电子,故Zn电极为负极,A项正确;Ag O中Ag从+1价变为0价,化合价降低,
2
得到电子,发生还原反应,B项正确;在碱性条件下,Zn2+与OH-结合生成Zn(OH) ,故Zn电
2极的电极反应式为Zn-2e-+2OH-===Zn(OH) ,C项正确;根据总反应可知,反应中HO被
2 2
不断地消耗,电解质溶液中OH-浓度增大,所以放电后电解质溶液的pH增大,D项错误。]
[通关2] (新教材链接)(人教选择性必修1·P100,3题改编)碱性锌锰电池的总反应为Zn
+2MnO +2HO===2MnO(OH)+Zn(OH) 。下列有关该电池的说法中不正确的是( )
2 2 2
A.Zn作负极,电极反应式为Zn-2e-+2OH-===Zn(OH)
2
B.MnO 作正极,发生还原反应
2
C.电池工作时,电流由MnO 经外电路流向Zn
2
D.电池工作时,KOH没有发挥作用
D [Zn作负极,被氧化生成Zn(OH) ,电极反应式为Zn-2e-+2OH-===Zn(OH) ,A项
2 2
正确;MnO 作正极,被还原生成MnO(OH),B项正确;电池工作时,电流由正极流向负极,则
2
电流由MnO 经外电路流向Zn,C项正确;电池工作时,KOH未参与电池总反应,但起到导
2
电作用,D项错误。]
[通关3] (2021·湖北武汉检测)如图为以Pt为电极的氢氧燃料电池的工作原理示意图,稀
HSO 为电解质溶液。下列有关说法不正确的是( )
2 4
A.a极为负极,电子由a极经外电路流向b极
B.a极的电极反应式:H-2e-===2H+
2
C.电池工作一段时间后,装置中c(H SO )增大
2 4
D.若将H 改为CH,消耗等物质的量的CH 时,O 的用量增多
2 4 4 2
C [在氢氧燃料电池中,氢气在负极失电子,生成氢离子,则a极为负极,电子由a极流
向b极,A项正确;a极的电极反应式:H-2e-===2H+,B项正确;在氢氧燃料电池中,电池
2
的总反应为2H+O===2H O,则电池工作一段时间后,装置中c(H SO )减小,C项错误;1
2 2 2 2 4
mol H 消耗0.5 mol O,1 mol CH 消耗2 mol O ,所以若将H 改为等物质的量CH,O 的用
2 2 4 2 2 4 2
量增多,D项正确。][通关4] (2020·山东卷)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理
有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图
装置处理有机废水(以含CHCOO-的溶液为例)。下列说法错误的是( )
3
A.负极反应为CHCOO-+2HO-8e-===2CO ↑+7H+
3 2 2
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1 mol电子时,模拟海水理论上除盐58.5 g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2∶1
B [由装置示意图可知,负极区CHCOO-发生氧化反应生成CO 和H+,A项正确;隔
3 2
膜1为阴离子交换膜,隔膜2为阳离子交换膜,才能使模拟海水中的氯离子移向负极,钠离子
移向正极,达到海水淡化的目的,B项错误;电路中有1 mol电子通过,则电解质溶液中有1
mol钠离子移向正极,1 mol氯离子移向负极,C项正确;负极产生CO:CHCOO-+2HO-
2 3 2
8e-===2CO ↑+7H+,正极产生H:2H++2e-===H ↑,根据电荷守恒,正、负极产生气体的
2 2 2
物质的量之比为2∶1,D项正确。]
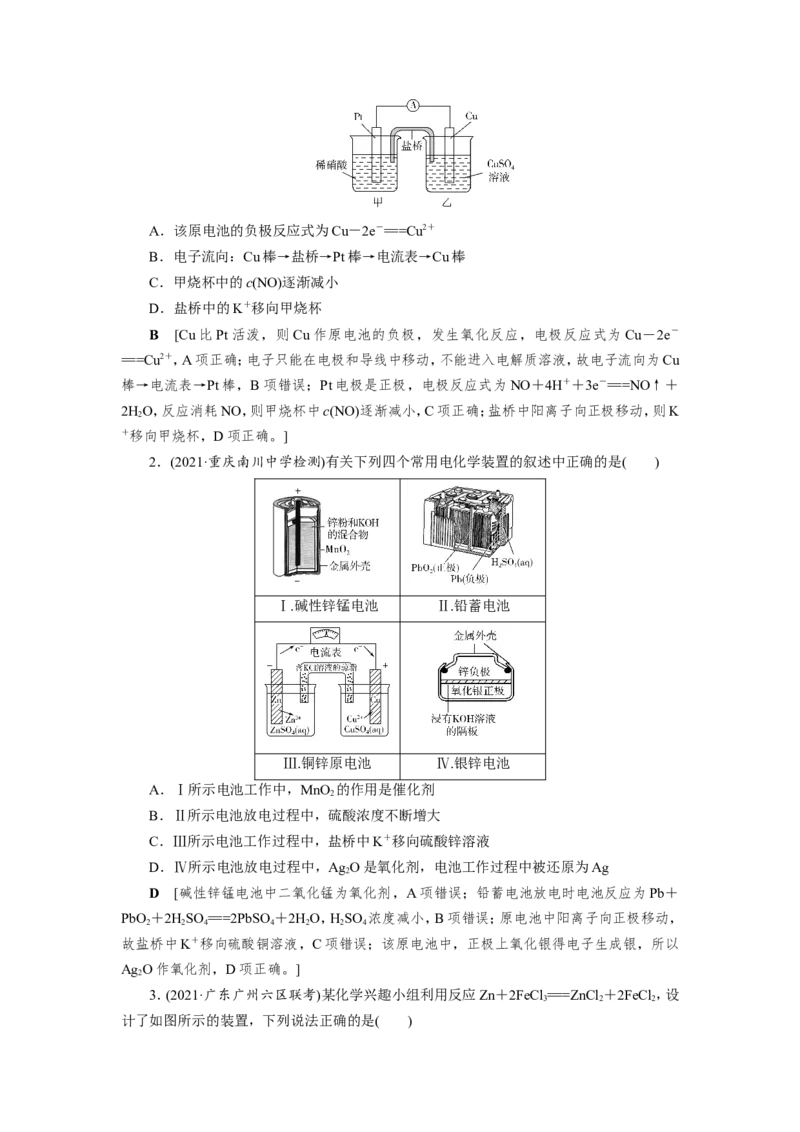
[通关5] (深度思考)(2020·全国卷Ⅰ)科学家近年发明了一种新型ZnCO 水介质电池。
2
电池示意图如图,电极为金属锌和选择性催化材料。放电时,温室气体CO 被转化为储氢物
2
质甲酸等,为解决环境和能源问题提供了一种新途径。下列说法错误的是( )
A.放电时,负极反应为Zn-2e-+4OH-===Zn(OH)
B.放电时,1 mol CO 转化为HCOOH,转移的电子数为2 mol
2
C.充电时,电池总反应为2Zn(OH)===2Zn+O↑+4OH-+2HO
2 2
D.充电时,正极溶液中OH-浓度升高
D [ 根据反应原理可知,Zn为负极,电解质溶液1显碱性,放电时,负极反应为Zn-2e
-+4OH-===Zn(OH),A项正确;放电时,1 mol CO 转化为HCOOH,C的化合价由+4降为
2
+2,转移的电子数为2 mol,B项正确;充电时,阴极反应为2Zn(OH)+4e-===2Zn+8OH-,
阳极反应为2HO-4e-===4H++O↑,故电池总反应为2Zn(OH)===2Zn+O↑+4OH-+
2 2 2
2HO,C项正确;充电时,阳极反应为2HO-4e-===4H++O↑,溶液中OH-浓度降低,D项
2 2 2
错误。]
训练(二十九) 原电池和常见化学电源
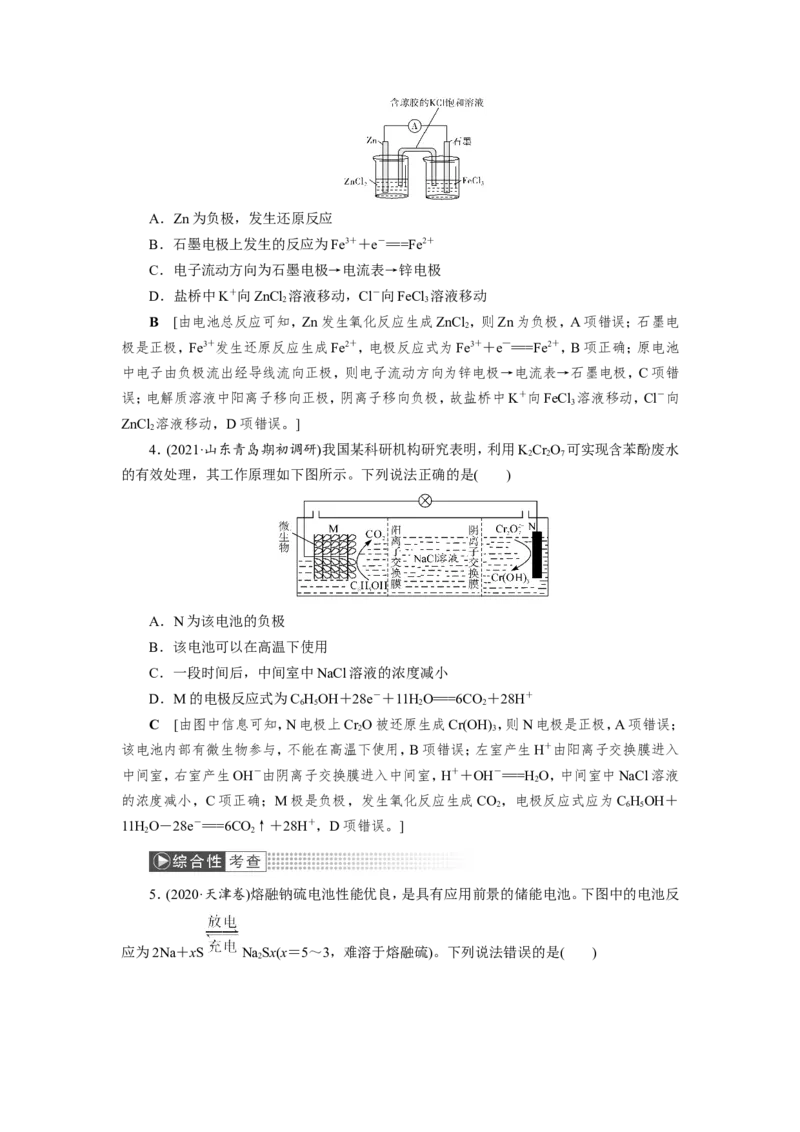
1.(2021·河南平顶山质检)下图是盐桥中吸附有饱和KCl溶液的原电池示意图。下列说
法错误的是( )A.该原电池的负极反应式为Cu-2e-===Cu2+
B.电子流向:Cu棒→盐桥→Pt棒→电流表→Cu棒
C.甲烧杯中的c(NO)逐渐减小
D.盐桥中的K+移向甲烧杯
B [Cu比Pt活泼,则Cu作原电池的负极,发生氧化反应,电极反应式为Cu-2e-
===Cu2+,A项正确;电子只能在电极和导线中移动,不能进入电解质溶液,故电子流向为Cu
棒→电流表→Pt棒,B项错误;Pt电极是正极,电极反应式为NO+4H++3e-===NO↑+
2HO,反应消耗NO,则甲烧杯中c(NO)逐渐减小,C项正确;盐桥中阳离子向正极移动,则K
2
+移向甲烧杯,D项正确。]
2.(2021·重庆南川中学检测)有关下列四个常用电化学装置的叙述中正确的是( )
Ⅰ.碱性锌锰电池 Ⅱ.铅蓄电池
Ⅲ.铜锌原电池 Ⅳ.银锌电池
A.Ⅰ所示电池工作中,MnO 的作用是催化剂
2
B.Ⅱ所示电池放电过程中,硫酸浓度不断增大
C.Ⅲ所示电池工作过程中,盐桥中K+移向硫酸锌溶液
D.Ⅳ所示电池放电过程中,Ag O是氧化剂,电池工作过程中被还原为Ag
2
D [碱性锌锰电池中二氧化锰为氧化剂,A项错误;铅蓄电池放电时电池反应为Pb+
PbO +2HSO ===2PbSO+2HO,HSO 浓度减小,B项错误;原电池中阳离子向正极移动,
2 2 4 4 2 2 4
故盐桥中K+移向硫酸铜溶液,C项错误;该原电池中,正极上氧化银得电子生成银,所以
Ag O作氧化剂,D项正确。]
2
3.(2021·广东广州六区联考)某化学兴趣小组利用反应Zn+2FeCl ===ZnCl +2FeCl ,设
3 2 2
计了如图所示的装置,下列说法正确的是( )A.Zn为负极,发生还原反应
B.石墨电极上发生的反应为Fe3++e-===Fe2+
C.电子流动方向为石墨电极→电流表→锌电极
D.盐桥中K+向ZnCl 溶液移动,Cl-向FeCl 溶液移动
2 3
B [由电池总反应可知,Zn发生氧化反应生成ZnCl,则Zn为负极,A项错误;石墨电
2
极是正极,Fe3+发生还原反应生成Fe2+,电极反应式为Fe3++e—===Fe2+,B项正确;原电池
中电子由负极流出经导线流向正极,则电子流动方向为锌电极→电流表→石墨电极,C项错
误;电解质溶液中阳离子移向正极,阴离子移向负极,故盐桥中K+向FeCl 溶液移动,Cl-向
3
ZnCl 溶液移动,D项错误。]
2
4.(2021·山东青岛期初调研)我国某科研机构研究表明,利用KCr O 可实现含苯酚废水
2 2 7
的有效处理,其工作原理如下图所示。下列说法正确的是( )
A.N为该电池的负极
B.该电池可以在高温下使用
C.一段时间后,中间室中NaCl溶液的浓度减小
D.M的电极反应式为C HOH+28e-+11HO===6CO +28H+
6 5 2 2
C [由图中信息可知,N电极上Cr O被还原生成Cr(OH) ,则N电极是正极,A项错误;
2 3
该电池内部有微生物参与,不能在高温下使用,B项错误;左室产生H+由阳离子交换膜进入
中间室,右室产生OH-由阴离子交换膜进入中间室,H++OH-===H O,中间室中NaCl溶液
2
的浓度减小,C项正确;M极是负极,发生氧化反应生成CO,电极反应式应为C HOH+
2 6 5
11HO-28e-===6CO ↑+28H+,D项错误。]
2 2
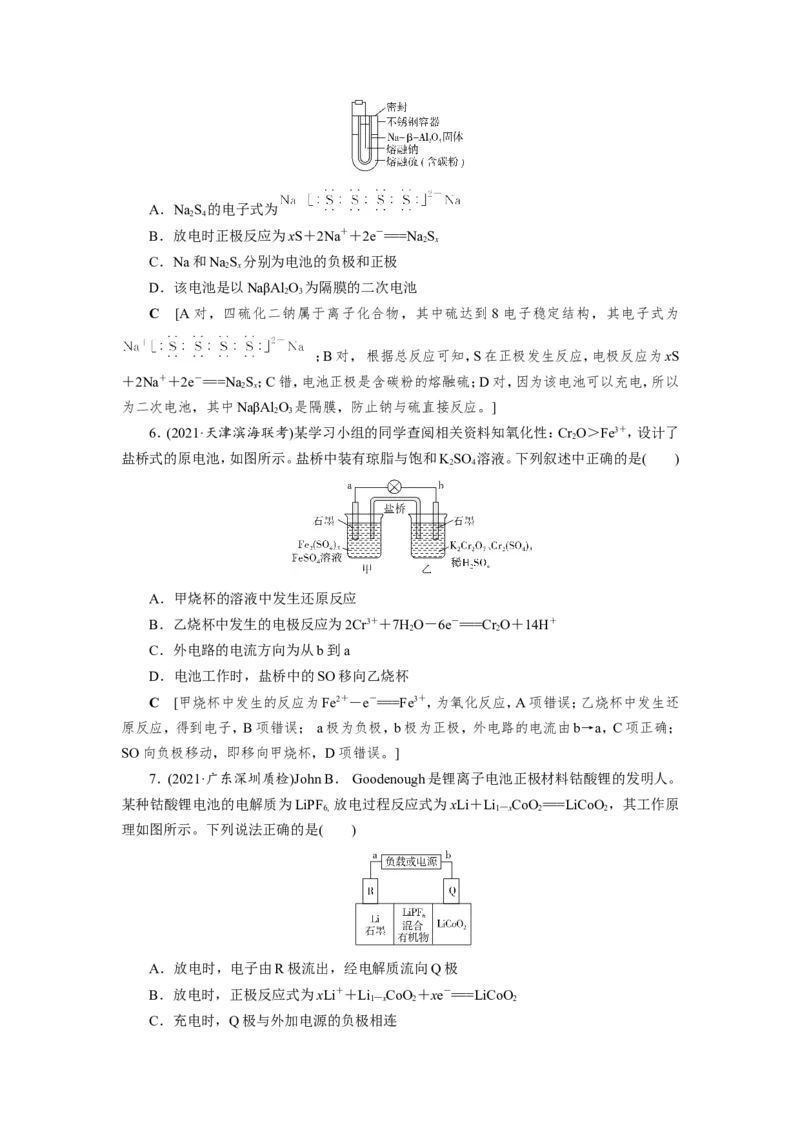
5.(2020·天津卷)熔融钠硫电池性能优良,是具有应用前景的储能电池。下图中的电池反
应为2Na+xS NaSx(x=5~3,难溶于熔融硫)。下列说法错误的是( )
2A.NaS 的电子式为
2 4
B.放电时正极反应为xS+2Na++2e-===Na S
2 x
C.Na和NaS 分别为电池的负极和正极
2 x
D.该电池是以NaβAl O 为隔膜的二次电池
2 3
C [A对,四硫化二钠属于离子化合物,其中硫达到8电子稳定结构,其电子式为
;B对, 根据总反应可知,S在正极发生反应,电极反应为xS
+2Na++2e-===Na S;C错,电池正极是含碳粉的熔融硫;D对,因为该电池可以充电,所以
2 x
为二次电池,其中NaβAl O 是隔膜,防止钠与硫直接反应。]
2 3
6.(2021·天津滨海联考)某学习小组的同学查阅相关资料知氧化性:Cr O>Fe3+,设计了
2
盐桥式的原电池,如图所示。盐桥中装有琼脂与饱和KSO 溶液。下列叙述中正确的是( )
2 4
A.甲烧杯的溶液中发生还原反应
B.乙烧杯中发生的电极反应为2Cr3++7HO-6e-===Cr O+14H+
2 2
C.外电路的电流方向为从b到a
D.电池工作时,盐桥中的SO移向乙烧杯
C [甲烧杯中发生的反应为Fe2+-e-===Fe3+,为氧化反应,A项错误;乙烧杯中发生还
原反应,得到电子,B项错误; a极为负极,b极为正极,外电路的电流由b→a,C项正确;
SO向负极移动,即移向甲烧杯,D项错误。]
7.(2021·广东深圳质检)John B. Goodenough是锂离子电池正极材料钴酸锂的发明人。
某种钴酸锂电池的电解质为LiPF 放电过程反应式为xLi+Li CoO===LiCoO ,其工作原
6, 1—x 2 2
理如图所示。下列说法正确的是( )
A.放电时,电子由R极流出,经电解质流向Q极
B.放电时,正极反应式为xLi++Li CoO+xe-===LiCoO
1—x 2 2
C.充电时,Q极与外加电源的负极相连D.充电时,R极电极反应为Li+-e-===Li
B [放电时,Li/石墨是负极,则电子由R极流出经负载流向Q极,不能进入电解质,A
项错误;放电时,LiCoO 是正极,发生还原反应,电极反应式为xLi++Li CoO +xe-
2 1—x 2
===LiCoO,B项正确;充电时,Q极是阳极,与外加电源的正极相连,C项错误;充电时,R极
2
是阴极,Li+得电子发生还原反应,电极反应式为Li++e-===Li,D项错误。]
8.(2021·河南南阳一中检测)如图所示装置中,可观察到电流计指针偏转,M棒变粗,N
棒变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
选项 M N P
A 锌 铜 稀硫酸
B 铜 锌 稀盐酸
C 锌 铁 硝酸铁溶液
D 银 锌 硝酸银溶液
D [据“电流计指针偏转,M棒变粗,N棒变细”判断,M棒作正极,N棒作负极,且金
属的活泼性:N>M,电解质溶液应为不活泼金属盐溶液,只有D项符合题意。]
9.(2020·全国卷Ⅰ,27题节选)为验证不同化合价铁的氧化还原能力,利用下列电池装置
进行实验。
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生
化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择________作为电
解质。
u∞×108/ u∞×108/
阳离子 阴离子
(m2·s-1·V-1) (m2·s-1·V-1)
Li+ 4.07 HCO 4.61
Na+ 5.19 NO 7.40
Ca2+ 6.59 Cl- 7.91
K+ 7.62 SO 8.27
(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________电极溶
液中。
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未
见Fe析出。可知,石墨电极溶液中c(Fe2+)=________________。
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为________________________,铁
电极的电极反应式为________________________。因此,验证了Fe2+氧化性小于__________,还原性小于________。
解析 (1)盐桥中阴、阳离子不与溶液中的物质发生化学反应,两烧杯溶液中含有Fe2+、
Fe3+和SO,Ca2+与SO生成微溶于水的CaSO,Fe2+、Fe3+均与HCO反应,酸性条件下NO与
4
Fe2+发生反应,故盐桥中不能含有Ca2+、HCO和NO。盐桥中阴、阳离子的电迁移率(u∞)应尽
可能相近,根据表中数据可知K+与Cl-的电迁移率较接近且与两端电解质溶液均不发生反
应,故盐桥中应选择KCl为电解质。(2)电子由铁电极经外电路流向石墨电极,则石墨电极为
正极,发生还原反应,为达到电荷平衡,盐桥中的K+进入石墨电极附近的溶液中。(3)铁电极
上发生氧化反应Fe-2e-===Fe2+,石墨电极上未见Fe析出,说明仅发生还原反应2Fe3++2e
-===2Fe2+,铁电极附近溶液中Fe2+的物质的量浓度增加0.02 mol·L-1,则石墨电极溶液中
Fe2+的物质的量浓度增加0.04 mol·L-1,因此石墨电极溶液中最终得到Fe2+的物质的量浓度
为0.05 mol·L-1+0.04 mol·L-1=0.09 mol·L-1。(4)根据(2)、(3)的实验结果易知石墨电极的电
极反应式为Fe3++e-===Fe2+,证明Fe2+的氧化性小于Fe3+;铁电极的电极反应式为Fe-2e
-===Fe2+,证明Fe2+的还原性小于Fe。
答案 (1)KCl (2)石墨 (3)0.09 mol·L-1
(4)Fe3++e-===Fe2+ Fe-2e-===Fe2+ Fe3+ Fe