文档内容
热点强化 9 重要含氯化合物制备探究
许多含氯化合物的制备都涉及氯气实验室制法,除考虑氯气的净化、尾气处理外,还应考虑
所制取物质的特殊性质(一般题干信息中提供)。如在制取易水解的氯化物时要特别注意,排
尽装置中空气,前挡后堵防水解;制取二氧化氯、次氯酸盐、亚氯酸盐时要注意控制温度等。
题组一 易水解无水氯化物的制备
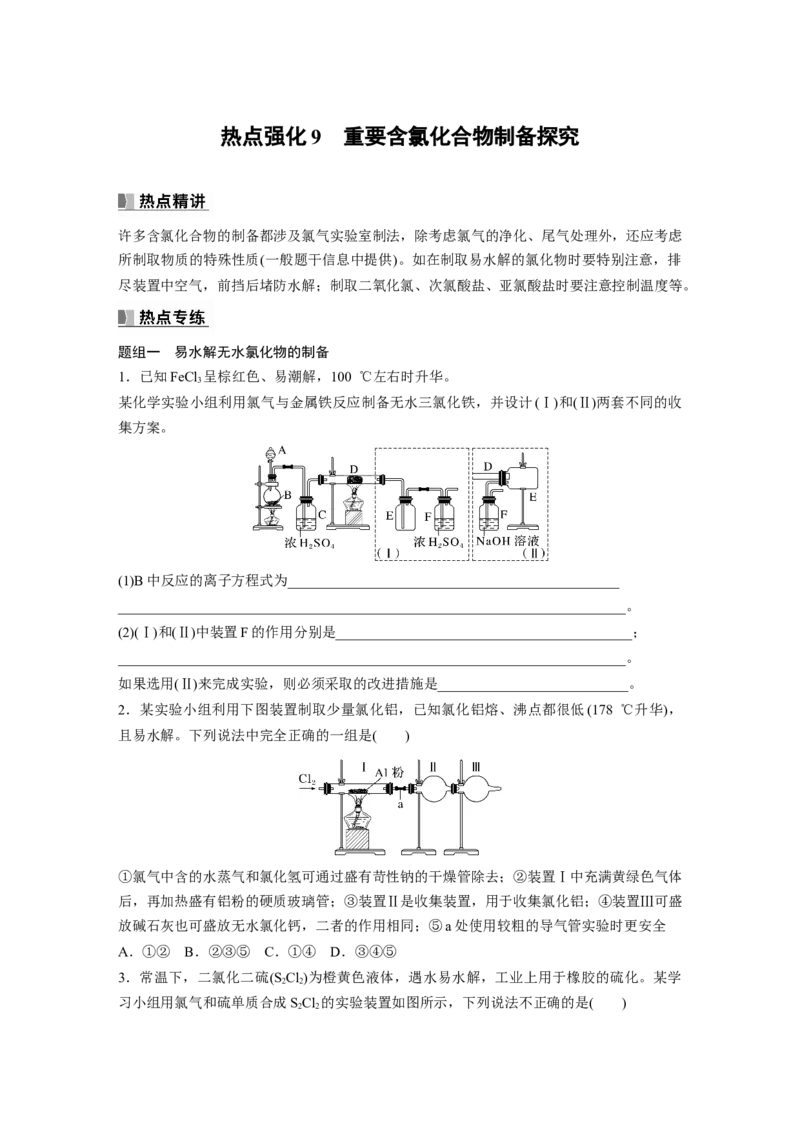
1.已知FeCl 呈棕红色、易潮解,100 ℃左右时升华。
3
某化学实验小组利用氯气与金属铁反应制备无水三氯化铁,并设计(Ⅰ)和(Ⅱ)两套不同的收
集方案。
(1)B中反应的离子方程式为_______________________________________________
________________________________________________________________________。
(2)(Ⅰ)和(Ⅱ)中装置F的作用分别是__________________________________________;
________________________________________________________________________。
如果选用(Ⅱ)来完成实验,则必须采取的改进措施是___________________________。
2.某实验小组利用下图装置制取少量氯化铝,已知氯化铝熔、沸点都很低(178 ℃升华),
且易水解。下列说法中完全正确的一组是( )
①氯气中含的水蒸气和氯化氢可通过盛有苛性钠的干燥管除去;②装置Ⅰ中充满黄绿色气体
后,再加热盛有铝粉的硬质玻璃管;③装置Ⅱ是收集装置,用于收集氯化铝;④装置Ⅲ可盛
放碱石灰也可盛放无水氯化钙,二者的作用相同;⑤a处使用较粗的导气管实验时更安全
A.①② B.②③⑤ C.①④ D.③④⑤
3.常温下,二氯化二硫(S Cl)为橙黄色液体,遇水易水解,工业上用于橡胶的硫化。某学
2 2
习小组用氯气和硫单质合成SCl 的实验装置如图所示,下列说法不正确的是( )
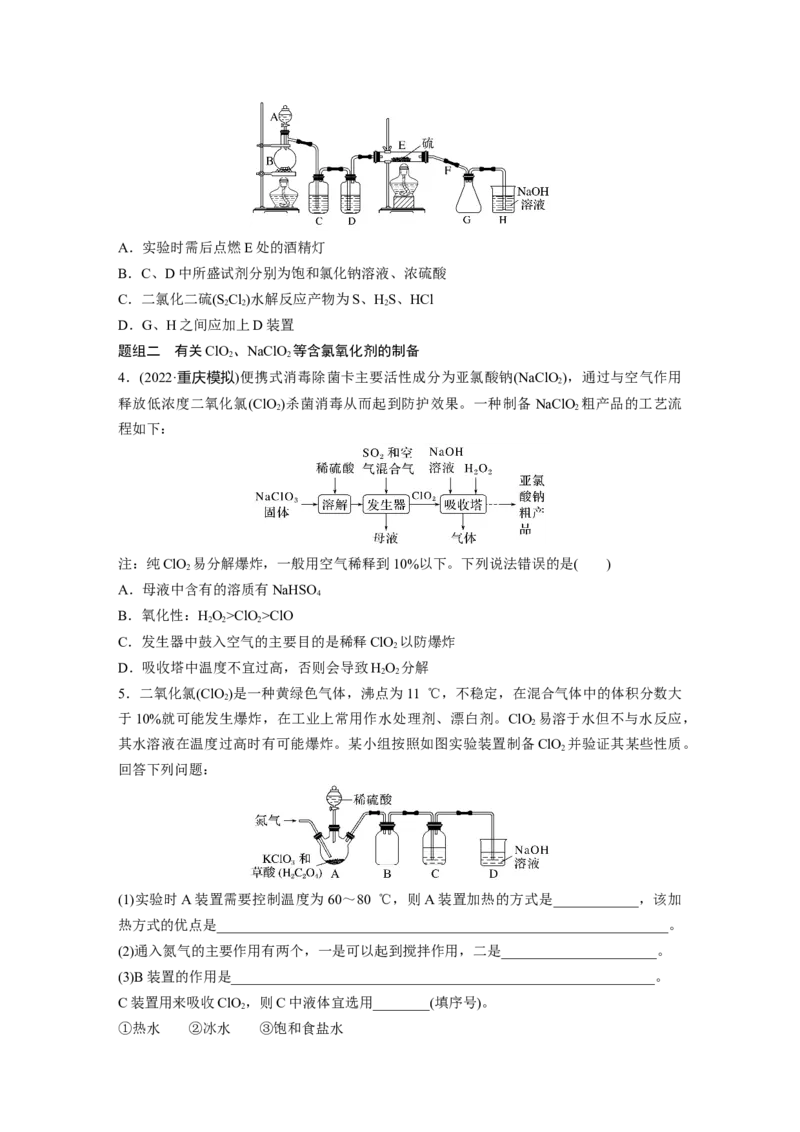
2 2A.实验时需后点燃E处的酒精灯
B.C、D中所盛试剂分别为饱和氯化钠溶液、浓硫酸
C.二氯化二硫(S Cl)水解反应产物为S、HS、HCl
2 2 2
D.G、H之间应加上D装置
题组二 有关ClO 、NaClO 等含氯氧化剂的制备
2 2
4.(2022·重庆模拟)便携式消毒除菌卡主要活性成分为亚氯酸钠(NaClO),通过与空气作用
2
释放低浓度二氧化氯(ClO )杀菌消毒从而起到防护效果。一种制备 NaClO 粗产品的工艺流
2 2
程如下:
注:纯ClO 易分解爆炸,一般用空气稀释到10%以下。下列说法错误的是( )
2
A.母液中含有的溶质有NaHSO
4
B.氧化性:HO>ClO >ClO
2 2 2
C.发生器中鼓入空气的主要目的是稀释ClO 以防爆炸
2
D.吸收塔中温度不宜过高,否则会导致HO 分解
2 2
5.二氧化氯(ClO )是一种黄绿色气体,沸点为11 ℃,不稳定,在混合气体中的体积分数大
2
于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。ClO 易溶于水但不与水反应,
2
其水溶液在温度过高时有可能爆炸。某小组按照如图实验装置制备ClO 并验证其某些性质。
2
回答下列问题:
(1)实验时A装置需要控制温度为60~80 ℃,则A装置加热的方式是____________,该加
热方式的优点是________________________________________________________________。
(2)通入氮气的主要作用有两个,一是可以起到搅拌作用,二是______________________。
(3)B装置的作用是____________________________________________________________。
C装置用来吸收ClO ,则C中液体宜选用________(填序号)。
2
①热水 ②冰水 ③饱和食盐水(4)D装置中ClO 与NaOH溶液反应可生成等物质的量的两种钠盐,其中一种为NaClO ,D
2 2
装置中生成这两种钠盐的化学方程式为___________________________________________
____________________________________________________________________________。
饱和NaClO 溶液在温度低于38 ℃时析出晶体NaClO·3H O,在温度高于38 ℃时析出晶体
2 2 2
NaClO 。请补充从 NaClO 溶液中制得 NaClO 晶体的操作步骤:a.______________;
2 2 2
b.____________;c.洗涤;d.干燥。
(5)设计一个简易实验证明二氧化氯具有永久的漂白性:__________________________
________________________________________________________________________。
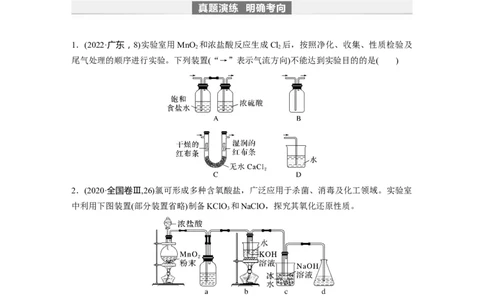
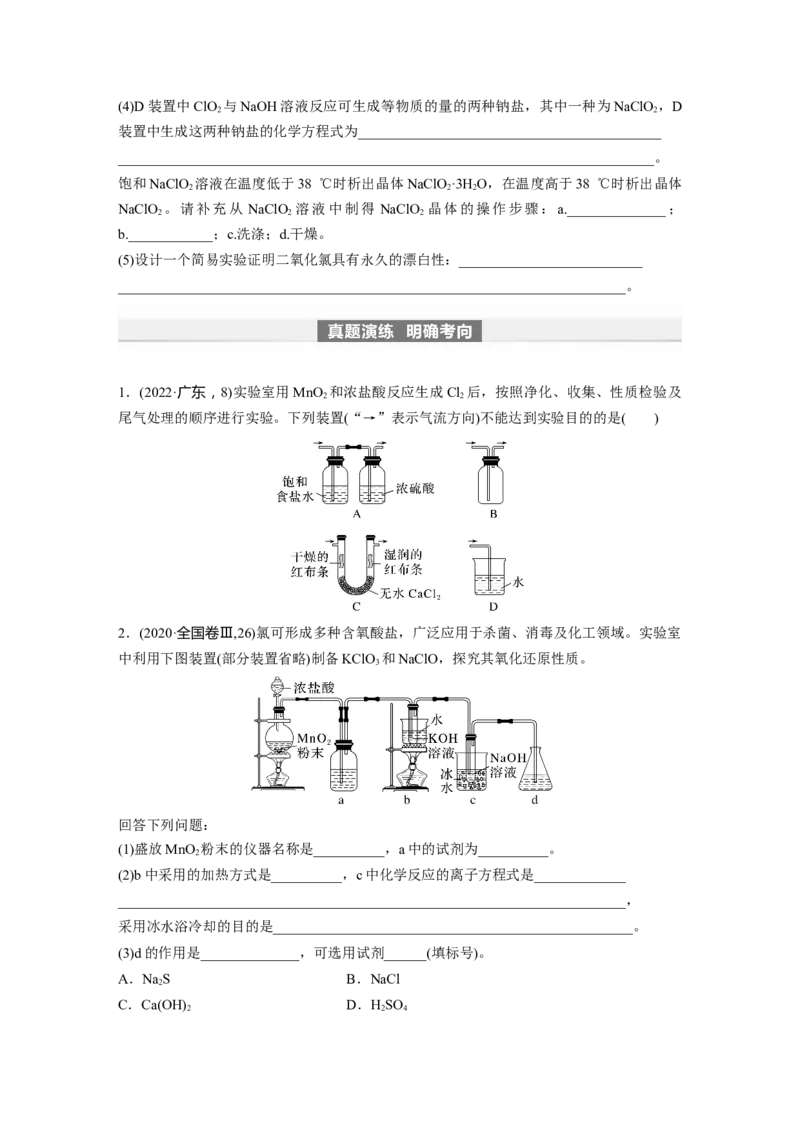
1.(2022·广东,8)实验室用MnO 和浓盐酸反应生成Cl 后,按照净化、收集、性质检验及
2 2
尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
2.(2020·全国卷Ⅲ,26)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室
中利用下图装置(部分装置省略)制备KClO 和NaClO,探究其氧化还原性质。
3
回答下列问题:
(1)盛放MnO 粉末的仪器名称是__________,a中的试剂为__________。
2
(2)b中采用的加热方式是__________,c中化学反应的离子方程式是_____________
________________________________________________________________________,
采用冰水浴冷却的目的是___________________________________________________。
(3)d的作用是______________,可选用试剂______(填标号)。
A.NaS B.NaCl
2
C.Ca(OH) D.HSO
2 2 4(4)反应结束后,取出b中试管,经冷却结晶,________,__________________,干燥,得
到KClO 晶体。
3
(5)取少量KClO 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶
3
液颜色不变。2号试管溶液变为棕色,加入CCl 振荡,静置后CCl 层显________色。可知
4 4
该条件下KClO 的氧化能力________NaClO(填“大于”或“小于”)。
3