文档内容
第 59 讲 无机化工流程题的解题策略
[复习目标] 1.培养从试题提供的新信息中准确地提取实质性内容,并与已有知识块整合重
组为新知识块的能力。2.培养将实际问题分解,通过运用相关知识,采用分析、综合的方法,
解决简单化学问题的能力。3.培养将分析和解决问题的过程及成果用正确的化学术语及文字、
图表、模型、图形等表达并做出解释的能力。
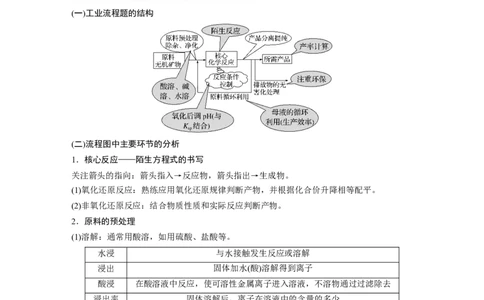
(一)工业流程题的结构
(二)流程图中主要环节的分析
1.核心反应——陌生方程式的书写
关注箭头的指向:箭头指入→反应物,箭头指出→生成物。
(1)氧化还原反应:熟练应用氧化还原规律判断产物,并根据化合价升降相等配平。
(2)非氧化还原反应:结合物质性质和实际反应判断产物。
2.原料的预处理
(1)溶解:通常用酸溶,如用硫酸、盐酸等。
水浸 与水接触发生反应或溶解
浸出 固体加水(酸)溶解得到离子
酸浸 在酸溶液中反应,使可溶性金属离子进入溶液,不溶物通过过滤除去
浸出率 固体溶解后,离子在溶液中的含量的多少
(2)灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质在高温下氧化、分解。
(3)审题时要“瞻前顾后”,注意物质性质及反应原理的前后联系。
3.常用的控制反应条件的方法
(1)调节溶液的pH。常用于使某些金属离子形成氢氧化物沉淀。调节 pH所需的物质一般应
满足两点:
①能与H+反应,使溶液pH增大;
②不引入新杂质。例如:若要除去Cu2+中混有的Fe3+,可加入CuO、CuCO 、Cu(OH) 、Cu (OH) CO 等物质
3 2 2 2 3
来调节溶液的pH,不可加入NaOH溶液、氨水等。
(2)控制温度。根据需要升温或降温,改变反应速率或使平衡向需要的方向移动。
(3)趁热过滤。防止某些物质降温时析出。
(4)冰水洗涤。洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗。
4.常用的分离方法
(1)过滤:分离难溶物和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法。
(2)萃取和分液:利用溶质在互不相溶的溶剂里的溶解度不同提取分离物质,如用 CCl 或苯
4
萃取溴水中的溴。
(3)蒸发结晶:提取溶解度随温度变化不大的溶质,如从溶液中提取NaCl。
(4)冷却结晶:提取溶解度随温度变化较大的溶质、易水解的溶质或结晶水合物,如KNO 、
3
FeCl 、CuCl 、CuSO ·5H O、FeSO ·7H O等。
3 2 4 2 4 2
(5)蒸馏或分馏:分离沸点不同且互溶的液体混合物,如分离乙醇和甘油。
(6)冷却法:利用气体液化的特点分离气体,如合成氨工业采用冷却法分离平衡混合气体中
的氨气。
一、条件控制与K 的计算
sp
1.(温度控制)辉铜矿石主要含有硫化亚铜(Cu S)及少量脉石(SiO)。一种以辉铜矿石为原料
2 2
制备硝酸铜的工艺流程如图所示:
(1)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是_______。
(2)“保温除铁”过程中,加入CuO的目的是_________________________________
________________________________________________________________________;
“蒸发浓缩、冷却结晶”过程中,要用HNO 溶液调节溶液的pH,其理由是______
3
________________________________________________________________________。
2.(酸碱度控制——调pH)利用某钴矿石(主要成分为Co O)制取Co(OH) 粗品及其他工业产
2 3 2
品的工艺流程如图1所示。已知:浸出液中含有的阳离子主要有H+、Cu2+、Co2+、Fe2+、Mg2+。
回答下列问题:
(1)钴矿石浸出时加入NaSO 的目的为________________________________。
2 3
(2)溶液中lg c(X)(X表示Fe3+、Cu2+、Fe2+、Co2+、Mg2+、Ca2+)与pH的变化关系如图2所
示(离子浓度小于10-5 mol·L-1时可认为已除尽),在萃取余液中通入空气的目的是
________________________________________________________________________,
用熟石灰调pH至3.2,过滤1所得滤渣的主要成分为________,萃取和反萃取的目的是
________________________________________________________________________。
(3)用氧化镁调滤液 1 的 pH 为 9.1 时,得到的氢氧化钴粗品中含有的主要杂质为
____________,多次洗涤可提高粗产品中钴含量。“过滤2”后所得滤液直接排放会造成水
体污染,须进行处理,用熟石灰调节 pH使c(Mg2+)≤10-5 mol·L-1,则K [Mg(OH) ]=
sp 2
________。
3.(调pH与K 计算)某废钒渣(主要成分为VO ,含有少量Al O 、CaO)为原料生产VO 的
sp 2 3 2 3 2 5
工艺流程如图:
已知:钒酸(H VO )是强酸,NH VO 难溶于水;+5价钒在溶液中的主要存在形式与溶液
3 4 4 3
pH的关系如表:
pH 4~6 6~8 8~10 10~12
主要离子 VO VO VO VO
2
(1)向钒渣中加入生石灰焙烧,将VO 转化为Ca(VO ) 的化学方程式为__________
2 3 3 2________________________________________________________________________。
(2)已知Ca(VO ) 难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO ) 溶于盐
3 2 3 2
酸的离子方程式为________________________________________________________。
(3)已知加入石灰乳后生成Ca (VO ) 沉淀,则加入石灰乳的作用是_______________
3 4 2
________________________________________________________________________。
(4)反应Ca (VO )(s)+3CO(aq)2VO(aq)+3CaCO (s)的平衡常数为______________(用含
3 4 2 3
m、n的代数式表示),已知:K (CaCO)=m,K [Ca (VO )]=n。
sp 3 sp 3 4 2
(5)沉钒2过程中加入氯化铵溶液,控制溶液的pH=7.5,当pH>8时,NH VO 的产量明显降
4 3
低,原因是____________________________________________________。
二、化工流程分析滤液、滤渣成分的确定
4.(2022·湖南岳阳模拟)锰常用于制造合金锰钢。某化工厂以软锰矿(主要成分是MnO ,含
2
有SiO、Fe O、CaO等少量杂质)为主要原料制取金属锰的工艺流程如图1所示。
2 2 3
(1)“浸锰”步骤中往往有副产物MnS O 生成,温度对“浸锰”反应的影响如图2所示。为
2 6
减少 MnS O 的生成,“浸锰”的适宜温度是________,“滤渣 Ⅰ”的成分是
2 6
____________(填化学式)。该步骤中可以再加入MnSO 以促进“滤渣 Ⅰ”析出,结合平衡
4
移动原理分析其原因:____________________________________________________
________________________________________________________________________。
(2)“滤液 Ⅰ”中需要先加入MnO 充分反应后再调pH,写出加入MnO 时发生反应的离子
2 2
方程式:________________________________________________________________。
(3)“滤液Ⅱ”中加入MnF 的目的是除去溶液中的Ca2+,已知25 ℃时,K (CaF )=3.2×
2 sp 2
10-11,则常温下CaF 在纯水中的溶解度为________g。
2
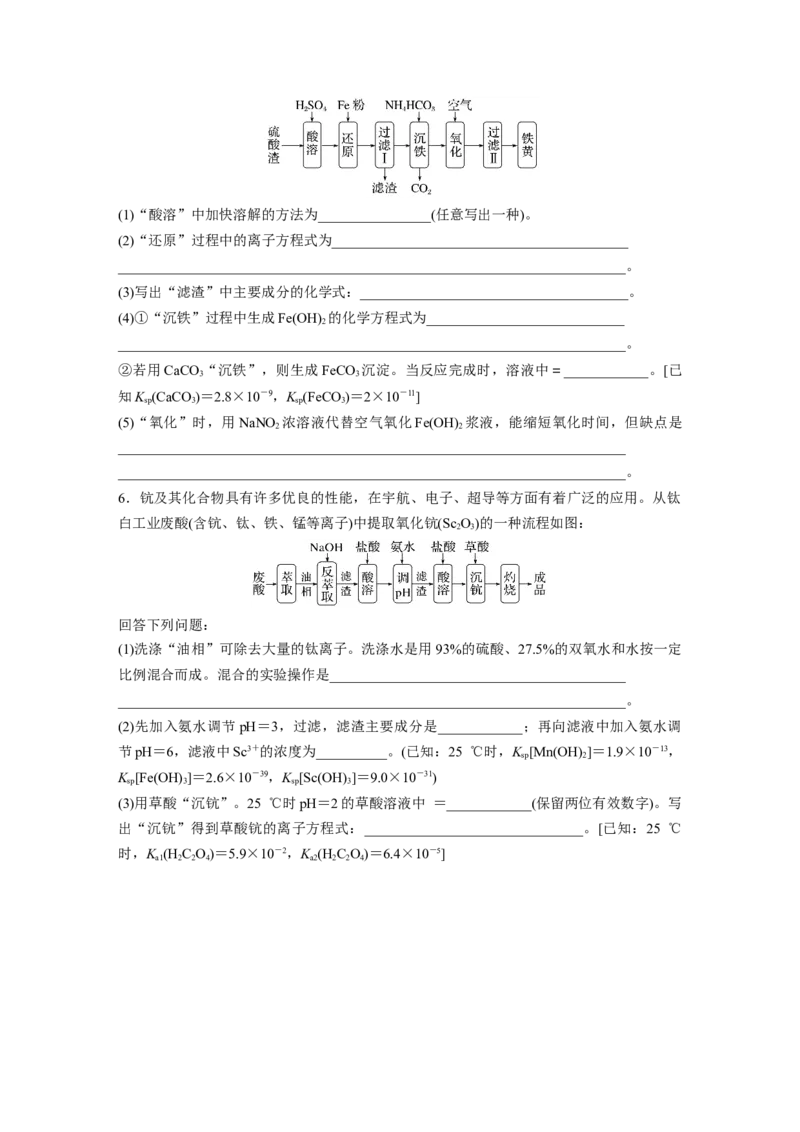
5.以硫酸渣(含Fe O、SiO 等)为原料制备铁黄(FeOOH)的一种工艺流程如图:
2 3 2(1)“酸溶”中加快溶解的方法为________________(任意写出一种)。
(2)“还原”过程中的离子方程式为__________________________________________
________________________________________________________________________。
(3)写出“滤渣”中主要成分的化学式:______________________________________。
(4)①“沉铁”过程中生成Fe(OH) 的化学方程式为____________________________
2
________________________________________________________________________。
②若用CaCO “沉铁”,则生成FeCO 沉淀。当反应完成时,溶液中=____________。[已
3 3
知K (CaCO)=2.8×10-9,K (FeCO)=2×10-11]
sp 3 sp 3
(5)“氧化”时,用NaNO 浓溶液代替空气氧化Fe(OH) 浆液,能缩短氧化时间,但缺点是
2 2
________________________________________________________________________
________________________________________________________________________。
6.钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛
白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc O)的一种流程如图:
2 3
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定
比例混合而成。混合的实验操作是__________________________________________
________________________________________________________________________。
(2)先加入氨水调节pH=3,过滤,滤渣主要成分是____________;再向滤液中加入氨水调
节pH=6,滤液中Sc3+的浓度为__________。(已知:25 ℃时,K [Mn(OH) ]=1.9×10-13,
sp 2
K [Fe(OH) ]=2.6×10-39,K [Sc(OH) ]=9.0×10-31)
sp 3 sp 3
(3)用草酸“沉钪”。25 ℃时pH=2的草酸溶液中 =____________(保留两位有效数字)。写
出“沉钪”得到草酸钪的离子方程式:_______________________________。[已知:25 ℃
时,K (H C O)=5.9×10-2,K (H C O)=6.4×10-5]
a1 2 2 4 a2 2 2 4