文档内容
第2讲 水的电离和溶液的酸碱性
【2020·备考】
最新考纲:1.了解水的电离和水的离子积常数。2.了解溶液pH的定义。3.了解测定
溶液pH的方法,能进行pH的简单计算。
核心素养:1.变化观念与平衡思想:认识水的电离有一定限度,是可以调控的。能
多角度、动态地分析水的电离,运用平衡移动原理解决实际问题。2.科学探究与创
新意识:能发现和提出酸碱中和滴定中有探究价值的问题;能从问题和假设出发,
确定探究目的,设计探究方案,进行实验探究;在探究中学会合作,面对“异常”
现象敢于提出自己的见解,进行误差分析。
考点一 水的电离
(频数:★★☆ 难度:★★☆)
INCLUDEPICTURE "名师课堂.tif" \* MERGEFORMAT INCLUDEPICTURE
" 名 师 课 堂 .tif" \* MERGEFORMAT
INCLUDEPICTURE " 书名号 .TIF " \* MERGEFORMAT INCLUDEPICTURE
" 书名号 .TIF" \* MERGEFORMAT 名师课堂导语 水的电离主要结合盐类的水
解反应进行考查,主要角度有:(1)水的电离影响因素;(2)水的离子积常数的理解
与应用。
1.水的电离
水是极弱的电解质,水的电离方程式为H O + H O INCLUDEPICTURE "KN.TIF"
2 2
\* MERGEFORMAT H O + + OH - 或H O INCLUDEPICTURE "KN.TIF" \*
3 2
MERGEFORMAT H + + OH - 。
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMATINCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
任何情况下水电离产生的c(H+)、c(OH-)总是相等的。
2.水的离子积常数
INCLUDEPICTURE "P810.TIF" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
水的离子积常数K =c(H+)·c(OH-),其实质是水溶液中的H+和OH-浓度的乘积,
w
不一定是水电离出的H+和OH-浓度的乘积,所以与其说K 是水的离子积常数,
w
不如说是水溶液中的H+和OH-的离子积常数。即K 不仅适用于水,还适用于酸
w
性或碱性的稀溶液。
3.影响水电离平衡的因素
(1)升高温度,水的电离程度增大,K 增大。
w
(2)加入酸或碱,水的电离程度减小,K 不变。
w
(3)加入可水解的盐(如FeCl 、Na CO ),水的电离程度增大,K 不变。
3 2 3 w
4.填写外界条件对水电离平衡的具体影响
体系变化 平衡移 水的电
K c(OH-) c(H+)
w
条件 动方向 离程度
HCl 逆 不变 减小 减小 增大
NaOH 逆 不变 减小 增大 减小
可水解 Na CO 正 不变 增大 增大 减小
2 3
的盐 NH Cl 正 不变 增大 减小 增大
4升温 正 增大 增大 增大 增大
温度
降温 逆 减小 减小 减小 减小
其他:如加入Na 正 不变 增大 增大 减小
INCLUDEPICTURE " 名 师 课 堂 实 录 .tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
水属于弱电解质,遵循弱电解质电离平衡原理,水的电离是动态平衡,也遵循勒夏
特列原理。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)在蒸馏水中滴加浓H SO ,K 不变(×)
2 4 w
(2)NaCl溶液和CH COONH 溶液均显中性,两溶液中水的电离程度相同(×)
3 4
(3)室温下,0.1 mol·L-1的HCl溶液与0.1 mol·L-1的NaOH溶液中水的电离程度相
同(√)
(4)25 ℃和60 ℃的水的pH,前者大于后者,但都显中性(√)
(5)室温下,pH值相同的NaOH溶液与CH COONa溶液,水的电离程度后者大(√)
3
2.(教材改编题)25 ℃时,相同物质的量浓度的下列溶液:
①NaCl、②NaOH、③H SO 、④(NH ) SO ,其中水的电离程度按由大到小顺序排
2 4 4 2 4
列的一组是( )
A.④>③>②>① B.②>③>①>④
C.④>①>②>③ D.③>②>①>④
答案 C
3.(思维探究题)甲同学认为,在水中加入H SO ,水的电离平衡向左移动,解释是加
2 4
入H SO 后c(H+)增大,平衡左移。乙同学认为,加入H SO 后,水的电离平衡向右
2 4 2 4
移动,解释为加入H SO 后,c(H+)浓度增大,H+与OH-中和,平衡右移。你认为哪
2 4
种说法正确?并说明原因。水的电离平衡移动后,溶液中c(H+)·c(OH-)是增大还
是减小?答案 甲正确,温度不变,K 是常数,加入H SO ,c(H+)增大,c(H+)·c(OH-)>K ,
w 2 4 w
平衡左移。
c(H+)·c(OH-)不变,因为K 仅与温度有关,温度不变,则K 不变,与外加酸、碱、
w w
盐无关。
INCLUDEPICTURE "题组诊断.tif" \* MERGEFORMAT INCLUDEPICTURE
" 题 组 诊 断 .tif" \* MERGEFORMAT
[A组 基础知识巩固]
1.(2019·泉州模拟)某温度下,向c(H+)=1×10-6 mol·L-1的蒸馏水中加入NaHSO
4
晶体,保持温度不变,测得溶液的c(H+)=1×10-2 mol·L-1。下列对该溶液的叙述
不正确的是( )
A.该温度高于25 ℃
B.由水电离出来的H+的浓度为1×10-10 mol·L-1
C.加入NaHSO 晶体抑制水的电离
4
D.取该溶液加水稀释100倍,溶液中的c(OH-)减小
解析 该温度下蒸馏水中c(H+)=1×10-6 mol·L-1,大于25 ℃时纯水中c(H+),故
温度高于25 ℃,A项正确;此温度下K =1×10-12,故该NaHSO 溶液中
w 4
c(OH-)==1×10-10 (mol·L-1),由水电离出的c(H+)与溶液中的c(OH-)相等,B
项正确;加入NaHSO 后,NaHSO 电离出的H+抑制了水的电离,C项正确;加水
4 4
稀释时,c(H+)减小,而K 不变,故c(OH-)增大,D项错误。
w
答案 D
2.(2018·双鸭山模拟)在25 ℃时,某稀溶液中由水电离产生的 H+浓度为1×10-13
mol·L-1,下列有关该溶液的叙述,正确的是( )
A.该溶液可能呈酸性
B.该溶液一定呈碱性
C.该溶液的pH一定是1
D.该溶液的pH不可能为13
解析 在25 ℃时,某稀溶液中由水电离产生的c(H+)为1×10-13 mol·L-1<1×
10-7 mol·L-1,说明溶液中的溶质抑制水的电离,溶质为酸或碱,溶液可能呈酸性或碱性,A正确,B错误;如果该溶液呈酸性,则溶液的pH=1,如果该溶液呈碱性,
则溶液的pH=13,C、D错误。
答案 A
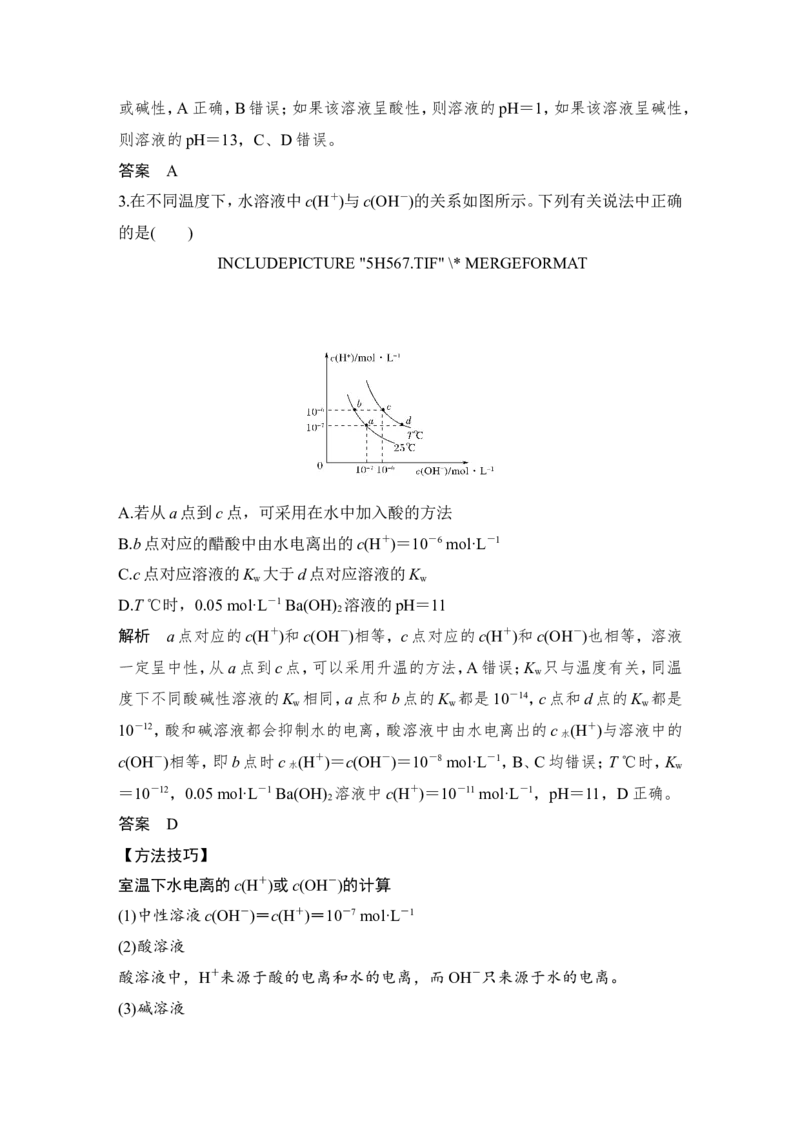
3.在不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示。下列有关说法中正确
的是( )
INCLUDEPICTURE "5H567.TIF" \* MERGEFORMAT
A.若从a点到c点,可采用在水中加入酸的方法
B.b点对应的醋酸中由水电离出的c(H+)=10-6 mol·L-1
C.c点对应溶液的K 大于d点对应溶液的K
w w
D.T ℃时,0.05 mol·L-1 Ba(OH) 溶液的pH=11
2
解析 a点对应的c(H+)和c(OH-)相等,c点对应的c(H+)和c(OH-)也相等,溶液
一定呈中性,从a点到c点,可以采用升温的方法,A错误;K 只与温度有关,同温
w
度下不同酸碱性溶液的K 相同,a点和b点的K 都是10-14,c点和d点的K 都是
w w w
10-12,酸和碱溶液都会抑制水的电离,酸溶液中由水电离出的c (H+)与溶液中的
水
c(OH-)相等,即b点时c (H+)=c(OH-)=10-8 mol·L-1,B、C均错误;T ℃时,K
水 w
=10-12,0.05 mol·L-1 Ba(OH) 溶液中c(H+)=10-11 mol·L-1,pH=11,D正确。
2
答案 D
【方法技巧】
室温下水电离的c(H+)或c(OH-)的计算
(1)中性溶液c(OH-)=c(H+)=10-7 mol·L-1
(2)酸溶液
酸溶液中,H+来源于酸的电离和水的电离,而OH-只来源于水的电离。
(3)碱溶液碱溶液中,OH-来源于碱的电离和水的电离,而H+只来源于水的电离。
(4)盐溶液
水解呈酸性或碱性的盐溶液中,H+和OH-均来源于水的电离。
[B组 考试能力过关]
4.(上海卷)水中加入下列溶液对水的电离平衡不产生影响的是( )
A.NaHSO 溶液 B. KF溶液
4
C. KAl(SO ) 溶液 D.NaI溶液
4 2
解析 NaHSO 在溶液中电离出H+,抑制水的电离;KF在水溶液中电离出的 F-
4
结合水电离出的H+生成弱酸HF而发生水解;KAl(SO ) 在溶液中电离出的Al3+
4 2
与水电离出的OH-结合生成Al(OH) 而发生水解,所以F-和Al3+均促进水的电离
3
HI是强酸,I-不水解,对水的电离平衡不影响。
答案 D
5.(四川卷)25 ℃时等体积的①pH=0的H SO 溶液,②0.05 mol·L-1的Ba(OH) 溶
2 4 2
液,③pH=10的Na S溶液,④pH=5的NH NO 溶液中,发生电离的水的物质的
2 4 3
量之比是( )
A.1∶10∶1010∶109 B.1∶5∶5×109∶5×109
C.1∶20∶1010∶109 D.1∶10∶104∶109
解析 设溶液的体积为1 L。①中pH=0的H SO 中c(H+)=1.0 mol·L-1,c(OH-)
2 4
=1.0×10-14mol·L-1,水电离的物质的量为 1.0×10-14mol;②中 c(OH-)=0.1
mol·L-1,c(H+)=1.0×10-13mol·L-1,水电离的物质的量为1.0×10-13mol;③中
c(OH-)=1.0×10-4mol·L-1,水电离的物质的量为1.0×10-4mol;④中c(H+)=
1.0×10-5mol·L-1,水电离的物质的量为1.0×10-5mol。故①②③④中水电离的物
质的量之比为 1.0×10-14mol∶1.0×10-13mol∶1.0×10-4mol∶1.0×10-5mol=
1∶10∶1010∶109,A项正确。
答案 A
6.(广东卷)一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确
的是( )INCLUDEPICTURE "ZYF23.tif" \* MERGEFORMAT
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
解析 A项,升高温度,促进水的电离平衡,则c(H+)和c(OH-)都同等程度地变大,
若由c向b变化,则c(H+)增大,c(OH-)将变小,错误;B项,根据b点对应的c(H+)
和c(OH-)都为1.0×10-7 mol·L-1,所以该温度下,水的离子积常数K =1.0×10-
w
7×1.0×10-7=1.0×10-14,错误;C项,加入FeCl 发生水解反应:Fe3++3H O
3 2
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Fe(OH) +3H+,破坏
3
水的电离平衡,c(H+)增大、K 不变,c(OH-)变小,则可能引起由b向a变化,正确;
w
D项,c点对应的溶液呈碱性,稀释溶液,c(OH-)变小,K 不变,c(H+)增大,故可引
w
起由c向b的变化,而不是向d变化,错误。
答案 C
考点二 溶液的酸碱性和pH
(频数:★☆☆ 难度:★★☆)
INCLUDEPICTURE "名师课堂.tif" \* MERGEFORMAT INCLUDEPICTURE
" 名 师 课 堂 .tif" \* MERGEFORMAT
INCLUDEPICTURE " 书名号 .TIF " \* MERGEFORMAT INCLUDEPICTURE
" 书名号 .TIF" \* MERGEFORMAT 名师课堂导语 本考点主要考查溶液酸碱性
的判断,溶液pH的求算,以及pH的使用, pH的求算是难点,复习时加以关注。
1.溶液的酸碱性常温下,溶液的酸碱性与c(H+)、c(OH-)的关系:
溶液的酸碱性 c(H+)与c(OH-)比较 c(H+)大小
酸性溶液 c(H+)>c(OH-) c(H+)>1×10-7mol·L-1
中性溶液 c(H+)=c(OH-) c(H+)=1×10-7mol·L-1
碱性溶液 c(H+)<c(OH-) c(H+)<1×10-7mol·L-1
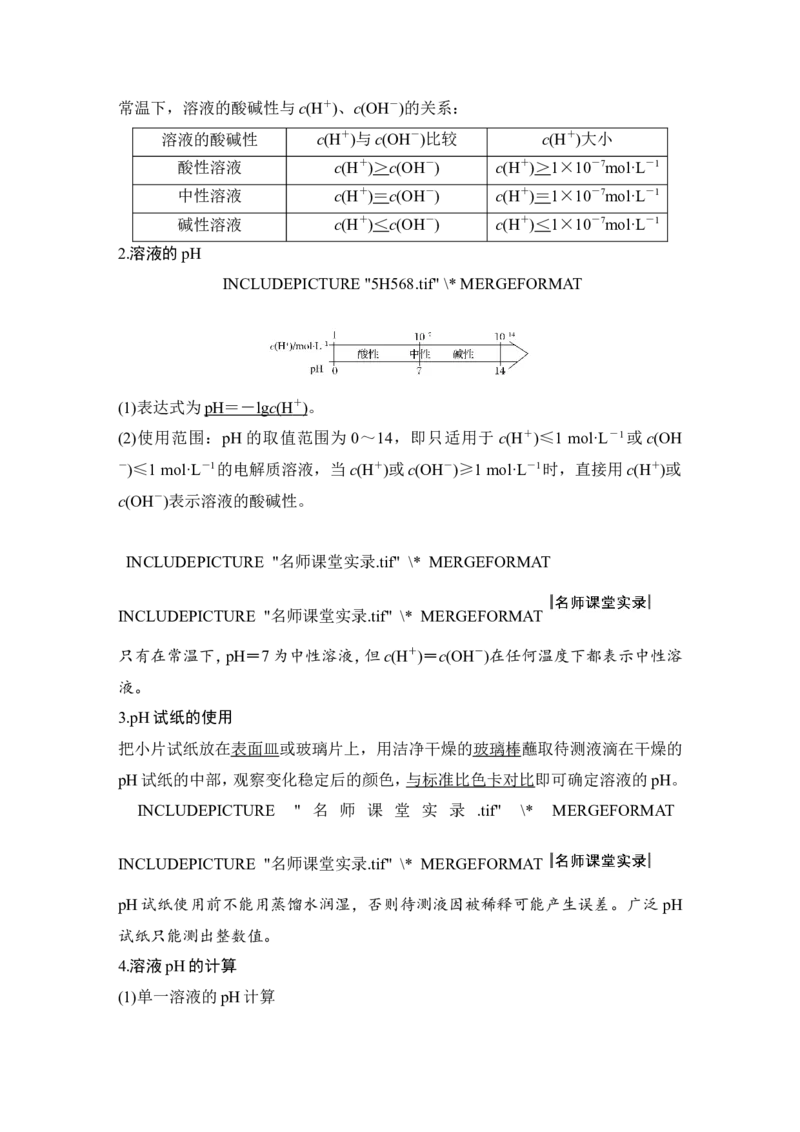
2.溶液的pH
INCLUDEPICTURE "5H568.tif" \* MERGEFORMAT
(1)表达式为 pH =- lg c (H + ) 。
(2)使用范围:pH的取值范围为 0~14,即只适用于 c(H+)≤1 mol·L-1或c(OH
-)≤1 mol·L-1的电解质溶液,当c(H+)或c(OH-)≥1 mol·L-1时,直接用c(H+)或
c(OH-)表示溶液的酸碱性。
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
只有在常温下,pH=7为中性溶液,但c(H+)=c(OH-)在任何温度下都表示中性溶
液。
3.pH试纸的使用
把小片试纸放在表面皿或玻璃片上,用洁净干燥的玻璃棒蘸取待测液滴在干燥的
pH试纸的中部,观察变化稳定后的颜色,与标准比色卡对比即可确定溶液的pH。
INCLUDEPICTURE " 名 师 课 堂 实 录 .tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
pH试纸使用前不能用蒸馏水润湿,否则待测液因被稀释可能产生误差。广泛 pH
试纸只能测出整数值。
4.溶液pH的计算
(1)单一溶液的pH计算强酸溶液:如H A,设浓度为c mol·L-1,c(H+)=nc mol·L-1,pH=-lgc(H+)=-
n
lg(nc)。
强碱溶液(25 ℃):如B(OH) ,设浓度为c mol·L-1,c(H+)= mol·L-1,pH=-lgc(H
n
+)=14+lg(nc)。
(2)混合溶液pH的计算类型
①两种强酸混合:直接求出c(H+) ,再据此求pH。c(H+) =。
混 混
②两种强碱混合:先求出c(OH-) ,再据K 求出c(H+) ,最后求pH。
混 w 混
c(OH-) =。
混
③强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,
最后求pH。
c(H+) 或c(OH-) =。
混 混
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)任何温度下,利用c(H+)和c(OH-)的相对大小均可判断溶液的酸碱性(√)
(2)某溶液的c(H+)>10-7mol·L-1,则该溶液呈酸性(×)
(3)用蒸馏水润湿的pH试纸测溶液的pH,一定会使结果偏低(×)
(4)一定温度下,pH=a的氨水,稀释10倍后,其pH=b,则a=b+1(×)
(5)常温常压时,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合后,滴入石
蕊溶液呈红色(√)
2.(教材改编题)甲溶液的pH是2,乙溶液的pH是5,甲溶液与乙溶液的c(H+)之比
为( )
A.1 000∶1 B.1∶1 000
C.2∶5 D.5∶2
答案 A
3.(思维探究题)用pH试纸测溶液的pH时如果湿润是否一定产生误差?能否可用
pH试纸测定氯水的pH?
答案 pH试纸使用前用蒸馏水润湿,相当于对原溶液稀释而产生误差,但中性溶
液的pH不变。不能用pH试纸测定氯水的pH,因为氯水既呈酸性又呈现强氧化性
(漂白性)。
INCLUDEPICTURE "题组诊断.tif" \* MERGEFORMAT INCLUDEPICTURE" 题 组 诊 断 .tif" \* MERGEFORMAT
[A组 基础知识巩固]
1.下列说法中正确的是( )
A.25 ℃时NH Cl溶液的K 大于100 ℃时NaCl的K
4 w w
B.常温下,pH均为5的醋酸和硫酸铝两种溶液中,由水电离出的氢离子浓度之比
为1∶104
C.根据溶液的pH与酸碱性的关系,推出pH=6.8的溶液一定显酸性
D.100 ℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性
解析 水的离子积常数只与温度有关,温度越高,K 越大,A错;醋酸中水电离出
w
的c(H+)=溶液中的c(OH-)=10-9mol·L-1,硫酸铝溶液中水电离出的 c(H+)等于
溶液中的c(H+)=10-5mol·L-1,B正确;C选项不知温度,无法判断,错误;100 ℃
时K =1×10-12,所以将pH=2的盐酸与pH=12的NaOH溶液等体积混合后,溶
w
液显碱性,D错。
答案 B
2.(2018·福建质检)常温下,溶液的pH最大的是( )
A.0.02 mol·L-1氨水与水等体积混合后的溶液
B.pH=2的盐酸与pH=12的NaOH溶液等体积混合后的溶液
C.0.02 mol·L-1盐酸与0.02 mol·L-1氨水等体积混合后的溶液
D.0.01 mol·L-1盐酸与0.03 mol·L-1氨水等体积混合后的溶液
解析 A 项混合后得到 0.01 mol·L-1氨水,NH ·H O 不能完全电离,则 c(OH
3 2
-)<0.01 mol·L-1,78.0蓝色
甲基橙 <3.1红色 3.1~4.4橙色 >4.4黄色
酚酞 <8.2无色 8.2~10.0浅红色 >10.0红色
INCLUDEPICTURE " 名 师 课 堂 实 录 .tif" \* MERGEFORMATINCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
①酸性、氧化性的试剂一般用酸式滴定管,因为酸性和氧化性物质易腐蚀橡胶管;
碱性的试剂一般用碱式滴定管,因为碱性物质易腐蚀玻璃,致使活塞无法打开。
②由于滴定管的“0”刻度在滴定管的上方;滴定管下端是没有刻度的,容量为25
mL的滴定管,滴定过程中用去10.00 mL的液体,故滴定管中剩余液体体积大于
15 mL。
5.中和滴定实验操作(以酚酞作指示剂,用盐酸滴定氢氧化钠溶液)。
(1)滴定前的准备。
INCLUDEPICTURE "5H572.tif" \* MERGEFORMAT
(2)滴定。
INCLUDEPICTURE "5H573.tif" \* MERGEFORMAT
(3)终点判断:等到滴入最后一滴反应液,指示剂变色,且在半分钟内不能恢复原来
的颜色,视为滴定终点,并记录标准液的体积。
(4)数据处理:按上述操作重复2~3次,求出用去标准盐酸体积的平均值,根据原理计算。
c(NaOH)=
6.酸碱中和滴定中常见误差分析
以标准酸溶液滴定未知浓度的碱(酚酞作指示剂)为例,常见的因操作不正确而引
起的误差有:
V(标
步骤 操作 c(待测)
准)
酸式滴定管未用标准溶液润洗 变大 偏高
碱式滴定管未用待测溶液润洗 ①变小 ②偏低
洗涤
锥形瓶用待测溶液润洗 ③变大 ④偏高
锥形瓶洗净后还留有蒸馏水 ⑤不变 ⑥无影响
放出碱液的滴定管开始有气泡,放出液体后气泡
取液 ⑦变小 ⑧偏低
消失
酸式滴定管滴定前有气泡,滴定终点时气泡消失 ⑨变大 ⑩偏高
振荡锥形瓶时部分液体溅出 ⑪变小 ⑫偏低
滴定
部分酸液滴出锥形瓶外 ⑬变大 ⑭偏高
溶液颜色较浅时滴入酸液过快,停止滴定后反加
⑮变大 ⑯偏高
一滴NaOH溶液无变化
酸式滴定管滴定前读数正确,滴定后俯视读数(或
⑰变小 ⑱偏低
前仰后俯)
读数
酸式滴定管滴定前读数正确,滴定后仰视读数(或
⑲变大 ⑳偏高
前俯后仰)
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
错误操作产生误差的结论不用死记硬背,可依据c(待测)=推断完成,因为c(标准)
与V(待测)已确定,所以只要分析出不正确操作引起V(标准)的变化,即分析出结
果。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)pH计不能用于酸碱中和滴定终点的判断(×)
(2)中和滴定实验时,用待测液润洗锥形瓶(×)
(3)滴定终点就是酸碱恰好中和的点(×)(4)滴定管盛标准液时,其液面一定要调在0刻度(×)
(5)用碱式滴定管量取20.00 mL KMnO 溶液(×)
4
2.(教材改编题)(RJ选修4·P 4 改编)用标准盐酸滴定未知浓度的NaOH溶液,下
52
列各操作中会引起实验误差的是( )
A.滴定前酸式滴定管需用标准盐酸润洗
B.用蒸馏水洗净锥形瓶后,立即装入一定体积的NaOH溶液后进行滴定
C.往盛有20.00 mL NaOH溶液的锥形瓶中,滴入几滴酚酞指示剂后进行滴定
D.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,然后装入一定体积的NaOH溶
液
解析 锥形瓶内存有少量蒸馏水,但待测液的物质的量不变,消耗标准液的体积
不变,B不会引起误差;锥形瓶不能用待测液润洗,否则会使测定结果偏高。
答案 D
3.(规范表述专练)(1)酸式滴定管怎样查漏?
______________________________________________________________________
______________________________________________________________________
_____________________________________________________________________
。
(2)写出下列反应过程的指示剂达到终点时颜色改变
①用标准酸性KMnO 溶液滴定Na SO 溶液以测量其浓度,指示剂:KMnO ,终点
4 2 3 4
现象:______________________________________________________________。
②利用“Ag++SCN-===AgSCN↓”原理,可用标准KSCN溶液测量AgNO 溶
3
液 浓 度 , 指 示 剂 : Fe(NO ) , 终 点 现 象 :
3 3
________________________________________。
③利用OH-+H+===H O来测量某盐酸的浓度时,指示剂:酚酞,终点现象:
2
____________________________________________________________________。
答案 (1)将旋塞关闭,向滴定管里注入一定量的水,把它固定在滴定管夹上,放置
10分钟,观察滴定管口及旋塞两端是否有水渗出,旋塞不渗水才可使用
(2)①溶液出现浅红色且半分钟不恢复原色 ②溶液变为红色且半分钟不恢复原
色 ③溶液出现浅红色且半分钟不恢复原色
INCLUDEPICTURE "题组诊断.tif" \* MERGEFORMAT INCLUDEPICTURE" 题 组 诊 断 .tif" \* MERGEFORMAT
[A组 基础知识巩固]
1.某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的 NaOH溶液时,
选择甲基橙作指示剂。下列操作中可能使所测NaOH溶液的浓度数值偏低的是(
)
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
解析 滴定管未用标准盐酸润洗,内壁附着一层水,可将加入的盐酸稀释,消耗相
同量的碱,所需盐酸的体积偏大,结果偏高;用碱式滴定管取出的待测NaOH溶液
的物质的量一旦确定,倒入锥形瓶后,水的加入不影响OH-的物质的量,也就不影
响结果;若排出气泡,液面会下降,故读取V 偏大,结果偏高;正确读数(虚线部
酸
分)和错误读数(实线部分)如图所示。
答案 D
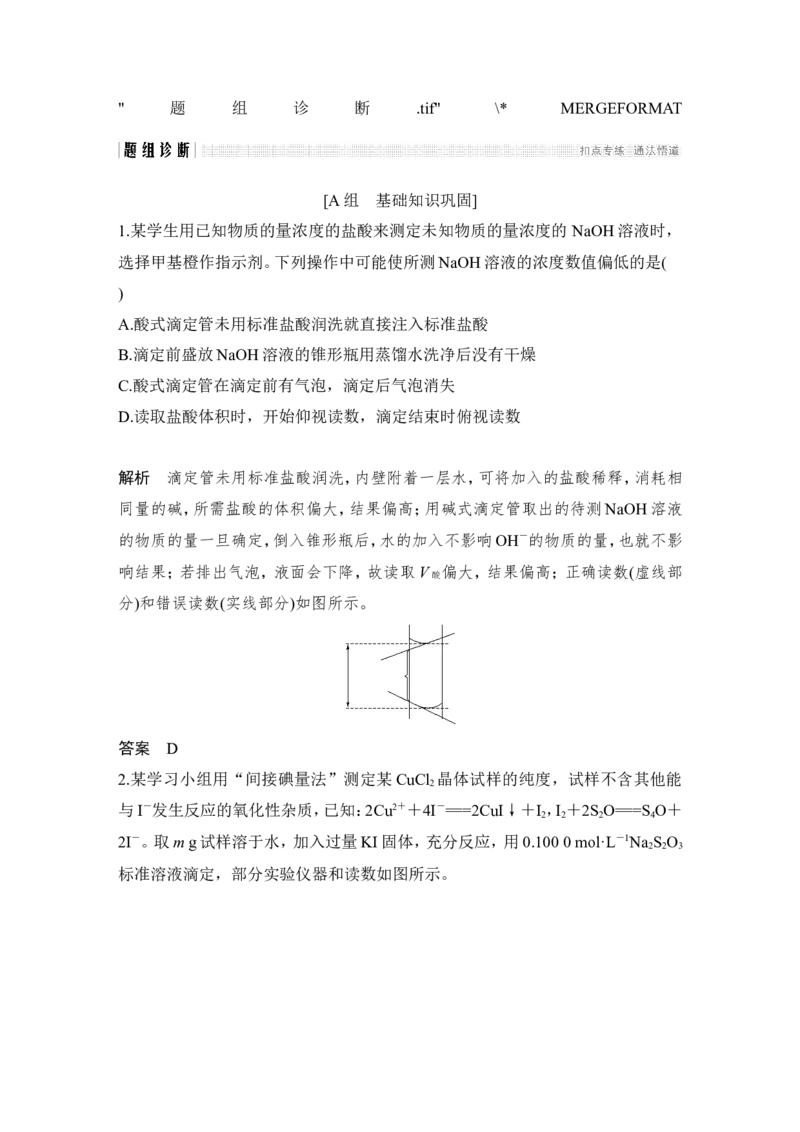
2.某学习小组用“间接碘量法”测定某CuCl 晶体试样的纯度,试样不含其他能
2
与I-发生反应的氧化性杂质,已知:2Cu2++4I-===2CuI↓+I ,I +2S O===S O+
2 2 2 4
2I-。取m g试样溶于水,加入过量KI固体,充分反应,用0.100 0 mol·L-1Na S O
2 2 3
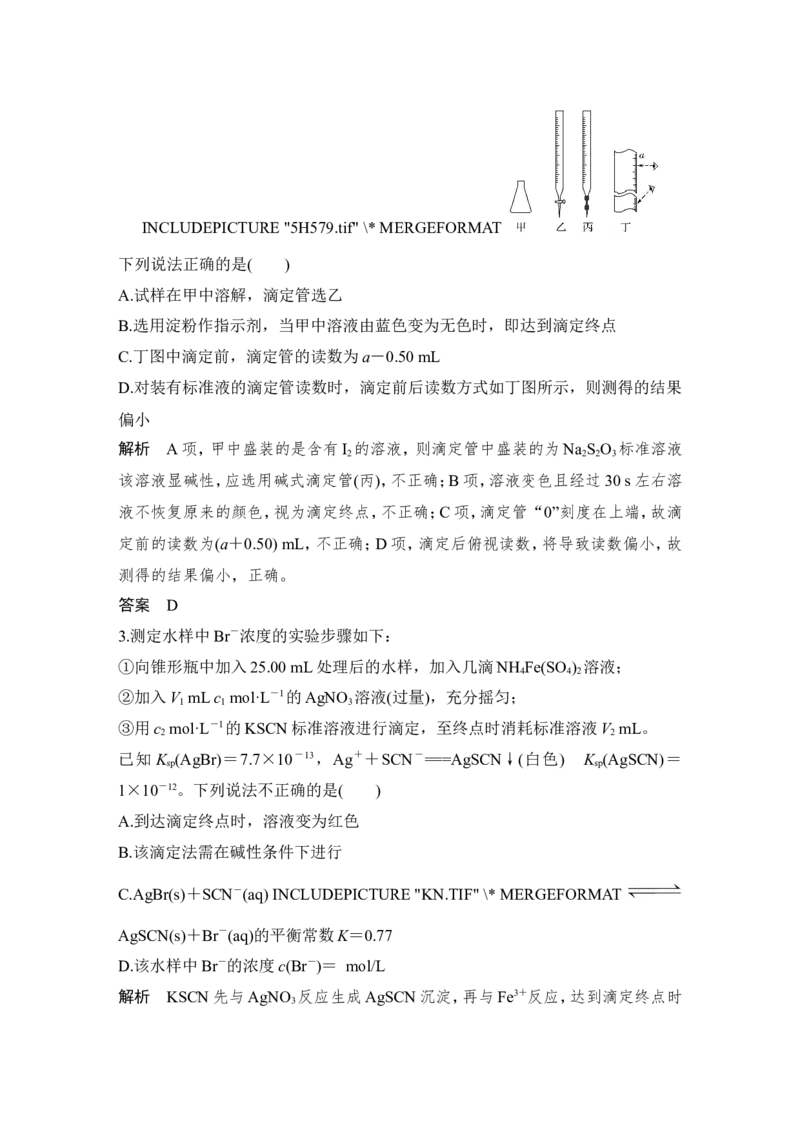
标准溶液滴定,部分实验仪器和读数如图所示。INCLUDEPICTURE "5H579.tif" \* MERGEFORMAT
下列说法正确的是( )
A.试样在甲中溶解,滴定管选乙
B.选用淀粉作指示剂,当甲中溶液由蓝色变为无色时,即达到滴定终点
C.丁图中滴定前,滴定管的读数为a-0.50 mL
D.对装有标准液的滴定管读数时,滴定前后读数方式如丁图所示,则测得的结果
偏小
解析 A项,甲中盛装的是含有I 的溶液,则滴定管中盛装的为Na S O 标准溶液
2 2 2 3
该溶液显碱性,应选用碱式滴定管(丙),不正确;B项,溶液变色且经过30 s左右溶
液不恢复原来的颜色,视为滴定终点,不正确;C项,滴定管“0”刻度在上端,故滴
定前的读数为(a+0.50) mL,不正确;D项,滴定后俯视读数,将导致读数偏小,故
测得的结果偏小,正确。
答案 D
3.测定水样中Br-浓度的实验步骤如下:
①向锥形瓶中加入25.00 mL处理后的水样,加入几滴NH Fe(SO ) 溶液;
4 4 2
②加入V mL c mol·L-1的AgNO 溶液(过量),充分摇匀;
1 1 3
③用c mol·L-1的KSCN标准溶液进行滴定,至终点时消耗标准溶液V mL。
2 2
已知 K (AgBr)=7.7×10-13,Ag++SCN-===AgSCN↓(白色) K (AgSCN)=
sp sp
1×10-12。下列说法不正确的是( )
A.到达滴定终点时,溶液变为红色
B.该滴定法需在碱性条件下进行
C.AgBr(s)+SCN-(aq) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
AgSCN(s)+Br-(aq)的平衡常数K=0.77
D.该水样中Br-的浓度c(Br-)= mol/L
解析 KSCN先与AgNO 反应生成AgSCN沉淀,再与Fe3+反应,达到滴定终点时
3溶液变为红色,A项正确;碱性条件下,Fe3+与OH-反应生成Fe(OH) 沉淀,B项错
3
误;反应 AgBr(s)+SCN-(aq) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
AgSCN(s)+Br-(aq)的平衡常数K==0.77,C项正确;水样中Br-的浓度
c(Br-)= mol/L,D项正确。
答案 B
【归纳总结】
两大拓展滴定法
1.沉淀滴定法
(1)概念:沉淀滴定是利用沉淀反应进行滴定、测量分析的方法,生成沉淀的反应很
多,但符合条件的却很少,实际上应用最多的是银量法,即利用Ag+与卤素离子的
反应来测定Cl-、Br-、I-浓度。
(2)原理:沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂与被滴定物反应的
生成物的溶解度要比滴定剂与指示剂反应的生成物的溶解度小,否则不能用这种
指示剂。如用AgNO 溶液测定溶液中Cl-的含量时常以CrO为指示剂,这是因为
3
AgCl比Ag CrO 更难溶的缘故。
2 4
2.氧化还原滴定法
(1)原理:以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,
或者间接滴定一些本身并没有还原性或氧化性,但能与某些还原剂或氧化剂反应
的物质。
(2)试剂:常见用于滴定的氧化剂有KMnO 、K Cr O 等;常见用于滴定的还原剂有
4 2 2 7
亚铁盐、草酸、维生素C等。
[B组 考试能力过关]
4.(广东卷)准确移取 20.00 mL 某待测 HCl 溶液于锥形瓶中,用 0.100 0 mol·L-
1NaOH溶液滴定,下列说法正确的是
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D.滴定达到终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
解析 A项,滴定管用蒸馏水洗涤后,还要用待装溶液润洗,否则将要引起误差,错误;B项,在用NaOH溶液滴定盐酸的过程中,锥形瓶内溶液由酸性逐渐变为中
性,溶液的pH由小变大,正确;C项,用酚酞作指示剂,锥形瓶中溶液应由无色变
为粉红色,且半分钟内不恢复原色时才能停止滴定,错误;D项,滴定达终点时,发
现滴定管尖嘴部分有悬滴,则碱液的体积偏大,测定结果偏大,错误。
答案 B
5.(2016·全国卷Ⅰ)298 K时,在20.0 mL 0.10 mol·L-1氨水中滴入0.10 mol·L-1的
盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol·L-1氨水的电离
度为1.32%,下列有关叙述正确的是( )
INCLUDEPICTURE "16H20.TIF" \* MERGEFORMAT
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
解析 A项,盐酸滴定氨水时,滴定终点溶液为NH Cl溶液,呈酸性,故指示剂应
4
选甲基橙,错误;B项,一水合氨属于弱碱,与盐酸正好反应生成NH Cl时溶液呈
4
酸性,故二者等浓度反应时,若溶液的pH=7,盐酸的体积应小于氨水的体积,即
小于20.0 mL,错误;C项,根据电荷守恒可知溶液中:c(NH)+c(H+)=c(Cl-)+
c(OH-),M点溶液的pH=7,即c(H+)=c(OH-),则c(NH)=c(Cl-),由于水的电离
是微弱的,故c(NH)=c(Cl-)>c(H+)=c(OH-),错误;D项,由图可知,N点即为
0.10 mol·L-1氨水,由其电离度为1.32%,可知0.10 mol·L-1氨水中c(OH-)=0.001
32 mol·L-1,故该氨水中11c(OH-)的措施是( )
A.向水中通入SO
2
B.将水加热煮沸
C.向纯水中投入一小块金属钠
D.向水中加入NaCl
解析 在水中存在水的电离 平衡:H O INCLUDEPICTURE "KN.TIF" \*
2
MERGEFORMAT H++OH-。当向水中通入SO 时发生反应:SO +H O
2 2 2
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT H SO , H SO
2 3 2 3
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT H++HSO,H SO 电离
2 3
产生的H+使溶液中的H+的浓度增大,对水的电离起抑制作用,最终使水电离产
生的H+(OH-)的浓度远远小于溶液中的H+浓度,即溶液中的c(H+)>c(OH-),A
项正确;水的电离是吸热过程,升高温度促进水的电离,所以将水加热煮沸促进了水的电离,但是水电离产生的H+和OH-的个数总是相同的,所以升温后水中的H
+和OH-的浓度仍然相等,B项错误;向纯水中投入一小块金属钠和水电离出的H
+反应,使水的电离平衡正向移动,对水的电离起到了促进作用,最终使整个溶液
中的c(OH-)>c(H+),C项错误;向水中加入NaCl,NaCl是强酸强碱盐,对水的电
离平衡无影响,所以溶液中的H+和OH-的浓度仍然相等,D项错误。
答案 A
2.下列说法正确的是( )
A.将Ca(OH) 饱和溶液加热,溶液的pH增大
2
B.常温下,pH=11的氨水与pH=3的盐酸等体积混合后,溶液的pH>7
C.将0.1 mol·L-1的HI溶液加水稀释100倍,溶液中所有离子的浓度随之减小
D.两种醋酸溶液的pH分别为a和(a+1),物质的量浓度分别为c 和c 则c =10c
1 2, 1 2
解析 Ca(OH) 的溶解度随温度的升高而降低,将 Ca(OH) 饱和溶液加热,有
2 2
Ca(OH) 析出,溶液的pH减小,A错误;将pH=11的氨水与pH=3的盐酸等体积
2
混合后,氨水过量,溶液的pH>7,B正确;将HI溶液稀释时,c(H+)减小,c(OH-)增
大,C错误;醋酸为弱电解质,浓度越小,电离程度越大,当pH分别为a和(a+1),
物质的量浓度分别为c 和c 时,有 则c >10c ,D错误。
1 2 1 2
答案 B
3.已知:室温下,K (CH COOH)=1.8×10-5、K (NH ·H O)=1.8×10-5。在室温下,
a 3 b 3 2
将pH=3的酸溶液和pH=11的碱溶液等体积混合,混合后溶液的pH大于7,则
该酸溶液和碱溶液的组合是( )
A.CH COOH溶液和氢氧化钡溶液
3
B.CH COOH溶液和氨水
3
C.HBr溶液和氨水
D.HI溶液和氢氧化钡溶液
解析 CH COOH是弱酸,常温下,pH=3的CH COOH溶液中c(CH COOH)远大
3 3 3
于1.0×10-3mol/L,氢氧化钡是强碱,pH=11的氢氧化钡溶液中c(OH-)=1.0×10
-3mol/L,二者等体积混合,CH COOH过量,溶液显酸性,pH小于7,A项错误。由
3
于CH COOH与NH ·H O的电离常数相等,故将pH=3的CH COOH溶液和pH
3 3 2 3
=11的氨水等体积混合,二者恰好完全反应生成CH COONH ,pH等于7,B项错
3 4
误。HBr是强酸,pH=3的HBr溶液中c(HBr)=1.0×10-3mol/L,NH ·H O是弱碱,
3 2pH=11的氨水中c(NH ·H O)远大于1.0×10-3mol/L,二者等体积混合氨水过量,
3 2
溶液显碱性,pH大于7,C项正确。HI和氢氧化钡分别是强酸和强碱,pH=3的HI
溶液中 c(HI)=1.0×10-3mol/L,pH=11 的氢氧化钡溶液中 c(OH-)=1.0×10-
3mol/L,二者等体积混合恰好完全反应,溶液显中性,pH等于7,D项错误。
答案 C
4.(2018·重庆联考)常温时,下列叙述正确的是( )
A.稀释pH=3的醋酸溶液,溶液中所有离子的浓度均降低
B.用标准盐酸滴定未知浓度的烧碱溶液,滴定前仰视,滴定后俯视,测得的烧碱溶
液浓度偏低
C.pH均为11的NaOH和NH ·H O溶液中,水的电离程度不相同
3 2
D.分别中和pH与体积均相同的硫酸和醋酸溶液,硫酸溶液消耗氢氧化钠的物质
的量多
解析 稀释pH=3的醋酸溶液,醋酸的电离程度增大,n(H+)、n(CH COO-)增大,
3
但c(H+)、c(CH COO-)减小,根据K =c(H+)·c(OH-)知,c(OH-)增大,A项错误;
3 W
滴定前仰视,读数偏大,滴定后俯视,读数偏小,则读取的标准盐酸的体积偏小,导
致测得的烧碱溶液浓度偏低,B项正确;pH均为11的NaOH和NH ·H O溶液中,
3 2
c(OH-)相同,故水的电离程度相同,C项错误;醋酸为弱酸,不完全电离,故分别中
和pH与体积均相同的硫酸和醋酸溶液时,醋酸溶液消耗氢氧化钠的物质的量多,
D项错误。
答案 B
5.(2018·湖北鄂东南市级示范高中联盟学校联考,14)下列说法中正确的是( )
A.NaHSO 和NaHSO 都属于酸式盐,二者不发生反应
4 3
B.95 ℃纯水的pH<7,说明加热可导致水呈酸性
C.在生产中可用Na CO 溶液处理锅炉水垢中的CaSO ,使之转化为疏松、易溶于
2 3 4
酸的CaCO
3
D.中和100 mL pH=1的醋酸溶液和100 mL pH=1的盐酸所消耗的NaOH的物质
的量相等
解析 二者能发反应:NaHSO +NaHSO ===Na SO +H O+SO ↑,A项错误;虽
4 3 2 4 2 2
然95 ℃纯水的pH<7,但纯水中H+浓度仍然等于OH-浓度,所以呈中性,B项错
误;在生产中可用Na CO 溶液处理锅炉水垢中的CaSO ,使之转化为疏松、易溶
2 3 4于酸的CaCO ,C项正确;HCl是强电解质,而醋酸是弱电解质,故等体积、等pH
3
的两溶液中HCl的物质的量小于醋酸的物质的量,即醋酸溶液消耗的氢氧化钠多
D项错误。
答案 C
6.pH=1的两种酸溶液X和Y分别与足量的锌反应,酸X比酸Y产生的氢气多,
下列结论正确的是( )
A.X是强酸,Y是弱酸
B.X是弱酸,Y是强酸
C.X是二元酸,Y是一元酸
D.无法判断X、Y的性质
解析 若两种酸均是强酸,又溶液中氢离子浓度相同,但是两种酸的体积未知,当
酸X的体积大于酸Y的体积时,则酸X比酸Y产生的氢气多;若X是弱酸,Y是
强酸,二者的体积相同,酸X比酸Y产生的氢气多,所以X、Y的性质无法判断,选
D。
答案 D
7.(2018·福建质检)H S O 是一种弱酸,实验室欲用0.01 mol·L-1的Na S O 溶液滴
2 2 3 2 2 3
定碘水发生的反应为I +2Na S O ===2NaI+Na S O ,下列说法正确的是( )
2 2 2 3 2 4 6
A.该滴定反应可用甲基橙作指示剂
B.Na S O 是该反应的还原剂
2 2 3
C.该滴定反应可选用如图所示装置
D.该反应中每消耗2 mol Na S O ,转移电子的物质的量为4 mol
2 2 3
解析 碘水显酸性,甲基橙在该溶液中显红色,当用Na S O 溶液滴定达到终点时
2 2 3
溶液由红色变为橙色,颜色变化不明显,因此该滴定反应不可用甲基橙作指示剂,
应该用淀粉溶液作指示剂,A项错误;在该反应中,I元素的化合价降低,得到电子,作氧化剂,Na S O 中的S元素的化合价升高,失去电子,Na S O 是该反应的还原
2 2 3 2 2 3
剂,B项正确;Na S O 是强碱弱酸盐,其溶液显碱性,应该使用碱式滴定管,不能
2 2 3
用酸式滴定管,C项错误;该反应中每消耗2 mol Na S O ,转移2 mol电子,D项错
2 2 3
误。
答案 B
8.常温下,取浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液的
pH等于12,则原溶液的浓度为( )
A.0.01 mol·L-1 B.0.17 mol·L-1
C.0.05 mol·L-1 D.0.50 mol·L-1
解析 由题意,可设原溶液物质的量浓度为 c mol·L-1,NaOH溶液体积为3 L,
HCl溶液体积为2 L,则二者混合后溶液体积为5 L,因为常温下二者混合反应后,
所得溶液pH=12,即c(H+)=10-12mol·L-1,所以c(OH-)=K ÷c(H+)=10-2mol·L
w
-1,则c mol·L-1×3 L-c mol·L-1×2 L=10-2mol·L-1×5 L,解得c=0.05,则原溶
液的浓度为0.05 mol·L-1,故选C。
答案 C
9.室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释,溶液的pH变化如
图所示。下列说法正确的是( )
A.稀释前,c(A)=10c(B)
B.稀释前,A溶液中由水电离出的c(OH-)>10-7mol/L
C.M点,A、B两种碱溶液中阳离子的物质的量浓度相等
D.用醋酸中和A溶液至恰好完全反应时,溶液的pH为7
解析 由图像可知,随着溶液的稀释,A溶液的pH变化较大,即A溶液的碱性大
于B溶液的碱性,且稀释前A溶液中OH-浓度是B溶液的10倍,但由于A的碱
性较强,故c(A)<10c(B),A错误;碱能抑制水的电离,故水电离的OH-浓度小于
10-7mol/L,B错误;M点两溶液pH相同,证明溶液中的H+浓度相同,根据K 可
W
知,溶液中的OH-浓度也相同,再由电荷守恒判断,两溶液中的阳离子浓度也相同,C正确;恰好完全反应时,无法判断生成物中阴离子即醋酸根离子的水解程度与
阳离子水解程度的相对大小,故不能判断中和后溶液的酸碱性,D错误。
答案 C
10.(2019·太原调研)已知:常温下,A酸的溶液pH=a,B碱的溶液pH=b。
(1)若A为盐酸,B为氢氧化钡,且a+b=14,两者等体积混合,溶液的pH=
________。酸碱按体积比为1∶10混合后溶液显中性,则a+b=________。
(2)若A为醋酸,B为氢氧化钠,且a=4,b=12,那么A溶液中水电离出的氢离子
浓度为________mol·L-1,B溶液中水电离出的氢离子浓度为________mol·L-1。
(3)若A为醋酸,B为氢氧化钠,且a+b=14,用体积为V 的醋酸和体积为V 的氢
A B
氧化钠溶液混合后,溶液显中性,则其体积关系V ________V ,混合后溶液中的离
A B
子浓度关系为c(Na+)________c(CH COO-)。
3
(4)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶
液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式
为_________________________________________________________________
____________________________________________________________________。
解析 (1)根据题意,盐酸中c(H+)=10-amol·L-1,氢氧化钡溶液中c(OH-)=10b-
14mol·L-1,酸碱发生中和反应呈中性时,n(H+)=n(OH-),有V ×10-a=V ×10b-
A B
14,V ∶V =10a+b-14,又a+b=14,故V =V 。(3)a+b=14的弱酸和强碱混合呈中
A B A B
性,则酸需要体积小。(4)a+b=14的一元酸和一元碱混合呈碱性,则碱是弱碱。
答案 (1)7 13 (2)10-10 10-12 (3)< =
(4)M++H O INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT MOH+
2
H+
11.过氧化氢的水溶液适用于医用消毒、环境消毒和食品消毒。
Ⅰ.过氧化氢性质探究实验
(1)酸性条件下H O 可将Fe2+转化成Fe3+,由此说明H O 具有________性。
2 2 2 2
(2)已知H O 是一种二元弱酸,其中K =2.20×10-12、K =1.05×10-25,则H O
2 2 a1 a2 2 2
的电离方程式为______________________________________________________,
常温下,1 mol/L的H O 溶液的pH约为________。
2 2
Ⅱ.过氧化氢含量的测定实验某兴趣小组同学用0.100 0 mol/L的酸性高锰酸钾标准溶液滴定试样中的过氧化
氢,反应原理为2MnO+5H O+6H+===2Mn2++8H O+5O ↑。
2 2 2
(3)滴定达到终点的现象是_______________________________________。
(4)用移液管移取25.00 mL试样置于锥形瓶中,重复滴定四次,每次消耗酸性高锰
酸钾标准溶液的体积如表所示:
第一次 第二次 第三次 第四次
V(KMnO 溶液)/mL 17.10 18.10 18.00 17.90
4
计算试样中过氧化氢的浓度为________mol/L。
(5)若滴定前滴定管尖嘴处有气泡,滴定后消失,则测定结果________(填“偏高”
“偏低”或“不变”)。
解析 Ⅰ.(1)酸性条件下,H O 可将Fe2+氧化为Fe3+,体现了过氧化氢的氧化性。
2 2
(2) 过 氧 化 氢 属 于 二 元 弱 酸 , 分 步 电 离 , 其 电 离 的 方 程 式 为 H O
2 2
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT H + + HO 、 HO
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT H++O;又 K =
a1
2.20×10-12,K =1.05×10-25,K K ,以第一步电离为主,则K ===2.20×10
a2 a1 a2 a1
-12,所以
≫
c(H+)≈1.48×10-6mol/L,即pH≈5.8。Ⅱ.(3)滴定达到终点的现象:当滴入最后一
滴标准液,锥形瓶内溶液恰好由无色变为紫色,且30秒内溶液不褪色。(4)由于第
一次数据误差过大,故舍去;其他三组数据的平均值为18.00 mL,根据反应2MnO
+5H O +6H+===2Mn2++8H O+5O ↑,n(H O )=2.5×n(MnO)=2.5×0.100 0
2 2 2 2 2 2
mol/L×0.018 L,c(H O )==0.180 0(mol/L)。
2 2
(5)滴定前滴定管尖嘴处有气泡,导致消耗的标准液体积偏大,则测定结果偏高。
答案 Ⅰ.(1)氧化 (2)H O INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2 2
H++HO、HO INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
H++O 5.8
Ⅱ.(3)当滴入最后一滴标准溶液 锥形瓶内溶液恰好由无色变为紫色,且 30秒内
溶液不褪色 (4)0.180 0 (5)偏高[B级 拔高选做题]
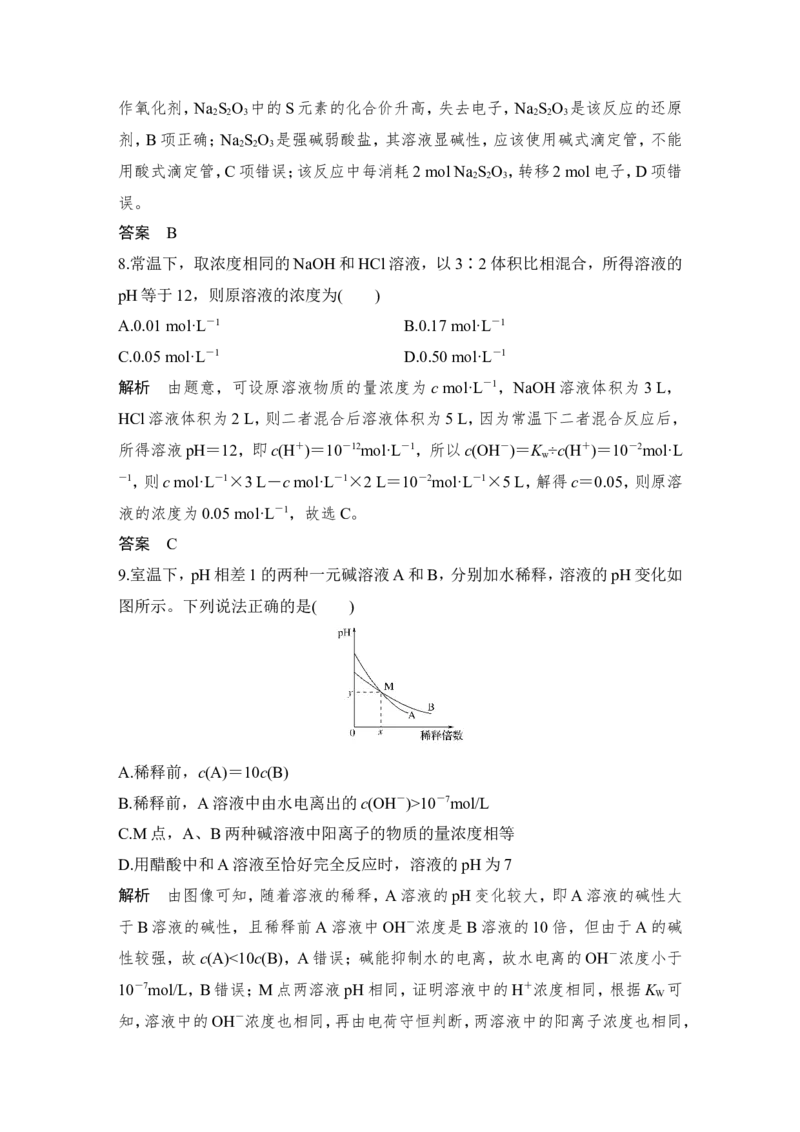
12.如图所示,用一定物质的量浓度的NaOH溶液Y滴定10 mL一定物质的量浓度
的盐酸X的图像,依据图像推出X和Y的物质的量浓度是表内各组中的( )
INCLUDEPICTURE "10X632.TIF" \* MERGEFORMAT
A B C D
X(mol·L-1) 0.12 0.04 0.03 0.09
Y(mol·L-1) 0.04 0.12 0.09 0.03
解析 由图知,加入 30 mL NaOH 溶液后溶液 pH=7,即 c(HCl)·V(盐酸)=
c(NaOH)·V(NaOH溶液),c(HCl)×10×10-3L=c(NaOH)×30×10-3L,c(HCl)=
3c(NaOH);又知加入20 mL NaOH溶液时,溶液pH=2,则=10-2mol·L-1;将
c(HCl)=3c(NaOH)代入得c(NaOH)=0.03 mol·L-1,c(HCl)=0.09 mol·L-1。
答案 D
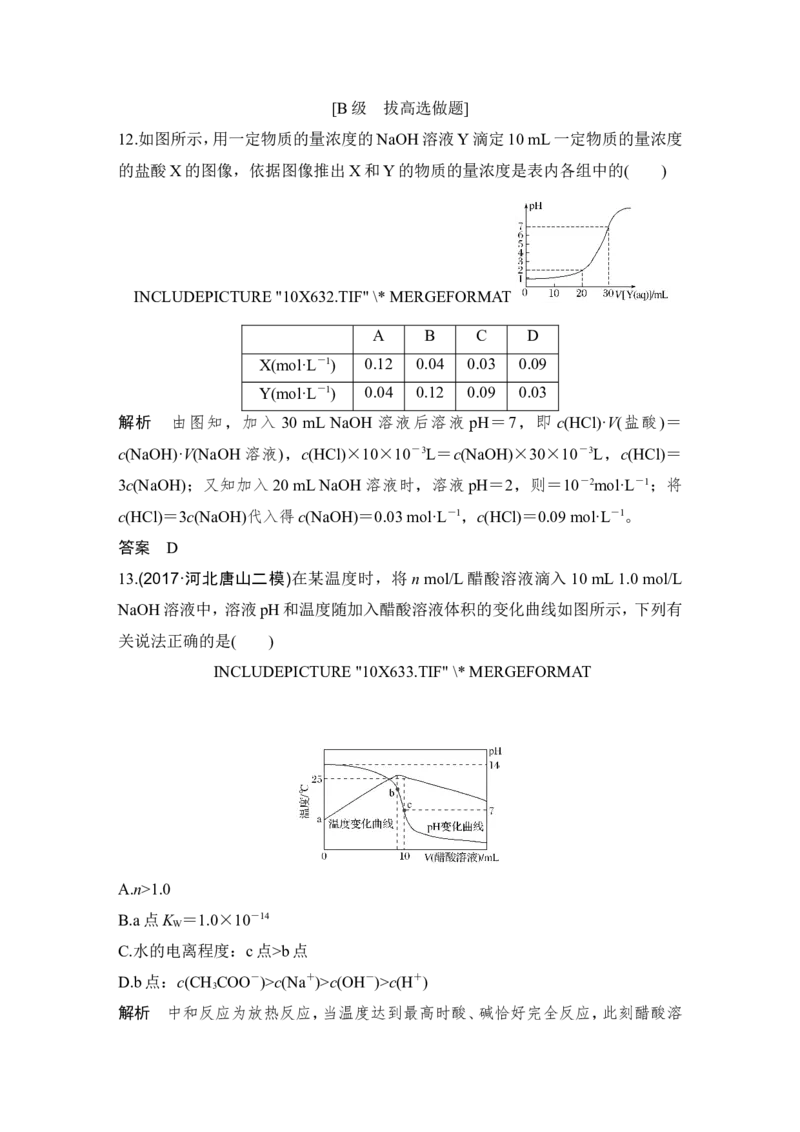
13.(2017·河北唐山二模)在某温度时,将 n mol/L醋酸溶液滴入 10 mL 1.0 mol/L
NaOH溶液中,溶液pH和温度随加入醋酸溶液体积的变化曲线如图所示,下列有
关说法正确的是( )
INCLUDEPICTURE "10X633.TIF" \* MERGEFORMAT
A.n>1.0
B.a点K =1.0×10-14
W
C.水的电离程度:c点>b点
D.b点:c(CH COO-)>c(Na+)>c(OH-)>c(H+)
3
解析 中和反应为放热反应,当温度达到最高时酸、碱恰好完全反应,此刻醋酸溶液的体积小于10 mL,所以n>1.0,A正确;a点温度低于25 ℃,K 随温度的降低
W
而减小,故a点K <1.0×10-14,B错误;b点酸、碱恰好完全反应生成醋酸钠,对水
W
的电离的促进作用最大,c点醋酸过量,过量的醋酸对水的电离又起抑制作用,故
水的电离程度:c点c(CH COO-)>c(OH-)>c(H+),D错误。
3
答案 A
14.(2018·厦门质检)铝锰合金可作炼钢脱氧剂。某课外小组欲测定铝锰合金中锰
的含量。
Ⅰ.硫酸亚铁铵[(NH ) Fe(SO ) ]溶液的浓度标定
4 2 4 2
步骤1:取20.00 mL 0.015 mol/L K Cr O 标准液于250 mL锥形瓶中,加入20 mL
2 2 7
稀硫酸和5 mL浓磷酸,用硫酸亚铁铵溶液滴定,接近终点时加2滴R溶液作指示
剂,继续滴定至终点,消耗的体积为V mL。
1
步骤2:重复步骤1实验,接近终点时加4滴R溶液,消耗的体积为V mL。
2
Ⅱ.过硫酸铵[(NH ) S O ]催化氧化滴定法测定锰含量。
4 2 2 8
取m g铝锰合金于锥形瓶中,加入适量的浓磷酸,加热至完全溶解,稀释冷却摇匀,
再加入少量的硝酸银溶液、过量的过硫酸铵溶液,加热煮沸至无大量气泡冒出,冷
却至室温(此时溶液中锰的化合价为+7),用标定的硫酸亚铁溶液进行滴定,根据
实验数据计算铝锰合金中锰的含量。
[查阅资料]①酸性条件下,Cr O具有很强的氧化性,易被还原为绿色的Cr3+。
2
②R溶液的变色原理:
\s\up7(RQ,(还原型,无色))
(1)Ⅰ中步骤1、2需要的玻璃仪器有锥形瓶、胶头滴管、________、________。
(2)Ⅰ 中 滴 定 过 程 , 主 要 反 应 的 离 子 方 程 式 是
______________________________________________________________________
_____________________________________________________________________
。
(3)Ⅰ 中 步 骤 2 的 主 要 作 用 是
______________________________________________。
(4)Ⅱ中硫酸亚铁铵溶液的标定浓度是_____________________________________
mol/L(用含V 、V 的代数式表示)。
1 2(5)Ⅱ中加入硝酸银溶液的目的是________________________________________。
(6)Ⅱ中若未加热煮沸无大量气泡冒出,锰含量测定结果将________(填“偏大”
“偏小”或“无影响”)。
(7)为了提高该实验的准确度和可靠度,需进行________。
解析 (1)因为硫酸亚铁铵[(NH ) Fe(SO ) ]溶液显酸性,K Cr O 溶液有强氧化性,
4 2 4 2 2 2 7
所以Ⅰ中滴定实验需要用到酸式滴定管,可使用量筒向滴定管中取液体,也可以
使用移液管取用,故Ⅰ中需要的玻璃仪器除了锥形瓶、胶头滴管外,还用酸式滴定
管、量筒(或移液管)。(2)Ⅰ 中滴定过程,酸性条件下用硫酸亚铁铵溶液滴定
K Cr O 标准液,Fe2+与Cr O发生氧化还原反应,离子方程式为 14H++Cr O+
2 2 7 2 2
6Fe2+===6Fe3++2Cr3++7H O。(3)根据[查阅资料]②R溶液的变色原理可得,变色
2
过程要消耗一定量的氧化剂或还原剂,所以对指示剂用量加以校正是提高准确度
的关键,因此Ⅰ中步骤2的主要作用是校正指示剂。(4)加2滴R溶液作指示剂时
消耗硫酸亚铁铵溶液V mL,为校正指示剂所造成的误差,加4滴R溶液时消耗硫
1
酸亚铁铵溶液V mL,所以K Cr O 标准液实际消耗的硫酸亚铁铵溶液为(2V -
2 2 2 7 1
V )mL,根据反应离子方程式可得关系:Cr O~6Fe2+,又根据已知20.00 mL 0.015
2 2
mol/L K Cr O 标准液,所以硫酸亚铁铵溶液的浓度为mol/L=mol/L。(5)由已知,
2 2 7
催化氧化滴定法测定铝锰合金中锰含量,过硫酸铵[(NH ) S O ]作氧化剂与锰在催
4 2 2 8
化剂作用下发生氧化还原反应,所以Ⅱ中加入硝酸银溶液的目的是作为催化剂,
加 快 氧 化 速 率 。 (6)Ⅱ 中 过 硫 酸 铵 是 过 量 的 , 存 在 反 应 (NH ) S O +
4 2 2 8
2H O===2NH HSO +H O ,加热煮沸至无大量气泡冒出,是为了除去溶液中氧化
2 4 4 2 2
性物质,若未加热煮沸无大量气泡冒出,则消耗还原剂硫酸亚铁铵的物质的量偏
大,锰含量测定结果将偏大。
(7)为了提高该实验的准确度和可靠度,需防止偶然误差的产生,可取两个以上相
同的样品,以完全一致的条件进行实验,看其结果的一致性,即进行平行实验
答案 (1)酸式滴定管 量筒(或移液管)
(2)14H++Cr O+6Fe2+===6Fe3++2Cr3++7H O
2 2
(3)校正指示剂
(4)1.8/(2V -V )
1 2
(5)作为催化剂,加快氧化速率
(6)偏大 (7)平行实验