文档内容
第十二章 物质结构与性质
能力提升检测卷
时间:90分钟 分值:100分
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2022·上海宝山·模拟预测)下列物质所属晶体类型分类正确的是
选项 A B C D
共价晶
石墨 生石灰 碳化硅 金刚石
体
分子晶
冰 固态氨 氯化铯 干冰
体
离子晶
氮化铝 食盐 明矾 芒硝
体
金属晶
铜 汞 铝 铁
体
2.(2022·湖北·枣阳一中模拟预测)用化学用语表示 中的相关微粒,
其中正确的是
A.中子数56,质量数102的Pd原子:
B.COS的结构式:O=C=S
C.硫原子核外电子排布式:
D. 的电子式:
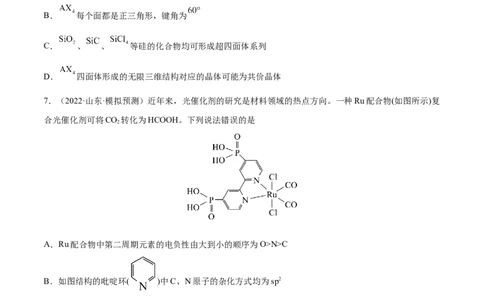
3.(2021·海南·模拟预测)PCl 在气态和液态时,分子结构如图所示,下列关于PCl 分子的说法中错误的
5 5
是A.每个原子都达到8电子稳定结构,且为非极性分子
B.键角(∠Cl-P-Cl)有120°、90°、180°几种
C.PCl 受热后会分解生成PCl ,PCl 分子呈三角锥形
5 3 3
D.分子中5个P-Cl键键能不都相同
4.(2021·上海黄浦·一模)关于氯化钠晶体,下列说法正确的是( )
A.硬度大于金刚石 B.熔点高于冰 C.沸点大于石墨 D.能导电
5.(2022·江苏·模拟预测)氨气是一种重要的化工原料,以氨为原料可以生产化肥和硝酸,在催化剂条件
下,氨催化氧化生成NO,进而继续被氧化为NO ,再与水反应生成硝酸,氨气与硝酸反应可得氮肥硝酸
2
铵。4NH (g)+5O(g) 4NO(g)+6H O(g) H=-905.8kJ·mol-1。工业上将含NO 废气通入氢氧化钠溶液中可
3 2 2 2
△
获得NaNO 和NaNO ,也可向废气中通入NH 在催化剂的条件转化为无毒无害的气体排放。下列说法正确
3 2 3
的是
A.NH 转化为NH ,键角变大
3
B.[Cu(NH )]+中含有离子键、配位键
3 4
C.NO 空间构型为直线形
D.氨气易溶于水的原因是氨气分子间存在氢键
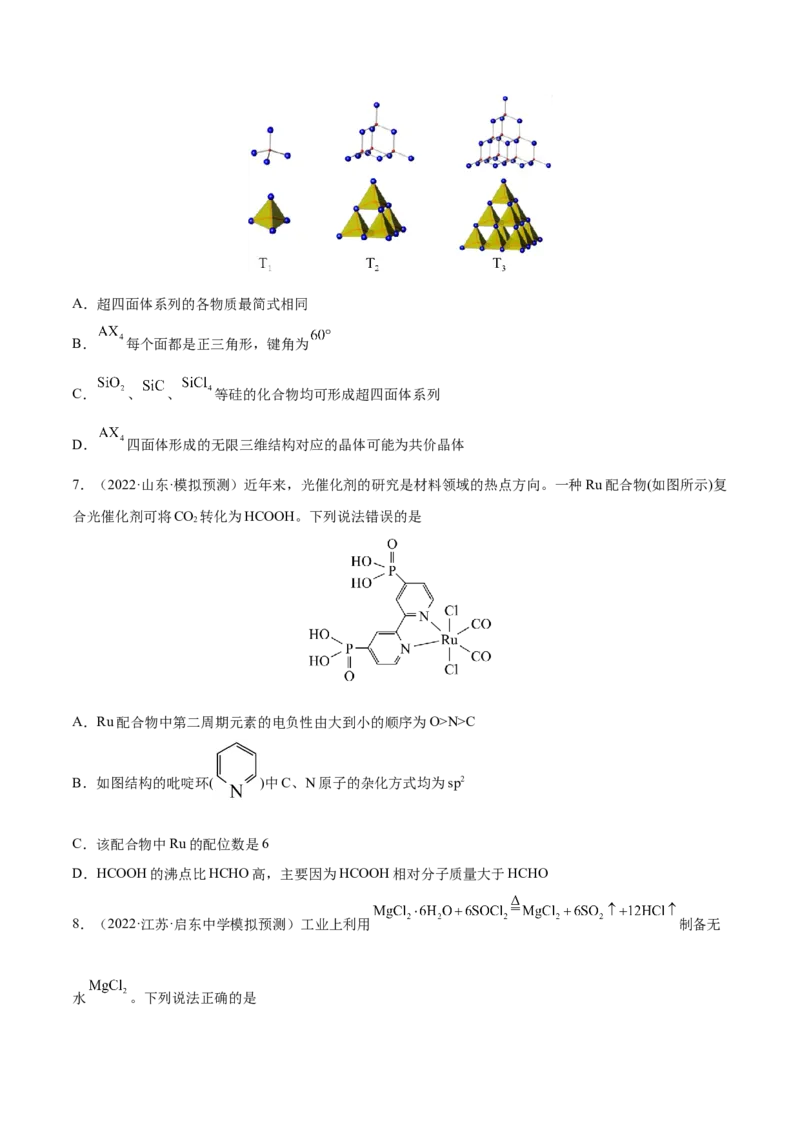
6.(2022·北京市十一学校三模) 四面体( )在无机化合物中很常见。 按图所示方式相连,可形成
一系列“超四面体”( 、 …),下列说法正确的是A.超四面体系列的各物质最简式相同
B. 每个面都是正三角形,键角为
C. 、 、 等硅的化合物均可形成超四面体系列
D. 四面体形成的无限三维结构对应的晶体可能为共价晶体
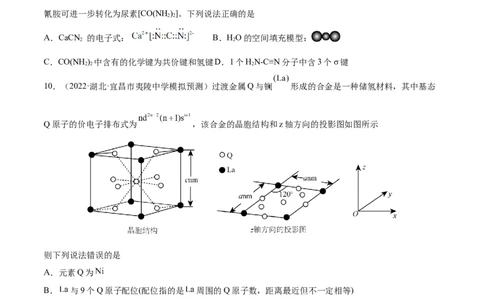
7.(2022·山东·模拟预测)近年来,光催化剂的研究是材料领域的热点方向。一种Ru配合物(如图所示)复
合光催化剂可将CO 转化为HCOOH。下列说法错误的是
2
A.Ru配合物中第二周期元素的电负性由大到小的顺序为O>N>C
B.如图结构的吡啶环( )中C、N原子的杂化方式均为sp2
C.该配合物中Ru的配位数是6
D.HCOOH的沸点比HCHO高,主要因为HCOOH相对分子质量大于HCHO
8.(2022·江苏·启东中学模拟预测)工业上利用 制备无
水 。下列说法正确的是A. 为非极性分子
B. 中既含离子键又含共价键
C. 的电子式为
D.基态O原子的价电子排布式为
9.(2022·江苏连云港·模拟预测)石灰氮(CaCN)是一种氮肥,与土壤中的HO反应生成氰胺(H N-C≡N),
2 2 2
氰胺可进一步转化为尿素[CO(NH)]。下列说法正确的是
2 2
A.CaCN 的电子式: B.HO的空间填充模型:
2 2
C.CO(NH) 中含有的化学键为共价键和氢键D.1个HN-C≡N分子中含3个σ键
2 2 2
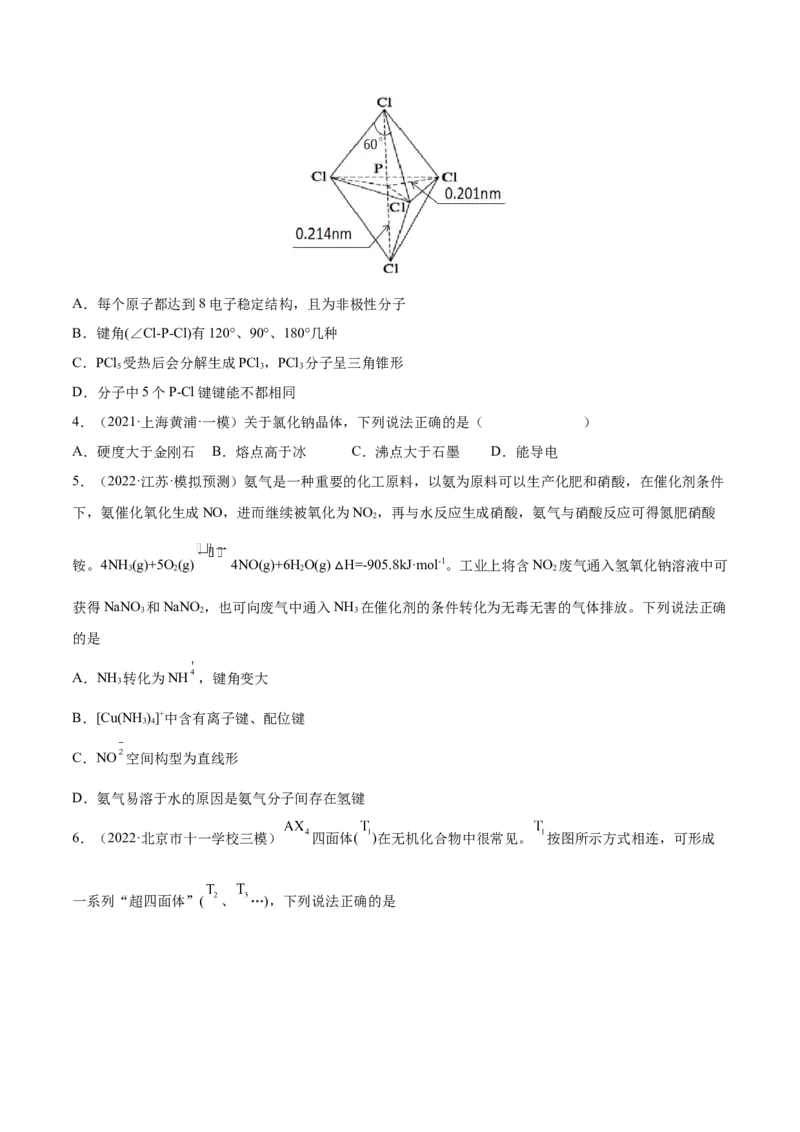
10.(2022·湖北·宜昌市夷陵中学模拟预测)过渡金属Q与镧 形成的合金是一种储氢材料,其中基态
Q原子的价电子排布式为 ,该合金的晶胞结构和z轴方向的投影图如图所示
则下列说法错误的是
A.元素Q为
B. 与9个Q原子配位(配位指的是 周围的Q原子数,距离最近但不一定相等)
C.该合金的晶胞含有Q、 原子个数分别为5、1
D.该合金的晶胞体积为
11.(2022·辽宁·大连市一0三中学模拟预测)依据元素周期律,下列判断不正确的是
A.第一电离能: B.原子半径:C.电负性: D.酸性:
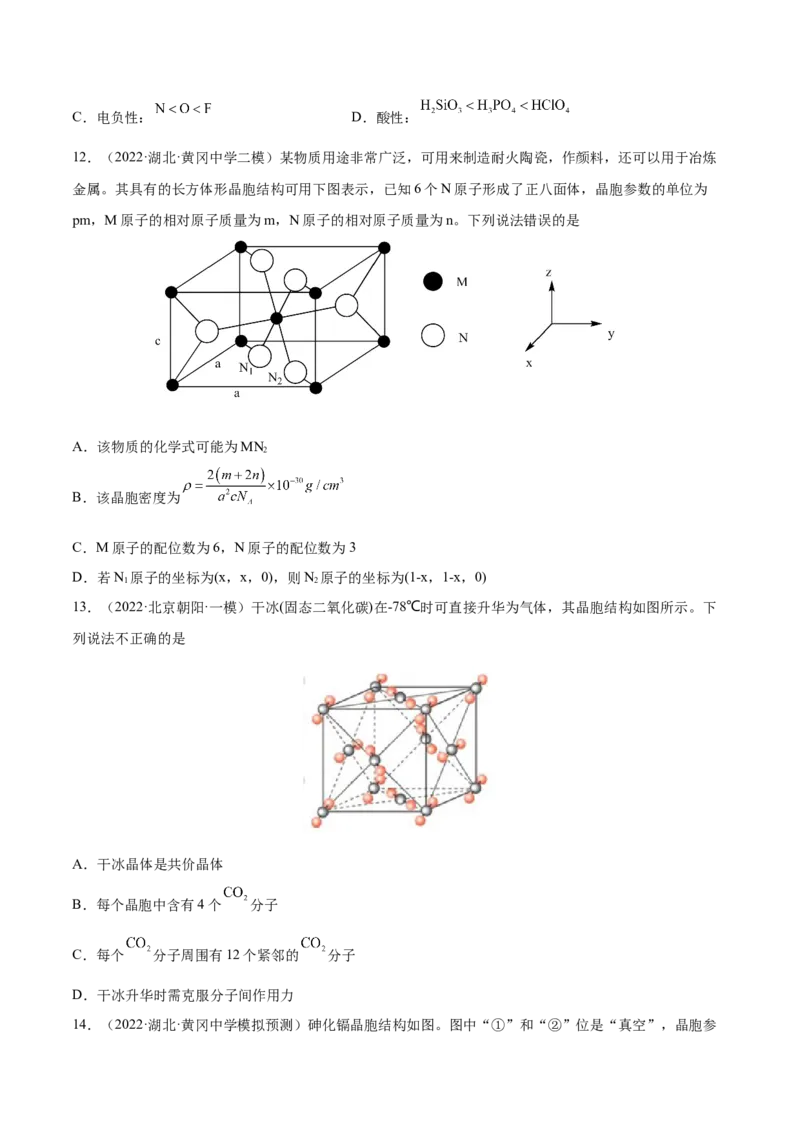
12.(2022·湖北·黄冈中学二模)某物质用途非常广泛,可用来制造耐火陶瓷,作颜料,还可以用于冶炼
金属。其具有的长方体形晶胞结构可用下图表示,已知6个N原子形成了正八面体,晶胞参数的单位为
pm,M原子的相对原子质量为m,N原子的相对原子质量为n。下列说法错误的是
A.该物质的化学式可能为MN
2
B.该晶胞密度为
C.M原子的配位数为6,N原子的配位数为3
D.若N 原子的坐标为(x,x,0),则N 原子的坐标为(1-x,1-x,0)
1 2
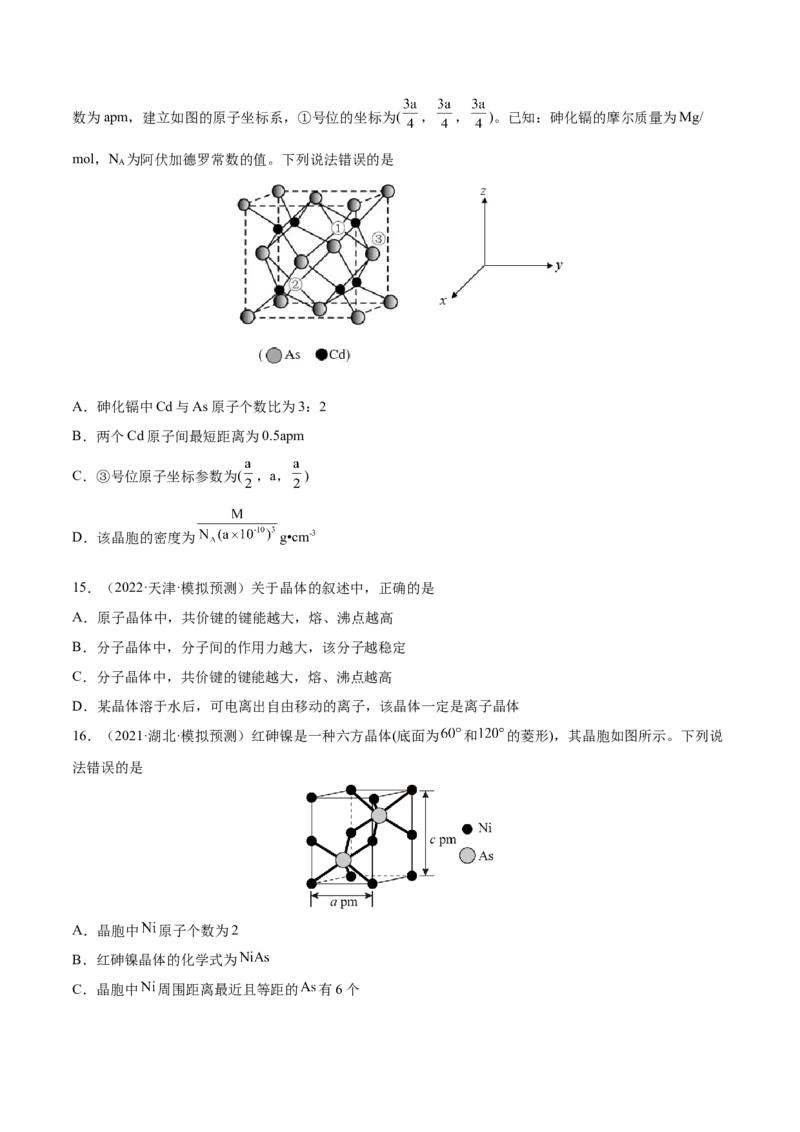
13.(2022·北京朝阳·一模)干冰(固态二氧化碳)在-78℃时可直接升华为气体,其晶胞结构如图所示。下
列说法不正确的是
A.干冰晶体是共价晶体
B.每个晶胞中含有4个 分子
C.每个 分子周围有12个紧邻的 分子
D.干冰升华时需克服分子间作用力
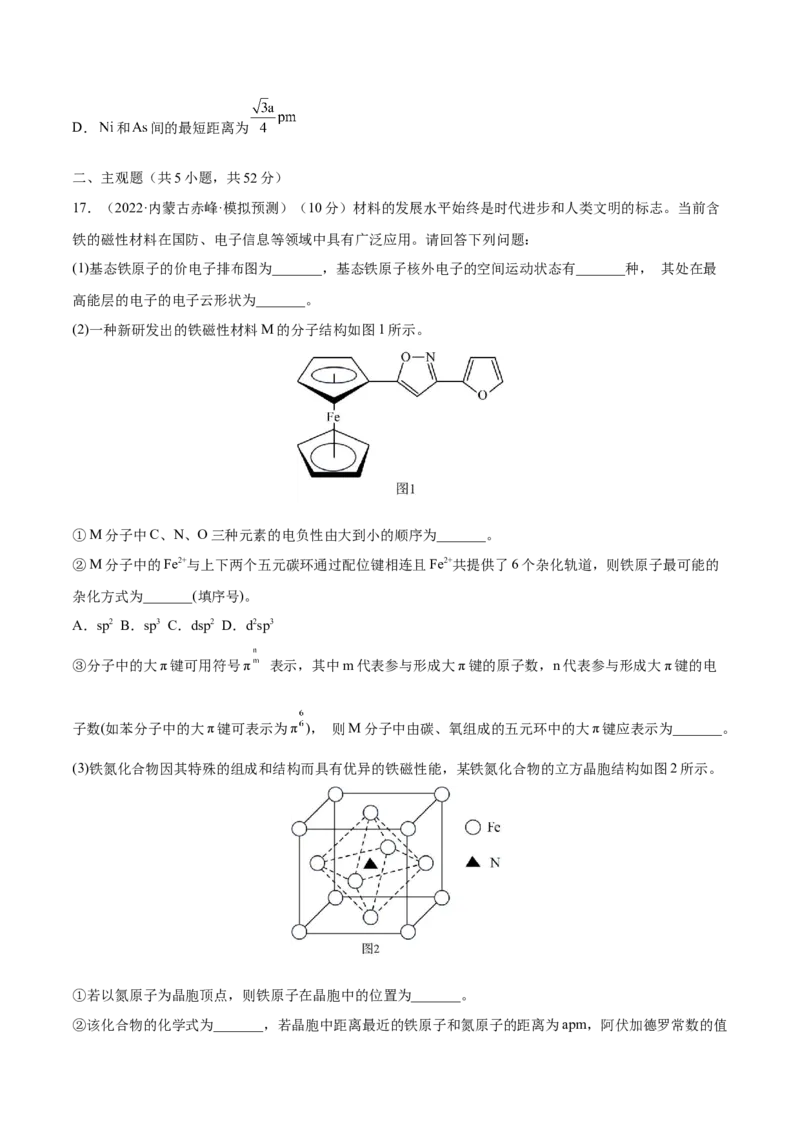
14.(2022·湖北·黄冈中学模拟预测)砷化镉晶胞结构如图。图中“①”和“②”位是“真空”,晶胞参数为apm,建立如图的原子坐标系,①号位的坐标为( , , )。已知:砷化镉的摩尔质量为Mg/
mol,N 为阿伏加德罗常数的值。下列说法错误的是
A
A.砷化镉中Cd与As原子个数比为3:2
B.两个Cd原子间最短距离为0.5apm
C.③号位原子坐标参数为( ,a, )
D.该晶胞的密度为 g•cm-3
15.(2022·天津·模拟预测)关于晶体的叙述中,正确的是
A.原子晶体中,共价键的键能越大,熔、沸点越高
B.分子晶体中,分子间的作用力越大,该分子越稳定
C.分子晶体中,共价键的键能越大,熔、沸点越高
D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体
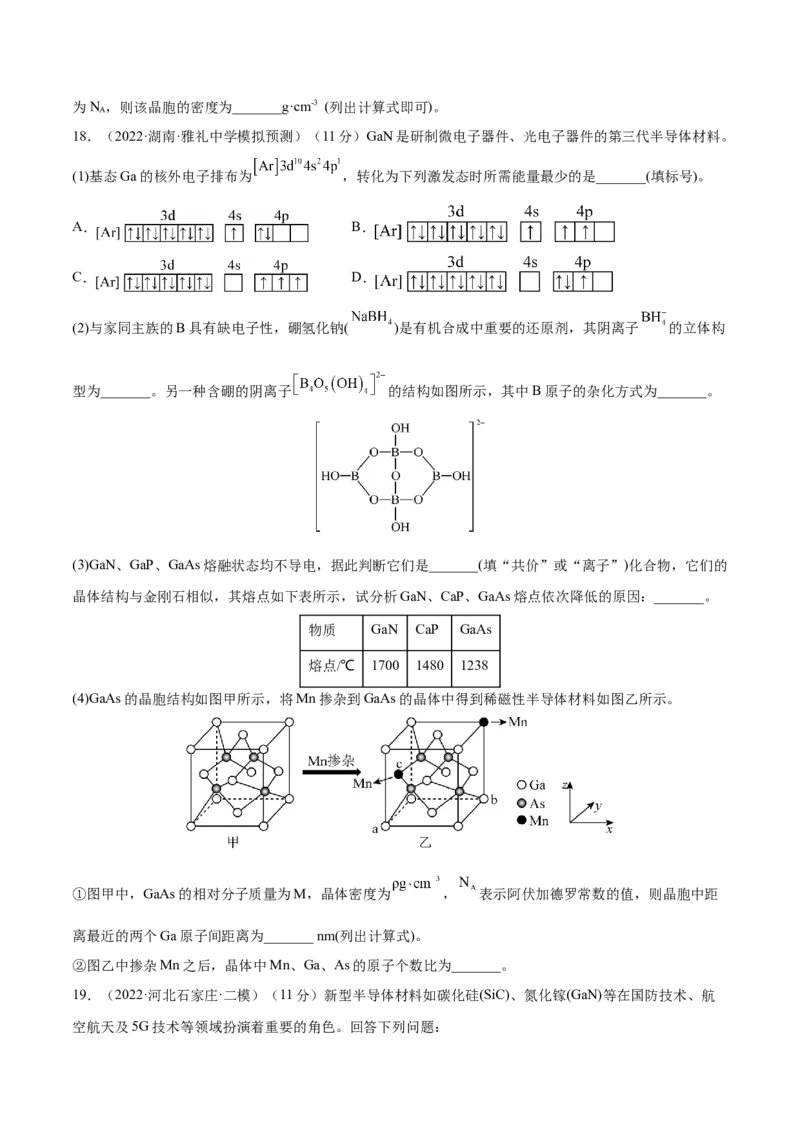
16.(2021·湖北·模拟预测)红砷镍是一种六方晶体(底面为 和 的菱形),其晶胞如图所示。下列说
法错误的是
A.晶胞中 原子个数为2
B.红砷镍晶体的化学式为
C.晶胞中 周围距离最近且等距的 有6个D. 和 间的最短距离为
二、主观题(共5小题,共52分)
17.(2022·内蒙古赤峰·模拟预测)(10分)材料的发展水平始终是时代进步和人类文明的标志。当前含
铁的磁性材料在国防、电子信息等领域中具有广泛应用。请回答下列问题:
(1)基态铁原子的价电子排布图为_______,基态铁原子核外电子的空间运动状态有_______种, 其处在最
高能层的电子的电子云形状为_______。
(2)一种新研发出的铁磁性材料M的分子结构如图1所示。
①M分子中C、N、O三种元素的电负性由大到小的顺序为_______。
②M分子中的Fe2+与上下两个五元碳环通过配位键相连且Fe2+共提供了6个杂化轨道,则铁原子最可能的
杂化方式为_______(填序号)。
A.sp2 B.sp3 C.dsp2 D.d2sp3
③分子中的大π键可用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电
子数(如苯分子中的大π键可表示为π ), 则M分子中由碳、氧组成的五元环中的大π键应表示为_______。
(3)铁氮化合物因其特殊的组成和结构而具有优异的铁磁性能,某铁氮化合物的立方晶胞结构如图2所示。
①若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为_______。
②该化合物的化学式为_______,若晶胞中距离最近的铁原子和氮原子的距离为apm,阿伏加德罗常数的值为N ,则该晶胞的密度为_______g·cm-3 (列出计算式即可)。
A
18.(2022·湖南·雅礼中学模拟预测)(11分)GaN是研制微电子器件、光电子器件的第三代半导体材料。
(1)基态Ga的核外电子排布为 ,转化为下列激发态时所需能量最少的是_______(填标号)。
A. B.
C. D.
(2)与家同主族的B具有缺电子性,硼氢化钠( )是有机合成中重要的还原剂,其阴离子 的立体构
型为_______。另一种含硼的阴离子 的结构如图所示,其中B原子的杂化方式为_______。
(3)GaN、GaP、GaAs熔融状态均不导电,据此判断它们是_______(填“共价”或“离子”)化合物,它们的
晶体结构与金刚石相似,其熔点如下表所示,试分析GaN、CaP、GaAs熔点依次降低的原因:_______。
物质 GaN CaP GaAs
熔点/℃ 1700 1480 1238
(4)GaAs的晶胞结构如图甲所示,将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料如图乙所示。
①图甲中,GaAs的相对分子质量为M,晶体密度为 , 表示阿伏加德罗常数的值,则晶胞中距
离最近的两个Ga原子间距离为_______ nm(列出计算式)。
②图乙中掺杂Mn之后,晶体中Mn、Ga、As的原子个数比为_______。
19.(2022·河北石家庄·二模)(11分)新型半导体材料如碳化硅(SiC)、氮化镓(GaN)等在国防技术、航
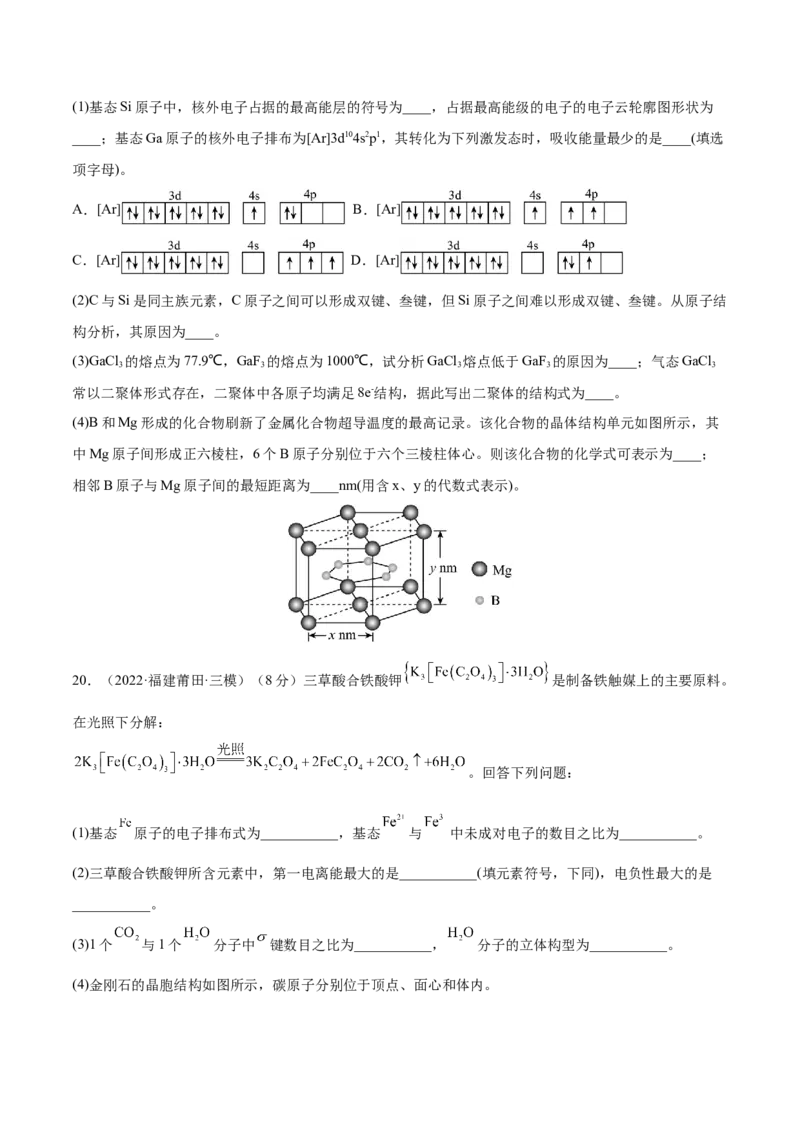
空航天及5G技术等领域扮演着重要的角色。回答下列问题:(1)基态Si原子中,核外电子占据的最高能层的符号为____,占据最高能级的电子的电子云轮廓图形状为
____;基态Ga原子的核外电子排布为[Ar]3d104s2p1,其转化为下列激发态时,吸收能量最少的是____(填选
项字母)。
A.[Ar] B.[Ar]
C.[Ar] D.[Ar]
(2)C与Si是同主族元素,C原子之间可以形成双键、叁键,但Si原子之间难以形成双键、叁键。从原子结
构分析,其原因为____。
(3)GaCl 的熔点为77.9℃,GaF 的熔点为1000℃,试分析GaCl 熔点低于GaF 的原因为____;气态GaCl
3 3 3 3 3
常以二聚体形式存在,二聚体中各原子均满足8e-结构,据此写出二聚体的结构式为____。
(4)B和Mg形成的化合物刷新了金属化合物超导温度的最高记录。该化合物的晶体结构单元如图所示,其
中Mg原子间形成正六棱柱,6个B原子分别位于六个三棱柱体心。则该化合物的化学式可表示为____;
相邻B原子与Mg原子间的最短距离为____nm(用含x、y的代数式表示)。
20.(2022·福建莆田·三模)(8分)三草酸合铁酸钾 是制备铁触媒上的主要原料。
在光照下分解:
。回答下列问题:
(1)基态 原子的电子排布式为___________,基态 与 中未成对电子的数目之比为___________。
(2)三草酸合铁酸钾所含元素中,第一电离能最大的是___________(填元素符号,下同),电负性最大的是
___________。
(3)1个 与1个 分子中 键数目之比为___________, 分子的立体构型为___________。
(4)金刚石的晶胞结构如图所示,碳原子分别位于顶点、面心和体内。若图中原子1的坐标为 ,则原子2的坐标为___________。
21.(2022·广西柳州·二模)(12分)黄金是一种非常重要的金属。不仅是用于储备和投资的特殊通货,
同时又是首饰业、电子业、现代通讯。航天航空业等部门的重要材料。
(1)金能溶解于王水中: ,请分析 中 的配体是
___________,配位数是___________。
(2)开采的金矿可用氰化法提取:先以氰化钠(NaCN)溶液处理粉碎的金矿石得到 ,再用锌还原:
。Zn与 形成的配离子为正四面体形,Au(+1价)与 形成的配
离子为直线形。
① 中配合离子 中σ键和π键个数之比是___________,配体 杂化方式是
___________。
②写出Zn的电子排布式___________,C、N、Na的第一电离能由大到小顺序为___________。
(3) 是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,它都是以二聚体
的形式存在。依据以上信息判断 晶体的结构属于___________晶体,写出 的结构式
___________。
(4)①Au单质的晶体为面心立方最密堆积,Au的配位数为___________。以下金属和金具有相同的堆积模
型的是___________。
a.Po b.Na c.Zn d.Cu
②若Au的原子半径为a nm,Au单质的摩尔质量为M g/mol,阿伏伽德罗常数为N ,求Au单质的密度为
A
___________ 。(用含a、N 、M的代数式表示)
A