文档内容
1.利用某钴矿石(主要成分为Co O)制取Co(OH) 粗品及其他工业产品的工艺流程如图1所
2 3 2
示。
已知:浸出液中含有的阳离子主要有H+、Cu2+、Co2+、Fe2+、Mg2+。回答下列问题:
(1)钴矿石浸出时加入NaSO 的目的为________________________________。
2 3
(2)溶液中lg c(X)(X表示Fe3+、Cu2+、Fe2+、Co2+、Mg2+、Ca2+)与pH的变化关系如图2所
示(离子浓度小于 10-5 mol·L-1时可认为已除尽),在萃取余液中通入空气的目的是
_______________________________________________________________________________
_______________________________________________________________________________
,
用熟石灰调pH至3.2,过滤1所得滤渣的主要成分为________________,萃取和反萃取的目
的是________________。
(3)用氧化镁调滤液 1 的 pH 为 9.1 时,得到的氢氧化钴粗品中含有的主要杂质为
____________,多次洗涤可提高粗产品中钴含量。“过滤2”后所得滤液直接排放会造成水
体污染,须进行处理,用熟石灰调节 pH使c(Mg2+)≤10-5 mol·L-1,则K [Mg(OH) ]=
sp 2
________。
2.锰常用于制造合金锰钢。某化工厂以软锰矿(主要成分是MnO ,含有SiO 、Fe O 、CaO
2 2 2 3
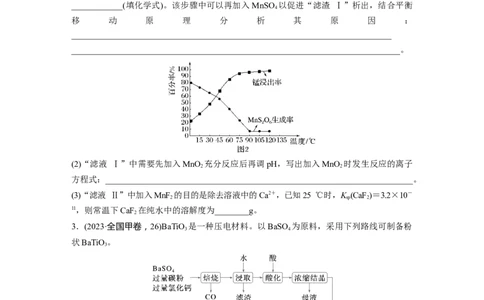
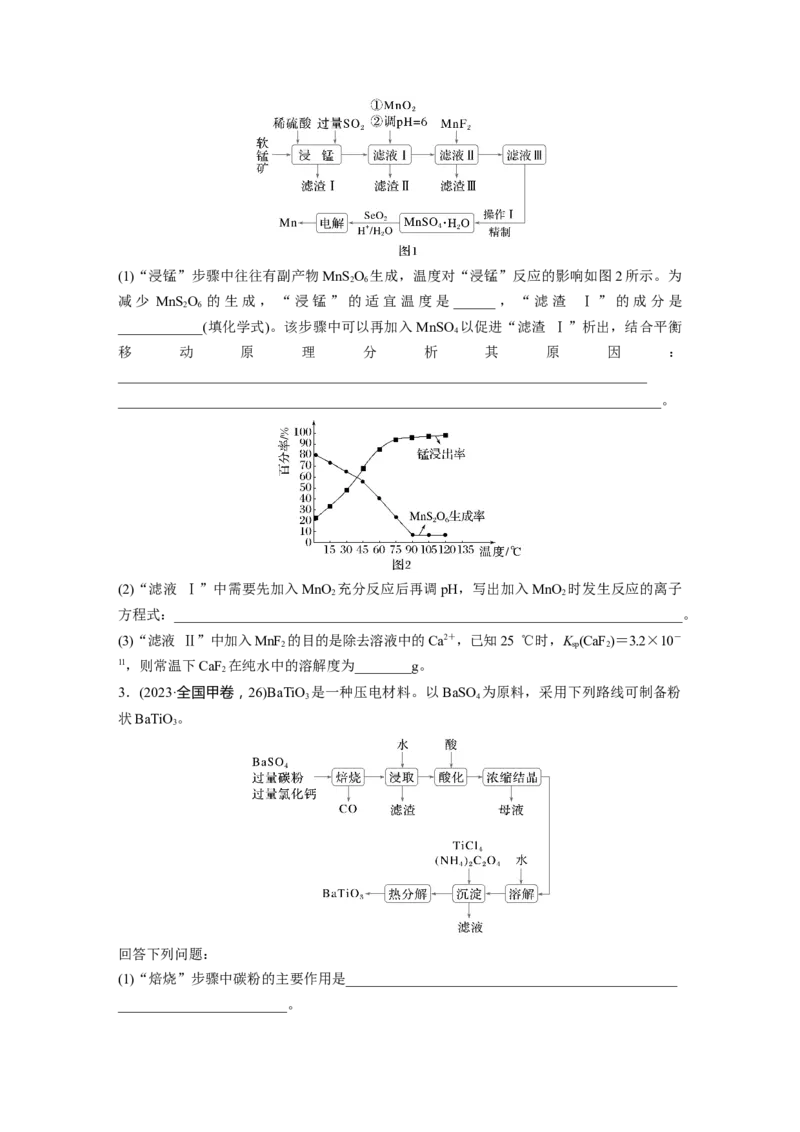
等少量杂质)为主要原料制取金属锰的工艺流程如图1所示。(1)“浸锰”步骤中往往有副产物MnS O 生成,温度对“浸锰”反应的影响如图2所示。为
2 6
减少 MnS O 的生成,“浸锰”的适宜温度是______,“滤渣 Ⅰ”的成分是
2 6
____________(填化学式)。该步骤中可以再加入MnSO 以促进“滤渣 Ⅰ”析出,结合平衡
4
移 动 原 理 分 析 其 原 因 :
___________________________________________________________________________
_____________________________________________________________________________。
(2)“滤液 Ⅰ”中需要先加入MnO 充分反应后再调pH,写出加入MnO 时发生反应的离子
2 2
方程式:________________________________________________________________________。
(3)“滤液 Ⅱ”中加入MnF 的目的是除去溶液中的Ca2+,已知25 ℃时,K (CaF )=3.2×10-
2 sp 2
11,则常温下CaF 在纯水中的溶解度为________g。
2
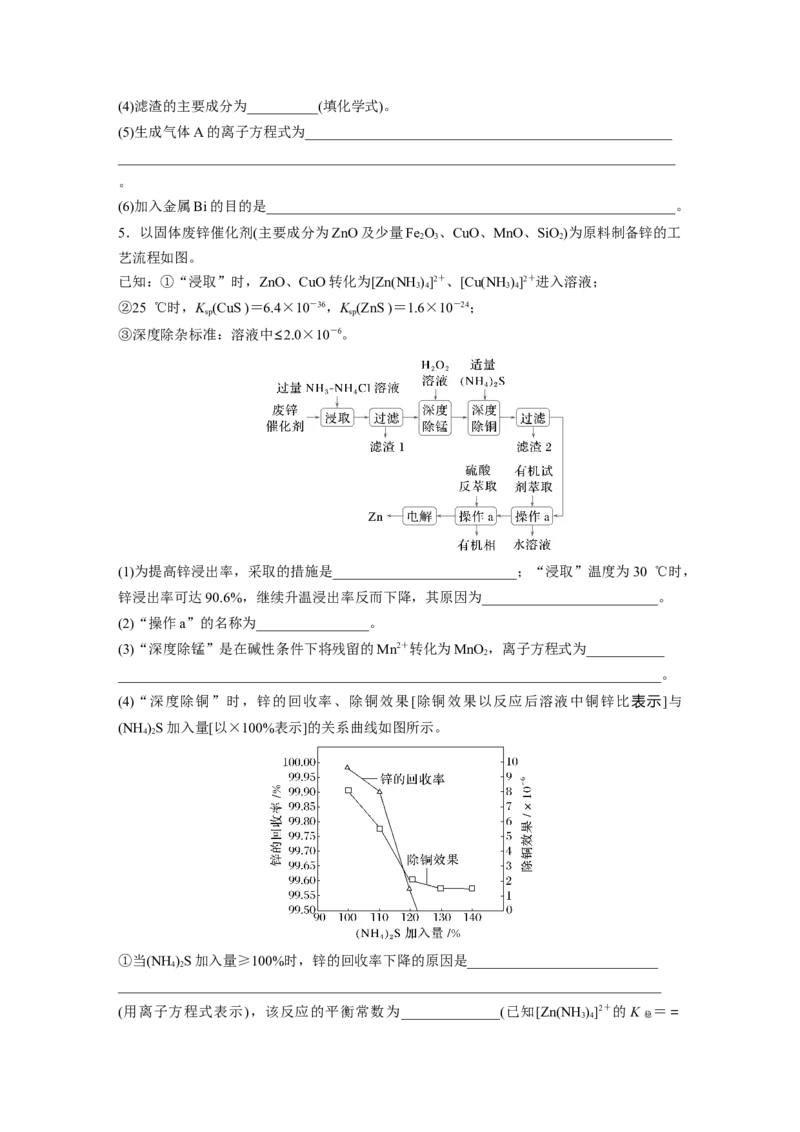
3.(2023·全国甲卷,26)BaTiO 是一种压电材料。以BaSO 为原料,采用下列路线可制备粉
3 4
状BaTiO 。
3
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是_______________________________________________
________________________。(2)“焙烧”后固体产物有BaCl 、易溶于水的BaS和微溶于水的CaS。“浸取”时主要反应
2
的离子方程式为_________________________________________________________________。
(3)“酸化”步骤应选用的酸是______(填标号)。
a.稀硫酸 b.浓硫酸
c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?_________________,其原因是__________
_______________________________________________________________________________
。
(5)“沉淀”步骤中生成BaTiO(C O) 的化学方程式为________________________________。
2 4 2
(6)“热分解”生成粉状钛酸钡,产生的 ∶n =______________。
CO
4.[2022·辽宁,16(1)(2)(3)(4)(5)(6)]某工厂采用辉铋矿(主要成分为BiS ,含有FeS 、SiO
2 3 2 2
杂质)与软锰矿(主要成分为MnO )联合焙烧法制备BiOCl和MnSO ,工艺流程如下:
2 4
已知:①焙烧时过量的MnO 分解为MnO,FeS 转变为Fe O;
2 2 3 2 2 3
②金属活动性:Fe>(H)>Bi>Cu;
③相关金属离子形成氢氧化物的pH范围如下:
开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为_______________________________________________。
a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度
(2)Bi S 在空气中单独焙烧生成BiO,反应的化学方程式为___________________________。
2 3 2 3
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出Bi3+和Mn2+;②_____________________。(4)滤渣的主要成分为__________(填化学式)。
(5)生成气体A的离子方程式为____________________________________________________
_______________________________________________________________________________
。
(6)加入金属Bi的目的是__________________________________________________________。
5.以固体废锌催化剂(主要成分为ZnO及少量Fe O 、CuO、MnO、SiO)为原料制备锌的工
2 3 2
艺流程如图。
已知:①“浸取”时,ZnO、CuO转化为[Zn(NH )]2+、[Cu(NH )]2+进入溶液;
3 4 3 4
②25 ℃时,K (CuS )=6.4×10-36,K (ZnS )=1.6×10-24;
sp sp
③深度除杂标准:溶液中≤2.0×10-6。
(1)为提高锌浸出率,采取的措施是__________________________;“浸取”温度为30 ℃时,
锌浸出率可达90.6%,继续升温浸出率反而下降,其原因为_________________________。
(2)“操作a”的名称为________________。
(3)“深度除锰”是在碱性条件下将残留的Mn2+转化为MnO ,离子方程式为___________
2
_____________________________________________________________________________。
(4)“深度除铜”时,锌的回收率、除铜效果[除铜效果以反应后溶液中铜锌比表示]与
(NH )S加入量[以×100%表示]的关系曲线如图所示。
4 2
①当(NH )S加入量≥100%时,锌的回收率下降的原因是___________________________
4 2
_____________________________________________________________________________
(用离子方程式表示),该反应的平衡常数为______________(已知[Zn(NH )]2+的K ==
3 4 稳2.9×109)。
②“深度除铜”时(NH )S加入量最好应选______(填字母)。
4 2
A.100% B.110% C.120% D.130%
(5)测定反萃取水相中Zn2+的浓度:量取20.00 mL反萃取水相于锥形瓶中,用0.010 0 mol·L-1
EDTA(乙二胺四乙酸钠NaHY)标准溶液滴定至终点(Zn2++HY2-===ZnY2-+2H+)。重复实
2 2 2
验三次,平均消耗标准溶液22.30 mL。则反萃取水相中Zn2+的浓度为________________(保
留两位小数)。