文档内容
考点 02 物质的量 气体摩尔体积
(好题冲关)
【基础过关】
1.每年10月23日上午6:02到晚上6: 02被誉为“摩尔日”(MoleDay)。下列说法正确的是
A.摩尔是物质的数量的单位
B.摩尔是联系宏观物质和微观粒子之间的物理量
C.二氧化碳的摩尔质量是44
D.0.5 mol HO中含有1 mol H
2
2.下列关于“物质的量”“摩尔”和“摩尔质量”的叙述中正确的是
A.物质的摩尔质量等于其相对分子(原子)质量
B.“物质的量”是国际单位制中的一个基本单位
C.“摩尔”是“物质的量”的单位
D.1mol任何物质都含有约6.02×1023个原子
3.火箭燃料为偏二甲肼(C HN),它是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推
2 8 2
动力。下列叙述正确的是( )
A.偏二甲肼(C HN)的摩尔质量为60
2 8 2
B.6.02×1023个偏二甲肼(C HN)分子的质量约为60g
2 8 2
C.1 mol 偏二甲肼(C HN)的质量为60 g·mol-1
2 8 2
D.60g偏二甲肼(C HN)中含有N 个氮原子
2 8 2 A
4.我国宇航员已经在太空泡茶了。茶装在特制包装袋中,注水后用加热器进行加热就可以喝了。下
列说法正确的是( )
A.宇航员太空泡茶用水的 HO的摩尔质量是18g
2
B.18g太空泡茶用水中含有原子的物质的量为3mol
C.在标准状况下,1mol水的体积约是22.4L
D.18g太空泡茶用水中含有6.02×1023个H原子
5.同温同压下,下列说法正确的是( )
A.等质量的NH 和HS所含原子个数比为
3 2
B.等体积的两种气体,具有相同的密度
C.等物质的量的CO和NO具有相同的质量
D.等体积的两种气体,所含的原子数必定相同
6.下列关于阿伏加德罗常数和气体摩尔体积等的说法正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.标准状况下,1摩尔HO的体积约为22.4 L
2
B.128 g SO 气体在标准状况下的体积约为44.8 L
2
C.同温同压下两种气体的体积之比等于摩尔质量之比
D.常温下,22.4 LO 所含的分子数为N
2 A
7.三种气体X、Y、Z的相对分子质量关系为M(X)ρ(Ne)>ρ(O )
2 2
B.当它们的温度和密度都相同时,三种气体的压强p(H )>p(Ne)>p(O )
2 2
C.当它们的质量、温度和压强均相同时,三种气体的体积V(O )>V(Ne)>V(H )
2 2
D.当它们的压强、体积和温度均相同时,三种气体的质量m(H )>m(Ne)>m(O )
2 2
9.设N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.标准状况下,2.24L的乙烯和2.24L的己烯,碳氢键都为0.2mN ,m为烯烃碳原子数
A
B.25℃,pH=12的NaOH溶液中含有OH-的数目约为0.01N
A
C.CHCHOH+3O+4OH- = 2CO2-+5HO,每消耗1molCH CHOH,有12N 电子发生转移
3 2 2 3 2 3 2 A
D.2NaO+2HO=4NaOH+O↑,该反应转移电子数为2N 时,生成0.5mol O
2 2 2 2 A 2
10.过氧化钠是宇宙飞船和潜水艇中氧气的主要来源,其作用原理中包含了反应
2NaO+2CO =2Na CO+O 。用N 表示阿伏加德罗常数,下列说法正确的是( )
2 2 2 2 3 2 A
A.11.2LO 含N 个氧原子
2 A
B.在0.1molNa CO 中含Na-C键的数目为0.2N
2 3 A
C.反应中每生成1molO 转移2mol电子
2
D.10.6gNa CO 溶于100mL水中,所得溶液的物质的量浓度为1mol/L
2 3
11.(2023·辽宁省大连市一模)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.0.1 mol/L Na CO 溶液中,含有 的数目为0.2N
2 3 A
B.标准状况下,22.4 L CH 和22.4 L Cl 在光照下充分反应后的分子数为2N
4 2 A
C.1mol CaC 晶体和1molCaH 晶体含有的离子数目均为2N
2 2 A
D.一定条件下,5.6 g Fe与0.1 mol Cl 充分反应,转移的电子数为0.3N
2 A
12.(2023·浙江省义乌市高三高考适应性考试)设N 为阿伏加德罗常数,下列有关说法正确的是
A
( )
A.在25℃时,pH为12的CHCOONa溶液中水电离出的H+数目为0.01N
3 A
资料收集整理【淘宝店铺:向阳百分百】B.标准状况下,4.48LSO 和足量O 反应,生成的SO 分子数目为0.2N
2 2 3 A
C.电解精炼粗铜时,阳极质量减少6.4g,外电路中通过电子的数目为0.2N
A
D.13g苯、苯乙烯、聚苯乙烯的混合物中所含氢原子数目为N
A
13.(2023·辽宁省抚顺市普通高中高三模拟)N 表示阿伏加德罗常数的值,下列说法正确的是( )
A
A.1.8g重水(D O)中所含质子数为N
2 A
B.常温下1L pH=13的Ba(OH) 中含有OH-的数目为0.2N
2 A
C.106gNaCO 固体中含有N 个CO2-
2 3 A 3
D.标准状况下,22.4LSO 中含有SO 的分子数为N
3 3 A
14.(2023·江西省景德镇市高三二模)N 是阿伏加德罗常数的值,下列说法正确的是( )
A
A.16.25gFeCl 完全水解形成的Fe(OH) 胶体粒子数小于0.1N
3 3 A
B.92.0g甘油(丙三醇)中含有羟基数为1.0N
A
C.22.4L(标准状况)三氧化硫含有的质子数为40N
A
D.1.0molCl 与足量的NaOH反应转移的电子数为2.0N
2 A
15.(2023·江西省赣州市高三二模)设N 为阿伏伽德罗常数的值,下列说法错误的是( )
A
A.室温下,20gKH固体中所含H-的数目为0.5N
A
B.1L0.01mol·L-1的Ca(HCO ) 溶液中含碳粒子总数为0.02N
3 2 A
C.50g质量分数为46%的乙醇水溶液中含有的氧原子总数为0.5N
A
D.2NH (g) 3H(g)+N(g) ΔH=+akJ·mol-1,若参加反应的NH 数目为2N ,反应会吸收akJ热量
3 2 2 3 A
16.(2023·河北省邢台市九师联盟高三联考)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.17gHO 中含有非极性键的数目为0.5N
2 2 A
B.标准状况下,11.2LCHOH含有原子核的数目为3N
3 A
C.1mol·L-1的KCl溶液中含有 的数目为N
A
D.1mol Na O 与足量HO反应,转移电子的数目为2N
2 2 2 A
17.(2023·四川省成都市高三第三次诊断考试)设N 代表阿伏加德罗常数的值。下列说法正确的是
A
( )
A.标准状况下,22.4LCH 中含极性键数目约为13N
4 10 A
B.39gNaO 固体含有离子数约为2N
2 2 A
C.1molNH NO 溶于某稀氨水后所得溶液呈中性,则该溶液中NH +数目为N
4 3 4 A
D.0.5molCl 溶于水后,溶液中的Cl-、ClO-、HClO三者之和为N
2 A
18.(2023·湖北省华大新高考联盟高三二模教学质量测评)设N 为阿佛加德罗常数的值。下列说法正
A
确的是( )
A.标准状况下,22.4L的CH 和CHCl 所含分子数均为N
4 3 A
B.1molSiO 中Si-O键的数目为4N
2 A
资料收集整理【淘宝店铺:向阳百分百】C.电解精炼铜时,阳极质量减少32g时,外电路中转移的电子数为N
A
D.F-水解能力弱于NH +则1L1mol·L-1的NH F溶液中,HF和NH +的总数大于N
4 4 4 A
19.(2023·四川省南充市三模)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.NaO 作供氧剂时,每生成5.6LO ,转移电子数为0.25N
2 2 2 A
B.工业合成氨时,每反应1molN ,生成的极性共价键数目为6N
2 A
C.电解精炼铜时,阳极质量每减少64g,电路中转移2mol电子
D.明矾净水时,0.1mol/LAl3+形成的Al(OH) 胶粒的数目为0.1N
3 A
20.C、N、O、S、H都是中学化学中常见的元素。按要求完成下列填空。
(1)0.5 mol CH 的质量为_______;标准状况下,4.48 L NH 所含分子数为_______。
4 3
(2)等物质的量的CH、NH 和N 三种气体,所含原子数之比为_______,等质量的CH 和N 物质的量
4 3 2 4 2
之比为_______。
(3)含有1.806×1024个电子的OH- 的物质的量为_______;0.5 mol HO分子中所含质子数与_______个
2
NH 中所含质子数相等。
3
(4)在标准状况下,由SO 和CO 组成的混合气体为8.96 L,质量为24 g,该混合气体的平均摩尔质量
2 2
是_______,混合气体中CO 的体积分数是_______。
2
21. (1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为 ,可能
是 气体。
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为 。
(3)在一定条件下,m g NHHCO 完全分解生成NH 、CO、HO(g),按要求填空。
4 3 3 2 2
①若所得混合气体对H 的相对密度为d,则混合气体的物质的量为 。NH HCO 的摩尔质
2 4 3
量为 (用含m、d的代数式表示)。
②若所得混合气体的密度折合成标准状况为ρ g·L-1,则混合气体的平均摩尔质量为
(用含ρ的代数式表示)。
③若在该条件下,所得NH 、CO 、HO(g)的体积分数分别为a%、b%、c%,则混合气体的平均相对
3 2 2
分子质量为 (用含a、b、c的代数式表示)。
【能力提升】
22.对于反应Mg(OH) +NHCl MgOHCl+NH ↑+H O,下列相关说法正确的是( )
2 4 3 2
A.1mol MgOHC1的质量为76.5g/mol
B.NH C的摩尔质量等于它的相对分子质量
4
C.一个 分子的质量约为
D.含有 个氢原子的 的物质的量为1mol
资料收集整理【淘宝店铺:向阳百分百】23.假定把 的相对原子质量改为 ,那么下列叙述错误的是( )
A.此时16O的相对原子质量为 B.N 个O 与N 个H 的质量比为16:1
A 2 A 2
C.N 的摩尔质量为56 g/mol D.标准状况下,16g O 的体积约为11.2L
2 2
24.标准状况下,11.2L由CO和CO 组成的混合气体的质量为16g,则下列说法不正确的( )
2
A.混合气体中,CO和CO 的物质的量之比为3:1
2
B.混合气体中CO和CO 气体的质量比为21:11
2
C.同温同压下,该混合气体的密度是H 密度的16倍
2
D.标准状况下,该混合气体中CO 的体积为8.4L
2
25.在恒温密闭容器中,某液态化合物XY 和一定量的氧气恰好完全燃烧,反应方程式为:XY (液)
2 2
+3O (气)=XO(气)+2YO(气)。在标准状况下测得生成物的体积是33.6L,密度是2.56g/L。下列叙述中正确
2 2 2
的是
A.在标准状况下,参加反应的O 体积为112L
2
B.XY 的摩尔质量为76g/mol
2
C.Y元素符号为C
D.在相同条件下测得反应后气压明显减小
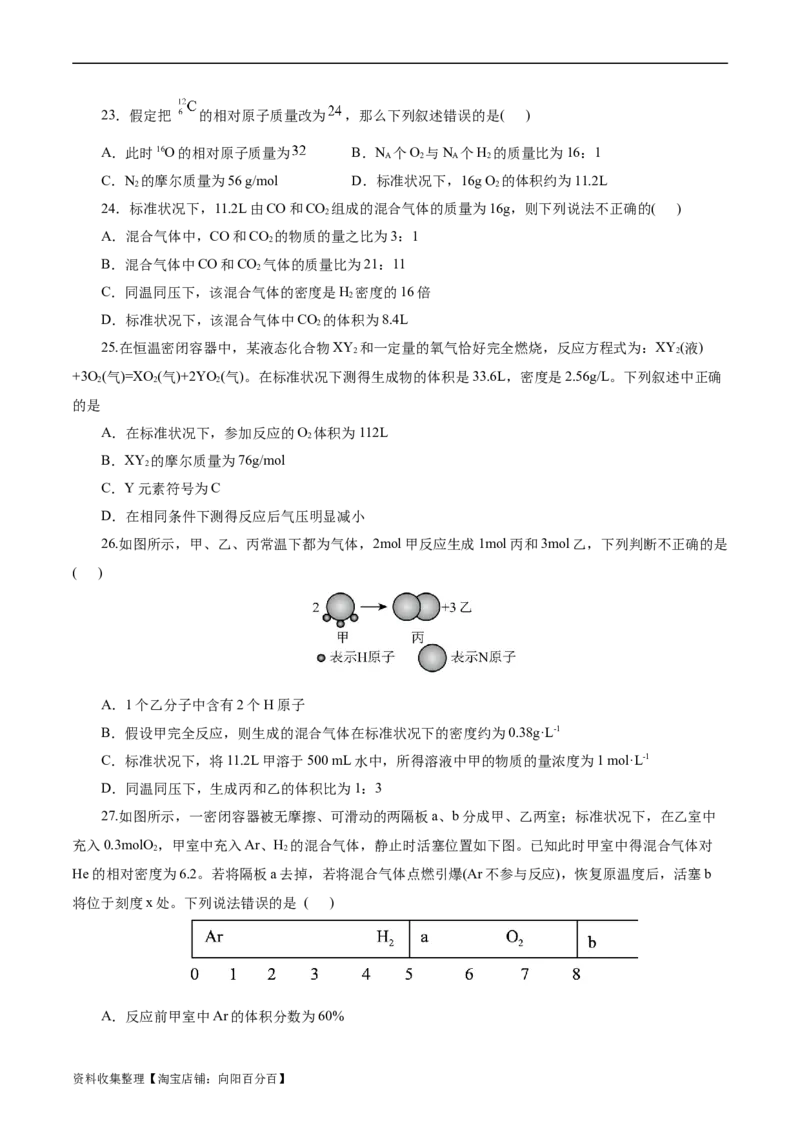
26.如图所示,甲、乙、丙常温下都为气体,2mol甲反应生成1mol丙和3mol乙,下列判断不正确的是
( )
A.1个乙分子中含有2个H原子
B.假设甲完全反应,则生成的混合气体在标准状况下的密度约为0.38g·L-1
C.标准状况下,将11.2L甲溶于500 mL水中,所得溶液中甲的物质的量浓度为1 mol·L-1
D.同温同压下,生成丙和乙的体积比为1:3
27.如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中
充入0.3molO,甲室中充入Ar、H 的混合气体,静止时活塞位置如下图。已知此时甲室中得混合气体对
2 2
He的相对密度为6.2。若将隔板a去掉,若将混合气体点燃引爆(Ar不参与反应),恢复原温度后,活塞b
将位于刻度x处。下列说法错误的是 ( )
A.反应前甲室中Ar的体积分数为60%
资料收集整理【淘宝店铺:向阳百分百】B.X=5
C.反应前甲室与反应后的混合气体的密度比为46:31
D.若将甲室的Ar和乙室的O 进行对换,在反应过程中,a隔板可左右滑动, b隔板始终保持固定,
2
其他条件相同,反应前后的压强比为8:5
28.(2023·山东高三联考)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.25℃, 下, 乙烯分子中 键的数目为2.5N
A
B.浓硝酸热分解生成NO 、NO 共 时,转移电子数为0.5N
2 2 4 A
C. 溶液中, 和 的离子数目之和为0.01N
A
D. 铁完全发生吸氧腐蚀生成铁锈(Fe O· xHO),在电化学过程中转移的电子数为0.3N
2 3 2 A
29.(2023·重庆市高三二诊考试)氨对水体的污染情况越来越受人们的重视。用次氯酸钠可以脱除水中
的NH ,其反应式为:2NH +3NaClO=N +3NaCl+3HO。设N 为阿伏加德罗常数值,下列说法正确的是
2 3 2 2 A
( )
A.33.6L NH 中所含的σ键数目为4.5N
3 A
B.2L 0.5mol/L NaClO溶液中含有的ClO-数目为N
A
C.若该反应生成27g H O时,转移的电子数为3N
2 A
D.2mol N 与3mol H 在密闭容器中反应生成的NH 分子数为2N
2 2 3 A
30.(2023·辽宁省葫芦岛市协作校高三联考)已知在酸性条件下,硫代硫酸钠会发生歧化反应:
HSO +Na SO=Na SO +SO↑+S↓+H O。设N 为阿伏加德罗常数的值,下列说法正确的是( )
2 4 2 2 3 2 4 2 2 A
A.常温常压下,20gDO中含有的氧原子的数目为N
2 A
B.pH=2的HSO 溶液中,含有的H+数目为0.02N
2 4 A
C.常温下,向100mL18mol•L-1浓硫酸中加入足量的Cu,该过程转移电子的数目为1.8N
A
D.32gSO 与足量的O 充分反应,生成的SO 分子总数为0.5N
2 2 3 A
31.(2023·江西省重点中学联盟高三第二次联考)胍盐是新冠病毒核酸保存液的重要成分之一、胍能吸
收空气中的CO ,且在碱性条件下水解为NH 和尿素[CO(NH)]。设N 为阿佛伽德罗常数的值,下列说法
2 3 2 2 A
正确的是( )
A.1mol胍中含有的共用电子对数目为8N
A
B.常温常压下,60g尿素分子中含有C-N键的数目为2N
A
C.22.4L N (标准状况)和足量H 反应,生成NH 分子的数目为2N
2 2 3 A
D.1molCO 和足量NH 合成尿素,转移电子数目为2N
2 3 A
32.(2023·湖北省高三5月适应性考试)在化工生产中常利用某分子筛作催化剂,催化 NH3脱除废气中
资料收集整理【淘宝店铺:向阳百分百】的 和NO ,生成两种无毒物质,其反应历程如图所示。设N 为阿伏伽德罗常数的值,下列说法中正确
2 A
的是( )
A.2L0.5mol·L-1NH Cl溶液中含有NH +的数目为N
4 4 A
B.常温下,4.6g二氧化氮气体中含有的分子数为0.1N
A
C.1mol NH +中含有完全相同的 共价键的数目为3N
4 A
D.总反应中生成11.2LN (标准状况)时转移电子数为1.5N
2 A
33.现有两种金属单质X和Y,取等物质的量的X、Y分别与足量稀硫酸完全反应,同温同压下产生
气体的体积分别为VmL、VmL。下列推断正确的是( )
1 2
A.参与反应的X、Y的质量之比为V:V
2 1
B.X、Y的摩尔质量之比为V:V
1 2
C.反应产物中X、Y对应元素的化合价之比为V:V
1 2
D.X、Y消耗稀硫酸的体积之比为2V:V
1 2
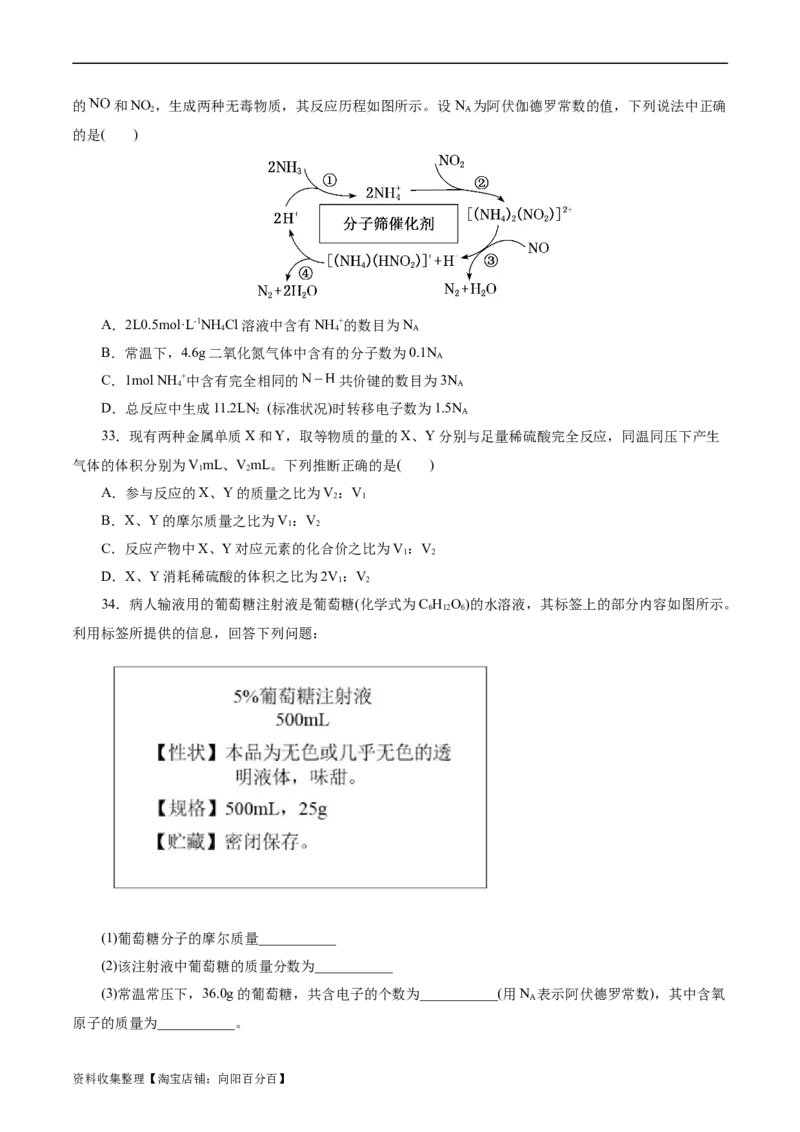
34.病人输液用的葡萄糖注射液是葡萄糖(化学式为C H O)的水溶液,其标签上的部分内容如图所示。
6 12 6
利用标签所提供的信息,回答下列问题:
(1)葡萄糖分子的摩尔质量___________
(2)该注射液中葡萄糖的质量分数为___________
(3)常温常压下,36.0g的葡萄糖,共含电子的个数为___________(用N 表示阿伏德罗常数),其中含氧
A
原子的质量为___________。
资料收集整理【淘宝店铺:向阳百分百】35.下表是某地市场中销售的一种“加碘食盐”包装袋上的部分文字说明:
配料:氯化钠(NaCl)、碘酸钾(KIO )
3
含碘量:20~40mg·kg-1
保质期:18个月
食用方法:勿长时间炖炒
储藏方法:避热、避光、防潮
(1)加碘盐不能长时间炖炒,且应避热、避光保存,你认为可能的原因是_______。
(2)实验分析发现,某批加碘盐中KIO 的含量为52mg·kg-1。计算每千克加碘盐中KIO 的物质的量
3 3
_______和碘的质量_______。
(3)若成人每天需摄入0.15~0.20mg碘才能满足人体健康需要,通过计算说明成人平均每天食用6.0g这
种加碘盐能否获得需要的碘_______。
36.甲烷(CH)是一种高效清洁能源,见天然气的主要成分。2017年我国在南海海域首次发现裸露的可
4
燃冰,可燃冰是天然气水合物晶体,假设可燃冰的水笼里装的都是甲烷,理想的甲烷水合物的化学式为
CH·8H O。请回答下列问题:
4 2
(1)甲烷水合物(CH·8H O)的摩尔质量为___________,其中质量分数最大的元素为___________(填元素
4 2
符号)。
(2)含有4.214×1024个氢原子的CH 的物质的量为___________mol,质量为___________ g
4
(3)含0.2N 个氢原子的CH,在标准状况下的体积约为___________ L
A 4
(4)常温常压下,等质量的CH 和H 的体积之比V(CH ):V(H )=___________,前者所含氢原子个数与
4 2 4 2
后者所含氢原子个数之比为___________
资料收集整理【淘宝店铺:向阳百分百】