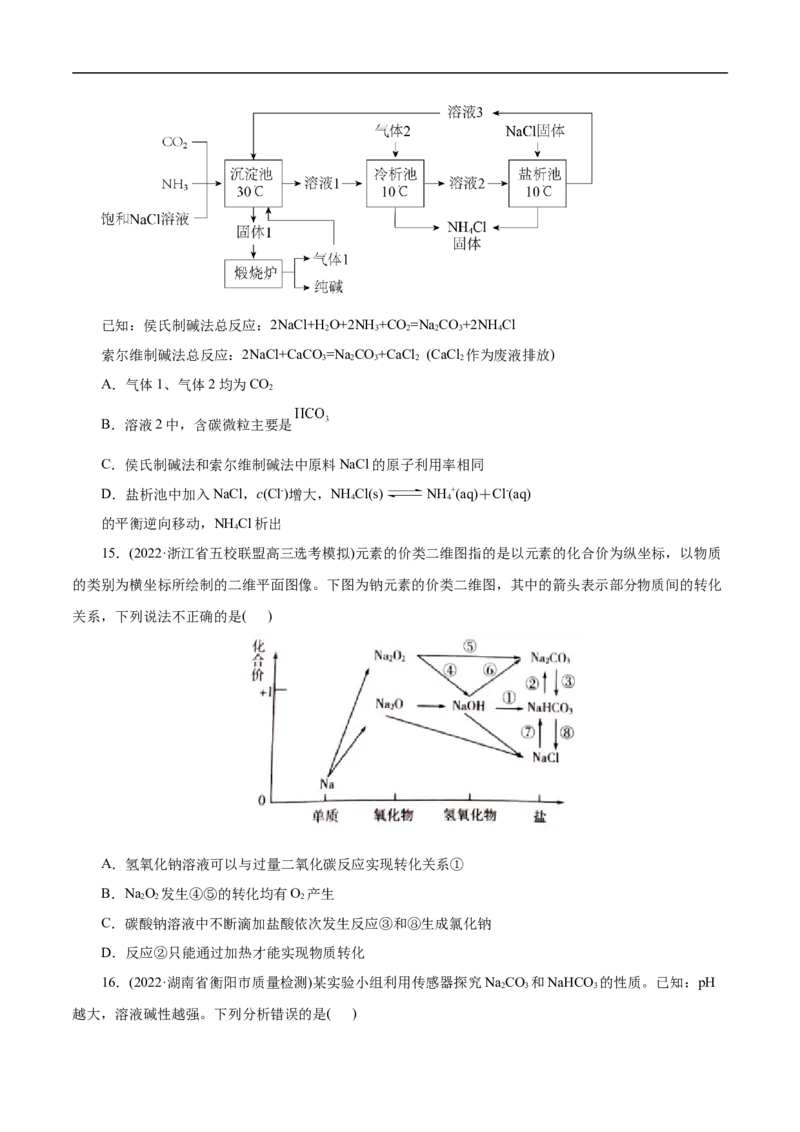
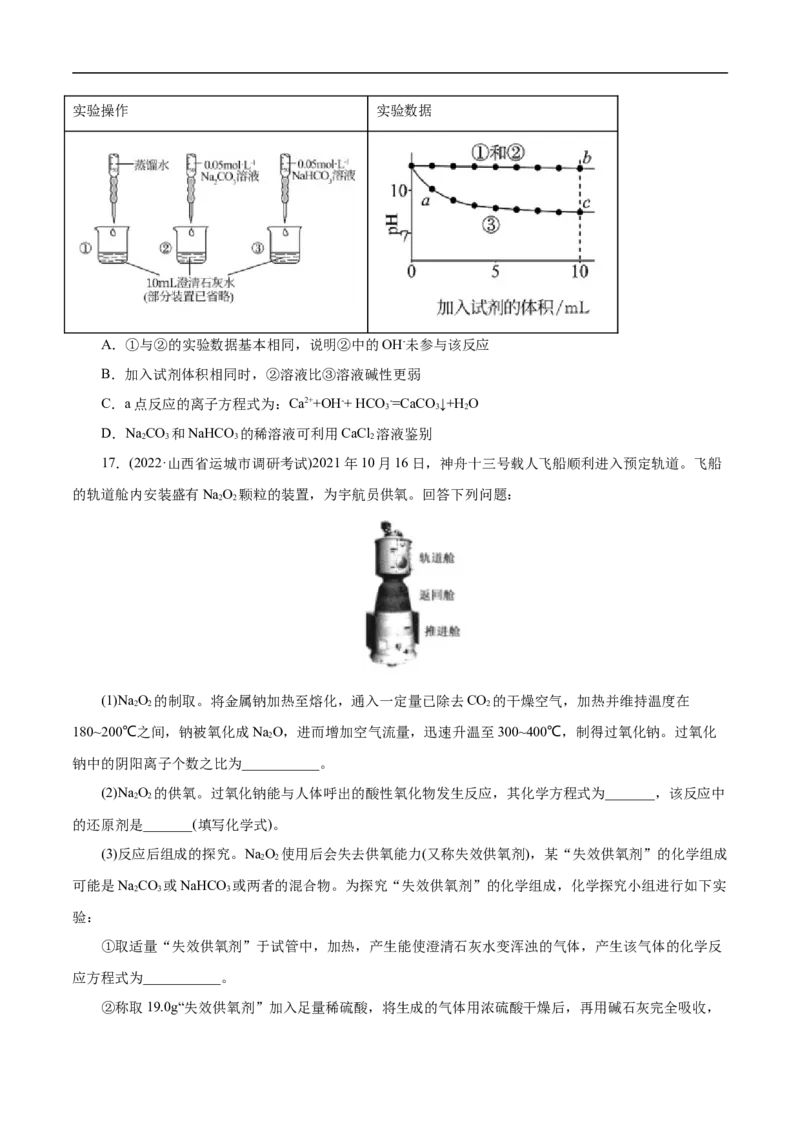
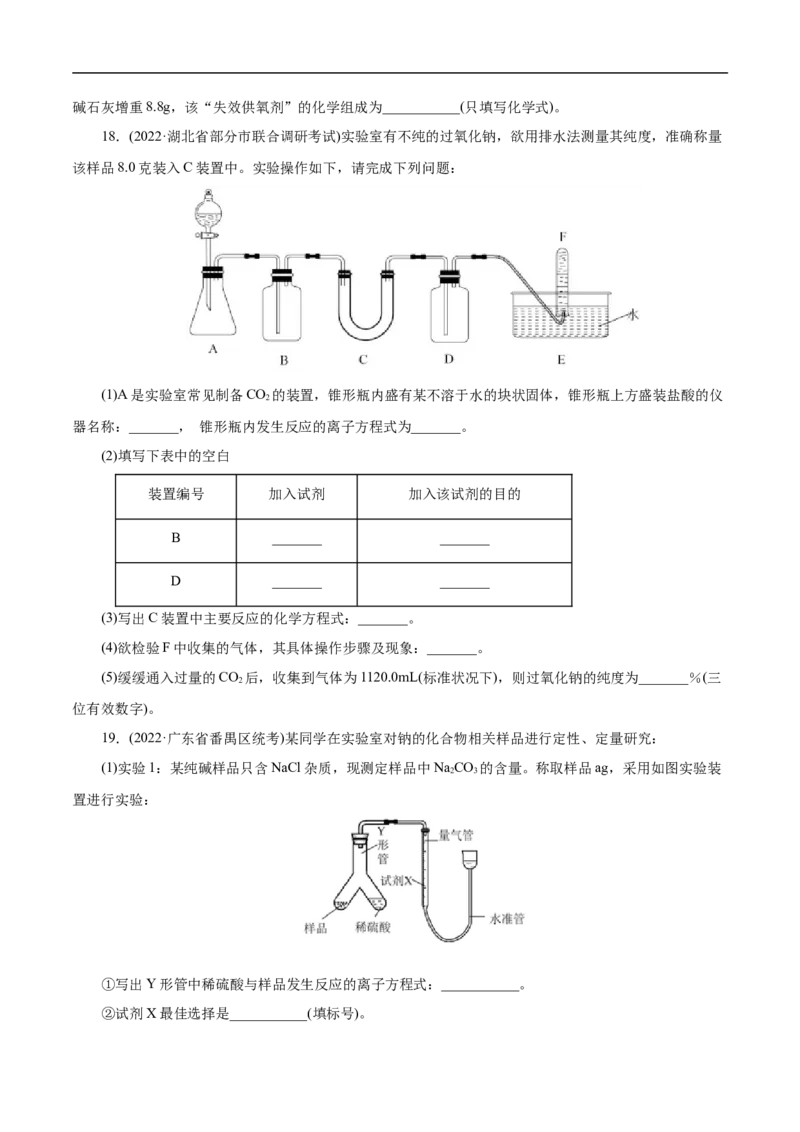
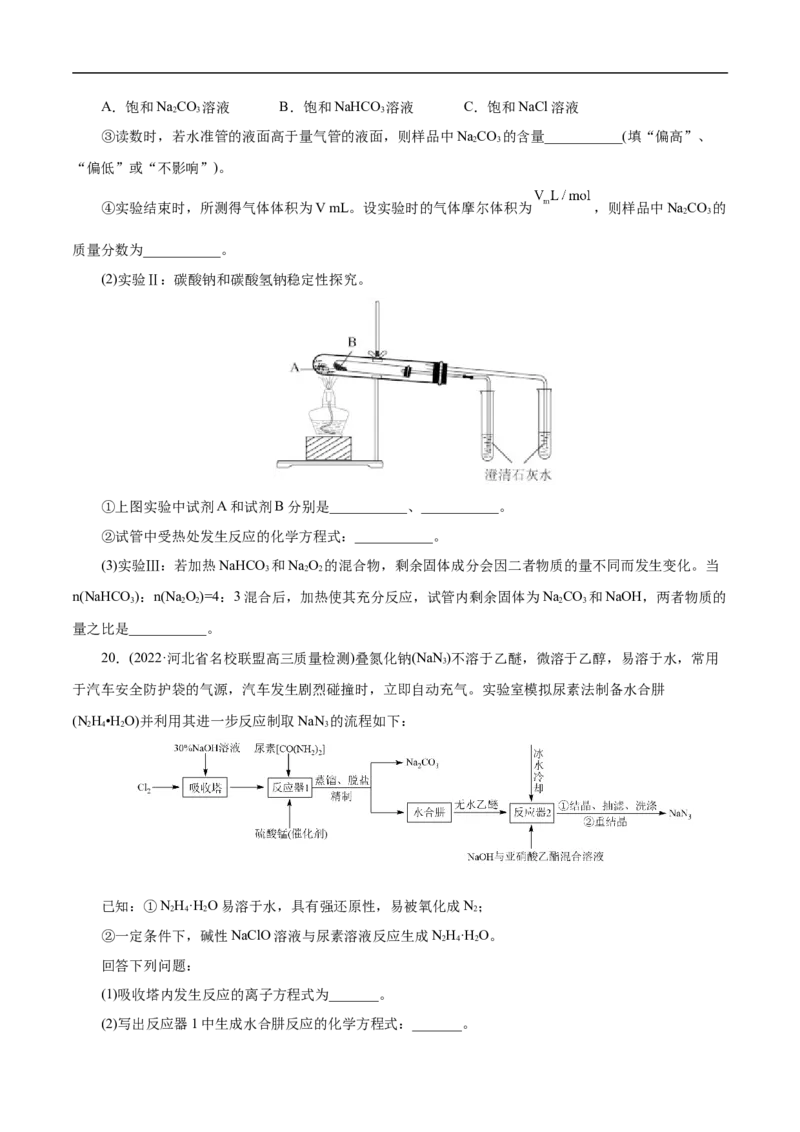
文档内容
考点 13 钠及其化合物
本专题一般与其他专题内容结合起来进行考查,常以一个选项或一个填空的形式考查钠与过氧化钠的
性质、碳酸钠与碳酸氢钠的鉴别及有关计算。
预测2023年高考对本专题的考查特点不变,直接出现大题的可能性不大,但有考查迁移能力的可能性,
考查物质的结构与性质(如钠的活泼性、过氧化钠的结构与性质、碳酸氢钠的热不稳定性)的选择题出现概
率较大。
一、钠的性质
二、钠的氧化物、氢氧化物
三、碳酸钠与碳酸氢钠
钠的性质
1.钠的物理性质
银白色,有金属光泽的固体,质地柔软,熔点低(小于100 ℃),密度比水的小,但比煤油的大。
2.从钠原子的原子结构认识钠的化学性质——还原性
Na ―――――――――→Na+
(1)与非金属单质(如O、Cl)的反应
2 2
O
2
Cl:2Na+Cl=====2NaCl
2 2
(2)与水反应
①离子方程式:2Na+2HO===2Na++2OH-+H↑。
2 2
②与滴加酚酞的水反应的现象及解释(3)与盐酸反应
离子方程式:2Na+2H+===2Na++H↑。
2
3.钠的制取及保存
(1)制取:化学方程式为2NaCl(熔融)=====2Na+Cl↑。
2
(2)保存:密封保存,通常保存在石蜡油或煤油中。
4.钠的用途
(1)钠钾合金(液态)可用于原子反应堆的导热剂。
(2)用作电光源,制作高压钠灯。
(3)冶炼某些金属
金属钠具有强还原性,熔融状态下可以用于制取金属,如4Na+TiCl =====4NaCl+Ti。
4
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)在氧气中加热时,金属钠剧烈燃烧,生成淡黄色的固体NaO( )
2 2
(2)金属钠着火时,可用泡沫灭火器或干燥的沙土灭火( )
(3)钠表面自然形成的氧化层能够保护内层金属不被空气氧化( )
(4)金属钠具有强还原性,可与TiCl 溶液反应制取金属Ti( )
4
(5)根据反应Na+KCl NaCl+K↑,知Na的金属性强于K( )
(6)实验完毕后剩余的金属钠不能随意丢弃,应放回原试剂瓶( )
(7)ⅠA族元素又称碱金属元素( )
(8)钠、氧化钠、碳酸钠的焰色反应均显黄色( )
(9)把一小块金属钠放入饱和NaOH溶液中:有气体放出,恢复至室温后溶液的pH增大( )
(10)把一小块金属钠放入稀CuSO 溶液中:有气体放出,有紫红色铜析出( )
4
【典例】
例1 下列关于金属钠的叙述中,说法正确的是( )
A.钠在空气中燃烧,发出黄色火焰 B.钠在空气中燃烧,产物是NaO
2
C.钠是银白色金属,硬度大,熔点高 D.取用金属钠时,剩余的钠不能放回原瓶
【答案】A
【解析】A项,钠的焰色为黄色,所以钠在空气中燃烧时,产生黄色火焰,A正确;B项,钠在空气
中燃烧,产物是NaO,B不正确;C项,钠是银白色金属,硬度小,熔点较低,C不正确;D项,钠为块
2 2状固体,取用金属钠时,剩余的钠应放回原瓶,D不正确;故选A。
例2 等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法
正确的是( )
A.第一块钠失去电子多 B.两块钠失去电子一样多
C.第二块钠的反应产物质量最大 D.两块钠的反应产物质量一样大
【答案】B
【解析】金属钠失电子均变为+1价的阳离子,等质量的两块钠,失电子是一样的。根据4Na+
O===2Na O,则1 mol 金属钠完全反应得氧化钠的质量是31 g,根据反应2Na+O=====NaO ,则1 mol
2 2 2 2 2
金属钠完全反应得过氧化钠的质量是39 g,等质量的两块钠,即金属钠的物质的量是相等的,所以生成过
氧化钠的质量大,即第一块钠的反应产物质量大。
【对点提升】
对点1 下列对金属钠的叙述正确的是( )
A.少量金属钠应该保存在煤油中
B.金属钠在空气中燃烧,生成NaO
2
C.火灾现场有大量金属钠存放时,可用水灭火
D.将一小粒金属钠放入硫酸铜溶液中,可置换出铜
对点2 向分别盛有100 mL水、100 mL 0.1 mol·L-1盐酸、100 mL 0.01 mol·L-1NaOH溶液的X、Y、Z
三个烧杯中各投入0.05 mol Na。下列有关说法正确的是( )
A.三个烧杯中均先发生的离子反应为
2Na+2HO===2Na++2OH-+H↑
2 2
B.三个烧杯中钠均在液面上剧烈反应,且X烧杯中的反应最剧烈
C.三个烧杯反应后,溶质的物质的量浓度相同
D.三个烧杯反应后,生成的气体的质量一定相同
【巧学妙记】
(1)钠与水、酸反应的实质都是与H+的反应。
(2)钠与乙醇反应的特点——慢、沉
钠与乙醇反应,钠块先沉在液面下,后上下浮动、能看到表面冒出气泡,并不能熔化成小球。
(3)钠与酸反应的特点——快,可能燃烧或爆炸。
钠的氧化物、氢氧化钠
1.氧化钠与过氧化钠的比较
NaO NaO
2 2 2电子式
氧元素化合价 -2 -1
色、态 白色固体 淡黄色固体
阴、阳离子个数比 1∶2 1∶2
是否为碱性氧化物 是 不是
与水反应 NaO+HO===2NaOH 2NaO+2HO===4NaOH+O↑
2 2 2 2 2 2
与CO 反应 NaO+CO===Na CO 2NaO+2CO===2Na CO+O
2 2 2 2 3 2 2 2 2 3 2
与盐酸反应 NaO+2HCl===2NaCl+HO 2NaO+4HCl===4NaCl+2HO+O↑
2 2 2 2 2 2
用途 氧化剂、供氧剂、漂白剂
2.氢氧化钠
(1)物理性质:NaOH的俗名为烧碱、火碱或苛性钠;它是一种白色固体,易溶于水并放出大量的热,
有吸水性;吸收空气中的水分而潮解;有很强的腐蚀性。
(2)化学性质
①具有碱的通性
②其他反应
与金属铝反应:2Al+2OH-+6HO===2Na[Al(OH) ]+3H↑
2 4 2
与非金属单质反应:Cl+2OH-===Cl-+ClO-+HO
2 2
酯类水解:CHCOOC H+NaOH――→CHCOONa+CHCHOH
3 2 5 3 3 2
(3)NaOH的制取
①土法制碱:NaCO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
②现代工业制碱:2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)烧碱、纯碱均属于碱,不能盛放在玻璃试剂瓶中( )
(2)NaOH在空气中久置,最终变为NaCO( )
2 3
(3)氧化钠、过氧化钠均为离子化合物( )
(4)1 mol Na O 固体中含离子总数为4N ( )
2 2 A
(5)H O 和NaO 都属于过氧化物,含有的化学键完全相同( )
2 2 2 2
(6)7.8 g过氧化钠含有的共用电子对数为0.2N ( )
A
(7)Na O 遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色( )
2 2
(8)Na O 与CO 反应生成0.1 mol O 时转移电子数目为0.4 mol( )
2 2 2 2
(9)Na O 投入到CuCl 溶液中有蓝色沉淀及气泡产生( )
2 2 2
(10)向饱和烧碱溶液中加入2 g Na O 充分反应完时,溶液中c(Na+)不变( )
2 2
【典例】
例1 下列不是NaO和NaO 的共同之处是( )
2 2 2A.均是碱性氧化物 B.均能与水反应生成碱
C.阴阳离子的个数比均为1:2 D.均能与CO 反应生成NaCO
2 2 3
【答案】A
【解析】A项,过氧化钠属于过氧化物不属于碱性氧化物,A选;B项,过氧化钠和氧化钠都可以与
水反应生成氢氧化钠,B不选;C项,氧化钠和过氧化钠的阴离子分别为O2-、O2-,阳离子为钠离子,故
2
阴阳离子的个数比均为1:2,C不选;D项,氧化钠和过氧化钠均能与二氧化碳生成碳酸钠,D不选。故
选A。
例2 下列有关NaO 的说法不正确的是( )
2 2
A.向包有NaO 粉末的脱脂棉上滴加几滴水,脱脂棉剧烈燃烧起来,说明NaO 与HO反应放热且有
2 2 2 2 2
氧气生成
B.NaO 与CO 反应时有单质O 生成,该反应属于置换反应
2 2 2 2
C.NaO 在空气中久置变白,涉及的氧化还原反应中,NaO 既是氧化剂,又是还原剂
2 2 2 2
D.NaO 粉末加入Ca(HCO ) 溶液中,会产生气体和浑浊
2 2 3 2
【答案】B
【解析】A项,燃烧的条件是达到着火点和具有助燃物质;B项,反应物中没有单质参加反应,不符
合置换反应的定义;C项,NaO 与CO 、HO的反应都是NaO 自身的氧化还原反应;D项,NaO 先和
2 2 2 2 2 2 2 2
水反应生成O 和NaOH,NaOH再与Ca(HCO ) 反应产生沉淀CaCO 。
2 3 2 3
【对点提升】
对点1 对NaO 与CO 和HO(g)混合气体的反应来说,下列说法错误的是( )
2 2 2 2
A.只要参加反应的NaO 一定,反应生成的氧气就一定
2 2
B.只要CO 和HO(g)的总的物质的量一定,反应所消耗的NaO 的量就一定
2 2 2 2
C.只要气体的总物质的量一定,反应中所转移的电子的物质的量就一定
D.只要混合气体的总物质的量一定,固体所增加的质量就一定
对点2 在一密闭容器中有CO、H 、O 共16.5 g和足量的NaO ,用电火花引燃,使其完全反应,
2 2 2 2
NaO 增重7.5 g,则原混合气体中O 的质量分数是( )
2 2 2
A.54.5% B.40% C.36% D.33.3%
【巧学妙记】
(1)金属钠露置在空气中会发生一系列变化,其过程:银白色金属钠――→表面变暗――→出现白色固
体接着表面变稀――→白色块状固体――→白色粉末状物质。
(2)Na O 中既有离子键又有共价键,过氧化钠的电子式为
2 2
NaO 与HO、CO 的反应规律
2 2 2 2
电子转移关系 当NaO 与CO 、HO反应时,物质的量的关系为2NaO ~O ~2e
2 2 2 2 2 2 2-,n(e-)=n(Na O)=2n(O )
2 2 2
CO 、水蒸气(或两混合气体)通过足量NaO 时,气体体积的减少量
2 2 2
气体体积变化关系
是原来气体体积的,等于生成氧气的量,即ΔV=V(O )=V(混合)
2
CO 、水蒸气分别与足量NaO 反应时,固体相当于吸收了CO 中的
2 2 2 2
固体质量变化关系 “CO”、水蒸气中的“H”,所以固体增加的质量Δm(CO)=
2 2
28 g·mol-1×n(CO),Δm(H O)=2 g·mol-1×n(H O)
2 2 2
碳酸钠与碳酸氢钠
1.NaCO 和NaHCO 的性质
2 3 3
2.转化关系
NaCO NaHCO
2 3 3
3.NaCO 和NaHCO 性质的应用
2 3 3
(1)Na CO、NaHCO 的鉴别
2 3 3
①固体的鉴别用加热法:产生使澄清石灰水变浑浊的气体的是NaHCO 固体。
3
②溶液的鉴别可用沉淀法、气体法和测pH法。
a.沉淀法:加入BaCl 溶液或CaCl 溶液,产生沉淀的是NaCO 溶液。
2 2 2 3
b.气体法:滴入稀盐酸,立即产生气泡的是NaHCO 溶液。
3
c.测pH法:用pH试纸测相同浓度的稀溶液,pH大的是NaCO 溶液。
2 3
(2)Na CO、NaHCO 的除杂
2 3 3
序号 混合物(括号内为杂质) 除杂方法
① NaCO(s)(NaHCO ) 加热法
2 3 3
② NaHCO (aq)(Na CO) 通入足量CO
3 2 3 2
③ NaCO(aq)(NaHCO ) 滴加适量NaOH溶液
2 3 3【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)在酒精灯加热条件下,NaCO、NaHCO 固体都会分解( )
2 3 3
(2)向NaCO 饱和溶液中通入足量CO,会有NaHCO 晶体析出( )
2 3 2 3
(3)用酚酞溶液可鉴别饱和食盐水和饱和碳酸钠溶液( )
(4)将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡( )
(5)用热的纯碱溶液清洗炊具上的油污时,不涉及化学变化( )
【典例】
例1 下列有关NaCO 和NaHCO 比较中,不正确的是( )
2 3 3
A.热稳定性:NaCO>NaHCO
2 3 3
B.相同温度下,0.1 mol·L-1盐溶液的pH:NaCO>NaHCO
2 3 3
C.等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应放出气体的量:NaCONaHCO
2 3 3
【答案】D
【解析】A 项,NaHCO 受热易分解,NaCO 受热不分解;B 项,相同条件下,pH:
3 2 3
NaCO>NaHCO ;C项,相同质量时,碳酸氢钠的物质的量大,故 C正确;D项,NaHCO 与盐酸反应一
2 3 3 3
步完成,而NaCO 与盐酸反应分两步进行,相同条件下NaHCO 比NaCO 反应放出气体剧烈,故D错误。
2 3 3 2 3
例2 有两试管分别装有等物质的量浓度的NaCO 和NaHCO 溶液,下列操作或判断正确的是( )
2 3 3
选项 操作 判断
A 分别加入澄清石灰水 产生沉淀者为NaCO
2 3
B 分别加入等浓度的稀盐酸 反应较剧烈者为NaCO
2 3
C 分别加入CaCl 溶液 产生沉淀者为NaCO
2 2 3
D 逐滴加入等浓度的盐酸 立即产生气泡者为NaCO
2 3
【答案】C
【解析】A项,发生的反应分别为NaCO+Ca(OH) =CaCO ↓+2NaOH,2NaHCO +Ca(OH) =CaCO ↓
2 3 2 3 3 2 3
+NaCO+2HO,两者现象相同(都产生白色沉淀),故A错误;B项,加入等浓度的稀盐酸时,NaHCO
2 3 2 3
溶液反应更剧烈,故B错误;C项,NaCO 与CaCl 发生反应:NaCO+CaCl =CaCO ↓+2NaCl,产生白
2 3 2 2 3 2 3
色沉淀,NaHCO 与CaCl 不反应,故C正确;D项,逐滴加入等浓度的盐酸时,NaHCO 立即产生气泡,
3 2 3
NaCO 开始无气泡产生,过一会儿才产生气泡,故D错误;故选C。
2 3
【对点提升】
对点1 有关NaHCO 和NaCO 的性质,以下叙述错误的是( )
3 2 3A.等质量的NaHCO 和NaCO 与足量盐酸反应,在相同条件下NaCO 产生的CO 体积小
3 2 3 2 3 2
B.等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积NaCO 是NaHCO 的两倍
2 3 3
C.等质量NaHCO 和NaCO 与盐酸完全反应,前者消耗盐酸较多
3 2 3
D.等物质的量的NaHCO 和NaCO 与足量盐酸反应产生CO 一样多
3 2 3 2
对点2 为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W g样品进行实验,下列
实验方法所对应的实验方案和测量数据合理的是( )
选项 实验方法 实验方案 测量数据
将样品配成100 mL溶液,取10 mL,加入
A 滴定法 消耗盐酸的体积
酚酞,用标准盐酸滴定
将样品与盐酸反应,生成的气体全部被碱石
B 量气法 碱石灰增加的质量
灰吸收
将样品放入烧瓶中,置于电子天平上,加入
C 重量法 减少的质量
足量盐酸
将样品与盐酸反应,气体通过排水量气装置
D 量气法 排出水的体积
量气
【巧学妙记】
1.依据图像特点判断溶液溶质成分的方法
若a=0(即图像从原点开始) 溶液中的溶质为NaHCO
3
若V(Oa)=V(ab)(即Oa段与ab段消耗盐酸的体积相同) 溶液中的溶质为NaCO
2 3
若V(Oa)>V(ab)(即Oa段消耗盐酸的体积大于ab段消耗 溶 液 中 的 溶 质 为 NaCO 和
2 3
盐酸的体积) NaOH
若V(Oa)