文档内容
考点 18 原电池 化学电源
化学电池是当今世界广泛用于供能的重要装置,属于考生应该掌握的知识。高考有关原电池的考查一
直是常考常新,设题背景新、设问角度新、解答方式新。虽电池的种类多样,但主要考查原电池的基本工
作原理,着重考查考生对原理的迁移应用能力。命题在选择题中,常以新型电池的形式对原电池的工作原
理进行考查;在非选择题中,常结合元素化合物、物质的分离和提纯等知识,考查电极反应式的书写,以
及利用电子守恒进行相关计算。
预测2023年高考仍然会以新型电池为切入点,考查原电池的工作原理及应用、电极反应式的书写及判
断、溶液中离子的迁移及浓度变化、二次电池的充放电过程分析以及其他有关问题。备考时注重实物图分
析、新型电池分析,从氧化还原反应的角度认识电化学,注重与元素化合物、有机化学、电解质溶液、化
学实验设计、新能源等知识的联系。通过原电池装置的应用,能对与化学有关的热点问题作出正确的价值
判断,能参与有关化学问题的社会实践。
一、原电池的工作原理
二、化学电源
原电池的工作原理
1.概念和反应本质
原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应。
2.构成条件
(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)。
(2)二看两电极:一般是活泼性不同的两电极。
(3)三看是否形成闭合回路,形成闭合回路需三个条件:①电解质溶液;②两电极直接或间接接触;③
两电极插入电解质溶液中。
3.工作原理
以锌铜原电池为例(1)反应原理
电极名称 负极 正极
电极材料 锌片 铜片
电极反应 Zn-2e-===Zn2+ Cu2++2e-===Cu
反应类型 氧化反应 还原反应
电子流向 由Zn片沿导线流向Cu片
盐桥中离子移向 盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极
(2)盐桥的组成和作用
①盐桥中装有饱和的KCl、NH NO 等溶液和琼胶制成的胶冻。
4 3
②盐桥的作用:A.连接内电路,形成闭合回路;B.平衡电荷,使原电池不断产生电流。
4.原电池原理的应用
(1)比较金属的活动性强弱:原电池中,负极一般是活动性较强的金属,正极一般是活动性较弱的金属
(或非金属)。
(2)加快化学反应速率:氧化还原反应形成原电池时,反应速率加快。
(3)用于金属的防护:将需要保护的金属制品作原电池的正极而受到保护。
(4)设计制作化学电源
①首先将氧化还原反应分成两个半反应。
②根据原电池的工作原理,结合两个半反应,选择正、负电极材料以及电解质溶液。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)理论上,任何自发的氧化还原反应都可设计成原电池( )
(2)在原电池中,发生氧化反应的一极一定是负极( )
(3)在锌铜原电池中,因为有电子通过电解质溶液形成闭合回路,所以有电流产生( )
(4)在原电池中,负极材料的活泼性一定比正极材料强( )
(5)在原电池中,正极本身一定不参与电极反应,负极本身一定要发生氧化反应( )
(6)在锌铜原电池中,因为有电子通过电解质溶液形成闭合回路,所以有电流产生( )
(7)两种活泼性不同的金属组成原电池的两极,活泼金属一定作负极( )
(8)原电池工作时,溶液中的阳离子向负极移动,盐桥中的阳离子向正极移动( )(9)两种活泼性不同的金属组成原电池的两极,活泼金属一定做负极( )
(10)一般来说,带有“盐桥”的原电池比不带“盐桥”的原电池效率高( )
答案:(1)√ (2)√ (3)× (4)× (5)× (6)× (7)× (8)× (9)× (10)√
【典例】
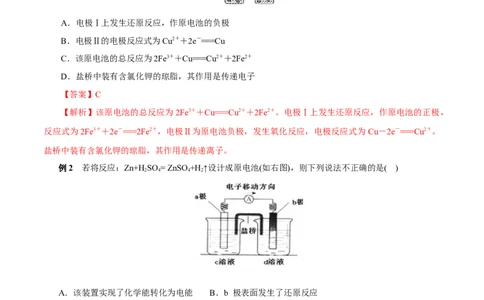
例1 如图是某同学设计的原电池装置,下列叙述中正确的是( )
A.电极Ⅰ上发生还原反应,作原电池的负极
B.电极Ⅱ的电极反应式为Cu2++2e-===Cu
C.该原电池的总反应为2Fe3++Cu===Cu2++2Fe2+
D.盐桥中装有含氯化钾的琼脂,其作用是传递电子
【答案】C
【解析】该原电池的总反应为2Fe3++Cu===Cu2++2Fe2+。电极Ⅰ上发生还原反应,作原电池的正极,
反应式为2Fe3++2e-===2Fe2+,电极Ⅱ为原电池负极,发生氧化反应,电极反应式为 Cu-2e-===Cu2+。
盐桥中装有含氯化钾的琼脂,其作用是传递离子。
例2 若将反应:Zn+H SO = ZnSO+H ↑设计成原电池(如右图),则下列说法不正确的是( )
2 4 4 2
A.该装置实现了化学能转化为电能 B.b 极表面发生了还原反应
C.c 溶液可以是ZnSO 溶液 D.盐桥中的Cl-移向右边烧杯
4
【答案】D
【解析】A项,形成原电池,是化学能变成电能,正确,不选A;B项,根据电子移动方向确定,说明
a为负极,b为正极,发生还原反应,正确,不选B;C项,锌做原电池的负极,所以c为硫酸锌,正确,
不选C;D项,盐桥中氯离子向负极移动,即向左侧烧杯移动,错误,选D。
【对点提升】
对点1 如图所示,在盛有稀HSO 的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所
2 4示,关于该装置的下列说法正确的是( )
A.外电路的电流方向为:X→外电路→Y
B.若两电极分别为Fe和碳棒,则X为碳棒,Y为Fe
C.X极上发生的是还原反应,Y极上发生的是氧化反应
D.若两电极都是金属,则它们的活动性顺序为X>Y
【答案】D
【解析】外电路的电子流向为X→外电路→Y,电流方向与其相反,A项错误;若两电极分别为Fe和
碳棒,则Y为碳棒,X为Fe,B项错误;X极失电子,作负极,Y极上发生的是还原反应,X极上发生的
是氧化反应,C项错误;电解质溶液为稀硫酸,两金属作电极,谁活泼谁作负极,D项正确。
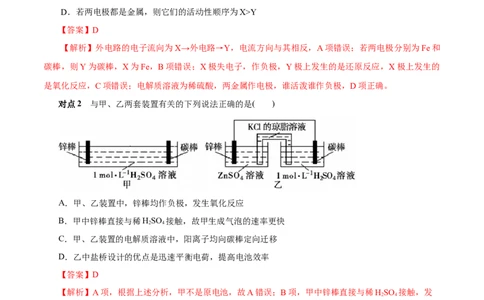
对点2 与甲、乙两套装置有关的下列说法正确的是( )
A.甲、乙装置中,锌棒均作负极,发生氧化反应
B.甲中锌棒直接与稀HSO 接触,故甲生成气泡的速率更快
2 4
C.甲、乙装置的电解质溶液中,阳离子均向碳棒定向迁移
D.乙中盐桥设计的优点是迅速平衡电荷,提高电池效率
【答案】D
【解析】A项,根据上述分析,甲不是原电池,故A错误;B项,甲中锌棒直接与稀HSO 接触,发
2 4
生化学腐蚀,乙中构成了原电池,负极失去电子的速率加快,因此正极放出氢气的速率增大,故B错误;
C项,甲不是原电池,电解质溶液中的阳离子向锌移动,故C错误;D项,盐桥中离子的定向迁移构成了
电流通路,盐桥既可沟通两方溶液,又能阻止反应物的直接接触,迅速平衡电荷,使由它连接的两溶液保
持电中性,提高电池效率,故D正确。
【巧学妙记】
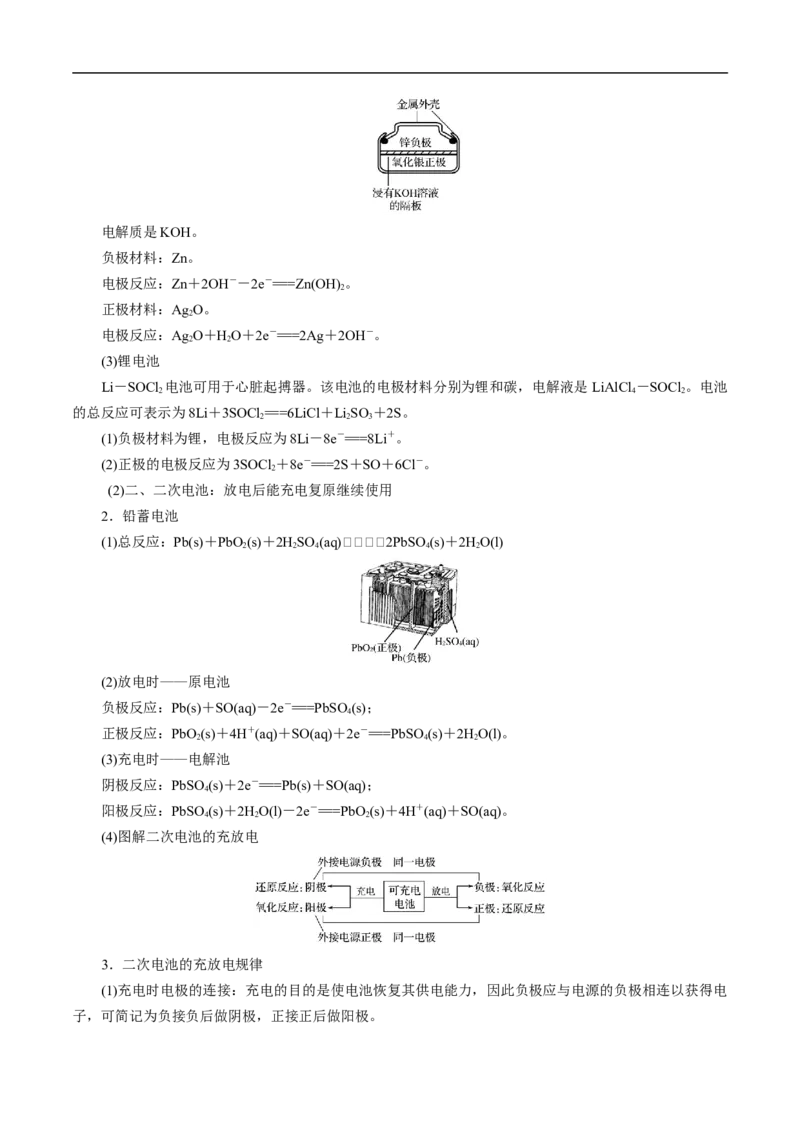
1.原电池的工作原理简图注意:
①电子移动方向:从负极流出沿导线流入正极,电子不能通过电解质溶液。
②若有盐桥,盐桥中的阴离子移向负极区,阳离子移向正极区。
③若有交换膜,离子可选择性通过交换膜,如阳离子交换膜,阳离子可通过交换膜移向正极。
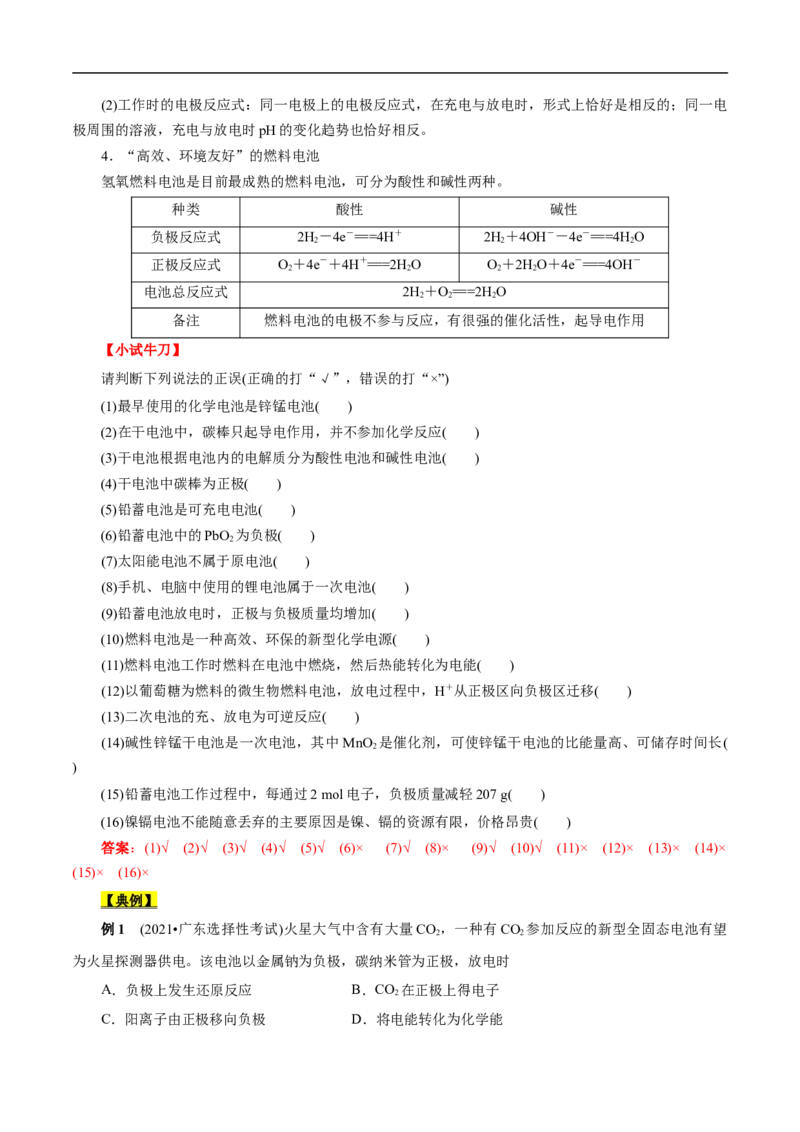
2.判断原电池正、负极的5种方法
化学电源
1.一次电池:只能使用一次,不能充电复原继续使用
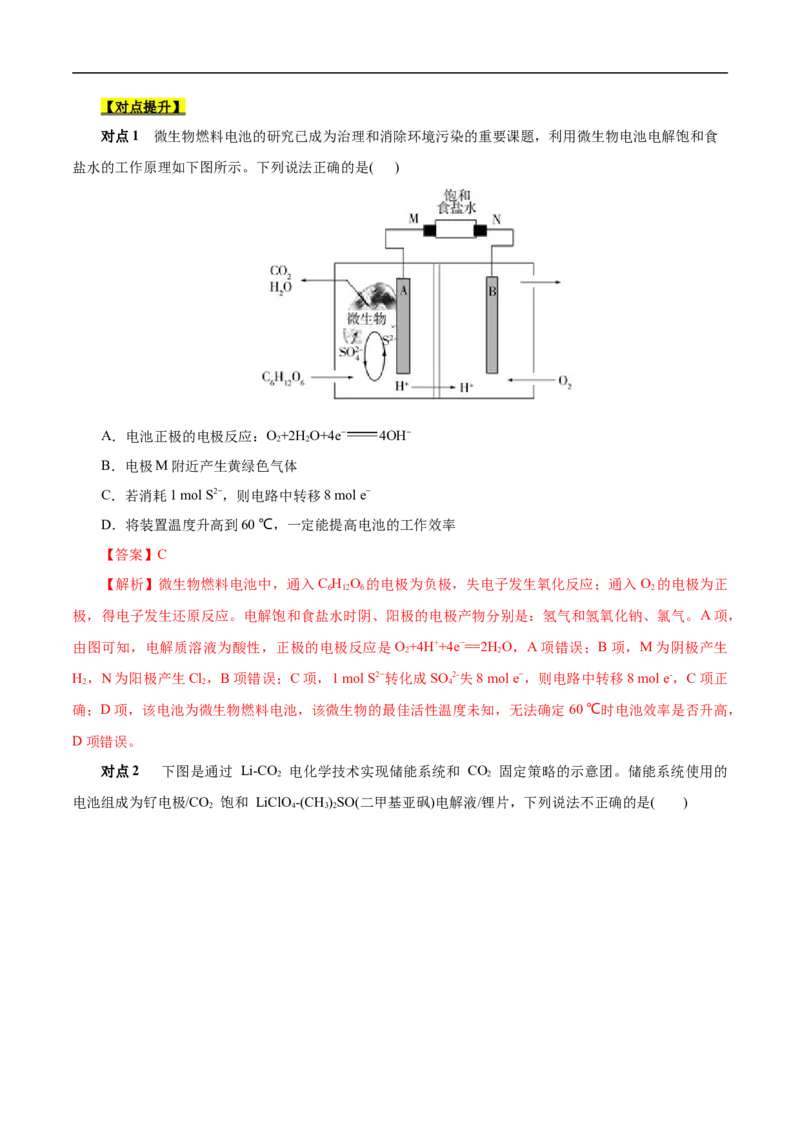
(1)碱性锌锰干电池
总反应:Zn+2MnO +2HO===2MnOOH+Zn(OH) 。
2 2 2
负极材料:Zn。
电极反应:Zn+2OH--2e-===Zn(OH) 。
2
正极材料:碳棒。
电极反应:2MnO +2HO+2e-===2MnOOH+2OH-。
2 2
(2)纽扣式锌银电池
总反应:Zn+Ag O+HO===Zn(OH) +2Ag。
2 2 2电解质是KOH。
负极材料:Zn。
电极反应:Zn+2OH--2e-===Zn(OH) 。
2
正极材料:Ag O。
2
电极反应:Ag O+HO+2e-===2Ag+2OH-。
2 2
(3)锂电池
Li-SOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl -SOCl 。电池
2 4 2
的总反应可表示为8Li+3SOCl ===6LiCl+LiSO +2S。
2 2 3
(1)负极材料为锂,电极反应为8Li-8e-===8Li+。
(2)正极的电极反应为3SOCl +8e-===2S+SO+6Cl-。
2
(2)二、二次电池:放电后能充电复原继续使用
2.铅蓄电池
(1)总反应:Pb(s)+PbO (s)+2HSO (aq)2PbSO (s)+2HO(l)
2 2 4 4 2
(2)放电时——原电池
负极反应:Pb(s)+SO(aq)-2e-===PbSO(s);
4
正极反应:PbO (s)+4H+(aq)+SO(aq)+2e-===PbSO(s)+2HO(l)。
2 4 2
(3)充电时——电解池
阴极反应:PbSO (s)+2e-===Pb(s)+SO(aq);
4
阳极反应:PbSO (s)+2HO(l)-2e-===PbO(s)+4H+(aq)+SO(aq)。
4 2 2
(4)图解二次电池的充放电
3.二次电池的充放电规律
(1)充电时电极的连接:充电的目的是使电池恢复其供电能力,因此负极应与电源的负极相连以获得电
子,可简记为负接负后做阴极,正接正后做阳极。(2)工作时的电极反应式:同一电极上的电极反应式,在充电与放电时,形式上恰好是相反的;同一电
极周围的溶液,充电与放电时pH的变化趋势也恰好相反。
4.“高效、环境友好”的燃料电池
氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种。
种类 酸性 碱性
负极反应式 2H-4e-===4H+ 2H+4OH--4e-===4H O
2 2 2
正极反应式 O+4e-+4H+===2H O O+2HO+4e-===4OH-
2 2 2 2
电池总反应式 2H+O===2H O
2 2 2
备注 燃料电池的电极不参与反应,有很强的催化活性,起导电作用
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)最早使用的化学电池是锌锰电池( )
(2)在干电池中,碳棒只起导电作用,并不参加化学反应( )
(3)干电池根据电池内的电解质分为酸性电池和碱性电池( )
(4)干电池中碳棒为正极( )
(5)铅蓄电池是可充电电池( )
(6)铅蓄电池中的PbO 为负极( )
2
(7)太阳能电池不属于原电池( )
(8)手机、电脑中使用的锂电池属于一次电池( )
(9)铅蓄电池放电时,正极与负极质量均增加( )
(10)燃料电池是一种高效、环保的新型化学电源( )
(11)燃料电池工作时燃料在电池中燃烧,然后热能转化为电能( )
(12)以葡萄糖为燃料的微生物燃料电池,放电过程中,H+从正极区向负极区迁移( )
(13)二次电池的充、放电为可逆反应( )
(14)碱性锌锰干电池是一次电池,其中MnO 是催化剂,可使锌锰干电池的比能量高、可储存时间长(
2
)
(15)铅蓄电池工作过程中,每通过2 mol电子,负极质量减轻207 g( )
(16)镍镉电池不能随意丢弃的主要原因是镍、镉的资源有限,价格昂贵( )
答案:(1)√ (2)√ (3)√ (4)√ (5)√ (6)× (7)√ (8)× (9)√ (10)√ (11)× (12)× (13)× (14)×
(15)× (16)×
【典例】
例1 (2021•广东选择性考试)火星大气中含有大量CO ,一种有CO 参加反应的新型全固态电池有望
2 2
为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应 B.CO 在正极上得电子
2
C.阳离子由正极移向负极 D.将电能转化为化学能【答案】B
【解析】根据题干信息可知,放电时总反应为4Na+3CO =2Na CO+C。A项,放电时负极上Na发生
2 2 3
氧化反应失去电子生成Na+,故A错误;B项,放电时正极为CO 得到电子生成C,故B正确;C项,放
2
电时阳离子移向还原电极,即阳离子由负极移向正极,故C错误;D项,放电时装置为原电池,能量转化
关系为化学能转化为电能和化学能等,故D正确;故选B。
例2 (2022•全国乙卷) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家
研究了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子(e-)和空穴(h+),驱动阴极反应
2
(Li++e-=Li+)和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是( )
2 2 2
A.充电时,电池的总反应LiO=2Li+O
2 2 2
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应O+2Li++2e-=Li O
2 2 2
【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应
(Li O+2h+=2Li++O ),则充电时总反应为LiO=2Li+O ,结合图示,充电时金属Li电极为阴极,光催化电
2 2 2 2 2 2
极为阳极;则放电时金属Li电极为负极,光催化电极为正极。A项,光照时,光催化电极产生电子和空穴,
驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳极反应,充电时电池的总反应为
LiO=2Li+O ,A正确;充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空
2 2 2
穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;C项,放电时,金属Li电极为负极,光催
化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;D项,放电时总反应为2Li+O=Li O,正
2 2 2
极反应为O+2Li++2e-=Li O,D正确;故选C。
2 2 2【对点提升】
对点1 微生物燃料电池的研究已成为治理和消除环境污染的重要课题,利用微生物电池电解饱和食
盐水的工作原理如下图所示。下列说法正确的是( )
A.电池正极的电极反应:O+2H O+4e− 4OH−
2 2
B.电极M附近产生黄绿色气体
C.若消耗1 mol S2−,则电路中转移8 mol e−
D.将装置温度升高到60 ℃,一定能提高电池的工作效率
【答案】C
【解析】微生物燃料电池中,通入C H O 的电极为负极,失电子发生氧化反应;通入 O 的电极为正
6 12 6 2
极,得电子发生还原反应。电解饱和食盐水时阴、阳极的电极产物分别是:氢气和氢氧化钠、氯气。A项,
由图可知,电解质溶液为酸性,正极的电极反应是O+4H++4e−==2H O,A项错误;B项,M为阴极产生
2 2
H ,N为阳极产生Cl ,B项错误;C项,1 mol S2−转化成SO 2-失8 mol e−,则电路中转移8 mol e-,C项正
2 2 4
确;D项,该电池为微生物燃料电池,该微生物的最佳活性温度未知,无法确定60 ℃时电池效率是否升高,
D项错误。
对点2 下图是通过 Li-CO 电化学技术实现储能系统和 CO 固定策略的示意团。储能系统使用的
2 2
电池组成为钌电极/CO 饱和 LiClO-(CH )SO(二甲基亚砜)电解液/锂片,下列说法不正确的是( )
2 4 3 2A.Li-CO 电池电解液为非水溶液
2
B.CO 的固定中,转秱 4mole-生成 1mol 气体
2
C.钌电极上的电极反应式为 2LiCO+C - 4e-=4Li++3CO ↑
2 3 2
D.通过储能系统和 CO 固定策略可将 CO 转化为固体产物 C
2 2
【答案】B
【解析】A 项,由题目可知,Li—CO 电池有活泼金属 Li,故电解液为非水溶液饱和 LiClO—
2 4
(CH)SO(二甲基亚砜)有机溶剂,故A正确;B项,由题目可知,CO 的固定中的电极方秳式为:2LiCO
3 2 2 2 3
= 4Li++ 2CO ↑+ O + 4e-,转移4mole-生成3mol气体,故B错误;C项,由题目可知,钌电极上的电极
2 2
反应式为 2LiCO + C- 4e-=4Li++3CO ↑,故C正确;D项,由题目可知,CO 通过储能系统和CO 固定策
2 3 2 2 2
略转化为固体产物C,故D正确。故选B。
【巧学妙记】
燃料电池电极反应式的书写(以氢氧燃料电池为例)
(1)注意介质环境
(2)掌握书写程序1.下列选项描述的过程能实现化学能转化为电能的是( )
A. 电池充电 B.光合作用 C.手机电池工作 D.太阳能板充电
【答案】C
【解析】A项,电池充电,是将电能转化为化学能,故A错误;B项,光合作用是太阳能转变化为化
学能,故B错误;C项,手机电池工作是化学能转化为电能,故C正确;
D项,太阳能板充电是光能转化为电能,并向蓄电池充电,将电能转化为化学能储存起来,故D错误。
2.有关如图所示原电池的叙述不正确的是( )
A.电子沿导线由Cu片流向Ag片B.正极的电极反应式是Ag++e-=Ag
C.Cu片上发生氧化反应,Ag片上发生还原反应
D.反应时盐桥中的阳离子移向Cu(NO ) 溶液
3 2
【答案】D
【解析】该装置是原电池装置,实质上发生的是Cu与硝酸银的反应,所以Cu失去电子,发生氧化反
应,则Cu是负极,Ag是正极,电子从负极流向正极,A项正确;正极是Ag+发生还原反应,得到电子生
成Ag,B项正确;根据以上分析,Cu片上发生氧化反应,Ag片上发生还原反应,C项正确;原电池中,
阳离子向正极移动,所以盐桥中的阳离子移向AgNO 溶液,D项错误。
3
3.肼(N H)碱性燃料电池的原理示意图如图所示,电池总反应为:NH+O =N +2H O。下列说法错误
2 4 2 4 2 2 2
的是( )
A.电极b发生还原反应 B.电流由电极a流出经用电器流入电极b
C.物质Y是NaOH溶液 D.电极a的电极反应式为NH + 4OH--4e-=N ↑ + 4H O
2 4 2 2
【答案】B
【解析】该燃料电池中,通入燃料肼的电极为负极、通入氧气的电极为正极,电解质溶液呈碱性,则
负极反应式为NH+4OH--4e-═N ↑+4H O,正极反应式为O+2H O+4e-=4OH-。A项,该燃料电池中通入氧
2 4 2 2 2 2
气的电极b为正极,正极上得电子,发生还原反应,故A正确;B项,a为负极、b为正极,电流从正极b
经用电器流入负极a,故B错误;C项,b电极上生成氢氧根离子,钠离子通过阳离子交换膜进入右侧,所
以Y为NaOH溶液,故C正确;D项,a电极上肼失电子,发生氧化反应,电极反应式为 NH+4OH--4e-
2 4
═N ↑+4H O,故D正确;故选B。
2 2
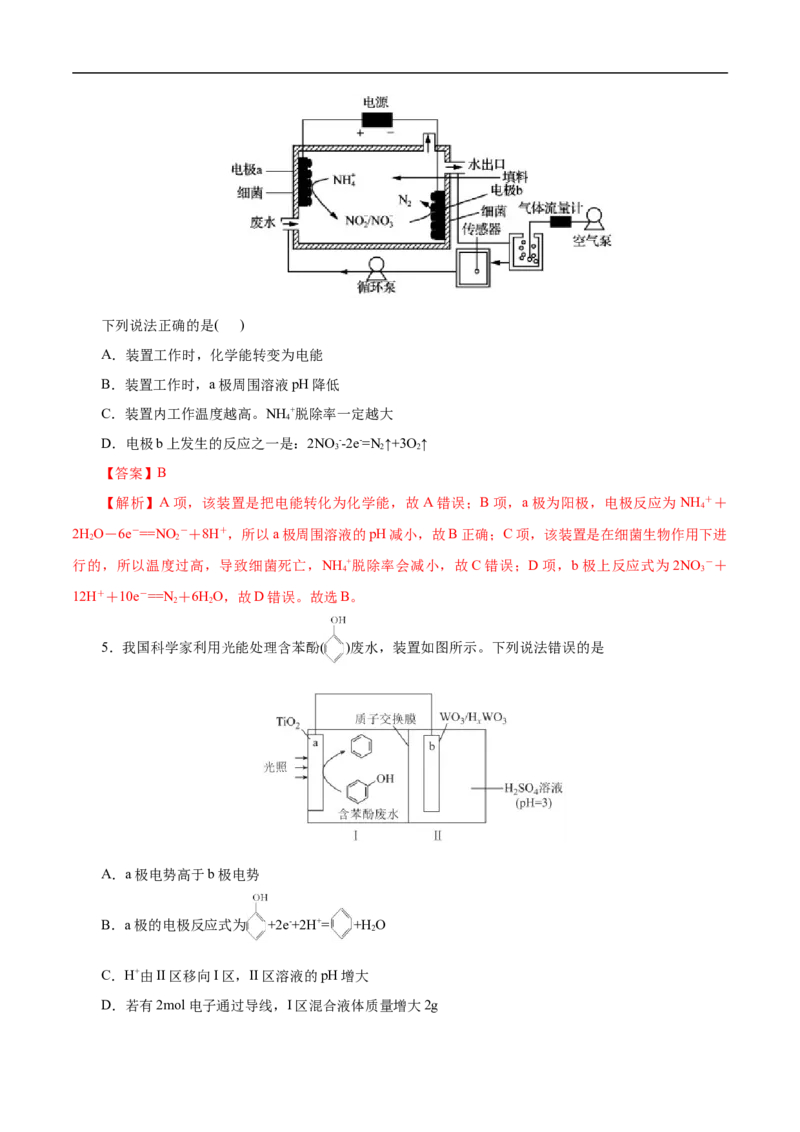
4.一种生物电化学方法脱除水体中NH +的原理如下图所示:
4下列说法正确的是( )
A.装置工作时,化学能转变为电能
B.装置工作时,a极周围溶液pH降低
C.装置内工作温度越高。NH +脱除率一定越大
4
D.电极b上发生的反应之一是:2NO --2e-=N ↑+3O ↑
3 2 2
【答案】B
【解析】A项,该装置是把电能转化为化学能,故 A错误;B项,a极为阳极,电极反应为NH ++
4
2HO-6e-==NO -+8H+,所以a极周围溶液的pH减小,故B正确;C项,该装置是在细菌生物作用下进
2 2
行的,所以温度过高,导致细菌死亡,NH +脱除率会减小,故C错误;D项,b极上反应式为2NO -+
4 3
12H++10e-==N +6HO,故D错误。故选B。
2 2
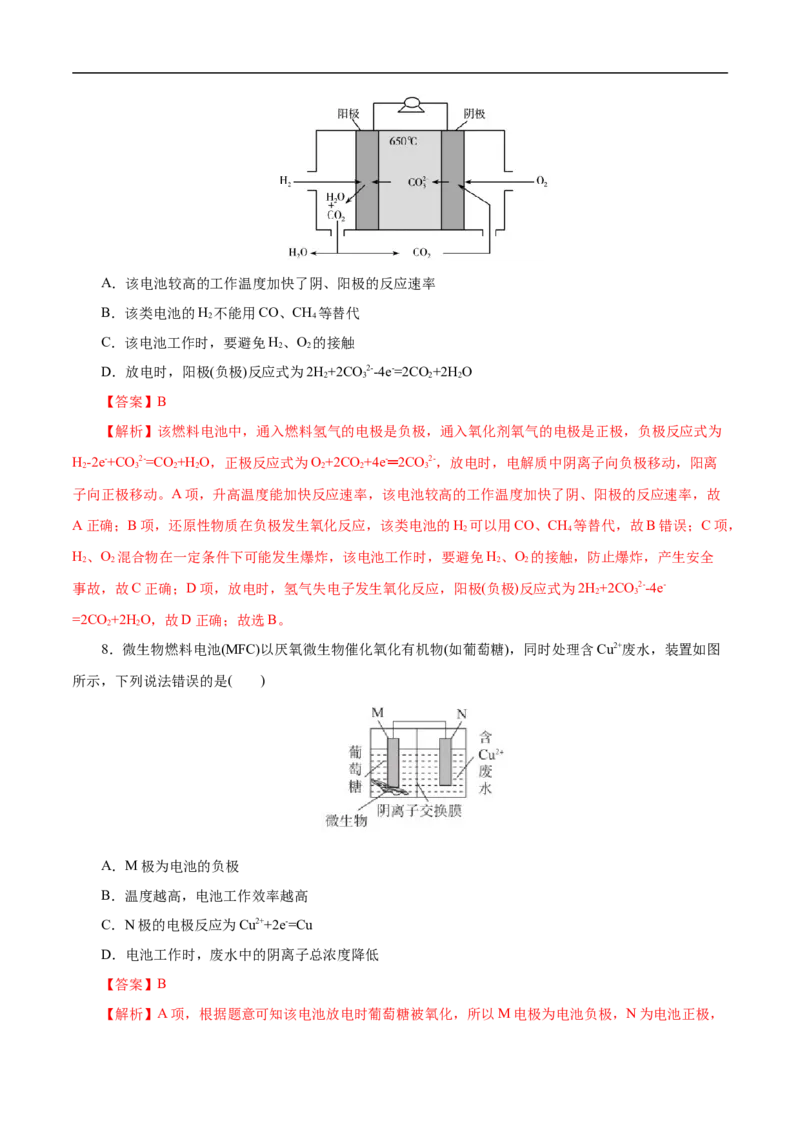
5.我国科学家利用光能处理含苯酚( )废水,装置如图所示。下列说法错误的是
A.a极电势高于b极电势
B.a极的电极反应式为 +2e-+2H+= +H O
2
C.H+由II区移向I区,II区溶液的pH增大
D.若有2mol电子通过导线,I区混合液体质量增大2g【答案】C
【解析】从图中可以看出,该装置为原电池装置,苯酚在a极得电子,被还原,所以a极为正极,b极
为负极。A项,a为正极,b为负极,a极电势高于b负极,故A正确;B项,苯酚在a极得电子被还原,
其电极反应为 +2e-+2H+= +H O,故B正确;C项,氢离子向阳极移动,负极反应为HWO- xe-
2 x 3
=WO + xH+,a极消耗的氢离子和b极产生的氢离子相等,pH不变,故C错误;D项,有2mol氢离子通过
3
导线,进入I区的氢离子为2mol,液体质量增加2g,故D正确;故选C。
6.一种锂电池的工作原理如下图所示,正极反应液可以在正极区和氧化罐间循环流通,氧化罐中加
入的(NH )SO 可以将Fe2+氧化,自身被还原为SO 2-。下列关于该电池说法正确的是
4 2 2 8 4
A.电池放电时将电能转化为化学能
B.放电时Li+由正极区移向负极区
C.放电时的负极反应为Fe3++e-=Fe2+
D.氧化罐中反应的离子方程式为:2Fe2++SO2-=2Fe3++2SO 2-
2 8 4
【答案】D
【解析】A项,电池放电是化学能变成电能,A错误;B项,放电时阳离子向正极移动,B错误;C
项,放电时,负极失去电子,C错误;D项,根据题意,氧化罐中加入的(NH )SO 可以将Fe2+氧化,自
4 2 2 8
身被还原为SO 2-,离子方程式为2Fe2++SO2-=2Fe3++2SO 2-,D正确;故选D。
4 2 8 4
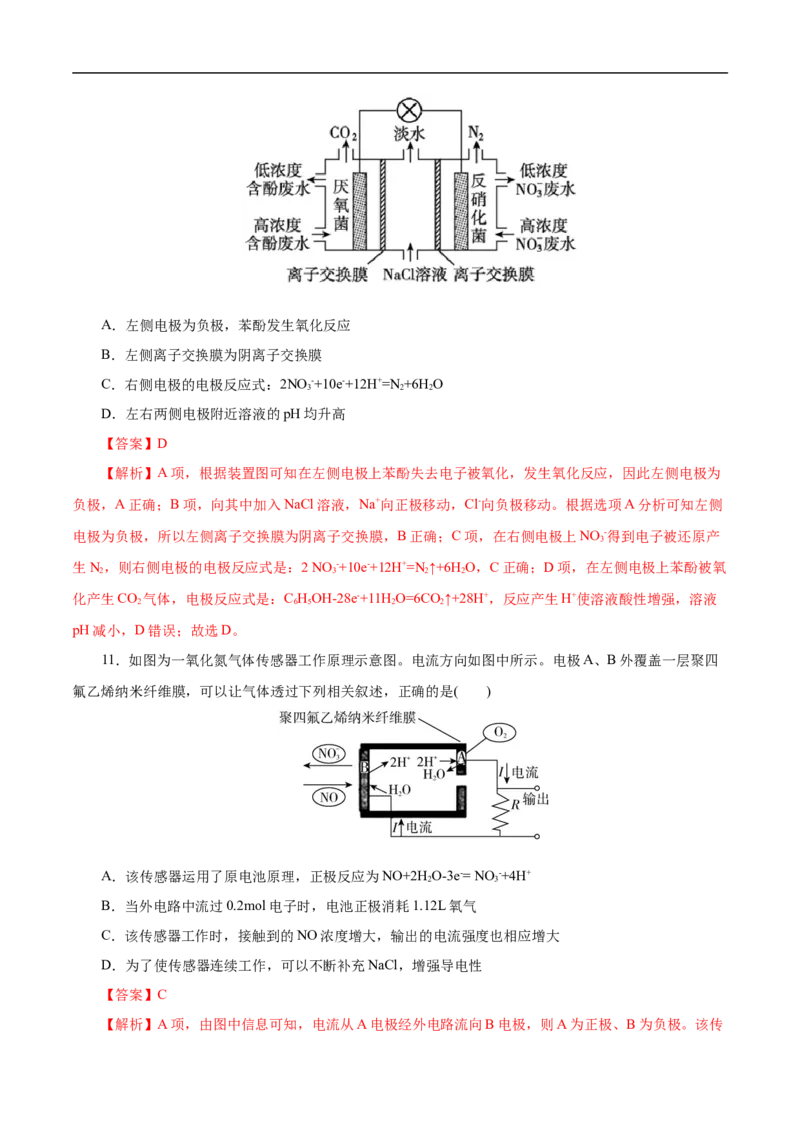
7.熔融碳酸盐燃料电池(MCFC)是由多孔陶瓷NiO阴极、多孔陶瓷电解质(熔融碱金属碳酸盐)隔膜、
多孔金属Ni阳极、金属极板构成的燃料电池。工作时,该电池的阴极(正极)反应为O+2CO +4e-=2CO 2-,
2 2 3
下列有关说法中错误的是( )A.该电池较高的工作温度加快了阴、阳极的反应速率
B.该类电池的H 不能用CO、CH 等替代
2 4
C.该电池工作时,要避免H、O 的接触
2 2
D.放电时,阳极(负极)反应式为2H+2CO 2--4e-=2CO +2H O
2 3 2 2
【答案】B
【解析】该燃料电池中,通入燃料氢气的电极是负极,通入氧化剂氧气的电极是正极,负极反应式为
H-2e-+CO 2-=CO +H O,正极反应式为O+2CO +4e-═2CO 2-,放电时,电解质中阴离子向负极移动,阳离
2 3 2 2 2 2 3
子向正极移动。A项,升高温度能加快反应速率,该电池较高的工作温度加快了阴、阳极的反应速率,故
A正确;B项,还原性物质在负极发生氧化反应,该类电池的H 可以用CO、CH 等替代,故B错误;C项,
2 4
H、O 混合物在一定条件下可能发生爆炸,该电池工作时,要避免H、O 的接触,防止爆炸,产生安全
2 2 2 2
事故,故C正确;D项,放电时,氢气失电子发生氧化反应,阳极(负极)反应式为2H+2CO 2--4e-
2 3
=2CO +2H O,故D正确;故选B。
2 2
8.微生物燃料电池(MFC)以厌氧微生物催化氧化有机物(如葡萄糖),同时处理含Cu2+废水,装置如图
所示,下列说法错误的是( )
A.M极为电池的负极
B.温度越高,电池工作效率越高
C.N极的电极反应为Cu2++2e-=Cu
D.电池工作时,废水中的阴离子总浓度降低
【答案】B
【解析】A项,根据题意可知该电池放电时葡萄糖被氧化,所以M电极为电池负极,N为电池正极,A项正确;B项,该电池以微生物催化有机物,温度不宜过高,B项错误;C项,N极为正极,铜离子被还
原得到Cu,电极反应为Cu2++2e-=Cu,C项正确;D项,电池工作时,废水中铜离子放电生成铜单质,为
平衡电荷,阴离子通过阴离子交换膜向负极,即左池移动,废水中的阴离子总浓度降低,D项正确;故选
B。
9.HCOOH燃料电池的装置如下图,两电极间用允许K+和H+通过的半透膜隔开。下列说法错误的是
A.电池工作时,电子由a电极经外电路流向b电极
B.负极的电极反应式为HCOO-+2OH-_2e-=HCO-+H O
3 2
C.理论上每消耗标准状况下22.4LO ,有2molK+通过半透膜
2
D.通入O 发生的反应为4Fe2++4H++O =4Fe3++2H O
2 2 2
【答案】C
【解析】左侧是HCOO-转化为HCO -,C元素化合价升高,失去电子,发生氧化反应,a是负极;右
3
侧是Fe3+转化为Fe2+,化合价降低,得到电子,发生还原反应,b是正极。A项,池工作时,电子由a电极
(负极)电极经外电路流向b电极(正极),A项正确;B项,负极是HCOO-转化为HCO -,电极反应式为:
3
HCOO-+2OH-_2e-= HCO -+H O,B项正确;C项,4Fe2++4H++O =4Fe3++2H O,每消耗标准状况下22.4L
3 2 2 2
O,O 的物质的量为1mol,转移电子4mol,应有4mol K+通过半透膜,C项错误;D项,通入O 发生的反
2 2 2
应为4Fe2++4H++O =4Fe3++2H O,D项正确;故选C。
2 2
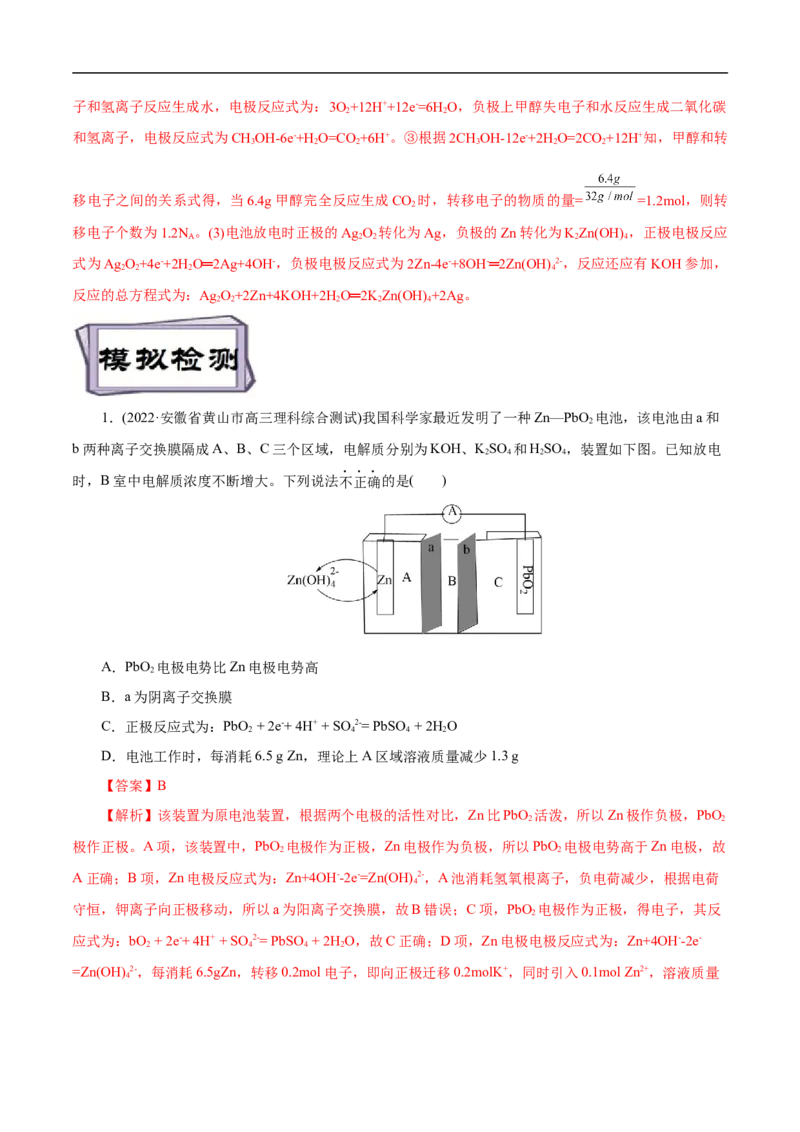
10.一种三室微生物燃料电池污水净化系统的原理如图所示,图中含酚废水中的有机物可用C HOH
6 5
表示。下列说法不正确的是A.左侧电极为负极,苯酚发生氧化反应
B.左侧离子交换膜为阴离子交换膜
C.右侧电极的电极反应式:2NO -+10e-+12H+=N +6H O
3 2 2
D.左右两侧电极附近溶液的pH均升高
【答案】D
【解析】A项,根据装置图可知在左侧电极上苯酚失去电子被氧化,发生氧化反应,因此左侧电极为
负极,A正确;B项,向其中加入NaCl溶液,Na+向正极移动,Cl-向负极移动。根据选项A分析可知左侧
电极为负极,所以左侧离子交换膜为阴离子交换膜,B正确;C项,在右侧电极上NO -得到电子被还原产
3
生N,则右侧电极的电极反应式是:2 NO-+10e-+12H+=N ↑+6H O,C正确;D项,在左侧电极上苯酚被氧
2 3 2 2
化产生CO 气体,电极反应式是:C HOH-28e-+11H O=6CO↑+28H+,反应产生H+使溶液酸性增强,溶液
2 6 5 2 2
pH减小,D错误;故选D。
11.如图为一氧化氮气体传感器工作原理示意图。电流方向如图中所示。电极A、B外覆盖一层聚四
氟乙烯纳米纤维膜,可以让气体透过下列相关叙述,正确的是( )
A.该传感器运用了原电池原理,正极反应为NO+2H O-3e-= NO -+4H+
2 3
B.当外电路中流过0.2mol电子时,电池正极消耗1.12L氧气
C.该传感器工作时,接触到的NO浓度增大,输出的电流强度也相应增大
D.为了使传感器连续工作,可以不断补充NaCl,增强导电性
【答案】C
【解析】A项,由图中信息可知,电流从A电极经外电路流向B电极,则A为正极、B为负极。该传感器运用了原电池原理,O 在正极上发生还原反应,电极反应式为O+4H++4e-=2H O,A项错误;B项,
2 2 2
由选项A分析可知,当外电路中流过0.2mol电子时,电池正极消耗0.05mol氧气,标准状况下体积为
1.12L,B项错误;C项,该传感器工作时,接触到的NO浓度增大,则化学反应速率加快,单位时间内化
学能转化的电能增多,输出的电流强度也相应增大,C项正确;D项,若补充氯化钠,Cl-也会失去电子生
成氯气,影响NO的测定,且造成污染,D项错误;故选C。
12.科学家设计的可充电电池的工作原理示意图如图所示。该可充电电池的放电反应为LiC +Li
x n (1-
CoO=LiCoO+nC。N 表示阿伏伽德罗常数的值。下列说法错误的是
x) 2 2 A
A.该电池用于电动汽车符合绿色化学观念
B.充电时,阳极反应为LiCoO -xe-=Li CoO+xLi+, 由B极移向A极
2 (1-x) 2
C.该电池用惰性电极电解某电解质溶液时,发现两极只有H 和O 生成。则电解一段时间后,该溶液
2 2
的浓度可能不变
D.若初始两电极质量相等,当转移4N 个电子时,两电极质量差为28g
A
【答案】D
【解析】根据可充电电池的工作原理示意图中电子流向可知,A为负极,B为正极;充电时,A为阴
极,B为阳极;可充电电池的放电反应为LiC +Li CoO=LiCoO+nC,则放电时正极反应为Li
x n (1-x) 2 2 (1-
CoO+xLi++xe-=LiCoO,充电时,原电池的正极即为电解池的阳极,反应逆转,则反应为LiCoO -xe-=Li
x) 2 2 2 (1-
CoO+xLi+。A项,汽车燃烧汽油等化石燃料,排放的汽车尾气含氮的氧化物,大量氮氧化物排放到空气
x) 2
中,电动汽车可有效减少大气污染,该电池用于电动汽车符合绿色化学观念,故A正确;B项,可充电电
池的放电反应为LiC +Li CoO=LiCoO+nC,则放电时正极反应为Li CoO+xLi++xe-=LiCoO,充电时,
x n (1-x) 2 2 (1-x) 2 2
原电池的正极即为电解池的阳极,反应逆转,则反应为LiCoO -xe-=Li CoO+xLi+,阳离子由阳极B向阴
2 (1-x) 2
极A移动,故B正确;C项,两极只有H 和O 生成,应为电解水型的电解,电解时阳极反应为:4OH--4e-
2 2
=2H O+O↑,阴极反应为:4H++4e-=2H ↑,可为电解含氧酸溶液、强碱溶液或活泼金属的含氧酸盐溶液,
2 2 2
由于溶剂HO减小,若电解的溶液为饱和溶液,则浓度不变,故C正确;D项,若初始两电极质量相等,
2当转移4N 个电子时,负极减少4molLi其质量为28g,正极有4molLi+迁入,其质量为28g,两电极质量差
A
为56g,故D错误;故选D。
13.人们应用原电池原理制作了多种电池以满足不同的需要。电池发挥着越来越重要的作用,如在
宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境
造成污染。请根据题中提供的信息,回答下列问题:
(1)研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,
在海水中电池反应可表示为:5MnO +2Ag+2NaCl=Na MnO +2AgCl
2 2 5 10
①该电池的负极反应式是______________;
②在电池中,Na+不断移动到“水”电池的_______极(填“正”或“负”);
③外电路每通过4mol电子时,生成NaMnO 的物质的量是______________。
2 5 10
(2)中国科学院应用化学研究所在甲醇(CHOH是一种可燃物)燃料电池技术方面获得新突破。甲醇燃
3
料电池的工作原理如右图所示。
①该电池工作时,b口通入的物质为______________。
②该电池负极的电极反应式______________。
③工作一段时间后,当6.4g甲醇完全反应生成CO 时,有___________N 个电子转移。
2 A
(3)Ag O 是银锌碱性电池的正极活性物质,当银锌碱性电池的电解质溶液为 KOH溶液,电池放电时
2 2
正极的Ag O 转化为Ag,负极的Zn转化为KZn(OH) ,写出该电池反应方程式:_______________。
2 2 2 4
【答案】(1)①Ag—e—+Cl—=AgCl ②正(1分) ③2mol
(2)①CHOH ②CHOH—6e—+H O=CO+6H+ ③1.2
3 3 2 2
(3)Ag O+2Zn+4KOH+2H O==2K Zn(OH) +2Ag
2 2 2 2 4
【解析】(1)①根据电池总反应:5MnO +2Ag+2NaCl=Na MnO +2AgCl,可判断出Ag应为原电池的
2 2 5 10
负极,负极发生反应的电极方程式为:Ag+Cl--e-=AgCl。②在原电池中阴离子向负极移动,阳离子向正极
移动,所以钠离子向正极移动。③根据方程式中5MnO 生成1NaMnO ,化合价共降低了2价,所以每生
2 2 5 10
成1molNa MnO 转移2mol电子,则外电路每通过4mol电子时,生成NaMnO 的物质的量是2mol。
2 5 10 2 5 10
(2)①据氢离子移动方向知,右侧电极为正极,左侧电极为负极,负极上通入燃料甲醇。②正极上氧气得电子和氢离子反应生成水,电极反应式为:3O+12H++12e-=6H O,负极上甲醇失电子和水反应生成二氧化碳
2 2
和氢离子,电极反应式为CHOH-6e-+H O=CO+6H+。③根据2CHOH-12e-+2H O=2CO+12H+知,甲醇和转
3 2 2 3 2 2
移电子之间的关系式得,当6.4g甲醇完全反应生成CO 时,转移电子的物质的量= =1.2mol,则转
2
移电子个数为1.2N 。(3)电池放电时正极的Ag O 转化为Ag,负极的Zn转化为KZn(OH) ,正极电极反应
A 2 2 2 4
式为Ag O+4e-+2H O═2Ag+4OH-,负极电极反应式为2Zn-4e-+8OH-═2Zn(OH) 2-,反应还应有KOH参加,
2 2 2 4
反应的总方程式为:Ag O+2Zn+4KOH+2H O═2K Zn(OH) +2Ag。
2 2 2 2 4
1.(2022·安徽省黄山市高三理科综合测试)我国科学家最近发明了一种Zn—PbO 电池,该电池由a和
2
b两种离子交换膜隔成A、B、C三个区域,电解质分别为KOH、KSO 和HSO ,装置如下图。已知放电
2 4 2 4
时,B室中电解质浓度不断增大。下列说法不正确的是( )
A.PbO 电极电势比Zn电极电势高
2
B.a为阴离子交换膜
C.正极反应式为:PbO + 2e-+ 4H+ + SO 2-= PbSO + 2H O
2 4 4 2
D.电池工作时,每消耗6.5 g Zn,理论上A区域溶液质量减少1.3 g
【答案】B
【解析】该装置为原电池装置,根据两个电极的活性对比,Zn比PbO 活泼,所以Zn极作负极,PbO
2 2
极作正极。A项,该装置中,PbO 电极作为正极,Zn电极作为负极,所以PbO 电极电势高于Zn电极,故
2 2
A正确;B项,Zn电极反应式为:Zn+4OH--2e-=Zn(OH) 2-,A池消耗氢氧根离子,负电荷减少,根据电荷
4
守恒,钾离子向正极移动,所以a为阳离子交换膜,故B错误;C项,PbO 电极作为正极,得电子,其反
2
应式为:bO + 2e-+ 4H+ + SO 2-= PbSO + 2H O,故C正确;D项,Zn电极电极反应式为:Zn+4OH--2e-
2 4 4 2
=Zn(OH) 2-,每消耗6.5gZn,转移0.2mol电子,即向正极迁移0.2molK+,同时引入0.1mol Zn2+,溶液质量
4差为 ,故D正确;故选B。
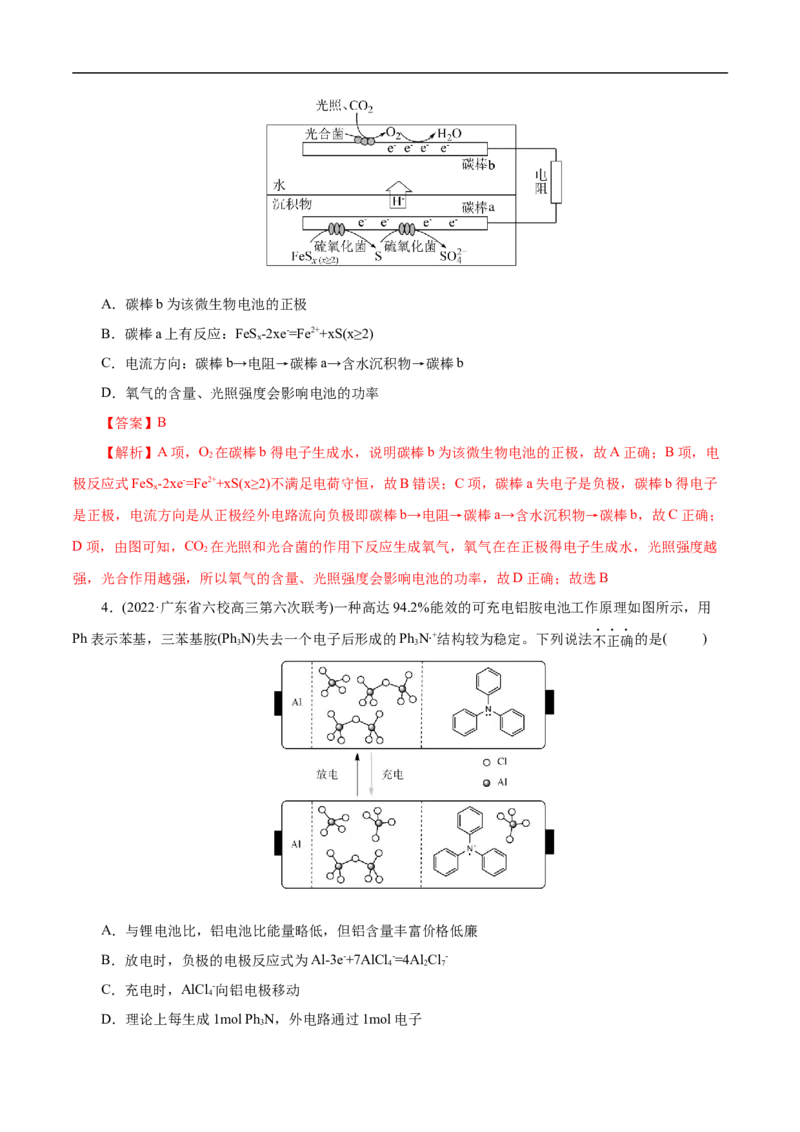
2.(2022·辽宁省大连市高三双基测试)“碳呼吸电池”是一种新型能源装置,其工作原理如图所示。下
列有关说法错误的是( )
A.通入CO 的一极电极反应式为:2CO+2e−=C O2-
2 2 2 4
B.金属铝电极发生氧化反应
C.每得到1molAl (C O),电路中转移3mol电子
2 2 4 3
D.以该装置为电源进行粗铜的电解精炼,金属铝质量减少27g时,理论上阴极质量增加96g
【答案】C
【解析】据图可知Al被氧化,所以金属铝为负极,通入CO 的电极为正极,CO 被还原为草酸根。A
2 2
项,据图可知CO 在正极被还原为草酸根,根据电子守恒、元素守恒可得反应式为2CO+2e−=C O2-,A正
2 2 2 4
确;B项,铝为金属,在负极被氧化为Al3+,B正确;C项,每得到1mol Al (C O),则需要2mol Al,根
2 2 4 3
据电极反应可知转移6mol电子,C错误;D项,金属铝质量减少27g,即减少1mol Al,根据电极反应
Al-3e−=Al3+可知,转移3mol电子,则电极铜时,阴极生成1.5mol铜,质量为1.5mol×64g/mol=96g,D正确;
故选C。
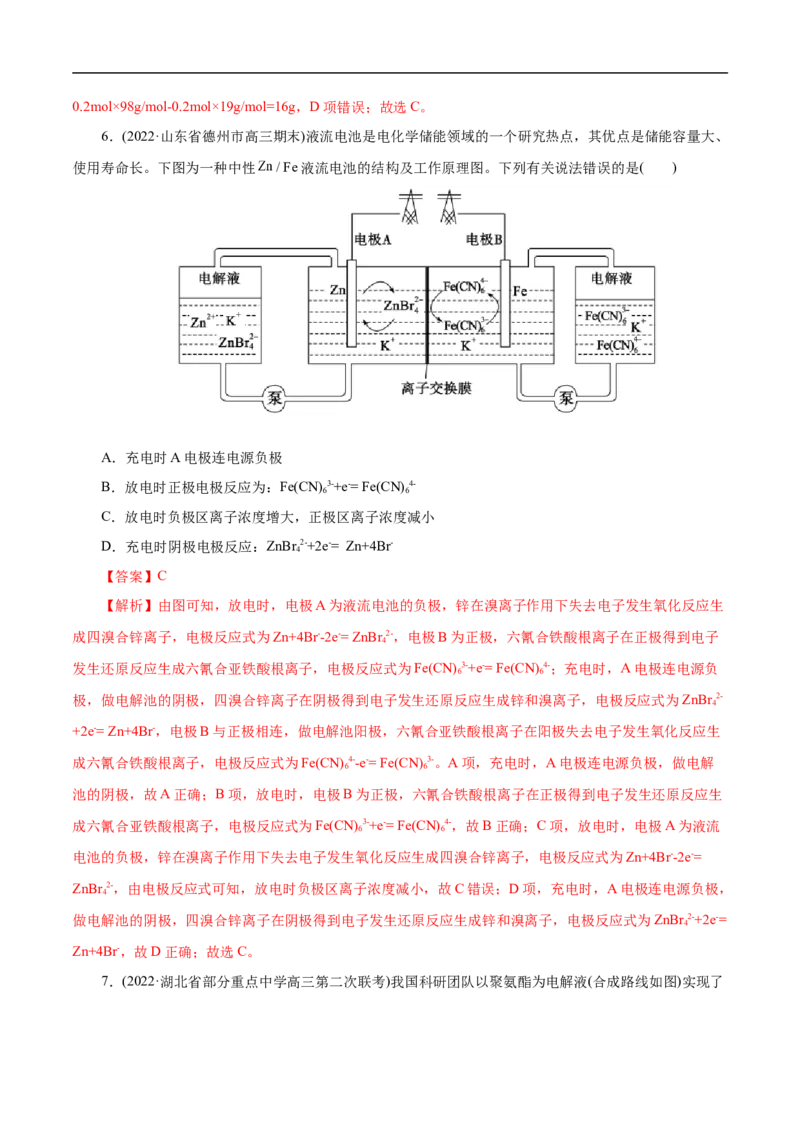
3.(2022·四川省泸县第二中学模拟预测)沉积物微生物燃料电池可处理含硫废水,其工作原理如图所
示。下列说法错误的是( )A.碳棒b为该微生物电池的正极
B.碳棒a上有反应:FeS-2xe-=Fe2++xS(x≥2)
x
C.电流方向:碳棒b→电阻→碳棒a→含水沉积物→碳棒b
D.氧气的含量、光照强度会影响电池的功率
【答案】B
【解析】A项,O 在碳棒b得电子生成水,说明碳棒b为该微生物电池的正极,故A正确;B项,电
2
极反应式FeS-2xe-=Fe2++xS(x≥2)不满足电荷守恒,故B错误;C项,碳棒a失电子是负极,碳棒b得电子
x
是正极,电流方向是从正极经外电路流向负极即碳棒b→电阻→碳棒a→含水沉积物→碳棒b,故C正确;
D项,由图可知,CO 在光照和光合菌的作用下反应生成氧气,氧气在在正极得电子生成水,光照强度越
2
强,光合作用越强,所以氧气的含量、光照强度会影响电池的功率,故D正确;故选B
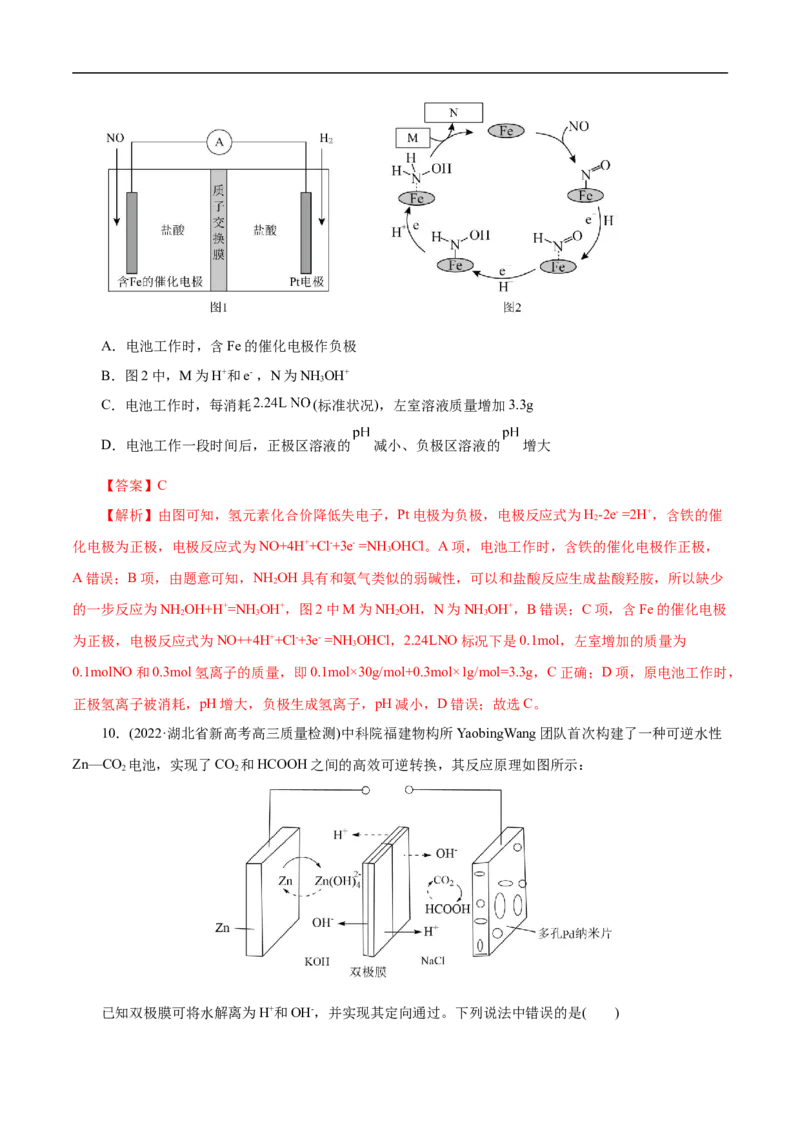
4.(2022·广东省六校高三第六次联考)一种高达94.2%能效的可充电铝胺电池工作原理如图所示,用
Ph表示苯基,三苯基胺(Ph N)失去一个电子后形成的Ph N∙+结构较为稳定。下列说法不正确的是( )
3 3
A.与锂电池比,铝电池比能量略低,但铝含量丰富价格低廉
B.放电时,负极的电极反应式为Al-3e-+7AlCl -=4AlCl-
4 2 7
C.充电时,AlCl -向铝电极移动
4
D.理论上每生成1mol Ph N,外电路通过1mol电子
3【答案】C
【解析】A项,铝电池比能量略低,且含量丰富价格低廉,A项错误;B项,放电时,负极上Al失电
子和AlCl -反应生成Al Cl-,电极反应式为Al-3e-+7AlCl -=4AlCl-,B项正确;C项,充电时Ph N失电子
4 2 7 4 2 7 3
生成Ph N+ , Ph N阳极、Al为阴极,阴离子向阳极移动,所以AlCl -向阳极Ph N移动,C项错误;D项,
3 3 4 3
充电时Ph N失电子生成Ph N+,则生成1个Ph N转移1个电子,所以理论上每生成1molPh N,外电路通
3 3 3 3
过1mol电子,D项正确。故选C。
5.(2022·山东省聊城市高三三模)科学家最近发明了一种Al-PbO 电池,电解质为KSO 、HSO 、
2 2 4 2 4
KOH,通过x(阳离子交换膜)和y(阴离子交换膜)将电解质溶液隔开,形成M、R、N三个电解质溶液区域,
结构示意图如图所示。下列说法正确的是( )
A.放电时,K+通过x膜移向M区
B.放电时,正极反应式为PbO +2e-+4H+=Pb2++2H O
2 2
C.与Zn-PbO 电池相比较,Al-PbO 电池的比能量更高
2 2
D.消耗1.8gAl时N区域电解质溶液减少19.2g
【答案】C
【解析】由图可知,原电池工作时,Al为负极,被氧化生成[Al(OH) ]-,PbO 为正极,发生还原反应,
4 2
电解质溶液M为KOH,R为KSO ,C为HSO ,原电池工作时,负极反应为Al-3e-+4OH-=[Al(OH) ]-,则
2 4 2 4 4
消耗OH-,钾离子向正极移动,正极电极反应式为PbO + SO 2-+2e-+4H+=PbSO+2H O,正极消耗氢离子,
2 4 4 2
阴离子向负极移动,则y是阳离子交换膜,x是阴离子交换膜,在同一闭合回路中电子转移数目相等,结
合溶液酸碱性及电极材料书写电极反应式和总反应的方程式,以此解答该题。根据图知,负极上Al失电子
生成[Al(OH) ]-负极反应为Al-3e-+4OH-=[Al(OH) ]-,消耗1.8g Al,正极反应为PbO + SO 2-+2e-
4 4 2 4
+4H+=PbSO+2H O,根据转移电子相等计算。A项,Al为负极, M区为负极区,阳离子流向正极区,故
4 2
K+通过x膜移向R区,A项错误;B项,放电时,正极反应为PbO + SO 2-+2e-+4H+=PbSO+2H O,B项错
2 4 4 2
误;C项,比能量是指参加电极反应的单位质量的电极材料放出电能的大小,Zn与Al相比质量更重,且
每一个Zn转移2个电子,1个Al转移3个电子,故Al-PbO 电池的比能量更高,C项正确;D项,消耗
2
1.8g Al时电路上转移的电子数目为0.20mol,则由N区溶液减少0.4mol氢离子和0.1mol硫酸根离子,同时
有0.1mol硫酸根离子移向R区,相当于减小0.2mol硫酸,同时生成0.2mol水,N极区实际减少质量为0.2mol×98g/mol-0.2mol×19g/mol=16g,D项错误;故选C。
6.(2022·山东省德州市高三期末)液流电池是电化学储能领域的一个研究热点,其优点是储能容量大、
使用寿命长。下图为一种中性 / Fe液流电池的结构及工作原理图。下列有关说法错误的是( )
A.充电时A电极连电源负极
B.放电时正极电极反应为:Fe(CN) 3-+e-= Fe(CN) 4-
6 6
C.放电时负极区离子浓度增大,正极区离子浓度减小
D.充电时阴极电极反应:ZnBr 2-+2e-= Zn+4Br-
4
【答案】C
【解析】由图可知,放电时,电极A为液流电池的负极,锌在溴离子作用下失去电子发生氧化反应生
成四溴合锌离子,电极反应式为Zn+4Br--2e-= ZnBr 2-,电极B为正极,六氰合铁酸根离子在正极得到电子
4
发生还原反应生成六氰合亚铁酸根离子,电极反应式为Fe(CN) 3-+e-= Fe(CN) 4-;充电时,A电极连电源负
6 6
极,做电解池的阴极,四溴合锌离子在阴极得到电子发生还原反应生成锌和溴离子,电极反应式为ZnBr 2-
4
+2e-= Zn+4Br-,电极B与正极相连,做电解池阳极,六氰合亚铁酸根离子在阳极失去电子发生氧化反应生
成六氰合铁酸根离子,电极反应式为Fe(CN) 4--e-= Fe(CN) 3-。A项,充电时,A电极连电源负极,做电解
6 6
池的阴极,故A正确;B项,放电时,电极B为正极,六氰合铁酸根离子在正极得到电子发生还原反应生
成六氰合亚铁酸根离子,电极反应式为Fe(CN) 3-+e-= Fe(CN) 4-,故B正确;C项,放电时,电极A为液流
6 6
电池的负极,锌在溴离子作用下失去电子发生氧化反应生成四溴合锌离子,电极反应式为Zn+4Br--2e-=
ZnBr 2-,由电极反应式可知,放电时负极区离子浓度减小,故C错误;D项,充电时,A电极连电源负极,
4
做电解池的阴极,四溴合锌离子在阴极得到电子发生还原反应生成锌和溴离子,电极反应式为ZnBr 2-+2e-=
4
Zn+4Br-,故D正确;故选C。
7.(2022·湖北省部分重点中学高三第二次联考)我国科研团队以聚氨酯为电解液(合成路线如图)实现了稳定高效且可逆循环的K-CO 电池。总反应为:4KSn+3CO 2KCO+4Sn,其中生成的KCO 附着在
2 2 2 3 2 3
正极上。下列说法错误的是( )
A.放电时,内电路中电流由KSn合金经酯基电解质流向羧基化碳纳米管
B.电池的正极反应式为4K++3CO +4e-=2K CO+C
2 2 3
C.羧基化碳纳米管中引入的羧基可促进电子的转移
D.充电时,电路中通过1mol电子,多壁碳纳米管减重36g
【答案】D
【解析】由总反应可知放电时KSn合金为负极,羧基化碳纳米管为正极;充电时KSn合金与电源负极
相连,为电解池阴极,羧基化碳纳米管为阳极。A项,放电时为原电池装置,内电路中电流是由负极流向
正极,即放电时,内电路中电流由KSn合金经酯基电解质流向羧基化碳纳米管,A正确;B项,根据总反
应式可知,负极反应式为:KSn-e-=Sn+K+,电池的正极反应式为4K++3CO +4e-=2K CO+C,B正确;C项,
2 2 3
电极材料为KSn和羧基化碳纳米管,KSn与水反应,-COOH与KOH反应,可促进电子的转移,C正确;
D项,充电时阳极反应为:C-4e-+ K CO=3 CO↑+4K+, 碳纳米管及附着的碳酸钾会减少,电路中通过
2 3 2
1mol电子,多壁碳纳米管减重3g,碳酸钾减少30g,D错误;故选D。
8.(2022·广东省汕头市高三期末教学质量监测iPON薄膜锂离子电池是目前研究最广泛的全固态薄膜
锂离子电池。下图为其工作示意图,LiPON薄膜只允许 通过,电池反应为LiSi+Li CoO
x 1-x 2
Si+LiCoO。下列有关说法正确的是。( )
2A.LiPON薄膜在充放电过程中质量发生变化
B.导电介质C可为Li SO 溶液
2 4
C.放电时b极为正极,发生反应:Li CoO+xLi++xe-═LiCoO
1-x 2 2
D.充电时,当外电路通过0.2mol电子时,非晶硅薄膜上质量减少1.4g
【答案】C
【解析】由题干信息中电池总反应可表示为LiSi+Li CoO Si+LiCoO 可知,电极a为非晶硅薄
x 1-x 2 2
膜,充电时Li+得电子成为Li嵌入该薄膜材料中,则电极a为阴极,电极反应式为xLi++xe-+Si=Li Si,电极
x
b为阳极,电极反应式为LiCoO -xe-═Li CoO+xLi+,放电时电极a为负极,电极反应为LiSi-xe-
2 1-x 2 x
═Si+xLi+,电极b为正极,电极反应式为Li CoO+xLi++xe-═LiCoO 。A项,LiPON薄膜在充放电过程中
1-x 2 2
仅仅起到盐桥的作用,并未参与电极反应,故其质量不发生变化,A错误;B项,由于
2Li+2HO=2LiOH+H ↑,故导电介质C中不能有水,则不可为Li SO 溶液,B错误;C项,放电时b极为
2 2 2 4
正极,发生反应:Li CoO+xLi++xe-═LiCoO ,C正确;D项,充电时,电极a为阴极,电极反应式为xLi+
1-x 2 2
+xe-+Si=Li Si,则当外电路通过0.2mol电子时,非晶硅薄膜上质量增重0.2mol×7g∙mol-1=1.4g,D错误;故
x
选C。
9.(2022·山东省日照市高三校际联考三模)盐酸羟胺NH OHCl是一种常见的还原剂和显像剂,其化学
3
性质与NH4Cl类似。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2
所示。不考虑溶液体积的变化,下列说法正确的是( )A.电池工作时,含Fe的催化电极作负极
B.图2中,M为H+和e- ,N为NH OH+
3
C.电池工作时,每消耗 (标准状况),左室溶液质量增加3.3g
D.电池工作一段时间后,正极区溶液的 减小、负极区溶液的 增大
【答案】C
【解析】由图可知,氢元素化合价降低失电子,Pt电极为负极,电极反应式为H-2e- =2H+,含铁的催
2
化电极为正极,电极反应式为NO+4H++Cl-+3e- =NH OHCl。A项,电池工作时,含铁的催化电极作正极,
3
A错误;B项,由题意可知,NH OH具有和氨气类似的弱碱性,可以和盐酸反应生成盐酸羟胺,所以缺少
2
的一步反应为NH OH+H+=NHOH+,图2中M为NH OH,N为NH OH+,B错误;C项,含Fe的催化电极
2 3 2 3
为正极,电极反应式为NO++4H++Cl-+3e- =NH OHCl,2.24LNO标况下是0.1mol,左室增加的质量为
3
0.1molNO和0.3mol氢离子的质量,即0.1mol×30g/mol+0.3mol×1g/mol=3.3g,C正确;D项,原电池工作时,
正极氢离子被消耗,pH增大,负极生成氢离子,pH减小,D错误;故选C。
10.(2022·湖北省新高考高三质量检测)中科院福建物构所YaobingWang团队首次构建了一种可逆水性
Zn—CO 电池,实现了CO 和HCOOH之间的高效可逆转换,其反应原理如图所示:
2 2
已知双极膜可将水解离为H+和OH-,并实现其定向通过。下列说法中错误的是( )A.放电时,负极电极反应式为Zn+4OH--2e-=Zn(OH) 2-
4
B.CO 转化为HCOOH过程中,Zn电极的电势低于多孔Pd电极的
2
C.充电过程中,甲酸在多孔Pd电极表面转化为CO
2
D.当外电路通过2mol电子时,双极膜中离解水的物质的量为1mol
【答案】D
【解析】由图中可知,Zn发生失去电子的反应,为电池的负极;CO 得电子生成HCOOH,多孔Pd为
2
电池的正极。A项,根据图中知,Zn发生失去电子的反应,电极反应式为Zn+4OH--2e-=Zn(OH) 2-,A项正
4
确;B项,CO 转化为HCOOH时为放电过程,Zn电极为负极,多孔Pd电极为正极,负极电势较低,B项
2
正确;C项,充电过程中,HCOOH转化为CO,C项正确;D项,根据溶液呈电中性,可知外电路通过
2
2mol电子时,双极膜中离解的水的物质的量为2mol,D项错误。故选D。
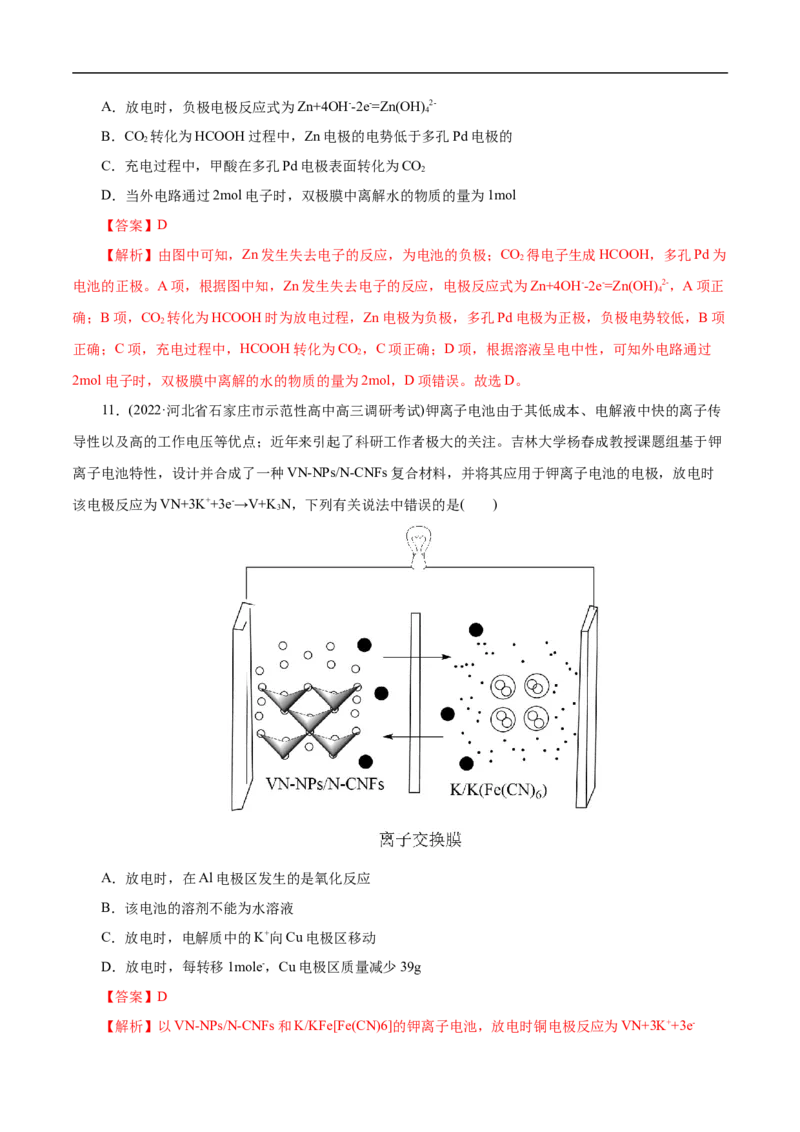
11.(2022·河北省石家庄市示范性高中高三调研考试)钾离子电池由于其低成本、电解液中快的离子传
导性以及高的工作电压等优点;近年来引起了科研工作者极大的关注。吉林大学杨春成教授课题组基于钾
离子电池特性,设计并合成了一种VN-NPs/N-CNFs复合材料,并将其应用于钾离子电池的电极,放电时
该电极反应为VN+3K++3e-→V+KN,下列有关说法中错误的是( )
3
A.放电时,在Al电极区发生的是氧化反应
B.该电池的溶剂不能为水溶液
C.放电时,电解质中的K+向Cu电极区移动
D.放电时,每转移1mole-,Cu电极区质量减少39g
【答案】D
【解析】以VN-NPs/N-CNFs和K/KFe[Fe(CN)6]的钾离子电池,放电时铜电极反应为VN+3K++3e-→V+KN,故放电时Cu电极为正极,Al电极为负极。A项,放电时,Al电极为负极,在Al电极区发生的
3
是氧化反应,故A正确;B项,电池中含有钾,钾性质活泼能与水反应,故该电池的溶剂为有机溶剂,该
电池的溶剂不能为水溶液,故B正确;C项,放电时,Al电极为负极,钾离子向正极移动,即放电时,电
解质中的K+向Cu电极区移动,故C正确;D项,放电时,铜电极反应为VN+3K++3e-→V+KN,每转移
3
1mole-,Cu电极区质量增加39g,故D错误;故选D。
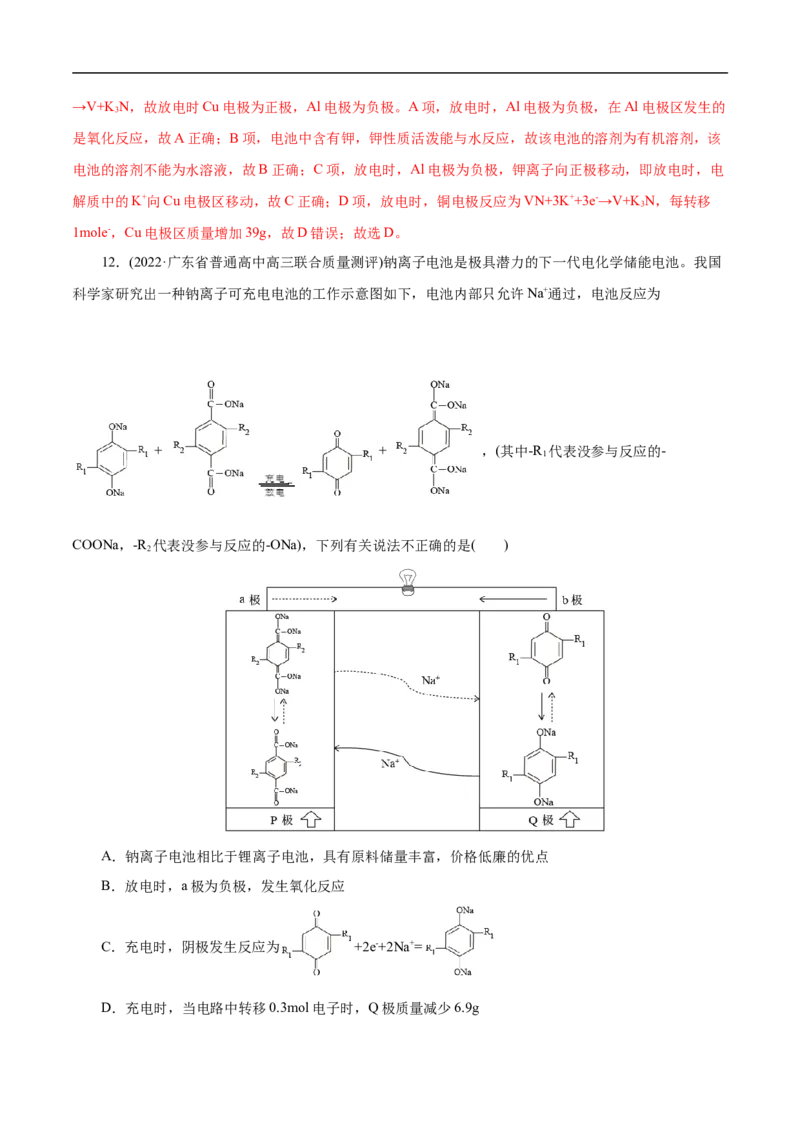
12.(2022·广东省普通高中高三联合质量测评)钠离子电池是极具潜力的下一代电化学储能电池。我国
科学家研究出一种钠离子可充电电池的工作示意图如下,电池内部只允许Na+通过,电池反应为
+ + ,(其中-R 代表没参与反应的-
1
COONa,-R 代表没参与反应的-ONa),下列有关说法不正确的是( )
2
A.钠离子电池相比于锂离子电池,具有原料储量丰富,价格低廉的优点
B.放电时,a极为负极,发生氧化反应
C.充电时,阴极发生反应为 +2e-+2Na+=
D.充电时,当电路中转移0.3mol电子时,Q极质量减少6.9g【答案】C
【解析】依据电池反应 可知,放电过程中负
极发生氧化反应: ,正极发生还原反应:
;而充电过程中阳极发生氧化反应:
,阴极发生还原反应:
。A项,解释钠离子电池相较于锂离子电池的优点,A
项正确;B项,依据电池反应可推断出虚线表示放电过程,根据物质的变化可判断a极为负极,发生氧化反应,B项正确;C项,根据充电时物质的变化结合分析可知,充电时,阴极发生反应为
,C项错误;D项,充电时Na+从Q极转移到P极,且2e-
~Na+,故当转移0.3mol电子时减少0.3mol Na+,质量为6.9g,D项正确;故选C。
13.(2022·山东省济南市高三学情检测)酸性水系锌锰电池在放电时存在电极上MnO 的剥落,会造成
2
电池效率“损失”。最新研究表明,向体系中加入少量KI固体后能使电池持续大电流放电,提高电池的
工作效率,原理如图所示,下列说法错误的是( )
A.加入KI降低了正极反应的活化能
B.I-与剥落的MnO 反应生成的 I-能恢复“损失”的能量
2 3
C.放电时,正极区溶液的pH减小
D.放电时,消耗1 mol Zn时,正极区电解质溶液增重87 g
【答案】CD
【解析】由题干中原电池装置图示可知,Zn所在石墨电极为负极,电极反应为:Zn-2e-=Zn2+,MnO
2
所在的石墨电极为正极,电极反应为:MnO +2e-+4H+=Mn2++2H O,加入KI后的反应机理为:MnO +3I-
2 2 2
+4H+=Mn2++I -+2H O,I-+2e-=3I-。A项,KI参与正极电极反应,且加入少量KI固体后能使电池持续大电
3 2 3
流放电,说明反应速率加快,故降低了正极反应的活化能,A正确;B项,I-与剥落的MnO 反应生成的
2
I-,然后I-能继续从正极上得到电子转化为I-,故能恢复“损失”的能量,B正确;C项,放电时,正极反
3 3
应式为:MnO +2e-+4H+=Mn2++2H O,故正极区溶液的pH增大,C错误;D项,根据得失电子总数相等,
2 2
结合正极反应式:MnO +2e-+4H+=Mn2++2H O可知,放电时,消耗1 mol Zn时,正极区电解质溶液增重87
2 2+4=91g,D错误;故选CD。
14.(2022·北京市西城区一模)氮掺杂的碳材料可以有效催化燃料电池中 的还原反应,其催化机理如
图。
途径一:A→B→C→F
途径二:A→B→C→D→E
下列说法不正确的是( )
A.途径一中存在极性共价键的断裂与形成
B.途径一的电极反应是O+2H++2e- =H O
2 2 2
C.途径二,1mol O 得到4mol
2
D.氮掺杂的碳材料降低了反应的焓变
【答案】D
【解析】A项,由图中信息可知,途径一中有C-O键、O-H键的形成,也有C-O键的断裂,A正确;
B项,途径一的过程中有O 的参与和二次增加H+、e-,最后从催化剂中放出HO,其电极反应是O+2H+
2 2 2 2
+2e- =H O,B正确;C项,途径二中,有O 参与,途中二次增加H+、e-和一次增加2H+、2e-,故1mol O
2 2 2 2
得到4mol e-,C正确;D项,氮掺杂的碳材料降低了反应的活化能,但不能改变焓变,D不正确;故选
D。
15.(2022·四川省成都市一模)如图,甲、乙是两个完全相同的光伏并网发电模拟装置,利用它们对煤
浆进行脱硫处理。下列叙述中错误的是( )A.光伏并网发电装置中b为正极
B.石墨1电极上消耗1molMn2+,甲、乙中各转移0.5mol电子
C.脱硫反应原理为:15Mn3++FeS +8H O=15Mn2++Fe3++2SO2-+16H+
2 2 4
D.处理60gFeS,石墨2电极上消耗7.5molH+
2
【答案】B
【解析】由图可知,石墨1电极上Mn元素价态升高失电子,故石墨1为阳极,电极反应式为Mn2+-e-
=Mn3+,Mn3+与FeS 反应实现脱硫,反应为15Mn3++FeS +8H O═15Mn2++Fe3++2 SO 2-+16H+,石墨2为阴极,
2 2 2 4
电极反应式为2H++2e-=H ↑。A项,石墨1为阳极极,则b极为电源的正极,A正确;B项,石墨1为阳极,
2
电极反应式为Mn2+-e-=Mn3+,消耗1molMn2+,电路中转移1mol电子,B错误;C项,阳极生成的Mn3+与
FeS 反应实现脱硫,反应为15Mn3++FeS +8H O═15Mn2++Fe3++2 SO 2-+16H+,C正确;D项,处理
2 2 2 4
60gFeS,消耗阳极生成的Mn3+的物质的量为 ×15=7.5mol,转移电子7.5mol,石墨2为阴极,电
2
极反应式为2H++2e-=H ↑,石墨2上消耗7.5molH+,D正确;故答案为:B。
2
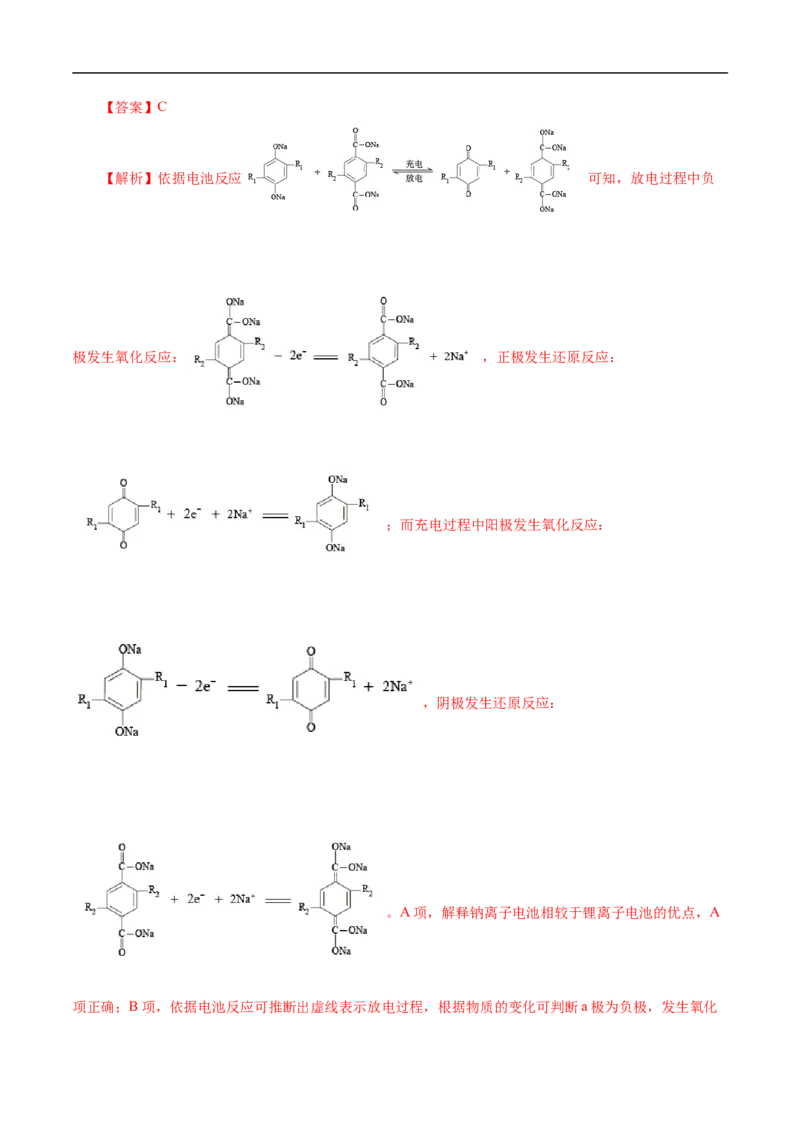
16.(2022·安徽省新未来联盟高三模拟预测)我国科研人员以二硫化钼(MoS )作为电极催化剂,研发出
2
一种Zn-NO电池系统,该电池同时具备合成氨和对外供电的功能,其工作原理如图所示(双极膜可将水解
离成H+和OH-,并实现其定向通过)。下列说法正确的是( )A.外电路中电子从MoS 电极流向Zn/ZnO电极
2
B.双极膜右侧为阴离子交换膜
C.当电路中转移0.2 mol电子时负极质量减小6.5 g
D.使用MoS 电极能加快合成氨的速率
2
【答案】D
【解析】Zn/ZnO电极为负极,失电子发生氧化反应,电极反应式为Zn-2e-+2OH-=ZnO+H O,MoS 电
2 2
极为正极,电极反应式为NO+4H O+5e-=NH+5OH-。A项,电子流向:负极→负载→正极,Zn/ZnO电极
2 3
为负极,MoS 电极为正极,外电路中电子从Zn/ZnO电极流向MoS 电极,故A错误;B项,Zn/ZnO电极
2 2
为负极,电极反应式为Zn-2e-+2OH-=ZnO+H O,OH-移向Zn/ZnO电极,双极膜左侧为阴离子交换膜,故B
2
错误;C项,负极电极反应式为Zn-2e-+2OH-=ZnO+H O,负极由Zn→ZnO,质量增加为O元素质量,转移
2
0.2 mol电子时增加0.1mol氧原子,负极质量增加m=nM=0.1mol×16g/mol=1.6 g,故C错误;D项,结合提
示,科研人员以二硫化钼MoS 作为电极催化剂,催化剂可以降低反应活化能,加快合成氨的反应速率,
2
故D正确;故选D。
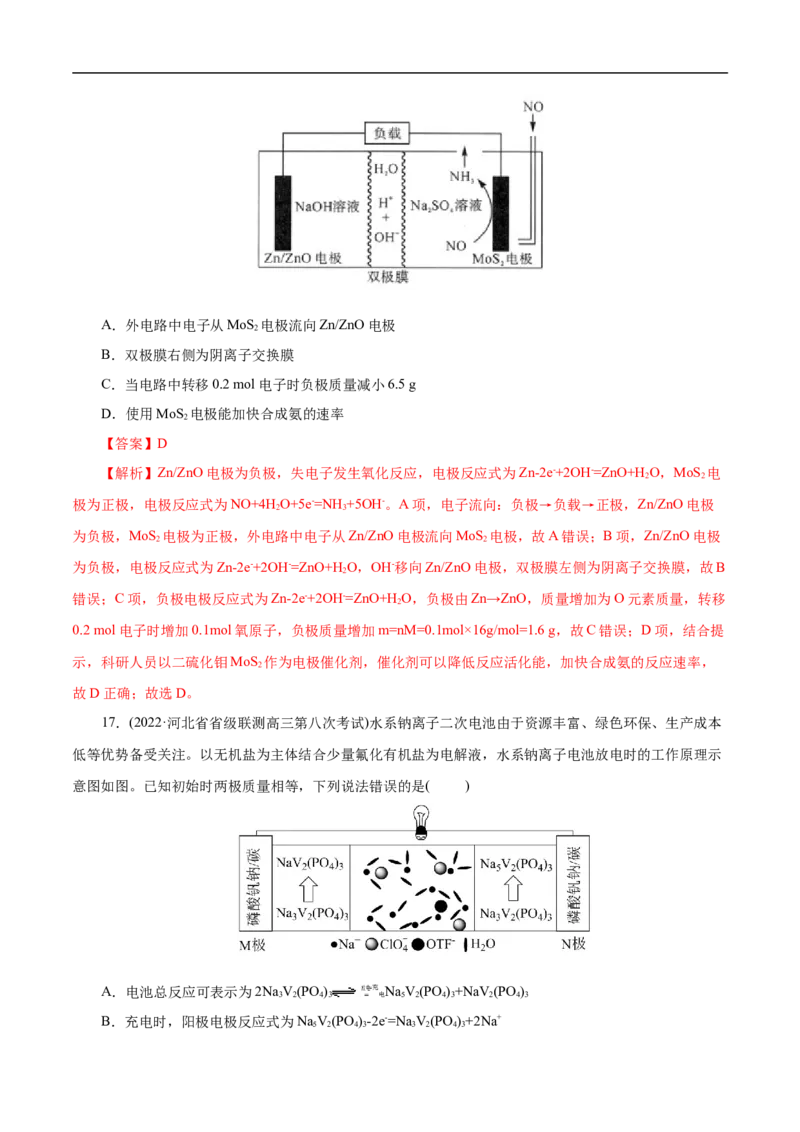
17.(2022·河北省省级联测高三第八次考试)水系钠离子二次电池由于资源丰富、绿色环保、生产成本
低等优势备受关注。以无机盐为主体结合少量氟化有机盐为电解液,水系钠离子电池放电时的工作原理示
意图如图。已知初始时两极质量相等,下列说法错误的是( )
A.电池总反应可表示为2NaV(PO ) 放电=充 NaV(PO )+NaV(PO )
3 2 4 3 == 电 5 2 4 3 2 4 3
B.充电时,阳极电极反应式为NaV(PO )-2e-=Na V(PO )+2Na+
5 2 4 3 3 2 4 3C.充电时,电子由M极经导线流向N极;放电时,M极为负极
D.放电时,电路中通过0.005mol电子时,理论上两极质量差为0.23g
【答案】C
【解析】由题意知该电池属于二次电池,示意图为放电过程,M极NaV(PO ) 转化为NaV (PO ),发
3 2 4 3 2 4 3
生失电子的氧化反应,为负极,N极NaV(PO ) 转化为NaV(PO ),发生得电子的还原反应,为正极,充
3 2 4 3 5 2 4 3
电时为电解池,M极为阴极,N极为阳极。A项,根据上述分析电池总反应可表示为2NaV(PO ) 放电=充
3 2 4 3 == 电
NaV(PO )+NaV(PO ),A项正确;B项,充电时,N极为阳极,阳极电极反应式为NaV(PO )-2e-
5 2 4 3 2 4 3 5 2 4 3
=Na V(PO )+2Na+,B项正确;C项,放电时,M极为负极,但充电时,M极为阴极,是电子流入的一极,
3 2 4 3
C项错误;D项,由电池总反应知,放电时,电路中通过0.005mol电子时,负极减少0.005molNa+的质量,
正极增加0.005molNa+的质量,两极质量差为 ,D项正确。故选C。
18.(2022·河北省沧州市高三二模)火星大气约95%是CO,Li-CO 电池在未来的火星探测领域有着重
2 2
要的应用前景。科学家设计了一系列Ru/M-CPY@ CNT(碳纳米管)杂化材料(M = Co、Zn、Ni、Mn, CNTs
碳纳米管是一种电导率高、比表面积大、通道和孔隙率丰富的导电基底)作为电极。已知该电池放电时的反
应为4Li+3CO=2Li CO+C,下列说法错误的是( )
2 2 3
A.放电时,Li电极作电池负极,有电子经导线流出
B.充电时,每转移1mol电子,两电极的质量变化差值为7g
C.充电时,阳极的电极反应式为C-4e-+2Li CO =3CO ↑+4Li+
2 3 2
D.杂化材料中CNTs增多了CO 的吸附位点,可使该电池表现出优异的电化学性能
2
【答案】B
【解析】由电池放电时的反应可知,Li化合价由0价变成+1价,故是原电池的负极,复杂材料电极是
正极。A项,放电时,Li电极作电池负极,有电子经导线流出,A正确;B项,充电时,阳极C变成二氧
化碳,阴极Li+变成Li,故每转移1mol电子,消耗0.25molC质量为3g,生成1molLi质量为7g,故两电极的质量变化差值为3g+7g=10g,B错误;C项,充电时,阳极上C失电子变成二氧化碳,故阳极的电极反
应式为C-4e-+2Li CO =3CO ↑+4Li+,C正确;D项,CNTs碳纳米管是一种电导率高、比表面积大、通道
2 3 2
和孔隙率丰富的导电基底,增加二氧化碳的吸收效率,故可使该电池表现出优异的电化学性能,D正确;
故选B。
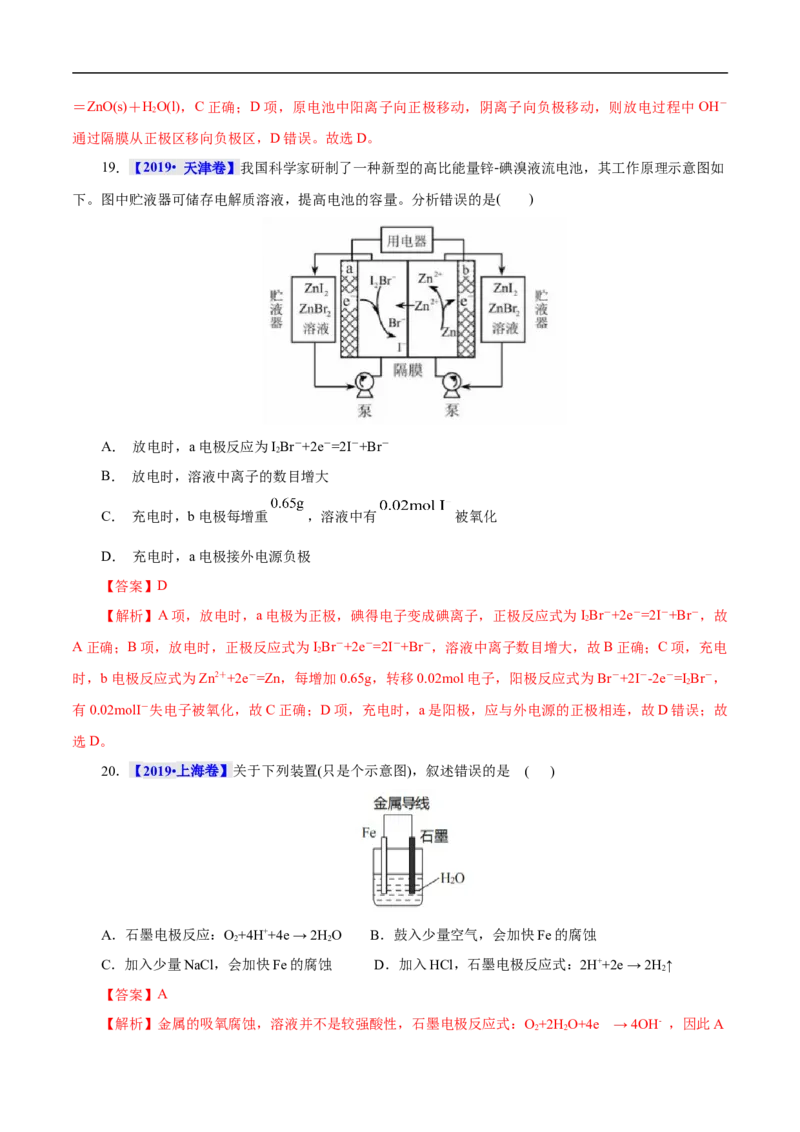
19.(2022·湖北省黄冈中学三模)一种双阴极微生物燃料电池装置如图所示。该装置可以同时进行硝化
和反硝化脱氮,下列叙述正确的是( )
A.电池工作时,H+的迁移方向:左→右
B.电池工作时,“缺氧阴极”电极附近的溶液pH减小
C.“好氧阴极”存在反应:NH +-6e-+ 8OH-=NO-+ 6H O
4 2 2
D.“厌氧阳极”区质量减少28.8g时,该电极输出电子2.4mol
【答案】D
【解析】如图所示,“厌氧阳极”上,C H O 失去电子生成CO 和H+,电极反应式为
6 12 6 2
C H O+6H O-24e-=6CO ↑+24H+;“缺氧阴极”上,NO -得到电子生成NO ,NO 再转化为N,电极反应
6 12 6 2 2 3 2 2 2
式分别为:NO -+e-+2H+=NO↑+H O,2NO +8e-+8H+=N ↑+4H O;“好氧阴极”上,O 得到电子生成HO,
3 2 2 2 2 2 2 2
电极反应式为O+4H++4e-=2H O,同时O 还能氧化NH +生成NO -,NO -还可以被O 氧化为NO -,反应方
2 2 2 4 2 2 2 3
程式分别为2 NH++3O =2 NO -+2H O+4H+,2 NO-+O =2 NO -。A项,电池工作时,“厌氧阳极”失去的
4 2 2 2 2 2 3
电子沿外电路流向“缺氧阴极”和“好氧阴极”,则“厌氧阳极”产生的H+通过质子交换膜向“缺氧阴
极”和“好氧阴极”迁移,故H+的迁移方向既有左(“厌氧阳极”)→右(“好氧阴极”),又有右(“厌氧阳
极”)→左(“缺氧阴极”),A错误;B项,电池工作时,“缺氧阴极”上消耗H+,其附近的溶液pH增大,
B错误;C项,“好氧阴极”上的反应有O+4H++4e-=2H O,2 NH++3O =2 NO -+2H O+4H+,2 NO-+O =2
2 2 4 2 2 2 2 2NO -,C错误;D项,“厌氧阳极”的电极反应式为C H O+6H O-24e-=6CO ↑+24H+,每1mol C H O 反
3 6 12 6 2 2 6 12 6
应,消耗6mol HO,转移24mol电子,“厌氧阳极”区质量减少288g,故“厌氧阳极”区质量减少28.8g
2
时,该电极输出电子2.4mol,D正确;故选D。
1.【2022•全国甲卷】一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以
2
Zn(OH) 2-存在)。电池放电时,下列叙述错误的是( )
4
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 2-通过隔膜向Ⅱ区迁移
4
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) 2-+Mn2++2H O
2 4 2
【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-
=Zn(OH) 2-,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2++2H O;电池在工作过程中,由于
4 2 2 2
两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此
可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO 2-向Ⅱ区移动,Ⅲ区消耗OH-,生成
4
Zn(OH) 2-,Ⅱ区的SO 2-向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。A项,Ⅱ区的K+只能向Ⅰ区移动,A错误;
4 4
B项,Ⅰ区的SO 2-向Ⅱ区移动,B正确;C项,MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C
4 2 2 2
正确;D项,电池的总反应为Zn+4OH-+MnO+4H+=Zn(OH) 2-+Mn2++2H O,D正确;故选A。
2 4 2
2.【2022•湖南选择性考试】海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。
下列说法错误的是( )A.海水起电解质溶液作用
B.N极仅发生的电极反应:2HO+2e-=2OH-+H ↑
2 2
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
【答案】C
【解析】锂海水电池的总反应为2Li+2HO═2LiOH+H ↑, M极上Li失去电子发生氧化反应,则M电
2 2
极为负极,电极反应为Li-e-=Li+,N极为正极,电极反应为2HO+2e-=2OH-+H ↑。A项,海水中含有丰富
2 2
的电解质,如氯化钠、氯化镁等,可作为电解质溶液,故A正确;B项,N为正极,电极反应为2HO+2e-
2
=2OH-+H ↑,故B正确;C项,Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,但不能
2
传导离子,故C错误;D项,该电池不可充电,属于一次电池,故D正确;故选C。
3.【2022•广东选择性考试】科学家基于Cl 易溶于CCl 的性质,发展了一种无需离子交换膜的新型
2 4
氯流电池,可作储能设备(如图)。充电时电极a的反应为:NaTi (PO )+2Na++2e-= Na Ti (PO )。下列说法
2 4 3 3 2 4 3
正确的是( )
A.充电时电极b是阴极
B.放电时NaCl溶液的 减小C.放电时NaCl溶液的浓度增大
D.每生成1molCl ,电极a质量理论上增加23g
2
【答案】C
【解析】A项,由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电
极b是阳极,故A错误;B项,放电时电极反应和充电时相反,则由放电时电极a的反应为NaTi (PO )-
3 2 4 3
2e-= NaTi (PO )+2Na+可知,NaCl溶液的pH不变,故B错误;C项,放电时负极反应为NaTi (PO )-2e-=
2 4 3 3 2 4 3
NaTi (PO )+2Na+,正极反应为Cl+2e-=2Cl-,反应后Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,
2 4 3 2
故C正确;D项,充电时阳极反应为2Cl- -2e-= Cl ↑,阴极反应为NaTi (PO )+2Na++2e-= Na Ti (PO ),由
2 2 4 3 3 2 4 3
得失电子守恒可知,每生成1molCl ,电极a质量理论上增加23g/mol 2mol=46g,故D错误;故选C。
2
4.【2022·浙江省1月选考】pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,以玻璃电
极(在特制玻璃薄膜球内放置已知浓度的HCl溶液,并插入Ag—AgCl电极)和另一Ag—AgCl电极插入待测
溶液中组成电池,pH与电池的电动势E存在关系:pH=(E-常数)/0.059。下列说法正确的是( )
A.如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-=Ag(s)+Cl(0.1mol·L-1)
B.玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C.分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH
D.pH计工作时,电能转化为化学能
【答案】C
【解析】A项,如果玻璃薄膜球内电极的电势低,则该电极为负极、负极发生氧化反应而不是还原反
应,A错误;B项,已知:pH与电池的电动势E存在关系:pH=(E-常数)/0.059,则玻璃膜内外氢离子浓度
的差异会引起电动势的变化,B错误;C项,pH与电池的电动势E存在关系:pH=(E-常数)/0.059,则分别
测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH,C正确;D项,pH计工作
时,利用原电池原理,则化学能转化为电能,D错误;故选C。
5.【2022•山东卷】设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成
CO,将废旧锂离子电池的正极材料LiCoO 转化为Co2+,工作时保持厌氧环境,并定时将乙室溶液转移至
2 2
甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是( )A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为LiCoO +2H O+e-+4H+=Li++Co2++4OH-
2 2
D.若甲室Co2+减少 ,乙室Co2+增加 ,则此时已进行过溶液转移
【答案】BD
【解析】A项,依据题意右侧装置为原电池,电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被
氧化为CO 气体,Co2+在另一个电极上得到电子,被还原产生Co单质,CHCOO-失去电子后,Na+通过阳
2 3
膜进入阴极室,溶液变为NaCl溶液,溶液由碱性变为中性,溶液pH减小,A错误;B项,对于乙室,正
极上LiCoO 得到电子,被还原为Co2+,同时得到Li+,其中的O与溶液中的H+结合HO,因此电池工作一
2 2
段时间后应该补充盐酸,B正确;C项,电解质溶液为酸性,不可能大量存在OH-,乙室电极反应式为:
LiCoO +e-+4H+=Li++Co2++2H O,C错误;D项,若甲室Co2+减少200 mg,电子转移物质的量为n(e-)=
2 2
,乙室Co2+增加300 mg,转移电子的物质的量为n(e-)= ,说
明此时已进行过溶液转移,D正确;故选BD。
6.【2021•全国甲卷】化学与人体健康及环境保护息息相关。下列叙述正确的是( )
A.食品加工时不可添加任何防腐剂 B.掩埋废旧电池不会造成环境污染
C.天然气不完全燃烧会产生有毒气体 D.使用含磷洗涤剂不会造成水体污染
【答案】C
【解析】A项,食品加工时,可适当添加食品添加剂和防腐剂等,如苯甲酸钠,故A错误;B项,废
旧电池中含有重金属等金属离子,会造成土壤污染,水体污染等,故B错误;C项,天然气主要成分为甲
烷,不完全燃烧会产生一氧化碳等有毒气体,故C正确;D项,含磷洗涤剂的排放,使水中磷过多,造成水中藻类疯长,消耗水中溶解的氧,水体变浑浊,故D错误;故选C。
7.【2021•河北选择性考试】K—O 电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该
2
电池,下列说法错误的是( )
A.隔膜允许K+通过,不允许O 通过
2
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO 的质量与消耗O 的质量比值约为2.22
2 2
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
【答案】D
【解析】由图可知,a电极为原电池的负极,单质钾片失去电子发生氧化反应生成钾离子,电极反应
式为K—e-=K+,b电极为正极,在钾离子作用下,氧气在正极得到电子发生还原反应生成超氧化钾。A项,
金属性强的金属钾易与氧气反应,为防止钾与氧气反应,电池所选择隔膜应允许K+通过,不允许O 通过,
2
故A正确;B项,由分析可知,放电时,a为负极,b为正极,电流由b电极沿导线流向a电极,充电时,
b电极应与直流电源的正极相连,做电解池的为阳极,故B正确;C项,由分析可知,生成1mol超氧化钾
时,消耗1mol氧气,两者的质量比值为1mol×71g/mol:1mol×32g/mol≈2.22:1,故C正确;D项,铅酸蓄
电池充电时的总反应方程式为2PbSO +2H O=PbO +Pb+2H SO ,反应消耗2mol水,转移2mol电子,由得
4 2 2 2 4
失电子数目守恒可知,耗3.9g钾时,铅酸蓄电池消耗水的质量为 ×18g/mol=1.8g,故D错误;故
选D。
8.【2021•湖南选择性考试】锌/溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储
能和智能电网的备用电源等。三单体串联锌/溴液流电池工作原理如图所示:下列说法错误的是( )
A.放电时,N极为正极
B.放电时,左侧贮液器中ZnBr 的浓度不断减小
2
C.充电时,M极的电极反应式为Zn2++2e﹣═Zn
D.隔膜允许阳离子通过,也允许阴离子通过
【答案】B
【解析】锌溴液流电池总反应为:Zn+Br ═ZnBr ,其中N为正极,发生还原反应,电极反应方程式为
2 2
Br +2e﹣=2Br﹣,M为负极,发生氧化反应,电极反应方程式为Zn﹣2e﹣=Zn2+,放电过程中,左侧Zn2+流
2
向右侧,左侧ZnBr 的浓度不断减少,充电过程中,发生反应ZnBr Zn+Br 。A项,依据分析可知,N
2 2 2
为正极,故A正确;B项,放电时,左侧为负极,发生氧化反应,电极反应方程式为 Zn﹣2e﹣=Zn2+,左
侧生成的Zn2+流向右侧,故左侧ZnBr 的浓度不变,右侧ZnBr 的浓度变大,故B错误;C项,.放电时,M
2 2
为负极,充电时,M及为阴极,发生还原反应,电极反应式为 Zn2++2e﹣═Zn,故C正确;D项,中间沉积
锌位置的作用为提供电解液,故其隔膜既可以允许阳离子通过,也允许阴离子通过,故D正确;故选B。
9.【2021•浙江6月 选考】某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电
时Li+得电子成为Li嵌入该薄膜材料中;电极B为LiCoO 薄膜;集流体起导电作用。下列说法不正确的是
2
( )
A.充电时,集流体A与外接电源的负极相连B.放电时,外电路通过a mol电子时,LiPON薄膜电解质损失a mol Li+
C.放电时,电极B为正极,反应可表示为Li CoO+ xLi+xe-= LiCoO
1- x 2 2
D.电池总反应可表示为Li Si+Li CoO Si+LiCoO
x 1- x 2 2
【答案】B
【解析】由题中信息可知,该电池充电时Li+得电子成为Li嵌入电极A中,可知电极A在充电时作阴
极,故其在放电时作电池的负极,而电极B是电池的正极。A项,由图可知,集流体A与电极A相连,充
电时电极A作阴极,故充电时集流体A与外接电源的负极相连,A正确;B项,放电时,外电路通过a
mol电子时,内电路中有a mol Li+通过LiPON薄膜电解质从负极迁移到正极,但是LiPON薄膜电解质没有
损失Li+,B不正确;C项,放电时,电极B为正极,发生还原反应,反应可表示为Li CoO+ xLi+xe-=
1- x 2
LiCoO ,C正确;D项,电池放电时,嵌入在非晶硅薄膜中的锂失去电子变成Li+,正极上Li CoO 得到
2 1- x 2
电子和Li+变为LiCoO ,故电池总反应可表示为Li Si+Li CoO Si+LiCoO,D正确。故选B。
2 x 1- x 2 2
10.【2021•浙江1月 选考】镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,K、K 为开
1 2
关,a、b为直流电源的两极)。
下列说法不正确的是( )
A.断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B.断开K、合上K,电极A为阴极,发生还原反应
1 2
C.电极B发生氧化反应过程中,溶液中KOH浓度不变
D.镍镉二次电池的总反应式:Cd+ 2NiOOH+2H O Ca(OH) +2Ni(OH)
2 2 2
【答案】C
【解析】根据图示,电极A充电时为阴极,则放电时电极A为负极,负极上Cd失电子发生氧化反应
生成Cd(OH) ,负极反应式为Cd-2e-+2OH-=Cd(OH) ,电极B充电时为阳极,则放电时电极B为正极,正
2 2
极上NiOOH得电子发生还原反应生成Ni(OH) ,正极反应式为2NiOOH+2e-+2H O=2Ni(OH) +2OH-,放电
2 2 2时总反应为Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) 。A项,断开K、合上K,为放电过程,镍镉电池能量
2 2 2 2 1
转化形式:化学能→电能,A正确;B项,断开K、合上K,为充电过程,电极A与直流电源的负极相连,
1 2
电极A为阴极,发生还原反应,电极反应式为Cd(OH) +2e-=Cd+2OH-,B正确;C项,电极B发生氧化反
2
应的电极反应式为2Ni(OH) -2e-+2OH-=2NiOOH+2H O,则电极A发生还原反应的电极反应式为
2 2
Cd(OH) +2e-=Cd+2OH-,此时为充电过程,总反应为Cd(OH) +2Ni(OH) Cd+2NiOOH+2H O,溶液中
2 2 2 2
KOH浓度减小,C错误;D项,根据分析,放电时总反应为Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) ,则镍
2 2 2
镉二次电池总反应式为Cd+2NiOOH+2H O Cd(OH) +2Ni(OH) ,D正确;故选C。
2 2 2
11.【2020•新课标Ⅰ卷】科学家近年发明了一种新型Zn−CO 水介质电池。电池示意图如图,电极为
2
金属锌和选择性催化材料,放电时,温室气体CO 被转化为储氢物质甲酸等,为解决环境和能源问题提供
2
了一种新途径。
下列说法错误的是( )
A.放电时,负极反应为Zn-2e-+4OH-=Zn(OH) 2+
4
B.放电时,1 mol CO 转化为HCOOH,转移的电子数为2 mol
2
C.充电时,电池总反应为2Zn(OH) 2+=2 Zn+O ↑+4OH-+2H O
4 2 2
D.充电时,正极溶液中OH−浓度升高
【答案】D
【解析】由题可知,放电时,CO 转化为HCOOH,即CO 发生还原反应,故放电时右侧电极为正极,
2 2
左侧电极为负极,Zn发生氧化反应生成Zn(OH) 2+;充电时,右侧为阳极,HO发生氧化反应生成O,左
4 2 2
侧为阴极,Zn(OH) 2+发生还原反应生成Zn。A项,放电时,负极上Zn发生氧化反应,电极反应式为:
4
Zn-2e-+4OH-=Zn(OH) 2+,故A正确,不选;B项,放电时,CO 转化为HCOOH,C元素化合价降低2,则
4 2
1molCO 转化为HCOOH时,转移电子数为2mol,故B正确,不选;C项,充电时,阳极上HO转化为
2 2
O,负极上Zn(OH) 2+转化为Zn,电池总反应为:2Zn(OH) 2+=2 Zn+O ↑+4OH-+2H O,故C正确,不选;D
2 4 4 2 2项,充电时,正极即为阳极,电极反应式为:2HO-4e-=4H++O ↑,溶液中H+浓度增大,溶液中
2 2
c(H+)•c(OH-)=K ,温度不变时,K 不变,因此溶液中OH-浓度降低,故D错误,符合题意;故选D。
W W
12.【2020•新课标Ⅱ卷】电致变色器件可智能调控太阳光透过率,从而实现节能。下图是某电致变色
器件的示意图。当通电时,Ag+注入到无色WO 薄膜中,生成AgWO,器件呈现蓝色,对于该变化过程,
3 x 3
下列叙述错误的是( )
A.Ag为阳极 B.Ag+由银电极向变色层迁移
C.W元素的化合价升高 D.总反应为:WO+xAg=AgWO
3 x 3
【答案】C
【解析】从题干可知,当通电时,Ag+注入到无色WO 薄膜中,生成Ag WO 器件呈现蓝色,说明通
3 x 3
电时,Ag电极有Ag+生成然后经固体电解质进入电致变色层,说明Ag电极为阳极,透明导电层时阴极,
故Ag电极上发生氧化反应,电致变色层发生还原反应。A项,通电时,Ag电极有Ag+生成,故Ag电极为
阳极,故A项正确;B项,通电时电致变色层变蓝色,说明有Ag+从Ag电极经固体电解质进入电致变色层,
故B项正确;C项,过程中,W由WO 的+6价降低到Ag WO 中的+(6-x)价,故C项错误;D项,该电解
3 x 3
池中阳极即Ag电极上发生的电极反应为:xAg-xe-= xAg+,而另一极阴极上发生的电极反应为:WO+xAg+
3
+xe- = AgxWO,故发生的总反应式为:xAg + WO =Ag WO,故D项正确;故选C。
3 3 x 3
13.【2020•新课标Ⅲ卷】一种高性能的碱性硼化钒(VB )—空气电池如下图所示,其中在VB 电极发
2 2
生反应:VB +16OH--11e-= VO 3-+2B(OH) -+ 4H O,该电池工作时,下列说法错误的是( )
2 4 4 2
A.负载通过0.04 mol电子时,有0.224 L(标准状况)O 参与反应
2
B.正极区溶液的pH降低、负极区溶液的pH升高C.电池总反应为4VB +11O +20OH-+6H O=8B(OH) -+4VO3-
2 2 2 4 4
D.电流由复合碳电极经负载、VB 电极、KOH溶液回到复合碳电极
2
【答案】B
【解析】根据图示的电池结构,左侧VB 发生失电子的反应生成VO 3-和B(OH) -,反应的电极方程式
2 4 4
如题干所示,右侧空气中的氧气发生得电子的反应生成OH-,反应的电极方程式为O+4e-+2H O=4OH-,电
2 2
池的总反应方程式为4VB +11O +20OH-+6H O=8B(OH) -+4VO3-。A项,当负极通过0.04mol电子时,正极
2 2 2 4 4
也通过0.04mol电子,根据正极的电极方程式,通过0.04mol电子消耗0.01mol氧气,在标况下为0.224L,
A正确;B项,反应过程中正极生成大量的OH-使正极区pH升高,负极消耗OH-使负极区OH-浓度减小pH
降低,B错误;C项,根据分析,电池的总反应为4VB +11O +20OH-+6H O=8B(OH) -+4VO3-,C正确;D
2 2 2 4 4
项,电池中,电子由VB 电极经负载流向复合碳电极,电流流向与电子流向相反,则电流流向为复合碳电
2
极→负载→VB 电极→KOH溶液→复合碳电极,D正确;故选B。
2
14.【2020• 天津卷】熔融钠-硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为
2Na+xS NaS (x=5~3,难溶于熔融硫),下列说法错误的是( )
2 x
A.NaS 的电子式为
2 4
B.放电时正极反应为2Na++xS+2e-= Na S
2 x
C.Na和NaS 分别为电池的负极和正极
2 x
D.该电池是以Na —β—AlO 为隔膜的二次电池
2 3
【答案】C
【解析】根据电池反应:2Na+xS NaS 可知,放电时,钠作负极,发生氧化反应,电极反应为:
2 x
Na-e-= Na+,硫作正极,发生还原反应,电极反应为2Na++xS+2e-= Na S。A项,NaS 属于离子化合物,4
2 x 2 4
个硫原子间形成三对共用电子对,电子式为 ,故A正确;B项,放电时发生的是
原电池反应,正极发生还原反应,电极反应为:2Na++xS+2e-= Na S,故B正确;C项,放电时,Na为电
2 x池的负极,正极为硫单质,故C错误;D项,放电时,该电池是以钠作负极,硫作正极的原电池,充电时,
是电解池,Na —β—AlO 为隔膜,起到电解质溶液的作用,该电池为二次电池,故D正确;故选C。
2 3
15.【2020• 山东卷】微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得
电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含
CHCOO-的溶液为例)。下列说法错误的是( )
3
A.负极反应为 CHCOOˉ+2H O-8eˉ=2CO↑+7H+
3 2 2
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
【答案】B
【解析】据图可知a极上CHCOOˉ转化为CO 和H+,C元素被氧化,所以a极为该原电池的负极,则b
3 2
极为正极。A项,a极为负极,CHCOOˉ失电子被氧化成CO 和H+,结合电荷守恒可得电极反应式为
3 2
CHCOOˉ+2H O-8eˉ=2CO↑+7H+,故A正确;B项,为了实现海水的淡化,模拟海水中的氯离子需要移向
3 2 2
负极,即a极,则隔膜1为阴离子交换膜,钠离子需要移向正极,即b极,则隔膜2为阳离子交换膜,故B
错误;C项,当电路中转移1mol电子时,根据电荷守恒可知,海水中会有1molClˉ移向负极,同时有
1molNa+移向正极,即除去1molNaCl,质量为58.5g,故C正确;D项,b极为正极,水溶液为酸性,所以
氢离子得电子产生氢气,电极反应式为2H++2eˉ=H↑,所以当转移8mol电子时,正极产生4mol气体,根
2
据负极反应式可知负极产生2mol气体,物质的量之比为4:2=2:1,故D正确;故选B。
13.【2020• 江苏卷】(2) HCOOH燃料电池。研究 HCOOH燃料电池性能的装置如图-2所示,两电极
区间用允许K+、H+通过的半透膜隔开。①电池负极电极反应式为_____________;放电过程中需补充的物质A为_________(填化学式)。
②图-2所示的 HCOOH燃料电池放电的本质是通过 HCOOH与O 的反应,将化学能转化为电能,其
2
反应的离子方程式为_______________。
【答案】(2)①HCOOˉ+2OHˉ-2eˉ= HCO -+H O H SO
3 2 2 4
②2HCOOH+O +2OHˉ = 2 HCO -+2H O或2HCOOˉ+O = 2 HCO-
2 3 2 2 3
【解析】(2)①左侧为负极,碱性环境中HCOOˉ失电子被氧化为HCO -,根据电荷守恒和元素守恒可
3
得电极反应式为HCOOˉ+2OHˉ-2eˉ= HCO -+H O;电池放电过程中,钾离子移向正极,即右侧,根据图示
3 2
可知右侧的阴离子为硫酸根,而随着硫酸钾不断被排除,硫酸根逐渐减少,铁离子和亚铁离子进行循环,
所以需要补充硫酸根,为增强氧气的氧化性,溶液最好显酸性,则物质A为HSO ;②根据装置图可知电
2 4
池放电的本质是HCOOH在碱性环境中被氧气氧化为HCO -,根据电子守恒和电荷守恒可得离子方程式为
3
2HCOOH+O +2OHˉ = 2 HCO -+2H O或2HCOOˉ+O = 2 HCO-。
2 3 2 2 3
17.【2019•新课标Ⅰ卷】利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极
与酶之间传递电子,示意图如下所示。下列说法错误的是( )
A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B. 阴极区, 氢化酶作用下发生反应H+2MV2+=2H++2MV+
2
C. 正极区,固氮酶 催化剂,N 发生还原反应生成NH
2 3
D. 电池工作时质子通过交换膜由负极区向正极区移动【答案】B
【解析】由生物燃料电池的示意图可知,左室电极为燃料电池的负极,MV+在负极失电子发生氧化反
应生成MV2+,电极反应式为MV+—e—= MV2+,放电生成的MV2+在氢化酶的作用下与H 反应生成H+和
2
MV+,反应的方程式为H+2MV2+=2H++2MV+;右室电极为燃料电池的正极,MV2+在正极得电子发生还原
2
反应生成MV+,电极反应式为MV2++e—= MV+,放电生成的MV+与N 在固氮酶的作用下反应生成NH 和
2 3
MV2+,反应的方程式为N+6H++6MV+=6MV2++NH ,电池工作时,氢离子通过交换膜由负极向正极移动。
2 3
A项,相比现有工业合成氨,该方法选用酶作催化剂,条件温和,同时利用 MV+和MV2+的相互转化,化
学能转化为电能,故可提供电能,故A正确;B项,左室为负极区,MV+在负极失电子发生氧化反应生成
MV2+,电极反应式为MV+—e—= MV2+,放电生成的MV2+在氢化酶的作用下与H 反应生成H+和MV+,反
2
应的方程式为H+2MV2+=2H++2MV+,故B错误;C项,右室为正极区,MV2+在正极得电子发生还原反应
2
生成 MV+,电极反应式为 MV2++e—= MV+,放电生成的 MV+与N 在固氮酶的作用下反应生成 NH 和
2 3
MV2+,故C正确;D项,电池工作时,氢离子(即质子)通过交换膜由负极向正极移动,故 D正确。故选
B。
18.【2019•新课标Ⅲ卷】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D−Zn)
可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D−Zn—NiOOH二次电池,结构如下图所示。电
池反应为Zn(s)+2NiOOH(s)+H O(l) ZnO(s)+2Ni(OH) (s)。下列说法错误的是( )
2 2
A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B. 充电时阳极反应为Ni(OH) (s)+OH−(aq)−e−=NiOOH(s)+H O(l)
2 2
C. 放电时负极反应为Zn(s)+2OH−(aq)−2e−=ZnO(s)+H O(l)
2
D. 放电过程中OH−通过隔膜从负极区移向正极区
【答案】D
【解析】A项,三维多孔海绵状Zn具有较高的表面积,吸附能力强,所沉积的ZnO分散度高,A正
确;B项,充电相当于是电解池,阳极发生失去电子的氧化反应,根据总反应式可知阳极是Ni(OH) 失去
2
电子转化为NiOOH,电极反应式为Ni(OH) (s)+OH-(aq)-e-=NiOOH(s)+HO(l),B正确;C项,放电时
2 2
相当于是原电池,负极发生失去电子的氧化反应,根据总反应式可知负极反应式为Zn(s)+2OH-(aq)-2e-=ZnO(s)+HO(l),C正确;D项,原电池中阳离子向正极移动,阴离子向负极移动,则放电过程中 OH-
2
通过隔膜从正极区移向负极区,D错误。故选D。
19.【2019• 天津卷】我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如
下。图中贮液器可储存电解质溶液,提高电池的容量。分析错误的是( )
A. 放电时,a电极反应为IBr-+2e-=2I-+Br-
2
B. 放电时,溶液中离子的数目增大
C. 充电时,b电极每增重 ,溶液中有 被氧化
D. 充电时,a电极接外电源负极
【答案】D
【解析】A项,放电时,a电极为正极,碘得电子变成碘离子,正极反应式为IBr-+2e-=2I-+Br-,故
2
A正确;B项,放电时,正极反应式为IBr-+2e-=2I-+Br-,溶液中离子数目增大,故B正确;C项,充电
2
时,b电极反应式为Zn2++2e-=Zn,每增加0.65g,转移0.02mol电子,阳极反应式为Br-+2I--2e-=I Br-,
2
有0.02molI-失电子被氧化,故C正确;D项,充电时,a是阳极,应与外电源的正极相连,故D错误;故
选D。
20.【2019•上海卷】关于下列装置(只是个示意图),叙述错误的是 ( )
A.石墨电极反应:O+4H++4e → 2H O B.鼓入少量空气,会加快Fe的腐蚀
2 2
C.加入少量NaCl,会加快Fe的腐蚀 D.加入HCl,石墨电极反应式:2H++2e → 2H ↑
2
【答案】A
【解析】金属的吸氧腐蚀,溶液并不是较强酸性,石墨电极反应式:O+2H O+4e → 4OH- ,因此A
2 2选项错误
21.【2019•浙江4月 选考】化学电源在日常生活和高科技领域中都有广泛应用。
下列说法不正确的是( )
A.甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.乙:正极的电极反应式为Ag O+2e−+HO===2Ag+2OH−
2 2
C.丙:锌筒作负极,发生氧化反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
【答案】A
【解析】A.甲装置属于原电池,Zn较Cu活泼,做负极,Zn失电子变Zn2+,电子经导线转移到铜电
极,铜电极负电荷变多,吸引了溶液中的阳离子,因而Zn2+和H+向Cu电极方向移动,H+氧化性较强,得
电子变H ,2H++2e=H↑,因而c(H+)减小,A项错误;B. Ag O作正极,得到来自Zn失去的电子,被还
2 2 2
原成Ag,结合KOH作电解液,故电极反应式为Ag O+2e−+HO 2Ag+2OH−,B项正确;C.Zn为较
2 2
活泼电极,做负极,发生氧化反应,电极反应式为 Zn-2e-=Zn2+,锌溶解,因而锌筒会变薄,C项正确;
D.铅蓄电池总反应式为PbO + Pb + 2H SO 2PbSO + 2H O,可知放电一段时间后,HSO 不断
2 2 4 4 2 2 4
被消耗,因而电解质溶液的酸性减弱,导电能力下降,D项正确。故选A。
22.【2018•新课标Ⅱ卷】我国科学家研发了一种室温下“可呼吸”的Na—CO 二次电池。将NaClO
2 4
溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO+4Na
2
2NaCO+C。下列说法错误的是( )
2 3
A.放电时,ClO -向负极移动
4B.充电时释放CO,放电时吸收CO
2 2
C.放电时,正极反应为:3CO+4e− =2CO2-+C
2 3
D.充电时,正极反应为:Na++e−=Na
【答案】D
【解析】A项,放电时是原电池,阴离子ClO -向负极移动,A正确;B项,电池的总反应为3CO+4Na
4 2
2NaCO+C,因此充电时释放CO ,放电时吸收CO ,B正确;C项,放电时是原电池,正极是二氧
2 3 2 2
化碳得到电子转化为碳,反应为:3CO+4e−=2CO2-+C,C正确;D项,充电时是电解,正极与电源的正
2 3
极相连,作阳极,发生失去电子的氧化反应,反应为2CO2-+C-4e−=3CO,D错误。
3 2
23.【2018•新课标Ⅲ卷】一种可充电锂-空气电池如图所示。当电池放电时,O 与Li+在多孔碳材料电
2
极处生成LiO (x=0或1)。下列说法正确的是( )
2 2-x
A.放电时,多孔碳材料电极为负极
B.放电时,外电路电子由多孔碳材料电极流向锂电极
C.充电时,电解质溶液中Li+向多孔碳材料区迁移
D.充电时,电池总反应为LiO =2Li+(1-x/2)O
2 2-x 2
【答案】D
【解析】A项,题目叙述为:放电时,O 与Li+在多孔碳电极处反应,说明电池内,Li+向多孔碳电极移
2
动,因为阳离子移向正极,所以多孔碳电极为正极,A错误;B项,因为多孔碳电极为正极,外电路电子
应该由锂电极流向多孔碳电极(由负极流向正极),B错误;C项,充电和放电时电池中离子的移动方向应该
相反,放电时,Li+向多孔碳电极移动,充电时向锂电极移动,C错误;D项,根据图示和上述分析,电池
的正极反应应该是O 与Li+得电子转化为LiO ,电池的负极反应应该是单质Li失电子转化为Li+,所以总
2 2 2-X
反应为:2Li + (1-x/2)O = LiO ,充电的反应与放电的反应相反,所以为LiO = 2Li + (1-x/2)O,
2 2 2-X 2 2-X 2
选项D正确。
24.【2018•北京卷】验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。① ② ③
在Fe表面生成蓝色沉淀 试管内无明显变化 试管内生成蓝色沉淀
下列说法不正确的是( )
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K[Fe(CN) ]可能将Fe氧化
3 6
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
【答案】D
【解析】A项,对比②③,②Fe附近的溶液中加入K[Fe(CN) ]无明显变化,②Fe附近的溶液中不含
3 6
Fe2+,③Fe附近的溶液中加入K[Fe(CN) ]产生蓝色沉淀,③Fe附近的溶液中含Fe2+,②中Fe被保护,A
3 6
项正确;B项,①加入K[Fe(CN) ]在Fe表面产生蓝色沉淀,Fe表面产生了Fe2+,对比①②的异同,①可
3 6
能是K[Fe(CN) ]将Fe氧化成Fe2+,B项正确;C项,对比①②,①加入K[Fe(CN) ]在Fe表面产生蓝色沉
3 6 3 6
淀,①也能检验出Fe2+,不能用①的方法验证Zn保护Fe,C项正确;D项,由实验可知K[Fe(CN) ]可能
3 6
将Fe氧化成Fe2+,将Zn换成Cu不能用①的方法证明Fe比Cu活泼,D项错误。
25.【2018•天津卷】CO 是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
2
(3)O 辅助的Al~CO 电池工作原理如图4所示。该电池电容量大,能有效利用CO ,电池反应产物
2 2 2
Al (C O) 是重要的化工原料。
2 2 4 3电池的负极反应式:________。
电池的正极反应式:6O+6e−=6O − 6CO +6O −=3C O2−
2 2 2 2 2 4
反应过程中O 的作用是________。该电池的总反应式:________。
2
【答案】(3)CO 2- 10 +120 kJ·mol-1 B 900 ℃时,合成气产率已经较高,再升高温度产率增幅不大,
3
但能耗升高,经济效益降低。 Al–3e–=Al3+(或2Al–6e–=2Al3+) 催化剂 2Al+6CO =Al(C O)
2 2 2 4 3
【解析】(3)明显电池的负极为Al,所以反应一定是Al失电子,该电解质为氯化铝离子液体,所以Al
失电子应转化为Al3+,方程式为:Al–3e–=Al3+(或2Al–6e–=2Al3+)。根据电池的正极反应,氧气再第一步被
消耗,又在第二步生成,所以氧气为正极反应的催化剂。将方程式加和得到,总反应为:
2Al+6CO =Al(C O)。
2 2 2 4 3