文档内容
考点 19 分子结构与性质、化学键
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................2
.............................................................................................................................................2
考法01 共价键及键参数...........................................................................................................................2
考法02 分子的空间结构...........................................................................................................................5
考法03 分子间作用力与分子的性质.......................................................................................................8
考法04 化学键与物质类别.....................................................................................................................12
...........................................................................................................................................15
1.高考真题考点分布
考点内容 考点分布
2024·山东卷,3分;2024·新课标卷,6分;2024·浙江卷,2分;2023山东卷16(2)
共价键及键参
题,12分;2022海南卷11题,4分;2022全国乙卷35(2)题,15分;2021河北卷
数
17(3)(4)(5)(6)题,15分;
2024·浙江卷6月,2分;2024·浙江卷1月,2分;2024·江苏卷,3分;2024·广东卷,
3分;2024·甘肃卷,3分;2024·湖南卷,3分;2024·安徽卷,3分;2023湖北卷9
分子的空间结
题,3分;2023浙江1月选考17(1)题,3分;2023北京卷15(3)题,10分;2022湖北
构
卷11题,3分;2022辽宁卷8题,3分;2022河北卷17(3)题,15分;2022湖南卷
18(3)题,15分;2022广东卷20(2)(4)(5)题,14分;
2024·江苏卷,3分;2024·北京卷,3分;2024·湖南卷,3分;2023山东卷3题,2
分;2023北京卷10题,3分;2023浙江1月选考12题,3分;2023浙江6月选考
17(2)题,10分;2023湖南卷4题,3分;2023湖北卷11题,3分;2023全国乙卷
微粒间作用力
35(2)题,15分; 2022湖北卷10题,3分;2022山东卷5题,2分; 2022全国甲卷
35(3)题,15分;2022海南卷19(3)题,14分;2022福建卷14题,10分;2022山东卷
16题,12分;
2.命题规律及备考策略
【命题规律】高频考点从近几年全国高考试题来看,物质的组成、分类及物质的转化、胶体的性质及其应用、丁达尔效
应仍是高考命题的热点。
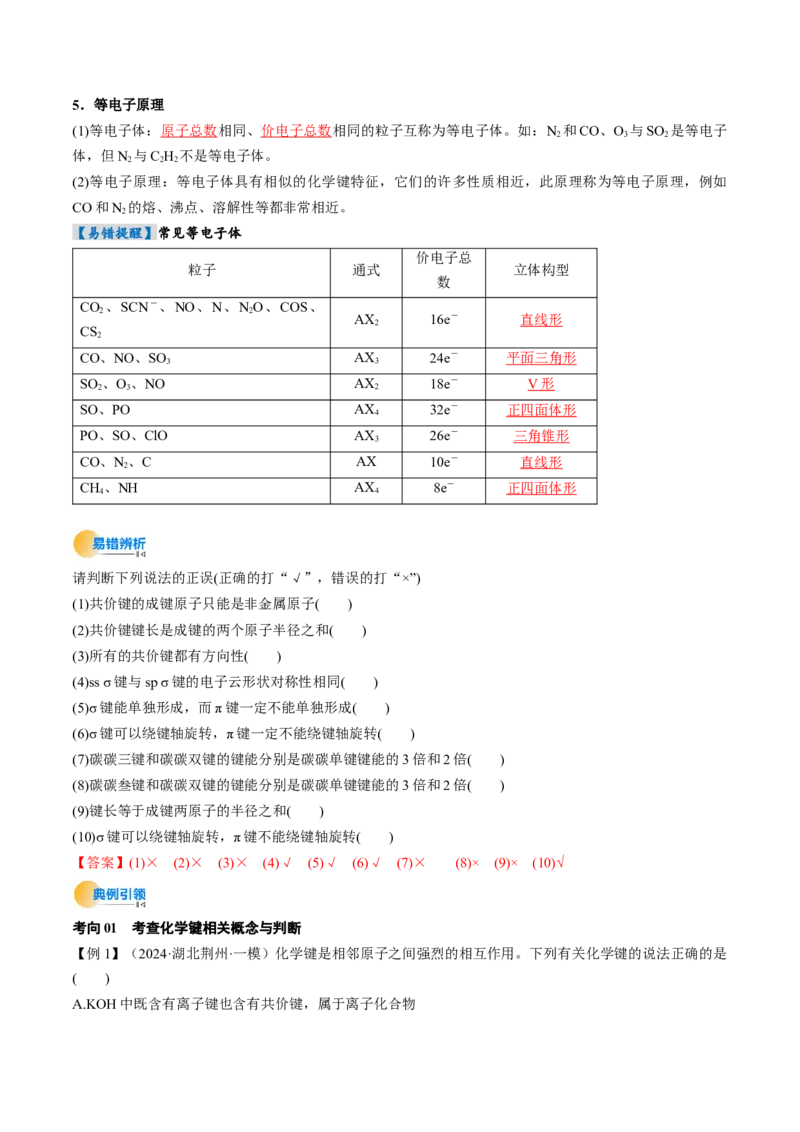
【备考策略】
【命题预测】
预计2025年高考会以新的情境载体考查分子的空间构型以及分子的杂化类型、σ键和π键的判断等,题目
难度一般适中。
考法01 共价键及键参数
1.本质:在原子之间形成共用电子对。
2.特征:具有饱和性和方向性。
3.分类
分类依据 类型
σ 键 电子云“头碰头”重叠
形成共价键的原子轨道重叠方式
π 键 电子云“肩并肩”重叠
极性键 共用电子对发生偏移
形成共价键的电子对是否偏移
非极性键 共用电子对不发生偏移
单键 原子间有一对共用电子对
原子间共用电子对的数目 双键 原子间有两对共用电子对
三键 原子间有三对共用电子对
4.键参数
(1)概念
①键能:气态分子中1 mol化学键解离成气态原子所吸收的能量,键能越大,化学键越稳定。
②键长:构成化学键的两个原子之间的核间距,键长越短,共价键越稳定。
③键角:在多原子分子中,两个相邻共价键之间的夹角。
(2)键参数对分子性质的影响5.等电子原理
(1)等电子体:原子总数相同、价电子总数相同的粒子互称为等电子体。如:N 和CO、O 与SO 是等电子
2 3 2
体,但N 与C H 不是等电子体。
2 2 2
(2)等电子原理:等电子体具有相似的化学键特征,它们的许多性质相近,此原理称为等电子原理,例如
CO和N 的熔、沸点、溶解性等都非常相近。
2
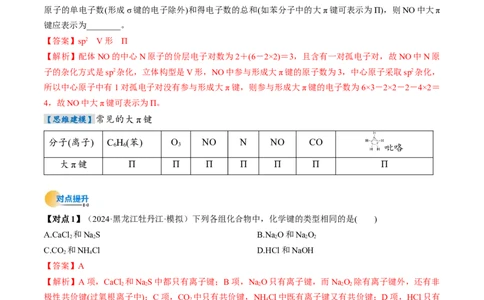
【易错提醒】常见等电子体
价电子总
粒子 通式 立体构型
数
CO 、SCN-、NO、N、NO、COS、
2 2
AX 16e- 直线形
2
CS
2
CO、NO、SO AX 24e- 平面三角形
3 3
SO 、O、NO AX 18e- V 形
2 3 2
SO、PO AX 32e- 正四面体形
4
PO、SO、ClO AX 26e- 三角锥形
3
CO、N、C AX 10e- 直线形
2
CH、NH AX 8e- 正四面体形
4 4
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)共价键的成键原子只能是非金属原子( )
(2)共价键键长是成键的两个原子半径之和( )
(3)所有的共价键都有方向性( )
(4)ss σ键与sp σ键的电子云形状对称性相同( )
(5)σ键能单独形成,而π键一定不能单独形成( )
(6)σ键可以绕键轴旋转,π键一定不能绕键轴旋转( )
(7)碳碳三键和碳碳双键的键能分别是碳碳单键键能的3倍和2倍( )
(8)碳碳叁键和碳碳双键的键能分别是碳碳单键键能的3倍和2倍( )
(9)键长等于成键两原子的半径之和( )
(10)σ键可以绕键轴旋转,π键不能绕键轴旋转( )
【答案】(1)× (2)× (3)× (4)√ (5)√ (6)√ (7)× (8)× (9)× (10)√
考向01 考查化学键相关概念与判断
【例1】(2024·湖北荆州·一模)化学键是相邻原子之间强烈的相互作用。下列有关化学键的说法正确的是
( )
A.KOH中既含有离子键也含有共价键,属于离子化合物B.N 属于单质,不存在化学键
2
C.MgCl 中既含有离子键,又含有共价键
2
D.NH Cl中含有共价键,又全部由非金属元素组成,属于共价化合物
4
【答案】A
【解析】N 中存在共价键;MgCl 中只含有离子键;NH Cl中虽然含有共价键,又全部由非金属元素组成,
2 2 4
但也含有离子键,属于离子化合物。
考向02 考查分子(或离子)中大π键的理解与判断
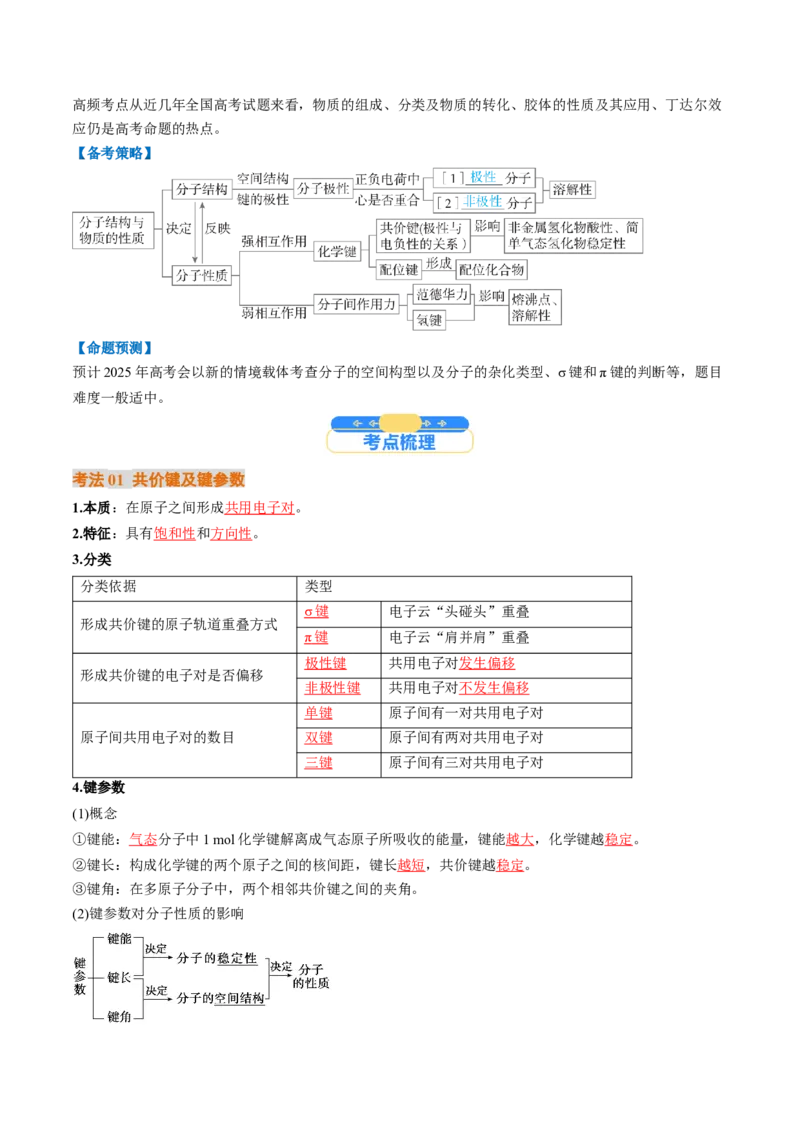
【例2】(2024·辽宁丹东·二模)Na[Co(NO )]常用作检验K+的试剂,配体NO的中心原子的杂化方式为
3 2 6
________,立体构型为________。大π键可用符号Π表示,其中m代表参与形成大π键的原子数,n为各
原子的单电子数(形成σ键的电子除外)和得电子数的总和(如苯分子中的大π键可表示为Π),则NO中大π
键应表示为________。
【答案】sp2 V形 Π
【解析】配体NO的中心N原子的价层电子对数为2+(6-2×2)=3,且含有一对孤电子对,故NO中N原
子的杂化方式是sp2杂化,立体构型是V形,NO中参与形成大π键的原子数为3,中心原子采取sp2杂化,
所以中心原子中有1对孤电子对没有参与形成大π键,则参与形成大π键的电子数为6×3-2×2-2-4×2=
4,故NO中大π键可表示为Π。
【思维建模】常见的大π键
分子(离子) C H (苯) O NO N NO CO
6 6 3 吡咯
大π键 Π Π Π Π Π Π Π
【对点1】(2024·黑龙江牡丹江·模拟)下列各组化合物中,化学键的类型相同的是( )
A.CaCl 和NaS B.Na O和NaO
2 2 2 2 2
C.CO 和NH Cl D.HCl和NaOH
2 4
【答案】A
【解析】A项,CaCl 和NaS中都只有离子键;B项,NaO只有离子键,而NaO 除有离子键外,还有非
2 2 2 2 2
极性共价键(过氧根离子中);C项,CO 中只有共价键,NH Cl中既有离子键又有共价键;D项,HCl只有
2 4
共价键,而NaOH中除有共价键(氢氧根离子中)外,还有离子键。
【对点2】(2024·江苏南通·模拟)苯分子中含有大π键,可记为Π(右下角“6”表示6个原子,右上角“6”
表示6个共用电子)。已知某化合物的结构简式为 ,不能使溴的四氯化碳溶液褪色,该分子中的大π键
可表示为________,Se的杂化方式为________。
【答案】Π sp2
【解析】该化合物不能使溴的Br /CCl 溶液褪色,说明分子结构中不存在碳碳双键,而是存在大π键;分
2 4
子中的碳原子均为sp2杂化,每个碳原子都有一个垂直于该平面的p轨道(该轨道上有一个单电子)参与形成
大π键,Se原子σ键数为2,还有2个孤电子对,其中有一个垂直于该平面的p轨道(该轨道上有2个电子)参与形成大π键,故参与形成大π键的电子总数为4×1+2=6,表示为Π;Se的价层电子对数为2+1=3,
为sp2杂化。
考法02 分子的空间结构
1.价层电子对互斥(VSEPR)理论
(1)理论要点
①价层电子对在空间上彼此相距最远时,排斥力最小,体系的能量最低。
②孤电子对的排斥力较大,孤电子对越多,排斥力越强,键角越小。
(2)用价层电子对互斥理论推测分子的空间结构的关键是判断分子中的中心原子上的价层电子对数。
其中:a是中心原子的价电子数(阳离子要减去电荷数、阴离子要加上电荷数),b是与中心原子结合的原子
最多能接受的电子数,x是与中心原子结合的原子数。
2.杂化轨道理论
(1)理论要点
当原子成键时,原子的价电子轨道相互混杂,形成与原轨道数相等且能量相同的杂化轨道。杂化轨道数不
同,轨道间的夹角不同,形成分子的空间结构不同。
(2)杂化轨道的类型
杂化类型 杂化轨道数目 杂化轨道间夹角 空间结构
sp 2 180° 直线形
sp2 3 120° 平面三角形
sp3 4 109°28′ 正四面体形
(3)杂化轨道数和杂化类型的判断
①杂化轨道用来形成σ键和容纳孤电子对;
②杂化轨道的数目=中心原子上的孤电子对数+中心原子的σ键电子对数(与中心原子直接相连的原子个
数)=中心原子的价层电子对数。
(4)分子(AB 型)、离子(AB型)的空间结构示例(填表)
n
σ键电 孤电子 价层电子对数 中心原子的杂 VSEPR 微粒的
实例
子对数 对数 (杂化轨道数) 化类型 模型 空间结构
BeCl
2
2 0 2 sp 直线形 直线形
CO
2
BF 3 0 平面三角形
3
3 sp 2 平面三角形
SO 2 1 V 形
2
CH 4 0 正四面体形
4
4 sp 3 四面体形
NH 3 1 三角锥形
3HO 2 2 V 形
2
CO 3 0 3 sp 2 平面三角形 平面三角形
NH 4 0 4 sp 3 四面体形 正四面体形
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对( )
(2)分子中中心原子若通过sp3杂化轨道成键,则该分子一定为正四面体结构( )
(3)NH 分子为三角锥形,N原子发生sp2杂化( )
3
(4)只要空间结构为平面三角形,中心原子均为sp2杂化( )
(5)中心原子是sp杂化的,其空间结构不一定为直线形( )
(6)价层电子对互斥理论中,π键电子对数不计入中心原子的价层电子对数( )
(7)PCl 分子是三角锥形,这是因为P原子是以sp2杂化的结果( )
3
(8)sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道( )
(9)凡中心原子采取sp3杂化的分子,其VSEPR模型都是四面体( )
(10)AB 型的分子空间构型必为平面三角形( )
3
【答案】(1)√ (2)× (3)× (4)√ (5)× (6)√ (7)× (8)× (9)√ (10)×
考向01 考查价层电子对互斥模型及杂化轨道理论理解与应用
【例1】(2024·河南商丘·一模)下列离子的VSEPR模型与离子的立体构型一致的是( )
A.SO B.ClO
C.NO D.ClO
【答案】B
【解析】当中心原子无孤电子对时,VSEPR模型与离子的立体构型一致。A项,SO的中心原子的孤电子
对数=×(6+2-3×2)=1;B项,ClO的中心原子的孤电子对数=×(7+1-4×2)=0;C项,NO的中心原子
的孤电子对数=×(5+1-2×2)=1;D项,ClO的中心原子的孤电子对数=×(7+1-3×2)=1。所以只有B项
符合题意。
考向02 考查杂化轨道类型、分子空间结构的判断
【例2】(2024·浙江丽水·二模)氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子的立体
构型为平面三角形,则其阳离子的立体构型和阳离子中氮的杂化方式为( )
A.直线形 sp杂化
B.V形 sp2杂化
C.三角锥形 sp3杂化
D.平面三角形 sp2杂化
【答案】A【解析】氮的最高价氧化物为NO ,根据N元素的化合价为+5和原子组成,可知阴离子为NO、阳离子
2 5
为NO,NO中N原子形成了2个σ键,孤电子对数目为0,所以杂化类型为sp,阳离子的立体构型为直线
形,故A项正确。
【思维建模】“五方法”判断分子中心原子的杂化类型
(1)根据杂化轨道的空间构型判断。
①若杂化轨道在空间的分布为正四面体形或三角锥形,则分子的中心原子发生sp3杂化。
②若杂化轨道在空间的分布呈平面三角形,则分子的中心原子发生sp2杂化。
③若杂化轨道在空间的分布呈直线形,则分子的中心原子发生sp1杂化。
(2)根据杂化轨道之间的夹角判断
若杂化轨道之间的夹角为109.5°,则分子的中心原子发生sp3杂化;若杂化轨道之间的夹角为120°,则分子
的中心原子发生sp2杂化;若杂化轨道之间的夹角为180°,则分子的中心原子发生sp1杂化。
(3)根据等电子原理进行判断
如CO 是直形线分子,CNS-、N与CO 互为等电子体,所以分子构型均为直线形,中心原子均采用sp1杂
2 2
化。
(4)根据中心原子的价电子对数判断
如中心原子的价电子对数为4,是sp3杂化,为3是sp2杂化,为2是sp1杂化。
(5)根据分子或离子中有无π键及π键数目判断
如没有π键为sp3杂化,含1个π键为sp2杂化,含2个π键为sp1杂化。
【对点1】(2024·吉林白城·模拟)血红素是吡咯(C HN)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性
4 5
贫血。吡咯的结构如图所示。已知吡咯分子中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类
型为( )
A.sp B.sp2
C.sp3 D.没有杂化轨道
【答案】B
【解析】已知吡咯分子中氮原子与其相连的原子均在同一平面内,则氮原子的杂化类型为sp2杂化。
【对点2】(2024·安徽黄山·模拟)关于CHOH、NH 和(CH)NNH 的结构与性质,下列说法错误的是(
3 2 4 3 2 2
)
A.CHOH为极性分子
3
B.N H 空间结构为平面形
2 4
C.N H 的沸点高于(CH)NNH
2 4 3 2 2
D.CHOH和(CH)NNH 中C、O、N杂化方式均相同
3 3 2 2
【答案】B【解析】A.甲醇可看成是甲烷中的一个氢原子被羟基取代得到的,为四面体结构,是由极性键组成的极性
分子,A正确;B.N H 中N原子的杂化方式为 sp3,不是平面形,B错误;C.N H 分子中连接N原子的H
2 4 2 4
原子数多,存在氢键的数目多,而偏二甲肼[(CH )NNH]只有一端可以形成氢键,另一端的两个甲基基团
3 2 2
比较大,影响了分子的排列,沸点较NH 的低,C正确;D.CHOH为四面体结构,—OH结构类似于水的
2 4 3
结构,(CH)NNH 的结构简式为 ,两者分子中C、O、N杂化方式均为 sp3,D正确;故选
3 2 2
B。
考法03 分子间作用力与分子的性质
1.分子间作用力
(1)概念:物质分子之间普遍存在的相互作用力,称为分子间作用力。
(2)分类:分子间作用力最常见的是范德华力和氢键。
(3)强弱:范德华力<氢键<化学键。
(4)范德华力:范德华力主要影响物质的熔点、沸点、硬度等物理性质。范德华力越强,物质的熔点、沸点
越高,硬度越大。一般来说,组成和结构相似的物质,随着相对分子质量的增加,范德华力逐渐增大。
(5)氢键
①形成:已经与电负性很强的原子(N、O、F)形成共价键的氢原子(该氢原子几乎为裸露的质子)与另一个分
子中电负性很强的原子(N、O、F)之间的作用力,称为氢键。
②表示方法:A—H…B
③特征:具有一定的方向性和饱和性。
④分类:氢键包括分子内氢键和分子间氢键两种。
⑤分子间氢键对物质性质的影响:使物质的熔、沸点升高,对电离和溶解度等产生影响。
2.分子的性质
(1)分子的极性
类型 非极性分子 极性分子
形成原因 正电中心和负电中心重合的分子 正电中心和负电中心不重合的分子
存在的共价键 非极性键或极性键 非极性键或极性键
分子内原子排列 对称 不对称
(2)分子的溶解性
①“相似相溶”的规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。若溶剂和溶
质分子之间可以形成氢键,则溶质的溶解度增大。
②随着溶质分子中憎水基的增大,溶质在水中的溶解度减小。如甲醇、乙醇和水以任意比互溶,而戊醇在
水中的溶解度明显减小。
(3)分子的手性
①手性异构:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,却在三维空间
里不能叠合的现象。
②手性分子:具有手性异构体的分子。
③手性碳原子:在有机物分子中,连有四个不同基团或原子的碳原子。含有手性碳原子的分子是手性分子,
如 (*所标碳原子为手性碳原子)。
(4)无机含氧酸分子的酸性
无机含氧酸的通式可写成(HO) RO,如果成酸元素R相同,则n值越大,R的正电性越高,使R—O—H
m n
中O的电子向R偏移,在水分子的作用下越易电离出H+,酸性越强,如酸性:
HClONH
3
【答案】C
【解析】
A.NH 中N与H形成共价键,其电子式为 ,A错误;
3
B.基态Cu的价层电子排布式是 ,因此基态Cu2+的价层电子排布式为 ,B错误;
C. 中C原子上的孤电子对= 、价层电子对数为3+0=3,故C原子为sp2杂化、空间构型
为平面正三角形,C正确;
D. 的价层电子对数=4+0=4,NH 的价层电子对数为3+1=4,存在的孤电子对数越多,键角越小,故
3
键角: >NH,D错误;故答案为C。
3
1.(2024·江西吉安·模拟预测)点击化学(Click Chemistry)是一种准确构建稳定分子连接的高效手段。
某点击试剂的结构如下:则关于N、O、P、Cl的叙述正确的是
A.O 属于非极性分子 B.PCl 分子的VSEPR 模型:
3 3
C.ClO-的电子式: D.键角:P>PH
4 3
【答案】B
【解析】A.O 属于极性分子,A项错误;
3
B.PCl 分子的中心原子价层电子对数为4,且有一个孤电子对,VSEPR模型为 ,B项正确;
3
C.ClO-的电子式: ,C项错误;
D.P 属正四面体分子,P位于正四面体的4个顶点,键角为60°, PH 的中心P原子采取sp3杂化,空间
4 3
结构为三角锥形,键角略小于109°28',键角:PH >P ,D项错误;
3 4
故选:B。
2.(2024·江西·模拟预测)对于 反应,下列叙述错误的是
A.Ca(OH) 的电子式:
2
B.HO的VSEPR模型:
2
C.NH 是只含极性键的极性分子
3
D.NH Cl和NH 中的N原子都采用sp3杂化
4 3
【答案】B
【解析】
A.Ca(OH) 是离子化合物,故其电子式为: ,A正确;
2
B.HO的价层电子对数为:2+ =4,根据价层电子对互斥理论可知,其VSEPR模型为:
2,B错误;
C.NH 是只含N-H极性键,分子中正、负电荷中心不重合,则为极性分子,C正确;
3
D.NH Cl和NH 中的N原子周围的价层电子对数均为4,则N原子都采用sp3杂化,D正确;
4 3
故答案为:B。
3.(2024·山东潍坊·二模)下列分子的空间结构相同的是
A. 和 B. 和 C. 和 D. 和
【答案】A
【解析】A. 分子中Xe原子价层电子对数=3+ (8-3 ,孤电子对数为1, 分子为三角锥
形结构, 分子中N原子的价层电子对数=3+ (5-3 ,孤电子对数为1,故 分子为三角锥形
结构,选项A正确;
B. 中C原子价层电子对数=3+ =3,无孤电子对,空间构型为平面三角形, 中S原子价
层电子对数=3+ =4,孤电子对数为1,空间构型为三角锥形,选项B错误;
C. 分子中Cl原子价层电子对数=3+ =5,为sp3d杂化,2对孤电子对,T形结构,BF 分子中B
3
原子的价层电子对数=3+ =3,没有孤电子对,B原子的杂化方式为sp2,空间构型为平面三角形,选项
C错误;
D.CO 分子中C原子的价层电子对数2+ =2,无孤电子对,空间构型均为直线形, 分子中S原子
2
的价层电子对数2+ =4,孤电子对数为2,空间构型均为V形,选项D错误;
答案选A。
4.(2024·山东聊城·二模)价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 是平面结构的分子
B. 和 均为非极性分子
C. 和 的空间结构均为平面三角形
D. 和 的 模型均为四面体形
【答案】C
【解析】A.过氧化氢的空间结构是二面角结构,也叫半开书页型结构,在这种结构中,两个氧原子位于
书轴上,两个氢原子分别与两个氧原子相连,但不在同一平面上,A错误;B. 为正四面体结构,属于非极性分子, 空间结构与水分子相似,属于极性分子,B错误;
C. 中心原子S价层电子对数: ,无孤电子对,空间结构均为平面三角形, 中心
原子N价层电子对数: ,无孤电子对,空间结构均为平面三角形,C正确;
D. 中心原子B价层电子对数: , 模型为平面三角形,D错误;
答案选C。
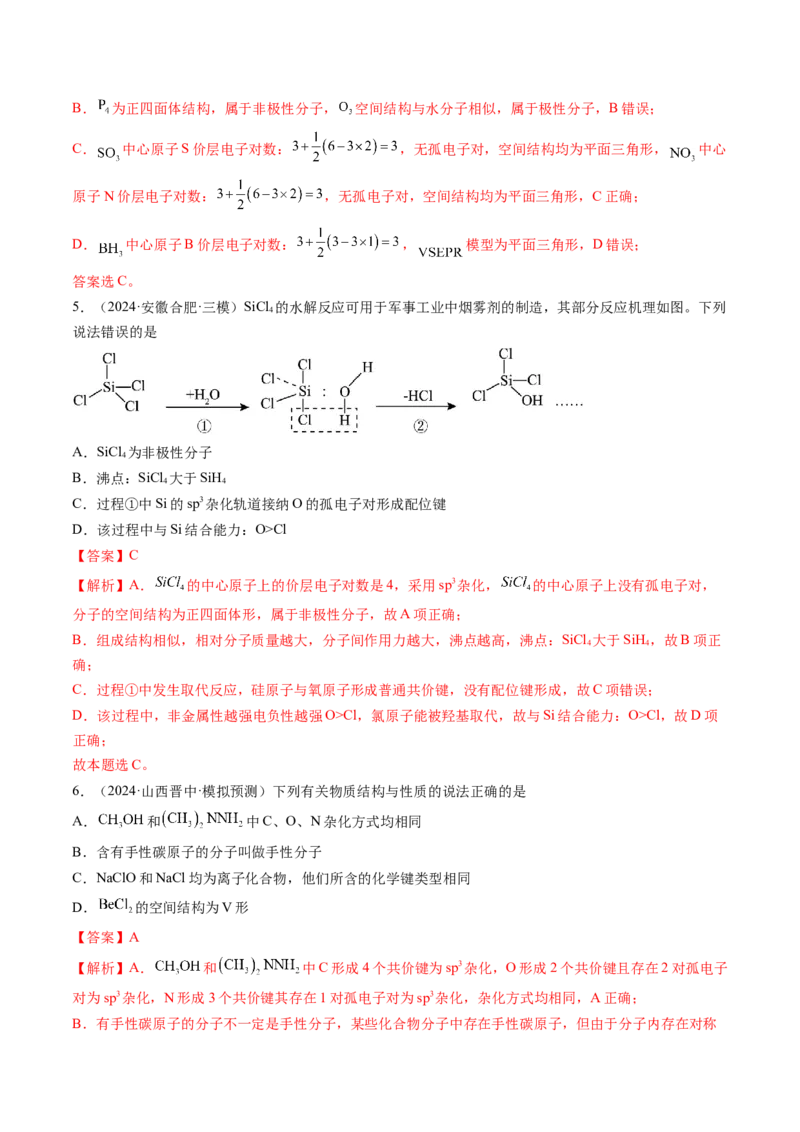
5.(2024·安徽合肥·三模)SiCl 的水解反应可用于军事工业中烟雾剂的制造,其部分反应机理如图。下列
4
说法错误的是
A.SiCl 为非极性分子
4
B.沸点:SiCl 大于SiH
4 4
C.过程①中Si的sp3杂化轨道接纳O的孤电子对形成配位键
D.该过程中与Si结合能力:O>Cl
【答案】C
【解析】A. 的中心原子上的价层电子对数是4,采用sp3杂化, 的中心原子上没有孤电子对,
分子的空间结构为正四面体形,属于非极性分子,故A项正确;
B.组成结构相似,相对分子质量越大,分子间作用力越大,沸点越高,沸点:SiCl 大于SiH,故B项正
4 4
确;
C.过程①中发生取代反应,硅原子与氧原子形成普通共价键,没有配位键形成,故C项错误;
D.该过程中,非金属性越强电负性越强O>Cl,氯原子能被羟基取代,故与Si结合能力:O>Cl,故D项
正确;
故本题选C。
6.(2024·山西晋中·模拟预测)下列有关物质结构与性质的说法正确的是
A. 和 中C、O、N杂化方式均相同
B.含有手性碳原子的分子叫做手性分子
C.NaClO和NaCl均为离子化合物,他们所含的化学键类型相同
D. 的空间结构为V形
【答案】A
【解析】A. 和 中C形成4个共价键为sp3杂化,O形成2个共价键且存在2对孤电子
对为sp3杂化,N形成3个共价键其存在1对孤电子对为sp3杂化,杂化方式均相同,A正确;
B.有手性碳原子的分子不一定是手性分子,某些化合物分子中存在手性碳原子,但由于分子内存在对称因素,使得分子没有旋光性,B错误;
C.NaClO含有离子键和氯氧共价键,NaCl只含有离子键,所含的化学键类型不相同,C错误;
D. 的Be形成2个共价键且无孤电子对,空间结构为直线形,D错误;
故选A。
7.(2024·湖北武汉·二模)键角是重要的键参数之一。下列键角的大小比较正确的是
选项 键角 键角的大小比较
A
B 金刚石>石墨
C
D
【答案】A
【解析】A.氨分子中氮原子的价层电子对数为4、孤对电子对数为1,四氨合铜离子中中心离子为提供空
轨道的铜离子,配体为提供孤对电子的氨分子,配离子中氮原子的价层电子对数为4、孤对电子对数为0,
孤对电子对数越多,对成键电子对的斥力越大,键角越小,则四氨合铜离子的键角 大于氨分
子,故A正确;
B.金刚石中碳原子的杂化方式为sp3杂化,石墨中碳原子的杂化方式为sp2杂化,则金刚石中键角
小于石墨,故B错误;
C.三氧化硫分子中硫原子的价层电子对数为3、孤对电子对数为0,分子的空间构型为平面三角形,亚硫
酸根离子中硫原子的价层电子对数为4、孤对电子对数为1,离子的空间构型为三角锥形,则三氧化硫分子
中键角 大于亚硫酸根离子,故C错误;
D. 离子中碳原子的价层电子对数为3、孤对电子对数为0,离子的空间构型为平面三角形, 离
子中碳原子的价层电子对数为4、孤对电子对数为1,离子的空间构型为三角锥形,则 离子中键角
大于 离子,故D错误;
故选A。
8.(2024·山东济宁·三模)下列有关物质结构与性质的比较正确的是
A.沸点:
B.分子的极性:
C.键角:
D.碱性强弱:【答案】C
【解析】A. 能形成分子间氢键,故沸点高于 , 的相对分子质量大于
,沸点比 高,即沸点 ,故A错误;
B. 为平面正三角形,为非极性分子, 为极性分子,故分子极性 ,故B错误;
C. 为平面三角形分子,键角为120 , 都是三角锥形分子,键角小于120 ,而N的电负
性强于P, 中的价层电子对更偏向于N,导致N上电子云密度变大,键角变大,故键角
,故C正确;
D. 中N的电子云密度最大,碱性最强, 中N的电子云密度最小,碱性最弱,故
D错误。
答案选C。
9.(2024·山东威海·二模)关于二氟化合物CF、SiF 和GeF 的结构和性质,下列说法错误的是
2 2 2
A.键角:CF<SiF<GeF B.沸点:CF<SiF<GeF
2 2 2 2 2 2
C.均为sp2杂化(中心原子)的角形结构 D.均为含极性键的极性分子
【答案】A
【解析】A.已知CF、SiF 和GeF 中中心原子周围的价层电子对数为:2+ =3,且原子半径C
2 2 2
<Si<Ge,则分子中共有电子对离中心原子的距离为:CF<SiF<GeF ,排斥力的大小为:CF>SiF>
2 2 2 2 2
GeF ,则键角:CF>SiF>GeF ,A错误;
2 2 2 2
B.已知CF、SiF 和GeF 均为分子晶体,且相对分子质量CF<SiF<GeF ,则分子间作用力CF<SiF<
2 2 2 2 2 2 2 2
GeF ,沸点:CF<SiF<GeF ,B正确;
2 2 2 2
C.已知CF、SiF 和GeF 中中心原子周围的价层电子对数为:2+ =3,均有1对孤电子对,根
2 2 2
据杂化轨道理论和价层电子对互斥理论可知,均为sp2杂化(中心原子)的角形即V形结构,C正确;
D.由C项分析可知,均为含C-F、Si-F和Ge-F极性键,分子中正、负电荷中心均不重合,均为极性分
子,D正确;
故答案为:A。
10.(2024·江西·模拟预测)下列关于N、O、F及其相关微粒的说法错误的是
A. 、OF 、NF 的键角大小顺序为 >NF >OF
2 3 3 2
B.基态N3-、O2-、F-核外电子空间运动状态均为5种
C.N、O、F三种元素形成的单质分子均为非极性分子
D. 、 的VSEPR模型相同,均为平面三角形
【答案】C【解析】A. 、OF 、NF 中心原子杂化方式分别为sp、sp3、sp3, 是直线型分子,键角是180°;
2 3
sp3、sp3的VSEPR模型是四面体形,但NF 分子中的中心N原子有1对孤电子对,OF 中的中心O原子上
3 2
有2对孤电子对,由于孤电子对对成键电子对的排斥作用大于成键电子对的排斥作用,导致键角减小,故
键角由大到小的顺序为: >NF >OF ,A正确;
3 2
B.N3-、O2-、F-三种离子均为10电子微粒,电子排布式为1s22s22p6,故基态离子的核外电子空间运动状态
均为5种,B正确;
C.O 为由非极性键构成的极性分子,C错误;
3
D. 和 中N原子杂化方式均为sp2,VSEPR模型相同,均为平面三角形,D正确;
故合理选项是C。
11.(2024·河北承德·三模)一种抗癌新药的分子结构如图所示。下列说法正确的是
A.C、N、O元素的第一电离能由小到大的顺序为
B.该化合物的一氯代物有10种
C.分子中碳原子采取 、 杂化,氮原子和硒原子均采取 杂化
D. 的键角小于 的键角
【答案】C
【解析】A.由于N原子的2p能级上有3个电子,处于半充满状态,比较稳定,而O原子的2p能级上有4
个电子,不是半充满,也不是全充满,故O原子不如N原子稳定,故第一电离能: ,A错误;
B.该化合物分子中有5种不同化学环境的H原子,故其一氯代物有5种,B错误;
C.分子中碳原子采取 、 杂化,氮原子和硒原子均采取 杂化,C正确;
D. 分子中的Se原子采取 杂化,分子的空间结构为平面三角形,键角为120°; 分子的空间结
构为V形,虽然 分子中的Se原子也采取 杂化,但由于Se原子的孤电子对对成键电子对的斥力较
大,使 分子的键角小于120°,故 的键角大于 的键角,D错误;
故答案为:C。
12.(2024·河南·模拟预测)H与O可以形成 和 两种化合物,其中 的分子结构如图所示。
可与 形成 。下列说法错误的是A.液态水中的作用力由强到弱的顺序是:氢键>O—H>范德华力
B.相同条件下, 在水中的溶解度大于在 中的溶解度
C. 分子中两个O原子均采取: 杂化轨道成键
D. 的空间结构为三角锥形
【答案】A
【解析】A.一般而言,共价键的作用力大于分子间作用力,则液态水中的作用力由强到弱的顺序是:O—
H>氢键>范德华力,A错误;
B. 和HO都是极性分子, 是非极性分子,根据相似相溶原理,相同条件下, 在水中的溶
2
解度大于在 中的溶解度,B正确;
C. 分子中两个O原子均形成2个共价键且存在2对孤电子对,采取 杂化轨道成键,C正确;
D.HO+中氧原子的价层电子对数为 ,O为sp3杂化,有一对孤对电子,故HO+的立体构型
3 3
为三角锥形,D正确;
故选A。
13.(2024·湖北黄冈·模拟预测)物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选
性质差异 结构因素
项
A 沸点:乙醇 高于乙醛 分子间氢键
B 熔点: 熔点远高于 的熔点 分子间作用力
C 键角: 小于 电负性差异
D 分解温度: 高于 键能大小
【答案】B
【解析】A.由于乙醇中存在和氧原子相连的氢原子,存在分子间氢键,而乙醛中不存在,导致乙醇
(78.3℃)的沸点高于乙醛(20.8℃),即与氢键作用有关,A不符合题意;
B.KAl Cl 是离子晶体,Al Cl 是分子晶体,作用力:离子键>范德华力,导致KAl Cl 的熔点远高于
2 7 2 6 2 7Al Cl,则KAl Cl 的熔点远高于Al Cl 与晶体类型有关,B符合题意;
2 6 2 7 2 6
C.电负性:F>Cl,故PF 中共用电子对离P更远,排斥力更小,键角更小,即键角与F、Cl的电负性差
3
异有关,C不符合题意;
D.由于半径I>Br,导致H-Br的键能比H-I的键能大,所以热分解温度:HBr大于HI,即稳定性HBr>
HI,故HBr和HI的热稳定性和键能有关,D不符合题意;
故答案为:B。
14.(2024·安徽安庆·模拟预测)一种工业洗涤剂中间体结构式如图所示,其中短周期元素X、Q、Z、
Y、W原子序数依次增大,X和W同主族但不相邻,Q、Z、Y为相邻元素,Y和Q最外层电子数之和是Z
原子L层电子数的二倍,下列说法错误的是
A. 和 均为极性分子 B.第一电离能:Z>Y>Q
C.原子半径:Q>Z>Y D.W与Y形成的化合物中只含离子键
【答案】D
【分析】一种工业洗涤剂中间体结构式如图所示,其中短周期元素X、Q、Z、Y、W原子序数依次增大,
X和W同主族但不相邻,W形成+1价阳离子,X形成1个共价键,则X为H,W为Na;Y形成2个共价
键,其原子序数小于Na,则Y为O;Q形成4个共价键,其最外层电子数为4,原子序数小于O,则Q为
C;Q、Z、Y为相邻元素,Y和Q最外层电子数之和是Z原子L层电子数的二倍,Z原子L呈电子数为
=5,则Z为N,以此分析解答。
【解析】A.HO和HO 的正负电荷的重心不重合,均为极性分子,A正确;
2 2 2
B.同一周期从左到右元素的第一电离能呈增大趋势,ⅡA和ⅤA族元素的第一电离能大于相邻元素,因
此第一电离能:N>O>C,即Z>Y>Q,B正确;
C.同一周期从左到右原子半径逐渐减小,因此原子半径:C>N>O,即Q>Z>Y,C正确;
D.W与Y形成的化合物可能为NaO或NaO,NaO只含离子键,但NaO 中既含离子键又含共价键,D
2 2 2 2 2 2
错误;
故答案为:D。
15.(2024·广西贵港·模拟预测)化合物 XY ZME 是良好的电和热绝缘体,组成元素原子序数均小于
3 3 2 12
20,且在前四个周期均有分布。仅X和M同族,电负性: ;Y和Z同周期,Y的基态原子价层电子
排布式为 ,Z的基态原子价层的s和p轨道电子数相同;E在地壳中含量最多。下列说法正确的
是
A.原子半径: B.同周期元素中比E第一电离能大的有2种
C.熔点: D. 中的E的杂化方式为【答案】C
【分析】Y的基态原子价层电子排布式为 ,可知 ,价层电子排布式为 ,Y为Al元素,
Y和Z同周期,因此Z也是在第三周期,Z的基态原子价层的s和p轨道电子数相同,可知Z的基态原子
价层电子排布式为 ,Z为Si元素,E在地壳中含量最多,因此E为O元素,由于组成元素原子序数
均小于20,且在前四个周期均有分布,还差第一周期和第四周期,根据仅X和M同族,电负性:
可知,M为H元素,X为K元素,则化合物为 ,据此作答。
【解析】A.Z为Si元素,Y为Al元素,同周期从左往右原子半径减小,因此原子半径为 ,A错
误;
B.E元素为O,同周期中比O第一电离能大的有N、F、Ne3种元素,B错误;
C. 为 , 为 , 为共价晶体, 为分子晶体,共价晶体熔点更高,因此熔点是
,C正确;
D. 为 ,中心原子O原子的价层电子对数为4,因此为 杂化,D错误;
故选C。
1.(2024·安徽卷)某催化剂结构简式如图所示。下列说法错误的是
A. 该物质中 为 价 B. 基态原子的第一电离能:
C. 该物质中C和P均采取 杂化 D. 基态 原子价电子排布式为
【答案】C
【解析】由结构简式可知,P原子的3个孤电子与苯环形成共用电子对,P原子剩余的孤电子对与Ni形成
配位键,Cl-提供孤电子对,与Ni形成配位键,由于整个分子呈电中性,故该物质中Ni为+2价,A项正
确;同周期元素随着原子序数的增大,第一电离能有增大趋势,故基态原子的第一电离能:Cl>P,B项正
确;该物质中,C均存在于苯环上,采取sp2杂化,P与苯环形成3对共用电子对,剩余的孤电子对与Ni形
成配位键,价层电子对数为4,采取sp3杂化,C项错误;Ni的原子序数为28,位于第四周期第Ⅷ族,基
态Ni原子价电子排布式为3d84s2,D项正确;故选C。
2.(2024·河北卷)从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与解释不符的是
选
实例 解释
项
A 原子光谱是不连续的线状谱线 原子的能级是量子化的孤电子对与成键电子对的斥力大于成键
B 键角依次减小
电子对之间的斥力
晶体中 与8个 配位,而 晶体中
C 比 的半径大
与6个 配位
D 逐个断开 中的 键,每步所需能量不同 各步中的 键所处化学环境不同
【答案】B
【解析】原子光谱是不连续的线状谱线,说明原子的能级是不连续的,即原子能级是量子化的,故A正
确; 中心C原子为 杂化,键角为 , 中心C原子为 杂化,键角大约为 ,
中心C原子为 杂化,键角为 ,三种物质中心C原子都没有孤电子对,三者键角大小与孤电子对
无关,故B错误;离子晶体的配位数取决于阴、阳离子半径的相对大小,离子半径比越大,配位数越大,
周围最多能排布8个 , 周围最多能排布6个 ,说明 比 半径大,故C正确;断开
第一个键时,碳原子周围的共用电子对多,原子核对共用电子对的吸引力较弱,需要能量较小,断开
键越多,碳原子周围共用电子对越少,原子核对共用电子对的吸引力越大,需要的能量变大,所以
各步中的 键所处化学环境不同,每步所需能量不同,故D正确;故选B。
3.(2024·河北卷) 是火箭固体燃料重要的氧载体,与某些易燃物作用可全部生成气态产物,
如: 。下列有关化学用语或表述正确的是
A. 的形成过程可表示为
B. 中的阴、阳离子有相同的VSEPR模型和空间结构
C. 在 、石墨、金刚石中,碳原子有 和 三种杂化方式
D. 和 都能作制冷剂是因为它们有相同类型的分子间作用力
【答案】B
【解析】 是共价化合物,其电子式为 , 的形成过程可表示为 ,故
A错误; 中 的中心N原子孤电子对数为 ,价层电子对数为4, 的中心
原子孤电子对数为 ,价层电子对数为4,则二者的 模型和空间结构均为正四面体形,故B正确; 、石墨、金刚石中碳原子的杂化方式分别为 、 、 ,共有2种杂化方
式,故C错误; 易液化,其气化时吸收热量,可作制冷剂,干冰易升华,升华时吸收热量,也可作
制冷剂, 分子间作用力为氢键和范德华力, 分子间仅存在范德华力,故D错误;故选B。
4.(2024·湖北卷)基本概念和理论是化学思维的基石。下列叙述错误的是
A. 理论认为 模型与分子的空间结构相同
B. 元素性质随着原子序数递增而呈周期性变化的规律称为元素周期律
C. 泡利原理认为一个原子轨道内最多只能容纳两个自旋相反的电子
D. 杂化轨道由1个s轨道和3个p轨道混杂而成
【答案】A
【解析】VSEPR模型是价层电子对的空间结构模型,而分子的空间结构指的是成键电子对的空间结构,不
包括孤电子对,当中心原子无孤电子对时,两者空间结构相同,当中心原子有孤电子对时,两者空间结构
不同,故A错误;元素的性质随着原子序数的递增而呈现周期性的变化,这一规律叫元素周期律,元素性
质的周期性的变化是元素原子的核外电子排布周期性变化的必然结果,故B正确;在一个原子轨道里,最
多只能容纳2个电子,它们的自旋相反,这个原理被称为泡利原理,故C正确;1个s轨道和3个p轨道混
杂形成4个能量相同、方向不同的轨道,称为sp3杂化轨道,故D正确;故选A。
5.(2024·湖北卷)结构决定性质,性质决定用途。下列事实解释错误的是
事实 解释
A 甘油是黏稠液体 甘油分子间的氢键较强
B 王水溶解铂 浓盐酸增强了浓硝酸的氧化性
C 冰的密度小于干冰 冰晶体中水分子的空间利用率相对较低
D 石墨能导电 未杂化的p轨道重叠使电子可在整个碳原子平面内运动
【答案】B
【解析】甘油分子中有3个羟基,分子间可以形成更多的氢键,且O元素的电负性较大,故其分子间形成
的氢键较强,因此甘油是黏稠液体,A正确;王水溶解铂,是因为浓盐酸提供的Cl-1能与被硝酸氧化产生
的高价态的铂离子形成稳定的配合物从而促进铂的溶解,在这个过程中浓盐酸没有表现氧化性,B不正
确;
冰晶体中水分子间形成较多的氢键,由于氢键具有方向性,因此,水分子间形成氢键后空隙变大,冰晶体
中水分子的空间利用率相对较低,冰的密度小于干冰,C正确;石墨属于混合型晶体,在石墨的二维结构
平面内,第个碳原子以C—C键与相邻的3个碳原子结合,形成六元环层。碳原子有4个价电子,而每个
碳原子仅用3个价电子通过sp2杂化轨道与相邻的碳原子形成共价键,还有1个电子处于碳原子的未杂化的
2p轨道上,层内碳原子的这些p轨道相互平行,相邻碳原子p轨道相互重叠形成大π键,这些p轨道的电
子可以在整个层内运动,因此石墨能导电,D正确;综上所述,本题选B。
6.(2024·山东卷)由O、F、I组成化学式为 的化合物,能体现其成键结构的片段如图所示。下列说法正确的是
A. 图中O代表F原子 B. 该化合物中存在过氧键
C. 该化合物中I原子存在孤对电子 D. 该化合物中所有碘氧键键长相等
【答案】C
【解析】由图中信息可知,白色的小球可形成2个共价键,灰色的小球只形成1个共价键,黑色的大球形
成了4个共价键,根据O、F、I的电负性大小(F最大、I最小)及其价电子数可以判断,白色的小球代表
O原子、灰色的小球代表F原子,黑色的大球代表I原子。图中O(白色的小球)代表O原子,灰色的小
球代表F原子,A不正确;根据该化合物结构片断可知,每个I原子与3个O原子形成共价键,根据均摊
法可以判断必须有2个O原子分别与2个I原子成键,才能确定该化合物化学式为 ,因此,该化合物
中不存在过氧键,B不正确;I原子的价电子数为7,该化合物中F元素的化合价为-1,O元素的化合价
为-2,则I元素的化合价为+5,据此可以判断每I原子与其他原子形成3个单键和1个双键,I原子的价电
子数不等于其形成共价键的数目,因此,该化合物中I原子存在孤对电子,C正确;该化合物中既存在I—
O单键,又存在I=O双键,单键和双键的键长是不相等的,因此,该化合物中所有碘氧键键长不相等,D
不正确;综上所述,本题选C。
7.(2024·新课标卷)我国科学家最近研究的一种无机盐 纳米药物具有高效的细胞内亚铁离
子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的
外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层未成对电子数
为4。下列叙述错误的是
A. W、X、Y、Z四种元素的单质中Z的熔点最高
B. 在X的简单氢化物中X原子轨道杂化类型为
C. Y的氢氧化物难溶于NaCl溶液,可以溶于 溶液
D. 中 提供电子对与 形成配位键
【答案】A
【解析】W、X 、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电子数
是其内层电子数的2倍,则W为C元素;每个周期的ⅡA和ⅤA的元素的第一电离能都比左右相邻元素
的高,由于配合物 中Y在外界,Y可形成简单阳离子,则Y属于金属元素,故X和Y分别
为N和Mg;Z的M层未成对电子数为4,则其3d轨道上有4个不成对电子,其价电子排布式为 ,
Z为Fe元素, 为 。W、X、 Y、Z四种元素的单质中,N元素的单质形成
分子晶体,Mg和Fe均形成金属晶体,C元素既可以形成金刚石又可以形成石墨,石墨的熔点最高,A不正确;在X的简单氢化物是 ,其中C原子轨道杂化类型为 ,B正确;Y的氢氧化物是
,其属于中强碱,其难溶于水,难溶于 溶液,但是,由于 电离产生的 可以破坏
的沉淀溶解平衡,因此 可以溶于 溶液,C正确; 中 提供
电子对与 形成配位键,D正确;综上所述,本题选A。
8.(2024·浙江卷1月)X、Y、Z、M和Q五种主族元素,原子序数依次增大,X原子半径最小,短周期中
M电负性最小,Z与Y、Q相邻,基态Z原子的s能级与p能级的电子数相等,下列说法不正确的是
A. 沸点:
B. M与Q可形成化合物 、
C. 化学键中离子键成分的百分数:
D. 与 离子空间结构均 为三角锥形
【答案】D
【解析】X半径最小为H,短周期电负性最小则M为Na,Z原子的s能级与p能级的电子数相等,则Z为
O,Z与Y、Q相邻,Y为N,Q为S,以此分析;HO中含有氢键,则沸点高于HS,A正确;Na与O形
2 2
成NaO、NaO,则O与S同族化学性质性质相似,B正确;NaO的电子式为 ,
2 2 2 2
NaS的电子式为 ,离子键百分比 = (电负性差值 / 总电负性差值),O的电负性大于
2
S,则NaO离子键成分的百分数大于NaS,C正确; 为sp2杂化,孤电子对为0,为平面三角形,
2 2
为sp3杂化,孤电子对为1,三角锥形,D错误;故选D。
9.(2024·江苏卷)反应 可用于壁画修复。下列说法正确的是
A. 的结构示意图为 B. 中既含离子键又含共价键
C. 中S元素的化合价为 D. 的空间构型为直线形
【答案】C
【解析】 核外有18个电子,其结构示意图为 ,A错误;HO 是共价化合物,其中只含共价
2 2
键,B错误; 中O元素化合价为-2,S元素的化合价为+6,C正确;HO中的O的杂化类型为 ,
2
O有2个孤电子对,因此HO的空间构型为V形,D错误;综上所述,本题选C。
2
10.(2024·江苏卷)下列有关反应描述正确的是
A. 催化氧化为 , 断裂 键B. 氟氯烃破坏臭氧层,氟氯烃产生的氯自由基改变 分解的历程
C. 丁烷催化裂化为乙烷和乙烯,丁烷断裂 键和 键
D. 石墨转化为金刚石,碳原子轨道的杂化类型由 转变为
【答案】B
【解析】 催化氧化为 , 断裂 键和 生成 ,A错误;根
据题意,氯自由基催化O 分解氟氯烃破坏臭氧层,则氟氯烃产生的氯自由基改变 分解的历程,B正
3
确;丁烷催化裂化为乙烷和乙烯,丁烷断裂 键,丁烷是饱和烷烃,没有 键,C错误;石墨碳原子轨道
的杂化类型为转化为 ,金刚石碳原子轨道的杂化类型为 ,石墨转化为金刚石,碳原子轨道的杂化类
型由 转变为 ,D错误;故选B。
11.(2024·北京卷)氘代氨( )可用于反应机理研究。下列两种方法均可得到 :① 与
的水解反应;② 与 反应。下列说法不正确的是
A. 和 可用质谱法区分
B. 和 均为极性分子
C. 方法①的化学方程式是
D. 方法②得到的产品纯度比方法①的高
【答案】D
【解析】 和 的相对分子质量不同,可以用质谱法区分,A正确; 和 的H原子不同,
但空间构型均为三角锥形,是极性分子,B正确;MgN 与DO发生水解生成Mg(OD) 和ND ,反应方法
3 2 2 2 3
①的化学方程式书写正确,C正确;方法②是通过 中D原子代替 中H原子的方式得到 ,代
换的个数不同,产物会不同,纯度低,D错误;故选D。
12.(2024·广东卷)一种可为运动员补充能量的物质,其分子结构式如图。已知R、W、Z、X、Y为原子
序数依次增大的短周期主族元素,Z和Y同族,则
A. 沸点: B. 最高价氧化物的水化物的酸性:
C. 第一电离能: D. 和 空间结构均为平面三角形
【答案】D【分析】Y可形成5个共价键,Z可形成3个共价键,Z和Y同族,Y原子序数比Z大,即Z为N元素,Y
为P元素,W可形成4个共价键,原子序数比N小,即W为C元素,R可形成1个共价键,原子序数比C
小,即R为H元素,X可形成2个共价键,原子序数在N和P之间,即X为O元素,综上:R为H元素、
W为C元素、Z为N元素、X为O元素、Y为P元素。
【解析】由于NH 可形成分子间氢键,而PH 不能,因此沸点:NH >YH ,故A错误;W为C元素、Z
3 3 3 3
为N元素,由于非金属性:C<N,因此最高价氧化物的水化物的酸性:HCO<HNO,故B错误;同周
2 3 3
期元素从左到右第一电离能有增大趋势,ⅡA族、ⅤA族原子第一电离能大于同周期相邻元素,即第一电
离能: ,故C错误; 的中心原子价层电子对数为 ,属于sp2杂化,为平
面三角形, 的中心原子价层电子对数为 ,属于sp2杂化,为平面三角形,故D
正确;故选D。
13.(2024·甘肃卷)下列说法错误的是
A. 相同条件下 比 稳定 B. 与 的空间构型相同
C. 中 键比 键更易断裂 D. 中 键和大 键 的数目不相等
【答案D
【解析】 分子中存在的 , 分子中虽然也存在叁键,但是其键能小于 ,因此,相同条
件下 比 稳定,A正确; 与 均为 的等电子体,故其均为直线形分子,两者空间构型相
同,B正确; 的中心原子是N,其在催化剂作用下可分解为 和 ,说明 中 键比
键更易断裂,C正确; 中 键和大 键的数目均为2,因此, 键和大 键的数目相等,D不正确;
综上所述,本题选D。
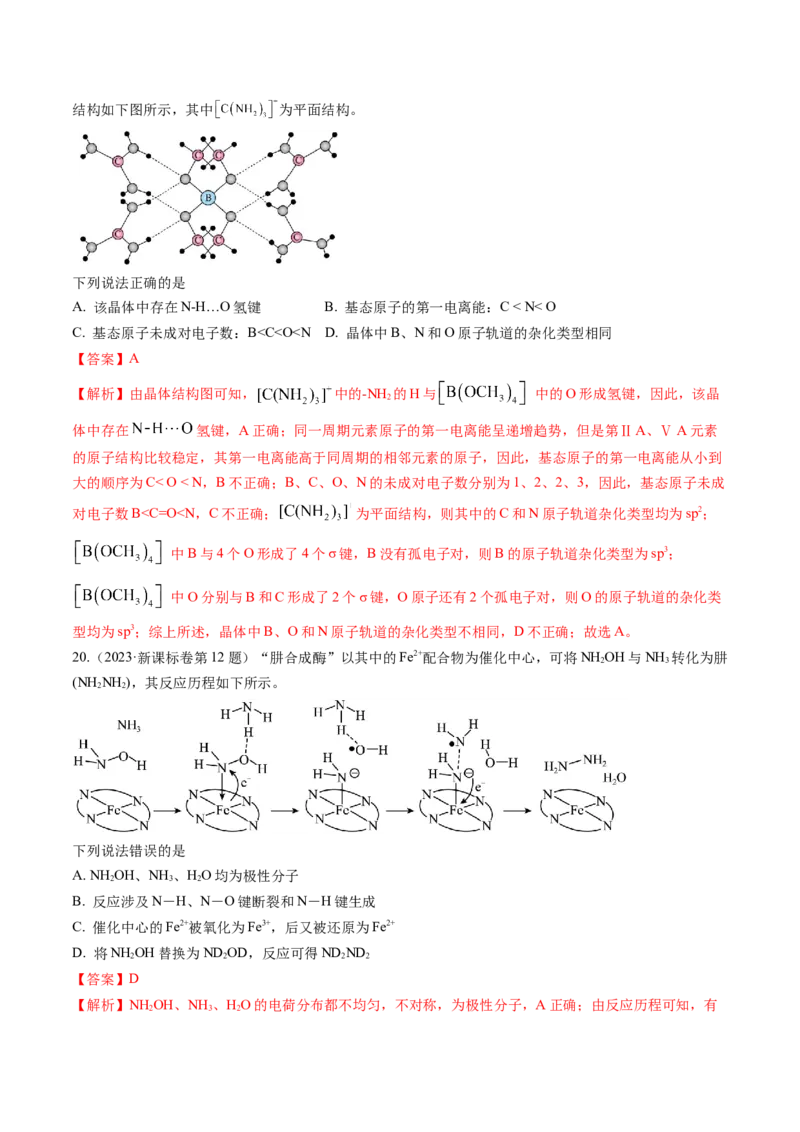
14.(2024·湖南卷)通过理论计算方法优化了P和Q的分子结构,P和Q呈平面六元并环结构,原子的连
接方式如图所示,下列说法错误的是
A. P为非极性分子,Q为极性分子 B. 第一电离能:
C. 和 所含电子数目相等 D. P和Q分子中C、B和N均为 杂化
【答案】A【解析】由所给分子结构图,P和Q分子都满足对称,正负电荷重心重合,都是非极性分子,A错误;同
周期元素,从左到右第一电离能呈增大趋势,氮原子的2p轨道为稳定的半充满结构,第一电离能大于相邻
元素,则第一电离能由小到大的顺序为BX
B. 最高正价:ZY
【答案】B
【解析】Y的s能级电子数量是p能级的两倍,Y为C,X的2s轨道全充满,原子序数XX,A正确;N最高正价为+5价,O无最高
正价,最高正价N大于O,B错误;Na和O形成的过氧化钠中含有非极性共价键,C正确;非金属性越
强,最高价氧化物对应水化物的酸性越强,非金属性N大于C,硝酸酸性强于碳酸,D正确;故选B。
22.(2023·浙江选考第12题)共价化合物 Al Cl 中所有原子均满足8电子稳定结构,一定条件下可发生反
2 6
应: ,下列说法不正确的是( )
A. Al Cl 的结构式为 B. Al Cl 为非极性分子
2 6 2 6
C. 该反应中NH 的配位能力大于氯 D. Al Br 比Al Cl 更难与NH 发生反应
3 2 6 2 6 3
【答案】D
【解析】由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为 ,
故A正确;由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为
,则双聚氯化铝分子为结构对称的非极性分子,故B正确;由反应方程式可知,氨分子更易与具有空轨道
的铝原子形成配位键,配位能力大于氯原子,故C正确;溴元素的电负性小于氯元素,原子的原子半径大
于氯原子,则铝溴键弱于铝氯键,所以双聚溴化铝的铝溴键更易断裂,比双聚氯化铝更易与氨气反应,故
D错误;故选D。
23.(2023·辽宁卷第6题)在光照下,螺呲喃发生开、闭环转换而变色,过程如下。下列关于开、闭环螺
呲喃说法正确的是( )A. 均有手性 B. 互为同分异构体
C. N原子杂化方式相同 D. 闭环螺吡喃亲水性更好
【答案】B
【解析】手性是碳原子上连有四个不同的原子或原子团,因此闭环螺吡喃含有手性碳原子如图所示,
,开环螺吡喃不含手性碳原子,故A错误;根据它们的结构简式,分子式均为C H NO,
19 19
它们结构不同,因此互为同分异构体,故B正确;闭环螺吡喃中N原子杂化方式为sp3,开环螺吡喃中N
原子杂化方式为sp2,故C错误;开环螺吡喃中氧原子显负价,电子云密度大,容易与水分子形成分子间氢
键,水溶性增大,因此开环螺吡喃亲水性更好,故D错误;答案为B。
24.(2023·辽宁卷第9题)某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、Y、Z、Q
是核电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2
倍。下列说法错误的是( )
A. W与Y的化合物为极性分子 B. 第一电离能
C. Q的氧化物是两性氧化物 D. 该阴离子中含有配位键
【答案】B
【解析】W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W形成1条单键且核电荷数最小,W为
H,X形成4条键,核电荷数大于H,且小于其他三种元素,X为C,Y形成2条单键,核电荷数大于C,
Y为O,W、Y原子序数之和等于Z,Z为F,Y原子价电子数为Q原子价电子数的2倍,Q为Al。W与X
的化合物不一定为极性分子,如HO是极性分子,A正确;同周期元素从左到右第一电离能呈增大趋势,
2
则第一电离能F>O>C,B错误;Q为Al,Al O 为两性氧化物,C正确;该阴离子中L与Q之间形成配位
2 3
键,D正确;故选B。