文档内容
考点 26 弱电解质的电离
弱电解质的电离是中学化学基本理论中的重要组成部分,也是学习中比较难理解的内容,更是近几年
高考命题的必考内容。全国卷对本专题的考查主要集中在弱电解质的电离平衡、电离常数的应用和计算等,
主要以选择题的形式出现;高考有关本部分内容的考查常以图表、图像创设新情境,考查考生的观察、理
解能力。
预测2023年高考应继续关注弱电解质的电离平衡、电离平衡常数的计算、中和滴定的迁移应用等考点,
对数形结合与分析推理型选题要加强训练。高考命题热点主要有影响弱电解质电离平衡的因素,通过图像
分析强、弱电解质,电离常数和电离度,比较微粒浓度大小和 pH的计算等,命题有时会与水解相结合增
加试题的难度。
一、电解质及其分类
二、弱电解质的电离平衡
三、电离度、电离平衡常数
四、强弱电解质的比较
电解质及其分类
1.电解质及其分类
3.电离方程式的书写
(1)电离:电解质在水溶液中或熔融状态下,离解成自由移动的离子的过程。(2)电离方程式
①强电解质完全电离,用“===”表示,写出下列物质在水溶液中的电离方程式。
(NH )SO :(NH )SO ===2NH+SO;
4 2 4 4 2 4
BaSO:BaSO===Ba2++SO;
4 4
KAl(SO ):KAl(SO )===K++Al3++2SO。
4 2 4 2
②弱电解质部分电离,用“ ”表示,多元弱酸的电离分步书写,多元弱碱分步电离一步书写。
写出下列物质在水溶液中的电离方程式:
NH ·H O:NH ·H O NH+OH-;
3 2 3 2
HCO:HCO H++HCO、HCO H++CO。
2 3 2 3
③酸式盐的电离。多元强酸酸式盐与多元弱酸酸式盐的阴离子电离方式不同。
写出下列物质在水溶液中的电离方程式:
NaHSO:NaHSO===Na++H++SO;
4 4
NaHCO :NaHCO ===Na++HCO、HCO H++CO。
3 3
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)Cl 的水溶液能导电,所以Cl 是电解质( )
2 2
(2)NaCl溶液在电流的作用下电离成钠离子和氯离子( )
(3)强电解质都是离子化合物,弱电解质都是共价化合物( )
(4)强电解质溶液的导电性比弱电解质溶液的导电性强( )
(5)HClO是弱电解质,但NaClO是强电解质( )
(6)BaSO 的水溶液不易导电,但BaSO 是强电解质( )
4 4
(7)CO 、NH 溶于水能导电,所以二者均为电解质( )
2 3
(8)烧碱、冰醋酸、四氯化碳均为电解质( )
(9)自由移动离子数目多的电解质溶液导电能力一定强( )
(10)NaHSO 在水溶液及熔融状态下均可电离出Na+、H+、SO( )
4
(11)NH 属于非电解质,但其水溶液能够导电( )
3
(12)BaSO 投入水中,导电性较弱,是弱电解质( )
4
(13)弱电解质溶液中至少存在两种共价化合物分子( )
(14)强电解质都是离子化合物,弱电解质都是共价化合物( )
(15)CaO是强电解质,是因为其水溶液能导电( )
(16)Cl 的水溶液能导电,所以Cl 是电解质( )
2 2
(17)Na CO 溶于水:NaCO===2Na++CO( )
2 3 2 3
(18)Al(OH) 碱式电离:Al(OH) ===Al3++3OH-( )
3 3
(19)H SO 在水溶液中电离:HSO 2H++SO( )
2 3 2 3
(20)HBr在水溶液中电离:HBr H++Br-( )
【典例】例1 (2022•浙江6月选考)下列物质属于强电解质的是( )
A.HCOOH B.Fe C.NaCO D.C H
2 3 2 2
【答案】C
【解析】A项,HCOOH是弱酸,在水溶液中只能部分电离,属于弱电解质,A不合题意;B项,Fe
是单质,不是电解质,B不合题意;C项,NaCO 是盐,在水溶液中能够完全电离,故属于强电解质,C
2 3
符合题意;D项,C H 是有机物,在水溶液和熔融状态下均不导电,属于非电解质,D不合题意;故选
2 2
C。
例2 (2021•浙江6月选考)下列物质属于弱电解质的是( )
A.CO B.HO C.HNO D.NaOH
2 2 3
【答案】B
【解析】A项,CO 在水溶液中或熔融状态下不能够电离,为非电解质,A不符合题意;B项,HO在
2 2
水溶液中或熔融状态下能够部分电离,为弱电解质,B符合题意;C项,HNO 为一种强酸,在水溶液中或
3
熔融状态下能够完全电离,为强电解质,C不符合题意;D项,NaOH为一种强碱,在水溶液中或熔融状
态下能够完全电离,为强电解质,D不符合题意;故选B。
【对点提升】
对点1 下列属于非电解质的是( )
A.CS B.CHCOOH C.HCl D.Cl
2 3 2
对点2 下列物质中在一定条件下能够导电,但不属于电解质的是( )
A.石墨 B.KNO C.HSO D.蔗糖
3 2 4
【巧学妙记】
常见的强电解质和弱电解质弱电解质的电离平衡
1.弱电解质的电离概念
(1)电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成分子的速率相等时,
电离过程达到了平衡。
(2)电离平衡的建立与特征
①开始时,v(电离)最大,而v(结合)为0。
②平衡的建立过程中,v(电离)>v(结合)。
③当v(电离)=v(结合)时,电离过程达到平衡状态。
2.外因对电离平衡的影响
(1)浓度:在一定温度下,同一弱电解质溶液,浓度越小,越易电离。
(2)温度:温度越高,电离程度越大。
(3)同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的方
向移动。
(4)化学反应:加入能与弱电解质电离出的离子反应的物质时,可使电离平衡向电离方向移动。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)强电解质稀溶液中不存在溶质分子,弱电解质稀溶液中存在溶质分子( )
(2)氨气溶于水,当NH ·H O电离出的c(OH-)= c(NH +时,表明NH ·H O电离处于平衡状态( )
3 2 4 3 2
(3)室温下,由0.1 mol·L-1一元碱BOH的pH=10,可知溶液中存在BOH==B++OH-( )
(4)电离平衡右移,电解质分子的浓度一定减小,离子浓度一定增大( )
(5)25 ℃时,0.1 mol·L-1 CHCOOH加水稀释,各离子浓度均减小( )
3
(6)电离平衡向右移动,弱电解质的电离度一定增大( )
(7)电离平衡向右移动,电解质的分子浓度一定减小( )
(8)Na SO 溶液与NaHSO 溶液中所含微粒的种类一定相同( )
2 3 3
【典例】
例1 饱和氨水中存在化学平衡和电离平衡:NH +HO NH ·H O NH+OH-。下列有关
3 2 3 2
说法正确的是( )
A.常温下饱和氨水的pH<7B.向氨水中滴加过量硫酸,上述平衡均正向移动,pH增大
C.电离是吸热过程,升高温度,上述平衡均正向移动
D.向氨水中加入少量NaOH固体,上述平衡均逆向移动,有NH 放出
3
【答案】D
【解析】常温下饱和氨水呈碱性,pH>7,A项错误;加入过量硫酸,H+浓度增大,pH减小,B项错
误;升温会使NH 逸出,NH +HO NH ·H O平衡向逆反应方向移动,C项错误;加入少量NaOH固
3 3 2 3 2
体,OH-浓度增大,平衡向生成NH 的方向移动,有NH 放出,D项正确。
3 3
例2 (2022•全国乙卷)常温下,一元酸 的K(HA)=1.0×10-3。在某体系中, 与A-离子不能穿过隔
a
膜,未电离的 可自由穿过该膜(如图所示)。
设溶液中c (HA)=c(HA)+c(A-),当达到平衡时,下列叙述正确的是( )
总
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c (HA)之比为10-4
总
【答案】B
【解析】A项,常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol/L,c(H+)<c(OH-)+
c(A-),A错误;B项,常温下溶液II的pH=1.0,溶液中c(H+)=0.1mol/L,K = =1.0×10-3,c
a 总
(HA)=c(HA)+c(A-),则 =1.0×10-3,解得 = ,B正确;C项,根据题意,未电离的
HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,C错误;D项,常温下溶液I的pH=7.0,溶液I中c(H+)=1×10-7mol/L,K = =1.0×10-3,c (HA)=c(HA)+c(A-), =1.0×10-3,溶
a 总
液I中c (HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中c(H+)=0.1mol/L,K = =1.0×10-3,c
总 a 总
(HA)=c(HA)+c(A-), =1.0×10-3,溶液II中c (HA)=1.01c(HA),未电离的HA可自由穿
总
过隔膜,故溶液I和II中的c(HA)相等,溶液I和II中c (HA)之比为
总
[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,D错误;故选B。
【对点提升】
对点1 25℃时,醋酸溶液中存在电离平衡:CHCOOH CHCOO-+ H+,下列说法正确的是(
3 3
)
A.向体系中加入少量CHCOONa固体,平衡向左移动,c(CHCOO-)下降
3 3
B.向体系中加水稀释,平衡向右移动,溶液中所有离子的浓度都减小
C.加入少量NaOH固体(忽略溶解热效应),平衡向右移动,水的电离程度也随之增大
D.升高体系温度(忽略醋酸挥发),溶液中H+数目增多,平衡一定向左移动
对点2 已知人体体液中存在如下平衡:CO +HO HCO H++HCO,以维持体液pH的
2 2 2 3
相对稳定。下列说法不合理的是( )
A.当强酸性物质进入体液后,上述平衡向左移动,以维持体液pH的相对稳定
B.当强碱性物质进入体液后,上述平衡向右移动,以维持体液pH的相对稳定
C.若静脉滴注大量生理盐水,则体液的pH减小
D.进行呼吸活动时,如果CO 进入血液,会使体液的pH减小
2
【巧学妙记】
电离过程是可逆过程,可直接用化学平衡移动原理分析电离平衡。
以0.1 mol·L-1CHCOOH溶液为例:CHCOOH CHCOO-+H+(正向吸热)。
3 3 3
实例(稀溶液) CHCOOH H++CHCOO- ΔH>0
3 3
改变条件 平衡移动方向 n(H+) c(H+) 导电能力 K
a
加水稀释 → 增大 减小 减弱 不变
加入少量冰醋酸 → 增大 增大 增强 不变
通入HCl(g) ← 增大 增大 增强 不变
加NaOH(s) → 减小 减小 增强 不变加入镁粉 → 减小 减小 增强 不变
升高温度 → 增大 增大 增强 增大
加CHCOONa(s) ← 减小 减小 增强 不变
3
电离度、电离平衡常数
1.电离度
(1)电离度概念与表达式
一定条件下,当弱电解质在水溶液中达到电离平衡时,溶液中已经电离的弱电解质分子数占弱电解质
分子总数的百分数。(常用符号α表示)
可用数学式表达为
α=×100%或α=×100%
或α=×100%
即α=×100%(c:电解质初始浓度,Δc:已电离电解质浓度)
(2)影响电离度的因素
①温度:在其他条件不变时,升高溶液温度,电离平衡向电离方向移动,电离度增大。
②浓度:其他条件不变时,增大弱电解质溶液的浓度,平衡向电离方向移动,但电离度减小。若降低
弱电解质溶液的浓度,平衡向电离方向移动,电离度增大。
③其他电解质的加入:如同离子效应,加入与弱电解质电离有相同离子的强电解质时,平衡向左移动,
会使弱电解质电离度降低。
2.电离平衡常数
(1)①填写下表(25 ℃)
弱电解质 电离方程式 电离常数
NH ·H O NH ·H O NH+OH- K =1.8×10-5
3 2 3 2 b
CHCOOH CHCOOH CHCOO-+H+ K=1.8×10-5
3 3 3 a
HClO HClO H++ClO- K=3.0×10-8
a
②CHCOOH酸性大于(填“大于”“小于”或“等于”)HClO酸性,判断的依据:相同条件下,电离
3
常数越大,电离程度越大,c(H+)越大,酸性越强。
③电离平衡常数的意义:弱酸、弱碱的电离平衡常数能够反映酸碱性的相对强弱。电离平衡常数越大,
电离程度越大。多元弱酸的电离以第一步电离为主,各级电离平衡常数的大小差距较大。
④外因对电离平衡常数的影响:电离平衡常数与其他化学平衡常数一样只与温度有关,与电解质的浓
度无关,升高温度,K值增大,原因是电离是吸热过程。(2)多元弱酸的分步电离,以碳酸为例,碳酸是二元弱酸,在水溶液中的电离是分步进行。
①电离方程式是HCO H++HCO,HCO H++CO。
2 3
②电离平衡常数表达式: , 。
③比较大小:K >K 。
a1 a2
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)弱电解质的电离平衡右移,电离平衡常数一定增大( )
(2)电离常数大的酸溶液中的[H+]一定比电离常数小的酸溶液中的c(H+)大( )
(3)某一弱电解质,电离度越大,电离常数就越大( )
(4)相同温度下,向1 mol·L-1的醋酸溶液中加入少量冰醋酸,其电离度变小( )
(5)常温时,0.1 mol·L-1氨水的pH=11.1:NH ·H O NH+OH-( )
3 2
(6)常温下,0.1 mol·L-1 CHCOONa溶液的pH大于7能证明乙酸是弱酸( )
3
(7)室温下,稀释0.1 mol·L-1 CHCOOH溶液,溶液的导电能力增强( )
3
(8)稀醋酸中加入少量醋酸钠能增大醋酸的电离程度( )
(9)向0.1 mol·L-1 CHCOOH溶液中加入少量水,溶液中减小( )
3
(10)室温下向10 mL 0.1 mol/L 的氨水中加水稀释后,溶液中不变( )
(11)等体积、等物质的量浓度的NaCO 和NaHCO 溶液混合: < ( )
2 3 3
(12)将浓度为0.1 mol·L-1 HF溶液加水不断稀释过程中,电离平衡常数K(HF)保持不变,c(F-)/ c(H+)始
a
终增大( )
【典例】
例1 已知25 ℃时有关弱酸的电离平衡常数如下表:
弱酸化学式 HX HY HCO
2 3
K =4.4×10-7
1
电离平衡常数/mol·L-1 7.8×10-9 3.7×10-15
K =4.7×10-11
2
下列推断正确的是( )
A.HX、HY两种弱酸的酸性:HX>HY
B.相同条件下溶液的碱性:NaX>NaCO>NaY>NaHCO
2 3 3
C.结合H+的能力:CO>Y->X->HCO
D.HX和HY酸性相同,都比HCO 弱
2 3
【答案】A
【解析】根据电离平衡常数可知酸性:HCO >HX>HCO>HY,则结合H+的能力:Y->CO>X->
2 3
HCO,故A正确、C、D错误;酸越弱,其对应的盐的水解能力越强,故相同条件下溶液的碱性:NaY>
NaCO>NaX>NaHCO ,故B错误。
2 3 3例2 (2022·浙江省6月选考) 25℃时,苯酚(C HOH)的K=1.0×10-10,下列说法正确的是( )
6 5 a
A.相同温度下,等 的C HONa和CHCOONa溶液中,c (C HO-)>c(CHCOO-)
6 5 3 6 5 3
B.将浓度均为0.1mol·L-1的C HONa和NaOH溶液加热,两种溶液的 均变大
6 5
C. 时,C HOH溶液与NaOH溶液混合,测得 ,则此时溶液中c (C HO-)= c
6 5 6 5
(C HOH)
6 5
D. 时,0.1mol·L-1的C HOH溶液中加少量C HONa固体,水的电离程度变小
6 5 6 5
【答案】C
【解析】A项,醋酸的酸性大于苯酚,则醋酸根离子的水解程度较小,则相同温度下,等pH的
C HONa和CHCOONa溶液中c(C HO-)H CO>HCO
3 2 3
电离常数越大,对应的盐水解程度越小,碱性(或酸性)越弱。如:利用
判断盐溶液的酸
上面电离常数的数值可知等浓度的CHCOONa、NaHCO 、NaCO 溶液
性(或碱性)强弱 3 3 2 3
的pH由大到小的顺序为NaCO>NaHCO>CH COONa
2 3 3 3
一般符合“强酸制弱酸”规律。如:利用上面中电离常数的数值可知,
判断复分解反应
向NaCO 溶液中加入足量CHCOOH的离子方程式为CO+
能否发生 2 3 3
2CHCOOH===2CH COO-+HO+CO↑
3 3 2 2
弱电解质加水稀释时,能促进弱电解质的电离,溶液中离子和分子的浓
判断微粒浓度比 度会发生相应的变化,但电离常数不变,题目中经常利用电离常数来判
值的变化 断溶液中微粒浓度比值的变化情况。如把0.1 mol·L-1 CHCOOH溶液加
3
水稀释,==稀释时,c(H+)减小,K 值不变,则变大
a
弱强电解质的比较
1.一元强酸和一元弱酸的比较
浓度均为0.01 mol·L-1的 pH均为2的强酸HA与弱
强酸HA与弱酸HB 酸HB
0.01 mol·L-1=c(HA)<
pH或物质的量浓度 2=pH <pH
HA HB
c(HB)
开始与金属反应的速率 HA>HB HA=HB
体积相同时与过量的碱反应
HA=HB HA<HB
时消耗碱的量
体积相同时与过量活泼金属
HA=HB HA<HB
反应产生H 的量
2
c(A-)与c(B-)的大小 c(A-)>c(B-) c(A-)=c(B-)
分别加入固体NaA、NaB后
HA:不变HB:变大 HA:不变HB:变大
pH变化
加水稀释10倍后 3=pH <pH 3=pH >pH >2
HA HB HA HB
溶液的导电性 HA>HB HA=HB
水的电离程度 HA10-7mol·L-1( )
(25)己知某分散系中存在:M(OH) (s) M2+(aq)+2OH-(aq),K=a,c(M2+)=b mol·L-1时,溶液
2
1 b
14+ lg( )
的pH等于 2 a ( )
【典例】
例1 (2020•浙江1月选考)下列说法不正确的是( )
A.pH>7的溶液不一定呈碱性
B.中和pH和体积均相等的氨水、NaOH溶液,所需HCl的物质的量相同
C.相同温度下,pH相等的盐酸、CHCOOH溶液中,c(OH−)相等
3
D.氨水和盐酸反应后的溶液,若溶液呈中性,则c(Cl−)=c(NH)
【答案】B
【解析】A项,温度影响水的电离,则pH>7的溶液不一定呈碱性;溶液酸碱性与溶液中氢离子、氢
氧根离子浓度有关,当c(H+)苯甲酸溶液
D.C HCOONa溶液中存在关系:c(C HCOO—)=c(Na+)=c(H+)=c(OH—)
6 5 6 5
2.(2022·江西省赣州市高三模拟)室温下,在10 mL 0.1 mol/L某二元酸HA溶液中,滴加0.1
2
mol/LNaOH溶液。已知:HA=H++HA-,HA- H++A2-。下列说法正确的是( )
2
A.A2-可经过两步水解得到HA
2
B.滴加NaOH溶液10 mL时,溶液中离子浓度大小为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.当滴加至中性时,溶液中有c(Na+)=c(HA-)+c(A2-)D.当用去NaOH溶液体积20 mL时,此时溶液中有2c(Na+)=c(HA-)+c(A2-)
3.(2022·浙江省镇海中学高三选考适应性测试)下列叙述正确的是( )
A.常温下 的HA溶液与 的BOH等体积混合,溶液 ,则BOH为强碱
B.含1molKOH的溶液与1molCO 完全反应后的溶液中:c(K+) =c(HCO -)
2 3
C. 氨水的,pH=a,加入适量的氯化铵固体可使溶液pH=a+1
D.物质的量浓度相等的(NH )SO 溶液与(NH )CO 溶液中, 前者大于后者
4 2 4 4 2 3
4.(2022·浙江省宁波市鄞州中学高三考前模拟预测)下列说法正确的是( )
A.相同温度下,等pH的盐酸和醋酸加水稀释10倍后,c(Cl-)<c(CHCOO-)
3
B.0.1 mol·L-1的KA溶液pH=6.5,则HA为弱酸
C.常温下pH=3的盐酸和pH=11的氨水等体积混合:c(Cl-)+c(H+)=c(NH+)+c(OH-)
4
D.某温度下,向氨水中通入CO,随着CO 的通入, 不断增大
2 2
5.(2022·广东省四校高三联考)乙二胺(H NCH CHNH )是二元弱碱(已知:25℃时,K =10-4,K =10-
2 2 2 2 b1 b2
7),其水溶液与NH 水溶液的电离方式相似。现用锥形瓶装10 mL0.1 mol·L-1乙二胺溶液,用0.1 mol·L-1盐
3
酸滴定。下列叙述错误的是( )
A.乙二胺在水溶液中的第一步电离方程式HNCH CHNH +H O [H NCH CHNH ]++OH-
2 2 2 2 2 2 2 2 3
B.选用甲基橙作指示剂,可以很好地判断滴定终点 ⇌
C.滴入10.00 mL盐酸时,溶液呈碱性
D.滴入20.00 mL盐酸时,混合溶液中有c(H NCH CHNH )+c([H NCH CHNH ]+)
2 2 2 2 2 2 2 3
+c([H NCH CHNH ]2+)=c(Cl-)
3 2 2 3
6.(2022·江苏省苏州市高三适应性模拟)硫酸工业尾气(主要含SO 、N 和O),用NaSO 溶液吸收可
2 2 2 2 3
转化为NaHSO,当c(HSO -)∶c(SO 2-)≈10时,吸收能力下降,需要加热再生为NaSO 溶液。已知
3 3 3 2 3
K (H SO )=10-1.9,K (H SO )=10-7.2,下列说法不正确的是( )
a1 2 3 a2 2 3
A.NaSO 溶液中存在:c(OH—)= c(H+) + c(HSO -) +2c(H SO )
2 3 3 2 3
B.NaSO 溶液吸收SO 的离子方程式为:SO 2-+SO +HO=2HSO -
2 3 2 3 2 2 3
C.当c(HSO -):c(SO 2-)=10时,此时吸收液的pH=6.2
3 3
D.与原NaSO 溶液相比,吸收液充分分解放出SO 再生后吸收SO 能力几乎不变
2 3 2 2
7.(2022·湖北省华中师大一附中模拟预测)已知:NH OH、苯酚分别为一元弱碱和一元弱酸。25℃时,
2将10mL浓度均为0.1mol·L-1的NH OH。苯酚两种溶液分别加水稀释的曲线如图所示,V是溶液体积
2
(mL)。pOH=-lgc(OH-)。下列说法正确的是( )
A.曲线m为NH OH溶液加水稀释的曲线
2
B.lgV=1时,水的电离程度:NH OH>苯酚
2
C.同浓度同体积的NH OH和苯酚混合后溶液显酸性
2
D.电离常数:K(NH OH)>K(苯酚)
b 2 a
8.(2022·辽宁省沈阳市三模)H C O 为二元弱酸,K =5.9×10-2,K =6.4×10-5, ,向
2 2 4 a1 a2
20mL0.1mol/LH C O 溶液中滴加0.2mol/LKOH溶液,溶液中含碳微粒的存在形式与物质的量百分比随
2 2 4
KOH溶液体积变化如图所示,下列说法中错误的是( )
A.当c(HC O-)=c(C O2-)时,混合溶液pH≈4.2
2 4 2 4
B.滴入10mLKOH溶液时,溶液呈酸性
C.滴入20mLKOH溶液时,溶液中(H C O)+c(HC O-)+c(C O2-)=0.1mol/L
2 2 4 2 4 2 4
D.滴入KOH溶液的过程中,可能出现c(H+)>c(HC O-)>c(C O2-)>c(OH-)
2 4 2 4
9.(2022·陕西省西北工业大学附属中学考前模拟)常温下,向20mL浓度均为0.1mol·L-1的HX和
CHCOOH的混合溶液中滴加0.1mol·L-1的氨水,测得溶液的电阻率(溶液的电阻率越大,导电能力越弱)与
3
加入氨水的体积(V)的关系如图。(CHCOOH的K=1.8×10-5,NH ·H O的K=1.8×10-5),下列说法正确的是(
3 a 3 2 b
)A.常温时,同浓度的HX溶液比CHCOOH溶液的pH大
3
B.a→c过程,水的电离程度先减小后增大
C.溶液pH=7时对应的点在c点和d点之间,此时溶液中存在:
D.混合时若忽略体积变化,d点时:4c(NH )+4c(NH·H O)=0.3mol·L-1
3 2
10.(2022·湖南省新化县第一中学模拟预测)牙形石(一种微型古生物遗体)主要成分为Ca (PO ),存在
3 4 2
于灰岩(主要成分为CaCO )中。可以通过合适的酸除去灰岩显示出牙形石的形态,进而分析当时的地层环
3
境。根据以下数据,有关合适的酸分析错误的是( )
已知:(1)酸的电离平衡常数
弱酸 HPO CHCOOH HCO
3 4 3 2 3
K =6.9×10-3
a1
K =4.5×10-7
a1
电离平衡常数(25℃) K =6.2×10-8 K=1.8×10-5
a2 a
K =4.7×10-11
a2
K =4.8×10-13
a3
(2)K [Ca (PO )]=2.07×10-33
sp 3 4 2
(3)钙的磷酸盐中只有磷酸二氢钙可溶于水,其余难溶于水
A.当加入过量的盐酸时与牙形石反应为:Ca (PO )+2H+=H PO -+3Ca2+
3 4 2 2 4
B.过量的醋酸可以溶解灰岩:CaCO +2CH COOH=Ca2++2CH COO-+H O+CO↑
3 3 3 2 2
C.过量醋酸与牙形石:Ca (PO )+4CH COOH=3Ca2++4CH COO-+2 H PO -,该反应K≈2.5×10-13
3 4 2 3 3 2 4
D.醋酸能溶解灰岩,不溶解牙形石,可用于除去灰岩显示出牙形石
11.(2022·山东省济南高三模拟联考)室温下,通过下列实验探究HC O 溶液的性质:
2 2 4
编号 实验操作
1 用pH试纸测定0.1molL-1的HC O 溶液,测得pH约为2
2 2 4
2 向0.1 mol·L-1的HC O ⋅ 溶液中逐滴加入等体积0.1molL-1的KOH 溶
2 2 4
⋅液,测得所得溶液的pH约为4
将4mL0.01mol·L-1 KMnO 酸性溶液与4 mL0.1mol·L-1 HC O 溶液混
3 4 2 2 4
合,溶液褪色
下列说法正确的是( )
A.HC O 的K 约为10-2
2 2 4 a1
B.实验2溶液pH由2到4的过程中水的电离程度不断减小
C.实验2所得溶液中继续加 溶液至溶液呈中性:c(K+)>2c(HC O-)+c(C O2-)
2 4 2 4
D.实验3中酸性KMnO 溶液褪色证明HC O 具有漂白性
4 2 2 4
12.(2022·北京市东城区高三期末统一检测)电离常数是研究电解质在水溶液中的行为的重要工具。现
有 、 和 三种酸,各酸及其盐之间不发生氧化还原反应,它们的电离常数如下表所示。
酸 电离常数(25℃)
HX K=1.0×10-9.2
a
HY K =1.0×10-6.4,K =1.0×10-10.3
2 a1 a2
HZ K =1.0×10-1.9,K =1.0×10-7.2
2 a1 a2
下列说法正确的是( )
A.在水溶液中结合 的能力: Y2-<Z2-
B. 溶液中离子浓度的关系:c(Na+)<c(X-)
C.NaY溶液与过量 反应的离子方程式:HX+Y2-=HY-+X-
2
D.25℃时,浓度均为0.1mol·L-1的HY和HZ溶液的 :HY<HZ
2 2 2 2
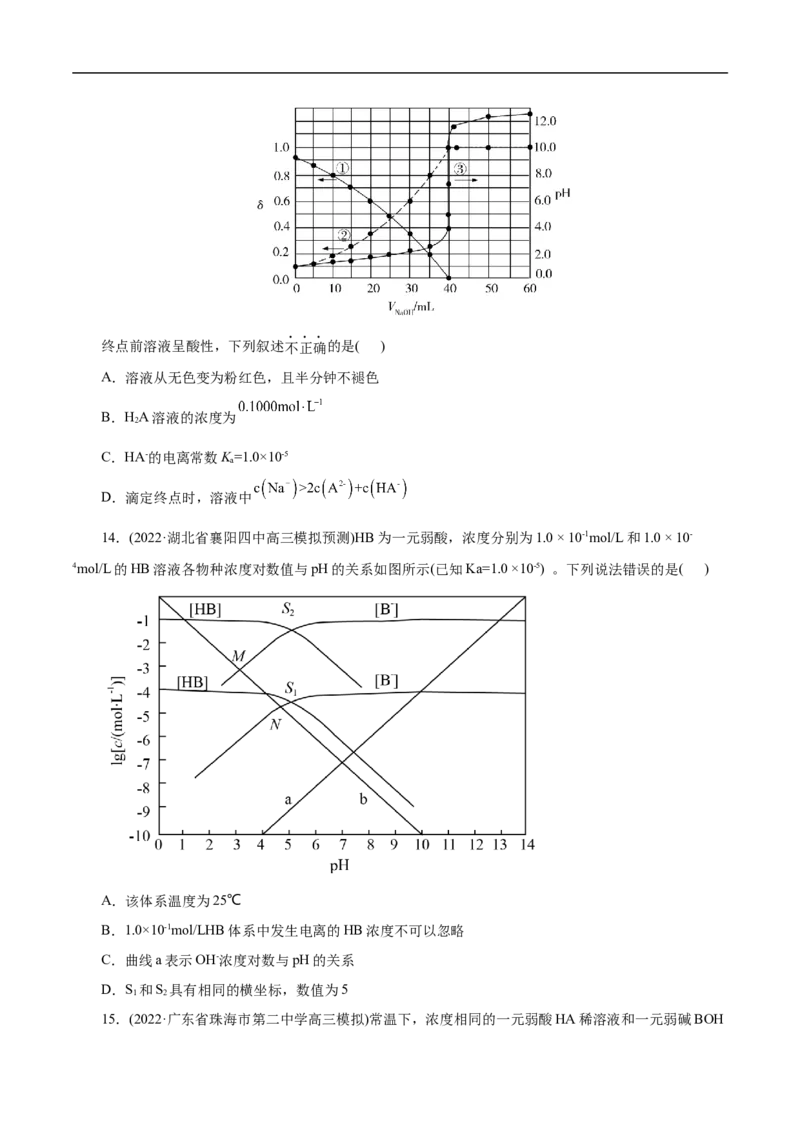
13.(2022·北京市和平街第一中学三模)以酚酞为指示剂,用 的 溶液滴定20.00mL
未知浓度的二元酸HA溶液。溶液中,pH、分布系数 随滴加 溶液体积 的变化关系如下图所示。
2
[比如A2-的分布系数: ]终点前溶液呈酸性,下列叙述不正确的是( )
A.溶液从无色变为粉红色,且半分钟不褪色
B.HA溶液的浓度为
2
C.HA-的电离常数K=1.0×10-5
a
D.滴定终点时,溶液中
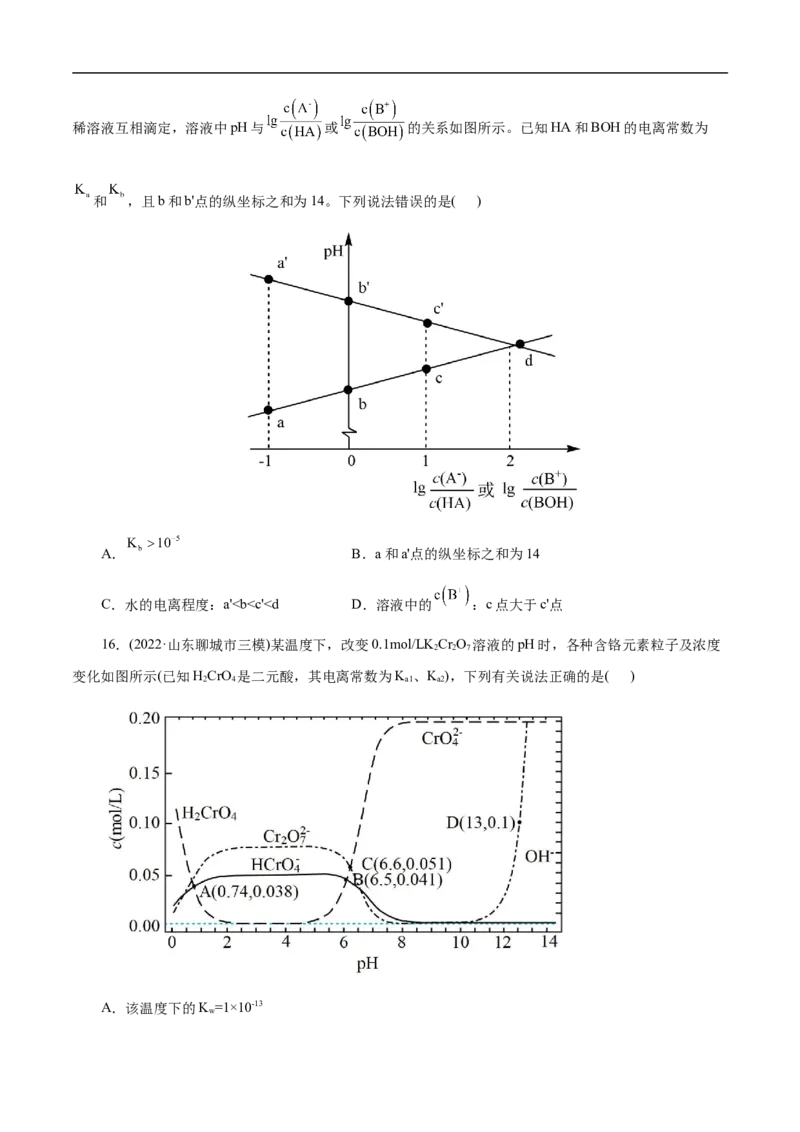
14.(2022·湖北省襄阳四中高三模拟预测)HB为一元弱酸,浓度分别为1.0 × 10-1mol/L和1.0 × 10-
4mol/L的HB溶液各物种浓度对数值与pH的关系如图所示(已知Ka=1.0 ×10-5) 。下列说法错误的是( )
A.该体系温度为25℃
B.1.0×10-1mol/LHB体系中发生电离的HB浓度不可以忽略
C.曲线a表示OH-浓度对数与pH的关系
D.S 和S 具有相同的横坐标,数值为5
1 2
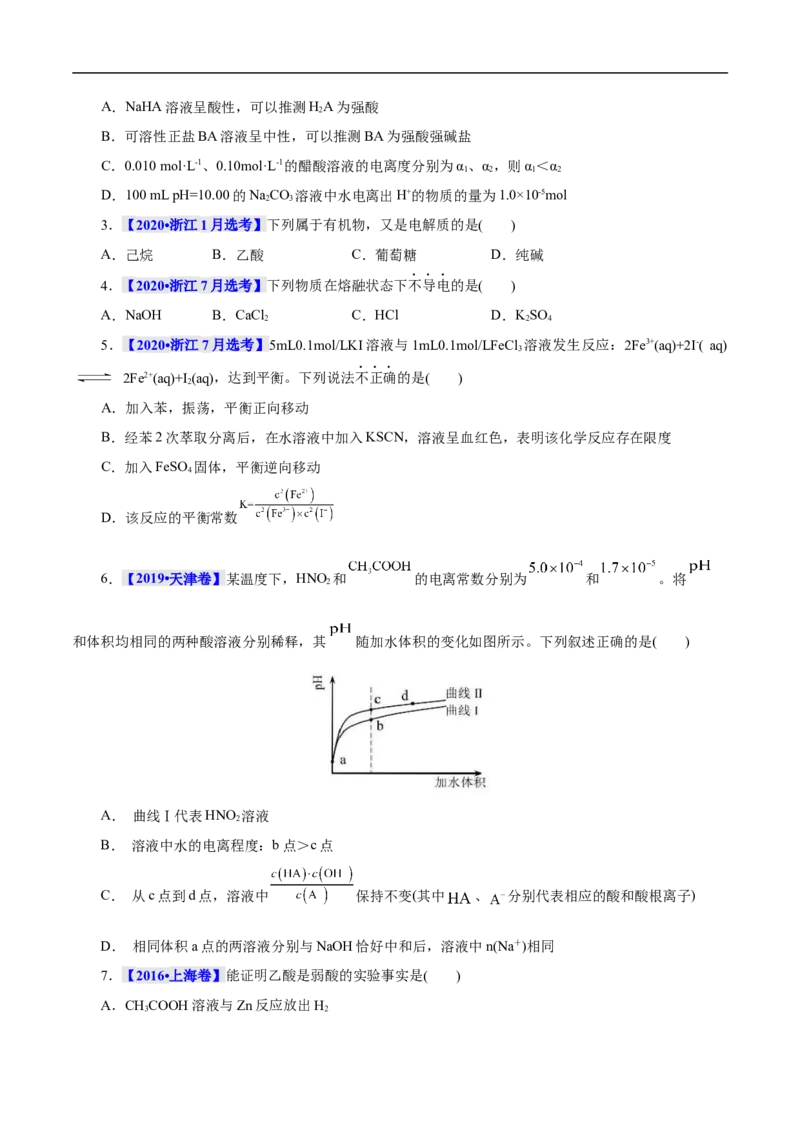
15.(2022·广东省珠海市第二中学高三模拟)常温下,浓度相同的一元弱酸HA稀溶液和一元弱碱BOH稀溶液互相滴定,溶液中pH与 或 的关系如图所示。已知HA和BOH的电离常数为
和 ,且b和b'点的纵坐标之和为14。下列说法错误的是( )
A. B.a和a'点的纵坐标之和为14
C.水的电离程度:a'2c(Cr O2-)+3c(CrO 2-)
2 7 4
C.KHCrO 溶液:c(HCrO -)>c(CrO 2-)>c(H CrO)
4 4 4 2 4
D.该温度下反应Cr O2-+H O 2CrO2-+2H+的平衡常数为1×10-13.2
2 7 2 4
17.(2022·安徽省江淮名校高三第三次模拟联考)某小组从反应速率和产物角度探究Mg与NaHCO 溶
3
液反应。
实验I、25°C, 相同镁条分别与下列试剂反应
序 浓度 体积
试剂 pH 现象
号 (mol·L-1) (mL)
i HO —— 7.5 7 镁条表面有微量气泡附着
2
ii NaHCO 溶 1.0 7.5 8.4 镁条表面持续产生大量气泡,溶液略显浑浊,点燃气
3
液 泡有爆鸣声
(1)已知: Mg(OH) 固体致密,易包裹在金属表面成膜。根据上述现象,推测在实验ii中。
2
①Mg可以提高HCO -的电离程度,原因是___________;
3
②浑浊的主要原因是产生了___________(填化学式) ;
③实验ii中产生气泡的速率快于实验i的原因可能是___________。
(2)补充实验II,证实(1)的推测:
浓度
序号 试剂 体积(mL) pH 现象
(mol·L-1)
iii NaNO 溶液 1.0 7.5 7 镁条表面有微量气泡附着
3
iv NaCO 溶液 0.5 7.5 11.8 持续产生少量气泡,溶液显浑浊
2 3
①小组设计实验iii 的目的是___________ ; 甲同学结合实验iv的现象认为可以不必进行实验iii,他
的理由是___________;
②实验ii生成气体的速率快于实验iv,原因可能是___________ ;
③查资料知HCO -+Mg2+ [Mg(HCO)]+,请从平衡移动的角度解释实验ii产生气体速率更快的原
3 3
因___________。
1.【2022·浙江省1月选考】下列物质属于非电解质的是( )
A.CH B.KI C.NaOH D.CHCOOH
4 3
2.【2021•浙江1月选考】25℃时,下列说法正确的是( )A.NaHA溶液呈酸性,可以推测HA为强酸
2
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 mol·L-1、0.10mol·L-1的醋酸溶液的电离度分别为α 、α ,则α <α
1 2 1 2
D.100 mL pH=10.00的NaCO 溶液中水电离出H+的物质的量为1.0×10-5mol
2 3
3.【2020•浙江1月选考】下列属于有机物,又是电解质的是( )
A.己烷 B.乙酸 C.葡萄糖 D.纯碱
4.【2020•浙江7月选考】下列物质在熔融状态下不导电的是( )
A.NaOH B.CaCl C.HCl D.KSO
2 2 4
5.【2020•浙江7月选考】5mL0.1mol/LKI溶液与1mL0.1mol/LFeCl 溶液发生反应:2Fe3+(aq)+2I-( aq)
3
2Fe2+(aq)+I (aq),达到平衡。下列说法不正确的是( )
2
A.加入苯,振荡,平衡正向移动
B.经苯2次萃取分离后,在水溶液中加入KSCN,溶液呈血红色,表明该化学反应存在限度
C.加入FeSO 固体,平衡逆向移动
4
D.该反应的平衡常数
6.【2019•天津卷】某温度下,HNO 和 的电离常数分别为 和 。将
2
和体积均相同的两种酸溶液分别稀释,其 随加水体积的变化如图所示。下列叙述正确的是( )
A. 曲线Ⅰ代表HNO 溶液
2
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中 保持不变(其中 、 分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
7.【2016•上海卷】能证明乙酸是弱酸的实验事实是( )
A.CHCOOH溶液与Zn反应放出H
3 2B.0.1 mol/L CH COONa溶液的pH大于7
3
C.CHCOOH溶液与NaCO 反应生成CO
3 2 3 2
D.0.1 mol/L CH COOH溶液可使紫色石蕊变红
3